El objetivo de los autores es realizar una revisión sistemática de la bibliografía para evaluar la efectividad de los modelos predictivos de inteligencia artificial en la predicción de complicaciones en pacientes adultos tratados mediante cirugía por enfermedad toracolumbar degenerativa, en comparación con otras técnicas predictivas de uso habitual.
Materiales y métodosSe realizó una revisión sistemática de la bibliografía en Medline/Pubmed, Cochrane Library y Lilacs/Portal de la BVS sobre la efectividad del uso de modelos predictivos de inteligencia artificial para las posibles complicaciones en pacientes operados por enfermedad degenerativa de la columna toracolumbar durante el periodo de 1 de enero de 2000 y 1 de mayo de 2023. El riesgo de sesgo se evaluó con las herramientas ROBINS-I y PROBAST. Se registraron características de los estudios y resultados, contemplando como desenlace complicaciones generales o específicas.
ResultadosSe identificaron 2.321 títulos, 763 eran duplicados. Se realizó el cribado de 1.558 títulos; 22 fueron elegidos para su lectura completa con exclusión de 18 y elección final de 4 publicaciones para la siguiente revisión. Adicionalmente, se incluyeron 8 publicaciones desde otras fuentes (Biblioteca Asociación Argentina de Ortopedia y Traumatología, con búsqueda manual de citas). En 5 artículos (41,6%) se compararon la efectividad de modelos predictivos de inteligencia artificial frente a técnicas habituales. Todos fueron catalogados globalmente con muy alto riesgo de sesgo. Dada la heterogeneidad de las muestras, los resultados de interés y las métricas de evaluación de los algoritmos, no se realizó un metaanálisis.
ConclusiónSi bien la evidencia disponible es limitada y presenta un alto riesgo de sesgo, los estudios analizados indican que estos modelos pueden alcanzar un desempeño prometedor en la predicción de complicaciones, con valores del área bajo la curva que, en su mayoría, oscilan entre aceptables y excelentes.
We aim to conduct a systematic review of the literature to evaluate the effectiveness of artificial intelligence prediction models in predicting complications in adult patients undergoing surgery for degenerative thoracolumbar pathology compared with other commonly used prediction techniques.
MethodsA systematic literature review was conducted in Medline/Pubmed, Cochrane Library, and Lilacs/Portal de la BVS to identify machine learning models in predicting complications in patients undergoing surgery for degenerative thoracolumbar spine pathology between January 1, 2000, and May 1, 2023. The risk of bias was assessed using the PROBAST tool. Study characteristics and outcomes focusing on general or specific complications were recorded.
ResultsA total of 2,341 titles were identified (763 were duplicates). Screening was performed on 1,578 titles, and 22 were selected for full-text reading, with 18 exclusions and 4 publications selected for the subsequent review. Additionally, 8 publications were included from other sources (Argentine Association of Orthopedics and Traumatology Library; manual citation search). In 5 (41.6%) articles, the effectiveness of artificial intelligence predictive models was compared with conventional techniques. All were globally classified as having a very high risk of bias. Due to heterogeneity in samples, outcomes of interest, and algorithm evaluation metrics, a meta-analysis was not performed.
ConclusionAlthough the available evidence is limited and carries a high risk of bias, the studies analysed suggest that these models may achieve promising performance in predicting complications, with area under the curve values mostly ranging from acceptable to excellent.
Según estadísticas de Estados Unidos, el costo estimado de la enfermedad vertebral degenerativa es de alrededor de 100 billones de dólares anuales1. Se calcula que 2 de cada 3 adultos experimentarán de dolor lumbar bajo en algún momento de su vida2. La complejidad de los pacientes con enfermedad de la columna vertebral y las complicaciones asociadas con la cirugía han motivado la investigación de estrategias para una predicción precisa de estos episodios, así como para la estimación anticipada de los resultados clínicos. Tradicionalmente distintos modelos de análisis estadístico han permitido identificar factores predicativos para las complicaciones, con gran popularidad de los modelos de análisis multivariado, como la regresión logística, que produce una medida de riesgo (odds ratio) para variables independientes sobre un efecto o resultado específico3.
El campo de la inteligencia artificial (IA) ha impactado notablemente en múltiples áreas de la salud y la cirugía de columna no es la excepción3,4. La IA se ocupa no solo de comprender, sino también de construir «entidades inteligentes»: máquinas que pueden calcular cómo actuar de manera efectiva y segura4. La IA comprende diversas disciplinas que incluyen: el procesamiento natural del lenguaje, la representación del conocimiento, el razonamiento automatizado, el aprendizaje de la máquina (machine learning o ML) y la robótica. El ML es una subárea que permite al sistema aprender y retroalimentarse a sí mismo; es decir, desarrollar algoritmos que mejoran con la experiencia. El ML involucra numerosos métodos, como el aprendizaje profundo (deep learning), basado en redes neuronales artificiales3,4. El ML ha permitido desarrollar modelos predictivos y en la última década se han publicado numerosos artículos para su aplicación en áreas específicas, como la de la cirugía de columna vertebral3,4.
El objetivo de los autores es realizar una revisión sistemática de la bibliografía para evaluar la efectividad de los modelos predictivos de inteligencia artificial en la predicción de complicaciones en pacientes adultos tratados mediante cirugía por enfermedad toracolumbar degenerativa, en comparación con otras técnicas predictivas de uso habitual.
Materiales y métodosSe realizó una revisión sistemática de la bibliografía en las principales bases de datos biomédicos (Medline/Pubmed, Cochrane Library y Lilacs/Portal de la BVS) sobre la efectividad del uso de modelos predictivos de IA para predecir complicaciones en pacientes operados por enfermedad degenerativa de la columna toracolumbar durante el periodo comprendido entre el 1 de enero de 2000 y el 1 de mayo de 2023.
Criterios de elegibilidadSe seleccionaron estudios de acuerdo con los siguientes criterios de elegibilidad:
Diseños de estudios: ensayos clínicos controlados y aleatorizados, estudios prospectivos no aleatorizados, estudios observacionales de cohortes prospectivos y retrospectivos, estudios transversales y series descriptivas con más de 10 casos. Fueron excluidos los reportes de caso, revisiones (sistemáticas, narrativas), editoriales, cartas al editor y consensos.
Participantes: pacientes adultos (18-65 años) de ambos sexos tratados quirúrgicamente por enfermedad degenerativa de la columna toracolumbar (hernia de disco, canal estrecho lumbar y deformidad del adulto, sagital o coronal). Fueron excluidos los estudios de población con escoliosis idiopática, neuromuscular, congénita o sindrómica, fracturas por osteoporosis/enfermedad metabólica, artritis reumatoide, espondilitis anquilosante/hiperostosis esquelética idiopática difusa, enfermedad oncológica vertebral y los de pacientes tratados mediante bloqueos como procedimiento terapéutico único (sin cirugía).
Intervención: uso de IA para la creación de modelos predictivos de complicaciones contemplando modelos de aprendizaje profundo (deep learning), aprendizaje mecánico (machine learning), red neuronal artificial (artificial neural network) y otros métodos novedosos cuyo desarrollo implique el uso de inteligencia artificial. Se excluyeron los estudios que utilizaran modelos de IA para otros objetivos distintos de la predicción de complicaciones, como evaluación de pacientes e imágenes, clasificación, aplicación en cirugía navegada o robótica.
Comparador: otros métodos habituales para predecir complicaciones como métodos estadísticos o escalas. Debido a la novedad del tema, adicionalmente se contemplaron estudios sin comparador.
Resultados (outcomes): estudios que registran complicaciones en pacientes quirúrgicos por enfermedad toracolumbar degenerativa, contemplando, principalmente complicaciones intraoperatorias y postoperatorias tempranas (90 días desde la cirugía). Secundariamente, complicaciones en plazos mayores (6 meses, 1 y 2 años) y otras variables de resultados, como dolor, discapacidad funcional, tiempo de internación, reingresos y morbimortalidad.
Tiempo: estudios con tiempo de seguimiento mayor o igual a 90 días.
Idioma: estudios en inglés, español y portugués.
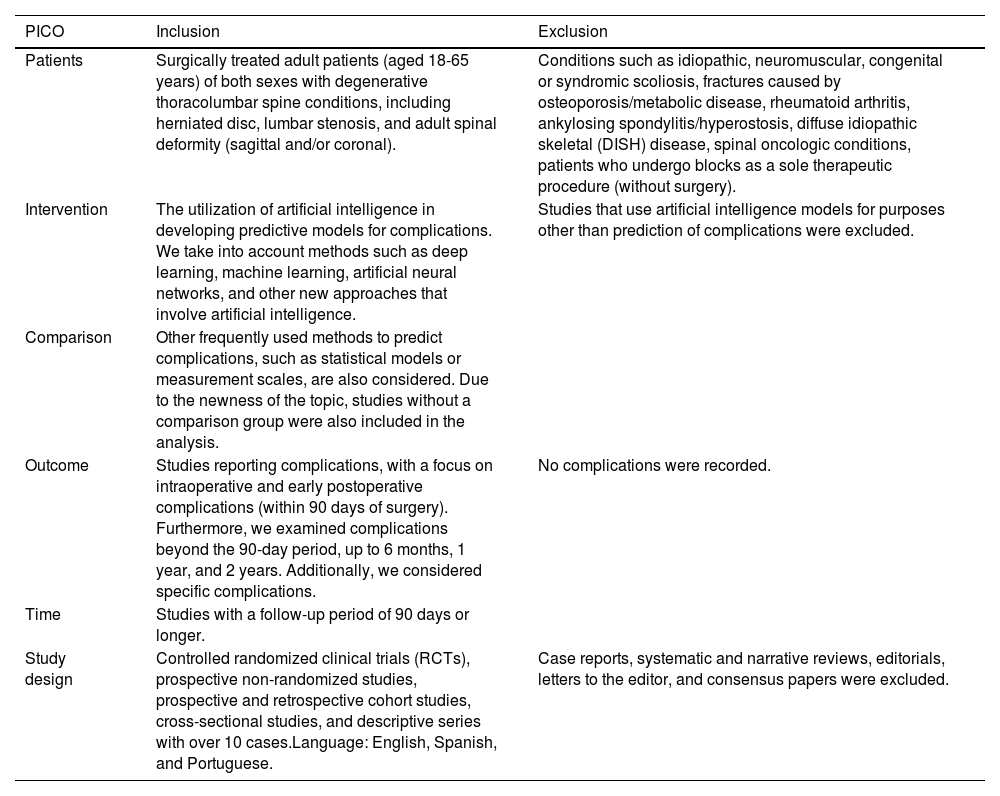
En la tabla 1 se resume la pregunta de investigación de acuerdo con el modelo PICO, que permitió estructurar el problema científico, describir los criterios de elegibilidad y guiar la búsqueda bibliográfica.
Research question according to PICO model
| PICO | Inclusion | Exclusion |
|---|---|---|
| Patients | Surgically treated adult patients (aged 18-65 years) of both sexes with degenerative thoracolumbar spine conditions, including herniated disc, lumbar stenosis, and adult spinal deformity (sagittal and/or coronal). | Conditions such as idiopathic, neuromuscular, congenital or syndromic scoliosis, fractures caused by osteoporosis/metabolic disease, rheumatoid arthritis, ankylosing spondylitis/hyperostosis, diffuse idiopathic skeletal (DISH) disease, spinal oncologic conditions, patients who undergo blocks as a sole therapeutic procedure (without surgery). |
| Intervention | The utilization of artificial intelligence in developing predictive models for complications. We take into account methods such as deep learning, machine learning, artificial neural networks, and other new approaches that involve artificial intelligence. | Studies that use artificial intelligence models for purposes other than prediction of complications were excluded. |
| Comparison | Other frequently used methods to predict complications, such as statistical models or measurement scales, are also considered. Due to the newness of the topic, studies without a comparison group were also included in the analysis. | |
| Outcome | Studies reporting complications, with a focus on intraoperative and early postoperative complications (within 90 days of surgery). Furthermore, we examined complications beyond the 90-day period, up to 6 months, 1 year, and 2 years. Additionally, we considered specific complications. | No complications were recorded. |
| Time | Studies with a follow-up period of 90 days or longer. | |
| Study design | Controlled randomized clinical trials (RCTs), prospective non-randomized studies, prospective and retrospective cohort studies, cross-sectional studies, and descriptive series with over 10 cases.Language: English, Spanish, and Portuguese. | Case reports, systematic and narrative reviews, editorials, letters to the editor, and consensus papers were excluded. |
PICO: P=Patient; I=Intervention; C=Comparator; O=Outcome.
Se desarrolló una estrategia de búsqueda bibliográfica en las bases de datos MEDLINE, Cochrane y LILACS (Literatura Latinoamericana y del Caribe en Ciencias de la Salud) a través de los buscadores Pubmed, Cochrane Library y el portal de la Biblioteca Virtual en Salud (BVS). Adicionalmente, se contemplaron otras fuentes de citas bibliográficas, como la consulta a la biblioteca de la Asociación Argentina de Ortopedia y Traumatología y la búsqueda manual en las listas de referencias de los estudios incluidos o revisiones (narrativas/sistemáticas) identificadas durante la búsqueda (snowballing o bola de nieve).
Estrategia de búsquedaSe desarrolló una estrategia de búsqueda con términos MESH y palabras clave sobre el uso de inteligencia artificial en la predicción de complicaciones de pacientes tratados con cirugías de columna toracolumbar degenerativa. La estrategia fue desarrollada por el equipo de investigadores y se describe a continuación: ((((((artificial intelligence) OR (deep learning)) OR (machine learning)) OR (AI)) OR (inteligencia artificial)) AND (spine)) AND ((((thoracolumbar) OR (lumbar)) OR (thoracic)) OR (lumbosacral)). La búsqueda bibliográfica se limitó, según los filtros de idioma (español, inglés y portugués) y fecha, contemplando como periodo de tiempo el comprendido entre el 1 de enero del 2000 y el 1 de mayo del 2023. No se utilizaron filtros de búsqueda sobre el diseño o tipo de estudio.
Gestión de datosLos resultados de la búsqueda bibliográfica fueron cargados en el programa Zotero, programa para administrar citas bibliográficas y facilitar la colaboración entre los revisores durante el proceso de selección de estudios. Se cargaron los resúmenes. Se eliminaron los duplicados. Antes del proceso de selección formal, se proporcionó capacitación a los miembros del equipo de revisión que no estaban familiarizados con el programa.
Proceso de selecciónLos revisores se agruparon en 2grupos de 2miembros cada uno; ambos grupos examinaron de forma independiente los títulos y resúmenes según los criterios de inclusión. Los desacuerdos fueron resueltos a través de la discusión entre los revisores y, eventualmente, por tercera opinión de un revisor adicional, miembro experimentado del equipo de investigadores. Después de la selección de artículos elegibles para la revisión de texto completo, todos los artículos de texto completo se recuperaron a través de fuentes de la biblioteca. Ambos grupos de revisores procedieron a evaluar los artículos de texto completo que habían sido seleccionados por el otro, y viceversa, (diseño cruzado) para limitar el posible sesgo de selección del revisor. Durante la revisión del texto completo, las referencias de los artículos también se revisaron para determinar su posible elegibilidad (bola de nieve). Nuevamente, cualquier posible conflicto fue resuelto primero por los revisores de cada grupo y, si era necesario, por la tercera opinión de un revisor adicional con experiencia.
Extracción de datosLa extracción de datos fue realizada por duplicado y los revisores a cargo trabajaron de forma independiente. Se registraron los datos en tablas. Una tabla sobre las características de los estudios incluidos contemplaba: autor, año, países participantes enfermedad en estudio, algoritmo utilizado, número de sitios participantes, tamaño de la muestra, variable de resultado (complicaciones en general o de tipo específico), origen de los datos (base de datos), validación, resultados reportados, precisión (porcentaje), área bajo la curva (AUC ROC), características operativas (sensibilidad, especificidad). También se registraron los criterios de inclusión y exclusión, características demográficas de los participantes, periodo de seguimiento, datos sobre financiación y posibles conflictos de interés.
Evaluación del riesgo de sesgoEl riesgo de sesgo de los estudios observacionales no aleatorios se evaluó con la herramienta ROBINS-I5. Para evaluar el riesgo de sesgo en el uso de modelos predictivos de riesgo, se contempló la herramienta PROBAST6. La evaluación del sesgo fue realizada por al menos 2 evaluadores en forma independiente. Los conflictos se resolvieron por consenso.
Para garantizar la consistencia, el autor principal examinó todos los resúmenes y textos completos para verificar su elegibilidad, extrajo los datos y evaluó el riesgo de sesgo en todos los estudios incluidos.
Estrategia para la síntesis de datosPosteriormente, todos los resultados de los revisores individuales se combinaron en una sola tabla de datos. Esta tabla fue discutida con el equipo completo de revisores para llegar a un consenso sobre los resultados de nuestra revisión.
Para la evaluación del rendimiento de los modelos predictivos se contemplará principalmente el AUC, para su categorización se contempló la siguiente clasificación: AUC=0,5 inútil, AUC=0,6-0,7 posiblemente útil; AUC=0,7-0,8 aceptable; AUC=0,8-0,9 excelente y AUC>0,9=excepcional7.
Por otro lado, se consideraron otros parámetros que reflejan el rendimiento de los modelos predictivo: exactitud (accuracy), sensibilidad (recall), especificidad, valor predictivo positivo (precisión).
Para la evaluación de la efectividad de los modelos predictivos frente a otros métodos, contemplamos como alternativas el uso de instrumentos como escalas o puntajes y la comparación con métodos estadísticos tradicionales, ya sea regresión lineal o logística multivariable. Estos métodos de análisis estadísticos mencionados se usan más típicamente para generar modelos clínicos predictivos o pronósticos y su uso puede considerarse como un indicador de rendimiento de referencia. Cabe aclarar que cualquier tipo de algoritmo más avanzado puede contemplarse como una forma de ML.
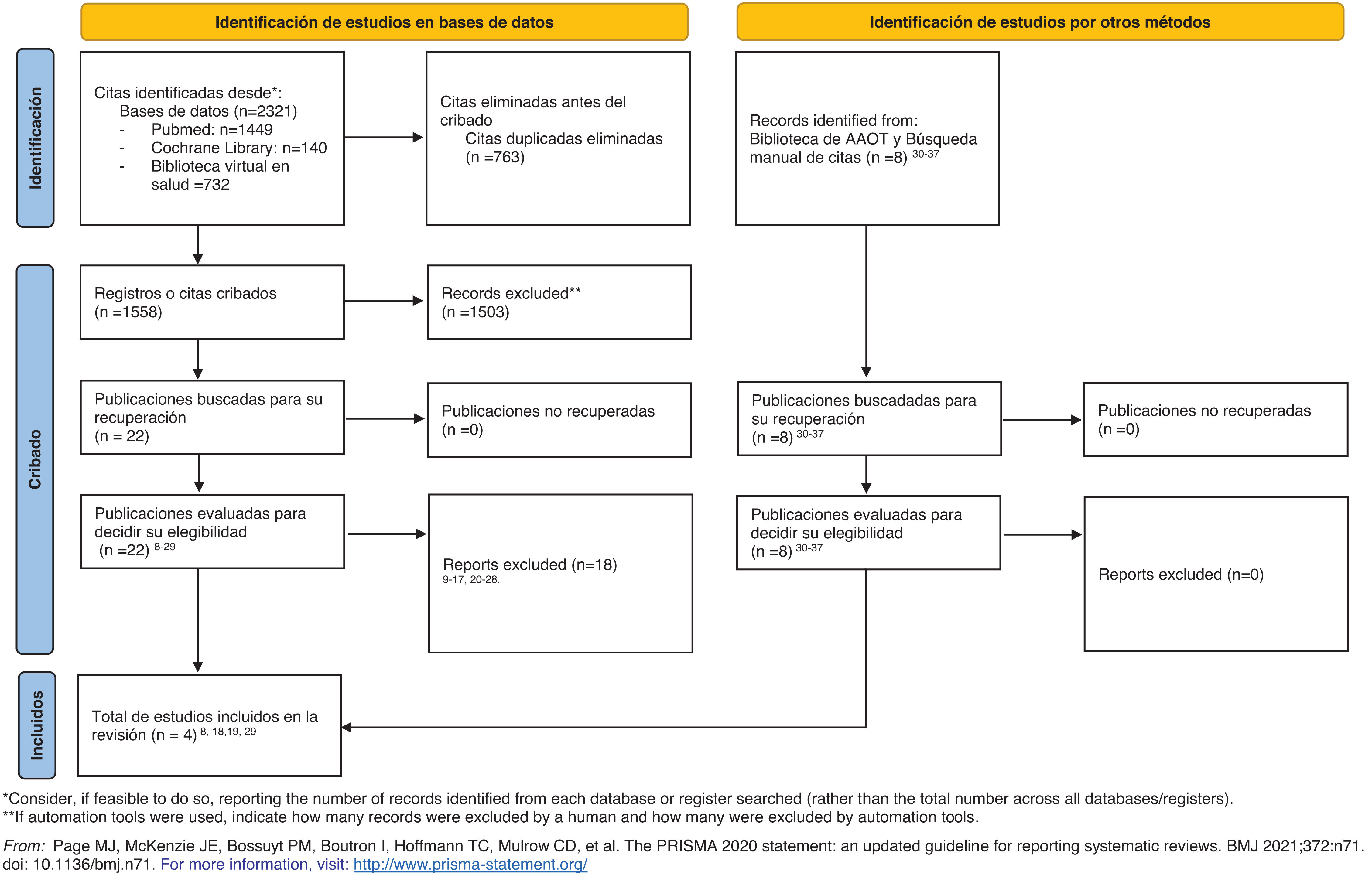
ResultadosSe identificaron un total de 2.321 títulos, de los cuales 763 eran duplicados. Se realizó el cribado (screening) de 1.558 títulos, de los cuales 22 fueron elegidos para su lectura completa8-29. Se excluyeron 18 artículos de acuerdo con los criterios de selección propuestos9-17,20-28. Por último, 4 artículos fueron elegidos para la siguiente revisión8,18,19,29. Además, se recuperaron 8 publicaciones desde otras fuentes (Biblioteca de la Asociación Argentina de Ortopedia y Traumatología y búsqueda manual de citas o snowballing)30-37. La figura 1 presenta el diagrama de flujo PRISMA.
Diagrama de flujo según PRISMA 2020. Page MJ, McKenzie JE, Bossuyt PM, Boutron I, Hoffmann TC, Mulrow CD, et al. The PRISMA 2020 statement: An updated guideline for reporting systematic reviews. BMJ 2021;372:n71. doi: 10.1136/bmj.n71. Para más información: http://www.prisma-statement.org/.
Todos los estudios incluidos describen el desarrollo y la validación interna de modelos predictivos basados en el uso de IA para la predicción de complicaciones en cirugía de columna toracolumbar por enfermedad degenerativa. No se encontraron estudios que lleven a cabo la validación externa de modelos predictivos previamente desarrollados.
De acuerdo al tipo de enfermedad degenerativa, 7 publicaciones (58,3%) incluyen pacientes con escoliosis del adulto30-34,37; 4 (33%) incluyen pacientes con enfermedad degenerativa en general (no escoliosis)18,19,29,36 y una (8,33%) pacientes con espondilolistesis degenerativa, exclusivamente8.
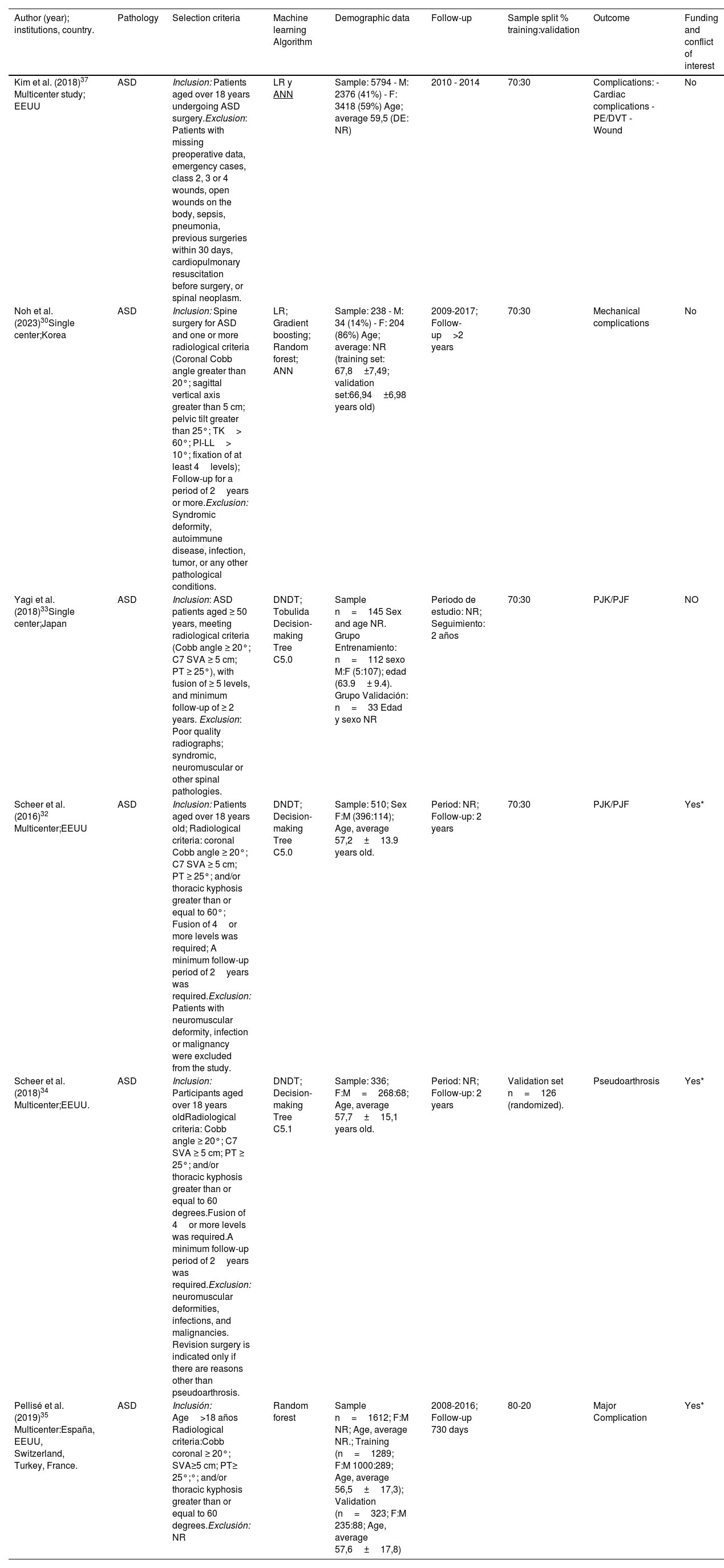
Si bien todas la publicaciones evalúan complicaciones como resultado primario, la variable «complicaciones» registra diferentes definiciones en todas las publicaciones. En 5 artículos (41,6%) se evalúan complicaciones perioperatorias como desenlace primario, incluyendo clínicas y quirúrgicas, sin consenso en la definición8,31,37. En 2 artículos (16,6%) se contempla infección de sitio quirúrgico19,29, en 2 (16,6%) la cifosis o falla de la unión proximal32,33, en uno (8,33%) complicaciones mecánicas agrupadas (falla de unión proximal, cifosis de unión proximal, complicaciones del implante, rotura de barra)30, en otro (8,33%) seudoartrosis34 y en otro (8,33%) trombosis venosa profunda/tromboembolia de pulmón18. En la tabla 2 se resumen las características de los estudios incluidos.
Characteristics of the studies
| Author (year); institutions, country. | Pathology | Selection criteria | Machine learning Algorithm | Demographic data | Follow-up | Sample split % training:validation | Outcome | Funding and conflict of interest |
|---|---|---|---|---|---|---|---|---|
| Kim et al. (2018)37 Multicenter study; EEUU | ASD | Inclusion: Patients aged over 18 years undergoing ASD surgery.Exclusion: Patients with missing preoperative data, emergency cases, class 2, 3 or 4 wounds, open wounds on the body, sepsis, pneumonia, previous surgeries within 30 days, cardiopulmonary resuscitation before surgery, or spinal neoplasm. | LR y ANN | Sample: 5794 - M: 2376 (41%) - F: 3418 (59%) Age; average 59,5 (DE: NR) | 2010 - 2014 | 70:30 | Complications: - Cardiac complications - PE/DVT - Wound | No |
| Noh et al. (2023)30Single center;Korea | ASD | Inclusion: Spine surgery for ASD and one or more radiological criteria (Coronal Cobb angle greater than 20°; sagittal vertical axis greater than 5 cm; pelvic tilt greater than 25°; TK> 60°; PI-LL> 10°; fixation of at least 4levels); Follow-up for a period of 2years or more.Exclusion: Syndromic deformity, autoimmune disease, infection, tumor, or any other pathological conditions. | LR; Gradient boosting; Random forest; ANN | Sample: 238 - M: 34 (14%) - F: 204 (86%) Age; average: NR (training set: 67,8±7,49; validation set:66,94±6,98 years old) | 2009-2017; Follow-up>2 years | 70:30 | Mechanical complications | No |
| Yagi et al. (2018)33Single center;Japan | ASD | Inclusion: ASD patients aged ≥ 50 years, meeting radiological criteria (Cobb angle ≥ 20°; C7 SVA ≥ 5 cm; PT ≥ 25°), with fusion of ≥ 5 levels, and minimum follow-up of ≥ 2 years. Exclusion: Poor quality radiographs; syndromic, neuromuscular or other spinal pathologies. | DNDT; Tobulida Decision-making Tree C5.0 | Sample n=145 Sex and age NR. Grupo Entrenamiento: n=112 sexo M:F (5:107); edad (63.9± 9.4). Grupo Validación: n=33 Edad y sexo NR | Periodo de estudio: NR; Seguimiento: 2 años | 70:30 | PJK/PJF | NO |
| Scheer et al. (2016)32 Multicenter;EEUU | ASD | Inclusion: Patients aged over 18 years old; Radiological criteria: coronal Cobb angle ≥ 20°; C7 SVA ≥ 5 cm; PT ≥ 25°; and/or thoracic kyphosis greater than or equal to 60°; Fusion of 4or more levels was required; A minimum follow-up period of 2years was required.Exclusion: Patients with neuromuscular deformity, infection or malignancy were excluded from the study. | DNDT; Decision-making Tree C5.0 | Sample: 510; Sex F:M (396:114); Age, average 57,2±13.9 years old. | Period: NR; Follow-up: 2 years | 70:30 | PJK/PJF | Yes* |
| Scheer et al. (2018)34 Multicenter;EEUU. | ASD | Inclusion: Participants aged over 18 years oldRadiological criteria: Cobb angle ≥ 20°; C7 SVA ≥ 5 cm; PT ≥ 25°; and/or thoracic kyphosis greater than or equal to 60 degrees.Fusion of 4or more levels was required.A minimum follow-up period of 2years was required.Exclusion: neuromuscular deformities, infections, and malignancies. Revision surgery is indicated only if there are reasons other than pseudoarthrosis. | DNDT; Decision-making Tree C5.1 | Sample: 336; F:M=268:68; Age, average 57,7±15,1 years old. | Period: NR; Follow-up: 2 years | Validation set n=126 (randomized). | Pseudoarthrosis | Yes* |
| Pellisé et al. (2019)35 Multicenter:España, EEUU, Switzerland, Turkey, France. | ASD | Inclusión: Age>18 años Radiological criteria:Cobb coronal ≥ 20°; SVA≥5 cm; PT≥ 25°;°; and/or thoracic kyphosis greater than or equal to 60 degrees.Exclusión: NR | Random forest | Sample n=1612; F:M NR; Age, average NR.; Training (n=1289; F:M 1000:289; Age, average 56,5±17,3); Validation (n=323; F:M 235:88; Age, average 57,6±17,8) | 2008-2016; Follow-up 730 days | 80-20 | Major Complication | Yes* |
| Author (year); institutions, country. | Pathology | Selection criteria | Machine learning Algorithm | Demographic data | Follow-up | Sample split % training:validation | Outcome | Funding and conflict of interest |
|---|---|---|---|---|---|---|---|---|
| Xiong (2022)29 Single center; China. | DSD | Inclusion: Patients aged 18 years or older with degenerative lumbar disease which includes herniated disc, lumbar stenosis, spondylolisthesis, or instability and have undergone posterior lumbar interbody fusion (at least one level). Exclusion: history of spine surgery, active infection or tumor, and deformity. | Boosted Classification Trees, Boosted Logistic Regression, Extreme Gradient Boosting, Stochastic Gradient Boosting, Generalized Linear Model, AdaBoost Classification Trees*, and Random Forest. | Sample: 584; F:M 321:263; Age, average 58,36±13:76 years old; Disc herniation: 284; Lumbar stenosis:137; spondylolisthesis/instability: 163. | 2019-2021 Follow-up: 90 days. | 50:50 | Surgical site infection | No |
| Fatima (2020)8 Multicenter study; EEUU. | DSD | Inclusión: Cirugía de descompresión, artrodesis o instrumentación de la columna lumbar; espondilolisgtesis degenerativa lumbar; Operados entre 2005 y 2016; por neurocirugía o traumatología, bajo anestesia general y pacientes internados. Exclusión: NR | LR y LASSO: least absolute shrinkage and selection operator | Sample: 80610; Age, median 58 years old (range:18-89); F:M 38874:41654. | 2005-2016 Follow-up: 30 days | 70:30 | Advetrse events | No |
| Zehnder (2021)36 Multicenter study. Switzerland, UK, Italy. | DSD | Inclusión: cirugía de columna por enfermedad lumbar degenerativa; Edad 18-95 años. Exclusión: casos con datos perdidos. | Shrinkage Algorithm (dfbeta method) | Sample: 23714; F:M 12264:11450; Age, average 58,9±15,7 years old. | 2012-2017 Follow-up until hospital discharge. | NR | Surgical complications: perioperative and general. | No |
| Scheer (2017)31 Multicenter study; EEUU | ASD | Inclusión: Edad>18 años Criterios radiológicos:Cobb coronal ≥ 20°; SVA≥5 cm; PT≥ 25°; o cifosis torácica ≥60°. Exclusión: deformidad neuromuscular, infección o neoplasia maligna. | DNDT; Decision-making Tree C5.0 | Sample: 557 F:M=439:118; Age, average 57,5±15,3 years old. | Period: NR; Follow-up: 6 weeks. | 70:30 | Major Complication | Yes* |
| Wang (2021)18 Multicenter study. EEUU | DSD | Inclusión: fusion lumbar posterior (1 nivel). Exclusión: trauma, tumores, cirugía de revisión. | XGBoost (extreme gradient boosting) | Sample n=13500 Age, categories n(%): 19-34 years old=490 (3,63); 35-49 years old=2146(15,9); 50-65 years old=5050 (37,41);>65 years old=5814(43,07). F:M 7516:5984. | 2010-2017 Follow-up: 30 days. | 80:20 | PE/DVT | No |
| Liu (2022)19 Single center;China | DSD | Inclusión: enfermedad lumbar degenerativa (estenosis de canal; hernia de disco; espondilolistesis degenerativa); Cirugía vía posterior única; Cirugía electiva. Exclusión: cirugía de urgencia. | RL, multilayer perceptron, decision tree, random forest, gradient boosting machine, and XGBoost (extreme gradient boosting) | Sample: 288; Age, average: 55,3±12,3 F:M NR | 2010-2019Follow-up: NR | 70:30 | Surgical site infection | Yes* |
Abbreviations: ASD=Adult Spinal Deformity; ANN=Artificial Neural Network; DNDT=Deep Neural Decision Tree; F:M=Female:Male; NR=Not reported; SD=Standard deviation; PE/DVT=Pulmonary embolism/Deep venous thrombosis; PJK/PJF=Proximal junctional kyphosis/failure; SVA:Sagittal vertical alignment; PT=Pelvic tilt; PI=Pelvic incidence; PI-LL=Pelvic incidence minus lumbar lordosis.
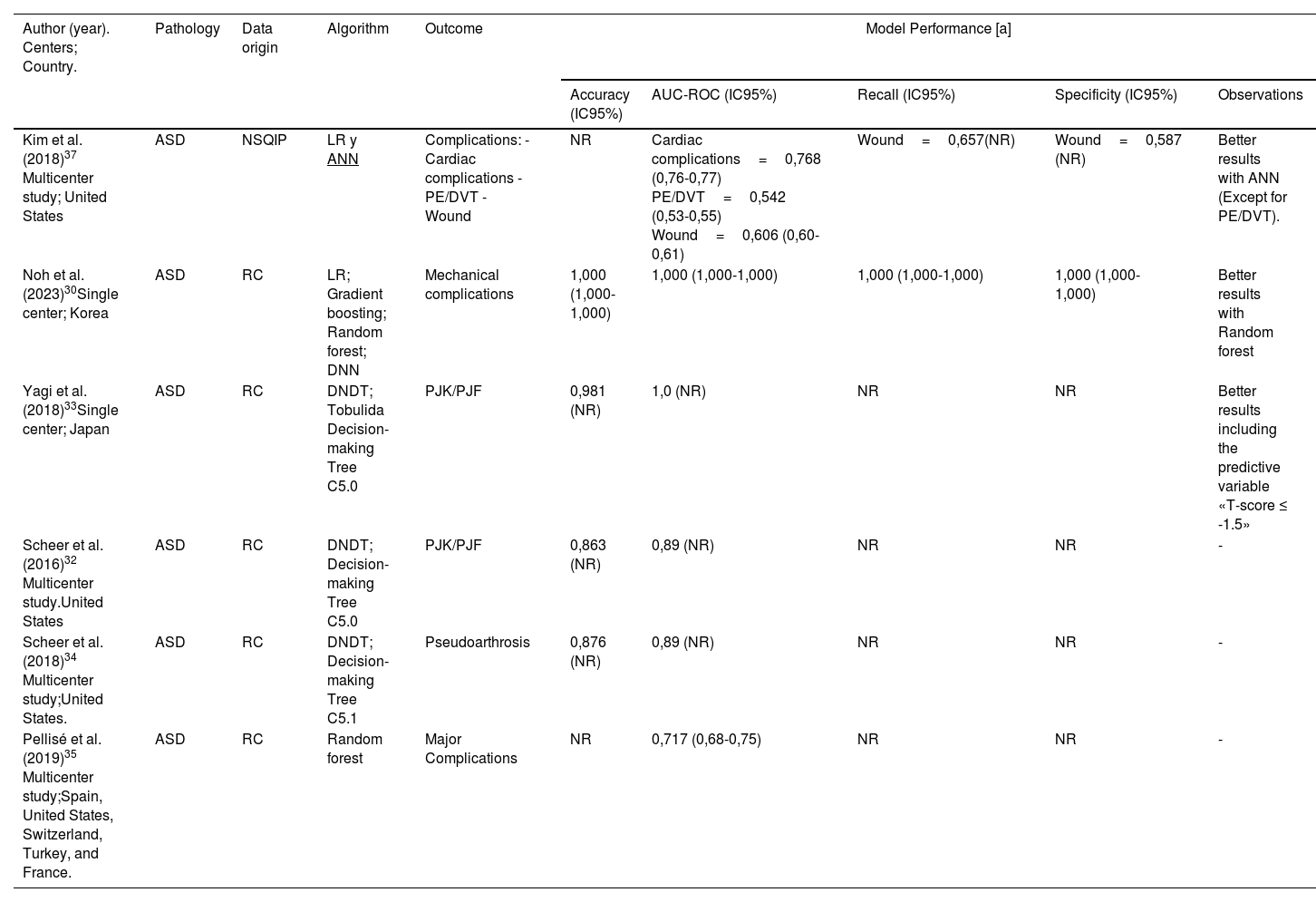
Las medidas comúnmente utilizadas para evaluar el rendimiento de los modelos predictivos fueron el área bajo la curva (n=12; 100%) y la exactitud (accuracy) del modelo (n=7; 58,3%). En menor medida, fueron reportados sensibilidad (recall; n=4; 33%, especificidad n=3; 25%) y, rara vez, el valor predictivo positivo (precisión). El rendimiento de los modelos predictivos fue variable, según el resultado contemplado (complicaciones generales versus específicas) y el tipo modelo de aprendizaje mecánico utilizado. Considerando el modelo con mejor rendimiento de cada publicación, el área bajo la curva (AUC) osciló entre 0,6 y 1,0; fue excelente o excepcional (AUC>0,8) en más de la mitad de las publicaciones (n=7; 58,3%)19,29-34. En las otras 5 publicaciones el rendimiento según el AUC fue aceptable (AUC=0,7-0,8) en al menos una de las variables de resultado analizadas8,18,35-37. La mitad de los estudios no reportaron la precisión (IC95%) del AUC estimada. Los resultados de los estudios se describen en la tabla 3.
Results of the studies
| Author (year). Centers; Country. | Pathology | Data origin | Algorithm | Outcome | Model Performance [a] | ||||
|---|---|---|---|---|---|---|---|---|---|
| Accuracy (IC95%) | AUC-ROC (IC95%) | Recall (IC95%) | Specificity (IC95%) | Observations | |||||
| Kim et al. (2018)37 Multicenter study; United States | ASD | NSQIP | LR y ANN | Complications: - Cardiac complications - PE/DVT - Wound | NR | Cardiac complications=0,768 (0,76-0,77) PE/DVT=0,542 (0,53-0,55) Wound=0,606 (0,60-0,61) | Wound=0,657(NR) | Wound=0,587 (NR) | Better results with ANN (Except for PE/DVT). |
| Noh et al. (2023)30Single center; Korea | ASD | RC | LR; Gradient boosting; Random forest; DNN | Mechanical complications | 1,000 (1,000-1,000) | 1,000 (1,000-1,000) | 1,000 (1,000-1,000) | 1,000 (1,000-1,000) | Better results with Random forest |
| Yagi et al. (2018)33Single center; Japan | ASD | RC | DNDT; Tobulida Decision-making Tree C5.0 | PJK/PJF | 0,981 (NR) | 1,0 (NR) | NR | NR | Better results including the predictive variable «T-score ≤ -1.5» |
| Scheer et al. (2016)32 Multicenter study.United States | ASD | RC | DNDT; Decision-making Tree C5.0 | PJK/PJF | 0,863 (NR) | 0,89 (NR) | NR | NR | - |
| Scheer et al. (2018)34 Multicenter study;United States. | ASD | RC | DNDT; Decision-making Tree C5.1 | Pseudoarthrosis | 0,876 (NR) | 0,89 (NR) | NR | NR | - |
| Pellisé et al. (2019)35 Multicenter study;Spain, United States, Switzerland, Turkey, and France. | ASD | RC | Random forest | Major Complications | NR | 0,717 (0,68-0,75) | NR | NR | - |
| Author (year). Centers; Country. | Pathology | Data origin | Algorithm | Outcome | Model performance [a] | ||||
|---|---|---|---|---|---|---|---|---|---|
| Accuracy (IC95%) | AUC-ROC (IC95%) | Recall (IC95%) | Specificity (IC95%) | Observations | |||||
| Xiong (2022)29 Single center; China. | DSD | RC | Boosted Classification Trees, Boosted Logistic Regression, Extreme Gradient Boosting, Stochastic Gradient Boosting, Generalized Linear Model, AdaBoost Classification Trees*, and Random Forest. | Surgical site infection | 0,8247 (NR) | 0,906 (NR) | 0,9375 (NR) | 0,818 (NR) | Better results with AdaBoost Classification Tress |
| Fatima (2020)8 Multicenter study; EEUU. | ESD | NSQIP | LR y LASSO: least absolute shrinkage and selection operator | Advetrse events | NR | General: 0.70 (0.62-0.74); Surgical complications 0,70 (NR); Clinical complications 0,70 (NR) | NR | NR | Better results with LR |
| Zehnder (2021)36 Multicenter study. Switzerland, UK, Italy. | DSD | EUROSPINE Spine Tang | Shrinkage Algorithm (dfbeta method) | Surgical complications: perioperative and general. | NR | Generales 0.74 (0.72-0.76); Quirúrgicas 0.64 (0.62-0.65). | NR | NR | - |
| Scheer (2017)31 Multicenter study; EEUU | ASD | RC | DNDT; Decision-making Tree C5.0 | Major Complication | 0,876 (NR) | 0,89 (NR) | NR | NR | - |
| Wang (2021)18 Multicenter study. EEUU | DSD | NSQIP | XGBoost (extreme gradient boosting) | PE/DVT | NR | 0,716 (0,701-0,731) | NR | NR | - |
| Liu (2022)19 Single center;China | DSD | RC | LR, multilayer perceptron, decision tree, random forest, gradient boosting machine, and XGBoost (extreme gradient boosting) | Surgical site infection | 0,860 (NR) | 0,923 (NR) | 0,834 (NR) | NR | Better results with XGBoost |
Abbreviations: ANN=Artificial Neural Network; ASD=Adult Spinal Deformity; AUC=Area Under the Curve; DNDT=Deep Neural Decision Tree; DNN=Deep Neural Network; DSD=Degenerative Spine disorders; LR=Logistic Regression; NR=Not reported; NSQIP=The National Surgical Quality Improvement Program; PE/DVT=Pulmonary Embolism/Deep Vein Thrombosis; PJK/PJF=Proximal Junctional Kyphosis/Proximal Junctional Failure; RC=retrospective cohort; SSIs=Surgical Site Infections.
[a]=In case of multiple predictive models, results of the best predictive model are reported.
En 5 publicaciones (41,6%) se comparó la efectividad de modelos predictivos de IA para la predicción de complicaciones generales o específicas8,18,19,30,37.
Kim et al. compararon el rendimiento del algoritmo predictivo de aprendizaje mecánico basado en una red neuronal artificial (ANN) con la regresión logística y la escala de la American Society of Anesthesiologists (ASA) de evaluación preanestésica para la predicción de 3 variables de resultados (complicaciones cardíacas, trombosis venosa profunda/tromboembolia de pulmón/complicaciones de la herida); el desempeño según el AUC del algoritmo predictivo de IA fue superior en 2 de los 3 resultados estimados a la regresión logística (excepto en la predicción de trombosis venosa profunda/tromboembolia de pulmón) y en todos con respecto a la escala ASA. Adicionalmente, la sensibilidad de ANN fue mayor que la de la regresión logística en la predicción de complicaciones de heridas37: [ANN AUC: complicaciones cardíacas 0,768 (IC95%: 0,76-0,77); TVP/TEP: 0,542 (IC95%: 0,53-0,55); complicaciones de la herida 0,606 (IC95%: 0,60-0,61). Regresión logística AUC: complicaciones cardíacas 0,690 (IC95%: 0,68-0,69); TVP/TEP: 0,547 (IC95%: 0,54-0,55); complicaciones de la herida 0,575 (IC95%: 0,56-0,58); ASA AUC: complicaciones cardíacas 0,469 (IC95%: 0,46-0,47); TVP/TEP: 0,485 (IC95%: 0,47-0,49); complicaciones de la herida 0,508 (IC95%: 0,50-0,51)].
En la publicación de Wang et al. sobre la predicción de trombosis venosa profunda/tromboembolia de pulmón, el AUC del modelo predictivo (0,716; IC95%: 0,701-0,731) de aprendizaje mecánico fue significativamente mayor (p<0,001) que el AUC para el ASA y del Charlson Comorbidity Index18.
Noh et al. compararon 3 modelos de predictivos de aprendizaje mecánico (gradientboosting, randomforest y deep neural network) con regresión logística. El modelo de IA random forest [AUC=1.000 (IC95%: 1.000-1.000)] logró el mejor rendimiento predictivo30.
Fatima et al. compararon el modelo predictivo de aprendizaje mecánico (LASSO) con 2índices de fragilidad (mFI-5 y mFI-11) y con el método de regresión logística. El rendimiento del modelo predictivo basado en IA [AUC: 0,65; IC95%: 0,61-0,69] fue menor que el de la regresión logística [AUC=0,70; IC95%: 0,62-0,74] para la predicción general de episodios adversos y para los específicos. No obstante, el rendimiento fue significativamente mejor (p<0,001) que con los 2índices de fragilidad [mFI-5 AUC=0,50 (IC 95%: 0,47-0,53); mFI-11 AUC=0,56 (IC95%: 0,54-0,59)]8.
Liu et al. compararon el rendimiento de 6 modelos predictivos incluyendo la regresión logística (AUC=0,871) y determinaron que el modelo extreme gradient boosting tuvo el mejor rendimiento de predicción (AUC=0,923)19.
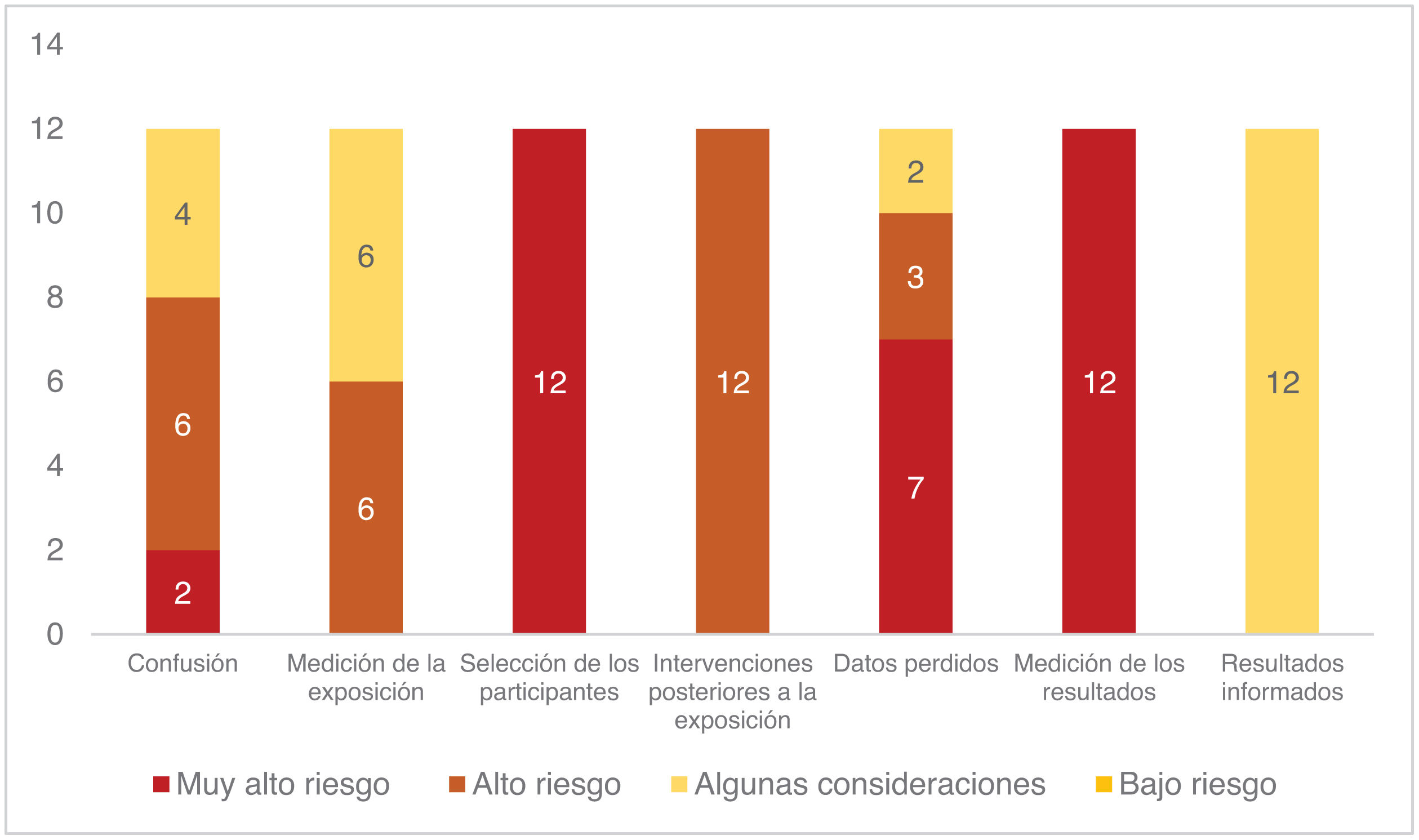
Riesgo de sesgoUtilizando la herramienta Robins-E (The Risk Of Bias In Non-randomized Studies of Exposure) para la evaluación del riesgo de sesgo en estudios observacionales no aleatorizados, todos los artículos incluidos fueron catalogados globalmente con muy alto riesgo de sesgo, con riesgo alto o muy alto en casi todos los dominios de la herramienta (confusión, medición de la exposición, selección de los participantes, datos perdidos (fig. 2).
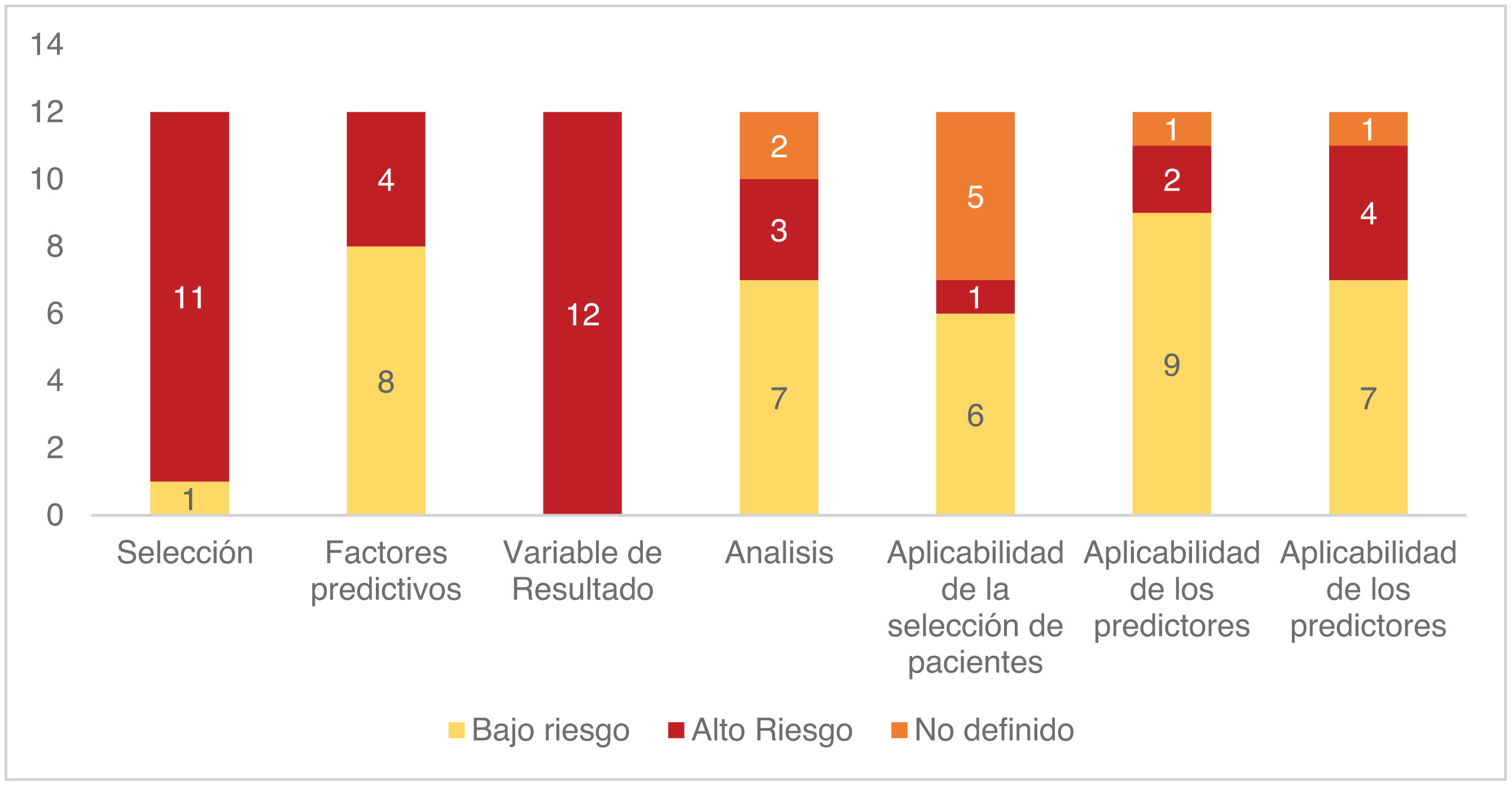
Con la herramienta PROBAST (Prediction Model Risk Of Bias Assessment Tool) todos los estudios (n=12; 100%) presentaron alto riesgo de sesgo en al menos uno de los 4dominios que conforman la escala (sesgo de selección; sesgo asociado con los factores predictivos; sesgo en la valoración del resultado; sesgo en el análisis). La selección de los pacientes y la valoración de la variable de resultado fueron los 2dominios valorados más frecuentemente con alto riesgo de sesgo (fig. 3).
Dada la heterogeneidad de las muestras (cohortes o bases de datos), los resultados de interés (definición de complicaciones) y las métricas de evaluación de los algoritmos, no se realizó un metaanálisis.
DiscusiónEl campo de la IA incluye diversas áreas con aplicaciones actuales o potenciales en el cuidado de la salud. Entre ellas, el ML (foco de esta revisión), el procesamiento del lenguaje natural utilizado en chatbots, la realidad aumentada, mixta y virtual, y la cirugía robótica. Estas tecnologías no solo impactan la cirugía de columna, sino también amplias áreas de la práctica médica y otras disciplinas3,4,38.
El aprendizaje mecanizado es una rama de la IA que permite a las computadoras aprender. Implica el desarrollo de algoritmos que mejoran su rendimiento con la experiencia y la incorporación de nuevos datos al sistema permite mejorar su rendimiento7. El aprendizaje mecanizado tiene una amplia gama de aplicaciones, una de ellas es el desarrollo de modelos predictivos mutlivariable3,4. Un modelo de predicción multivariable es una ecuación matemática que relaciona múltiples predictores (factores de riesgo, predictivos, variables independientes, covariables) para un individuo particular con la probabilidad o el riesgo de la presencia (diagnóstico) o la ocurrencia futura (pronóstico) de un resultado particular38. El desarrollo de modelos predictivos implica la selección de predictores y su combinación en un modelo multivariable. Tradicionalmente, la estimación de resultados pronósticos multivariables se basaba en técnicas estadísticas, como la regresión logística y la regresión de Cox37. El uso de técnicas de IA permite enfrentar un factor limitante de la metodología estadística tradicional, que es que la condición de que el poder estadístico disminuye a medida que crece la dimensión del análisis multivariado. Además, en el aprendizaje mecanizado no se propone necesariamente una hipótesis predeterminada al inicio del estudio y los algoritmos pueden correlacionar información y asociaciones, que de otro modo, podrían haberse pasado por alto o haber pasado desapercibidos debido a su complejidad y orígenes multifactoriales3.
En esta revisión, los autores nos propusimos evaluar la efectividad de los modelos predictivos basados en IA para la predicción de complicaciones en pacientes tratados mediante cirugías de columna vertebral toracolumbar degenerativa. Como resultado, no encontramos evidencias robustas en favor del rendimiento de algoritmos basados en IA frente a otros métodos predictivos tradicionales. Predominaron los estudios de desarrollo y validación interna de modelos predictivos con buen rendimiento según el AUC, que osciló mayoritariamente entre aceptable y excelente. No obstante, solo 5 (41%) estudios compararon su rendimiento con técnicas estadísticas tradicionales o con escalas o sistemas de puntajes8,18,19,30,37.
La evidencia fue débil, debido al alto riesgo de sesgo en todos de los estudios, con predominio de los sesgos en la evaluación de la variable de resultado y la selección de los pacientes. En las publicaciones recuperadas existe una heterogeneidad en la definición de la variable de resultado «complicaciones» que impide sintetizar los datos y guiar una recomendación. En ocasiones, la definición de complicación perioperatoria incluyó las acontecidas durante el intraoperatorio y el postoperatorio inmediato, lo cual, según criterio de los investigadores es una debilidad, ya que pueden estar condicionadas por diferentes variables de riesgo y agruparlas adhiere la posibilidad de sesgo de confusión8,31,35,36. Por otra parte, en algunas de las publicaciones, la estimación de la complicación fue realizada en función de la información disponible en bases de datos nacionales, previamente confeccionadas para otro fin y con tiempos de seguimiento limitados (30 días)18,37.
Cabe destacar que, en una especialidad quirúrgica cuyo desempeño puede verse condicionado por el medio, la experiencia de los cirujanos-instituciones, los recursos y características del sistema de salud de cada país o región, es difícil expresar los beneficios de algoritmos predictivos de complicaciones quirúrgicas sobre muestras conformadas por cohortes retrospectivas de un solo centro, cohortes multicéntricas no representativas, bases de datos confeccionadas con otra finalidad o muestras obtenidas por técnicas de muestreo no probabilístico sujetas al sesgo de selección. Por otro lado, podemos mencionar otras fuentes principales de sesgo en las publicaciones incluidas en esta revisión como: la falta de estudios prospectivos o muestras de casos seleccionados al azar o la ausencia de estudios de validación externa de los algoritmos predictivos que permitan estimar su rendimiento con datos ajenos a la base de datos utilizada para su desarrollo, entrenamiento y validación. Solo la mitad de los artículos publicaron los puntos estimados (ejemplo el AUC) con sus respectivos intervalos de confianza, lo que impide valorar la precisión de las estimaciones.
A pesar de lo dicho y a la evidente baja calidad de la evidencia disponible, los autores observamos una tendencia hacia el beneficio del uso de modelos predictivos basados en IA como herramienta para conocer el riesgo individual de complicaciones de la cirugía de columna en pacientes con enfermedad vertebral toracolumbar degenerativa. En un futuro cercano, estas técnicas podrían guiar la toma de decisiones de los cirujanos de columna. Estimar el riesgo quirúrgico en un paciente dado representa un verdadero desafío por la gran cantidad de variables que interactúan de forma compleja e impactan sobre el riesgo general. Variables que comprenden características que pueden generalizarse y otras que son propias del medio. Por ende, el registro de datos propios locales y regionales es la base para el desarrollo de futuros algoritmos predictivos que permitan reconocer el riesgo de nuestros pacientes con exactitud y precisión.
Esta revisión tiene como limitaciones predominantes que cierta bibliografía relevante puede no haberse recuperado debido a que la búsqueda se hizo exclusivamente en las bases de datos MEDLINE, Cochrane Library y Lilacs. La búsqueda fue restringida a artículos en inglés, español y portugués. Además, no fue consultada la bibliografía gris. Existen consensos sobre el adecuado reporte de investigaciones de algoritmos predictivos, lo que permitiría una selección más rigurosa de los artículos para la síntesis de datos. Sin embargo, la escasez de estudios disponibles y la falta de revisiones sistemáticas previas sobre el tema llevaron a los autores de la presente revisión a adoptar criterios de elegibilidad más flexibles.
ConclusionesEsta revisión sistemática proporciona una visión actualizada sobre la aplicación de modelos predictivos de IA, en particular, el aprendizaje mecanizado, para la identificación del riesgo de complicaciones en pacientes tratados mediante cirugía por enfermedad degenerativa de la columna toracolumbar. Si bien la evidencia disponible es limitada y presenta un alto riesgo de sesgo, los estudios analizados indican que estos modelos pueden alcanzar un desempeño prometedor en la predicción de complicaciones, con valores del AUC que en su mayoría oscilan entre aceptables y excelentes. Son necesarias investigaciones futuras con bases de datos regionales, metodologías más robustas y validaciones externas que permitan mejorar la confiabilidad y aplicabilidad de estos modelos.
Nivel de evidenciaNivel de evidencia III.
FinanciaciónSin financiación externa.
Consideraciones éticasEl siguiente trabajo es una revisión sistemática de la bibliografía, basada en datos de estudios primarios publicados, por lo cual esta exceptuada de evaluación por un comité de ética. No incluye datos primarios de pacientes ni animales.
Conflicto de interesesLos autores no tienen conflictos de interés que declarar.
Los autores agradecen al Dr. Víctor Barrientos, del Hospital del Trabajador (Santiago, Chile) su ayuda con la metodología.