Analizar en la práctica clínica diaria española la efectividad y seguridad de rivaroxaban vs. el tratamiento estándar (TE) en la prevención del tromboembolismo venoso tras artroplastia de cadera o rodilla.
Material y métodoSubanálisis de datos españoles del estudio observacional internacional XAMOS, que incluyó a pacientes>18 años que recibieron 10mg o.d. rivaroxaban o TE. Seguimiento: hasta 3 meses tras la cirugía. Variables primarias: incidencia de eventos tromboembólicos sintomáticos/asintomáticos, sangrados, mortalidad, otros acontecimientos adversos; variables secundarias: consumo de recursos sanitarios/satisfacción tras el alta.
ResultadosSe incluyeron 801 pacientes: 410 recibieron rivaroxaban y 391 TE (un 64,7% heparina, un 24% fondaparinux y un 11% dabigatran). La incidencia de eventos tromboembólicos sintomáticos y de sangrado mayor fue similar en ambos grupos (0,2 vs. 0,8% con TE y 0,7 vs. 1,3% con TE [criterios EMA]/0 vs. 0,3% con TE [criterios RECORD]). La incidencia de acontecimientos adversos relacionados con el fármaco fue significativamente superior con rivaroxaban (globales: 4,4 vs. 0,8% con TE [p=0,001]; graves: 1,5 vs. 0% con TE [p=0,03]). El grupo rivaroxaban consumió menos recursos sanitarios tras el alta y consideró la tolerabilidad «muy buena» y el tratamiento «muy cómodo» en una proporción mayor.
DiscusiónRivaroxaban es al menos tan efectivo como el TE en la prevención del tromboembolismo venoso en la práctica clínica diaria, con una incidencia similar de hemorragias. Aporta mayor satisfacción/comodidad, y menor gasto de recursos sanitarios tras el alta. Estos resultados han de ser interpretados considerando a las limitaciones inherentes a los estudios observacionales.
To analyse the effectiveness and safety of rivaroxaban vs. standard treatment (ST) in the prevention of venous thromboembolism after hip or knee replacement in daily clinical practice in Spain.
Material and methodA sub-analysis of the Spanish data in the XAMOS international observational study that included patients>18 years who received 10mg o.d. rivaroxaban or ST. Follow-up: up to 3 months after surgery. Primary outcomes: incidence of symptomatic/asymptomatic thromboembolic events, bleeding, mortality, and other adverse events; Secondary outcomes: use of health resources and satisfaction after hospital discharge.
ResultsOf the total 801 patients included, 410 received rivaroxaban and 391 ST (64.7% heparin, 24.0% fondaparinux, 11% dabigatran). The incidence of symptomatic thromboembolic events and major bleeding was similar in both groups (0.2% vs. 0.8% wit ST and 0.7% vs. 1.3% with ST [EMA criteria]/0.0% vs. 0.3% with ST [RECORD criteria]). The adverse events incidence associated with the drug was significantly higher rivaroxaban (overall: 4.4% vs. 0.8% with ST, P=.001; serious: 1.5% vs. 0.0% with ST, P=.03). The rivaroxaban used less health resources after discharge, and the majority considered the tolerability as «very good« and the treatment as «very comfortable».
DiscussionRivaroxaban is at least as effective as ST in the prevention of venous thromboembolism prevention in daily clinical practice, with a similar incidence of haemorrhages. It provides greater satisfaction/comfort, and less health resources after discharge. These results should be interpreted taking into account the limitations inherent in observational studies.
La enfermedad tromboembólica venosa (ETV) es una dolencia grave, a menudo asintomática, que es frecuente en pacientes que han sido sometidos a artroplastia de rodilla o de cadera1. Debido a su naturaleza crónica, a sus frecuentes recurrencias y a las complicaciones asociadas, la ETV tiene un importante impacto sobre el paciente2 y se asocia a una alta morbimortalidad3. Su manejo consume una importante cantidad de recursos sanitarios4. El progresivo envejecimiento de la población, que conllevará un aumento de las artroplastias de cadera o rodilla, contribuirá de forma importante a incrementar la enorme carga de la ETV en la sociedad3. La prevención de la ETV puede devenir un pilar esencial en la reducción de sus consecuencias.
La necesidad de realizar tromboprofilaxis perioperatoria en pacientes quirúrgicos es incuestionable en nuestros días5,6. Actualmente se dispone de tratamientos farmacológicos como las heparinas de bajo peso molecular, los antagonistas de la vitamina K, la heparina no fraccionada, el fondaparinux y, más recientemente, los nuevos anticoagulantes orales directos. La evidencia acerca de la efectividad y la seguridad de los anticoagulantes orales en las condiciones reales de la práctica clínica, normalmente alejada de las condiciones ideales de los ensayos clínicos, es limitada.
El estudio internacional en fase iv XAMOS (XArelto in the prophylaxis of postsurgical VTE after elective Major Orthopaedic Surgery of hip or knee) fue diseñado con el fin de analizar, en la práctica clínica diaria, la efectividad y la seguridad de rivaroxaban en pacientes sometidos a artroplastia de cadera o rodilla en comparación con las de otros tratamientos tromboprofilácticos estándar (TE). Este estudio, en el que participaron 252 centros de 37 países, con un total de 17.701 pacientes, ha confirmado el perfil beneficio-riesgo de rivaroxaban observado en el programa de ensayos clínicos en fase iii RECORD7, en el que una dosis única diaria de 10mg de rivaroxaban fue más eficaz que enoxaparina subcutánea, con un perfil de seguridad similar, en pacientes sometidos a artroplastia de cadera (RECORD 1 y 2)8,9 o de rodilla (RECORD 3 y 4)10,11. Este estudio ha permitido, además, el análisis de aspectos que no son posibles de analizar en ensayos clínicos controlados, como es la utilización de recursos sanitarios.
Los estudios observacionales internacionales como el XAMOS agrupan datos de una gran cantidad de países que presentan una amplia variedad de perfiles de pacientes, de estándares sanitarios y de actuaciones clínicas guiadas por instituciones nacionales o supranacionales. En la presente publicación presentamos los resultados obtenidos en los centros participantes del estudio XAMOS en España con el fin de analizar el manejo de pacientes y la efectividad y seguridad de rivaroxaban frente el TE en las condiciones particulares de nuestro entorno.
Material y métodoDiseño y participantesXAMOS fue un estudio prospectivo, abierto, multicéntrico y no intervencionista. La inclusión de pacientes tuvo lugar desde febrero de 2009 hasta junio de 2011. Se incluyeron pacientes mayores de 18 años que fueran a someterse a una artroplastia de cadera o rodilla, en los que se hubiese tomado la decisión de administrar tratamiento tromboprofiláctico y que hubiesen firmado un documento de consentimiento informado. Los criterios de exclusión se basaron en las contraindicaciones especificadas en las fichas técnicas de los tratamientos antitrombóticos administrados de cada país. El diseño y la metodología del estudio XAMOS han sido detallados con anterioridad12, por lo que a continuación se describen brevemente aquellos aspectos relevantes para el análisis de datos recogidos en España.
Cada médico participante determinó el tipo, la dosis y la duración de cada uno de los tratamientos tromboprofilácticos administrados e incluyó un número similar de pacientes en ambos grupos de tratamiento. El estudio siguió la regulación y las recomendaciones relacionadas con la realización de estudios no intervencionistas, las normas de buena práctica clínica y lo establecido por las leyes, regulaciones y organizaciones pertinentes locales. El protocolo fue aprobado por los comités éticos/paneles de revisión institucionales correspondientes. Número de registro: NCT00831714 (ClinicalTrials.gov).
Recogida de datos y seguimientoLa recogida de datos de los pacientes se estructuró en 4 visitas. En la visita basal (inclusión en el estudio; V0) se recogieron datos demográficos y antropométricos (edad, sexo, raza, índice de masa corporal), el historial médico, las enfermedades concomitantes y la toma medicamentos, y el lugar de la artroplastia. Durante la visita 1 (V1), que incluye el tiempo desde que el paciente ingresado es sometido a la intervención quirúrgica y comienza el tratamiento tromboprofiláctico hasta el alta hospitalaria, se recogieron los siguientes acontecimientos adversos (AA): eventos tromboembólicos sintomáticos arteriales o venosos, sangrados, AA no comunes y la mortalidad por cualquier causa. El seguimiento de los AA graves se realizó hasta que se dispuso de un resultado final de los mismos. Los AA se clasificaron según la terminología MedDRA (Medical Dictionary for Regulatory Activities). En la V1 se recogieron además datos acerca de la intervención (tipo de cirugía, modo de fijación, tipo de anestesia), el tiempo hasta el inicio de la profilaxis y la duración de esta, el tiempo desde la intervención hasta la movilización y desde esta hasta el alta hospitalaria, el destino tras el alta, los preparativos para la administración del tratamiento tromboprofiláctico tras el alta y la formación recibida. Con el fin de recoger los AA ocurridos tras el alta hospitalaria y la necesidad de visitas médicas no planificadas, se siguió a los pacientes durante un periodo comprendido entre una semana después de finalizar la profilaxis (visita 2, V2) y 3 meses después de la cirugía (visita 3, V3). Se valoró también la tolerabilidad y la percepción de comodidad del tratamiento por parte del paciente en el momento del alta y tras finalizar el tratamiento tromboprofiláctico.
Valoración de los acontecimientos adversosLa variable principal de seguridad fue la tasa de sangrado mayor, definida según el mismo criterio usado en los estudios RECORD13: sangrado mortal o en un órgano crítico (intracraneal, intraocular, intraespinal, pericárdica, retroperitoneal, en una articulación no operada, o intramuscular con síndrome compartimental) o que requiere una reintervención, o bien un sangrado clínicamente manifiesto en una zona extraquirúrgica asociada a un descenso de hemoglobina≥ 2g/dl (calculado desde el valor inicial postoperatorio en el día 1) o la necesidad de infusión de≥2 unidades de sangre completa o de concentrados de eritrocitos. Se usó además la definición establecida por la European Medicines Agency14, similar a la anterior pero que incluye los sangrados que justifican el cese del tratamiento y los sangrados en el lugar donde se realizó la cirugía, con los mismos criterios que las extraquirúrgicas. Los AA se clasificaron como emergentes del tratamiento cuando comenzaron en el día de la primera dosis del tratamiento tromboprofiláctico o posteriormente a este, y hasta las 48h tras la última dosis.
Análisis estadísticoEl análisis estadístico se llevó a cabo con el paquete informático SAS System Versión 9.1.3 Service Pack 3. Las variables categóricas se expresan mediante porcentajes y se comparan mediante la prueba de Chi-cuadrado o el test de Fisher, según fuese apropiado. Las variables cuantitativas se expresan mediante la media y la desviación estándar una vez comprobada su distribución normal, y se comparan mediante la prueba t de Student. Este análisis solo se realizó en variables que se consideraron relevantes (características de los pacientes y variables de eficacia/seguridad), y cuyo número de sucesos permitió el análisis. La población de seguridad incluyó a aquellos pacientes que recibieron al menos una dosis de tratamiento tromboprofiláctico. Se excluyó de esta a los pacientes que hubiesen retirado el consentimiento informado, que hubiesen sido incluidos de forma retrospectiva, que hubiesen abandonado el tratamiento a causa de AA antes del tratamiento, cuyo cuaderno de recogida de datos no estuviese firmado por el médico, o por cualquier otro motivo que justificara la exclusión. La significación estadística se estableció en p<0,05.
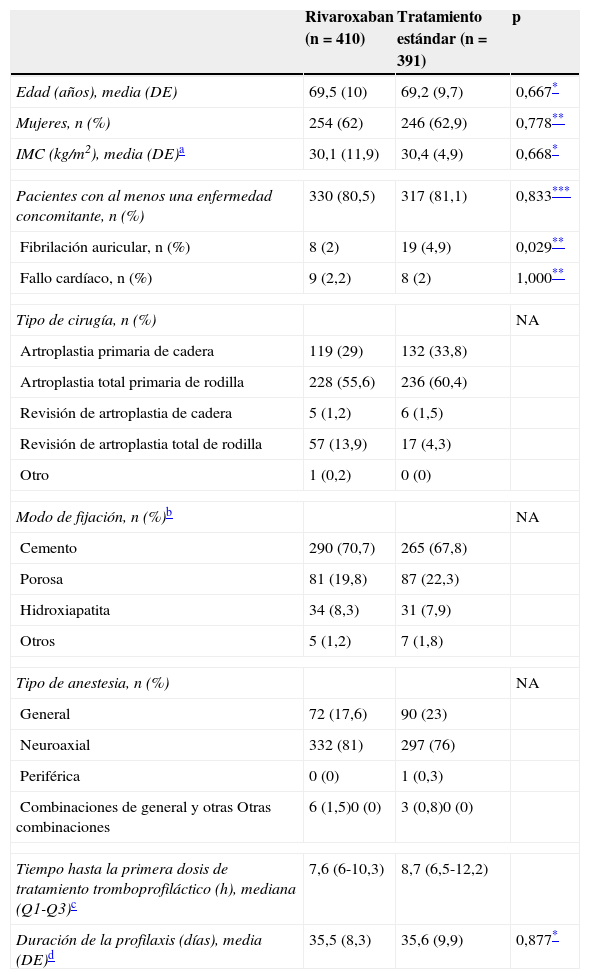
ResultadosCaracterísticas de los participantesSe incluyeron 801 pacientes de 15 centros de España, que constituyeron en su totalidad la población de seguridad. De estos, 410 recibieron rivaroxaban y 391 TE (el 64,7% heparinas de bajo peso molecular, el 24% fondaparinux y el 11% dabigatran). Las características demográficas y clínicas de los pacientes se muestran en la tabla 1. No se observaron diferencias significativas en la edad o el género de los pacientes. La media del índice de masa corporal indicó un alto grado de sobrepeso/obesidad, sin diferencias entre ambos grupos. La mayoría de los pacientes presentaba al menos una enfermedad concomitante, sin diferencias entre ambos grupos (tabla 1). La hipertensión, la hipercolesterolemia y la diabetes mellitus fueron las más frecuentes en ambos (56,8; 17,1 y 15,1% respectivamente en el grupo rivaroxaban, y 58,8; 15,9 y 16,9% en el grupo TE). Más pacientes del grupo TE padecían fibrilación auricular.
Características demográficas y clínicas de la intervención quirúrgica y del tratamiento tromboprofiláctico administrado (población de seguridad)
| Rivaroxaban (n=410) | Tratamiento estándar (n=391) | p | |
|---|---|---|---|
| Edad (años), media (DE) | 69,5 (10) | 69,2 (9,7) | 0,667* |
| Mujeres, n (%) | 254 (62) | 246 (62,9) | 0,778** |
| IMC (kg/m2), media (DE)a | 30,1 (11,9) | 30,4 (4,9) | 0,668* |
| Pacientes con al menos una enfermedad concomitante, n (%) | 330 (80,5) | 317 (81,1) | 0,833*** |
| Fibrilación auricular, n (%) | 8 (2) | 19 (4,9) | 0,029** |
| Fallo cardíaco, n (%) | 9 (2,2) | 8 (2) | 1,000** |
| Tipo de cirugía, n (%) | NA | ||
| Artroplastia primaria de cadera | 119 (29) | 132 (33,8) | |
| Artroplastia total primaria de rodilla | 228 (55,6) | 236 (60,4) | |
| Revisión de artroplastia de cadera | 5 (1,2) | 6 (1,5) | |
| Revisión de artroplastia total de rodilla | 57 (13,9) | 17 (4,3) | |
| Otro | 1 (0,2) | 0 (0) | |
| Modo de fijación, n (%)b | NA | ||
| Cemento | 290 (70,7) | 265 (67,8) | |
| Porosa | 81 (19,8) | 87 (22,3) | |
| Hidroxiapatita | 34 (8,3) | 31 (7,9) | |
| Otros | 5 (1,2) | 7 (1,8) | |
| Tipo de anestesia, n (%) | NA | ||
| General | 72 (17,6) | 90 (23) | |
| Neuroaxial | 332 (81) | 297 (76) | |
| Periférica | 0 (0) | 1 (0,3) | |
| Combinaciones de general y otrasOtras combinaciones | 6 (1,5)0 (0) | 3 (0,8)0 (0) | |
| Tiempo hasta la primera dosis de tratamiento tromboprofiláctico (h), mediana (Q1-Q3)c | 7,6 (6-10,3) | 8,7 (6,5-12,2) | |
| Duración de la profilaxis (días), media (DE)d | 35,5 (8,3) | 35,6 (9,9) | 0,877* |
DE: desviación estándar; IMC: índice de masa corporal; NA: no analizado.
El 85% de las intervenciones quirúrgicas en el grupo rivaroxaban y el 94% en el grupo TE fueron una artroplastia primaria de rodilla o de cadera (tabla 1), en casi todos los casos unilateral (> 99%). El modo de fijación mayoritario en ambos grupos fue el cemento. El tipo de anestesia más frecuente fue la neuraxial (tabla 1). La media de duración de la intervención fue de 1,62±0,49h en ambos grupos. Solo 4 pacientes (1%) en el grupo rivaroxaban y 2 en el grupo TE (0,5%) sufrieron complicaciones relacionadas con la intervención quirúrgica.
Administración de tratamiento tromboprofilácticoLa media del tiempo hasta la recepción de la primera dosis de tratamiento tromboembólico y la media de duración del tratamiento fueron similares en ambos grupos (tabla 1). Cerca de la mitad de los pacientes recibió la primera dosis de tratamiento tromboprofiláctico entre las 6 y 10 primeras horas tras la intervención (el 47,3% en el grupo rivaroxaban y el 42,7% en el grupo TE). En ambos grupos, la duración de tratamiento más frecuente fue de 35-42 días (41,2% en el grupo rivaroxaban, 43% en el grupo TE). Le siguió el tratamiento durante 28-35 días, que fue más frecuente en el grupo rivaroxaban (36,8 vs. 24,8% de los pacientes del grupo TE).
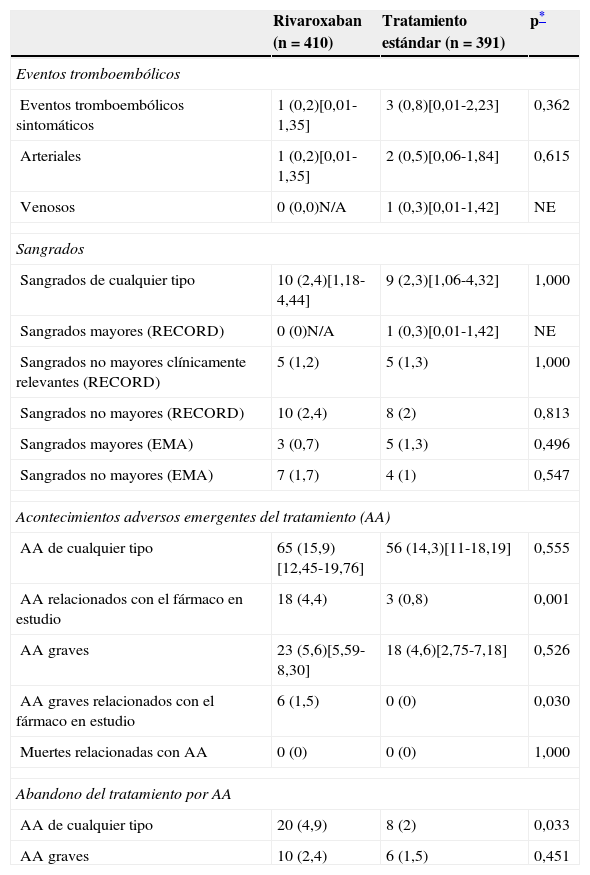
Resultados clínicosEl número de eventos tromboembólicos fue similar en ambos grupos (0,8% en el grupo TE vs. 0,2% en el grupo rivaroxaban, p=0,362) (tabla 2). La incidencia de sangrados emergentes del tratamiento fue también similar en ambos grupos, incluida la de sangrados mayores definidos por los criterios EMA o RECORD (el 1,3% y el 0,3% respectivamente en el grupo TE vs. el 0,7% y el 0% en el grupo rivaroxaban) (tabla 2).
Incidencia de eventos tromboembólicos sintomáticos, sangrados y otros acontecimientos adversos emergentes del tratamiento (población de seguridad)
| Rivaroxaban (n=410) | Tratamiento estándar (n=391) | p* | |
|---|---|---|---|
| Eventos tromboembólicos | |||
| Eventos tromboembólicos sintomáticos | 1 (0,2)[0,01-1,35] | 3 (0,8)[0,01-2,23] | 0,362 |
| Arteriales | 1 (0,2)[0,01-1,35] | 2 (0,5)[0,06-1,84] | 0,615 |
| Venosos | 0 (0,0)N/A | 1 (0,3)[0,01-1,42] | NE |
| Sangrados | |||
| Sangrados de cualquier tipo | 10 (2,4)[1,18-4,44] | 9 (2,3)[1,06-4,32] | 1,000 |
| Sangrados mayores (RECORD) | 0 (0)N/A | 1 (0,3)[0,01-1,42] | NE |
| Sangrados no mayores clínicamente relevantes (RECORD) | 5 (1,2) | 5 (1,3) | 1,000 |
| Sangrados no mayores (RECORD) | 10 (2,4) | 8 (2) | 0,813 |
| Sangrados mayores (EMA) | 3 (0,7) | 5 (1,3) | 0,496 |
| Sangrados no mayores (EMA) | 7 (1,7) | 4 (1) | 0,547 |
| Acontecimientos adversos emergentes del tratamiento (AA) | |||
| AA de cualquier tipo | 65 (15,9)[12,45-19,76] | 56 (14,3)[11-18,19] | 0,555 |
| AA relacionados con el fármaco en estudio | 18 (4,4) | 3 (0,8) | 0,001 |
| AA graves | 23 (5,6)[5,59-8,30] | 18 (4,6)[2,75-7,18] | 0,526 |
| AA graves relacionados con el fármaco en estudio | 6 (1,5) | 0 (0) | 0,030 |
| Muertes relacionadas con AA | 0 (0) | 0 (0) | 1,000 |
| Abandono del tratamiento por AA | |||
| AA de cualquier tipo | 20 (4,9) | 8 (2) | 0,033 |
| AA graves | 10 (2,4) | 6 (1,5) | 0,451 |
NE: no evaluable.
Los datos se expresan como n (%) y el intervalo de confianza al 95% [IC 95%] cuando se dispone del mismo.
La incidencia de AA relacionados con el fármaco y la de AA graves (especialmente los relacionados con el fármaco) fue significativamente superior en el grupo rivaroxaban y llevaron a un mayor abandono del tratamiento por este motivo (tabla 2). Los AA más frecuentes relacionados con el fármaco fueron los asociados con daños, intoxicación o complicaciones derivadas del procedimiento, con una incidencia del 5,1% en el grupo rivaroxaban y del 2,6% en el grupo TE, aunque a nivel individual la incidencia de cada uno de los AA englobados en esta categoría no mostró diferencia y ninguna superó el 1%. Le siguieron en importancia las infecciones e infestaciones (2,7 vs. 2,6%), las complicaciones gastrointestinales (2,5 vs. 1%), las complicaciones sanguíneas y linfáticas (anemia) (1,7 vs. 1,5%) y las complicaciones generales y en el lugar de administración (1,5 vs. 1,9%). En ninguno de los grupos se observaron muertes relacionadas con los AA.
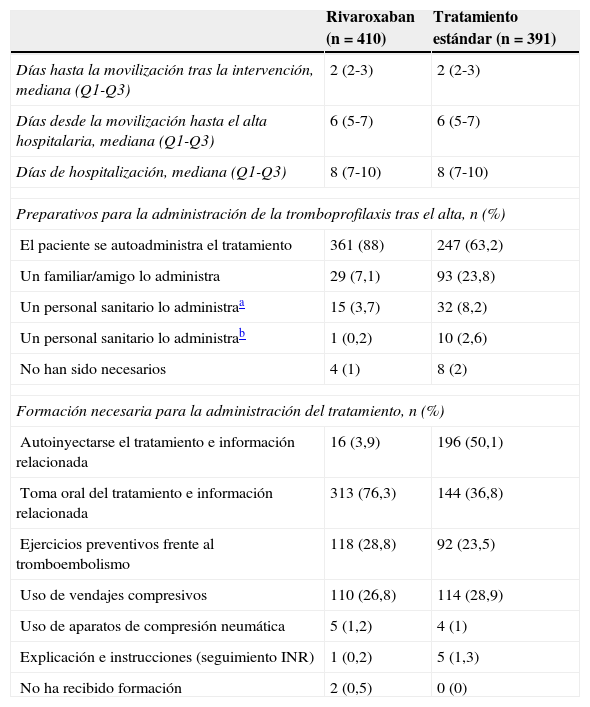
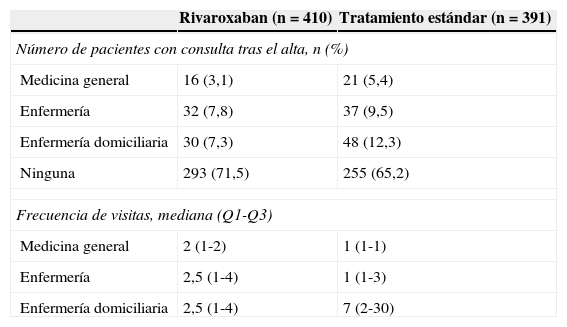
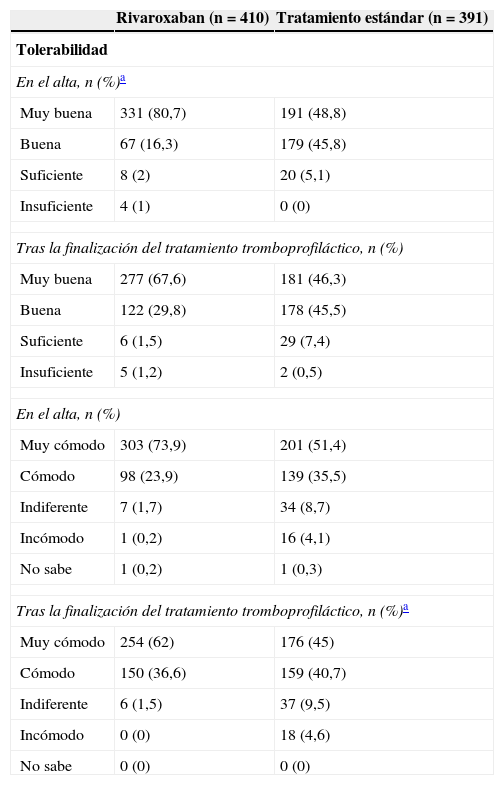
La tabla 3 muestra los datos más relevantes acerca del postoperatorio de los pacientes hasta su alta hospitalaria. La mediana de días hasta el inicio de la movilización tras la intervención quirúrgica fue de 2 días en ambos grupos. La mediana de días desde el inicio de la movilización hasta el alta hospitalaria y de estancia hospitalarias también fueron similares (mediana de 6 y 8 días en ambos casos respectivamente). Tras el alta, el paciente fue trasladado a su domicilio en la mayoría de los casos (92,6%), sin diferencias entre ambos grupos de tratamiento. Los pacientes del grupo TE dependieron más de personas externas para la administración del tratamiento tromboprofiláctico tras el alta (tabla 3) y consumieron más recursos sanitarios tras esta (tabla 4). La tolerabilidad fue calificada como muy buena en el momento del alta hospitalaria por el 80,7% de los pacientes del grupo rivaroxaban y el 48,8% de los pacientes del grupo TE. Estos resultados se mantuvieron con poca variación tras la finalización del tratamiento tromboprofiláctico. El tratamiento con rivaroxaban fue calificado como «muy cómodo» por el 73% de los pacientes, frente al 51,4% del grupo TE. Las diferencias se nivelaron algo más, sin llegar a igualarse, tras la finalización del tratamiento tromboprofiláctico (tabla 5).
Datos sobre el periodo postoperatorio hasta el alta hospitalaria
| Rivaroxaban (n=410) | Tratamiento estándar (n=391) | |
|---|---|---|
| Días hasta la movilización tras la intervención, mediana (Q1-Q3) | 2 (2-3) | 2 (2-3) |
| Días desde la movilización hasta el alta hospitalaria, mediana (Q1-Q3) | 6 (5-7) | 6 (5-7) |
| Días de hospitalización, mediana (Q1-Q3) | 8 (7-10) | 8 (7-10) |
| Preparativos para la administración de la tromboprofilaxis tras el alta, n (%) | ||
| El paciente se autoadministra el tratamiento | 361 (88) | 247 (63,2) |
| Un familiar/amigo lo administra | 29 (7,1) | 93 (23,8) |
| Un personal sanitario lo administraa | 15 (3,7) | 32 (8,2) |
| Un personal sanitario lo administrab | 1 (0,2) | 10 (2,6) |
| No han sido necesarios | 4 (1) | 8 (2) |
| Formación necesaria para la administración del tratamiento, n (%) | ||
| Autoinyectarse el tratamiento e información relacionada | 16 (3,9) | 196 (50,1) |
| Toma oral del tratamiento e información relacionada | 313 (76,3) | 144 (36,8) |
| Ejercicios preventivos frente al tromboembolismo | 118 (28,8) | 92 (23,5) |
| Uso de vendajes compresivos | 110 (26,8) | 114 (28,9) |
| Uso de aparatos de compresión neumática | 5 (1,2) | 4 (1) |
| Explicación e instrucciones (seguimiento INR) | 1 (0,2) | 5 (1,3) |
| No ha recibido formación | 2 (0,5) | 0 (0) |
INR: ratio internacional normalizado.
Consumo de recursos sanitarios tras el alta
| Rivaroxaban (n=410) | Tratamiento estándar (n=391) | |
|---|---|---|
| Número de pacientes con consulta tras el alta, n (%) | ||
| Medicina general | 16 (3,1) | 21 (5,4) |
| Enfermería | 32 (7,8) | 37 (9,5) |
| Enfermería domiciliaria | 30 (7,3) | 48 (12,3) |
| Ninguna | 293 (71,5) | 255 (65,2) |
| Frecuencia de visitas, mediana (Q1-Q3) | ||
| Medicina general | 2 (1-2) | 1 (1-1) |
| Enfermería | 2,5 (1-4) | 1 (1-3) |
| Enfermería domiciliaria | 2,5 (1-4) | 7 (2-30) |
Tolerabilidad y comodidad del tratamiento tromboprofiláctico
| Rivaroxaban (n=410) | Tratamiento estándar (n=391) | |
|---|---|---|
| Tolerabilidad | ||
| En el alta, n (%)a | ||
| Muy buena | 331 (80,7) | 191 (48,8) |
| Buena | 67 (16,3) | 179 (45,8) |
| Suficiente | 8 (2) | 20 (5,1) |
| Insuficiente | 4 (1) | 0 (0) |
| Tras la finalización del tratamiento tromboprofiláctico, n (%) | ||
| Muy buena | 277 (67,6) | 181 (46,3) |
| Buena | 122 (29,8) | 178 (45,5) |
| Suficiente | 6 (1,5) | 29 (7,4) |
| Insuficiente | 5 (1,2) | 2 (0,5) |
| En el alta, n (%) | ||
| Muy cómodo | 303 (73,9) | 201 (51,4) |
| Cómodo | 98 (23,9) | 139 (35,5) |
| Indiferente | 7 (1,7) | 34 (8,7) |
| Incómodo | 1 (0,2) | 16 (4,1) |
| No sabe | 1 (0,2) | 1 (0,3) |
| Tras la finalización del tratamiento tromboprofiláctico, n (%)a | ||
| Muy cómodo | 254 (62) | 176 (45) |
| Cómodo | 150 (36,6) | 159 (40,7) |
| Indiferente | 6 (1,5) | 37 (9,5) |
| Incómodo | 0 (0) | 18 (4,6) |
| No sabe | 0 (0) | 0 (0) |
El análisis de los datos de los centros españoles participantes en el estudio en fase iv internacional XAMOS aporta información de interés sobre el manejo de pacientes, la efectividad y seguridad de rivaroxaban frente a tratamientos usados habitualmente para la prevención de eventos tromboembólicos en pacientes sometidos a artroplastia de cadera o rodilla en nuestro entorno. Estos datos revelan que el tratamiento tromboprofiláctico con rivaroxaban se asocia a una incidencia de eventos tromboembólicos sintomáticos y a una incidencia de sangrados, incluida la de sangrados, similar a la del TE usado habitualmente. La incidencia de AA relacionados con el fármaco, tanto generales como graves, fue significativamente superior con rivaroxaban respecto al TE.
En la interpretación de estos resultados es importante considerar que la población a estudio consiste en un subgrupo de pacientes incluidos en un estudio internacional, por lo que se carece de una determinación del tamaño muestral que permita una potencia estadística adecuada, especialmente si se tiene en cuenta el bajo número de eventos a análisis. Algunas de las diferencias en los grupos a estudio y los procedimientos quirúrgicos aplicados a uno y a otro pueden afectar asimismo a la interpretación de los resultados y merece la pena ser comentados.
Las características de los pacientes fueron similares en ambos grupos, destacando una edad elevada (>69 años) y un índice de masa corporal medio indicador de obesidad (30kg/m2). Destaca la mayor prevalencia de fibrilación auricular en el grupo TE, que podría afectar a la incidencia de eventos tromboembólicos arteriales. Pese a ello, no se observaron diferencias entre ambos grupos, lo que podría deberse al bajo número de eventos. Se observaron igualmente diferencias en el tipo de cirugía que conllevaría diferencias en el riesgo trombogénico. Destaca un uso superior de rivaroxaban frente al TE en revisión de artroplastia total de rodilla (13,9 vs. 4,9%), mientras que no hubo diferencias en lo que se refiere a la revisión de artroplastia de cadera. Este procedimiento quirúrgico se ha asociado a un mayor riesgo trombogénico que la cirugía primaria de rodilla o cadera15. Consecuentemente, el uso de TE como tratamiento tromboprofiláctico fue superior en el caso de artroplastia primaria, tanto de rodilla como de cadera. El tipo de anestesia usado es otro aspecto de interés. En el grupo rivaroxaban se utilizó con mayor frecuencia la anestesia neuroaxial (81 vs. 76%), que se ha asociado a una menor incidencia de eventos tromboembólicos16, aunque de nuevo la diferencia no fue estadísticamente significativa. Se desconoce cómo puede haber afectado a los resultados dado el bajo número de eventos.
En lo que respecta a la seguridad, no se observaron diferencias en la incidencia de sangrados, mayores o no mayores. Destaca, sin embargo, la incidencia superior de AA considerados relacionados con el fármaco, tanto globales como graves, respecto al TE (4,4 vs. 0,8% y 1,5 vs. 0% respectivamente) que además provocaron un mayor número de abandonos por este motivo. Las mayores diferencias se observaron en los relacionados con daños, intoxicación o complicaciones derivadas del procedimiento, aunque dada la baja incidencia a nivel de cada uno de los AA englobados en esta categoría (<1%) no fue posible analizar las diferencias entre ambos grupos. No se observaron diferencias entre ambos grupos en la incidencia de AA de cualquier tipo y graves (relacionados con el fármaco o no), que fueron comparativamente mucho más frecuentes. El bajo número de AA relacionados con el fármaco hace de nuevo difícil la interpretación de resultados. En cualquier caso, hasta que no se disponga de registros en una población más amplia de pacientes, es necesario un seguimiento adecuado de estos. Los AA observados con más frecuencia con rivaroxaban coinciden con los informados en la ficha técnica de producto17. Estos aspectos adquieren especial interés si se tiene en cuenta que, aunque la media de tratamiento tromboprofiláctico fue similar en ambos grupos (35,5±8,3 días en el grupo rivaroxaban y 35,6±9,9 días en el grupo TE), el porcentaje de pacientes en los que el tratamiento se extendió hasta los 35 días fue superior en el grupo rivaroxaban (36,8%) vs. TE (24,8%). Aunque la incidencia de hemorragias no se analizó en función de la duración de la tromboprofilaxis, el mayor porcentaje de pacientes con tromboprofilaxis prolongada no se tradujo en una diferencia significativa en el número de eventos hemorrágicos. Se desconoce cómo puede haber afectado a la incidencia de AA relacionados con el fármaco. La duración óptima del tratamiento tromboprofiláctico es un aspecto en el que no existe consenso entre las principales guías de referencia18. Aunque las guías del National Institute for Health and Clinical Excellence (NICE) y del American College of Chest Physicians (AACP) recomiendan una duración de hasta 35 días en la artroplastia de cadera6,19, no existe un acuerdo en lo que respecta a la duración óptima en artroplastia de rodilla: mientras que la primera recomienda hasta 14 días19, la segunda recomienda hasta 35 días (o 14 días con un grado de evidencia 2B)6. En nuestro país, la Guía de profilaxis tromboembólica en cirugía ortopédica y traumatología, promovida por el Grupo de Estudio del Tromboembolismo (Sociedad Española de Cirugía Ortopédica y Traumatología, SECOT), disponible desde 2003 y actualizada en 2007 y en 201320, recomienda el tratamiento profiláctico prolongado (durante 4-6 semanas) tanto en artroplastia cadera como en rodilla. La conveniencia de alargar el tratamiento tromboprofiláctico ha sido puesta de nuevo de manifiesto en un consenso de expertos reciente realizado en nuestro país, donde se establece que el tratamiento profiláctico en pacientes sometidos a artroplastia de rodilla o de cadera debe mantenerse hasta los 28-35 días21.
Tras el alta hospitalaria, los pacientes tratados con rivaroxaban requirieron menos ayuda para la administración del tratamiento por parte de personal sanitario (incluido a domicilio), de familiares o amigos, y necesitaron menos consultas médicas, lo que supone un ahorro de recursos sanitarios. Como era de esperar, los pacientes del grupo TE requirieron más visitas de enfermería domiciliaria, debido sobre todo a la necesidad de administración subcutánea de la heparina de bajo peso molecular. La formación que recibieron los pacientes se relacionó con el tratamiento administrado. Tanto la tolerabilidad como la comodidad del tratamiento recibieron una mejor valoración entre los pacientes que recibieron rivaroxaban.
Además de las limitaciones propias de los estudios observacionales, otras limitaciones importantes a la hora de interpretar estos resultados han sido comentadas en el texto. Es importante también resaltar que en este estudio la decisión de tratamiento siguió el criterio de cada facultativo, por lo que no se excluye la posibilidad de que las indicaciones en ocasiones no siguieran la ficha técnica, que se considera como indicadora de recomendaciones. Se desconoce el número de casos que se han realizado «off label», y no se ha exigido para el reclutamiento que los tratamientos se realicen según ficha técnica, con lo que no puede descartarse variabilidad por este aspecto.
En resumen, los datos españoles del estudio XAMOS muestran que rivaroxaban es al menos tan efectivo como el TE en la prevención del tromboembolismo venoso en la práctica clínica diaria, aportando mayor comodidad y un menor gasto de recursos sanitarios tras el alta. Aunque la incidencia de hemorragias mayores y no mayores fue similar a la del TE pese a una mayor proporción de pacientes que fueron tratados hasta 35 días, la incidencia superior de AA relacionados por el investigador con el tratamiento aconsejan un seguimiento adecuado de estos hasta que se disponga de datos de seguridad en una población de pacientes más amplia.
Nivel de evidenciaNivel de evidencia iv.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
Conflicto de interesesLos autores declaran no tener conflictos de intereses en relación con el presente artículo.
Los autores agradecen la colaboración de todos los médicos participantes en el estudio XAMOS en España. También agradecen a Beatriz Viejo, PhD, su contribución en la redacción y edición del manuscrito. El presente estudio ha sido financiado por Bayer Healthcare.
Juan Antonio Alba. Clínica del Ángel de Málaga (Málaga)
Miguel Álvarez. Hospital Carlos Haya (Málaga)
Vicente Casa. Hospital la Princesa (Madrid)
Pablo Díaz de Rada. Clínica Universitaria de Navarra (Navarra).
José Luis Díaz. Hospital General de Castellón (Castellón)
Francisco Goma. Hospital Clínico Universitario de Valencia (Valencia)
Claudio Gómez. Hospital Santa Ana de Motril (Granada)
Javier Granero. Hospital Germans Trias i Pujol (Barcelona)
Antonio Herrera. Hospital Miguel Servet (Zaragoza)
Luis María Lozano. Hospital Clínic de Barcelona (Barcelona)
Javier Martínez. Hospital Universitario Fundación Alcorcón (Madrid)
José Luis Martínez. Hospital Virgen de las Nieves (Granada)
Antonio Murcia. Hospital Santa María del Rosell (Cartagena, Murcia)
Ángels Salvador. Hospital Plató (Barcelona)
José Ricardo Troncoso. Hospital Povisa (Vigo, Pontevedra)