El objetivo de este consenso de la Sociedad Europea de Traumatología Deportiva, Cirugía de Rodilla y Artroscopia (ESSKA) es proporcionar recomendaciones basadas en evidencia y opinión de expertos para mejorar las indicaciones, las decisiones y los aspectos relacionados con la administración de ortobiológicos derivados de la sangre (para simplificar, PRP [Plasma Rico en Plaquetas], siendo el PRP el producto más común) para el manejo de la osteoartritis (OA) de rodilla.
MétodosLos principales expertos clínicos y científicos europeos se dividieron en grupo directivo, grupo de calificación y grupo de evaluadores. El grupo directivo preparó 28 preguntas/declaraciones divididas en tres secciones: fundamentos e indicaciones del PRP, preparación y caracterización del PRP, y protocolo de PRP. La calidad de las declaraciones recibió grados de recomendación que van desde A(apoyo científico de alto nivel), B(presunción científica), C(apoyo científico de bajo nivel) o D(opinión de expertos). Las preguntas/declaraciones fueron evaluadas por el grupo de calificación, quienes puntuaron las declaraciones de 1 a 9 según su grado de consenso. Tras alcanzar un consenso general entre los grupos directivo y de calificación, el documento se presentó al grupo de evaluación, que evaluó la adaptabilidad geográfica y aprobó el documento. Se celebró una reunión final conjunta con todos los miembros del consenso para producir el documento oficial.
ResultadosLa revisión de la literatura sobre el uso de productos derivados de la sangre para la OA de rodilla reveló que 9 de las 28 preguntas/declaraciones contaban con el respaldo de literatura científica de alto nivel, mientras que las otras 19 estaban respaldadas por una calidad científica media-baja. Tres de las 28 recomendaciones fueron de gradoA: 1)Existe suficiente evidencia preclínica y clínica para respaldar el uso de PRP en la OA de rodilla. Esta recomendación se consideró apropiada con un fuerte consenso (Media:8). 2)La evidencia clínica ha demostrado la eficacia del PRP en pacientes con grados leves a moderados de OA de rodilla (KL ≤3). Esta recomendación se consideró apropiada con un fuerte consenso (Media:8,1). 3)Las inyecciones de PRP han demostrado proporcionar un efecto más prolongado en comparación con el efecto a corto plazo de las inyecciones de corticosteroides. También parecen ofrecer un perfil de uso más seguro con menos complicaciones potenciales relacionadas. Esta recomendación se consideró apropiada con un acuerdo muy fuerte (Media:8,7). Seis declaraciones fueron recomendaciones de gradoB, siete fueron de gradoC y doce fueron recomendaciones de gradoD. La puntuación media de valoración fue de 8,2±0,3.
ConclusionesEl grupo de consenso alcanzó un alto nivel de acuerdo en todas las preguntas/declaraciones, a pesar de la falta de evidencia clara para algunas preguntas. Según los resultados de este grupo de consenso, dada la amplia literatura existente y las opiniones de expertos, el PRP se consideró una opción de tratamiento válida para la OA de rodilla, y como una posible opción de tratamiento inyectable de primera línea para el manejo no quirúrgico de la OA de rodilla, principalmente para grados KL1-3.
The aim of this European Society of Sports Traumatology, Knee Surgery and Arthroscopy (ESSKA) consensus is to provide recommendations based on evidence and expert opinion to improve indications, decision making, and administration related aspects when using blood-derived orthobiologics (for simplicity indicated as PRP [Platelet Rich Plasma] being PRP the most common product) for the management of knee osteoarthritis (OA).
MethodsLeading European expert clinicians and scientists were divided into a steering group, a rating group and a peer review group. The steering group prepared 28 question-statement sets divided into three sections: PRP rationale and indications, PRP preparation and characterization, and PRP protocol. The quality of the statements received grades of recommendation ranging from A(high-level scientific support), to B(scientific presumption), C(low level scientific support) or D(expert opinion). The question-statement sets were then evaluated by the rating group and the statements scored from1 to9 based on their degree of agreement with the statements produced by the steering group. Once a general consensus was reached between the steering and rating groups, the document was submitted to the peer review group who evaluated the geographic adaptability and approved the document. A final combined meeting of all the members of the consensus was held to produce the official document.
ResultsThe literature review on the use of blood-derived products for knee OA revealed that 9 of 28 questions/statements had the support of high-level scientific literature, while the other 19 were supported by a medium-low scientific quality. Three of the 28 recommendations were gradeA recommendations: (1)There is enough preclinical and clinical evidence to support the use of PRP in knee OA. This recommendation was considered appropriate with a strong agreement (Mean:8). (2)Clinical evidence has shown the effectiveness of PRP in patients for mild to moderate degrees of knee OA (KL≤3). This recommendation was considered appropriate with a strong agreement (Mean:8.1). (3)PRP injections have been shown to provide a longer effect in comparison to the shorter-term effect of corticosteroids injections. They also seem to provide a safer use profile with less potential related complications. This recommendation was considered appropriate with a very strong agreement (Mean:8.7). Six statements were gradeB recommendations, seven were gradeC and twelve were a gradeD recommendation. The mean rating score was 8.2±0.3.
ConclusionsThe consensus group reached a high level of agreement on all the questions/statements despite the lack of clear evidence for some questions. According to the results from this consensus group, given the large body of existing literature and expert opinions, PRP was regarded as a valid treatment option for knee OA, and as a possible first line injectable treatment option for non-operative management of knee OA, mainly for KL grades1-3.
La European Society of Sports Traumatology, Knee Surgery and Arthroscopy - Orthobiologics Initiative (ESSKA-ORBIT) publicó recientemente en la revista Knee, Surgery, Sports, Traumatology and Arthroscopy (KSSTA)1 recomendaciones sobre el uso y la preparación de productos derivados de la sangre (principalmente plasma rico en plaquetas) en la artrosis de rodilla. El presente manuscrito es una traducción idéntica al español de este trabajo original con el fin de favorecer una mayor difusión entre las sociedades científicas nacionales. El manuscrito original está disponible en formato PDF en el siguiente enlace: https://esskajournals.onlinelibrary.wiley.com/doi/epdf/10.1002/ksa.12077.
Esta traducción del inglés se ha realizado con la autorización del editor Wiley y de Laura de Girolamo/Lior Laver, coordinadores del grupo de trabajo ORBIT de ESSKA, que posee los derechos de la obra original publicada en Knee Surgery, Sports Traumatology, Arthroscopy (KSSTA), y respeta los derechos de autor de acuerdo con la legislación vigente.
IntroducciónSe estima que la artrosis u osteoartritis (OA) afecta a más de 500 millones de personas en todo el mundo, con un aumento constante de casos anuales debido al envejecimiento de la población y con un coste medio anual por paciente de aproximadamente 700 a 1.000euros2. La rodilla es la articulación más comúnmente afectada por la OA3, cuyo tratamiento sigue siendo objeto de debate. De hecho, aunque el tratamiento de la OA en fases avanzadas suele derivar en una prótesis de rodilla, existen diversas opciones de manejo conservador para las fases iniciales, aunque no siempre proporcionan resultados consistentes o a largo plazo4. En este contexto, el campo de los ortobiológicos ha experimentado un auge como resultado del creciente interés por los tratamientos biológicos para la regeneración tisular en diversas afecciones musculoesqueléticas, entre las que se encuentra la OA de rodilla, tanto como tratamiento inyectable conservador como en combinación con procedimientos quirúrgicos. Las opciones de tratamientos ortobiológicos inyectables para la OA de rodilla se han convertido, sin duda, en un actor principal en el manejo no quirúrgico de esta patología. No obstante, es necesario abordar la falta de una opinión unánime por parte de los profesionales en cuanto a las indicaciones para los pacientes, los protocolos de administración y, aún más, en la elección de las opciones/dispositivos disponibles.
El tratamiento ortobiológico más utilizado actualmente para abordar la OA de rodilla es la inyección de plasma rico en plaquetas (PRP). Los estudios preclínicos han demostrado efectos favorables de modificación de la enfermedad del PRP en modelos animales5 en términos de progresión del daño del cartílago, reducción de la inflamación sinovial y cambios en los niveles de biomarcadores. En humanos, algunos estudios han demostrado efectos modificadores de la enfermedad. Entre ellos, un reciente ensayo aleatorizado controlado analizó el líquido sinovial de las rodillas con OA de leve a moderada tratadas con PRP o solución salina. Los resultados mostraron cambios significativos en el biomarcador A2M, la expresión de marcadores celulares y los perfiles de expresión génica en células madre mesenquimales (MSC) para metaloproteinasas de la matriz y marcadores inflamatorios a favor del grupo tratado con PRP6.
A pesar de la amplia variedad de formulaciones de PRP, protocolos y grupos de control utilizados en estudios clínicos, en el momento de la conclusión del proceso de consenso se recuperaron 48ensayos controlados aleatorizados sobre el uso de PRP para el manejo de la OA de rodilla escritos en inglés en Medline, la mayoría (38, de los cuales 24 con nivel de evidenciaI y 14 con nivelII) mostrando la superioridad del tratamiento con PRP en comparación con otras opciones inyectables como corticosteroides, ácido hialurónico o solución salina. Los 10 restantes mostraron resultados similares de las inyecciones de PRP respecto a corticosteroides, ácido hialurónico, concentrado de aspirado de médula ósea o incluso solución salina. Sin embargo, aunque la mayoría de los ensayos controlados aleatorizados informan de la superioridad del PRP frente a la solución salina en el tratamiento de la OA de rodilla7–12, algunos estudios mostraron que en pacientes con OA de rodilla sintomática de leve a moderada, la inyección intraarticular de PRP no produjo una diferencia significativa en los síntomas o en la estructura articular a los 12meses en comparación con la inyección de solución salina13–15. Se ha sugerido que esto se debe a la amplia heterogeneidad de los productos de PRP, la variabilidad en las poblaciones de pacientes, la multifactorialidad de la OA de rodilla y diversos posibles sesgos. En cualquier caso, el hecho de que algunos estudios hayan mostrado falta de superioridad sigue requiriendo cierta cautela a la hora de evaluar la eficacia de los tratamientos ortobiológicos y podría explicar por qué es necesario implementar medidas adicionales de evaluación y calidad al analizar el potencial completo de estos tratamientos.
Es indiscutible que todavía se encuentran algunos resultados contradictorios en la literatura. Sin embargo, en los últimos años ha habido un aumento de informes más consistentes y homogéneos sobre el efecto de los concentrados plaquetarios que demuestran que las inyecciones de PRP proporcionan resultados satisfactorios en el tratamiento de la OA de rodilla. Un metaanálisis reciente mostró que los pacientes sometidos a tratamiento para la OA de rodilla con PRP pueden experimentar mejores resultados clínicos en comparación con la solución salina16 o con ácido hialurónico a los 12meses de seguimiento16–18 con un perfil de seguridad comparable entre ambas opciones de tratamiento.
Como la mayor asociación europea de especialistas musculoesqueléticos, la Sociedad Europea de Traumatología Deportiva, Cirugía de Rodilla y Artroscopia (ESSKA), más allá de desempeñar un papel fundamental en la formación de jóvenes cirujanos ortopédicos y otros profesionales del sector19,20, ha sentido la responsabilidad de proporcionar a sus miembros, y en general a la comunidad ortopédica, fuentes de referencia y orientación prácticas. Por ello, la ESSKA estableció la Iniciativa ORthoBIologics (ORBIT) para reunir una colaboración paneuropea que creara un lenguaje común y una voz uniforme y fiable en el campo de los ortobiológicos, así como para impulsar un buen estándar de atención en este ámbito.
El enfoque específico de este manuscrito es sobre productos derivados de la sangre (incluyendo, pero no limitado a, PRP). Tras experiencias colaborativas previas de éxito llevadas a cabo bajo el proceso formal de consenso de ESSKA en otros temas21–24, los resultados del consenso actual proporcionan recomendaciones basadas en la evidencia y la opinión de expertos para mejorar las indicaciones, la toma de decisiones y los aspectos relacionados con la administración al utilizar ortobiológicos derivados de la sangre para el manejo no quirúrgico de la OA de rodilla.
Material y métodosTerminologíaEl término «productos derivados de la sangre» (en inglés, blood-derived products) se refiere a una amplia variedad de productos que se obtienen procesando sangre periférica con diferentes sistemas/técnicas, dando lugar a fracciones sanguíneas enriquecidas en moléculas terapéuticas. Entre ellos, los más conocidos y utilizados son el PRP, la fibrina rica en plaquetas (PRF), el plasma rico en factores de crecimiento (PRGF), el plasma autólogo condicionado (ACP), la solución proteica autóloga (APS), todos ellos basados en la concentración de plaquetas, así como otros productos como el suero autólogo condicionado (ACS, por su denominación en inglés, autologous conditioned serum) y la alfa-2-macroglobulina (A2M). En aras de la simplicidad, al ser el PRP el producto más común, se utilizará genéricamente para referirse a cualquier producto autólogo derivado de la sangre basado en la concentración de plaquetas mediante una manipulación mínima de la sangre (no se incluyen en este término los productos no basados en la concentración de plaquetas, como el ACS o el A2M, que se abordaron en preguntas-respuesta específicas discutidas brevemente por separado).
Aunque los autores reconocen que existe una gran variabilidad entre los distintos productos, el objetivo de este Consenso no es proporcionar información sobre ninguna técnica específica o sistema comercial disponible, sino ofrecer recomendaciones generales sobre el uso de productos derivados de la sangre para el tratamiento de la OA de rodilla.
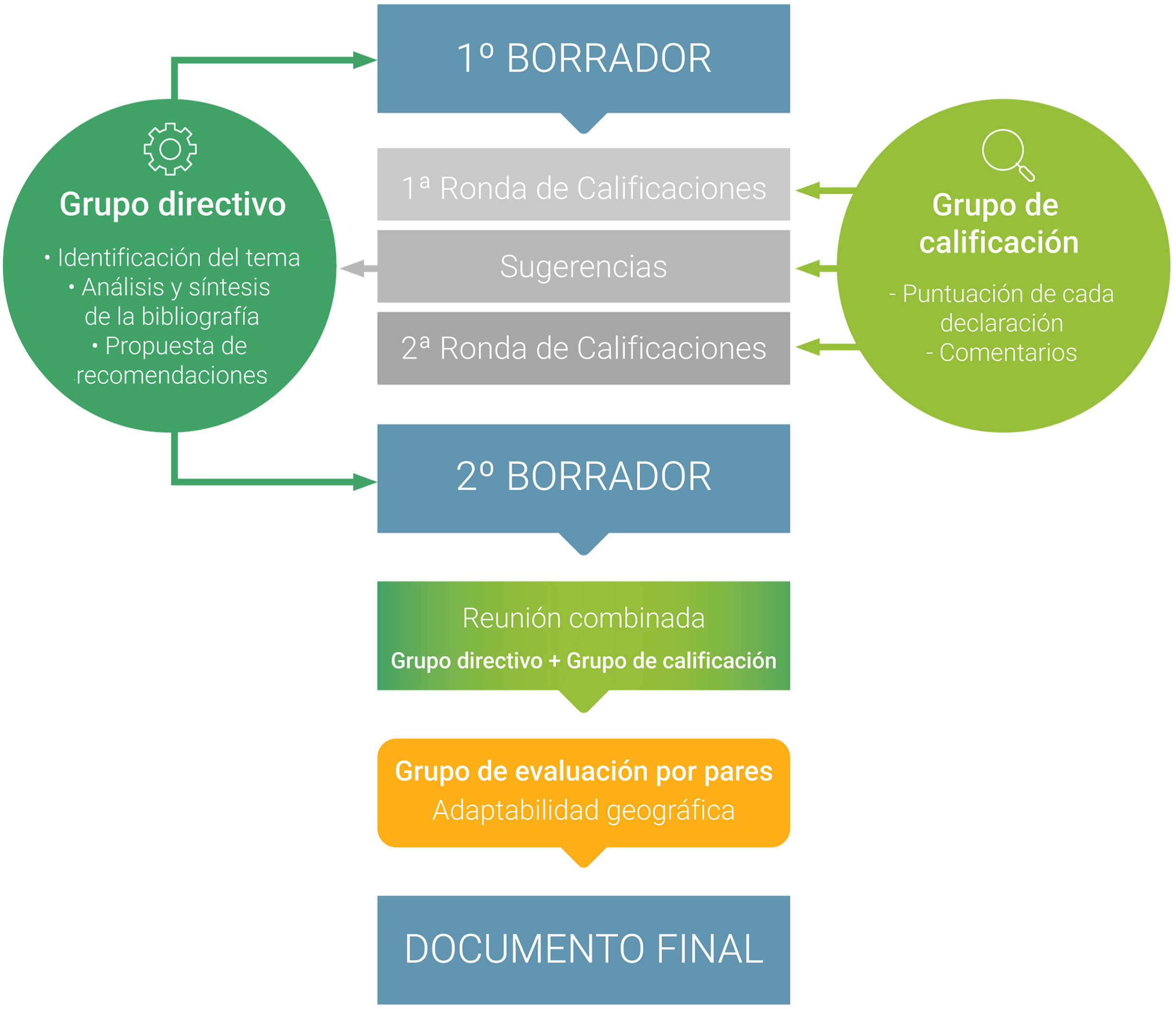
Metodología del ConsensoEl proceso de este proyecto de consenso fue similar a los proyectos de consensos formales de la ESSKA publicados anteriormente21,23,24, y siguió el «proceso de Consenso Formal» de la ESSKA derivado de la metodología Delphi descrita por la Haute Autorité de Santé [HAS] de la Institución Nacional de Sanidad Francesa25,26 (fig. 1). Todas las reuniones de trabajo para el presente consenso se realizaron online debido a las restricciones derivadas de la pandemia de COVID-19. El proceso incluyó tres grupos de cirujanos ortopédicos y científicos experimentados: grupo directivo, incluido el grupo de bibliografía, n=14; grupo de calificación, n=22, y grupo de evaluación o revisión por pares, n=35. El grupo directivo, que incluía a 14 cirujanos ortopédicos y científicos expertos bajo la dirección de dos especialistas con un interés específico en ortobiología (LL y LdG) y bajo la orientación del asesor de proyectos de consenso de la ESSKA (PB), se dividió a partes iguales en un grupo de preguntas y un grupo de bibliografía. El primer grupo realizó una serie de preguntas relevantes que se formularon con el objetivo de abordar las áreas de interés, la práctica diaria y las controversias actuales con respecto al uso de PRP para el tratamiento de la OA de rodilla. Las preguntas se priorizaron en función de su significación clínica, capacidad de respuesta e importancia científica mediante un programa informático de toma de decisiones (1000minds.com). Este programa informático presentaba repetidamente a los miembros del grupo pares de preguntas de investigación y les pedía que eligieran una en función de su importancia clínica, su capacidad de respuesta o su importancia científica o investigadora. Las comparaciones repetidas entre todos los miembros del grupo dieron lugar a una lista ordenada de preguntas de investigación, que el grupo directivo redujo y afinó hasta obtener 28 preguntas.
Las preguntas se dividieron en 3temas principales que representarían las 3 secciones de la lista de preguntas: fundamentos e indicaciones del PRP (preguntas 1-14); preparación y caracterización del PRP (preguntas 15-18), y protocolo del PRP (preguntas 19-28).
Para cada pregunta, el grupo de bibliografía realizó de forma independiente una búsqueda bibliográfica específica para determinar el estado actual de los conocimientos. La búsqueda bibliográfica se realizó entre junio de 2021 y noviembre de 2021 en PubMed, según las palabras clave pertinentes para cada pregunta específica. También se examinaron las referencias de los estudios identificados para obtener información adicional basada en la evidencia. También se incluyeron los artículos pertinentes publicados durante la realización del estudio de consenso. Se examinaron el título y el resumen de todas las referencias, y a continuación se obtuvo el artículo completo correspondiente para el grupo directivo y se resumió en un breve informe. Solo se tuvieron en cuenta los trabajos publicados en inglés entre 2000 y 2022, con un total de 275 citas correspondientes a 217 manuscritos (media de citas por pregunta=10).
Una vez concluidas las revisiones bibliográficas por parte del grupo de bibliografía para cada una de las preguntas, los miembros del grupo directivo, excepto los encargados de la búsqueda bibliográfica, elaboraron las respectivas declaraciones basadas en la literatura encontrada, así como en la opinión experta de todo el grupo directivo. Para cada declaración se utilizó un sistema de calificación para determinar su nivel científico. Las calificaciones, basadas en el nivel de evidencia (LOE, por su denominación en inglés, level of evidence) de los estudios existentes, indican si la literatura aporta pruebas suficientes y claras para producir una respuesta clara a cada pregunta y si la literatura está de acuerdo con la experiencia del consenso de expertos.
- •
Grado A (cuando había al menos tres documentos LOE1).
- •
Grado B (cuando había al menos tres documentos LOE2).
- •
Grado C (series de cohortes/estudios comparativos, con conclusiones concordantes. O estudios de alto nivel, pero con resultados contradictorios o no concluyentes).
- •
Grado D (la bibliografía es muy escasa o inexistente=opinión experta del grupo).
La asignación de la calificación se basó en el LOE de la literatura existente sobre el tema relacionado con la pregunta siguiendo las directrices internacionales con ligeras modificaciones27.
Todas las preguntas se debatieron a fondo, y el grupo directivo llegó a un consenso según la calificación científica. Una vez alcanzado un acuerdo general en el seno del grupo directivo, las preguntas/declaraciones se presentaron al grupo de calificación, compuesto por un panel independiente de 22clínicos experimentados a los que se pidió que puntuaran todas las declaraciones. La fase de calificación constó de dos rondas, en las que el panel evaluó y puntuó cada declaración según una escala numérica discreta (escala Likert de 1 [menor grado de consenso/totalmente inapropiado] a 9 [máximo grado de consenso/totalmente apropiado]. Un valor de «5» indicaría incertidumbre y, por tanto, cualquier valor por debajo de este umbral se consideraría no apropiado. Tras la primera ronda de calificación, el texto fue modificado por el grupo directivo, teniendo en cuenta los comentarios del grupo de calificación, y se llevó a cabo una segunda ronda de valoración por el grupo de calificación. Tras esta fase, se organizó una reunión conjunta de los grupos directivo y de calificación para validar el borrador y ultimar el texto de las declaraciones.
Debe tenerse en cuenta que el nivel de evidencia (que da lugar al grado de recomendación) y el consenso no están relacionados. El acuerdo es una característica específica de un consenso, lo que significa que los calificadores han llegado a un consenso común sobre una pregunta/declaración determinada. Obviamente, si existe un alto LOE en la bibliografía, teóricamente será fácil lograr un alto consenso entre los calificadores. Pero incluso en caso de bajo LOE (es decir, gradoC) o ausencia de bibliografía (es decir, gradoD) es posible lograr un alto consenso (es decir, 8, 8,5), siempre que la declaración esté bien redactada.
En el último paso, el texto definitivo se distribuyó entre el grupo de evaluación o revisión por pares compuesto por delegados elegidos por las sociedades afiliadas a la ESSKA de toda Europa para evaluar la claridad, la adaptabilidad geográfica y la aceptación de las declaraciones en toda Europa. En total, 18 sociedades afiliadas (16 países europeos) participaron en la revisión por pares del documento. A continuación se celebró una reunión final de todo el grupo directivo para finalizar el texto completo.
ResultadosEl documento de consenso completo, que incluye las referencias utilizadas, puede consultarse en los sitios web de la ESSKA y de la Academia ESSKA (http://www.esska.org/page/projects y https://academy.esska.org), así como en el Archivo suplementario 1.
Tras la segunda ronda de evaluación, las recomendaciones fueron calificadas con una media de 8,2±0,3 puntos sobre un máximo de 9puntos. Las puntuaciones medias de consenso para cada pregunta/declaración oscilaron entre 7,5 y 8,8. Solo seis de las 28 declaraciones recibieron una puntuación inferior a8. Tres recibieron una puntuación de 7,9, una de 7,8 y una pregunta dividida en dos declaraciones recibió una puntuación de 8,0 para la primera parte y de 7,5 para la otra. Todas las demás preguntas obtuvieron un consenso superior a 8,0 puntos. Por lo tanto, todas las declaraciones se consideraron adecuadas. Tres preguntas/declaraciones se evaluaron como gradoA, seis como gradoB, siete como gradoC y doce como gradoD (tabla 1).
Resumen de los resultados del consenso
| Pregunta | Título de la pregunta | Grado científico | Calificación | N. de referencias citadas (mejor evidencia) |
|---|---|---|---|---|
| 1 | ¿Apoya la evidencia clínica actual el uso de PRP para la OA de rodilla? | A | 8 | 10 (5 MA; 1 RS; 4 ECA) |
| 2 | ¿Para qué grados de OA de rodilla está mejor indicado el PRP? | A | 8,1 | 13 (6 ECA) |
| 3 | ¿Se puede utilizar el PRP en la OA severa de rodilla (KL4)? | C | 8,1 | 13 (6 ECA) |
| 4 | ¿Está indicado el PRP para el tratamiento de la femoropatelar (PFOA)? | C | 7,6 | 5 (2 ECA) |
| 5 | ¿Existen contraindicaciones específicas para el uso del PRP en la OA de rodilla? | D | 8 | 17 (2 RS; 2 ECA) |
| 6 | ¿Para qué franja de edad se recomienda el PRP? | D | 8,4 | 10 (3 MA; 2 ECA) |
| 7 | ¿Podría utilizarse el PRP para la OA de rodilla durante la fase inflamatoria cuando hay derrame articular (tras la aspiración del derrame)? | D | 7,9 | 10 (2 ECA; 4 ECL) |
| 8 | ¿Se recomienda un ciclo repetido de inyecciones de PRP tras un tratamiento previo con éxito de PRP para la OA de rodilla ante la reaparición de síntomas? | D | 8,4 | 7 (3 ECA; 1 EPA) |
| 9 | ¿Está justificada la inyección de PRP en la OA de rodilla temprana asintomática? (¿Prevención?) | D | 8,7 | 6 (3 RS) |
| 10 | ¿Existen ventajas en el uso de PRP en comparación con los corticosteroides para el tratamiento de la OA de rodilla? | A | 8,7 | 11 (6 MA; 2 RS; 1 ECA) |
| 11 | ¿Es el PRP una opción inyectable clínicamente mejor que el ácido hialurónico para el tratamiento de la OA de rodilla? | B | 8,1 | 10 (10 MA) |
| 12 | ¿Induce el PRP efectos modificadores de la enfermedad en la OA de rodilla? | C | 8,3 | 11 (1 RS; 8 ECA) |
| 13 | ¿Apoya la evidencia clínica actual el uso de suero autólogo condicionado (ACS) para la OA de rodilla? | B | 8,8 | 10 (2 ECA; 3 EPC) |
| 14 | ¿Apoya la evidencia clínica actual el uso de alfa-2-macroglobulina (A2M) para la OA de rodilla? | D | 8,7 | 8 (1 animal ECA; 1 EPC; 2 EIV) |
| 15 | ¿Qué PRP es preferible para la OA de rodilla: el PRP rico en leucocitos (LR-PRP) o el PRP pobre en leucocitos (LP-PRP)? | B | 8,1 | 7 (5 MA; 2 ECA) |
| 16 | ¿Cuál es el rango recomendado de número/concentración de plaquetas para las inyecciones de PRP en la OA de rodilla? | C | 8,2 | 9 (1 RS; 4 ECA) |
| 17 | Preparados/productos PRP para la OA de rodilla: ¿qué debemos medir en el PRP/control de calidad? | D | 8 | 10 (10 PEO) |
| 18 | ¿Cuál es el volumen recomendado de PRP para inyectar en una rodilla para el tratamiento de la OA de rodilla? | D | 8,7 | 14 (1 MA; 2 ECA; 1 EPC, 1 consenso) |
| 19 | ¿Cuántas inyecciones de PRP se recomiendan para el tratamiento de la OA de rodilla? | B | 8 | 20 (15 ECA) |
| 20 | Cuando se utiliza un protocolo de tratamiento con más de una inyección para la OA de rodilla, ¿cuál es el intervalo recomendado entre cada inyección de PRP? | B | 8 | 19 (1 RS; 11 ECA) |
| 21 | ¿Importan el tamaño de la jeringa y la aguja para la extracción de sangre y la inyección de PRP? | C (D1) D (D2) | 7,9 (D1) 7,9 (D2) | 2 (1 EPC; 1 EO) |
| 22 | ¿Están permitidos los antiinflamatorios no esteroideos (AINE) en torno al uso del PRP? | C (D1) C (D2) | 8,1 (D1) 8,3 (D2) | 9 (1 ECA; 3 EPC; 3 EIV) |
| 23 | ¿Deben utilizarse anestésicos locales intraarticulares al inyectar PRP? | D | 8,7 | 3 (3 EIV) |
| 24 | ¿Se recomienda la administración de antibióticos en torno al uso de PRP? | D | 8,6 | 4 (1 RS) |
| 25 | ¿Se recomienda ayunar antes de utilizar PRP? ¿Algún otro comportamiento de los pacientes podría afectar al tratamiento? | D (D1) D (D2) | 8,0 (D1) 7,5 (D2) | 15 (2 ECA) |
| 26 | ¿Pueden las inyecciones de corticosteroides previas al PRP mejorar los resultados en la OA de rodilla? | D | 8,3 | 13 (1 MA; 1 RS; 1 ECA; 1 EPC) |
| 27 | ¿Tienen el PRP y el ácido hialurónico un efecto sinérgico? | C | 7,8 | 6 (3 MA; 1 RS; 1 ECA) |
| 28 | ¿Existe alguna sinergia entre los PRP y las terapias celulares para la OA de rodilla? | B | 8 | 16 (5 ECA; 4 ECL; 1 EPC) |
D1 and D2: declaración 1 y 2, respectivamente, cuando se haya producido más de una declaración para la pregunta en cuestión; ECA: estudio controlado aleatorizado; ECL: estudio controlado de laboratorio; EIV: estudio in vitro; EO: estudio observacional; EPA: ensayo prospectivo aleatorizado; EPC: estudio prospectivo de cohortes; MA: metaanálisis; PEO: publicación «expert opinion»; RS: revisión sistemática.
La evidencia clínica confirma la eficacia del PRP en el tratamiento de la OA de rodilla. Los estudios clínicos de nivelI yII, así como otros estudios prospectivos, apoyan la seguridad y el beneficio clínico del PRP para la OA de rodilla en comparación con placebo (solución salina) y tratamientos de control como ácido hialurónico o corticosteroides. La eficacia del PRP en el tratamiento de la OA de rodilla también ha sido respaldada por metaanálisis y confirma los hallazgos de la investigación preclínica.
El grupo de consenso concluyó que hay suficiente evidencia preclínica y clínica para apoyar el uso de PRP en la OA de rodilla (ver las siguientes preguntas que abordan las especificaciones e indicaciones del PRP). (Grado A, Consenso: 8,0)
2. ¿Para qué grados de OA de rodilla está mejor indicado el PRP?La evidencia clínica ha mostrado la efectividad del PRP en pacientes con OA de rodilla de grados leve a moderado (KL≤3). El grupo de consenso concluye que el PRP se puede indicar principalmente en casos leves y moderados de OA de rodilla. (Grado A, Consenso: 8,1)
3. ¿Se puede utilizar el PRP en OA severa de rodilla (KL4)?El grupo de consenso está de acuerdo en que el tratamiento con PRP podría considerarse en casos seleccionados de OA de rodilla severa (KL4), por ejemplo, en pacientes que rechazan o no son aptos para cirugía debido a comorbilidades, aunque se podrían esperar resultados más bajos y los médicos deben proporcionar expectativas cautelosas al discutir o sugerir este enfoque. (Grado C, Consenso: 8,1)
4. ¿Está indicado el PRP para el tratamiento de la OA femoropatelar (PFOA)?A pesar de que la literatura actual sobre el efecto del PRP para la PFOA es limitada, la evidencia sugiere que puede tener efectos positivos, especialmente en la enfermedad en etapas tempranas. El grupo de consenso no considera que la presencia de PFOA sea una contraindicación o un factor limitante al considerar el PRP como una opción inyectable para la OA de rodilla. Además, como se ha demostrado que el PRP afecta el entorno de la rodilla en general, el grupo de consenso considera el PRP como una opción en presencia de PFOA. (Grado C, Consenso: 7,6)
5. ¿Existen contraindicaciones específicas para el uso del PRP en la OA de rodilla?Además de las contraindicaciones generalmente aceptadas para cualquier inyección en la rodilla, se han identificado otras contraindicaciones específicas para las inyecciones de PRP en el tratamiento de la OA de rodilla. Si bien la mayoría de las contraindicaciones sugeridas no han sido estudiadas de manera exhaustiva o suficiente, el grupo de consenso recomendó precaución en presencia de malignidades coexistentes o condiciones sistémicas debido a la posibilidad de interacciones desconocidas.
- •
Contraindicaciones debido a problemas locales en el área de inyección: cualquier contraindicación para las inyecciones en la rodilla, como infecciones, problemas cutáneos, otros.
- •
Contraindicaciones debido a problemas sistémicos (se pueden agrupar en 4 grupos principales):
- ∘
Infecciones
Además de las razones bien conocidas para no realizar una inyección en la rodilla en un paciente con infecciones sistémicas activas, las infecciones sistémicas también afectan negativamente el rendimiento/funcionalidad del PRP, ya que además del proceso inmune e inflamatorio que generan a nivel sistémico, las plaquetas se modifican en estos procesos y pueden volverse más hiperreactivas, alterando su funcionalidad.
- ∘
Cáncer
Existen contraindicaciones específicas para el uso de PRP en pacientes con malignidades activas.
En cuanto a las malignidades, la literatura actual no ha demostrado un vínculo claro entre los contenidos del PRP y el riesgo de proliferación tumoral, ya sea local o a distancia. Sin embargo, debido al riesgo teórico de que el PRP y los factores de crecimiento puedan contribuir a la promoción del crecimiento tumoral en situaciones en las que exista un tumor benigno o maligno en la articulación de la rodilla, el grupo de consenso considera estas condiciones como una contraindicación para inyectar PRP. Debido a preocupaciones similares y hasta que haya más evidencia disponible, el grupo de consenso recomienda que esta recomendación también se aplique a tumores con o sin metástasis ubicados en otras localizaciones fuera/incluso lejos de la rodilla, aunque se debe consultar con el oncólogo/médico tratante en casos específicos.
- ∘
Enfermedades inflamatorias
La presencia de enfermedades inflamatorias locales o sistémicas (artritis reumatoide, enfermedad de Crohn y otras enfermedades autoinmunes) no impide la posibilidad de inyectar PRP en la rodilla. Sin embargo, la naturaleza de estas enfermedades puede llevar a un plasma con un alto contenido de moléculas proinflamatorias que podrían generar resultados menores.
- ∘
Trastornos sanguíneos y de plaquetas cuantitativos y cualitativos
Problemas como trombocitopenia, trombocitosis o coagulopatías también pueden alterar el número de plaquetas y su funcionalidad.
- ∘
El uso de terapia antiplaquetaria debe considerarse una contraindicación relativa para el PRP. Esto está principalmente relacionado con pacientes que no pueden someterse a cirugía u otros tipos de tratamientos más invasivos, sin muchas alternativas en la búsqueda de alivio sintomático temporal. Sin embargo, debe ser obligatoria la información sobre los inferiores resultados esperados. (Grado D, Consenso: 8,0)
6. ¿Para qué franja de edad se recomienda el PRP?La mayoría de los estudios incluyeron pacientes con una edad media entre 55 y 65años. El grupo de consenso está de acuerdo en que no se puede recomendar un rango de edad específico, aunque reconoce que hay evidencia de una respuesta reducida en pacientes mayores. El grupo de consenso sugiere que se deben considerar otros factores y que la decisión no debe basarse solo en la edad cronológica. (Grado D, Consenso: 8,4)
7. ¿Podría utilizarse el PRP para la OA de rodilla durante la fase inflamatoria cuando hay derrame articular (tras la aspiración del derrame)?Actualmente no existe evidencia clínica sobre la inyección de PRP durante la fase inflamatoria en la OA de rodilla, ni sobre la aspiración del derrame antes de la inyección de PRP.
Estudios preclínicos y clínicos han sugerido propiedades antiinflamatorias en el PRP, lo que podría apoyar la justificación de su uso durante la fase inflamatoria.
Aunque no existe evidencia sobre el momento óptimo de la inyección de PRP para la OA de rodilla cuando hay derrame, el grupo de consenso reconoce que, cuando está presente, la aspiración del derrame es probablemente beneficiosa para mejorar el dolor y aliviar las limitaciones funcionales. El grupo de consenso recomienda la aspiración del derrame también para evitar la dilución del PRP tras la inyección. (Grado D, Consenso: 7,9)
8. ¿Se recomienda un ciclo repetido de inyecciones de PRP tras un tratamiento previo con éxito de PRP para la OA de rodilla ante la reaparición de síntomas?Aunque la evidencia actual con respecto a los ciclos repetidos de tratamiento con PRP para la OA de rodilla es limitada, se ha sugerido que esta estrategia puede tener beneficios clínicos. Dado que la evidencia sugiere una disminución de los efectos del PRP para la OA de rodilla a lo largo del tiempo, el grupo de consenso está de acuerdo en que podría considerarse un ciclo adicional ante la reaparición de los síntomas. (Grado D, Consenso: 8,4)
9. Está justificada la inyección de PRP en la OA de rodilla temprana asintomática? (¿Prevención?)En la actualidad,no hay suficientes estudios clínicos que aborden esta cuestión, por lo que no se puede afirmar que la aplicación de PRP en la OA asintomática prevenga su progresión. Aunque los estudios preclínicos sugieren un papel condroprotector del PRP, no existe suficiente evidencia clínica sobre el efecto condroprotector del PRP en pacientes con estadios iniciales asintomáticos de OA. Por lo tanto, el grupo de consenso no aboga actualmente por el uso de PRP en la OA de rodilla temprana asintomática. (Grado D, Consenso: 8,7)
10. ¿Existen ventajas en el uso de PRP en comparación con los corticosteroides para el tratamiento de la OA de rodilla?Aunque los corticosteroides son potentes agentes antiinflamatorios y pueden proporcionar un alivio a corto plazo en la OA de rodilla, se ha demostrado que tienen efectos perjudiciales sobre los condrocitos y pueden acelerar la degeneración del cartílago, especialmente con inyecciones múltiples/repetidas. Se ha demostrado que las inyecciones de PRP tienen un efecto más prolongado en comparación con el efecto a corto plazo de las inyecciones de corticosteroides. También parecen ofrecer un perfil de uso más seguro, con menos complicaciones potenciales relacionadas. El grupo de consenso considera que las inyecciones de PRP son una opción de tratamiento más segura, no condrotóxica y más eficaz, con mejoras clínicas a más largo plazo en comparación con las inyecciones de corticosteroides. (Grado A, Consenso: 8,7)
11. ¿Es el PRP una opción inyectable clínicamente mejor que el ácido hialurónico para el tratamiento de la OA de rodilla?Existen varios estudios de alto nivel, así como múltiples metaanálisis, que comparan la eficacia del PRP con la del ácido hialurónico para la OA de rodilla, y la mayoría favorecen al PRP en términos de mejoría clínica global y de un efecto más duradero.
Basándose en la evidencia actual disponible, el grupo de consenso apoya el uso de PRP sobre el ácido hialurónico para la OA de rodilla debido a la mejoría clínica general y los efectos esperados más duraderos, aunque reconoce que existen diferentes formulaciones de los productos que pueden introducir algún sesgo en las conclusiones de los metaanálisis. (Grado B, Consenso: 8,1)
12. ¿Induce el PRP efectos modificadores de la enfermedad en la OA de rodilla?Los estudios preclínicos (modelos animales) sugieren algunos efectos modificadores de la enfermedad, con cambios positivos en el tejido cartilaginoso y en la membrana sinovial. Aunque algunos estudios clínicos han sugerido un potencial modificador de la enfermedad del PRP en el cartílago degenerativo, el grupo de consenso reconoce que la evidencia clínica actual con respecto a los efectos modificadores de la enfermedad del PRP en la OA de rodilla en humanos es insuficiente. (Grado C, Consenso: 8,3)
13. ¿Apoya la evidencia clínica actual el uso de suero autólogo condicionado (ACS) para la OA de rodilla?En comparación con el PRP, el ACS está menos investigado. No existe evidencia clara con respecto al papel del ACS en el tratamiento de la OA. Aunque puede tener un papel como posible agente modulador de la inflamación debido a la presencia del receptor antagonista de la IL-1 en este producto, los resultados sobre la eficacia clínica de este abordaje son inconsistentes. Actualmente no se pueden ofrecer recomendaciones debido a la falta de evidencia suficiente. (Grado B, Consenso: 8,8)
14. ¿Apoya la evidencia clínica actual el uso de alfa-2-macroglobulina (A2M) para la OA de rodilla?En comparación con el PRP, la A2M está menos investigada. Los estudios preclínicos demostraron que la administración intraarticular de A2M induce un mecanismo antiinflamatorio y ralentiza el daño del cartílago y la resorción ósea. Sin embargo, como no hay ensayos clínicos aleatorizados sobre el uso de A2M para la OA de rodilla, actualmente no se pueden ofrecer recomendaciones. (Grado D, Consenso: 8,7)
Sección 2: Preparación/caracterización del PRP15. ¿Qué PRP es preferible para la OA de rodilla: el PRP rico en leucocitos (LR-PRP) o el PRP pobre en leucocitos (LP-PRP)?Varios metaanálisis y metaanálisis en red han comparado la eficacia del LP-PRP con el LR-PRP para la OA de rodilla, con resultados en general poco concluyentes.
El grupo de consenso reconoce que la eficacia del PRP es probablemente multifactorial y, por lo tanto, la dependencia de la presencia de leucocitos por sí sola podría estar sobrevalorada, ya que otros factores también pueden contribuir. Por lo tanto, el grupo de consenso actualmente no apoya un tipo de PRP sobre el otro y considera que tanto la LP-PRP como la LR-PRP son opciones válidas para el tratamiento de la OA de rodilla cuando se considere el PRP. (Grado B, Consenso: 8,1)
16. ¿Cuál es el rango recomendado de número/concentración de plaquetas para las inyecciones de PRP en la OA de rodilla?El efecto del PRP es complejo y multifactorial, en el que los numerosos factores de crecimiento liberados desempeñan un papel importante, así como las citoquinas pro y antiinflamatorias liberadas tras la activación de las plaquetas. Sin embargo, no se ha establecido una correlación clara entre el número de plaquetas en el PRP y la respuesta clínica. No hay duda de que las plaquetas son el actor central en los productos PRP; sin embargo, el grupo de consenso concluye que la caracterización óptima del PRP para la OA de rodilla es compleja e incluye muchas variables, por lo que actualmente no se pueden definir los rangos óptimos de plaquetas para el tratamiento de la OA de rodilla. (Grado C, Consenso: 8,2)
17. Preparados/productos PRP para la OA de rodilla: ¿qué debemos medir en el PRP/control de calidad?Las preparaciones y los productos de PRP varían en cuanto al número y la concentración de plaquetas, los niveles de factores de crecimiento específicos, el contenido de glóbulos blancos y el volumen, y también están influidos por los parámetros sanguíneos basales (como el recuento de plaquetas basal). Por lo tanto, las preparaciones de PRP obtenidas mediante kits comerciales pueden variar en contenido y podrían producir preparaciones inconsistentes. Por estas razones, el grupo de consenso sugiere que el registro de al menos la composición celular y plaquetaria basal de la sangre total, así como de la preparación de PRP producida, mejoraría la comprensión de la eficacia del PRP para la OA de rodilla y debería recomendarse como medida de control de calidad en el marco de la investigación clínica, con el objetivo de fomentar en el futuro el uso rutinario de dichas medidas de control de calidad en los procedimientos clínicos. La recopilación de estos parámetros permitiría incorporar los datos en alguna de las clasificaciones de PRP disponibles en la actualidad, lo que a su vez permitiría realizar comparaciones entre productos y un análisis más profundo del control de calidad. (Grado D, Consenso: 8,0)
18. ¿Cuál es el volumen recomendado de PRP para inyectar en una rodilla para el tratamiento de la OA de rodilla?Aunque el volumen total de PRP inyectado puede ser importante, actualmente no existe evidencia en la literatura sobre el volumen óptimo a inyectar, con volúmenes que oscilan entre 2 y 12ml.
El grupo de consenso no puede ofrecer ninguna recomendación sobre el volumen, aunque sugiere que se tenga en cuenta el tamaño de la rodilla. (Grado D, Consenso: 8,7)
Sección 3: Protocolo de PRP19. ¿Cuántas inyecciones de PRP se recomiendan para el tratamiento de la OA de rodilla?Aunque la literatura no es concluyente con respecto al número óptimo de inyecciones por ciclo de tratamiento con PRP para la OA de rodilla, la mayoría de los artículos informan que los protocolos con más de una inyección proporcionan una mejoría clínica, al menos con la OA temprana.
El grupo de consenso es consciente de que factores como el volumen de inyección y la concentración de plaquetas pueden diferir en gran medida entre los productos de PRP disponibles y pueden influir en el efecto de cada inyección. El grupo de consenso recomienda un intervalo de 2-4 inyecciones. (Grado B, Consenso: 8,0)
20. Cuando se utiliza un protocolo de tratamiento con más de una inyección para la OA de rodilla, ¿cuál es el intervalo recomendado entre cada inyección de PRP?Aunque la bibliografía no es concluyente sobre el intervalo óptimo entre inyecciones cuando se utiliza un protocolo de inyecciones múltiples de PRP (>1 inyección por ciclo de tratamiento) para la OA de rodilla, se han notificado intervalos que oscilan entre 1 y 4semanas.
Dado que el principal período de actividad del factor de crecimiento liberado tiene lugar en las 3primeras semanas desde la inyección, el grupo de consenso sugiere que los intervalos de 1 a 3semanas pueden ser más apropiados. (Grado B, Consenso: 8,0)
21. ¿Importan el tamaño de la jeringa y la aguja para la extracción de sangre y la inyección de PRP?La evidencia actual no sugiere que el tamaño de la aguja sea un factor que influya en la integridad de las plaquetas. El grupo de consenso recomienda que el tamaño de la aguja no debería importar ni para la inyección de PRP ni para la extracción de sangre en la preparación de PRP para trastornos musculoesqueléticos. (Grado C, Consenso: 7,9)
Debe tenerse precaución con el caudal durante la aspiración de la sangre cuando se utilicen jeringas de gran tamaño en una técnica manual para evitar la hemólisis de la sangre. (Grado D, Consenso: 7,9)
22. ¿Están permitidos los antiinflamatorios no esteroideos (AINE) en torno al uso PRP?Con respecto al uso de AINE en torno a las inyecciones de PRP, aunque las pruebas actuales no son concluyentes, los posibles efectos de los AINE sobre las plaquetas y la liberación de factores de crecimiento in vivo siguen justificando la precaución. Por lo tanto, el grupo de consenso recomienda evitar el uso de AINE durante las dos semanas previas a la administración de PRP. (Grado C, Consenso: 8,1)
Para el tratamiento del dolor tras las inyecciones de PRP, dado que los AINE pueden afectar a la liberación del factor de crecimiento incluso después de la inyección, el grupo de consenso recomienda evitar los AINE durante la primera semana tras la inyección y, en caso necesario, utilizar analgésicos no antiinflamatorios (por ejemplo, paracetamol, metamizol, tramadol). (Grado C, Consenso: 8,3)
23. ¿Deben utilizarse anestésicos locales intraarticulares al inyectar PRP?Actualmente no existen estudios clínicos de alto nivel sobre el efecto de los anestésicos locales en el PRP; sin embargo, los estudios in vitro han demostrado que los anestésicos locales interfieren en la integridad y la funcionalidad de las plaquetas, además de disminuir los efectos positivos del PRP en la proliferación celular. Por lo tanto, el grupo de consenso no recomienda actualmente el uso de anestésicos locales intraarticulares al inyectar PRP.
Sin embargo, el grupo de consenso está de acuerdo en que los anestésicos locales pueden administrarse por vía subcutánea, sin penetrar en la cápsula. (Grado D, Consenso: 8,7)
24. ¿Se recomienda la administración de antibióticos en torno al uso de PRP?La evidencia clínica actual no respalda el uso de antibióticos en torno al uso del PRP. Por lo tanto, el grupo de consenso no recomienda el uso de antibióticos en torno al uso del PRP. (Grado D, Consenso: 8,6)
25. ¿Se recomienda ayunar antes de utilizar PRP? ¿Algún otro comportamiento de los pacientes podría afectar al tratamiento?Faltan datos sobre el impacto directo del ayuno sobre los efectos terapéuticos del PRP. Sin embargo, dado que existe evidencia sobre el efecto de diversos alimentos y dietas altas en grasas y colesterol sobre el comportamiento de las plaquetas, tanto en número como en función, así como en la activación plaquetaria, el grupo de consenso recomienda que los pacientes eviten los alimentos ricos en grasas durante al menos las 24horas previas a la extracción de sangre. (Grado D, Consenso: 8,0)
La eliminación del alcohol durante al menos 48horas previas a la preparación del PRP puede permitir que las plaquetas restablezcan su contenido normal en factores y propiedades de agregación; por lo tanto, el grupo de consenso lo considera una sugerencia segura. (Grado D, Consenso: 7,5)
26. ¿Pueden las inyecciones de corticoesteroides previas al PRP mejorar los resultados de la OA de rodilla?El grupo de consenso recomienda evitar el uso de PRP cercano a los corticosteroides. Sin embargo, el grupo de consenso reconoce que los pacientes pueden haber recibido inyecciones recientes de corticosteroides y, en este escenario, el grupo de consenso sugiere un intervalo mínimo de 6semanas desde una reciente inyección de corticosteroides. (Grado D, Consenso: 8,3)
27. ¿Tienen el PRP y el ácido hialurónico un efecto sinérgico?Si bien la literatura preclínica y clínica actual sugiere algunos beneficios potenciales de combinar estos dos productos, aún falta evidencia de los beneficios claros de combinar estos tratamientos. Por lo tanto, el grupo de consenso reconoce que se necesitan más datos antes de recomendar la combinación de PRP y ácido hialurónico en lugar de PRP solo para la OA de rodilla. (Grado C, Consenso: 7,8)
28. ¿Existe alguna sinergia entre los PRP y las terapias celulares para la OA de rodilla?Si bien la literatura preclínica y clínica actual sugiere algunos beneficios potenciales de combinar PRP y terapia celular, con la mayoría de los estudios centrados en el cultivo de células expandidas, aún falta evidencia sobre los beneficios claros del uso de estos productos combinados en lugar de su uso independiente. Por lo tanto, según la evidencia actual, el grupo de consenso no sugiere la combinación de PRP y terapia celular sola para la OA de rodilla. (Grado B, Consenso: 8,0)
DiscusiónEl grupo de consenso ESSKA-ORBIT produjo un documento de consenso sobre el uso de productos ortobiológicos derivados de la sangre para el tratamiento no quirúrgico de la OA de rodilla, donde el principal hallazgo es que, según la evidencia actual, existe un acuerdo dentro del grupo de consenso para apoyar el uso de PRP como una opción de tratamiento no quirúrgico válida para la OA de rodilla de grados KL1-3, que podría considerarse como una opción de tratamiento inyectable de primera línea en estos pacientes (fig. 2).
A pesar de que los resultados clínicos documentados se ven afectados por la variabilidad en las indicaciones, en los protocolos de preparación, en los protocolos de administración y en las características del producto, el grupo de consenso pudo alcanzar un alto nivel de conformidad en todas las preguntas. No obstante, no hay que pasar por alto que aún existen controversias en relación con su plena eficacia. Sin embargo, estas discrepancias se han reducido progresivamente con el tiempo, con resultados cada vez más consistentes que muestran resultados clínicos significativos y duraderos cuando se utiliza PRP para el tratamiento conservador de la OA de rodilla.
En cuanto a los tratamientos de competencia, aunque el ácido hialurónico todavía podría considerarse el tratamiento conservador de primera línea más común por razones prácticas, se ha demostrado que el PRP es superior al ácido hialurónico, con más de 25 estudios controlados aleatorios de nivelI publicados entre 2011 y 2019 que respaldan consistentemente esta evidencia8,28–31. Curiosamente, no se han observado diferencias después de 1mes desde la inyección entre los dos tratamientos, mientras que el PRP obtuvo una puntuación clínicamente mejor a los 3, 6 y 12meses de seguimiento, lo que confirma la mayor durabilidad de los resultados en comparación con otros tratamientos18,20,32,33. En comparación con los corticosteroides, el PRP también demostró ser superior por múltiples metaanálisis incluyendo estudios de nivelI33 o de nivelI yII32, más allá de haber reportado ser más seguro y sin efectos secundarios en comparación con los corticosteroides.
El consenso estaba dirigido a responder y proporcionar recomendaciones sobre las cuestiones claves que los médicos pueden encontrar al considerar el uso de ortobiológicos para la OA de rodilla. Por lo tanto, por razones prácticas, el documento se dividió en 3secciones principales que abordan la idoneidad de este enfoque y las indicaciones relevantes, aspectos relacionados con la variabilidad del producto y las características de los diferentes productos disponibles, así como aspectos relacionados con la administración, la seguridad y la peri-administración. Además, el documento analiza el papel del PRP en comparación con otros agentes inyectables.
Reunir un grupo líder de expertos en un campo específico es crucial para generar un consenso de alta calidad. Otro factor clave para llevar a cabo y completar con éxito un proyecto de consenso es el estricto cumplimiento de una metodología bien definida y validada25,26,34 que incluye un proceso iterativo que es necesario para garantizar un acuerdo cada vez mayor y ayuda a lograr un alto nivel de consenso.
Otro punto fuerte del consenso actual es su representación geográfica paneuropea: el proyecto del consenso involucra 75 médicos y científicos de un total de 23 países europeos. Por lo tanto, el documento del consenso debe considerarse como una descripción fiable de la posición europea sobre este tema, haciéndolo más amplio que los ya publicados por grupos nacionales sobre el mismo tema, aunque sea de buena calidad35. Además, este grupo de consenso se centró en aspectos como la comparación con otros tratamientos inyectables, la diferencia con productos derivados de la sangre que no se basan en la concentración de plaquetas, el posible efecto modificador de la enfermedad del tratamiento con PRP, así como la posible influencia del comportamiento de los pacientes sobre la eficacia clínica del PRP que no fueron abordados en trabajos de consensos anteriores35.
Dada la participación activa de 18 sociedades ortopédicas nacionales europeas, sería importante difundir los resultados del consenso en sus respectivas comunidades para crear un enfoque continental homogéneo. Sin embargo, también es importante reconocer que los sistemas de atención médica son diferentes entre los diferentes países y pueden influir en la toma de decisiones clínicas en la práctica diaria y no siempre estar en línea con los datos científicos. De este modo, las declaraciones y las recomendaciones proporcionadas en este consenso no representan valores absolutos ni parámetros independientes, sino que más bien deben interpretarse de manera crítica para cada paciente individual y usarse en combinación con la evaluación clínica y otras evaluaciones objetivas para desarrollar una planificación preoperativa adecuada caso por caso.
El documento también incluye algunas limitaciones. En primer lugar, un consenso suele incluir aspectos con alta evidencia científica y otros con baja evidencia científica. En estos últimos casos se ha recurrido a la opinión de expertos para dar la mejor recomendación disponible. Sin embargo, si bien las revisiones sistemáticas de alto nivel incluyen solo evidencia científica de alto nivel, a menudo no son capaces de responder las preguntas que formulan los profesionales cotidianamente. Este es el alcance de un consenso: incluso si para algunas preguntas el grado de recomendación es bajo, el documento proporciona la mejor ayuda práctica disponible para los profesionales.
En segundo lugar, este consenso informa recomendaciones en un momento específico, pero a medida que el conocimiento evolucione con el tiempo, el tratamiento de la OA de rodilla puede evolucionar y desarrollarse consecuentemente. Un reconocimiento importante al interpretar estas recomendaciones es que perfilar al paciente con OA de rodilla ideal para el uso de PRP/productos derivados de la sangre es complejo y multifactorial. La decisión de tratamiento a menudo no se basa en factores aislados y es la comprensión de en qué parte del proceso de OA el médico se encuentra con el paciente, integrando factores variables, objetivos y subjetivos, incluida la experiencia personal del médico. Además, es importante recordar que la OA de rodilla suele ser multifactorial y la mala alineación mecánica puede desempeñar un papel importante en ciertos casos (mala alineación femorotibial y patelofemoral), que podría abordarse quirúrgicamente cuando sea relevante. Si bien el consenso no puede abordar todos y cada uno de los escenarios específicos, cuando se analizan las inyecciones ortobiológicas para la OA de rodilla no nos referimos a escenarios de mala alineación mecánica grave que puedan requerir intervención quirúrgica, aunque las decisiones deben tomarse caso por caso. En tercer lugar, dado que habría sido imposible llevar a cabo un proceso de consenso para cada tipo diferente de producto derivado de la sangre, el documento del consenso recopila información y resultados derivados de varios tipos de productos con características diferentes. Por tanto, los resultados del consenso son aplicables a aquellos productos que van acompañados de un buen nivel de evidencia clínica.
Por lo tanto, el alcance de este consenso no fue proporcionar un menú «a la carta» para perfilar al paciente/candidato ideal, sino más bien brindar recomendaciones que aborden escenarios comunes cuando se considera la terapia con hemoderivados para la OA de rodilla.
Todos los posibles conflictos de intereses de todos los involucrados en la redacción del consenso (grupo directivo y de calificación) se informan en el documento de consenso completo disponible en el Archivo complementario 1 y en los sitios web de ESSKA y ESSKA Academy (http://www.esska.org/page/projects y https://academy.esska.org).
Dado que los grupos directivos y calificador del consenso estaban compuestos por expertos activos en los campos, algunas de las referencias incluidas en el documento del consenso obviamente involucraban a estos miembros. Sin embargo, el porcentaje de referencias que incluye como autores a miembros del grupo directivo y/o calificador (en primera, última o intermedia posición) es solo del 15% (33 de 217 artículos citados, con un promedio de menos de un artículo por miembro, siendo el número total de miembros del grupo directivo y calificador igual a 36). Esto se suma a la equidad del proceso y a la imparcialidad del análisis, lo que se ve respaldado por el elevado número de médicos y científicos involucrados en el proceso (75 en total).
ConclusionesEl tratamiento de la OA de rodilla es complejo y el uso de ortobiológicos es cada vez mayor en este campo de la medicina. El consenso europeo ESSKA-ORBIT ha sido desarrollado para ayudar y mejorar la toma de decisiones al considerar el uso de productos derivados de la sangre para el tratamiento de la OA de rodilla. Según los resultados de este grupo de consenso, dada la gran cantidad de literatura y opiniones de expertos existentes, el PRP se consideró una opción válida de tratamiento para la OA de rodilla, y como una posible opción de tratamiento inyectable de primera línea para el tratamiento no quirúrgico de la OA de rodilla, principalmente para los grados KL1-3.
Este proyecto debe considerarse más como «marco de trabajo» que como «pautas estrictas», cuyo objetivo es proporcionar un marco de referencia para el uso de productos derivados de la sangre para el tratamiento de la OA de rodilla, basado en la literatura científica actual predominante y en el punto de vista de los expertos.
Nivel de evidenciaNivel de evidencia II.
FinanciaciónEl proyecto de consenso fue respaldado y promovido por la Sociedad Europea de Traumatología Deportiva, Cirugía de Rodilla y Artroscopia - The European Society for Sports Traumatology, Knee Surgery and Arthroscopy (ESSKA).
Consideraciones éticas- 1.
¿Su trabajo ha comportado experimentación en animales?: No.
- 2.
¿En su trabajo intervienen pacientes o sujetos humanos?: No.
- 3.
¿Su trabajo incluye un ensayo clínico?: No.
- 4.
¿Todos los datos mostrados en las figuras y tablas incluidas en el manuscrito se recogen en el apartado de resultados y las conclusiones?: Sí.
Conflicto de intereses de los participantes en el grupo directivo del consenso:
Laura de Girolamo: honorarios u honorarios de consultoría: Lipogems International (IT); subvenciones/apoyos a la investigación: Fidia (IT).
Elizaveta Kon: honorarios u honorarios de consultoría: Cartiheal (IL), Green Bone (IT), Geistlich (CH); subvenciones/apoyos a la investigación: Zimmer Biomet (EE.UU.), Mastelli (IT), Fidia (IT), Cartiheal (IL); honorarios como ponente de empresa: Zimmer Biomet (EE.UU.), Fidia (IT); accionista: CARTIHEAL (IL).
Jeremy Magalon: apoyo educativo: Fidia (IT), Horiba (JP), Malopharma (FR), Arthrex (EE.UU.), Horus (FR); cofundador de Remedex (FR).
Todos los demás miembros del grupo de dirección declaran no tener conflicto de intereses.
Nuestro reconocimiento a los miembros del grupo de calificación: Eduard Alentorn-Geli, Isabel Andia, Lars Blønd, Berte Bøe, Tomislav Cengic, Ignacio Dallo, Philipp Heuberer, Kaiwan Izadpanah, Ladislav Kovacic, Koen Carl Lagae, Laura Mangiavini, Jacques Menetrey, Stefan Mogos, Emmanuel Papakostas, Yiannis Pengas, Helder Pereira, Tim Spalding, Tomasz Piontek, Patricia Thoreux, Trifon Totlis, Kerem Tekin Ulku, Yaniv Yonai, Stefano Zaffagnini, así como a los revisores de las sociedades nacionales afiliadas (AEA, AGA, BAKAST, BKS, EASTS, GOTS, HAA, LIROMS, NVA, PTA, SETRADE, SFA, SFTS, SIAGASCOT, SPAT, SPOT, SSASST y TUSYAD) por su revisión. Un agradecimiento especial a la Junta de ESSKA y en particular a Jacques Menetrey, Roland Becker y Joan Carlos Monnlau por su apoyo y liderazgo, así como a la oficina de ESSKA, en particular a Anna Hansen, por la ayuda administrativa. Gracias también a João Espregueira Mendes por su apoyo y el de su equipo a este proyecto. El proyecto de consenso fue respaldado y promovido por la Sociedad Europea de Traumatología del Deporte, Cirugía de Rodilla y Artroscopia (ESSKA).
Versión española del artículo publicado anteriormente en open access: «The use of injectable orthobiologics for knee osteoarthritis: A European ESSKA- ORBIT consensus. Part 1 — blood-derived products (platelet-rich plasma)».
El grupo de trabajo ORBIT está compuesto por: Laura de Girolamo, Lior Laver, Giuseppe Filardo, Ferran Abat, Ricardo Bastos, Ramon Cugat, Michael Iosifidis, Baris Kocaoglu, Elizaveta Kon, Jeremy Magalon, Rodica Marinescu, Marko Ostojic, Mikel Sanchez, Thomas Tischer, Diego Delgado, Patricia Laiz, Yosef Sourougeon y Montserrat García-Balletbó.