La reparación de una fractura es un proceso en el que intervienen factores a) biológicos (celulares y tisulares) desde la proliferación y diferenciación celular hasta la regeneración vascular; b) bioquímicos, una cascada de sustancias que se activan o modifican durante el proceso y c) mecánicos, ya que una fractura no puede curar si las condiciones mecánicas no son las adecuadas.
El proceso biológico tiene como función transformar una estructura inestable en estable produciendo un tejido primitivo que rellene el espacio interfragmentario y evite los movimientos y las deformaciones. La reacción perióstica y medular dan lugar a tejidos de aparición rápida: cartilaginoso y fibroso, que luego se transformarán en hueso.
La función del cirujano en la reparación de una fractura se debe limitar a evitar las deformaciones y prevenir las consolidaciones viciosas con la aplicación correcta de los métodos de osteosíntesis que requiere el conocimiento de su mecánica, respetar las necesidades biológicas y bioquímicas del proceso de consolidación y conocer la compatibilidad entre los tejidos receptores y los materiales implantados.
Un hueso se fractura cuando las tensiones deformantes exceden la resistencia del material. Bajo solicitaciones axiales en el lado de la convexidad se produce una solicitación de tensión y en el lado de la concavidad de compresión y como el hueso es más vulnerable a la tracción que a la compresión,5,21 el lado convexo (sometido a tracción) falla primero. El fallo a tracción ocurre progresivamente a través del hueso, creando una fractura transversa. En ocasiones, la zona cortical sometida a compresión se puede romper antes que la zona que soporta la tracción originándose un tercer fragmento «en mariposa» o múltiples fragmentos.16
Proceso de reparación
En toda fractura, el proceso de consolidación empieza en el mismo momento de su producción y, siempre que las condiciones sean favorables, la reparación sigue un proceso dividido en tres fases: inflamatoria, de regeneración y de remodelación del callo, que puede verse modificado por multitud de factores externos, mecánicos o químicos, que la aceleran, retardan o incluso la impiden.
Desde el punto de vista mecánico, Burny,4 en 1968, distinguió tres fases en la curación de una fractura. La primera, durante las tres primeras semanas, en la que aumenta la movilidad del foco por la necrosis ósea y la reabsorción de los fragmentos óseos disminuyendo temporalmente su estabilidad. En la segunda fase se produce un aumento progresivo de la estabilidad disminuyendo la deformación y al tercer periodo, cuando el callo alcanza ya un 50% del módulo elástico del hueso sano.
En los años 60 se observó, clínica y experimentalmente, que la fijación rígida de una osteotomía con una placa a compresión, inhibía la formación del callo perióstico y los extremos óseos se unían directamente mediante una remodelación haversiana,26 estableciendo dos patrones de consolidación de las fracturas, primario y secundario (o espontáneo). La consolidación primaria8 consistía en la formación y remodelación simultánea de hueso nuevo en el foco de fractura, sin aparición de fibrocartílago, una reconstrucción directa mediante remodelación haversiana, sin callo perióstico y sin reabsorción de los extremos óseos. La consolidación con formación de callo perióstico y endóstico se consideró secundaria, por el hecho de formarse inicialmente un tejido fibroso o fibrocartílago entre los extremos de la fractura.2,6,13,26
En una fractura no sólo se rompe el tejido óseo. El periostio se desgarra, la médula se lesiona y se dañan los tejidos blandos circundantes. Los vasos se rompen y la sangre afluye al foco de fractura, se coagula y forma un hematoma en el interior y alrededor de la fractura.17 Los osteocitos cercanos al foco de fractura mueren por falta de vascularización y por los productos tóxicos liberados durante la fase de inflamación. En el foco se liberan mediadores químicos por la disminución del oxígeno hístico, el pH (ácido) y la liberación de enzimas lisosomales, que estimulan a las células supervivientes. Además, los músculos dañados se desvitalizan de tal manera que algunos se necrosan y otros degeneran por el edema y otros cambios vasculares. También se produce una degeneración grasa en la cavidad medular con la invasión de macrófagos, que aumentan la actividad proliferativa de las capas del periostio.17
Después de la primera semana, el coágulo es invadido por capilares neoformados y fibroblastos, que lo transforman en tejido conjuntivo, embrionario, de granulación con mamelones vasculares intensamente activos. Posteriormente, el hematoma organizado será invadido por los vasos procedentes de capilares periósticos, endósticos y del sistema haversiano. Existe una asociación entre el aporte vascular y la reparación de la fractura.22-24,26 Al principio hay una fragilidad capilar ya que las deformaciones locales impiden la revascularización primaria e interrumpen el aporte vascular a las osteonas en desarrollo. La proliferación y diferenciación celular produce nuevos condroblastos y osteoblastos en el tejido de granulación que los macrófagos se encargan de eliminar. Este tejido será ocupado por células mesenquimales pluripotenciales desde los tejidos vecinos y del endotelio de los capilares que invaden el hematoma,20,31 con sus fibras de colágeno y células osteogénicas,14 que se transformará, después de algunas semanas, en cartílago y en hueso. En el callo fibroso entre los extremos fracturarios, formado a partir del coágulo organizado, existen diferentes zonas. En unas, los fibroblastos se transforman en osteoblastos y, a partir de éstos se forma directamente hueso. En otras, surgen islotes de células cartilaginosas por metaplasia de las células del tejido de granulación que siguen el modelo endocondral y, en otros, permanece tejido fibroso que forma trabéculas óseas (Fig. 1).
Figura 1. Reparación secundaria de una fractura. A: Invasión vascular (v) de una zona de cartílago (c) y osificación encondral (o) (Tricrómico de Masson, ×40). B: Banda de cartílago (c) con dos frentes de osificación encondral (o) (SafraninaO, x100).
Por último, durante la fase de remodelación tiene lugar una reabsorción osteoclástica que sustituye el hueso trabecular por hueso haversiano, más denso y compacto. La estructura se adapta a la función, reforzando unas partes y reabsorbiendo otras, orientando las trabéculas en un sentido funcional según las líneas de fuerza y tracción. En trabajos experimentales sobre ratas1 y perros,18 el contenido de calcio en el espacio interfragmentario de la fractura aumenta con el tiempo y a las doce semanas alcanza los valores normales del hueso cortical. También se produce en el callo de fractura un aumento de la rigidez a la indentación por la maduración de los cristales de hidroxiapatita.12
Estabilidad de una fractura. Sistemas de fijación
La relación entre la biología y la mecánica se pone de manifiesto en la respuesta que constituye la curación de las fracturas con diferentes sistemas de tratamiento. El vendaje de yeso se caracteriza por la formación de un callo externo perióstico, abundante, y otro interno endóstico. La osteosíntesis rígida a compresión, con una placa, inhibe la formación del callo perióstico mientras que el clavo intramedular, por el contrario, impide la formación de hueso endóstico y desarrolla un importante callo perióstico.
Las microdeformaciones del espacio interfragmentario aumentan el exudado de sustancias que junto con las células y la formación de nuevos vasos producen un callo exuberante. Grundnes y Reikeras,9 comparando la evolución de osteotomías en ratas, en carga y en descarga, llegaron a la conclusión en 1991 de que la carga estimula la reparación ósea. Molster y cols.15 en 1982, también encontraron una mayor resistencia en el hueso tratado con clavos intramedulares flexibles en los que se ha permitido la carga. El aumento de la carga en un miembro produce una función fisiológica de los músculos y de las articulaciones, con una mejor circulación sanguínea local y rápida normalización del metabolismo óseo.25,30
También se han demostrado interacciones específicas entre los sistemas inmune, hematopoyético y músculo-esquelético después de una fractura. La producción de interleuquina-1, que es un factor estimulante de colonias granulocito-macrófago y de interleuquina-6, encontrada en el callo sugiere que las citoquinas pueden tener un papel importante en el proceso de la reparación esquelética.7
Mecánica de la reparación ósea con el clavo intramedular
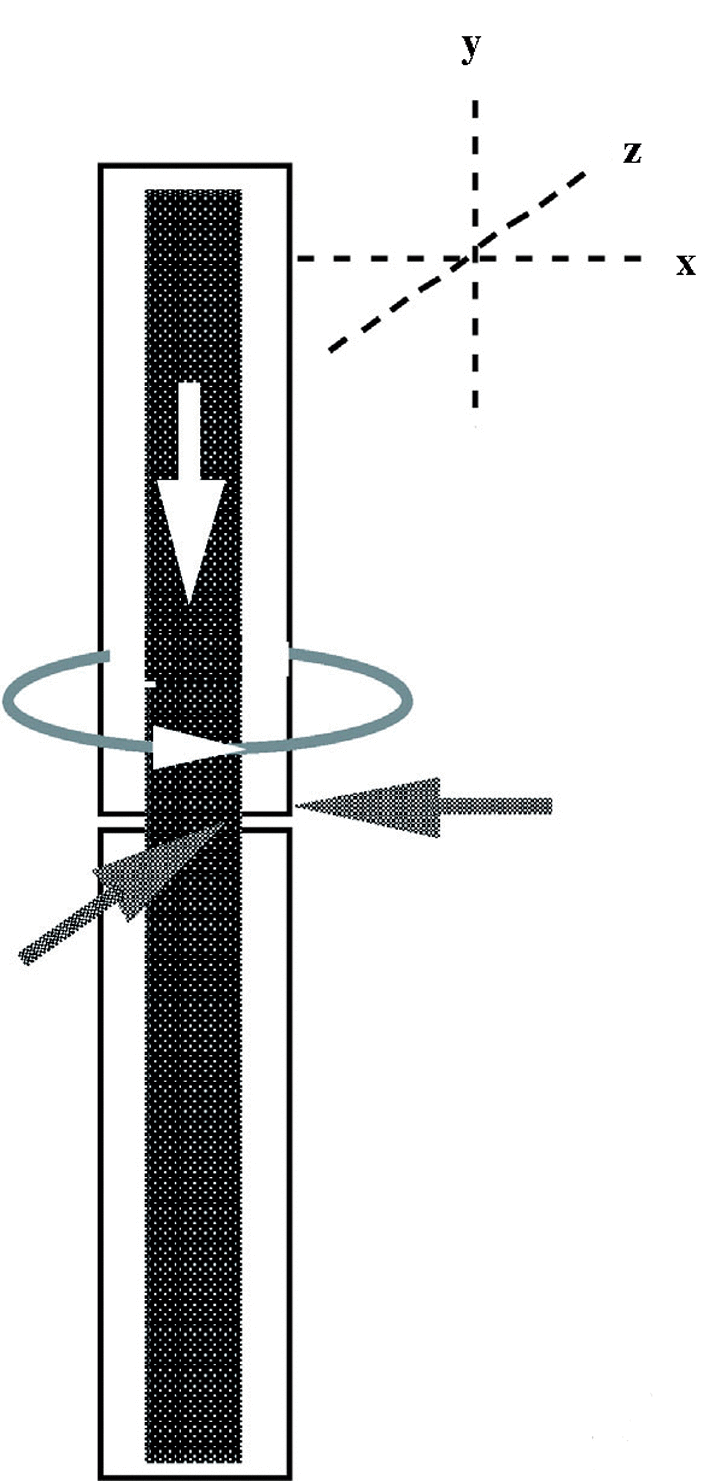
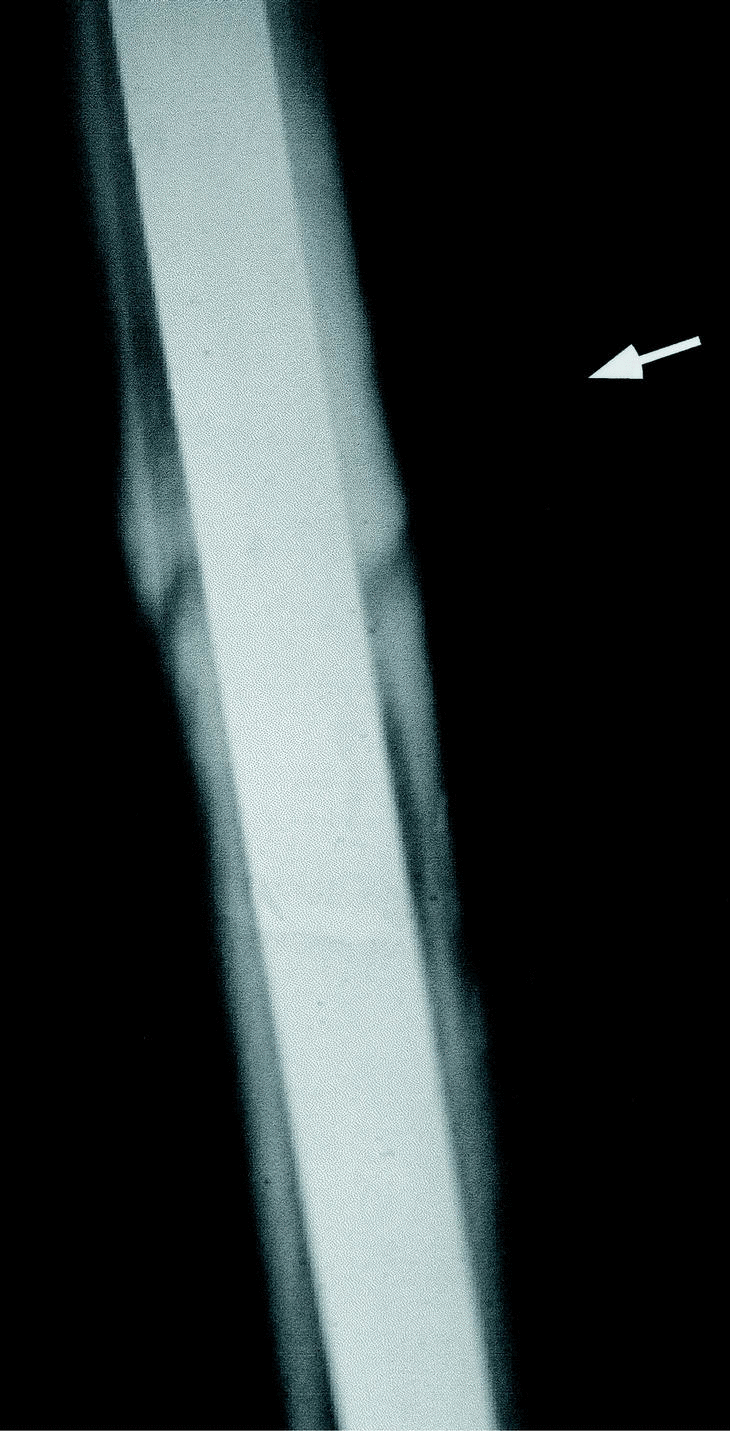
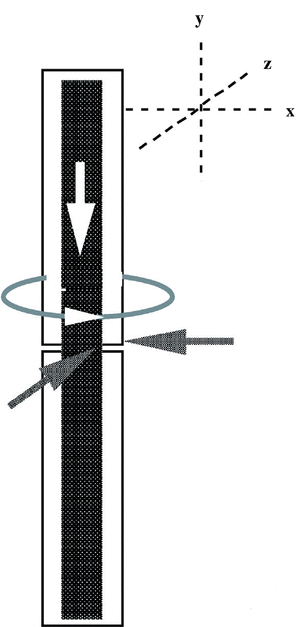
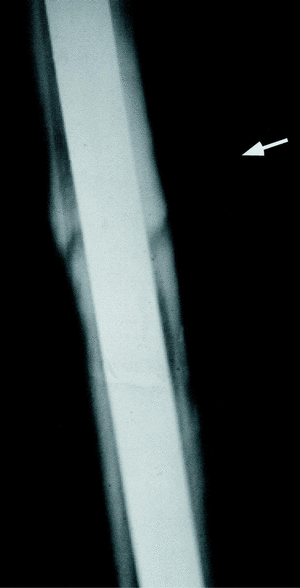
En los extremos óseos del foco de fractura se pueden presentar cuatro tipos de solicitaciones, una carga axial, dos momentos flectores (antero-posterior y lateral) y otra carga de torsión. Frente a cada una de estas solicitaciones debe oponerse una rigidez (axial, antero-posterior, lateral y torsional) (Fig. 2). Es necesario establecer un compromiso entre la estabilidad y la elasticidad para fijar los fragmentos óseos y prevenir los desplazamientos que desarrollan deformaciones. La reparación ósea con clavo intramedular produce un callo, fundamentalmente perióstico, abundante en muchas ocasiones y que, por la flexión del clavo, puede ser más exuberante en una porción que en otra (Fig. 3).
Figura 2. En el foco de fractura se pueden presentar cuatro tipos de solicitaciones, axial, medio-lateral, antero-posterior y de torsión.
Figura 3. En el clavo intramedular el callo perióstico es más abundante radiológicamente en la zona sometida a compresión que en la zona sometida a tensión.
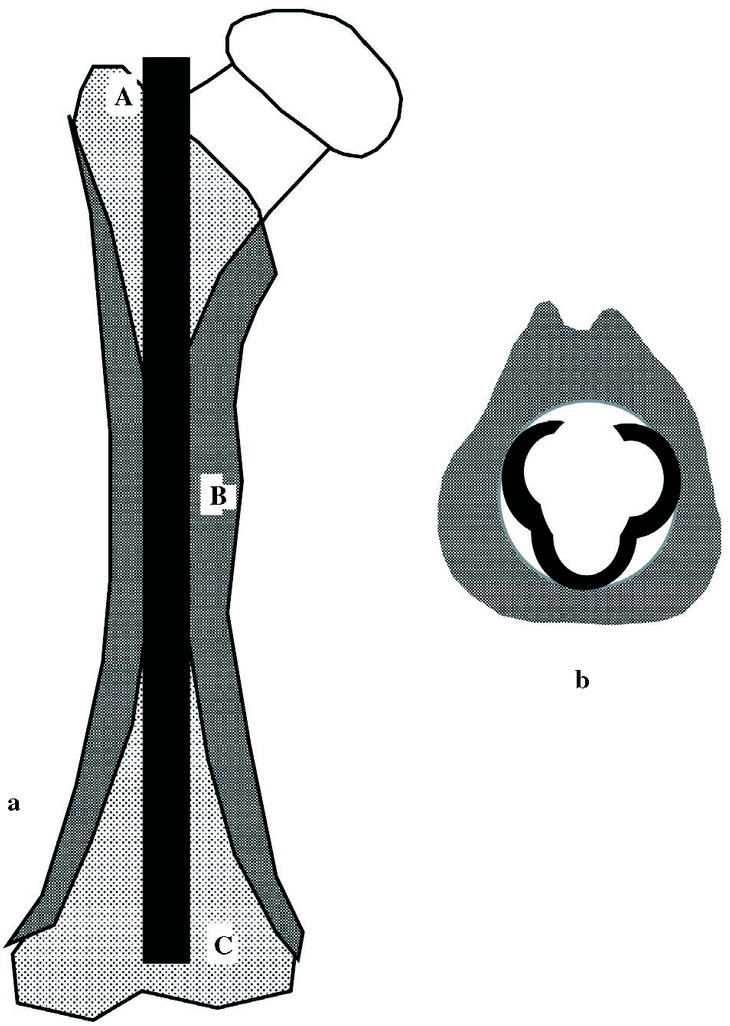
Küntscher ideó el clavo intramedular para estabilizar el clavo al hueso por medio de una compresión radial, aunque en realidad los clavos intramedulares son estables por su contacto con el hueso en tres puntos (Fig. 4), ya que el clavo de Küntscher no es un simple enclavijamiento, una varilla que mantiene unidos dos fragmentos entre sí, el clavo de Küntscher comprime el material que lo rodea, produciendo una unión elástica entre el clavo y el hueso. Por eso diseñó un clavo con una sección abierta en hoja de trébol que permite introducir clavos de mayor diámetro que el canal óseo, facilitando su introducción al comprimirlo y que permite su expansión para adaptarse al tamaño de la cavidad medular. La ranura del clavo reduce su rigidez y permite su torsión a medida que se inserta en el hueso.
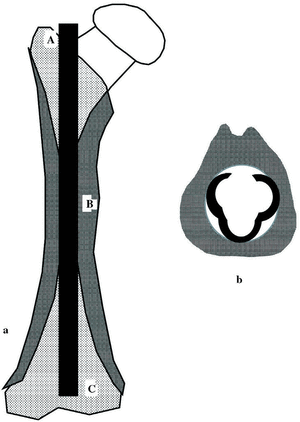
Figura 4. El clavo intramedular de Küntscher se basa a) en el apoyo en tres puntos del hueso: A. punto de entrada, B. zona medular de contacto y C: hueso esponjoso de la extremidad distal, b) sección en trébol de tres hojas.
El clavo intramedular actúa como una férula y mantiene tres puntos de contacto con el hueso, el punto de entrada, el segmento más estrecho del canal medular y el hueso esponjoso epifisario del extremo opuesto, lo que permite solicitaciones axiales que ponen en contacto un fragmento con otro y previene la angulación, la traslación y, en menor medida, la rotación de los fragmentos entre sí.
Sin embargo, la idea inicial de Küntscher se ha ido modificando para aumentar las indicaciones y conseguir una mayor garantía de los tratamientos. En los inicios se presentaron problemas mecánicos importantes, como son el escaso control del clavo sobre las solicitaciones a torsión, el acortamiento en las fracturas con inestabilidad axial y, el que los clavos con diámetros grandes podían causar una conminución adicional de la fractura.
La mayoría de los clavos endomedulares se fabrican de acero inoxidable o con aleaciones de titanio cuyo módulo de elasticidad son, aproximadamente, la mitad del módulo de acero inoxidable.
Reparación ósea con el clavo intramedular
Un clavo intramedular plantea la interferencia de la circulación intramedular y aunque la llegada de los vasos es fundamental en la reparación de las fracturas, los dos sistemas de riego óseo, perióstico y endóstico, se compensan y el daño que se produce al fresar el canal medular se repara con el tiempo sin mayores consecuencias para el hueso.22,23,27
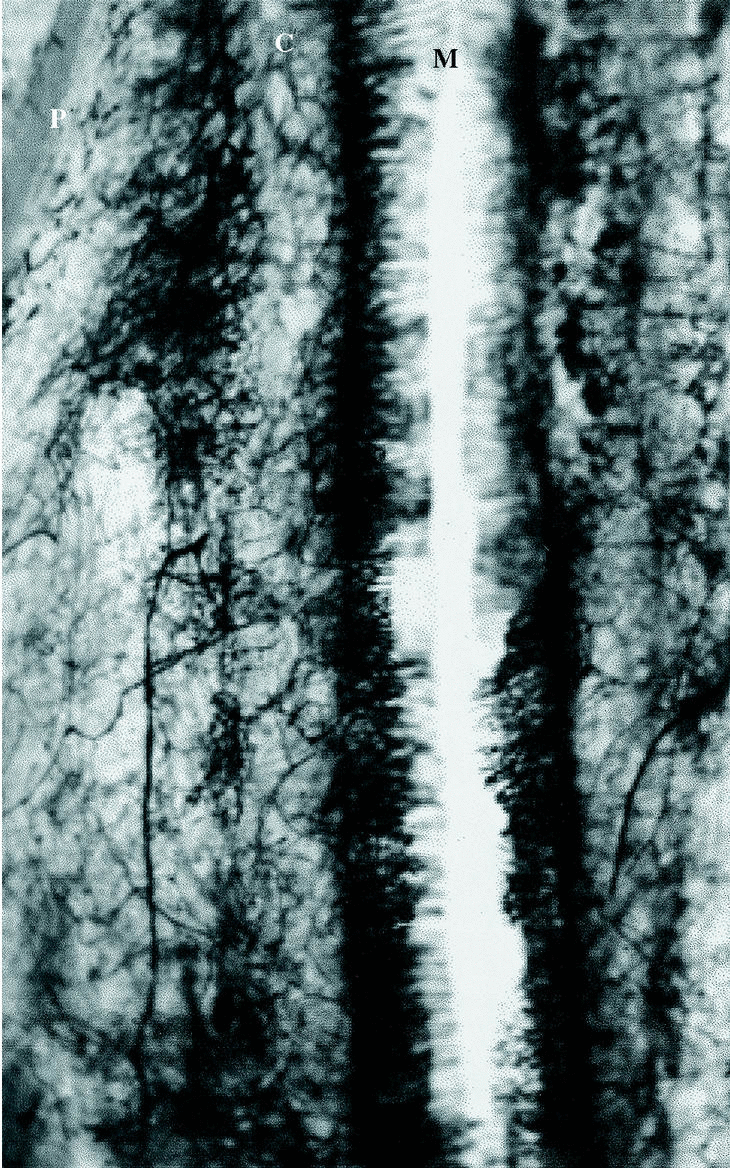
La vascularización de la cortical es un equilibrio entre el aporte externo y el interno, cuando falla uno de ellos es reemplazado por el otro y cuando hay alteraciones en una zona ésta recibe sangre desde puntos más proximales y distales. En una sección transversal de la porción diafisaria de un hueso largo, se considera que los dos tercios internos de la cortical están irrigados por vasos endósticos y el tercio externo restante por vasos procedentes de las partes blandas (Fig. 5). El fresado y el enclavado endomedular tienen efectos claros sobre el flujo vascular, si bien hay que señalar que después de muchos años de experiencia clínica, no se han observado alteraciones en la consolidación de las fracturas.10
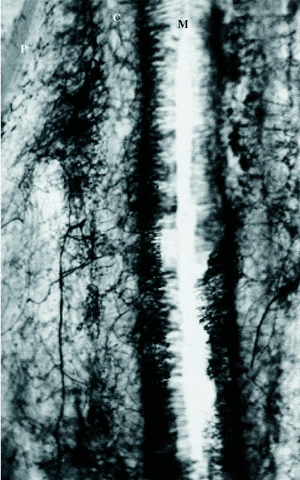
Figura 5. Vasos medulares durante la reparación de una fractura experimental, en cordero, con clavo intramedular sin fresar (P: periostio; C: cortical; M: cavidad medular) (Técnica de Spalteholz, ×6).
El fresado simplifica la técnica quirúrgica pues crea un canal medular a medida del clavo produciendo una mayor superficie de contacto entre él y el hueso y permite introducir clavos de mayor diámetro con menor riesgo de fracturar el hueso. En el caso de fracturas complejas o conminutas puede estar contraindicado siendo, en este caso, necesarios clavos de menor diámetro. Tampoco es aconsejable el fresado en el caso de fracturas abiertas.
El fresado de un canal medular produce una reacción hiperémica apreciable entre las dos y las cuatro semanas en animales de experimentación.18 Braten y cols.,3 en 1993, analizaron, con TAC, fracturas de la diáfisis femoral consolidadas y después de retirado el clavo endomedular, en 10 pacientes estudiados entre uno y cuatro años después de la fractura. Todos ellos mostraron una reducción de la densidad cortical en la zona media de la fractura que se vio compensada por un aumento de su espesor. El fresado puede tener, además de su acción sobre la circulación medular, efectos colaterales de mayor importancia como la necrosis ósea, por exceso de calor, y la embolia grasa, al aumentar la presión del canal medular y sin olvidar que la merma del grosor de la cortical femoral con el fresado disminuye las propiedades mecánicas del hueso. Temperaturas superiores a los 44 °C tienen un efecto negativo sobre la reparación ósea y superiores a 47 °C producen necrosis ósea.
El fresado del canal medular y la introducción del clavo pueden provocar una embolia de grasa y de otros elementos medulares óseos a la circulación general por los numerosos vasos que llegan al hueso.11,14,28,32 Este efecto se puede reducir utilizando un taladro o fresa del conducto proximal, un orificio de salida en el extremo distal, fresas cónicas y efectuando un fresado suave. La fresa actúa como un pistón en una camisa llena de sangre, grasa, coágulos y desechos óseos. Para evitar la embolia grasa se recomienda retirar el contenido de la cavidad medular antes de comenzar a fresar. Una presión excesiva introduce el contenido de la cavidad medular en los vasos corticales llegando al sistema venoso. Intentar preservar la circulación medular y evitar la movilización de la grasa medular ha impulsado al diseño de clavos que no precisan de fresado.
El diseño de los clavos intramedulares
También se utilizan clavos de pequeño diámetro introducidos en una cavidad medular sin fresar. Su principio se basa en que cada aguja tiene tres o cuatro puntos de contacto con el hueso. Los clavos de Ender y de Rush son los más conocidos aunque para la extremidad superior también se han utilizado las agujas de Kirschner. Este método tiene la ventaja de que se pueden introducir varios clavos sin necesidad de una guía, se adaptan muy bien en los huesos osteoporóticos, se pueden introducir un número de clavos suficiente para rellenar el canal medular y el abordaje quirúrgico es mínimo. Aunque Küntscher trabajó sobre distintos tipos de clavo, se han buscado innovaciones y diseños que mejoren sus condiciones mecánicas, que amplíen las indicaciones y faciliten su colocación y retirada. Para ello se han variado y se encuentran en el mercado clavos de diferentes materiales, secciones, diámetros, longitudes, extremos y curvas que requieren del fresado previo o pueden ser introducidos directamente.
Las características geométricas de un clavo son la longitud, la curvatura anterior, el diámetro transverso y la sección transversal. Los clavos intramedulares han presentado los más variados diseños, desde el clavo cilíndrico macizo pasando por diferentes formas como el clavo en hoja de trébol, cilíndrico hueco, rectangular, en forma de cruz, en «V», en diamante o rómbico, etc. La forma, la longitud y la superficie de su sección determinan su rigidez a torsión y a flexión. Un clavo circular tendrá un área y un momento polar de inercia proporcional a su diámetro mientras que en un clavo de sección rectangular será proporcional a la longitud de su lado. El momento de inercia de los clavos endomedulares aumenta según la cuarta potencia de su diámetro.29
El diámetro de un clavo intramedular es el factor más importante para determinar su rigidez. Un clavo intramedular de 16 mm es 1,5 veces más rígido a la flexión que un clavo de 14 mm y 2,5 veces más que otro de 12 mm. Un clavo de Küntscher de 12 mm de diámetro y una pared de 2 mm de grosor tiene una rigidez a flexión semejante a la del fémur intacto.29
Los clavos intramedulares son curvos para simplificar su colocación y presentar una mayor superficie de contacto con el hueso, adaptándose a la curva del canal medular de los huesos largos. Sin embargo, como el radio de curvatura no es el mismo en toda la longitud del hueso, se requiere, en ocasiones, un gran esfuerzo para introducirlo. Un punto de entrada falso o mal calculado puede transformar una fractura transversal en una fractura conminuta. Este hecho es muy evidente en el clavo intramedular para la tibia que precisa de una angulación para facilitar la penetración del clavo.
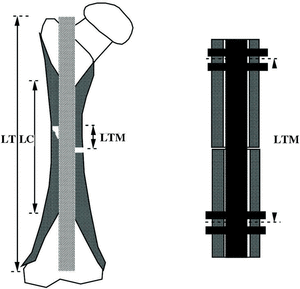
La longitud de un clavo intramedular se puede ver desde tres puntos de vista, la longitud total del clavo; la longitud de la interfaz o zona de contacto entre el clavo y el hueso y la zona de discontinuidad o longitud de trabajo (Fig. 6). La longitud total del clavo depende del tamaño anatómico del hueso. Un clavo muy largo protruye, causa dolor y limitación funcional. Por el contrario, un clavo muy corto compromete la estabilidad de la fractura. La longitud de interfaz entre el hueso y el clavo refleja la superficie de contacto entre ambos y cuanto mayor sea, mayor será la rigidez del montaje.
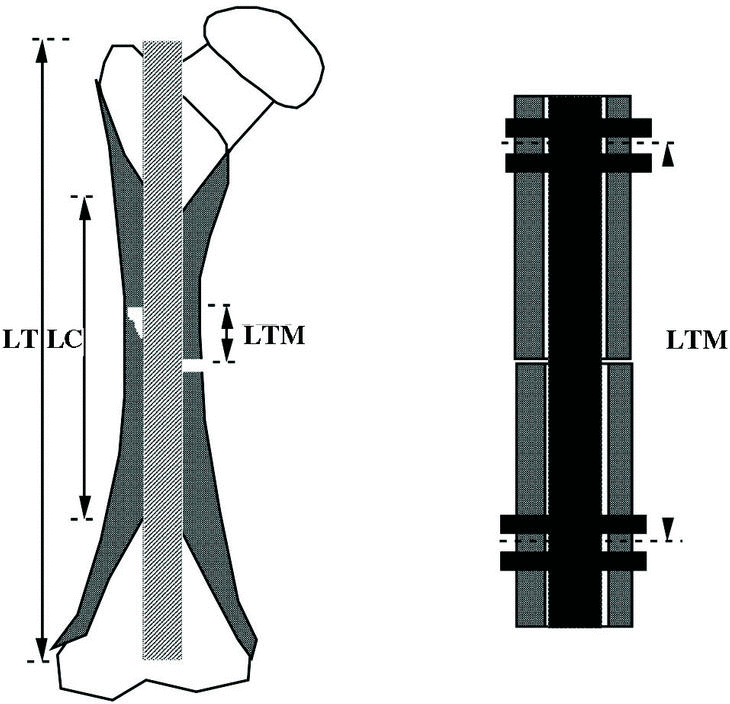
Figura 6. Longitudes del clavo intramedular. LT: longitud total; LC: longitud de contacto o interfaz; LTM: longitud de trabajo mecánico.
La longitud de trabajo mecánico del clavo es la longitud desde el punto más distal en el fragmento proximal hasta el punto más proximal en el fragmento distal a ambos lados de la fractura o la distancia entre los dos puntos, uno en cada fragmento, donde el hueso se adapta perfectamente al clavo, es decir, la porción del clavo que debe soportar la transmisión de fuerzas que no pasan por el hueso. Por otro lado, la rigidez a flexión de un clavo es inversamente proporcional al cuadrado de su longitud de trabajo mientras que la rigidez a torsión es inversamente proporcional a su longitud de trabajo y cuanto menor sea la longitud de trabajo mayor será la rigidez del montaje. Este parámetro se puede ver afectado por diferentes situaciones. Un clavo tiene una longitud de trabajo a flexión menor cuando fija una fractura transversa que cuando lo hace con una fractura conminuta. Técnicamente se puede modificar la longitud de trabajo fresando y, también, encerrojando el clavo. El fresado, modifica la morfología del canal intramedular adaptándolo mejor al clavo y reduciendo, por tanto, la longitud de trabajo. El encerrojado, por su parte, también modifica la longitud de trabajo a torsión fijando el clavo al hueso por medio de los tornillos en puntos determinados y la estabilidad a torsión será proporcional a la distancia que hay entre los tornillos (Fig. 6).
El clavo encerrojado
Actualmente han tenido gran predicamento los clavos encerrojados. Los sistemas más conocidos y utilizados son los de Grosse-Kempf; AO; Klemm; Russell-Taylor y FD.
La colocación de tornillos perpendiculares al clavo intramedular lo encerroja evitando el desplazamiento del clavo en el canal medular y estabilizando los fragmentos entre sí. Es una técnica que a pesar de sus inconvenientes (mayor radiación, dificultad de encontrar el punto de entrada de los tornillos, mayor tiempo de cirugía), ha mejorado con el tiempo hasta populizarse, aumentando el número de indicaciones del enclavado intramedular.
El encerrojado estático, tornillos proximales y distales, evita los acortamientos y la protusión del clavo, y mejora la resistencia a la torsión. La colocación de tornillos en ambos extremos del clavo estabiliza un fragmento sobre el otro previniendo el deslizamiento del clavo. Está indicado en fracturas conminutas, fracturas segmentarias, oblicuas largas o espiroideas o para estabilizar una fractura con pérdida ósea o en el caso de una pseudoartrosis. Para conseguir un buen contacto entre los fragmentos se introdujo el encerrojado dinámico, colocando tornillos en uno solo de los fragmentos o retirándolos durante la consolidación de la fractura.
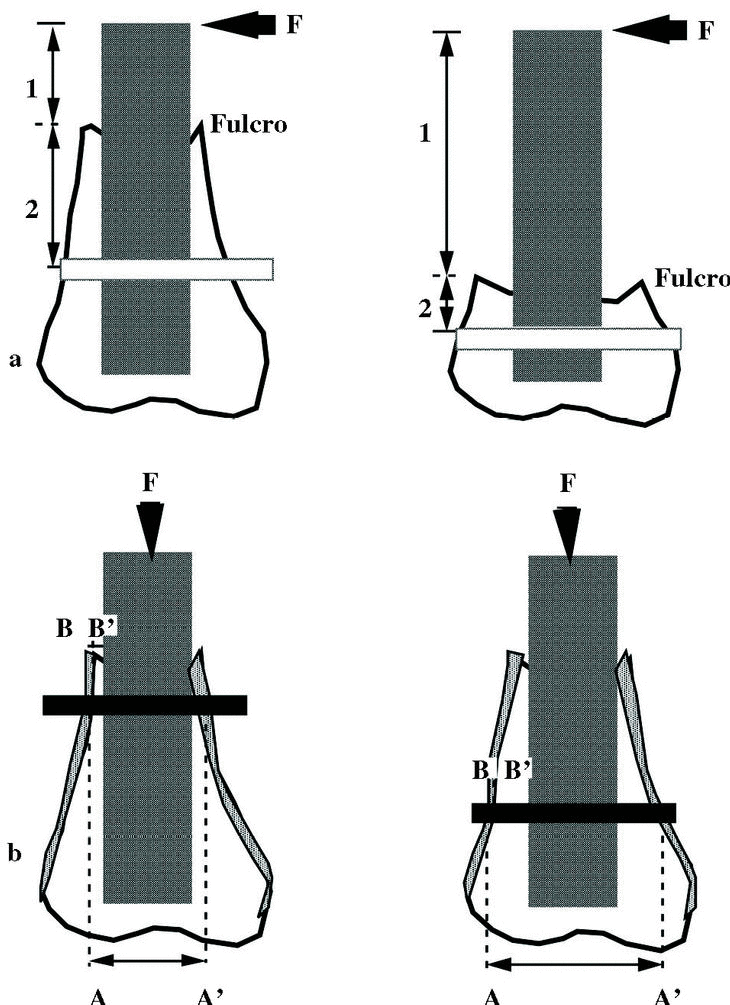
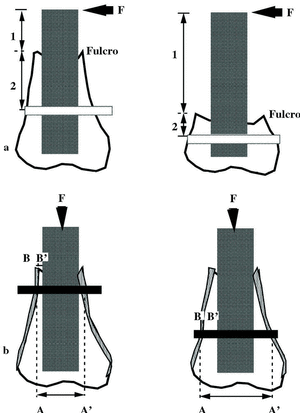
Los orificios para la entrada de los tornillos son puntos de menor resistencia y de concentración de tensiones. Las solicitaciones sobre un clavo encerrojado aumentan cuando la fractura está localizada distalmente pues el clavo es cargado como una palanca. Cuando el trazo de una fractura está a cinco centímetros del más proximal de los tornillos distales, el pico de solicitaciones alrededor del orificio puede producir una rotura por fatiga. Se deben utilizar dos tornillos distales cuando el fragmento distal sea menor que un 60% de la distancia entre el punto medio de la diáfisis femoral y la línea articular29 (Fig. 7). Durante la marcha y el apoyo de la extremidad, los tornillos distales solicitan a la flexión en cuatro puntos, apoyándose sobre la cortical del hueso y es mayor al aumentar el diámetro del hueso o cuanto mayor es la diferencia entre el diámetro medular del hueso y el diámetro del clavo (Fig. 7).
Figura 7. Fractura distal de un hueso largo tratadas con clavo encerrojado, a) cuanto más distal es una fractura mayor es el brazo de potencia (1) frente al brazo de resistencia (2) ante una fuerza lateral; b) ante solicitaciones axiales, los tornillos distales solicitan a flexión en cuatro puntos. Siendo mayor el riesgo de fatiga al aumentar el diámetro del hueso (A-A') o la diferencia entre el diámetro de la cavidad medular y el diámetro del clavo (B-B').
El enclavado encerrojado produce un puente de tensiones desde los clavos proximales a los distales, saltando el foco de fractura y una gran parte del hueso sano. Este tipo de fijación, en el caso de fracturas muy conminutas o con defectos óseos segmentarios, no permite un apoyo inmediato ante el peligro de rotura del material, por lo que hay que esperar a la visualización de hueso en las radiografías para recomendar la carga.