Desde la comercialización de fármacos que actúan sobre el remodelado óseo se han registrado numerosos casos de osteonecrosis de los maxilares (ONM), pero hasta hace poco solo se habían descrito casos de ONM asociados a la administración de bifosfonatos. Con la introducción de nuevos agentes antirresortivos han aparecido varios casos de ONM asociados a denosumab. Presentamos el caso de una paciente de 84 años con osteoporosis, que presentó osteonecrosis mandibular tras la colocación de 6 implantes 5 meses después de la administración de denosumab. Una ortopantomografía y una TC mostraron pérdida ósea de la cresta mandibular y exposición ósea periimplantar. Tras el tratamiento conservador con antibióticos y la suspensión de denosumab, se inició el tratamiento con teriparatida reduciéndose la infección del hueso necrótico y se observó nueva remodelación ósea. La patogénesis de la ONM por denosumab no está claramente definida, pero parece que la tasa del éxito de curación es superior a la ONM por bifosfonatos.
Since the introduction of drugs acting on bone remodeling, numerous cases of drug-induced osteonecrosis of the jaw (ONJ) have been reported. Until recently these cases were exclusively associated with the administration of bisphosphonates. With the introduction of new antiresorptive agents such as denosumab, several cases of ONJ associated with its treatment have been recently reported. The case is presented of an 84 year-old osteoporotic female patient who developed mandibular osteochemonecrosis after the placement of 6 implants five months after the administration of denosumab. A panoramic radiograph and CT, showed mandibular crestal bone loss and peri-implant exposure. Conservative treatment with antibiotics and discontinuing denosumab, and starting treatment with teriparatide, decreased the necrotic bone infection and new bone remodeling could be observed. The pathogenesis of denosumab-induced ONJ is not clearly defined, but it seems that the success rate in healing after drug discontinuation is higher than in bisphosphonates-induced ONJ.
Denosumab es un anticuerpo monoclonal IgG2 humano (no quimérico), que se une con gran afinidad y especificidad al ligando del receptor activador del factor nuclear kappa-B (RANKL), impidiendo la activación de su receptor RANK en la superficie de los precursores de los osteoclastos y en los osteoclastos. Al impedir la interacción RANKL/RANK, se inhibe la formación, la función y la supervivencia de los osteoclastos, lo que a su vez provoca una disminución de la resorción ósea1.
Denosumab está indicado para el tratamiento de la osteoporosis en mujeres posmenopáusicas, para reducir la pérdida de masa ósea como consecuencia de un tratamiento de cáncer de mama, y para prevenir la pérdida ósea asociada con la supresión hormonal en varones con cáncer de próstata. Los efectos adversos a medio y largo plazo de este antirresortivo son desconocidos y están siendo estudiados2.
El propósito de este trabajo es presentar un caso de osteonecrosis de mandíbula después de la colocación de implantes dentales en una paciente osteoporótica que estaba en tratamiento con denosumab y poner en alerta sobre los efectos secundarios sobre los maxilares de la terapia con denosumab a la vez que informar del beneficio del tratameinto con teriparatida como adyuvante en la ONM.
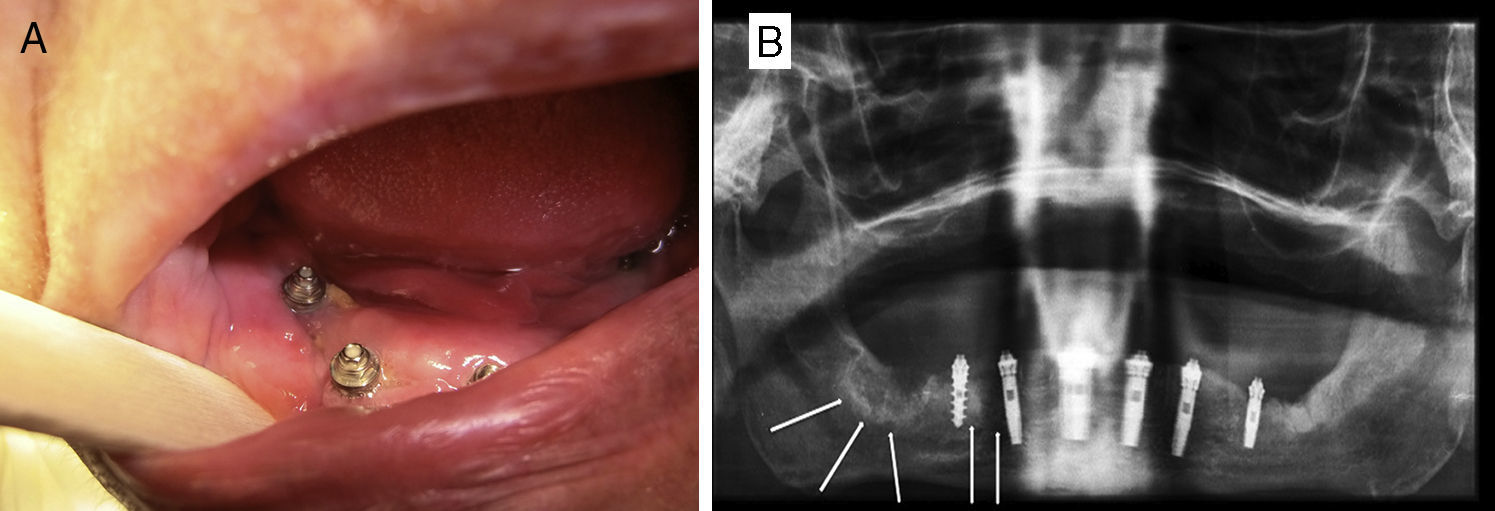
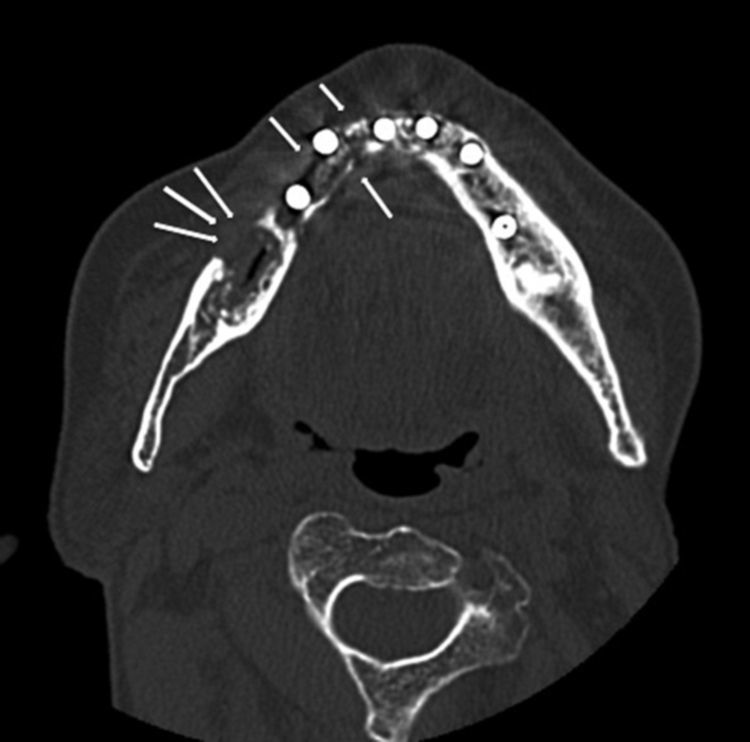
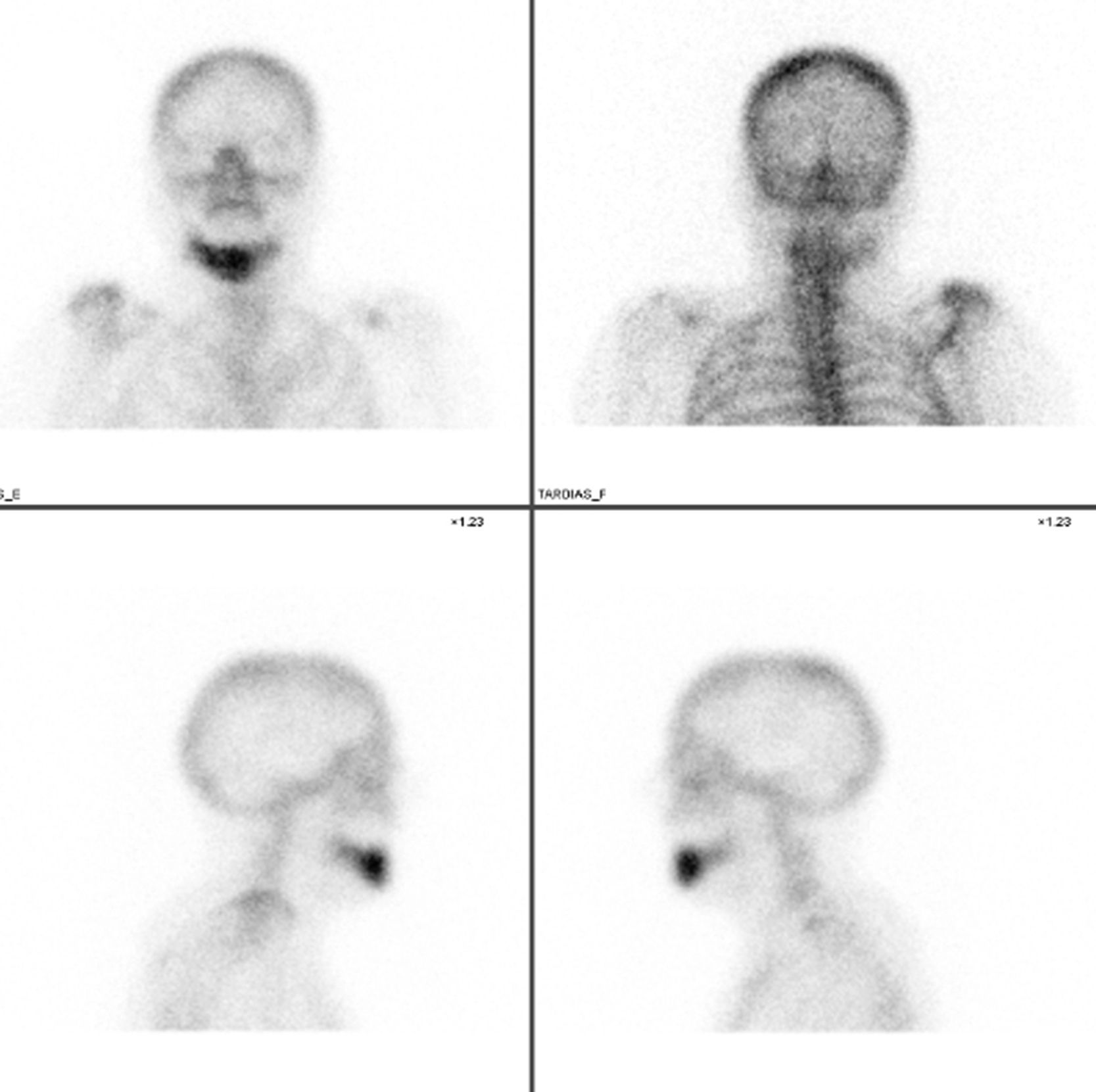
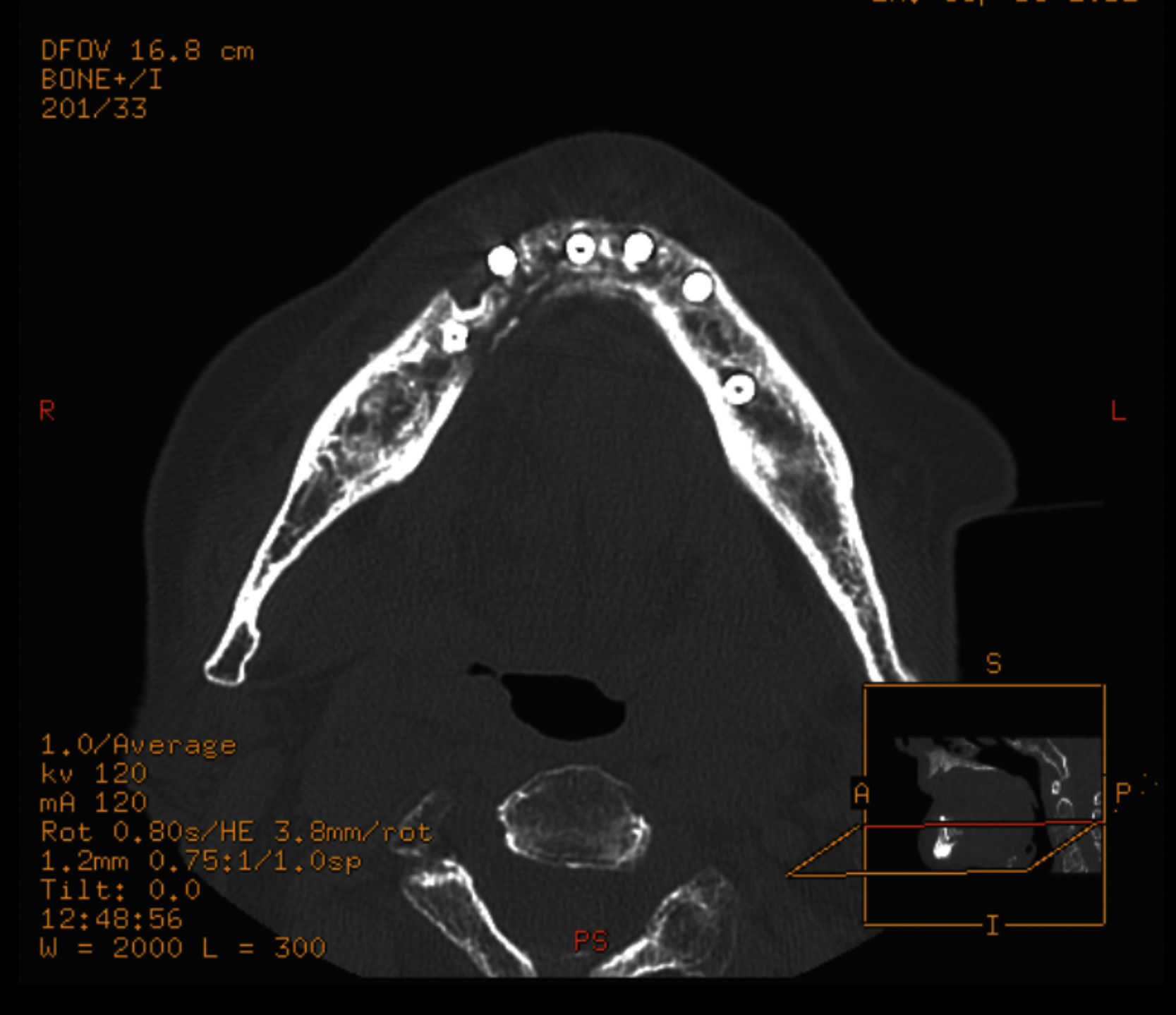
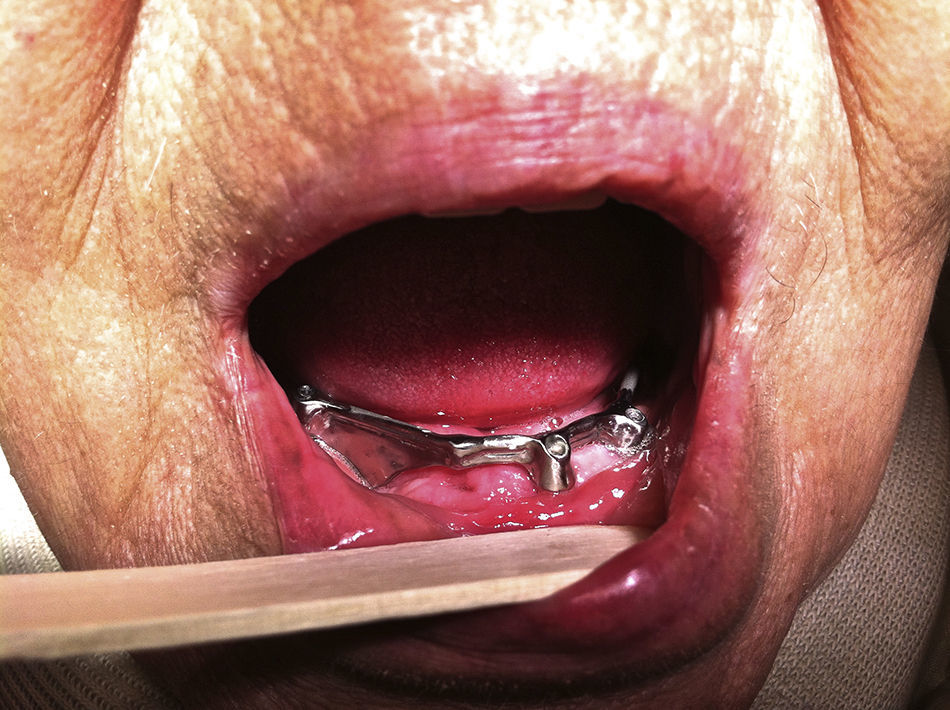
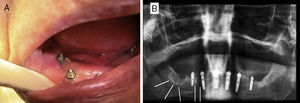
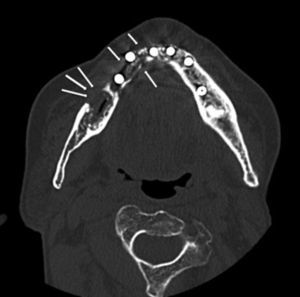
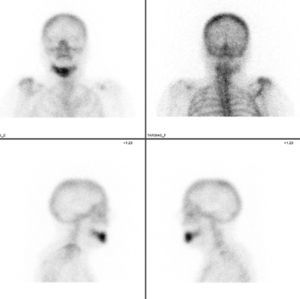
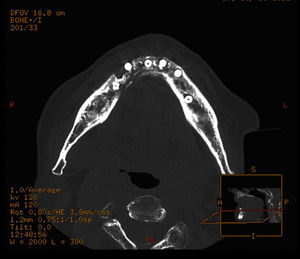
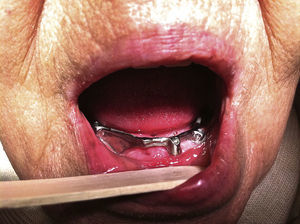
Caso clínicoMujer de 84 años, que nos fue remitida al servicio de cirugía oral y maxilofacial por su dentista al presentar exposición de hueso crestal mandibular y supuración periimplantar 3 semanas después de la colocación de 6 implantes dentales con carga inmediata. Como antecedentes personales de la paciente solo destaca la presencia de hipertensión y osteoporosis. No tomó ningún medicamento con regularidad y la paciente nunca fue tratada con bifosfonatos. Cinco meses antes de la cirugía de colocación de implantes, la paciente comenzó tratamiento antirresortivo con denosumab 60mg por vía subcutánea para tratar la osteoporosis. Solo se administró una sola dosis de 60mg de denosumab. El examen físico mostró dolor a la palpación del reborde alveolar mandibular a nivel de las zonas de exposición ósea que correspondían con las extracciones dentales previas a la cirugía de los dientes 48 y 47 (fig. 1A). Una ortopantomografía puso de manifiesto la presencia de varias zonas osteolíticas a nivel del cuerpo mandibular derecho y alrededor de los implantes (fig. 1B). En una TC mandibular para determinar la extensión de las lesiones se observó una destrucción de 1,7cm de longitud de la cortical vestibular del cuerpo mandibular derecho, espacios trabeculares dilatados e irregulares con áreas hipodensas compatibles con osteonecrosis a nivel de los implantes y de los alveolos de los dientes extraídos (fig. 2). Una gammagrafía ósea objetivó una infección severa a nivel mandibular (fig. 3). Se inició tratamiento conservador con antibióticos según protocolo de nuestro servicio (amoxicilina-clavulánico vía oral 875/125mg, 3 veces/día durante 15 días asociados con enjuagues de clorhexidina al 0,12%, 2-3 veces/día) y se interrumpió el tratamiento con denosumab. A las 2 semanas de iniciar el tratamiento, la paciente presentó mejoría del dolor, con desaparición de la supuración y mejoría de la periimplantitis. Se inició entonces el tratamiento a dosis bajas con teriparatida 20μg subcutánea en inyección diaria durante 6 meses. Pasado este tiempo, se suspendió en ese momento el tratamiento con teriparatida, ya que los focos de exposición ósea fueron cubiertos por mucosa oral sana, observándose en una TC de control una recuperación de la densidad ósea a nivel de las zonas osteolíticas con cierto grado de esclerosis (fig. 4). En la actualidad, 8 meses después de la finalización del tratamiento con teriparida, la paciente se encuentra asintomática, habiéndose realizado la rehabilitación protésica sobre los implantes viables 6 meses de la remisión completa de las lesiones (fig. 5).
En los últimos años muchos estudios y revisiones han sido publicadas sobre la acción de los bifosfonatos sobre los maxilares como agentes causantes de osteoquimionecrosis. Desde la comercialización de denosumab varios artículos publicados han advertido de la existencia de osteonecrosis de los maxilares (ONM) en pacientes tratados con este antirresortivo. En 3 ensayos clínicos denosumab (n=52) demostró un mayor riesgo de desarrollar osteonecrosis mandibular en comparación con ácido zoledrónico (ZA) (n=37) con una relación de 1,4:1 (p>0,05) (tabla 1)3, siendo la mandíbula en ambos casos, la localización más frecuente de aparición de ONM.
Casos de ONM de 3 ensayos clínicos inducidos por ácido zoledrónico y denosumab. Comparativa de los episodio asociados y de la localización de la ONM
| ONM | Zoledrónico (n=37) | Denosumab (n=52) | Total (N=89) |
|---|---|---|---|
| Episodio oral asociado*: | |||
| Extracción dental | 24 (64,9) | 31 (59,6) | 55 (61,8) |
| Coincidiendo con infección oral | 17 (45,9) | 26 (50,0) | 43 (48,3) |
| Dolor maxilar-mandíbula | 25 (67,9) | 48 (93,2) | 73 (82,0) |
| Localización de la ONM: | |||
| Mandíbula | 31 (83,8) | 34 (65,4) | 65 (73,0) |
| Maxilar | 5 (13,5) | 15 (28,8) | 20 (22,5) |
| Ambos | 1 (2,7) | 3 (5,8) | 4 (4,5) |
ONM: osteonecrosis de los maxilares.
La patogénesis de la ONM asociada a agentes antirresortivos no está completamente definida, a pesar de que hay muchas publicaciones que tratan de explicar su etiología4.
Haciendo referencia a denosumab se ha establecido la hipótesis de que una inhibición exagerada de la osteoclastogénesis y una disminución rápida del recambio óseo añadido a un daño tisular macrofágico, podrían desencadenar el desarrollo de osteonecrosis5.
La cirugía dentoalveolar, las extracciones dentales, una mala higiene bucal, prótesis dentales entre otros, han sido propuestos como factores de riesgo independientes para la ONM6. Por lo tanto, un adecuado cuidado dental preventivo antes de comenzar el tratamiento con denosumab puede reducir la incidencia de osteonecrosis mandibular en pacientes tratados con este medicamento. Hasta la fecha no hay estudios que indiquen cuánto tiempo se debe esperar antes de realizar procedimientos dentales invasivos tras haber interrumpido el tratamiento con denosumab, y cuánto tiempo después del tratamiento con denosumab, el riesgo de ONM sigue siendo elevado.
Sin embargo, a diferencia de los bifosfonatos, denosumab no se incorpora a la matriz ósea, es por eso que en el caso de la ONM por denosumab las lesiones podrían curar con una tasa de éxito mayor7.
En nuestro caso, la infección y la supuración desaparecieron con el tratamiento antibiótico descrito. Tras suspender la administración de denosumab e iniciar tratamiento con 20μg de teriparatida diarios en inyección subcutánea se observó con solo un mes de tratamiento una mejoría de todos los síntomas y una disminución en la extensión de las lesiones.
Recientemente, se han presentado 7 informes de casos independientes en los que pacientes con ONM por bifosfonatos fueron tratados con teriparatida consiguiéndose la resolución de las lesiones óseas8–14, Subramanian et al.4 recogen cada uno de estos casos en los que la duración del tratamiento con teriparatida hasta obtener la curación de las lesiones osciló entre las 8 semanas en el mejor de los casos hasta los 10 meses. Todos los pacientes fueron tratados con alendronato excepto el caso descrito por Lau y Adachi10 que fue tratado con una combinación de bifosfonatos, y el caso publicado por Iwamoto et al.14 que fue tratado con risendronato.
Actualmente no se han publicado casos de pacientes con ONM por denosumab tratados con teriparatida. Sin embargo, el mecanismo de acción de la teriparatida, que administrada de forma intermitente tiene un efecto anabólico sobre el hueso, podría justificar su uso en estos casos, ya que la teriparatida promueve la expresión del RANKL en preosteoblastos, incrementado la activación y el reclutamiento de osteoclastos mediado por osteoblastos. Estos fenómenos, descritos en el modelo patogénico para la osteonecrosis por bifosfonatos propuesto por Subramanian et al.4 y válido para la osteonecrosis por denosumab, se traducen en un incremento del remodelado óseo contrarrestando el efecto antirresortivo de denosumab.
Es importante destacar que la teriparatida no está indicada en pacientes con hipercalcemia, enfermedad ósea metastásica, enfermedad de Paget del hueso, embarazo, pacientes con enfermedad ósea sometidos a radioterapia, insuficiencia renal y hepática15. También se debe tener en cuenta que la teriparatida no debe administrarse durante más de 24 meses. Esta limitación temporal se debe al informe de un estudio con ratas Fisher tratadas con teriparatida en el que un único espécimen sufrió un osteosarcoma15. Este efecto no se ha observado en otras especies. La duración y dosis óptima de teriparatida para tratar la ONM asociadas a bifosfonatos o a denosumab se desconocen. En nuestro caso fueron suficientes 6 meses de tratamiento con teriparatida 20μg diarios para conseguir la remisión de las lesiones y obtener una recuperación ósea de las lesiones osteolíticas.
ConclusiónLos odontoestomatólogos y los cirujanos orales y maxilofaciales deben ser conscientes de los potenciales efectos adversos en pacientes que han sido tratados con denosumab y que van a someterse a un procedimiento oral invasivo. Un adecuado programa preventivo dental antes de comenzar el tratamiento con denosumab puede reducir la incidencia de ONM, ya que una sola dosis del fármaco puede inducir esta enfermedad.
Los pacientes con ONM por denosumab pueden beneficiarse del tratamiento adyuvante con teriparatida a bajas dosis, ya que contrarrestan los efectos antirresortivos del denosumab favoreciendo el remodelado óseo.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable y de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.