El presente trabajo tiene como objetivo describir el manejo anestésico de 2 pacientes sometidos a cirugía de carina, y cuyo soporte ventilatorio intraoperatorio se consiguió mediante oxigenación a través de membrana extracorporéa, configuración veno-venosa (ECMO V-V). En ambos pacientes, después de la inducción anestésica y mantenimiento inhalatorio durante la neumonectomía y la mediastinoscopia (respectivamente), se canularon las venas yugular y femoral, y tras heparinización se inició la ECMO V-V. Uno de los pacientes presentó una complicación hemorrágica durante la cirugía, que fue tratada mediante vasopresores (noradrenalina) con dosis bajas y transfusión de plaquetas, plasma fresco congelado y concentrados de hematíes. El mantenimiento de la anestesia durante la ECMO V-V se consiguió mediante una infusión controlada por objetivo de propofol. El uso de ECMO V-V es una nueva alternativa para oxigenar en la cirugía traqueal, cuyo uso mejoraría las condiciones quirúrgicas, pero la experiencia actual es limitada. En pacientes seleccionados garantizaría el soporte ventilatorio en la cirugía de carina, pero es esencial la planificación del mantenimiento y las complicaciones asociadas. Se aconseja su realización en centros terciarios con experiencia en su manejo.
The aim of this study is to describe the anaesthesia management of two patients undergoing carinal resection under veno-venous extracorporeal membrane oxygenation (VV ECMO). In both cases, anaesthesia was induced and then maintained with inhalational agents during pneumonectomy and mediastinoscopy (respectively). Then the jugular and femoral veins were cannulated and VV ECMO was started after heparinization. One of the patients presented bleeding during surgery, which was treated with low-dose vasopressors (norepinephrine) and transfusion of platelets, fresh frozen plasma, and red blood cells. During VV ECMO, anaesthesia was maintained with target-controlled infusion of propofol. VV ECMO can be expected to improve surgical conditions in tracheal surgery; however, it is still a novel technique in this context. In selected patients, it would guarantee ventilatory support during carinal resection, but it is essential to carefully plan anaesthesia maintenance and prepare for VV ECMO-related complications. This technique should only be used in tertiary centres with experience in VV ECMO management.
La cirugía de resección traqueal supone un reto para el anestesiólogo. Se han descrito diversas aproximaciones ventilatorias que permiten mantener la oxigenación y facilitar al máximo la técnica quirúrgica. Las más extendidas y usadas serían: a) la ventilación intracampo, en la que el bronquio no operado se canula directamente por el cirujano en el campo quirúrgico, permitiendo la anestesia inhalatoria y protegiendo el bronquio no operado de los restos quirúrgicos1; y b) la ventilación en jet a alta o baja frecuencia, que consiste en la aplicación de un volumen corriente a alta presión a través de un tubo endobronquial de superficie reducida. Una nueva alternativa consistiría en la utilización de sistemas de oxigenación extracorpórea (ECMO veno-venoso [V-V]) que mejoraría las condiciones quirúrgicas, pero cuya experiencia actualmente es reducida2.
Otra alternativa, menor extendida aunque no por ello despreciable, es la utilización de la ventilación controlada por flujo a través del tubo ultrafino Tritube® asociado al respirador Evone®. En cualquier caso, la ventilación intracampo y la ventilación en jet se asocian con una exposición quirúrgica inadecuada de la zona a intervenir, prolongando la duración del tiempo quirúrgico de la operación debido a la necesidad de retirar repetidamente el tubo endotraqueal, con el consiguiente riesgo de daño luminal endobronquial3.
El presente trabajo tiene como objetivo describir el manejo anestésico de 2 pacientes sometidos a cirugía de carina y cuyo soporte ventilatorio intraoperatorio se consiguió mediante ECMO V-V.
Primer casoMujer de 57 años, cuya talla es de 159cm y peso 80kg, diagnosticada de un tumor sarcomatoide en el bronquio principal derecho que se interviene quirúrgicamente de neumonectomía derecha y carinectomía. Como antecedentes relevantes destacan una alergia a los AINE e inhibidores de COX-1, HTA, dislipidemia, polimialgia reumática, bocio uninodular, hernia de hiato y un episodio de angina inestable en 1996 que no precisó intervencionismo cardíaco y sin recurrencia desde entonces. Como tratamiento habitual la paciente tomaba pantoprazol 40mg al día, telmisartán 20mg al día, atorvastatina 20mg al día y alprazolam 0,5mg por la noche. En las pruebas preoperatorias cabe destacar unas pruebas de función respiratoria normales (FEV1: 87%, DLCO: 88%), una gammagrafía de ventilación y perfusión que mostró un 16% de perfusión en el pulmón derecho, una ecocardiografía transtorácica que reflejaba morfología y función ventricular normal y un hemograma, bioquímica y coagulación en rango.
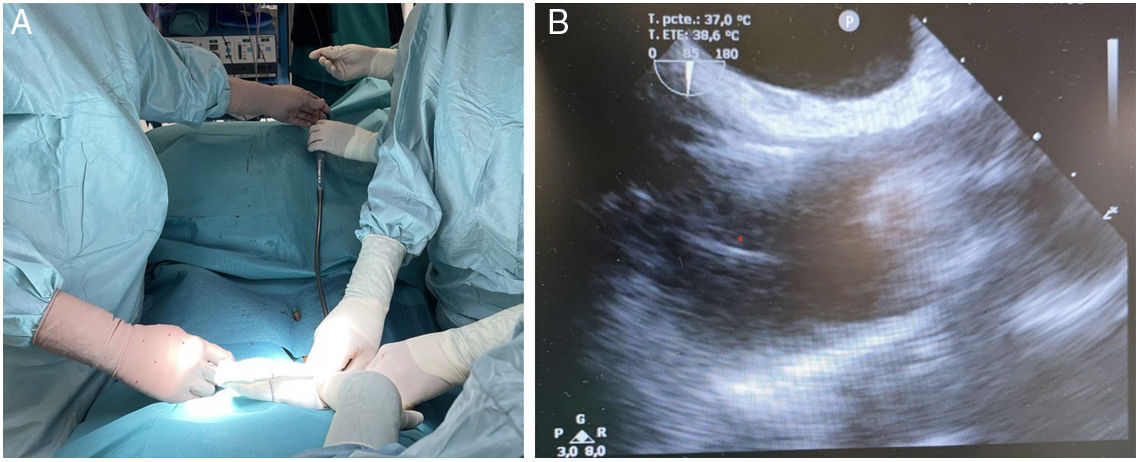
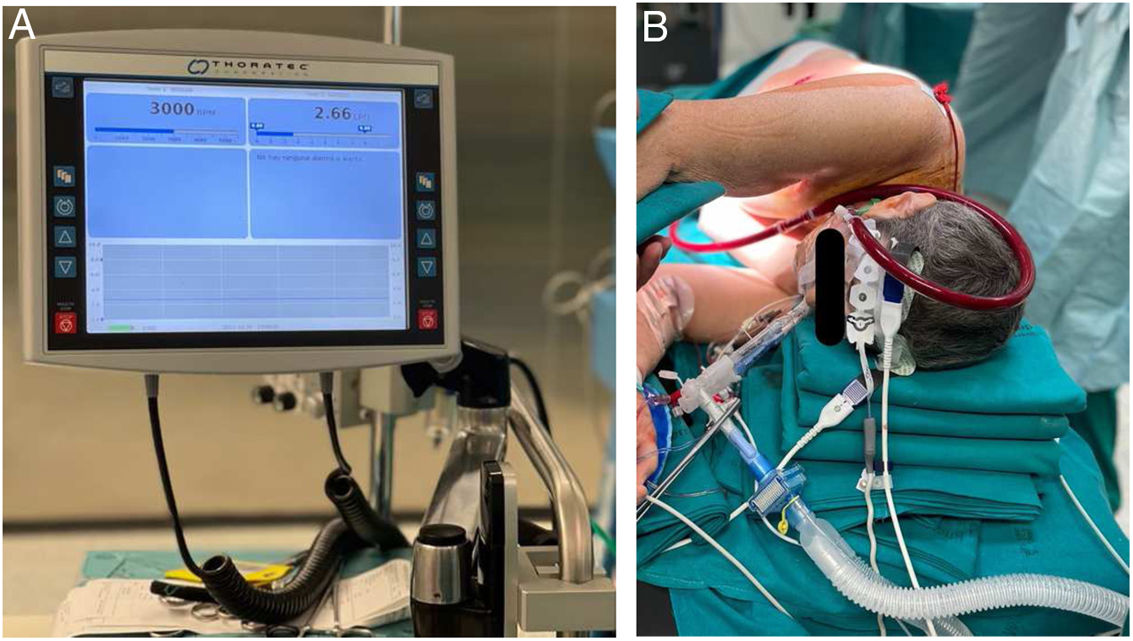
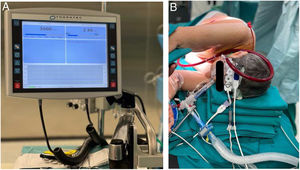
El día de la cirugía, tras recibir una profilaxis antibiótica con cefazolina 2g, y una ansiólisis mediante 2,5mg de midazolam, se monitorizó a la paciente (monitorización estándar junto a la monitorización de presión arterial invasiva, de profundidad anestésica mediante BIS® y de oximetría cerebral mediante el sistema INVOS®) y se procedió a la inducción con de anestesia general (con lidocaína, propofol, fentanilo y rocuronio) e intubación orotraqueal con un tubo de doble luz izquierdo de 37French (Fr) y se comprobó con fibrobroncoscopio. Se canalizó una vía venosa central además de 2 vías periféricas de calibre 18G. El mantenimiento se realizó inicialmente con sevoflurano 2,5% (manteniendo una concentración alveolar mínima superior a 0,8), para mantener un BIS entre 40-60 y un end tidal CO2 (etCO2) en torno a 40mmHg mediante una ventilación mandatoria continua controlada por presión (PC-CMV), con una presión positiva al final de la espiración (PEEP) de 5cm H2O y driving pressure de 12cm H2O, fracción inspirada de oxígeno (FiO2) 0,4 y frecuencia respiratoria (FR): 14rpm. Se canalizó la arteria radial derecha con cánula de 36Fr y se introdujo una vía central de 3 luces (39Fr) en la vena yugular interna izquierda. Se colocó a la paciente en decúbito lateral izquierdo, realizándose un bloqueo paravertebral con levobupivacaína 0,5% 15ml guiado con ecografía con una aguja de 27G (ml). Se procedió a la neumonectomía derecha. Una vez completada la neumonectomía se recolocó a la paciente en supino y se procedió a la canulación de la vena yugular (17Fr) y de la vena femoral (23Fr) derechas (fig. 1A), cuya correcta posición se comprobó con ecocardiografía transesofágica (ETE) (fig. 1B). Se heparinizó con 0,6mg/kg de heparina sódica no fraccionada para mantener un tiempo de coagulación activada (ACT) mayor a 180segundos y se inició la ECMO V-V, que se programó con los siguientes parámetros: 3.000rpm, 2,7lpm, FiO2 1 y flujo de gas fresco 3lpm (fig. 2). Se descartó recirculación sanguínea entre las cánulas mediante gasometrías pre y posmembrana de oxigenación. Se estableció una ventilación protectora (ventilación mandatoria continua controlada por volumen [VC-CMV] con un volumen corriente [VT] de 3ml/kg de peso ideal, FiO2: 0,4, PEEP 5cm H2O) retirando el tubo de doble luz hasta una posición subglótica, y el mantenimiento anestésico se logró mediante una infusión controlada por objetivo de propofol (TCI). Una vez confirmado el correcto funcionamiento de la ECMO, se vuelve a colocar al paciente en decúbito lateral izquierdo.
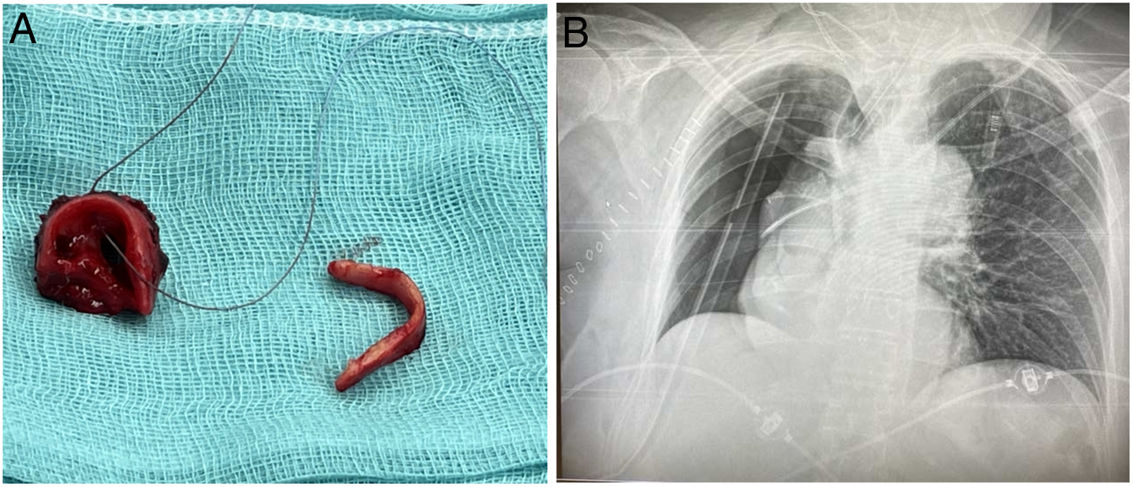
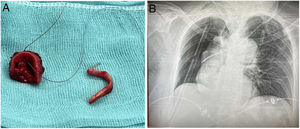
Se realizó la carinectomía sin incidencias (fig. 3A) y la saturación periférica de oxígeno (SpO2) del paciente se mantuvo siempre por encima de 92%, incluso durante los periodos de apnea, que se compensaron con el aumento de los flujos de la ECMO. El tiempo quirúrgico fue de 6h y el tiempo de ECMO fue de 2h 50min. No hubo incidencias en la desconexión y retirada de la ECMO V-V. Al finalizar la cirugía se decidió mantener a la paciente intubada hasta valorar la situación clínica, analítica y la radiografía de tórax (fig. 3B). Se cambió el tubo de doble luz por un tubo de 7mm con un intercambiador y se trasladó a la UCI con los siguientes valores relevantes de analítica y gasometría: pH 7,33, PaCO2 45mmHg, PaO2: 308mmHg, bicarbonato: 23,4mmol/l; hemoglobina: 11,1g/dl, lactato: 1,1 mmol/l. Se extubó a la paciente a las 2h de la cirugía sin incidencias y se dio de alta de nuestra UCI al tercer día postoperatorio.
Segundo casoVarón de 76 años, con talla de 164cm y peso de 72kg, con un tumor escamoso en el lóbulo superior derecho que obstruye el bronquio superior derecho y se extiende hasta la entrada de la carina. Se decide lobectomía superior derecha y carinectomía. Como antecedentes relevantes el paciente es fumador activo (un paquete de cigarrillos al día) y tiene enfermedad pulmonar obstructiva crónica (EPOC) estadio ii de GOLD. Su tratamiento habitual: budesonida-formoterol 160mcg/4,5mcg cada 12h. Las pruebas preoperatorias fueron normales, a excepción de una FEV1 del 66%.
La inducción, monitorización, analgesia y mantenimiento realizados coinciden con lo presentado en el caso anterior. Tras la realización de una mediastinoscopia se canalizaron la vena femoral derecha (23Fr) y la vena yugular derecha (17Fr), y se comprobó su correcta colocación mediante ETE. Tras una correcta heparinización (0,6mg/kg de heparina sódica no fraccionada para ACT>180segundos), se inició la circulación por la ECMO y se instauró una ventilación protectora con VT 3ml/kg. La ECMO V-V se programó con los siguientes parámetros: 3.100rpm, 2.8lpm, FiO2 100% y flujo de gas fresco 5lpm. Se estableció una ventilación protectora (VC-CMV Vt: 3ml/kg de peso ideal, FiO2: 0,4, PEEP 5cm H2O) ajustando los parámetros según gasometrías seriadas.
Se realizó la carinectomía y la SpO2 del paciente se mantuvo siempre por encima de 95%. El mantenimiento de la hipnosis durante la ECMO se realizó con TCI de propofol guiada por BIS. Durante la cirugía el paciente precisó en momentos puntuales noradrenalina 0,1 mcg/kg/min debido a sangrado quirúrgico moderado, necesitando además 5 concentrados de hematíes, 2 pool de plaquetas y 4 unidades de plasma fresco congelado. El tiempo quirúrgico fue de 11h y el tiempo de ECMO fue de 7h 50min. No hubo incidencias en la desconexión y retirada de la ECMO V-V. Al finalizar la cirugía se decidió mantener al paciente intubado hasta valorar la situación clínica, hemodinámica, analíticas y radiografía de tórax. Se cambió el tubo de doble luz por un tubo de 8mm con un intercambiador y se trasladó a la UCI con los siguientes valores relevantes de analítica y gasometría: pH 7,32, PaCO2 45mmHg, PaO2: 195mmHg, bicarbonato: 28,4mmol/l; hemoglobina: 10,1g/dl, lactato: 1,8mmol/l, plaquetas: 120.000/mcl, fibrinógeno 188mg/dl. Se extubó al paciente a las 12h de la cirugía sin incidencias y se dio de alta de nuestra UCI al 2.° día postoperatorio.
DiscusiónLa ventilación intracampo y la ventilación en jet aumentan el tiempo quirúrgico y el riesgo de lesiones bronquiales en la cirugía traqueal3. Además, los manguitos de los tubos endotraqueales son propensos a romperse cuando se repara la tráquea4 en la ventilación intracampo y durante la ventilación en jet, ya que el aumento de las presiones de conducción y los tiempos de inspiración pueden provocar una impedancia en el flujo de gas espiratorio, el desarrollo de auto-PEEP y alteración de la eliminación de CO25.
Debido a la excelente experiencia de ECMO V-V durante el trasplante de pulmón6, el uso de este para cirugía traqueal puede representar una opción válida que evitaría estas complicaciones, puesto que además de facilitar la técnica quirúrgica asegura una oxigenación y lavado de carbónico del paciente, aun en caso de lesión en la vía aérea inferior durante la cirugía. Sin embargo, también plantea nuevos retos a resolver: el impacto del circuito de la ECMO sobre la distribución y el metabolismo de fármacos está poco dilucidado7, afectando principalmente a aquellos fármacos que son lipofílicos. El fenómeno de secuestro puede ser impredecible, ya que los fármacos pueden unirse inicialmente al circuito y luego continuar siendo liberados con el tiempo8. Además, la heparinización podría favorecer las complicaciones hemorrágicas (sería preciso la realización de estudios clínicos relevantes que estudien este hecho), aunque en nuestro segundo caso se manejó con éxito con transfusiones y soporte vasopresor. Las complicaciones relacionadas con la mala posición de las cánulas de ECMO, la colocación del paciente y el riesgo de acodamiento de las cánulas pueden prevenirse y resolverse con el uso apropiado de ETE y un personal con adecuada formación en este aspecto, aunque puede alargar el tiempo anestésico previo a la cirugía. Además, la planificación coordinada con el equipo quirúrgico es fundamental (en uno de los casos expuestos la ECMO se inició al principio de la cirugía para facilitar la técnica quirúrgica teniendo en cuenta el caso específico). Es muy importante planificar la monitorización estrecha y la titulación regular de los fármacos a los niveles de concentración deseados, si se requiere (como antibioterapia, inmunosupresores, etc.). Así, la ECMO sería una alternativa válida para los pacientes que requieren cirugía traqueal.
ConclusionesLa ECMO V-V nos asegura la oxigenación en pacientes durante la cirugía de tráquea y supone una alternativa viable en pacientes seleccionados, siempre de acuerdo con el equipo quirúrgico. Resulta fundamental la valoración y planificación minuciosa de todos los pasos intraoperatorios, así como las complicaciones asociadas. Futuros estudios deben explorar el balance riesgo/beneficio de la introducción de esta técnica para casos seleccionados, siendo recomendable realizarla en centros con experiencia en el manejo de sistemas de oxigenación extracorpóreos.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.