Al igual que la aparición del virus de la inmunodeficiencia humana en la década de los ochenta significó un cambio de paradigma en las medidas de protección utilizadas por el personal sanitario (uso de guantes, manejo de accesos venosos, etc.), la aparición del virus SARS-CoV-2 va a significar un cambio en la forma de actuar, sobre todo en aquellas situaciones que pueden suponer un elevado riesgo de contagio (ventilación manual, intubación orotraqueal, etc.).
Desde su detección en Wuhan a finales de 2019, el virus se ha propagado rápidamente por todo el mundo y fue clasificado por la OMS como una emergencia de salud pública de importancia internacional1. El SARS-CoV-2 es conocido por propagarse a través de contacto directo, gotas respiratorias y aerosol de individuos infectados.
El virus SARS-CoV-2, con un número de reproducción básico de alrededor de 2,5, es altamente contagioso2,3, incluso durante el período de incubación4, estimado en 14 días. La clínica puede aparecer a los 4 o 5 días de la exposición5,6. Los portadores asintomáticos infectados por SARS-CoV-2, que representan un 1% de los casos confirmados7, pueden transmitir potencialmente el virus durante el tiempo de incubación8, lo que hace que la identificación y la prevención de la infección por SARS-CoV-2 sea un desafío importante.
Según el único estudio que hay en la actualidad sobre el impacto de la cirugía realizada durante el período de incubación de la COVID-19, en pacientes sin infección conocida9 (estudio retrospectivo, multicéntrico, realizado en hospitales de China), un 44% de los pacientes terminaron en la Unidad de Cuidados Intensivos, cuando habitualmente esta cifra no supera el 26%, y un 20,6% murieron, cuando la tasa de mortalidad normalmente no supera el 1%, es decir, los pacientes operados durante este período presentaron una tasa de mortalidad de 10 a 20 veces superior a la normal. Actualmente está en marcha un estudio multicéntrico, prospectivo, de cohorte, que pretende determinar el momento óptimo para realizar intervenciones quirúrgicas tras la infección por SARS-CoV-2 y evaluar indicadores quirúrgicos clave. El estudio se ha llevado a cabo en 116 países y 1.644 hospitales. Finalizada la fase de recogida de datos se ha completado el registro de 137.169 pacientes10.
Por otro lado, aunque estandaricemos el uso de la PCR de frotis nasal o faríngea y la serología para la detección de anticuerpos, se han reportado casos que tras una intervención quirúrgica han desarrollado clínica y radiológicamente signos y síntomas de COVID-19 entre los días 2 y 4 del postoperatorio9.
Además, existen bastantes interrogantes en cuanto a la inmunización y duración de la misma. Incluso después de establecer un control efectivo del virus tendremos que estar preparados para las infecciones y rebrotes que se producirán. Las intervenciones programadas que se realizan para atender a una amplia variedad de pacientes que son sometidos a cirugía electiva son uno de los procedimientos donde más tenemos que estrechar la vigilancia.
La elaboración de planes y recomendaciones que minimicen la transmisión perioperatoria de patógenos y permitan la realización de intervenciones en entornos seguros ha ido creciendo desde la aparición de la presente pandemia de COVID-1911,12; dichos planes deben sumarse a los protocolos ya existentes para la vigilancia y control de las infecciones de localización quirúrgica13. El presente trabajo pretende hacer una revisión crítica de las recomendaciones existentes, remarcando aquellas que deberán dirigir nuestras actuaciones a partir de estos momentos.
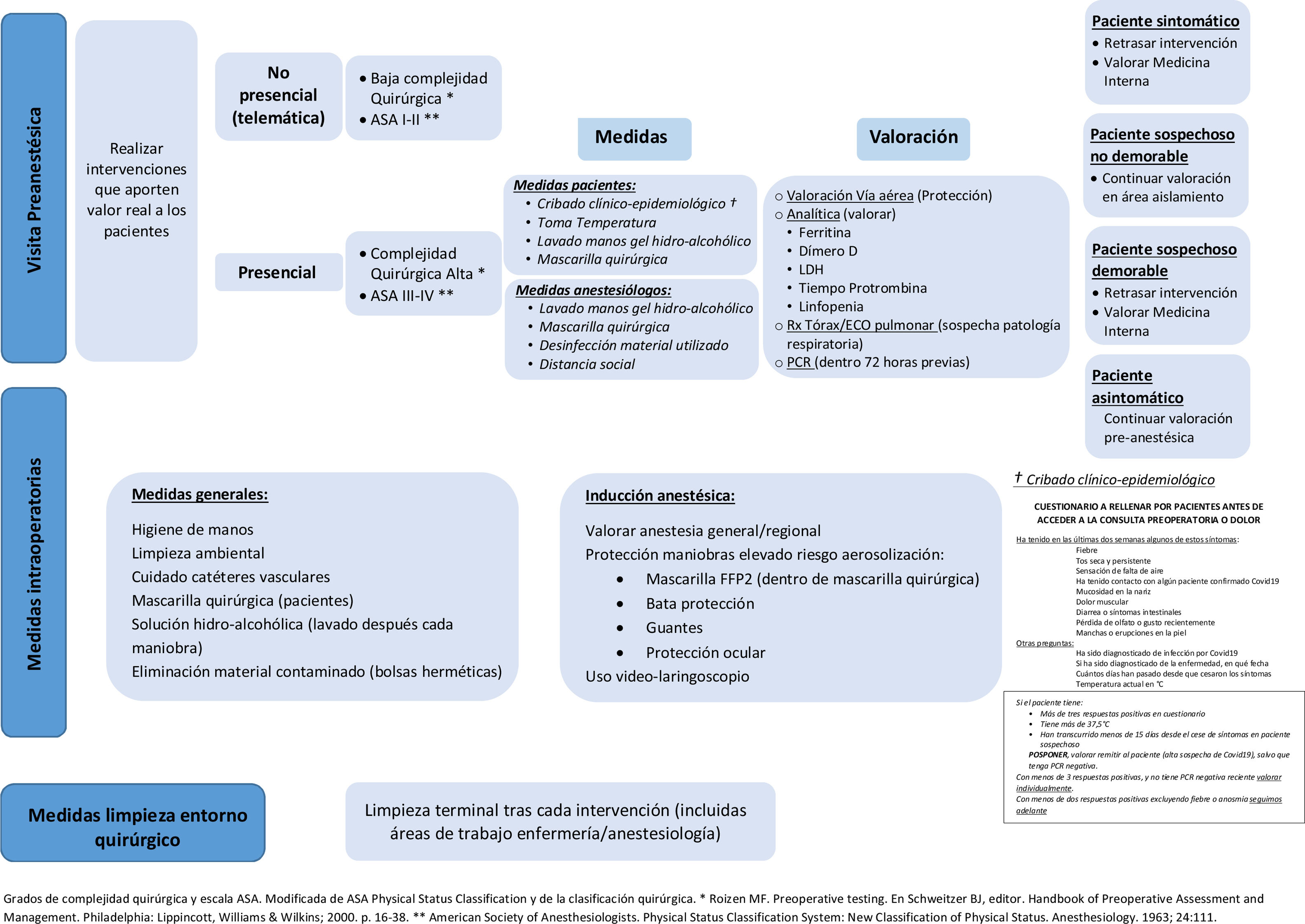
Visita preanestésicaEn primer lugar, una vez pasadas las diferentes fases de alerta, en las que hemos ajustado nuestra actividad quirúrgica a los diversos escenarios posibles14, debemos aprovechar la situación que se nos presenta para replantearnos las listas de espera quirúrgicas y valorar la realización de aquellas intervenciones que realmente supongan un beneficio evidente para los pacientes. El cese de actividad que ha supuesto el tener que atender la emergencia sanitaria producida por el virus SARS-CoV-2 no nos tiene que permitir reanudarla cometiendo los mismos errores. Hay que definir con el equipo quirúrgico aquellas intervenciones cuyo índice de riesgo quirúrgico, añadido al riesgo definido por las comorbilidades del paciente, sea asumible cuando se enfrenta al riesgo de no realizar la intervención, y por otro lado, que supongan una mejora clara de la calidad de vida. En esta toma de decisiones es fundamental la participación conjunta con los pacientes, que permite pactar el tratamiento más adecuado para el enfermo tras la discusión de las opciones, los beneficios y los perjuicios, de acuerdo con las preferencias y los valores personales del individuo o el conocimiento científico existente, valorando las ventajas e inconvenientes de cada opción (decisión clínica compartida)15. Hagamos solo aquellas intervenciones que aporten valor real a los enfermos.
Consulta preoperatoriaUna de las herramientas que se han implementado durante las fases iniciales de la pandemia han sido las consultas preoperatorias no presenciales mediante visita telefónica, bien para reevaluar pacientes ya vistos, bien para la realización de valoraciones preanestésicas con la idea de minimizar las visitas de pacientes a los hospitales y disminuir los riesgos de contagio. Su viabilidad ha sido valorada en diferentes estudios, que han concluido que la evaluación preanestésica mediante telemedicina versus presencial fue equivalente, sin mayor número de suspensiones y con predicciones del manejo de la vía aérea similares16. Las visitas deben estar claramente definidas y protocolizadas, con las garantías de cumplimiento de la Ley Orgánica de Protección de Datos, como una herramienta pactada con el paciente, con todas las garantías legales, y deben disponer de un tiempo determinado en la agenda para garantizar su calidad y la buena praxis17. Se debe valorar en cada centro la posibilidad de implementar un sistema de firma electrónica, un registro del consentimiento informado para intervención quirúrgica o un sistema de recogida del consentimiento enviado a los pacientes por correo electrónico y devuelto mediante el mismo sistema una vez firmado.
Este tipo de valoración telemática se debe desarrollar sobre todo en pacientes con baja complejidad quirúrgica, en aquellos que sepan manejar las nuevas tecnologías, con comorbilidades no limitantes (ASA I o II) y que consientan en la realización de este tipo de valoración (fig. 1).
En las consultas preoperatorias presenciales se tienen que implementar toda una serie de medidas para evitar la posibilidad de contagio entre los profesionales y los pacientes. Antes del acceso a la consulta hay que hacer un cribado clínico epidemiológico: los pacientes tienen que rellenar un cuestionario que incluye preguntas sobre su historial epidemiológico (contactos con casos positivos en los últimos 14 días y/o procedencia de una residencia o institución cerrada) y sobre detección de síntomas o signos sospechosos de posible infección por SARS-CoV-2 (fiebre, tos seca, cuadro constitucional leve, anosmia, diarrea, cefalea). Se debe tomar la temperatura (termómetros de rayos infrarrojos), disponer de gel hidroalcohólico para el lavado de manos y proporcionar mascarilla quirúrgica. La toma de temperatura y la comprobación del uso de mascarilla quirúrgica debe realizarse al ingreso en el centro hospitalario. El profesional, a su vez, tiene que extremar las medidas de asepsia y antisepsia (mascarilla, lavado de manos con solución hidroalcohólica, toallitas de desinfección de superficies con solución hidroalcohólica para limpieza de aquellos elementos que se puedan tocar durante la visita, ordenadores, teclados, ratones, fonendoscopio, etc.), así como implementar medidas para mantener la distancia física de seguridad.
En la evaluación de la vía aérea hay que valorar la dificultad de ventilación, los factores predictores de dificultad de ventilación de Langeron et al.18, y la dificultad de intubación, por ejemplo mediante el índice de riesgo de dificultad de intubación de El-Ganzouri et al.19, la valoración de la apertura bucal y subluxación mandibular y la clase de Mallampati. Todas estas valoraciones se deben realizar extremando las medidas de protección.
En la analítica hay que incluir parámetros bioquímicos que se elevan de forma precoz en los casos de enfermedad por COVID-19, como son la ferritina, que es el más precoz, comenzando a elevarse a partir del cuarto día, el dímero D, que se eleva después de la primera semana y va progresivamente aumentando, y la lactato deshidrogenasa. Por otro lado, hay que tener especial cuidado en la valoración del tiempo de protrombina y la presencia de linfopenia en el hemograma.
En cuanto a la radiografía de tórax, hay que tener en cuenta que durante la fase inicial de la infección el virus no ha llegado a los alvéolos, por lo que la imagen radiológica es normal. Por otro lado, en la fase de infección pulmonar (cuyas imágenes radiológicas pueden consistir en opacidades periféricas, aumento de densidad tenue difusa, patrón intersticial focal, patrón intersticial difuso, patrón alveolointersticial) la radiografía de tórax presenta una sensibilidad en la detección de una consolidación pulmonar del 68% y una especificidad del 95%. En el caso de la detección de un síndrome alveolointersticial a través de una radiografía de tórax, la sensibilidad es del 60% y la especificidad del 100%20. Tenemos, por otro lado, otra herramienta útil a nivel preoperatorio que no podemos despreciar, como es la ecografía pulmonar, con una sensibilidad y una especificidad del 93 y el 100% para la detección de una consolidación alveolar y del 98 y el 88% para la detección de un síndrome alveolointersticial, respectivamente20. Recordemos que, en ausencia de síntomas, las radiografías de tórax producen pocos diagnósticos y muchos falsos positivos. No mejoran la predicción o estratificación del riesgo y deben reservarse para pacientes con síntomas compatibles con enfermedad cardiopulmonar aguda (disnea, sibilancias, esputo productivo, etc.)21, por tanto, la solicitud de una radiografía de rutina no es recomendable, quedando indicada solo en aquellos pacientes en los que por clínica, antecedentes o exploración se sospeche alteración pulmonar.
La consulta presencial se debe realizar en aquellos pacientes que precisen una mayor preparación preanestésica por complejidad quirúrgica o presencia de comorbilidades limitantes (ASA III o IV) (fig. 1).
La PCR de exudado nasofaríngeo es la prueba de elección para el diagnóstico de infección activa por SARS-CoV-2. Se estima que la sensibilidad es del 70-80%, dependiendo de la fase evolutiva de la infección y la calidad de la muestra. La especificidad es superior al 95%. La prueba debería realizarse lo más cerca posible de la cirugía, considerando un margen de 48-72h y adoptando medidas para evitar infecciones en los días previos a esta.
La petición de la prueba de PCR de frotis nasal o faríngeo se debe realizar teniendo en cuenta las limitaciones propias de las técnicas y que el resultado va a depender del momento de la toma de la muestra, de la calidad de la misma y de la sensibilidad y especificidad de la prueba. La positividad de la PCR nos va a servir para decidir retrasar la intervención al menos 15 días, si el procedimiento quirúrgico no es urgente. Sin embargo, una PCR negativa (que puede representar un falso negativo o una infección activa en fase muy inicial) no nos puede hacer bajar la guardia sobre las medidas de protección universal que debemos implementar de cara al procedimiento quirúrgico.
Se debe definir un circuito de actuación según los diferentes escenarios que nos podemos encontrar al realizar la evaluación preoperatoria (paciente sintomático, paciente asintomático con fiebre, alteraciones analíticas con/sin sintomatología) y que marcarán los siguientes pasos: continuar la visita preoperatoria, pero en un área de aislamiento (paciente sospechoso no demorable), retrasar la intervención quirúrgica y valoración por Medicina Interna (paciente sospechoso demorable), etc.
Al finalizar la valoración preoperatoria debemos, de una forma clara y concisa, proporcionar información a los pacientes sobre los riesgos de las infecciones de localización quirúrgica, y cómo prevenirlas, controlarlas, identificarlas o cuidarlas; aconsejar la ducha el día previo a la intervención, el lavado de dientes y boca y la no eliminación del vello de forma rutinaria22; favorecer el ingreso el mismo día de la intervención quirúrgica.
Dentro del documento elaborado por diferentes sociedades científicas y avalado por el Ministerio de Sanidad, Recomendaciones para la programación de cirugía en condiciones de seguridad durante la pandemia COVID-19, la versión del 2 de junio del 202012 recomienda la realización de un cribado clínico epidemiológico al menos 14 días antes de la intervención quirúrgica con control riguroso de las medidas de distanciamiento físico y protección durante las 2 semanas previas a la intervención. Aconseja una segunda visita clínica de valoración en las 72h previas a la cirugía, en la que se realizaría la prueba de PCR. Estas recomendaciones son difíciles de cumplir en la práctica diaria y deben adaptarse a la carga de trabajo de cada hospital. En nuestro caso, la complejidad de la intervención quirúrgica, la prioridad a la hora de programar la operación y la comorbilidad de los pacientes (definidas por el cirujano en la solicitud de intervención quirúrgica) son las que definen el momento de la visita preoperatoria, siendo más precoz cuanto mayor sea la complejidad, más compleja sea la intervención y más comorbilidades tenga el paciente. Una vez valorado el riesgo quirúrgico del paciente, optimizada su situación clínica, informado el paciente (incluyendo el control de las medidas de protección y distanciamiento físico) y obtenido el consentimiento informado, se programa el paciente. La PCR de cribado quirúrgico se realiza 72h antes de la intervención, recomendando de nuevo al paciente que extreme las medidas de protección y distanciamiento físico hasta que tenga que acudir para intervenirse.
Medidas intraoperatoriasEl SARS-CoV-2 puede sobrevivir durante al menos 3 días en una variedad de materiales comúnmente encontrados en los quirófanos (acero inoxidable, plástico)23. La sólida evidencia generada por las publicaciones de los últimos 12 años indica que un enfoque multimodal es necesario para atenuar al máximo el alto riesgo de eventos de transmisión de patógenos intraoperatorios. Se debe mejorar la higiene de las manos, la limpieza ambiental, el cuidado de los catéteres vasculares (tanto arteriales como venosos), la descolonización del paciente y la optimización de la vigilancia. Todos ellos deben ser empleados de forma conjunta para mejorar el control perioperatorio de infecciones por patógenos bacterianos y virales11.
Se debe valorar que todos los pacientes ingresen en el área quirúrgica provistos de mascarilla quirúrgica para la protección inversa.
Disponer de dispensadores con desinfectante de manos de base hidroalcohólica en la cercanía del área de trabajo del anestesiólogo, disponer de bolsas con cierre hermético para colocar todo el material contaminado durante la inducción, limpiar de forma sistemática nuestra área de trabajo tras la inducción anestésica y tras cada manipulación con toallitas desinfectantes son medidas imprescindibles para mantener un entorno de trabajo seguro y descontaminado.
Durante la inducción y sobre todo en las urgencias anestésicas existe un elevado número de maniobras que se realizan en el entorno del paciente que constituyen un alto riesgo de transmisión viral o bacteriana; se han cuantificado unas 350 actuaciones posibles de contaminación durante la práctica rutinaria intraoperatoria de un paciente24. Con la simple colocación de botes de solución hidroalcohólica en la cercanía del anestesiólogo o en su lugar toallitas con desinfectante de superficies con base hidroalcohólica, mediante el lavado de manos tras cada maniobra, pueden reducirse hasta 20 veces las maniobras de riesgo25.
Inducción anestésicaEn cuanto al tipo de anestesia indicada, dependerá de las condiciones respiratorias del paciente y del tipo de intervención quirúrgica. Debe primar, siempre que sea posible, la anestesia regional, permaneciendo el paciente durante todo el proceso con mascarilla quirúrgica.
Microbios, virus y bacterias colonizan nuestra piel26. La boca es el mayor reservorio de bacterias; al hablar se dispersan por el aire y el entorno inmediato. Las secreciones respiratorias, bien durante la aerosolización en la intubación, bien por contaminación de superficies, con posterior contacto y transmisión a ojos, nariz y/o boca, son posibles causas de infección. Se deben implementar medidas de protección universal durante aquellos procedimientos donde exista un riesgo elevado de aerosolización para los profesionales que van a realizar dichas técnicas (mascarillas de protección al menos FFP2 bajo mascarilla quirúrgica, bata, guantes y protección ocular). No está recomendada de forma rutinaria la descontaminación nasal con antimicrobianos tópicos para eliminar el estafilococo dorado y reducir el riesgo de infección de localización quirúrgica22.
En cuanto al procedimiento de intubación, para disminuir la cercanía a la fuente de posible aerosolización se debe generalizar el uso de videolaringoscopios desechables o esterilizables.
Debemos tener un especial cuidado con los catéteres intravasculares (arteriales o venosos), ya que están en contacto directo con el sistema circulatorio del paciente, con posibilidad de contaminación repetida, con un aumento de la mortalidad asociada directamente a la infección. Limpiar todos los accesos antes de cada inyección y mantenerlos cubiertos con tapas desinfectantes durante y después del procedimiento representan medidas imprescindibles27.
Tras la inducción anestésica se deben limpiar todas las superficies del área de trabajo del anestesiólogo con toallitas con desinfectante de base hidroalcohólica o que contengan amonio cuaternario.
Medidas de limpieza en el entorno quirúrgicoToda esta situación que estamos viviendo nos obliga a mejorar la organización y calidad de la limpieza para reducir de forma sustancial la posible contaminación de nuestra área de trabajo.
La limpieza rutinaria y/o terminal de los quirófanos tras cada intervención, incluidas las diferentes áreas de trabajo de anestesiología y enfermería (con especial atención a teclados, pantallas y ratones de los ordenadores), debe realizarse de forma cuidadosa y exhaustiva, para reducir de forma importante la carga biológica vírica y bacteriana.
No existe evidencia sobre la eficacia y seguridad de la desinfección de SARS-CoV-2 con dispositivos de radiación con luz ultravioleta u ozono. La evidencia disponible apunta a que ambos dispositivos pueden reducir la población de virus de una superficie, sin embargo, se desconoce si esa reducción es suficiente para conseguir la desinfección. Ambos implican riesgos para la salud, ya que pueden causar daños oculares, en la piel o irritación de las vías respiratorias. En ambos casos, la utilización de los dispositivos debe realizarse de forma controlada28.
Para finalizar, es imprescindible promover programas de prevención, control de infecciones y sistemas de vigilancia de las infecciones asociadas a la asistencia sanitaria para permitir el control de su evolución y la comparabilidad de resultados29.
ConclusionesLa aparición de la COVID-19 ya ha significado un cambio en nuestra forma de actuar, sobre todo en aquellas actuaciones que puedan suponer un elevado riesgo de contagio (ventilación manual, intubación orotraqueal, etc.). Muchas de las medidas que en estos momentos se están tomando en la mayoría de los hospitales para evitar la propagación de la COVID-19 han venido para quedarse. La aparición del SARS-CoV-2 ha puesto en evidencia la debilidad de las medidas epidemiológicas que se usaban de forma universal para impedir la transmisión bacteriana o vírica en entornos supuestamente limpios. Muchos de los focos de transmisión han sido los propios hospitales, por lo que la puesta en marcha y el mantenimiento de estas medidas evitarán la propagación de aquellos patógenos que en el futuro puedan ser un nuevo reto médico.
La mayoría de las medidas que se proponen son procedimientos habituales que se deberían tomar en cualquier aislamiento de contacto o como medidas de barrera para impedir la transmisión de patógenos en un entorno perioperatorio. La realidad es que hemos vivido en los últimos años una relajación en las medidas preventivas a la sombra de los potentes tratamientos antibióticos. Esta pandemia nos debería enseñar a no bajar los brazos y mejorar el control de las infecciones perioperatorias, siendo sistemáticos en la aplicación de protocolos de control de patógenos transmisibles.