Las condiciones de obtención y transporte de las muestras tienen influencia en los resultados del análisis de semen en el laboratorio. El diseño y la implementación de un protocolo adecuado para la fase preanalítica es necesario para generar resultados fiables. Este documento trata de proporcionar una serie de recomendaciones en la información que debe ser incluida en las instrucciones a los pacientes. También caracteriza variables y factores de confusión, como el periodo de abstinencia, el lugar de obtención de la muestra, etc. en un listado de verificación.
Collection and transport of semen samples can have an influence on the laboratory analysis results. The design and implementation of a protocol suitable for the pre-analytical phase is required in order to offer accurate results. This document is intended to provide a series of recommendations on the information that should be included in the instructions to the patients. Furthermore, it mentions pre-analytical confounders, such as the period of sexual abstinence, the location where the semen sample was obtain, as well as explanatory variables, included in a sample reception checklist.
Las circunstancias bajo las cuales se recoge una muestra de semen y se transporta al laboratorio influyen en los resultados del análisis. El diseño y la implementación de un protocolo adecuado para la fase preanalítica tendrá consecuencias en el resultado final, independientemente de cuál sea su destino: diagnóstico, pronóstico o terapéutico. Sería preceptivo poner en funcionamiento un sistema de gestión de la calidad en los laboratorios de andrología, ya sea mediante el cumplimiento de los requisitos de las normas de calidad international Organization for Standardization (ISO), a través de una certificación por la norma UNE-EN ISO 9001:20151 o una acreditación por la Norma UNE-EN ISO 15189:20132. La gestión del proceso preanalítico del análisis de semen debe realizarse independientemente de la estrategia/opción del sistema de gestión de la calidad escogido por el laboratorio. En el año 2013 se creó una norma adaptando los requisitos de la ISO 9001 a los laboratorios de reproducción asistida, en la que se establecen requisitos específicos. La norma UNE 1790073 establece que el laboratorio de reproducción debe definir e implantar indicadores de calidad para los procesos operativos.
El laboratorio de andrología acreditado debe asegurar que el control y la gestión del proceso preanalítico cumple con los requisitos de la norma UNE-EN ISO 15189:2013. Para ello debe garantizar que todas aquellas actividades propias de la fase preanalítica no afectarán a los resultados obtenidos en el proceso analítico, del análisis de semen que se ofrece al paciente, a la trazabilidad de las muestras primarias ni a los aspectos relativos a la interpretación de los resultados. Es destacable que la acreditación en un laboratorio de andrología incluye necesariamente el proceso preanalítico, independientemente del alcance definido por el propio laboratorio, por lo que los requisitos preanalíticos deben estar adecuadamente establecidos.
La secuencia de etapas del proceso preanalítico es prácticamente común para todos los procedimientos analíticos del semen. La comunidad científica, mientras que diverge sustancialmente en otros aspectos metodológicos, presenta un alto grado de concordancia en las instrucciones del proceso preanalítico para el estudio del semen, como viene especificado en numerosas guías y documentos de consenso publicados4–6. La armonización del proceso extraanalítico del análisis de semen es un aspecto clave del proceso.
Objetivo y campo de aplicaciónEl objetivo principal de este documento es actualizar los conocimientos en el proceso preanalítico de las muestras de semen, independientemente de que los laboratorios estén certificados o acreditados y/o dispongan de otro modelo de gestión de la calidad. Este objetivo general se desglosa en los siguientes objetivos específicos:
- •
Revisar las evidencias en la preanalítica del espermiograma.
- •
Aportar las recomendaciones para la estandarización de la fase preanalítica del análisis de semen en el laboratorio clínico.
- •
Proporcionar la documentación necesaria para desarrollar la fase preanalítica del análisis de semen atendiendo a los principios de seguridad y calidad.
El campo de aplicación del documento es el análisis de semen con fines diagnósticos, pronósticos o terapéuticos. Este documento complementa al documento publicado por la Comisión de Andrología y Técnicas de Reproducción Asistida en 20067.
Características genéricas de las instrucciones al pacienteResponsabilidadesEl laboratorio clínico tiene la responsabilidad de elaborar las instrucciones de preanalítica, como parte del proceso del análisis, con el objeto de garantizar la validez del resultado solicitado. El facultativo especialista del laboratorio de andrología es el responsable último de la elaboración del procedimiento documentado de la fase preanalítica y de aceptar o rechazar los especímenes en función del cumplimiento por el usuario. Si el laboratorio de andrología está acreditado o quiere acreditarse debe preparar un procedimiento documentado de la gestión del proceso preanalítico definiendo los responsables de cada una de las etapas de dicho proceso1,2.
Se deben establecer los criterios y procedimientos para:
- •
Aceptación o rechazo de las muestras de semen.
- •
Actuación en situaciones especiales (por ejemplo qué hacer si llega poca muestra en el caso de pacientes oncológicos, muestras de pacientes seropositivos, etc.).
- •
Registro de incidencias detectadas en cualquier fase del proceso (recogida adecuada de la muestra, transporte, recepción de muestras, etc.).
- •
Comunicación con los centros y profesionales implicados.
La estrategia de difusión e implantación de los requisitos preanalíticos varía en cada centro sanitario, pero siempre se monitorizará con indicadores. El cálculo de los indicadores debe realizarlo el laboratorio de andrología o, si existe, el responsable de preanalítica del servicio, departamento o unidad de gestión al que esté adscrito, según proceda.
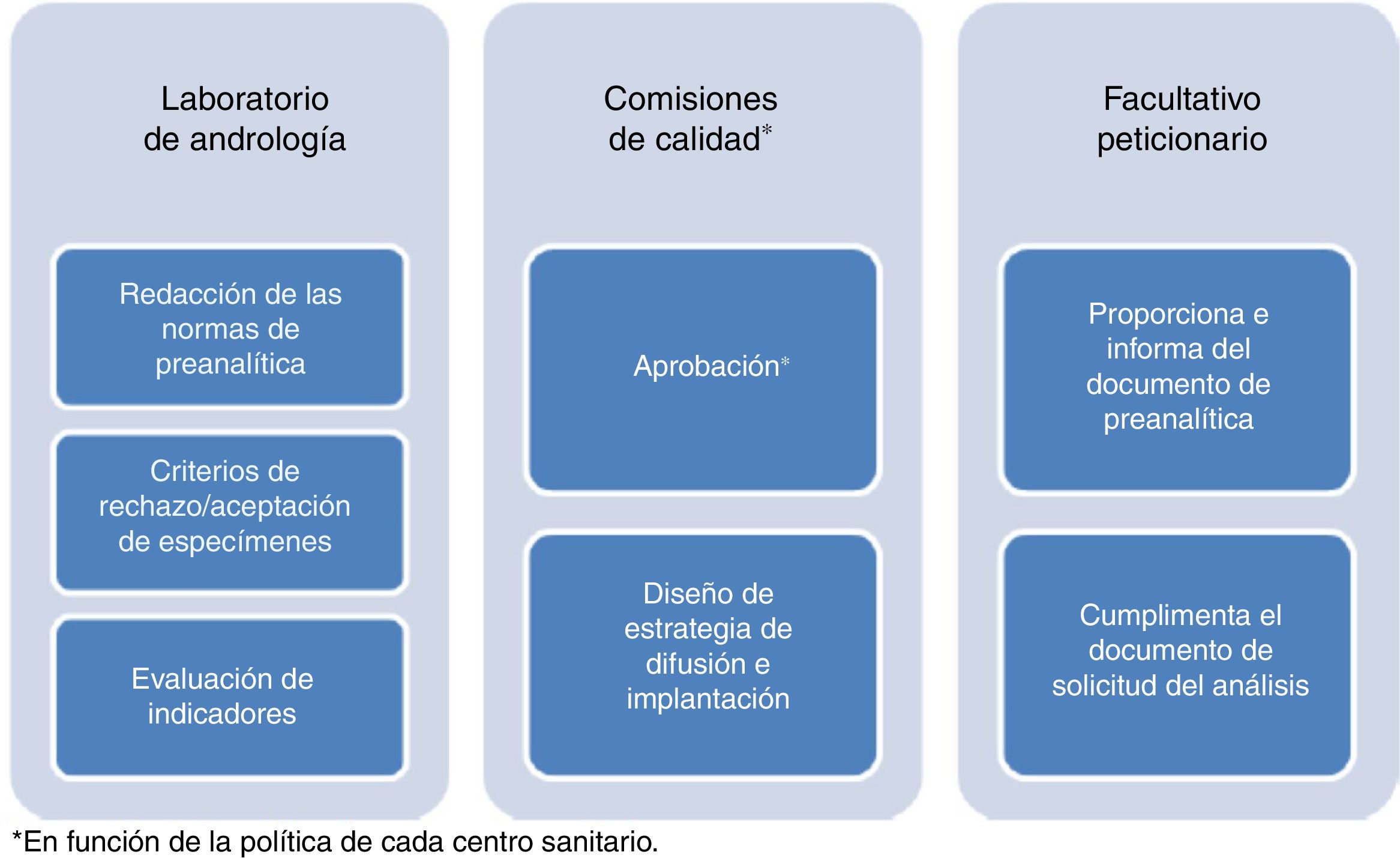
Habitualmente, los requisitos preanalíticos están incluidos en los protocolos diagnósticos o asistenciales específicos, y estos deben ser aprobados por las comisiones de documentación, protocolos y/o de calidad del centro (fig. 1).
Redacción del documentoPara la redacción de los requisitos preanalíticos debe utilizarse un lenguaje legible, claro, conciso y de fácil comprensión8. El documento, además de incluir los requisitos en una secuencia lógica, debe explicar las razones de cada epígrafe con objeto de favorecer su cumplimiento. Antes de difundir el documento en la población usuaria es conveniente realizar pruebas (ensayo de campo) para comprobar su eficacia. Se seguirán las normas de estilo pautadas por la comisión de documentación del centro.
EpígrafesLos requisitos preanalíticos deben incluir los siguientes epígrafes:
De carácter general- •
Ubicación del lugar de recepción de la muestra de semen y teléfono de contacto.
- •
Instrucciones sobre del procedimiento de solicitud de cita para el análisis.
- •
Horario de entrega de la muestra de semen.
- •
Tiempo de abstinencia eyaculatoria.
- •
Método de obtención del eyaculado.
- •
Lugar de obtención del espécimen: ambiente sanitario o doméstico.
- •
Condiciones de transporte.
- •
Tiempo desde la eyaculación hasta la recepción e inicio de análisis en el laboratorio.
Tal como indica el Real Decreto-Ley 9/20149, cualquier cambio en los documentos de los procedimientos operativos o de las normas de actuación debe ser revisado, fechado, documentado y puesto en marcha. Además, deberá existir un sistema que asegure la revisión periódica de los documentos, el registro de los cambios introducidos para que solo las versiones actualizadas estén en uso.
Obtención del eyaculadoTiempo de abstinencia eyaculatoriaLa Organización Mundial de la Salud recomienda un periodo de abstinencia eyaculatoria de 2-7 días5, pero la evidencia científica muestra variaciones en la concentración espermática probablemente causadas por diferencias en el número de días de abstinencia. Cuando el tiempo de abstinencia se ajusta a 3-4 días esta variabilidad disminuye. Se aconseja que en caso de repetición del espermiograma se mantengan los mismos días de abstinencia para que las condiciones preanalíticas sean lo más parecidas entre sí. Además, se han descrito diferencias intraindividuales significativas en función del número de eyaculaciones producidas en la semana previa al análisis10, por lo que se aconseja anotar también cuándo sucedió la penúltima eyaculación. El tiempo de abstinencia y la frecuencia eyaculatoria influyen en el volumen, concentración y movilidad de los espermatozoides6.
Si la muestra se va a utilizar para una técnica de selección de espermatozoides con fines terapéuticos el tiempo de abstinencia recomendado puede variar. En el epidídimo el espermatozoide madura y adquiere potencial fertilizante. El tránsito en el epidídimo se estima que varía entre 2 y 11 días y depende de la frecuencia eyaculatoria. El almacenamiento prolongado tiene efecto negativo en la movilidad11 por efecto de especies reactivas de oxígeno y nitrógeno12. Algunos autores muestran mayor tasa de gestación cuando el tiempo de abstinencia previo a una inseminación es inferior a 2 días, aunque la concentración de espermatozoides recuperados sea menor13.
Ambiente y condiciones de la eyaculaciónEl lugar más apropiado para la recogida de la muestra es el propio centro donde vaya a procesarse. Además de evitar fluctuaciones de temperatura durante el transporte, existen mayores garantías de que el sujeto que entrega el espécimen es quien lo ha producido.
Es preceptivo contar con un habitáculo donde se pueda obtener la muestra de forma íntima, así en el apartado 5.2.5 Instalaciones para la toma de muestras de los pacientes de la norma UNE-EN ISO 15189:2013, queda reflejado que «(…) Las instalaciones para la toma de muestras de los pacientes deben disponer de zonas separadas para la recepción/sala de espera y toma de la muestra. Se deben de tener en cuenta las discapacidades, comodidad y privacidad de los pacientes (…) durante la toma de la muestra»2,14. Debe ser un lugar próximo que garantice la privacidad y donde el paciente no se sienta coaccionado ni apremiado por el personal del laboratorio.
En circunstancias excepcionales, como la incapacidad del paciente para obtener una muestra por masturbación en el centro, el espécimen se puede obtener fuera y ser transportarlo al laboratorio lo antes posible para poder comenzar el análisis en cuanto se complete la licuefacción. Varios estudios han tratado de investigar si existen diferencias en la calidad seminal entre muestras obtenidas en el domicilio y en el centro sanitario, resultando ser no concluyentes15.
Método de obtención de la muestraLo ideal es que el eyaculado se produzca por masturbación y sea recogido en un frasco estéril de material testado no tóxico5,16 (tabla 1).
Test de contenedores para uso diagnóstico en el laboratorio de andrología
| Confirmar la compatibilidad del frasco para recoger muestras de semen |
|---|
| Hacer un pool de muestras con buena movilidad (por ejemplo muestras recuperadas). Se sugiere una concentración de 5 millones de espermatozoides/ml |
| Poner 1ml del pool en el frasco control (material probado no-tóxico) y 1ml del pool en 5 frascos a testar |
| Evaluar la movilidad espermática en intervalos de 1h a 37°C durante 4h y a las 24h |
| Si no hay diferencias (p>0,05 t-test pareado), los frascos se consideran no-tóxicos y aptos para la recogida de muestras de semen |
Adaptado de WHO 20105.
Para evitar contaminación con cuerpos extraños (fibras, pelos, papel, etc.) o restos biológicos se recomienda orinar, lavar los genitales antes de la masturbación y aclarar bien el jabón. Los productos de higiene y tratamiento como cremas, lociones y lubricantes pueden interferir en el análisis de la muestra, y como norma general no deben usarse. Cualquier producto que se emplee para obtener la muestra debe estar testado y no ser tóxico para los espermatozoides (por ejemplo lubricante Pre-Seed®).
Existen evidencias que indican que la calidad de los especímenes varía en función de cómo se produzca el eyaculado17. Las muestras producidas por masturbación pueden ser de calidad más baja que las muestras recuperadas en preservativos de poliuretano sin espermicida durante el coito. Esta variación puede deberse a la diferencia en estímulos sexuales y al tiempo necesario para producir el eyaculado. Se ha demostrado que la duración del estímulo preeyaculatorio tiene una asociación positiva con la calidad seminal18.
Los preservativos comerciales contienen látex y poliisopreno, que son espermiotóxicos y no son válidos para obtener la muestra19. Solo productos testados no tóxicos pueden emplearse (por ejemplo Male-factor Pak®).
Los inhibidores de la 5-fosfodiesterasa como sildenafilo, tadalafilo, vardenafilo, avanafilo, etc. se pueden prescribir, si no existen contraindicaciones clínicas, cuando haya dificultades en la erección y eyaculación.
En los estudios de eyaculación retrógrada debe confirmarse la presencia de espermatozoides en la orina postorgasmo. Si se hallan espermatozoides se programará una prueba diagnóstica en la que es necesario alcalinizar previamente la orina. Si no existen contraindicaciones por enfermedad renal concomitante se administran bicarbonato sódico o comprimidos de citrato potásico unas 2horas antes de obtener la muestra. Cuando la recepción de muestras se realiza por la mañana se puede recomendar alcalinizar la orina la noche previa (8-10h antes). Se mide el pH de una orina basal y, si está por encima de 7,5, se indica al paciente que alcance un orgasmo por masturbación. Se recoge la orina postorgasmo en un frasco que contenga medio de cultivo para alcalinizar aún más la orina5.
La electroeyaculación por sonda rectal se puede emplear en lesionados medulares y otras enfermedades neurológicas para obtener semen. Se realiza en quirófano y bajo anestesia general.
Recepción de la muestraLa recepción de la muestra es un punto clave del proceso donde se pueden cometer errores con graves implicaciones para la seguridad del paciente. Aunque la recepción habitualmente la realiza un técnico especialista de laboratorio, es responsabilidad del facultativo la elaboración y supervisión del protocolo de recepción.
Es recomendable que la identificación del frasco que contiene el semen se haga en presencia de testigos, es decir, del paciente que hace la entrega. Para la relación unívoca del paciente y su muestra se debe establecer una secuencia que permita evitar y detectar errores, por ejemplo:
Pegar códigos de barras en → tapón frasco →pared frasco →hoja de trabajo/petición de laboratorio → resguardo de entrega (fig. 2).
El registro de muestras en el sistema informático del laboratorio se llevará a cabo de la misma manera que para el resto de especímenes a procesar; es decir, se comprueba la cumplimentación de todos los campos de la petición: etiqueta de historia clínica, códigos de médico y de servicio peticionario, diagnóstico de presunción, etc. y se le asigna el número de laboratorio (código de barras) (tabla 2). En los laboratorios de andrología que estén acreditados se deben cumplir los requisitos del apartado 5.4.3 Información a cumplimentar en la hoja de petición de la norma UNE-EN ISO 15189:2013. En la petición analítica deben constar los datos necesarios que se especifican: identificación inequívoca del paciente (número de historia y de tarjeta sanitaria, género, fecha de nacimiento, etc.); identificación del médico clínico peticionario o persona legalmente autorizada que solicita el análisis clínico; destino del informe (lugar y persona); tipo de muestra y su procedencia anatómica, en este caso semen; pruebas analíticas solicitadas; información clínica o de diferente naturaleza relativa al paciente y relevante para la correcta interpretación de los resultados; fecha y hora de la obtención de la muestra y de la recepción de la muestras en el laboratorio clínico. Asimismo, se recomienda especificar la persona que recepciona la muestra (semen)2.
Lista de verificación para recepción de muestras
| Datos de filiación | Nombre y Apellido |
| Teléfono de contacto | |
| Número de historia clínica | |
| Cumplimiento de requisitos preanalíticos | Horas desde la última eyaculación |
| Hora de obtención/hora de recepción | |
| Muestra completa | |
| Lugar de obtención del eyaculado | Centro sanitario/externo |
| Condiciones de transporte: luz, temperatura | |
| Cuestionario de preanalítica | Hábitos tóxicos |
| Enfermedades intercurrentes, proceso febril, etc. | |
| Medicamentos | |
| Seguridad del paciente/Trazabilidad | Identificación del frasco y hojas de trabajo en presencia del paciente (testigo) |
| Firma del paciente de la entrega de muestra para técnicas de reproducción asistida | |
| Entrega de comprobante de entrega de muestra (código de barras) | |
| Información sobre la emisión de resultados |
Se debe realizar una entrevista de preanalítica precisa donde se verifiquen los datos de filiación del paciente: nombre, apellido, número de historia clínica y teléfono. Es conveniente preguntar el tiempo de abstinencia eyaculatoria en lugar del tiempo de abstinencia sexual, habitualmente interpretado como coito (tabla 3). Se deben anotar las horas de obtención y recepción de la muestra y el lugar, así si se estima oportuno (por ejemplo necrozoospermia, astenozoospermia severa) se puede solicitar una nueva muestra recogida en condiciones diferentes o distintas.
Encuesta de preanalítica. Ítems para incluir en el cuestionario
| Edad |
| Índice de masa corporal |
| Dieta |
| Actividad física |
| Consumo de tabaco, alcohol, cafeína |
| Medicamentos, drogas de abuso |
| Exposición ocupacional o ambiental a tóxicos |
| Infecciones por: Neisseria gonorrhoeae (gonococo), Chlamydia trachomatis, Mixovirus parotiditis (parotiditis) |
| Enfermedad testicular: criptorquidia, testículos en ascensor, traumatismo, varicocele |
| Paternidad previa (gestación) |
En unas condiciones predeterminadas la calidad seminal dependerá de factores no modificables como producción de espermatozoides por los testículos, secreción de glándulas accesorias, afecciones recientes (fiebre) y otros factores que deben tenerse en cuenta a la hora de interpretar los resultados. Por tanto, la encuesta de preanalítica debe incluir factores que pueden influir en el resultado del análisis de semen o suponer un sesgo en el caso de que los datos se vayan a utilizar posteriormente en un estudio. Proponemos un ejemplo con algunos aspectos a considerar (tabla 3).
La colección de una muestra incompleta debe ser criterio de rechazo si la prueba tiene fines diagnósticos (tabla 4). El eyaculado recogido en un frasco y mezclado constituye en realidad un artefacto de laboratorio. Se han aislado hasta 6 fracciones en el eyaculado con diferente composición bioquímica y celular. Fisiológicamente, es la primera fracción la que contiene la mayor parte de los espermatozoides resuspendidos en fluido prostático20. En el caso de recepción de muestras incompletas para técnicas de reproducción asistida es interesante preguntar si la parte del eyaculado perdida fue la primera fracción, y valorar la necesidad inmediata de solicitar una nueva muestra.
Criterios de rechazo de muestras para diagnóstico
| Trazabilidad de las muestras y documentación | Imposibilidad de identificar al paciente |
| Imposibilidad de identificar la muestra | |
| Ausencia de solicitud analítica | |
| Cumplimentación incorrecta de la petición | |
| Análisis fuera de la cartera de servicios del peticionario | |
| Estabilidad de la muestra | Exposición a la luz |
| Temperatura inadecuada (<20°C o>37°C) | |
| Tiempo de transporte>45min | |
| Recipiente | Recipiente inadecuado |
| Recipiente mal cerrado | |
| Recipiente roto | |
| Muestra derramada | |
| Normas de preanalítica | Abstinencia eyaculatoria (<2 o >7 días) |
| Muestra incompleta (pérdida de alguna fracción del eyaculado) | |
| Muestra contaminada con lubricantes, pomadas, etc. | |
| En análisis de semen posvasectomía, menos de 4 meses desde la intervención quirúrgica |
Si la muestra se ha obtenido en un lugar diferente al centro sanitario se deben conocer las circunstancias en las que el frasco ha sido transportado: protegido de la luz, a temperatura adecuada (∼20-37°C) y recipiente apto bien cerrado.
Se debe preguntar sobre o acerca de: la existencia en los 2 meses y medio previos a la recepción de la muestra (tiempo medio de la espermatogénesis) de procesos febriles; presencia de enfermedades y consumo de drogas o medicamentos que puedan influir en los resultados. El listado de drogas de uso recreativo y medicamentos que alteran la capacidad de producir una muestra de semen y/o la calidad de los espermatozoides es muy amplio (tabla 5).
Medicamentos comunes que pueden influir en la eyaculación y o calidad del semen
| Testosterona |
| Inhibidores de la 5α-reductasa |
| Bloqueadores beta |
| Inhibidores de la fosfodiesterasa |
| Psicotrópicos: inhibidores selectivos de la recaptación de serotonina, antidepresivos tricíclicos, inhibidores de la monoaminooxidasa, litio |
| Antihipertensivos: bloqueadores beta, diuréticos, bloqueantes de los canales de calcio, inhibidores de la enzima convertidora de angiotensina |
| Antiinfeciosos: trimetoprim-sulfametoxazol, nitrofurantoína, macrólidos, aminoglucósidos, ketoconazol |
| Anticancerosos: quimioterápicos, imatinib |
Fuente: adaptado de Samplaski y Nangia21.
Cuando se recoge una muestra para su uso en técnicas de reproducción asistida el paciente debería firmar la entrega en el laboratorio indicando su nombre, apellidos, identificación (DNI, pasaporte) y firma (fig. 3).
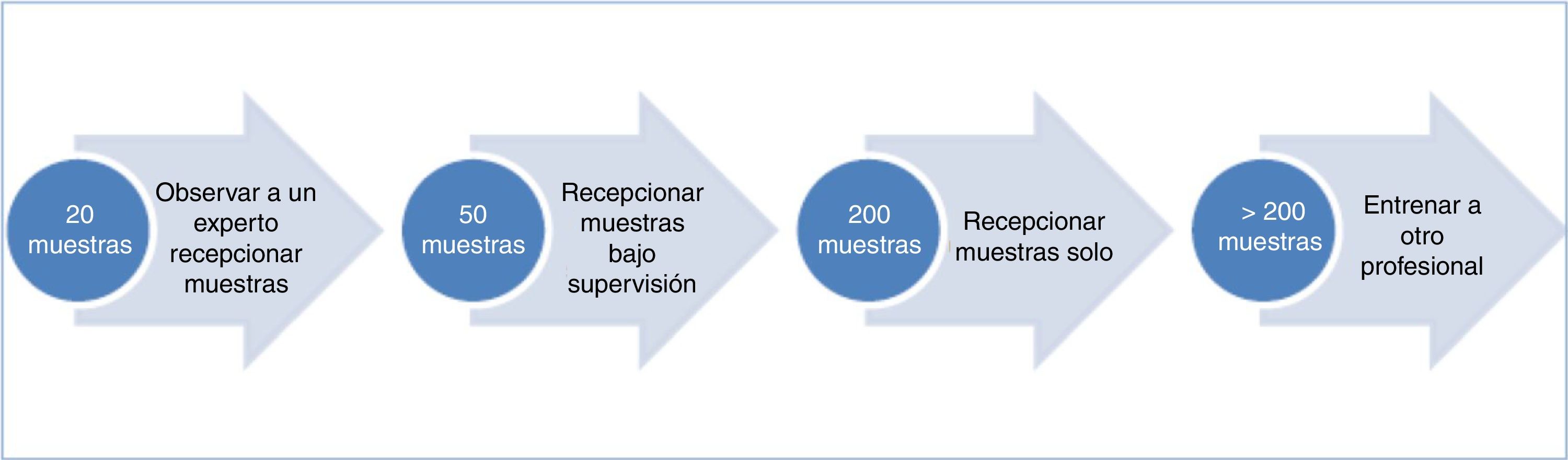
El personal que recepciona las muestras debe contar con el entrenamiento adecuado para hacerlo. Lo ideal sería establecer un protocolo formativo (fig. 4) y contar con un listado de verificación para la recepción de muestras con el objeto de identificar errores fácilmente (tabla 2).
El laboratorio debe contar con criterios de rechazo establecidos (tabla 4).
Cualquier incidente o cuasi-incidente acontecido durante la recepción de muestras en el laboratorio de andrología debe quedar registrado en una ficha donde consten la fecha, la descripción del tipo de incidente y la causa con el objeto de establecer medidas correctivas y preventivas. Si el laboratorio está certificado o acreditado deberá registrar todas las no conformidades y establecer todas las acciones correctivas y preventivas correspondientes, así como establecer un seguimiento de dichas acciones.
Indicadores de calidadEl laboratorio de andrología debe registrar el seguimiento y control de las distintas actividades preanalíticas mediante evaluación de los indicadores definidos y las incidencias detectadas en cada centro, el resultado y seguimiento de las auditorías internas, el análisis de los resultados obtenidos tras la participación del laboratorio en programas de control externo de la calidad para el proceso preanalítico, etc.
El establecimiento de indicadores en el proceso preanalítico es un aspecto esencial para llevar a cabo una mejora tras el análisis de los mismos y el establecimiento de acciones de mejora.
El laboratorio priorizará aquellos indicadores que suministren información fiable y cercana a los objetivos propuestos. Se puede dar preferencia en función de la experiencia del laboratorio, o mediante un análisis previo del registro de las no conformidades y de las incidencias más frecuentes y críticas presentes en el propio laboratorio.
Proponemos los siguientes ejemplos para elaboración de indicadores:
- •
Número de reclamaciones.
- •
Número de muestras rechazadas.
- •
Faltas a citas.
- •
Tiempo de espera para cita en el laboratorio.
- •
Tiempo de espera en el laboratorio.
- •
Condiciones de transporte inadecuadas.
- •
Petición ininteligible.
En el anexo 1 de este documento se dan ejemplos de las instrucciones que se deberían dar a los pacientes para garantizar que se cumplen los requisitos definidos de preanalítica para diferentes muestras. Se recomienda que el laboratorio disponga de estas instrucciones bien documentadas y actualizadas, de forma que el paciente pueda entender con claridad los pasos a seguir y garantizar de esta manera la calidad de la muestra durante todo el proceso preanalítico. Si bien aquellos laboratorios que estén acreditados (toma y manipulación de la muestra primaria; subapartado 5.4.4 de la norma UNE-EN ISO 15189:2013) es un requisito y no una recomendación que dispongan de estas instrucciones documentadas para entregar a los pacientes.
Se recomienda que conste el lugar de recepción de la muestra y los datos de contacto con el laboratorio (teléfono, correo electrónico) donde el paciente pueda dirigirse para consultar las dudas de preanalítica o modificar las citas. En circunstancias especiales dichas instrucciones se modificarán en función de las características del paciente, por ejemplo: imposibilidad de recoger una muestra mediante masturbación, necesidad de empleo de lubricantes, dificultad para recoger la muestra en el centro sanitario, bloqueos, etc.
Además, se recomienda tener en cuenta:
- •
Los aspectos a verificar en la recepción de las muestras (tabla 2).
- •
Ítems a incluir en el cuestionario a realizar al paciente (tabla 3).
- •
Los criterios de rechazo de las muestras (tabla 4).
- •
Evitar la toma de los medicamentos listados en la tabla 5 que pueden influir en la eyaculación o en la calidad del semen.
Ninguno de los autores declara tener conflicto de intereses en la publicación de este artículo.
Ejemplo de instrucciones a seguir en la adecuada recogida de la muestra para la realización del espermiograma y recuperación de espermatozoides móviles diagnóstico
Cómo solicitar la cita.
Cuándo debe entregar la muestra.
Dónde debe entregar la muestra.
Datos de contacto del laboratorio.
- •
Periodo de abstinencia: antes de recoger la muestra calcule que hayan transcurrido 3 días desde la última eyaculación (no menos de 2 días ni más de 7 días). Esto implica no tener ninguna pérdida de semen por coito, masturbación, polución nocturna (eyaculación involuntaria) o cualquier otra circunstancia durante estos días. Si el periodo es menor o mayor la muestra no será válida para su estudio.
- •
Medidas higiénicas: antes de masturbarse debe orinar y lavarse las manos y los genitales, aclarándose bien para eliminar cualquier resto de jabón. No se debe aplicar ningún tipo de pomada. Es importante evitar una posible contaminación de la muestra.
- •
Obtención de la muestra: la obtención de semen se hará siempre por masturbación. Los preservativos no pueden usarse porque contienen lubricantes y espermicidas. El coitus interruptus es inaceptable debido a que la primera fracción, rica en espermatozoides, se puede perder fácilmente.
- •
Recogida de la muestra: para recoger la muestra utilice el frasco estéril de boca ancha con tapadera que le han entregado en la consulta o en el laboratorio. También puede adquirirse en oficinas de farmacia solicitando «frasco estéril de boca ancha». Asegúrese de que queda bien cerrado. La muestra debe ser completa (todo el volumen eyaculado). La muestra no será válida para estudio si se derrama o se pierde parte de la misma.
- •
Transporte al laboratorio: anote la hora de recogida de la muestra. Deberá entregarla en el laboratorio lo antes posible. Como máximo deben transcurrir 60minutos desde la obtención hasta el inicio del estudio, por lo que deberá transcurrir menos tiempo hasta la entrega en el laboratorio. Durante el transporte deberá llevar el frasco protegido de la luz (por ejemplo, envuelto en papel de aluminio) y evitar fluctuaciones de temperatura (por ejemplo, guardando el frasco en un bolsillo cerca del cuerpo).
Para los pacientes que vivan a más de 45minutos del laboratorio, tenemos una sala habilitada para recoger la muestra.
- •
Sea puntual. Si no pudiera acudir a su cita avísenos con antelación, otro paciente se lo agradecerá.
Cuándo debe entregar la muestra.
Dónde debe entregar la muestra.
Datos de contacto del laboratorio.
El éxito de la intervención de vasectomía se comprueba con al menos un análisis de semen. Después de operarse y antes de hacerse el primer análisis deben haber transcurrido un mínimo de 4 meses y haber tenido al menos 24 eyaculaciones. Si se realiza el análisis demasiado pronto se pueden encontrar espermatozoides. Algunos pacientes tardan más de un año en eliminar todos los espermatozoides del tracto urogenital.
- •
Periodo de abstinencia: antes de recoger la muestra calcule que hayan transcurrido 3 días desde la última eyaculación (no menos de 2 días, ni más de 7 días). Esto implica no tener ninguna pérdida de semen por coito, masturbación, polución nocturna (eyaculación involuntaria) o cualquier otra circunstancia durante estos días. Si el periodo es menor o mayor la muestra no será válida para su estudio.
- •
Medidas higiénicas: antes de masturbarse debe orinar y lavarse las manos y los genitales, aclarándose bien para eliminar cualquier resto de jabón. No se debe aplicar ningún tipo de pomada. Es importante evitar una posible contaminación de la muestra.
- •
Obtención de la muestra: la obtención de semen se hará siempre por masturbación. Los preservativos no pueden usarse porque contienen lubricantes y espermicidas. El coitus interruptus es inaceptable debido a que la primera fracción, rica en espermatozoides, se puede perder fácilmente.
- •
Recogida de la muestra: para recoger la muestra utilice el frasco estéril de boca ancha con tapadera que le han entregado en la consulta o en el laboratorio. También puede adquirirse en oficinas de farmacia solicitando «frasco estéril de boca ancha». Asegúrese de que queda bien cerrado. La muestra debe ser completa (todo el volumen eyaculado). La muestra no será válida para estudio si se derrama o se pierde parte de la misma.
- •
Transporte al laboratorio: anote la hora de recogida de la muestra. Deberá entregarla en el laboratorio lo antes posible. Como máximo deben transcurrir 60minutos desde la obtención hasta el inicio del estudio, por lo que deberá transcurrir menos tiempo hasta la entrega en el laboratorio. Durante el transporte deberá llevar el frasco protegido de la luz (por ejemplo, envuelto en papel de aluminio) y evitar fluctuaciones de temperatura (por ejemplo, guardando el frasco en un bolsillo cerca del cuerpo).
Para los pacientes que vivan a más de 45minutos del laboratorio tenemos una sala habilitada para recoger la muestra.
- •
Sea puntual. Si no pudiera acudir a su cita avísenos con antelación, otro paciente se lo agradecerá.
Cómo solicitar la cita.
Cuándo debe entregar la muestra.
Dónde debe entregar la muestra.
Datos de contacto del laboratorio.
1. Periodo de abstinencia: antes de la cita en el laboratorio calcule que hayan transcurrido 3 días desde el último orgasmo (no menos de 2 días ni más de 7 días).
2. Preparación:
- •
Tome 2 cucharadas de bicarbonato disueltas en un vaso de agua la noche previa a la cita del análisis.
- •
Tome 2 cucharadas de bicarbonato disueltas en un vaso de agua cuando despierte.
- •
Recoja la primera orina de la mañana en el frasco de boca ancha que le hemos entregado, ciérrelo bien y tráigalo al laboratorio. Comprobaremos el pH de la muestra. Si la orina no tiene pH básico debe seguir tomando bicarbonato.
3. Recogida de las muestras: las muestras se obtendrán en una sala habilitada próxima al laboratorio. En el laboratorio le entregaremos varios frascos numerados. Debe abrirlos antes de comenzar con el siguiente paso.
4. Obtención de la muestra:
- •
Debe lavarse las manos y los genitales, aclarándose bien para eliminar cualquier resto de jabón. No se debe aplicar ningún tipo de pomada. Es importante evitar una posible contaminación de la muestra.
- •
Primero debe masturbarse hasta alcanzar el orgasmo. Si eyacula, recoja la totalidad del eyaculado en el frasco número 1.
- •
Tanto si ha eyaculado como si no ha eyaculado orine en los otros frascos (número 2). Es importante que recoja toda la orina.
- •
Entregue todos los frascos en el laboratorio. Aunque el primer frasco (para el semen) no contenga muestra entréguelo también.