La neurosífilis es una presentación clínica de la sífilis y puede suceder en estadios tempranos o tardíos de la infección. Aunque el tratamiento específico para todas las formas clínicas de la sífilis existe desde hace mucho tiempo, los estadios avanzados de la enfermedad aún son prevalentes, con las secuelas neurológicas irreversibles que ocasionan. Este artículo revisa la evidencia actual, los métodos diagnósticos y el tratamiento específico para la sífilis terciaria
Neurosyphilis is the clinical manifestation of syphilis that can arise during either the early or late stages of infection. Even though dedicated treatment for all clinical forms of syphilis has been available for many years, the advanced stages of the disease are still prevalent, with irreversible sequelae. This article reviews the current evidence, diagnostic methods and specific treatment for tertiary syphilis
La sífilis es una infección ocasionada por la espiroqueta Treponema pallidum y su principal forma de transmisión es la sexual. Hoy, pese a que existe un tratamiento eficaz, económico y de fácil acceso, continúa siendo un problema de salud pública mundial debido a las altas tasas de infección que se registran año a año1–3.
Colombia tiene regiones en donde la sífilis es endémica y esto se ve reflejado, por ejemplo, en la alta incidencia de sífilis en el embarazo, con reportes en 2013 de 2,43 casos de sífilis congénita cada 1.000 nacidos vivos4. Como en Colombia la neurosífilis no es un diagnóstico de notificación obligatoria, no se tienen datos estadísticos sobre esta en el país.
En cuanto a la neurosífilis, diferentes estudios retrospectivos han aportado datos de su magnitud entre diferentes grupos demográficos de pacientes. En Los Ángeles, California, entre 2001 y 2004 se encontró que la tasa de neurosífilis entre los pacientes con sífilis temprana era del 2,1% de los infectados por el VIH y el 0,6% de los que no5, y en Países Bajos se mostró que, entre 1999 y 2010, la incidencia anual de neurosífilis fue de 0,7/100.000 varones y 0,2/100.000 mujeres, con medianas de edad de 47 y 54 años respectivamente6.
La neurosífilis se describía en la era preantibiótica como una entidad clínica común, que afectaba a un 25-35% de los pacientes con sífilis7. No obstante y a pesar de una importante disminución de casos tras la aparición de la penicilina, en el mundo se observó un aumento en la ocurrencia y la presentación de la neurosífilis a partir de las décadas de los ochenta y los noventa, en asociación con infección por el VIH y bajo recuento de linfocitos T CD4+8,9.
Patogenia de la neuroinfecciónAlgunos trabajos documentan cepas específicas de T. pallidum que se asocian de manera más clara con la aparición de neurosífilis10.
Se describe que la neuroinfección por T. pallidum se inicia tras la invasión del líquido cefalorraquídeo (LCR) por este, lo cual puede ocurrir en estadios tempranos de la infección y posiblemente horas después de la infección inicial; se ha identificado la espiroqueta por métodos de reacción en cadena de la polimerasa (PCR) hasta en un 25% de las muestras de LCR de grupos de pacientes con sífilis temprana. Algunos autores sostienen que la invasión del sistema nervioso central (SNC) ocurre casi de manera universal a todos los infectados por T. pallidum11, por lo que no se debería considerarlo una manifestación exclusiva de la sífilis tardía.
A pesar de que se han descrito anormalidades comunes en el estudio citoquímico y serológico del LCR de pacientes con neurosífilis, tales como pleocitosis, concentración elevada de proteínas o el Venereal Disease Research Laboratory test (VDRL) reactivo, no existe una combinación precisa de hallazgos que la indiquen de manera determinante10–13.
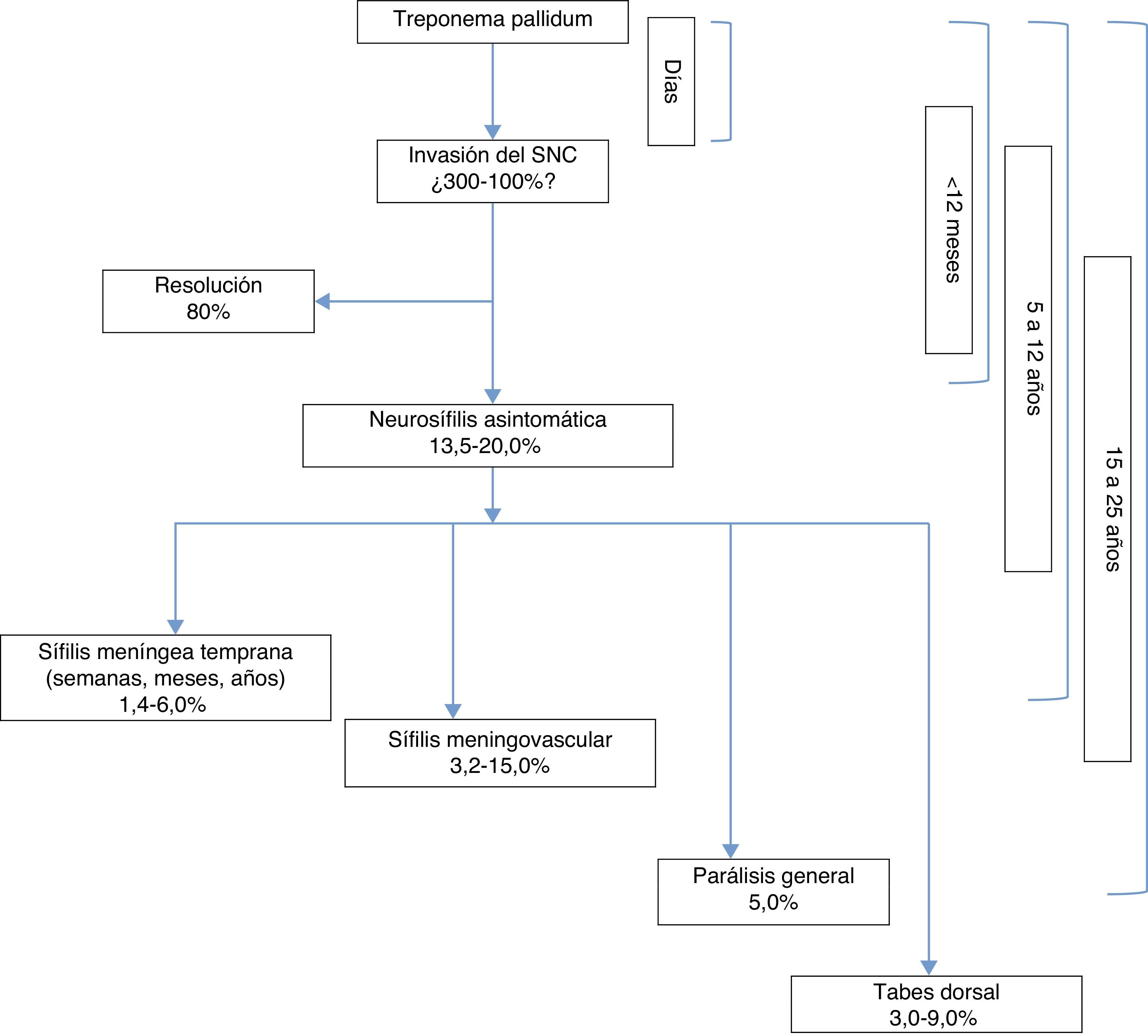
Llama la atención que, pese a la alta frecuencia de invasión del SNC por T. pallidum, hasta un 25% de los pacientes sufre una neurosífilis persistente y apenas clínicamente reconocible, llamada neurosífilis asintomática, mientras que en el resto la neuroinfección parece controlada. Los resultados de estudios en primates no humanos muestran, en relación con la neuroinfección controlada, el incremento del número de linfocitos T CD4+ y de interferón gamma producido por estos en el LCR durante el periodo de eliminación bacteriana, es decir, evidencia de respuesta inmunitaria tipo 111,13. La figura 1 esquematiza el curso clínico de la enfermedad.
La neurosífilis se puede clasificar en formas tempranas y tardías. Las formas tempranas involucran el líquido cefalorraquídeo, las meninges y la vasculatura. Las formas tardías involucran el parénquima de la médula y el encéfalo. Modificado de Ghanem12.
La neurosífilis se puede clasificar entre formas tempranas (sífilis asintomática, meningitis sintomática, sífilis ocular, otosífilis y sífilis meningovascular) y tardías (paresia generalizada y tabes dorsal). Las formas tempranas de la neurosífilis ocurren los primeros meses y años después de la primera infección y afectan a las meninges y los vasos sanguíneos; no obstante, con el transcurrir de los años también se afectan el cerebro y el parénquima de la médula espinal11.
En la era previa al uso de la penicilina, aproximadamente el 20% de las personas con neurosífilis asintomática sufrían alguna de las formas sintomáticas de la enfermedad. Tras el descubrimiento de la penicilina y actualmente, las formas tempranas de la neurosífilis son más comunes que las tardías14.
Neurosífilis tempranaNeurosífilis asintomáticaEstos pacientes se presentan sin signos o síntomas de enfermedad del SNC, pero puede haber hallazgos propios periféricos de la infección por T. pallidum.
El diagnóstico se hace con base en el estudio del LCR, en el que se puede encontrar pleocitosis con un recuentos de linfocitos < 100/μl, concentración de proteínas elevadas pero < 100 mg/dl, un VDRL reactivo o una combinación de estos.
No obstante y a pesar de lo anterior, en los pacientes con sospecha de neurosífilis asintomática no infectados por el VIH, los recuentos de linfocitos en LCR > 5/μl o una concentración de proteínas > 45 mg/dl es congruente y muy indicativo del diagnóstico.
La infección por el VIH per se puede hacer difícil la interpretación del análisis citoquímico del LCR con VDRL no reactivo, por los cambios propios en la bioquímica y la citología del LCR que genera la infección por el virus.
Los pacientes con neurosífilis asintomática, independientemente de la combinación de los hallazgos previamente mencionados, deben ser tratados con el esquema una neurosífilis para evitar la progresión a sintomática.
Meningitis sintomáticaEs más frecuente en el primer año de infección por la espiroqueta, pero puede ocurrir después. De manera similar a la neurosífilis asintomática, puede haber hallazgos propios de la infección sistémica.
Los síntomas más frecuentemente referidos son cefalea, confusión, náuseas, vómitos y rigidez de nuca. Asimismo se puede afectar la agudeza visual debido a uveítis, vitritis, retinitis o neuropatía óptica, y neuropatías craneales facial y vestibulococlear.
También se puede encontrar síntomas y signos correspondientes a hidrocefalia y arteritis de pequeños, medianos y grandes vasos en el encéfalo y la médula espinal, secundarias al fenómeno inflamatorio meníngeo. Asimismo la inflamación meníngea local podría ocasionar una leptomeningitis difusa o gomas sifilíticas en las meninges, que generan efecto de masa. Y todo lo anterior puede generar convulsiones.
En la médula espinal, además, puede observarse meningomielitis o paquimeningitis hiperplásica con polirradiculopatía. Los síntomas incluyen dolor en la espalda, pérdida de sensibilidad, incontinencia, debilidad de las extremidades inferiores o atrofia muscular.
El estudio citoquímico del LCR se ve más afectado en esta presentación que en la forma asintomática de neuroinfección, con recuentos de linfocitos entre 200 y 400/μl, concentración de proteínas entre 100 y 200 mg/dl y VDRL casi siempre reactivo.
Sífilis meningovascularPuede afectar a cualquier vaso subaracnoideo y resultar en trombosis, isquemia o infartos cerebrales. Puede presentarse desde el primer mes hasta 7 años después de la primera infección. Debe ser un diagnóstico diferencial en el escenario de cualquier infarto cerebral en un paciente joven.
Diferentes expertos coinciden en que esta forma clínica de la enfermedad se caracteriza por pródromos como cefalea, mareo y cambios de personalidad en las semanas o días previos a la isquemia o el infarto cerebral.
El estudio citoquímico del LCR se ve menos afectado en esta presentación que en otras formas de neuroinfección por T. pallidum, con menores recuentos de linfocitos y concentración de proteínas; el VDRL suele ser reactivo, aunque no siempre.
Neurosífilis tardíaEn la época previa a la penicilina, era común encontrar demencia sifilítica, más frecuente entre los 35 y los 50 años de edad, y se observaba de 5 a 25 años tras la sífilis primaria.
Se considera que las manifestaciones clínicas de la neurosífilis pueden reproducir las manifestaciones de cualquier enfermedad psiquiátrica; en etapas tempranas se identifican pérdidas de la memoria y cambios en el comportamiento, y con el tiempo se puede desarrollar manía, depresión o psicosis. Luego, la mayoría de los pacientes simplemente sufren empeoramiento de los déficit de memoria y alteraciones del juicio que progresan a demencia franca15,16.
En etapas terminales puede haber negativismo, incontinencia y mayor riesgo de síndromes convulsivos; en el examen físico son frecuentes las anomalías pupilares. Además puede haber hipotonía facial, temblores de intención de la cara, la lengua y las manos, y anormalidades en los reflejos osteotendinosos15,16.
Inicialmente en el curso de la enfermedad, aparte de las alteraciones de la cognición, como se ha escrito, el resto del examen neurológico puede ser normal. Los casos de demencia sifilítica reportados en la era moderna se caracterizan por el deterioro cognitivo rápidamente progresivo con o sin rasgos psiquiátricos15.
Se considera formas terciarias de la neurosífilis la paresia generalizada y el tabes dorsal.
Paresia generalizadaEs una demencia progresiva que aparece generalmente a los 10-25 años de la infección inicial, pero puede ocurrir tan pronto como 2 años después de esta.
En 1897 Kraft-Ebbing demostró la asociación entre la sífilis y la paresia general, y en 1945 se hizo este diagnóstico a un 5-10% de todos los ingresos de un conjunto de hospitales psiquiátricos15.
En estadios tempranos, esta forma de enfermedad se asocia con olvidos y cambios de la personalidad, que progresan a alteraciones mnésicas, alteraciones del juicio y demencia grave.
Algunos pacientes cursan con síntomas mentales como depresión, manía o psicosis16. Se puede encontrar anormalidades como disartria, hipotonía facial y en extremidades, temblor intencional en la cara, la lengua, las manos y las pupilas de Argyll-Robertson15.
En el estudio del LCR se evidencia un alto recuento de linfocitos (25-75/μl), la concentración de proteínas está en 50-100mg/dl y el VRDL en el LCR es reactivo en todos los pacientes.
Tabes dorsalEs una manifestación tardía que consiste en alteración y deterioro de los cordones posteriores y las raíces dorsales de la médula espinal. El periodo latente entre la infección y la presentación de los síntomas puede estar alrededor de los 20 años, pero se ha visto en ocasiones con presentación a los 3 años de la infección temprana.
Los síntomas más frecuentes son ataxia sensorial y dolores lancinantes que progresan a episodios de dolor súbitos, breves e intensos que afectan a las extremidades, la espalda y la cara y pueden durar minutos o incluso días17.
Menos común es la aparición de parestesias, dolores abdominales epigástricos intensos, náuseas y vómitos. También se puede evidenciar disfunción vesical, con retención urinaria e incontinencia en estadios tempranos. Las alteraciones pupilares son el síntoma más común en los pacientes con tabes dorsal, y se puede encontrar pupilas de Argyll-Robertson en un 31-50% de los casos16. Otros signos encontrados son ausencia de reflejos en las extremidades inferiores, alteraciones en la sensación de vibración y posición y, con menos frecuenci, alteraciones del tacto, sensación dolorosa, ataxia sensorial y atrofia óptica.
El examen del LCR puede ser normal o presentar una ligera pleocitosis linfocitaria y aumento de proteínas (45-75 mg/dl). En un 25% de los casos, el VRDL es no reactivo.
Zheng et al.16 reportaron una serie retrospectiva de 116 pacientes con demencia sifilítica. Todos tenía pruebas treponémicas y no treponémicas reactivas en suero, el 48% tenía linfocitos en el LCR (el punto de corte no se definió), y el 86% tenía pruebas no treponémicas reactivas en LCR. Las edades oscilaban entre los 30 y los 76 años. Los hallazgos más comunes fueron demencia, cambios de personalidad, comportamiento anormal y problemas emocionales. El 39% de los pacientes tenían delirios y el 16%, convulsiones. Es de destacar que la neurosífilis no se sospechó inicialmente en el 36% de los pacientes, con un retraso diagnóstico entre 1 y 24 meses16.
En un grupo de 12 pacientes diagnosticados de neurosífilis en el Hospital Psiquiátrico Universitario del Valle (Cali, Colombia), en el periodo entre 1994 y 2016, se encontró que un 84% de los casos correspondieron a varones y el promedio de edad del grupo era 54 años, pero el de los varones era 46,7 años. El 50% había alcanzado al menos la educación media y el 67% no tenía diagnóstico de otro trastorno mental.
DiagnósticoPara la mayoría de los pacientes, el diagnóstico presuntivo de sífilis se realiza mediante pruebas serológicas de muestras de sangre, ya que las herramientas necesarias para detectar directamente T. pallidum no siempre están disponibles en la mayoría de los escenarios.
Existen dos tipos de pruebas serológicas para el diagnóstico presuntivo de sífilis: las pruebas no treponémicas y las treponémicas. En la práctica clínica, el uso de ambas es necesario, dado el alto número de falsos positivos que una prueba serológica única puede significar.
La pruebas no treponémicas incluyen la prueba rápida de reagina plasmática (RPR), el VDRL y el rojo de toluidina sin calefacción en prueba de suero (TRUST). Estos estudios miden los anticuerpos IgG e IgM del antígeno cardiolipina-lecitina-colesterol. Los resultados se expresan en general como un título, y con títulos más altos se refleja una mayor actividad de la enfermedad.
Factores y condiciones, como el embarazo, la edad avanzada, las enfermedades autoinmunitarias o el uso de drogas inyectables, pueden dar lugar a falsos positivos en el resultado de pruebas no treponémicas.
Las pruebas treponémicas son la fluorescent treponemal antibody absorption (FTA-ABS) y la Treponema pallidum particle agglutination (TPPA), así como una variedad de enzimoinmunoanálisis automatizados (EIA) e inmunoanálisis quimioluminiscentes (CIA).
Un enfoque general sobre el uso y la interpretación de pruebas no treponémicas y treponémicas para sífilis se muestra en la tabla 1.
Resultado e interpretación de las pruebas serológicas para sífilis
| Resultado | Interpretación |
|---|---|
| No treponémica (-) Treponémica (-) | Se puede excluir la infección a excepción de la infección reciente. Si hay sospecha, repetir las pruebas de 15-21 días |
| No treponémica (+) Treponémica (+) | Es una infección por sífilis. Si se confirma que se había diagnosticado y tratado correctamente, puede corresponder a cicatriz serológica, por lo que se debe hacer seguimiento cuantitativo con VDRL |
| No treponémica (-) Treponémica (+) | Reacción treponémica específica (99,5-100%). Refleja la persistencia normal de anticuerpos contra el treponema, y no infección activa |
| No treponémica (+) Treponémica (-) | Reacción cardiolipínica no muy específica que puede deberse a otras condiciones como la gestación; generalmente se trata de un falso positivo. Se confirma con el uso de otras pruebas treponémicas |
Cuando las pruebas treponémicas y no treponémicas son reactivas, la confirmación de neurosífilis temprana se facilita. Sin embargo, las pruebas no treponémicas pueden ser no reactivas en el tabes dorsal, por lo que en estas formas tardías de neurosífilis se debe realizar pruebas serológicas treponémicas. Estos tests confirman que el paciente tuvo sífilis alguna vez y que está en riesgo de neurosífilis. Los pacientes con pruebas treponémicas no reactivas no ameritan evaluación para neuroinfección por T. Pallidum a menos que tengan síntomas neurológicos que apunten al diagnóstico.
Se debe considerar18,19 la realización de una punción lumbar en:
- •
Pacientes con historia desconocida o conocida de sífilis y síntomas neurológicos y oculares que podrían ser causados por sífilis.
- •
Pacientes con infección por el VIH y sífilis en cualquier estadio, aun en ausencia de síntomas neurológicos u oculares.
- •
Evidencia de sífilis terciaria activa que afecta a otras partes del cuerpo.
- •
Fracaso de determinado tratamiento según el control con pruebas no treponémicas, en cualquier estadio de la infección.
- •
Pacientes con prueba treponémica positiva y signos o síntomas de alteraciones neurológicas, incluidos los síntomas mentales.
El diagnóstico de neurosífilis comúnmente se confirma con un VDRL reactivo en LCR18, pero un resultado no reactivo no descarta el diagnóstico y puede presentarse como un falso negativo en el 70% de los pacientes con neurosífilis19.
En pacientes con sospecha de neurosífilis sin infección por el VIH y con VDRL en LCR no reactivo, un recuento de linfocitos > 5/μl o una concentración de proteínas > 45 mg/dl son diagnósticos de neuroinfección.
Como se describió anteriormente, si el paciente tiene coinfección por el VIH, es difícil establecer o negar el diagnóstico de neurosífilis aun si el VDRL en LCR es no reactivo y hay una pleocitosis moderada, por los cambios que la infección por el VIH genera en el LCR.
ImagenologíaA pesar de que hasta 2 tercios de los pacientes con neurosífilis tienen reportes normales en la tomografía computarizada, la resonancia magnética o la angiografía20, la neurosífilis puede tener una amplia variedad de presentaciones en los diferentes tipos de ayudas imagenológicas cerebrales21–23.
Los cambios imagenológicos que tienen que ver con la neurosífilis son particularmente variables, pero por su mayor frecuencia destacan la atrofia encefálica leve-moderada, los infartos cerebrales típicamente lacunares o en el territorio de la arteria cerebral media, las lesiones inespecíficas en la sustancia blanca y la prominencia periventricular de esta, la hidrocefalia, las gomas cerebrales, la esclerosis mesial-temporal, el realce leptomeníngeo, los granulomas leptomeníngeos, la periostitis orbitaria gomatosa y la periostitis que afecta a la cápsula óptica20–23.
No obstante, algunos autores han planteado la posibilidad de que muchos de los hallazgos anteriormente mencionados pueden deberse a posibles coinfecciones, como se puede observar en pacientes con infección por el VIH, y siempre se debe tener en cuenta que existe una amplia gama de diagnósticos diferenciales una vez se encuentran lesiones de cualquier tipo en las imágenes cerebrales de ciertos grupos de pacientes22.
Asimismo, en pacientes sin infección por el VIH pueden darse diagnósticos como encefalitis por el virus del herpes simple, esclerosis mesial temporal, leucoaraiosis, hidrocefalia de presión normal y glioblastoma multiforme21.
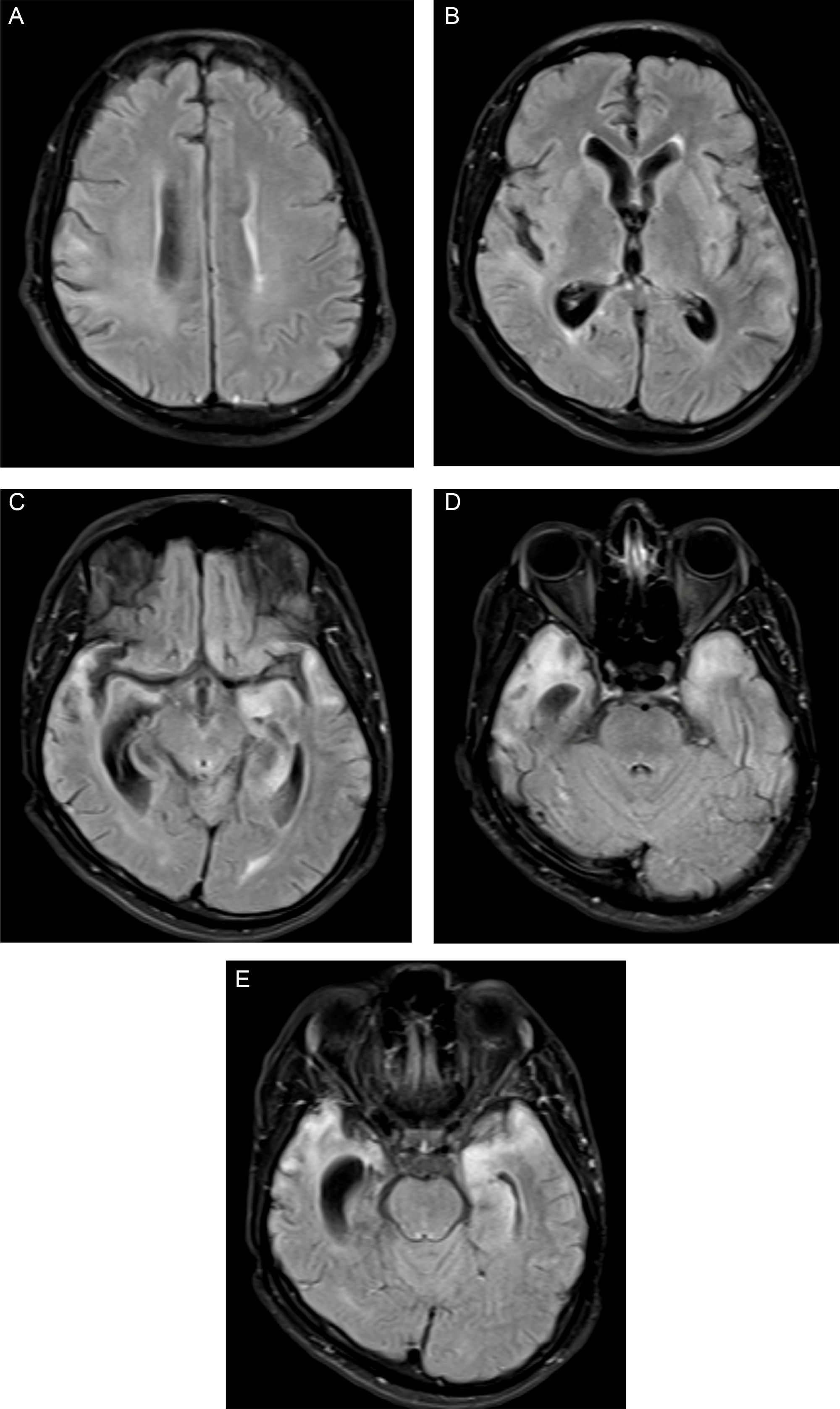
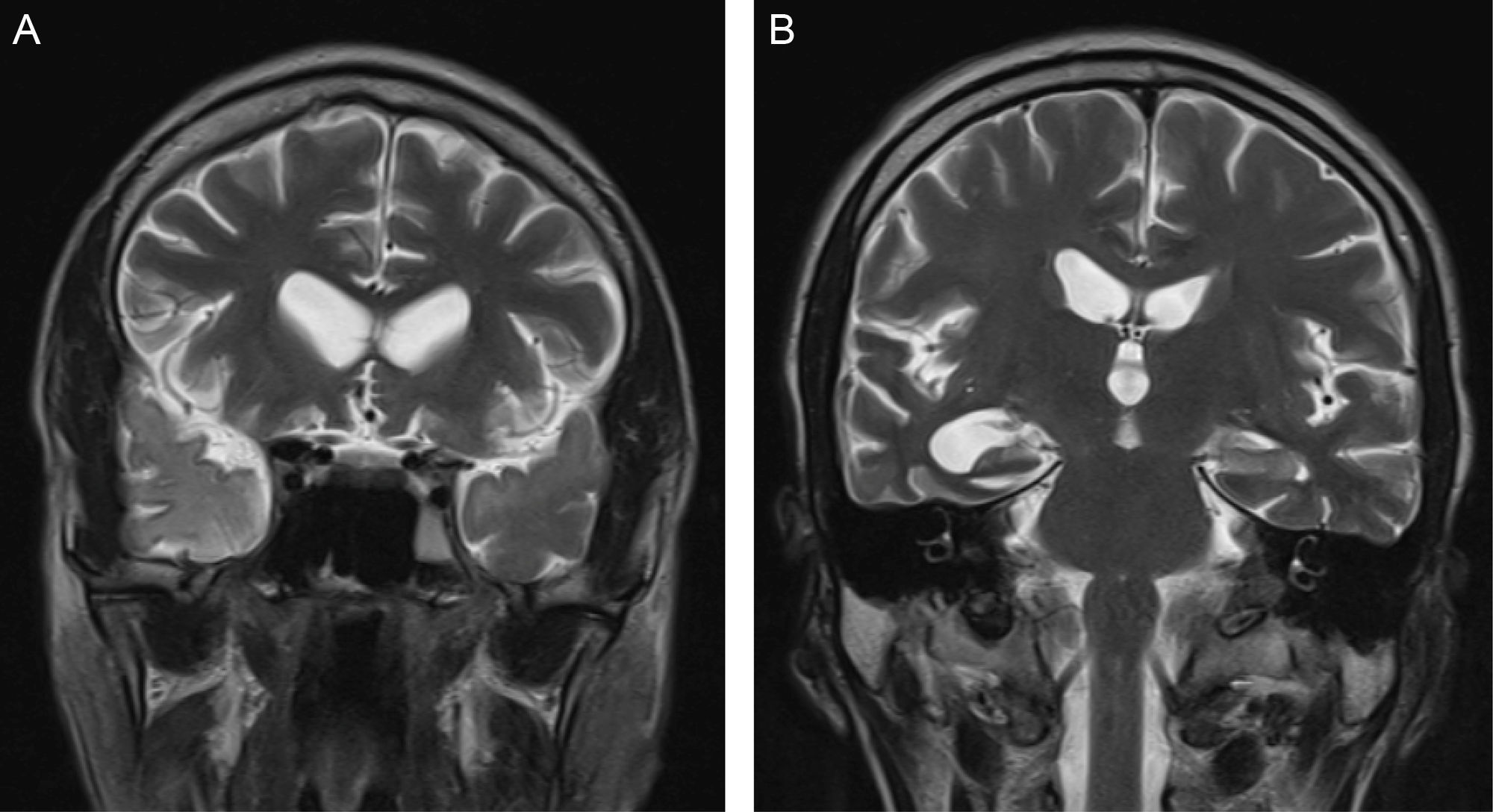
En las figuras 2–3 se presentan imágenes correspondientes a casos tratados en el Hospital Psiquiátrico Universitario del Valle en los cuales se llegó al diagnóstico de neurosífilis.
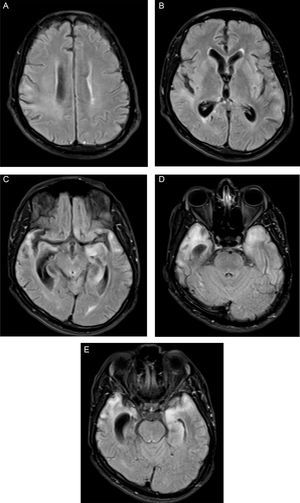
Imágenes axiales de resonancia magnética en secuencias FLAIR a diferentes niveles del encéfalo. A y B: se observan áreas de hiperintensidad de señal en la sustancia blanca de la corona radiada y a nivel subcortical, de predominio en el hemisferio cerebral derecho, así como prominencia del sistema ventricular por pérdida de volumen del parénquima. C-E: extensa afección de los lóbulos temporales, que son hiperintensos y atróficos, más evidentemente en el lado derecho, y generan dilatación compensatoria del cuerno temporal del ventrículo lateral (imágenes aportadas por Ana Lorena Abello, del Hospital Universitario del Valle Evaristo García ESE).
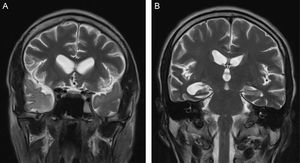
Imágenes coronales de resonancia magnética en secuencias T2, que muestran la especial afección de los lóbulos temporales. A: hiperintensidad de señal anormal en el polo temporal derecho (flechas azules). B: dilatación del cuerno temporal derecho y afección de la región mesial temporal izquierda, que es anormalmente hiperintensa (flecha negra) (imágenes aportadas por Ana Lorena Abello, del Hospital Universitario del Valle Evaristo García ESE).
Los pacientes con neurosífilis deben recibir terapia antitreponémica endovenosa. Se ha demostrado que la administración intramuscular de diferentes tipos de penicilina no logra por sí sola concentraciones treponemicidas en el LCR24. Además, se han publicado reportes de casos en los que en ciertos grupos de pacientes tratados con penicilina intramuscular de manera adecuada se ha diagnosticado neurosífilis después25.
También deben recibir terapia antitreponémica endovenosa los pacientes con alta sospecha diagnóstica de infección del SNC por T. pallidum (p. ej., pacientes con cuadro y síntomas compatibles con la enfermedad, con una prueba serológica en suero positiva para sífilis y en cuya citoquímica de LCR se evidencie pleocitosis), incluso si las pruebas no treponémicas realizadas en LCR son negativas, teniendo en cuenta el alto porcentaje de falsos negativos que se obtienen de estas en pacientes con neurosífilis.
En pacientes con alergias documentadas a la penicilina o a betalactámicos, debe asegurarse la desensibilización a estos fármacos, de modo que puedan recibir el tratamiento con penicilina G endovenosa convencional o tratamiento endovenoso con ceftriaxona (a dosis de 2 g/día de 10 a 14 días), en vez de esquemas alternativos de los que no se ha comprobado utilidad en el tratamiento de la neurosífilis18.
Según la guía para el tratamiento de la neurosífilis de los Centers of Disease Control and Prevention (CDC), los regímenes de tratamiento indicados para esta (pese a que no hay evidencia de ensayos clínicos controlados que lo respalde) son:
- •
Como primera línea, la administración intravenosa de penicilina G cristalina acuosa en dosis de 18-24×106 U/día, administradas a 3-4×106 U cada 4 h, o la administración de 24×106 U/día en infusión continua durante 10-14 días.
- •
la administración intramuscular de penicilina G procaínica en dosis de 2,4×106 U/día, más probenecid oral 500 mg 4 veces al día, ambas durante 10-14 días.
Ante la alergia a la penicilina, otras alternativas incluyen la administración endovenosa o intramuscular de ceftriaxona 2 g/día y doxiciclina oral a dosis altas (200 mg 2 veces/día durante 21-28 días). La tabla 2 muestra un resumen.
Líneas de tratamiento farmacológico para la neurosífilis
| Fármaco | Dosis y posología |
|---|---|
| Penicilina G cristalina acuosa | Dosis: 18-24×106 U/día Administrar: 3-4×106 U cada 4 h i.v. o 24×106 U/día en infusión continua durante 10-14 días |
| Penicilina G procaínica Probenecid | Dosis: 2,4×106 U/día 2g/día Administrar: 2,4 ×106 U/día en una sola aplicación i.m. y probenecid oral 500 mg 4 veces/día durante 10-14 días |
| Ceftriaxona | Dosis: 2 g/día Administrar: 2 g/día, i.v. o i.m., durante 10-14 días |
| Doxiciclina | Dosis: 400 mg/día Administrar: 200 mg/12 h durante 21-28 días |
i.m.: intramuscular; i.v.: intravenoso.
Los autores declaran no tener ningún conflicto de intereses.