La incidencia de infección en cirugía de columna puede ser hasta el 12%; con el uso de vancomicina tópica, previo al cierre, se ha logrado disminuir el riesgo de esta condición. El objetivo del estudio es determinar la incidencia de infección en cirugía de columna a quienes se aplicó vancomicina tópica previo al cierre de incisión en una institución de alta complejidad
Materiales y MétodosSe realizó un estudio observacional de tipo cohorte retrospectiva. Se incluyeron pacientes intervenidos en cirugía de columna con aplicación de vancomicina tópica previa al cierre entre el 2014 al 2018 en una institución de tercer nivel. Los pacientes fueron seguidos desde el momento de la cirugía hasta 3 meses postquirúrgico Se recolectó información sobre edad, comobilidades, índice masa corporal, tiempo quirúrgico, sangrado intraoperatorio, complicaciones, uso de drenajes.
ResultadosSe incluyeron 130 pacientes, 81 mujeres y 49 hombres con una edad pomedio de 64 años. 95.4% se les realizó vía posterior con laminectomía, artrodesis e instrumentación. El tiempo promedio fue de 207 minutos, con un sangrado de 400mL. Solo un paciente presentó ruptura de duramadre. Cinco pacientes presentaron infección del sitio operatorio para una incidencia de 3.8% (IC95% 1.5% - 8.9%).
DiscusiónEl uso de vancomicina parece reducir el riesgo de infección en cirugía de columna según la incidencia de esta infección reportada en la literatura; sin embargo, hacen falta estudios prospectivos o ensayos clínicos controlados que prueben las dosis ideales de esta terapéutica.
NIVEL DE EVIDENCIA: III
The incidence of infection in spine surgery can be up to 12%; With the use of topical vancomycin, prior to closure, the risk of this condition has been reduced. The aim of the study is to determine the incidence of infection in spinal surgery to which topical vancomycin was applied prior to the closure of an incision in a highly complex institution.
MethodsAn observational retrospective cohort study was conducted. Patients undergoing spinal surgery with application of topical vancomycin prior to closure between 2014 and 2018 in a third-level institution were included. The patients were followed from the moment of surgery until 3 months post-surgery. Information was collected on age, comorbilities, body mass index, surgical time, intraoperative bleeding, complications, use of drainages.
Results130 patients were included, 81 women and 49 men with an average age of 64 years. 95.4% were performed posteriorly with laminectomy, arthrodesis and instrumentation. The average time was 207minutes, with a bleeding of 400mL. Only one patient presented a dura mater rupture. Five patients presented surgical site infection for an incidence of 3.8% (95% CI 1.5% - 8.9%).
DiscussionThe use of vancomycin seems to reduce the risk of infection in spinal surgery according to the incidence of this infection reported in the literature; however, prospective studies or controlled clinical trials are needed to prove the ideal doses of this therapy.
EVIDENCE LEVEL: III
Según el Centers for Disease Control (CDC), las Infecciones de Sitio Operatorio (ISO) se definen como la infección que ocurre en la incisión quirúrgica o cerca de ella durante los primeros 30 días, o hasta un año, si se ha dejado un implante1. Las ISO son tema importante de salud, ya que complican cerca del 2 al 5% de todas las cirugías y representan un alto costo para el sistema; en 1996 se estimaba un costo de $100.000 dólares, y cada episodio de infección aumentaba el costo en salud en $4.067 comparado con los casos no complicados2. Además, la presencia de infecciones interfiere con la recuperación del paciente así como con el resultado final de la cirugía. Cahill et al, en un estudio en población pediátrica reportó que los pacientes infectados presentaban una incidencia del 25% de pseudoatrosis, secuelas neurológicas y posteriores deformidades, así como un aumento en la mortalidad3,4. En cirugía de columna la tasa de infección varía del 0.7% al 11.9% y esto varía de acuerdo con el tipo de procedimiento, indicación, así como el uso de instrumentación5,6. Así mismo, se han descrito algunos factores de riesgo para ISO en cirugía de columna, como la edad mayor de 65 años, diabetes mellitus (RR=2.22, CI 95% 1.38, 3.60; p=0.001), tabaquismo y obesidad mayor a IMC de 35 (RR=2.36, IC 95%:1.47, 3.80:p=0.000), así como el tiempo quirúrgico prolongado (>5 horas) (OR 2.8 IC 95%:1.296-6.268)7,8.
Varias estrategias se han prouesto para diminuir el riesgo de infección de sitio operatorio. El uso de Vancomicina tópica ha ganado interés para el uso en cirugía de columna por su bajo costo, disponibilidad y uso fácil9, además de ser segura por su pobre absorción sistémica. La aplicación de vancomicina tópica varía de acuerdo con el tipo de cirugía y su duración, se han descrito estudios con aplicación de 1 gramos versus 2 gramos, pero esto no ha mostrado ninguna diferencia. La guía del segundo Consenso Internacional sobre las infecciones musculoesqueléticas (ICM por sus siglas en inglés) recomienda el uso de vancomicina basándose en diferentes estudios reunidos en una revisión sistemática realizada por Xie et al. en donde revisaron 19 estudios cohorte retrospectivos y 1 estudio prospectivo, con resultados a favor del uso de la vancomicina, con un riesgo de 2.83 veces más riesgo de infección para el grupo sin vancomicina (IC 95%: 2.03–3.95), I2=32.2%, P=0.08310.
En Colombia, no se dispone de literatura que hable sobre la incidencia de infecciones del sitio operatorio en pacientes a quienes se les aplicó esta terapéutica. Por tanto, el objetivo de este estudio es determinar la incidencia de ISO en pacientes llevados a cirugía de columna en quienes se aplicó vancomicina entre enero 2014 a enero 2018 en una institución de alta complejidad.
Materiales y métodosSe realizó un estudio observacional de tipo cohorte única y retrospectiva en pacientes que fueron llevados a cirugía de columna y se les aplicó vancomicina tópica previo al cierre, entre enero 2014 a enero 2018 en una institución de tercer nivel.
El seguimiento inició al finalizar el procedimiento quirúrgico y continuó hasta los tres meses postoperatorios. Se definió ISO (desenlace principal) como la presencia de drenaje purulento, dolor intenso, enrojecimiento por la herida qurirúrgica que ocurría hasta 30 días o un año si existiese implantes. Además, con niveles elevados de Proteína C reactiva la cual se considera la prueba más sensible, que se encuentra elevada en más del 98% de los casos reportados11.
Se incluyeron todos los pacientes mayores de 18 años, con cirugía de columna electiva, por trauma o para manejo de patología oncológica, con instrumentación (cervical, dorsal o lumbosacra) y operados en la institución por el grupo de columna de Ortopedia y Traumatología de la institución y por el mismo cirujano, de forma consecutiva y a conveniencia. Se excluyeron pacientes con re-intervención al primer mes de cirugía.
En todos los casos se recolectó información sobre datos demográficos (edad y sexo), presencia de comorbilidades como diabetes, hipertensión arterial e hipotiroidismo; información clínica sobre peso, talla e Índice de Masa Corporal (IMC) y gramos usados de vancomicina tópica; información del procedimiento en relación al volumen de sangrado calculado por medio de la estimación de la pérdida sanguínea según consenso del personal de la sala de operaciones (estimación visual y contabilizando el recolector/compresas), tiempo quirúrgico en minutos, abordaje anterior o posterior, instrumentación y localización de segmento a operar, complicaciones intra y postoperatorias, presencia de ISO y patógeno aislado en caso de infección.
Los pacientes fueron identificados a partir de los registros de programación de cirugía (en caso de programados) y las descripciones quirúrgicas de los pacientes con procedimiento de urgencia con los siguientes códigos: 810812 artrodesis posterolateral e intercorporal (PLIF), artrodesis transforaminal e intercorporal (TLIF) de columna vertebral con instrumentación; 793952 reducción abierta de fractura de columna torácica, lumbar o sacra) vía posterior o posterolateral con instrumentación simple; corrección de escoliosis vía anterior y posterior. De los pacientes seleccionados, se revisaron las historias clínicas electrónicas con el fin de documentar las variables de interés.
Por protocolo institucional, todos los pacientes recibieron antibiótico profiláctico sistémico (cefazolina 1 gramo IV o en caso de presentar alergia documentada, clindamicina 600mg IV) antes de realzar incisión y cada 8 horas hasta completar tres dosis. A su vez, la preparación del campo estéril fue con jabón clorhexidina y solución clorhexina y campo de IOBAN. Previo al cierre, de acuerdo al tiempo estimado de cirugía y tamaño de incisión, se les colocó 1 o 2 gramos de vancomicina tópica sobre la fascia.
Se realizó un análsis descriptivo de la información recolectada. Las variables cualitativas se reportarán como frecuencias absolutas y relativas. Las variables cuantitativas se presentan a través de medidas de tendencia central y dispersión. La normalidad de estas variables se evaluó con el test de Shapiro-Wilks. La incidencia de ISO se reporta como proporción en conjunto con Intervalo de Confianza del 95% (IC95%). El estudio fue aprobado por el Comité de Ética en Investigación de la Fundación Universitaria Sanitas.
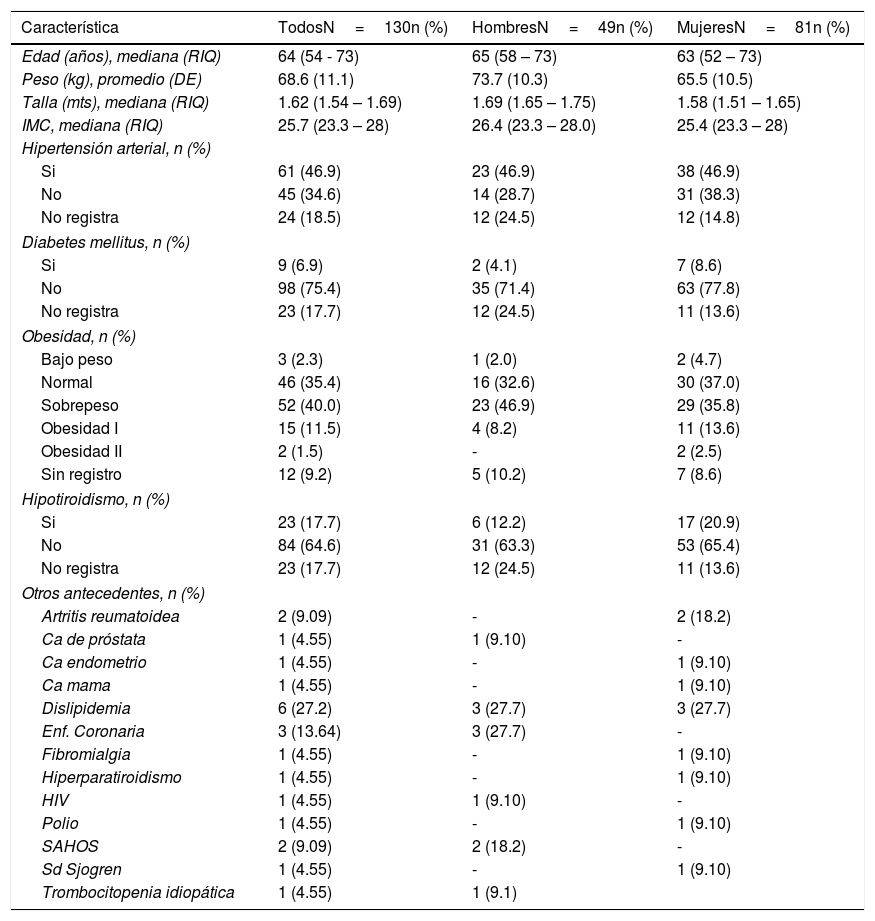
ResultadosSe incluyeron 130 pacientes y en uno de ellos, se realizaron dos procedimientos independientes. En la tabla 1, se describen las variables demográficas del estudio. La mayoría de los pacientes fueron mujeres, la edad mediana del grupo fue de 64 años (54-73 años). El peso promedio fue de 68.6kg, con un IMC de 25.7, de los cuales el 40% de los pacientes presentaron sobrepeso. Dentro de las comorbilidades encontradas en las historias clínicas, más del 50% de los pacientes tenían hipertensión arterial y menos del 10% tenían Diabetes Mellitus. Por otra parte, el 17.7% reportó hipotiroidismo y un paciente reportó el antecedente de Virus de Inmunodeficiencia Humana (VIH) en manejo con antirretrovirales.
Características demográficas de los pacientes incluidos
| Característica | TodosN=130n (%) | HombresN=49n (%) | MujeresN=81n (%) |
|---|---|---|---|
| Edad (años), mediana (RIQ) | 64 (54 - 73) | 65 (58 – 73) | 63 (52 – 73) |
| Peso (kg), promedio (DE) | 68.6 (11.1) | 73.7 (10.3) | 65.5 (10.5) |
| Talla (mts), mediana (RIQ) | 1.62 (1.54 – 1.69) | 1.69 (1.65 – 1.75) | 1.58 (1.51 – 1.65) |
| IMC, mediana (RIQ) | 25.7 (23.3 – 28) | 26.4 (23.3 – 28.0) | 25.4 (23.3 – 28) |
| Hipertensión arterial, n (%) | |||
| Si | 61 (46.9) | 23 (46.9) | 38 (46.9) |
| No | 45 (34.6) | 14 (28.7) | 31 (38.3) |
| No registra | 24 (18.5) | 12 (24.5) | 12 (14.8) |
| Diabetes mellitus, n (%) | |||
| Si | 9 (6.9) | 2 (4.1) | 7 (8.6) |
| No | 98 (75.4) | 35 (71.4) | 63 (77.8) |
| No registra | 23 (17.7) | 12 (24.5) | 11 (13.6) |
| Obesidad, n (%) | |||
| Bajo peso | 3 (2.3) | 1 (2.0) | 2 (4.7) |
| Normal | 46 (35.4) | 16 (32.6) | 30 (37.0) |
| Sobrepeso | 52 (40.0) | 23 (46.9) | 29 (35.8) |
| Obesidad I | 15 (11.5) | 4 (8.2) | 11 (13.6) |
| Obesidad II | 2 (1.5) | - | 2 (2.5) |
| Sin registro | 12 (9.2) | 5 (10.2) | 7 (8.6) |
| Hipotiroidismo, n (%) | |||
| Si | 23 (17.7) | 6 (12.2) | 17 (20.9) |
| No | 84 (64.6) | 31 (63.3) | 53 (65.4) |
| No registra | 23 (17.7) | 12 (24.5) | 11 (13.6) |
| Otros antecedentes, n (%) | |||
| Artritis reumatoidea | 2 (9.09) | - | 2 (18.2) |
| Ca de próstata | 1 (4.55) | 1 (9.10) | - |
| Ca endometrio | 1 (4.55) | - | 1 (9.10) |
| Ca mama | 1 (4.55) | - | 1 (9.10) |
| Dislipidemia | 6 (27.2) | 3 (27.7) | 3 (27.7) |
| Enf. Coronaria | 3 (13.64) | 3 (27.7) | - |
| Fibromialgia | 1 (4.55) | - | 1 (9.10) |
| Hiperparatiroidismo | 1 (4.55) | - | 1 (9.10) |
| HIV | 1 (4.55) | 1 (9.10) | - |
| Polio | 1 (4.55) | - | 1 (9.10) |
| SAHOS | 2 (9.09) | 2 (18.2) | - |
| Sd Sjogren | 1 (4.55) | - | 1 (9.10) |
| Trombocitopenia idiopática | 1 (4.55) | 1 (9.1) | |
DE: Desviación estándar. RIQ: Rango intercuartílico
El 95.4% fueron intervenidos por vía posterior para realización de laminectomía, artrodesis e instrumentación y colocación de aloinjerto. Del total de pacientes, el 18% se reintervino.
En relación a la información del procedimiento quirúrgico, el tiempo en promedio de cirugía fue de 207min, con un sangrado aproximado de 400mL (tabla 2). Al al 80.9% se le aplicó 1 gramo de vancomicina en polvo previo al cierre de la incisión.
Procedimiento Quirúrgico
| Información | N=131n (%) |
|---|---|
| Procedimiento | 125 (95.4) |
| Artrodesis e instrumentación + injerto óseo vía posterior (dorsal, dorsolumbar, lumbar) | 3 (2.3) |
| Corpectomía + artrodesis e instrumentación vía anterior (cervicales) | 3 (2.3) |
| Corrección escoliosis | |
| Reintervención, n (%) | |
| Si | 18 (13.7) |
| No | 113 (86.3) |
| Tiempo quirúrgico, (min) mediana (RIQ) | 207 (165 – 250) |
| Sangrado, (ml) mediana (RIQ) | 400 (200 – 600) |
| Vancomicina | |
| 1 gr | 106 (80.9) |
| 2 gr | 25 (19.1) |
| Drenaje | |
| Si | 12 (9.2) |
| No | 119 (90.8) |
| Ruptura de duramadre, n (%) | |
| Si | 1 (0.8) |
| No | 130 (99.2) |
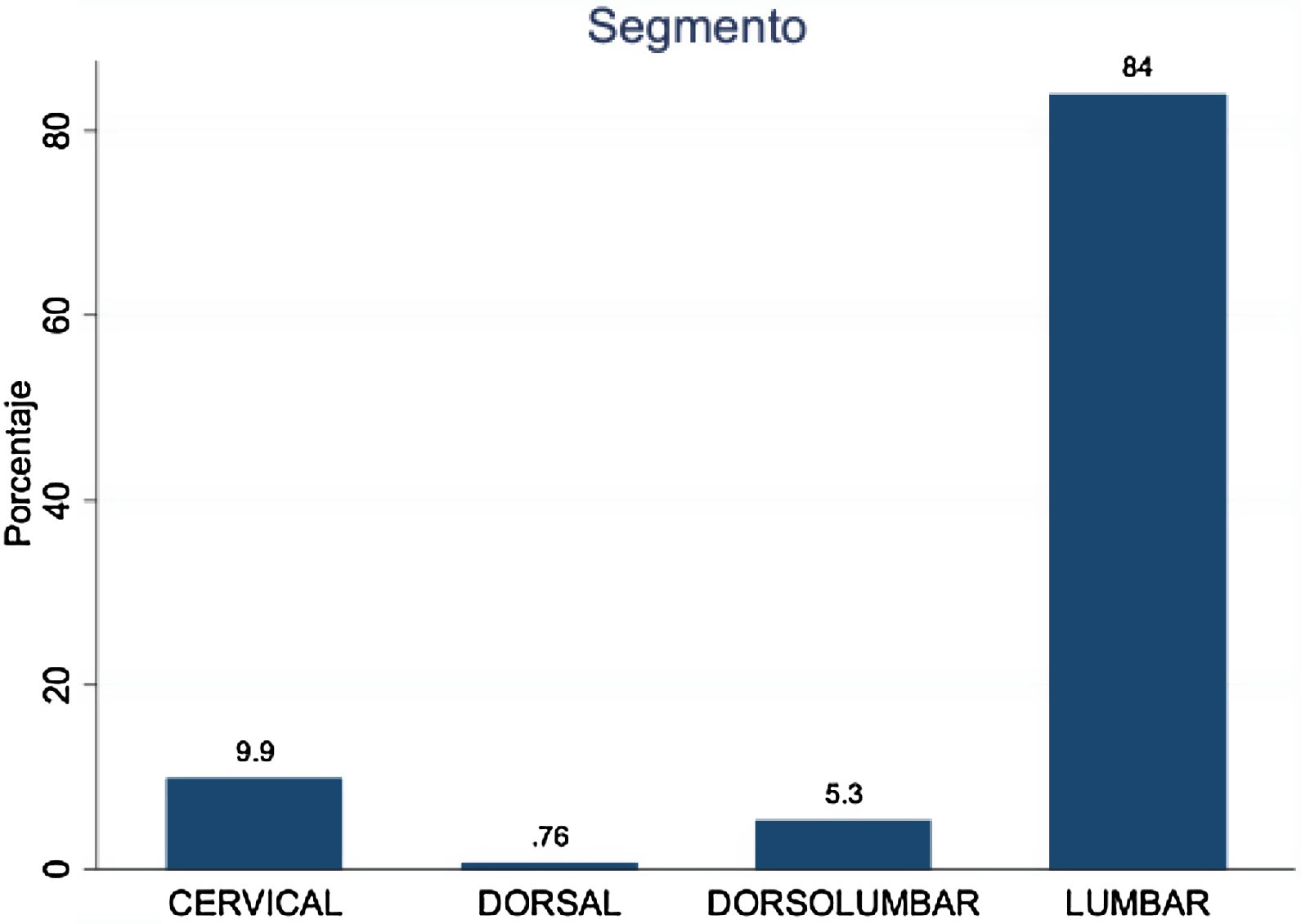
El segmento vertebral que más se intervino fue columna lumbar (fig. 1).
La incidencia de ISO fue de 3.8% (IC95% 1.5% - 8.9%) y en todos los casos fue profunda y localizada a nivel lumbar. Así mismo, en solo dos casos se aisló el microorganismo responsable (E. coli y P. mirabili). Dos de estas infecciones se identificaron a las 6 semanas postoperatorias
En cuanto a la presencia de otras complicaciones, solo 1 paciente presentó ruptura de duramadre, que se resolvió con parche hemático y reposo durante la hospitalización, sin presentar complicaciones durante el postoperatorio mediato o tardío. Se documentó en una paciente infección del sitio de toma de injerto ajeno al sitio intervenido, con una osteomielitis del ilíaco que requirió lavados posteriores. Los pacientes reconsultaron al servicio de urgencias por presentar dolor radicular en miembros inferiores, sin documentar infección (tabla 3).
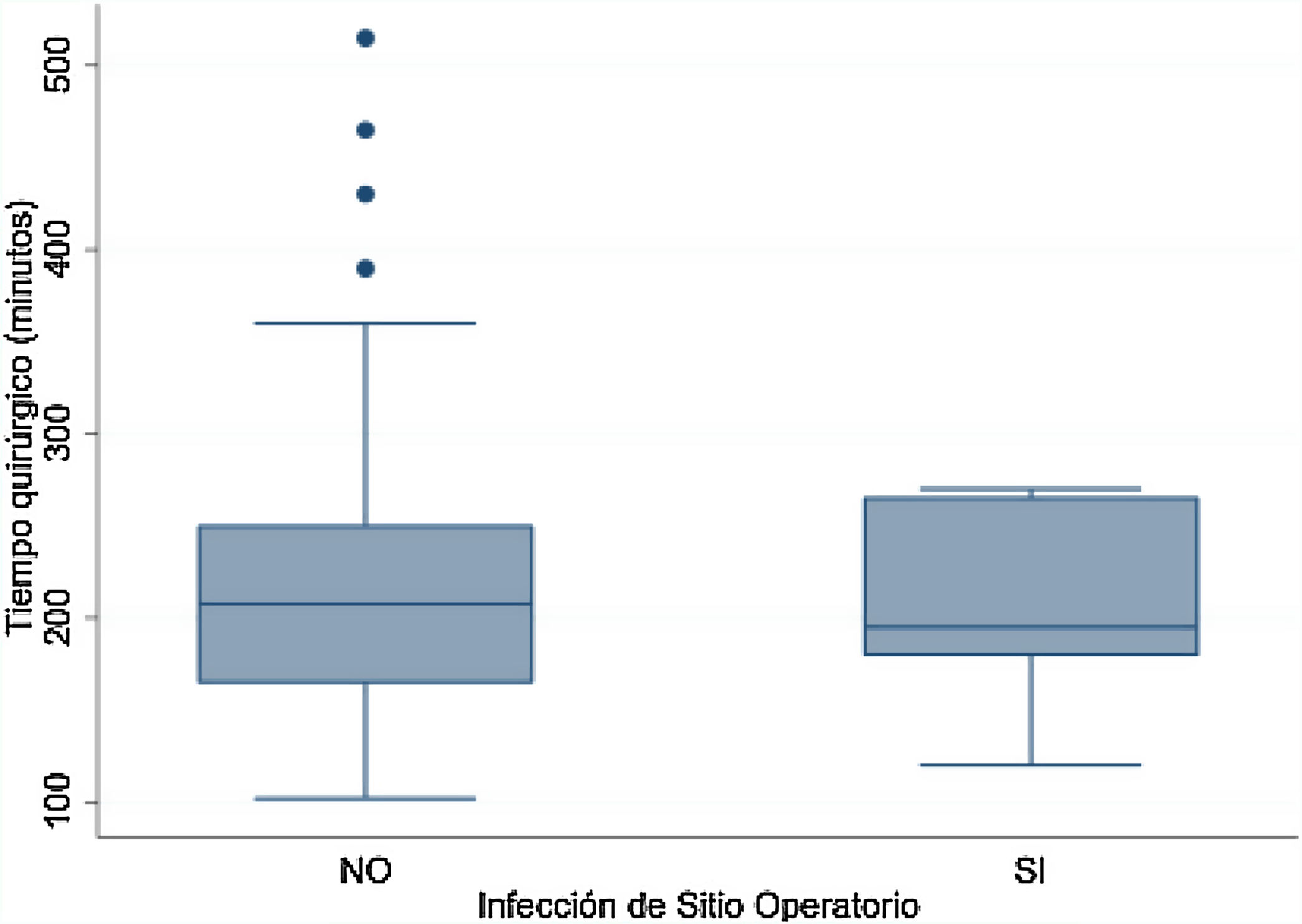
Finalmente, se evaluó el tiempo quirúrgico y sangrado de acuerdo a la incidencia de ISO encontrándose que la mediana de tiempo quirúrgico en quienes presentaron la infección fue de 195 minutos (RIQ 180 - 265) y 208 minutos (RIQ 165 - 250) en los demás pacientes (fig. 2).
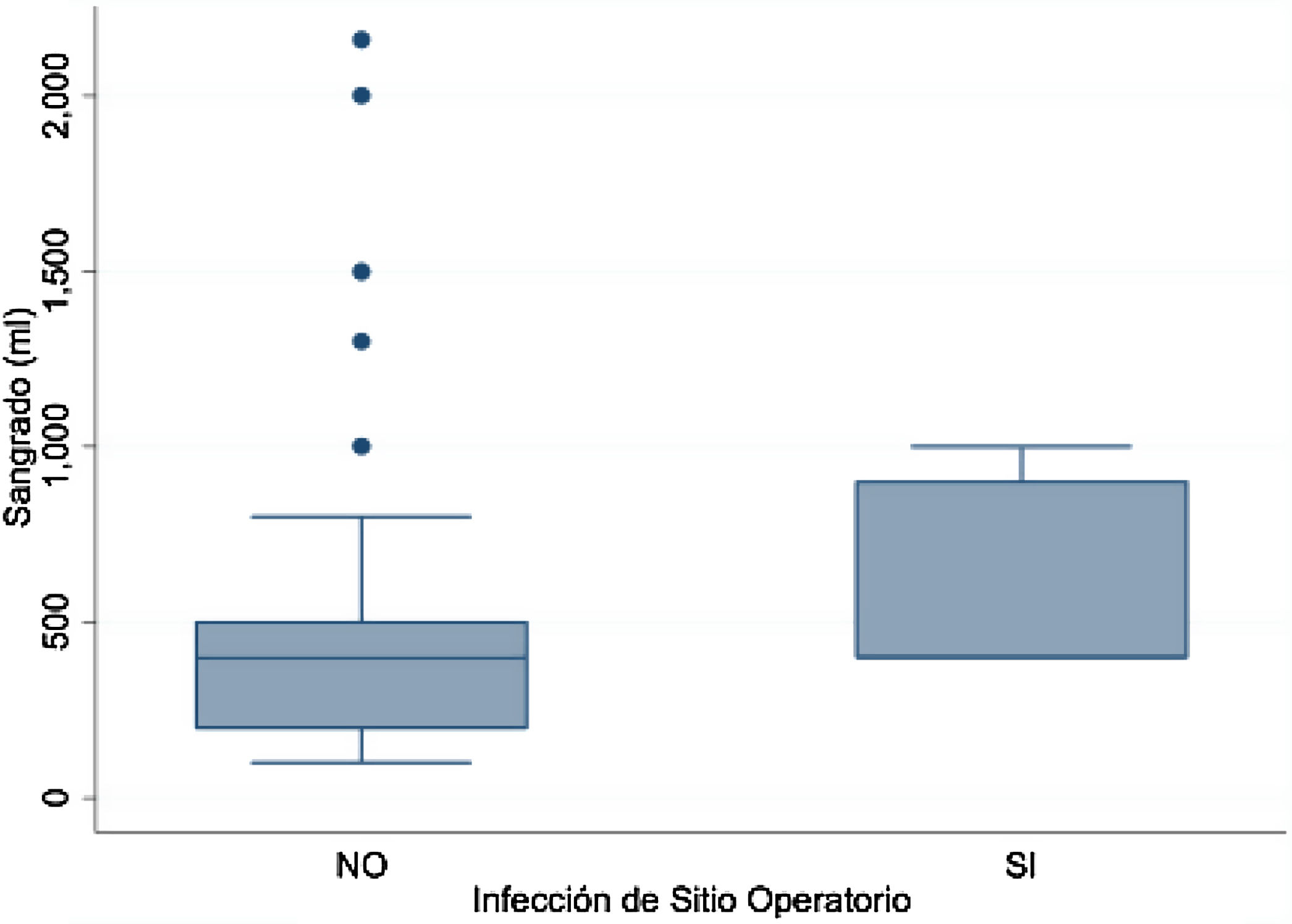
En cuanto al sangrado, la mediana fue de 400cc (RIQ 400 – 900) en quienes presentaron infección y 400cc (200 – 500) en los demás pacientes (fig. 3)
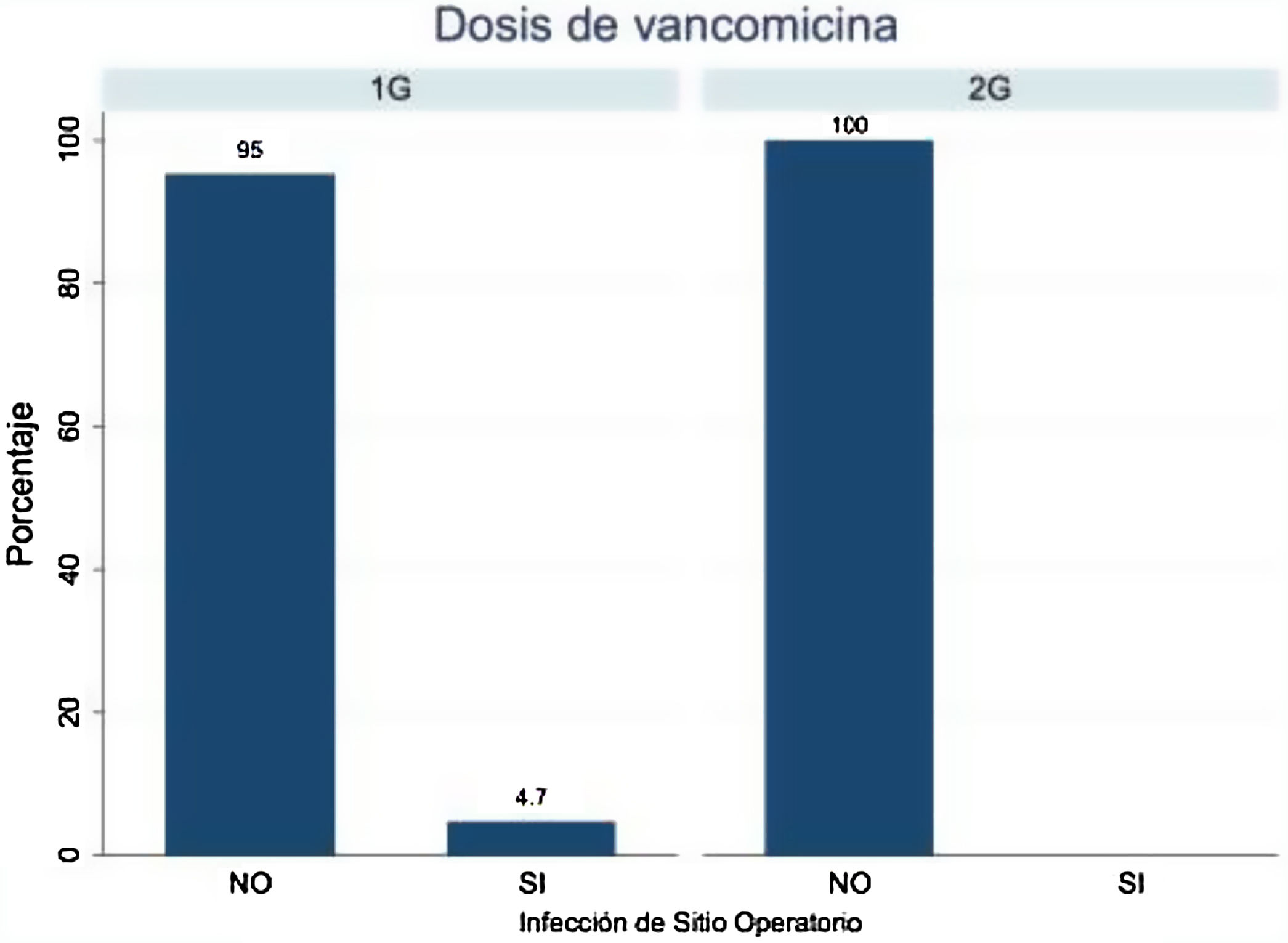
Por último, se encontró que el 4.7% de los pacientes infectados, previamente se les había aplicado 1 gramo de vancomicina (fig. 4)
DiscusiónEste estudio determinó la incidencia de ISO en pacientes a quienes se les aplicó vancomicina tópica previa al cierre de incisión en procedimiento quirúrgicos de columna. En comparación con la literatura disponible, la incidencia en esta población es similar e incluso más baja a lo reportado previamente (hasta el 10%)12.
Tubaki et al, en un estudio ensayo clínico aleatorizado controlado evaluó el uso de vancomicina en 907 pacientes y no encontró diferencias en la tasa de infección entre el grupo que recibió vancomicina comparado con el grupo control (1.61% versus 1.68%)13. Por su parte, Sweet et al., en su estudio comparativo de tipo cohorte retrospectiva con 1732 pacientes llevados a instrumentación posterior con o sin fusión en la región toracolumbar, les administró 1 gramo de vancomicina y además se mezcló vancomicina (1g) en los injertos (grupo con fusión). Se demostró una reducción significativa de infección de sitio operatorio cuando se añadió vancomicina, de 2.6% a 0%, p<0.0001)14. Strom et al, realizó un estudio retrospectivo donde observó la reducción de ISO en 253 pacientes llevados a laminectomía lumbar y fusión posterior (11% vs 0%, p=0.000018), además de observar el riesgo de infección en los grupos, evaluó el riesgo con los grupos llevados a instrumentación y observó que tenían mejores resultados el grupo que se complementaba la instrumentación con el uso de vancomicina tópica (12% vs 0%, p=0.000806)15. Molinari et al., en un estudio retrospectivo de 1512 pacientes, de los cuales 849 pacientes no tenían instrumentación comparado con 478 cirugías de instrumentación posterior como anterior, en quienes se aplicó 1 gramo de vancomicina previo al cierre, encontró que el patógeno más comúnmente aislado era S. aureus y de la muestra, solo 15 pacientes se infectaron. Comparando con la literatura, Molinari demostró que con el uso de vancomicina existió una disminución de la tasa de infección de 1.14% a 0.33%16.
Por otra parte, se han encontrado factores de riesgo para ISO como la presencia de obesidad, ser adultos mayores, tener antecedente de diabetes mellitus, tabaquismo, instrumentación, tiempo quirúrgico largo y hemorragias voluminosas17–22.
Varios estudios reportan que el uso de vancomicina como una terapia de bajo costo, con seguridad para el paciente sin mostrar efectos secundarios y que sirve para prevenir la ISO. Ghobrial et al. en una revisión sistemática con un total de 6701 pacientes encontró una tasa de infección de 1.36%, y reportaron 23 eventos adversos para una tasa de 0.3%, conluyendo así que el uso de vancomicina parece ser seguro y efectivo para disminuir las ISO con una tasa baja de morbilidad23.
Ningún estudió a la fecha ha evaluado si la dosis de vancomicina afecta a los resultados, pero sí se ha demostrado que el uso tópico tiene gran importancia en cuanto a disminución de ISO sobretodo las profundas. Texakalidis et al, en un metaanálisis y revisión sistemática encontró diferencias en el grupo de ISO profundas (OR:0.31: 95% IC: 0.22-0.45: P <.001; I2=29%)24. A pesar de que los estudios han demostrado su seguridad y eficacia, la mayoría son evidencia clase III, por lo que se requieren más estudios que demuestren su eficacia25.
Dentro de las limitaciones de este estudio, el componente retrospectivo pudiese hacer pensar la restricción en el acceso a la información disponible así como en una posible pérdida de sujetos durante el periodo de observación; sin embargo, las historias clínicas presentaron una baja frecuencia de datos perdidos para las variables de interés y se dio un seguimiento completo y apropiado a todos los pacientes, según las recomendaciones del CDC que son 3 meses postoperatorio. El tamaño de muestra puede considerarse como pequeño pero es un grupo heterogéneo y pueden extrapolarse los resultados a la población de la institución. Pese a que la mayoría de estudios sobre este tema son nivel III de evidencia, el uso de vancomicina tópica ha tomado fuerza en campos de cirugía ortopédica, más en concreto en cirugía de columna, así como en guías clínicas como ICM, quienes recomiendan su uso.
La incidencia de ISO en pacientes con cirugía de columna y uso de vancomicina tópica fue similar e incluso más baja que lo reportado por otros estudios. Sin embargo, se requieren estudios de tipo ensayos clínicos o estudios prospectivos, para medir la dosis ideal así como la seguridad de la vancomicina tópica previa al cierre de la incisión.
Fuentes de FinanciaciónRecursos propios de los autores.
Conflicto de InterésLos autores no refieren algún conflicto de interés.