La determinación de la viabilidad miocárdica se ha considerado como una herramienta primordial, principalmente para pacientes con enfermedad coronaria y disfunción ventricular izquierda significativa. En este escenario, se cree que los cardiomiocitos han sufrido un proceso de adaptación a un estado fisiológico alterado que es potencialmente reversible.
La ecocardiografía es un método diagnóstico que puede caracterizar diferentes parámetros de la función cardiaca; sin embargo, pese a haberse demostrado su utilidad en varios estudios, todavía hay algún grado de incertidumbre sobre el papel de este método diagnóstico en comparación con la medicina nuclear o la resonancia nuclear magnética en la práctica clínica.
El propósito de esta revisión es reflexionar sobre la base fisiológica de la viabilidad miocárdica, discutir la importancia de este método diagnóstico de amplia disponibilidad en nuestro medio y resumir los estudios más relevante y útiles para tomar decisiones y optimizar el manejo de los pacientes.
El concepto fisiopatológico y clínico de viabilidad miocárdica está vigente y el perfeccionamiento de los métodos tradicionales de su búsqueda y los nuevos desarrollos tecnológicos permitirán su uso para la optimización de las estrategias terapéuticas.
The determination of myocardial viability has been considered a fundamental tool, mainly for patients with significant coronary disease and left ventricular dysfunction. In this scenario, it is believed that the cardiomyocytes have suffered a process of adapting to an altered physiological state that is potentially reversible.
Echocardiography/cardiac ultrasound is a diagnostic method that can determine the different parameters of cardiac function. However, despite its usefulness having been demonstrated in various studies, there is still a level of uncertainty of the role of this diagnostic method in comparison with that of nuclear medicine or nuclear magnetic resonance in clinical practice.
The aim of this review is to reflect on the physiological basis of myocardial viability, to discuss the importance of this widely available diagnostic method, and to summarise the most relevant and useful results in order to make decisions and optimise the management of the patients.
The pathophysiological and clinical concept of myocardial viability is valid, and the searches for perfecting traditional methods, as well as the new technological developments allow its use for the optimisation of therapeutic strategies.
La insuficiencia cardíaca crónica es un problema de salud pública relevante con alta prevalencia, tratamiento complejo y alta mortalidad. Se requiere un análisis cuidadoso y exhaustivo para proporcionar la terapia adecuada, completa y personalizada a cada paciente en el momento oportuno.
Los datos más relevantes para este manejo son: 1) etiología subyacente (coronaria versus no coronaria), 2) necesidad de revascularización en pacientes coronarios, 3) evaluación de la anatomía y función del ventrículo izquierdo, 4) presencia de regurgitación mitral secundaria significativa, 5) necesidad de terapia con dispositivos como resincronización cardíaca y/o desfibrilador cardíaco implantable1.
Deben evaluarse estos cinco parámetros por completo. La evaluación aislada de cualquiera de ellos ofrece información fragmentada, parcial e insuficiente para el manejo óptimo del paciente.
En referencia a la necesidad de revascularización en el paciente con insuficiencia cardiaca crónica de etiología coronaria, es imprescindible diferenciar la presencia de “cicatriz” (necrosis), isquemia y viabilidad miocárdica entendiendo esta última como la presencia de cardiomiocitos que conservan su función celular y metabólica, además de su capacidad contráctil2. Las tres técnicas principales para la detección de viabilidad miocárdica son las imágenes nucleares, la ecocardiografía y la resonancia magnética (RM)1. Dentro de estas técnicas de imágenes nunca se ha podido negar la importancia de la determinación de reserva contráctil por ecocardiografía ya que resulta un método seguro, altamente disponible en las instituciones de salud y fácil de realizar, reproducir y al mismo tiempo de interpretar3.
Este documento está destinado a revisar el concepto de viabilidad miocárdica y su detección, especialmente mediante ecocardiografía.
Han surgido algunas controversias en cuanto al beneficio y la costo-efectividad de este método diagnóstico en el contexto del manejo de pacientes que serán llevados o considerados para revascularización u otro tipo de intervenciones para realizar un plan multidisciplinario teniendo en cuenta la importancia de la optimización de los recursos y dispositivos de ayuda ventricular, así como de las unidades de cuidados intensivos.
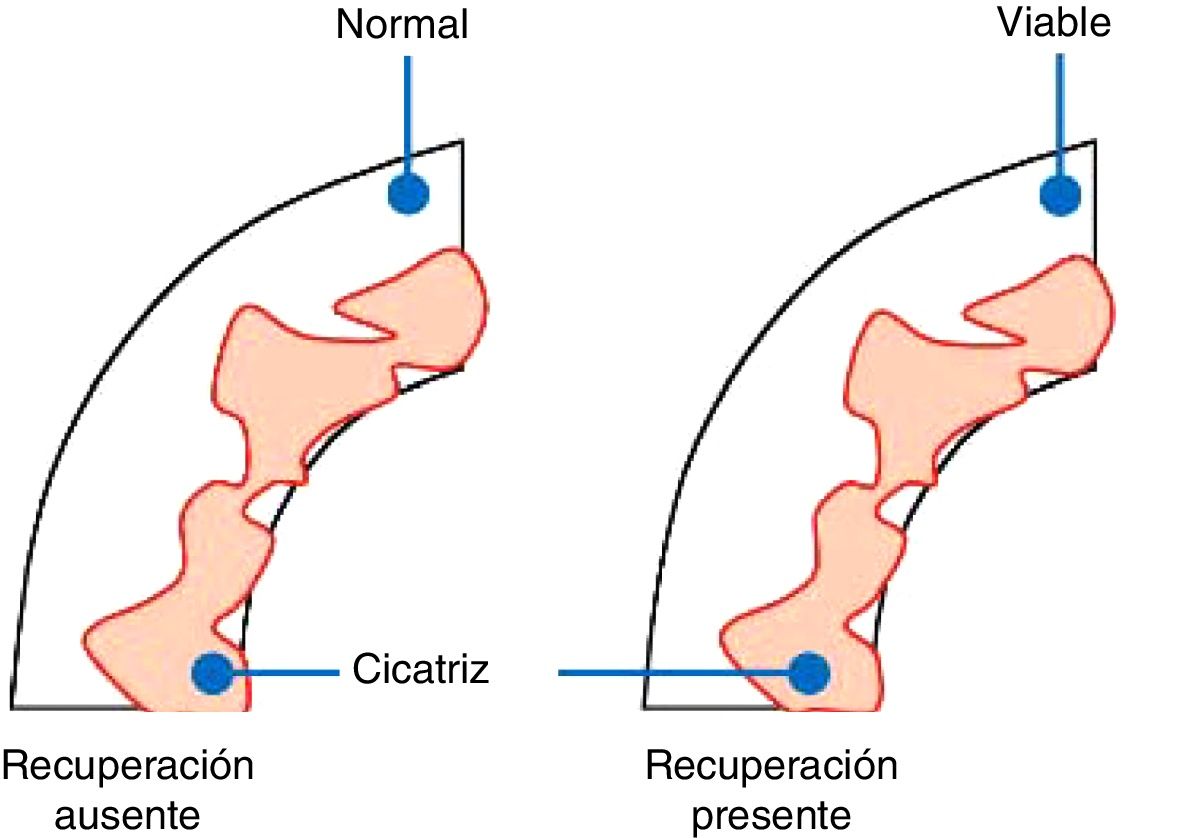
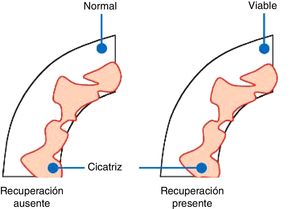
Definiciones de viabilidad miocárdica, hibernación y aturdimientoViabilidad miocárdica: presencia de cardiomiocitos activos, viables, por presentar función celular y metabólica conservada, pero contractilidad reducida o nula con potencial recuperación de la misma al mejorar la oferta de oxígeno (fig. 1). Desde el punto de vista clínico se considera que un paciente con insuficiencia cardiaca crónica de etiología coronaria presenta viabilidad miocárdica cuando posterior a la revascularización se observa mejoría en la evolución clínica, en la función cardíaca y en la clase funcional. Cuando la viabilidad miocárdica supera el 20% del miocardio, la revascularización disminuiría la mortalidad en comparación con el tratamiento médico óptimo. La viabilidad miocárdica a su vez se subdivide en hibernación y aturdimiento, ambos fenómenos crónicos miocárdicos, aunque puede existir yuxtaposición de estos dos2.
Predicción de recuperación después de revascularización en segmentos con cicatriz subendocárdica. Cuando el epicardio es normal no hay recuperación pues la contractilidad está preservada, a la izquierda. Cuando el epicardio es aturdido y hay zonas viables hay recuperación de la contractilidad, lado derecho.
Hibernación miocárdica: adaptación del cardiomiocito ante la persistente reducción significativa del flujo sanguíneo, que determina una disminución de la oferta de oxígeno (recuérdese que es prácticamente imposible aumentar la diferencia arterio-venosa de oxígeno en el lecho coronario) y, produce una disminución de la función contráctil sin ocasionar muerte (necrosis) celular2.
Aturdimiento crónico miocárdico: disfunción contráctil persistente pese a la recuperación del flujo sanguíneo luego de un periodo de reducción significativa de éste, que determina una disminución de la oferta de oxígeno2. Aunque haya recuperación del flujo sanguíneo suele existir una disminución de la reserva de flujo coronario1.
Fisiopatología de la viabilidad miocárdicaEl prerrequisito para que haya hibernación o aturdimiento, es la reducción en el flujo sanguíneo del miocardio. Una estenosis coronaria de hasta aproximadamente 40% no altera el flujo sanguíneo máximo ni la reserva de flujo coronario. Ante 40 a 80% de estenosis, el flujo sanguíneo de miocardio en reposo es normal pero el flujo sanguíneo máximo disminuye; en este contexto, los episodios de aumento de la demanda de oxígeno pueden provocar aturdimiento miocárdico. Una estenosis mayor al 80% se asocia con reducción en el flujo sanguíneo en reposo y puede conducir a una reducción de la contracción.
Hibernación miocárdica: estado de alteración persistente del miocardio y de la función del ventrículo izquierdo en reposo debido a reducción crónica del flujo coronario que puede restablecerse parcial o completamente al recuperar el flujo sanguíneo normal o al reducir la demanda de oxígeno4. La hibernación del miocardio puede ser aguda, subaguda o crónica, y se puede superponer a inestable o estable, angina e infarto de miocardio4.
El miocardio hibernado puede recuperarse del todo o casi por completo si la relación entre el suministro y la demanda de oxígeno del miocardio se modifica favorablemente, mejorando el flujo sanguíneo y/o reduciendo la demanda. Por otro lado, si el miocardio hibernado no es tratado de manera oportuna, puede estar asociado con daño celular progresivo, isquemia recurrente, infarto de miocardio, insuficiencia cardíaca y muerte.
Aturdimiento crónico miocárdico: situación en el laboratorio en que la oclusión total de una arteria coronaria por un lapso de 5 a 15min produce una anormalidad de la motilidad regional miocárdica que persiste por horas o días. Los elementos claves del aturdimiento radican en que se superpone a la isquemia, a la hibernación y al infarto cuando el flujo coronario se restablece5.
En la hibernación el flujo sanguíneo es bajo en reposo, mientras que en el aturdimiento, este es normal pero el flujo sanguíneo máximo está reducido. Puede haber una considerable superposición entre estos fenómenos. El flujo sanguíneo miocárdico absoluto puede ser normal o casi normal en algunos segmentos en hibernación. Sin embargo, la reserva de flujo coronario puede estar reducida dentro de estos segmentos, lo que lleva a la hipótesis de que la hibernación puede ser el resultado de aturdimiento repetitivo, secundario a episodios reiterados de isquemia o aturdimiento crónico6. Tanto el aturdimiento como la hibernación comparten otras características que sugieren que no se pueden considerar como fenómenos completamente separados. En ambos hay anormalidad en la motilidad parietal en reposo, que mejora después de la restauración del flujo. La contractilidad responde a los inotrópicos en ambas situaciones. Además, en el aturdimiento y la hibernación existe un cambio del sustrato preferencial del miocardio, de ácidos grasos libres a glucosa.
Diagnóstico de viabilidad miocárdicaEn la práctica clínica puede realizarse mediante imágenes nucleares, ecocardiografía o RM. Las principales técnicas empleadas nucleares son la tomografía computada con emisión de un fotón único (“single-photon emission computerized tomography” [SPECT]) y talio 201 (perfusión e integridad de la membrana celular), SPECT y tecnecio 99 (perfusión, integridad mitocondrial y de la membrana celular).
Protocolo para la determinación de viabilidad miocárdicaEn el momento existen varios protocolos para la determinación de isquemia, pero el más utilizado en nuestro medio es el de las bajas dosis, en el que se comienza por realizar un ecocardiograma transtorácico basal que permita determinar el puntaje de contractilidad (WMSI).
Deben obtenerse imágenes ecocardiográficas durante la infusión gradual de dobutamina, a fin de evaluar particularmente las alteraciones de la motilidad parietal regional. La fase inicial se realiza infundiendo dobutamina (5 a 10 mcg/kg/min). El principal hallazgo de viabilidad miocárdica es la mejoría en la motilidad (reserva contráctil) y el engrosamiento parietal regional ante esta infusión de dosis bajas de dobutamina. El protocolo puede continuarse con dosis altas de dobutamina (hasta 40 mcg/kg/min) y adición de atropina, que permite detectar también isquemia miocárdica. Las diferentes respuestas de movimiento de la pared durante la infusión de dosis bajas de dobutamina pueden ser: 1) bifásica (mejoría inicial seguida de empeoramiento de la motilidad parietal regional); 2) empeoramiento inicial inmediato de la motilidad parietal regional; 3) mejoría sostenida de la motilidad parietal regional o; 4) ausencia de cambio de la motilidad parietal regional. Las respuestas corresponden a: 1) viabilidad miocárdica e isquemia, 2) isquemia grave, 3) infarto subendocárdico y 4) cicatriz (necrosis) transmural1,7–9.
En definitiva se determina la existencia de viabilidad cuando las zonas inicialmente aquinéticas o hipoquinéticas, mejoran su contractilidad en uno o dos grados en dos segmentos contiguos disfuncionantes dentro de un área considerada infartada, y las no viables aquellas que no presentan mejoría de su contracción10. La zona inicialmente observada como aquinética que se torna disquinética no se considera como un marcador de isquemia ni tampoco de viabilidad.
Se reconocen varias respuestas a la estimulación de dobutamina, por ejemplo, mejoría en más de dos segmentos persistente, indicativa de segmentos viables o normales, mejoría con deterioro posterior o respuesta bifásica indicativa de isquemia, lo mismo que el deterioro en dosis pico de nuevos segmentos y ausencia de respuesta o zona no viable.
La sensibilidad de la ecocardiografía con dobutamina para predecir recuperación funcional (la cual varía de acuerdo con el protocolo utilizado) va desde un 71% hasta un 97%, con un rango de especificidad entre 63 y 95%. La mayor sensibilidad para la detección de viabilidad es considerada cuando se detecta mejoría con las dosis bajas de dobutamina; la mayor especificidad se alcanza al obtener una respuesta bifásica11.
Las ventajas de la ecocardiografía de estrés incluyen un tiempo más corto para la adquisición de imágenes, ausencia de radiación ionizante, portabilidad, disponibilidad inmediata de los resultados, bajo costo y disponibilidad de información auxiliar respecto a los tamaños de las cámaras y su función, válvulas, derrame pericárdico, enfermedad de la raíz aórtica y grosores parietales.
Determinación de viabilidad en el miocardio aturdido después de infarto agudo de miocardioEl infarto agudo de miocardio tratado con terapia de reperfusión, sea a través de procedimientos de trombólisis o angioplastia coronaria transluminal percutánea, es un hecho clínico íntimamente asociado con el aturdimiento miocárdico.
El pronóstico tras el infarto de miocardio se relaciona con la función ventricular izquierda, por lo cual la distinción entre miocardio aturdido y necrótico es clínicamente importante y puede afectar la estratificación del riesgo, así como intervenciones terapéuticas posteriores.
Múltiples estudios han evaluado el uso de ecocardiografía de estrés con dobutamina para la identificación de miocardio viable después de la terapia de reperfusión para infarto agudo de miocardio, y su exactitud predictiva positiva es de 71% a 88%, cuando se compara la respuesta de reserva contráctil obtenida en el estrés, con la subsiguiente mejora en reposo de la motilidad de la pared, con respuestas similares para los pacientes sometidos a angioplastia percutánea primaria o a trombólisis12.
Smart et al.13 demostraron que la reserva contráctil por ecocardiografía de estrés con dobutamina en baja dosis, fue un predictor independiente de recuperación funcional después de la trombólisis para infarto de miocardio y superior a los criterios clínicos como el infarto sin onda Q y pico creatina-fosfoquinasa <1.000 UI/ml. Otros criterios clínicos, tales como la permeabilidad de la arteria relacionada con el infarto y la revascularización, no eran predictores significativos de recuperación.
La viabilidad en una zona de infarto es un hecho común en estos estudios. El hallazgo de esta ha sido altamente predictivo de recuperación funcional espontánea durante el seguimiento clínico. Por otra parte, es necesario destacar que pacientes con isquemia superpuesta sobre zonas aquinéticas tienen menos recuperación regional durante el seguimiento que quienes solamente tienen viabilidad, y así el hallazgo de ésta parece identificar a pacientes con miocardio aturdido, que puede mejorar su función con tratamiento de revascularización temprana. En consecuencia, la evaluación de la viabilidad e isquemia por ecocardiografía de estrés con dobutamina después de infarto agudo de miocardio, puede ayudar a tomar la importante decisión respecto a la revascularización. Otros investigadores han señalado que la recuperación es más frecuente en referencia a segmentos observados inicialmente hipoquinéticos que a segmentos aquinéticos.
Barilla et al., informaron en sus estudios que los pacientes con miocardio viable médicamente tratados tuvieron menos recuperación de la función sistólica que quienes fueron revascularizados. Este hallazgo sugiere que la revascularización del miocardio viable identificado por dobutamina posinfarto puede llevar a mayor recuperación de la función ventricular y, por tanto, de su pronóstico14.
Determinación de viabilidad en el miocardio hibernadoLa ecocardiografía de estrés con dobutamina se ha utilizado también para evaluar miocardio crónicamente disfuncional, es decir miocardio hibernado, y puede predecir la recuperación de la función después de la revascularización con exactitud del 74 al 91%15. Esta exactitud de la prueba no es afectada por el grado de disfunción ventricular izquierda global, ya que datos recientes indican que la ecocardiografía de estrés con dobutamina puede ser más precisa en los segmentos aquinéticos que en los hipoquinéticos15.
Entre todas las respuestas a la estimulación con dobutamina, la respuesta bifásica tuvo los más altos valores predictivos positivos para recuperación segmentaria y recuperación de la función en más de dos segmentos contiguos.
En pacientes con miocardio isquémico o viable tratado médicamente, la tasa de eventos de muerte, infarto de miocardio y revascularización tardía como resultado de la angina inestable fue significativamente superior que en pacientes con cicatrices, es decir, miocardio no viable. Por otra parte, la viabilidad predijo eventos independientemente de la fracción de eyección y la edad.
En pacientes con disfunción ventricular por enfermedad coronaria crónica, Marzullo demostró similar sensibilidad y especificidad en estudios de redistribución de talio y ecocardiografía de estrés con dobutamina.
Ecocardiografía de contrasteLa ecocardiografía miocárdica de contraste es una técnica que se utiliza para evaluar la integridad de la microcirculación coronaria por medio de ecocardiografía de dos dimensiones o mientras se inyecta un medio de contraste ionizado.
La visualización de microburbujas por medio de esta técnica, evalúa el flujo a través de los vasos coronarios de menos de 10μm de diámetro, y evidencia la integridad microvascular, que es un marcador para el miocardio viable. En un paciente con infarto agudo de miocardio y obstrucción de la arteria relacionada con el infarto, la presencia de flujo colateral por contraste de miocardio se correlaciona con mejoría en el movimiento de la pared un mes después de una angioplastia coronaria exitosa.
Un estudio posterior demostró que en pacientes con evidencia documentada de permeabilidad de la arteria relacionada con el infarto después de un infarto reciente, hubo una correlación fuerte entre la evidencia de una microcirculación intacta y mejoría subsecuente en el movimiento de la pared regional. Durante el infarto agudo de miocardio, pacientes con evidencia de reperfusión o flujo coronario en la microcirculación por la ecocardiografía de contraste en el área de miocardio en riesgo después de la terapia de reperfusión, tenían una mejoría en la función ventricular global y regional en el seguimiento, que aquellos con no reflujo.
En el marco de la enfermedad coronaria crónica y disfunción ventricular izquierda, el ecocardiograma estrés con dobutamina y el ecocardiograma con contraste no tuvieron diferencias significativas para predecir la mejoría funcional con base en los segmentos hipoquinéticos, aunque la ecocardiografía de estrés con dobutamina fue significativamente más específica y tenía mejor valor predictivo positivo en segmentos observados aquinéticos en el estudio en reposo16.
Ecocardiograma estrés con estímulo farmacológico con dipiridamolAunque mucho menos estudiada y utilizada que la ecocardiografía de estrés con dobutamina, la ecocardiografía de estrés con dipiridamol se ha usado para delimitar la viabilidad. El dipiridamol es un potente vasodilatador que puede evidenciar la reserva contráctil de los segmentos del miocardio viable mediante el aumento de flujo coronario y cambios metabólicos en el miocardio. En cuanto al uso para evaluar la viabilidad, la dosis óptima de dipiridamol en el examen de la disfunción ventricular reversible puede ser “ultra baja” (0,28mg/kg durante 4 minutos).
En una comparación de estudio cabeza a cabeza entre la dosis “infrabaja” de dipiridamol vs. ecocardiografía de estrés con dobutamina, ambas pruebas tuvieron similar sensibilidad, de 78 y 76%, respectivamente y especificidades idénticas, de 94%17.
En definitiva, puede concluirse que aunque han existido algunas experiencias de infusión de dipiridamol en reemplazo de dobutamina, las evidencias de su utilidad son escasas.
Detección automática del borde endocárdico con uso de retrodispersión integrada (backscatter)La detección automática de bordes endocárdicos por retrodispersión de ultrasonido, es el uso de la energía promedio de las reflexiones de rayos de ultrasonido procedentes de una región determinada de interés dentro del tejido; esta reflectividad del ultrasonido de tejido se mide en decibelios (dB)18. La intensidad de la retrodispersión varía durante el ciclo cardíaco; los niveles máximos de dispersión ocurren en fin de diástole y los niveles mínimos en telesístole.
Los estudios experimentales en animales han demostrado aumento en el promedio de tiempo de retrodispersión integrada en miocardio isquémico agudo, respecto a miocardio normal; también se ha demostrado que la variación de retrodispersión es dependiente del ciclo cardiaco y se reduce en miocardio isquémico con relación a la medición de la retrodispersión ultrasónica, del miocardio normal. Dicha variación también se ha demostrado en los humanos, tan temprano como un minuto después de la obstrucción coronaria.
Los datos sugieren que el análisis ultrasónico del tejido también puede ayudar en la identificación exitosa de tejido reperfundido después de una oclusión coronaria y miocardio potencialmente viable. Se ha logrado evidenciar reversión de cambios en retrodispersión en caninos sometidos hasta 20 minutos de oclusión de las arterias coronarias y de las variaciones dependientes del ciclo cardiaco retornado a valores normales después de la reperfusión, con persistencia cambios incluso en la contractilidad segmentaria y el engrosamiento de pared.
Así, técnicas de caracterización de tejido de ultrasonido pueden ser útiles para diferenciar miocardio viable pero aturdido de tejido francamente necrótico. La variación cíclica es un indicador no específico del infarto agudo, que permite precisamente distinguir tejido isquémico reciente y miocardio viable en modelos animales de experimentación y en pacientes con infarto agudo de miocardio.
En un modelo de tórax abierto con aturdimiento, en perros, por medio de la oclusión coronaria transitoria, dependiente de la variación del ciclo cardiaco recuperaban mucho más rápido la caracterización de los tejidos y la variación cíclica tras la reperfusión, que el engrosamiento de pared. En pacientes con infarto agudo de miocardio, con arteria permeable relacionada con el infarto, es decir, miocardio aturdido, se demostró recuperación en la variación cíclica hasta 24 horas después del inicio de los síntomas, mientras que aquellos que permanecían con oclusión de las arterias, no demostraban ninguna recuperación.
Los cambios acústicos característicos pueden ayudar a detectar el infarto del miocardio que ha estado presente durante varios días sin diagnóstico. En estudios con animales, Mimbs et al.19 encontraron que las señales de la atenuación del ultrasonido por el miocardio infartado fueron mayores que en condiciones normales, y que dichos cambios comenzaban hasta aproximadamente tres días después de la oclusión. Los cambios iniciales sugieren que pueden estar relacionadas con cambios en la perfusión miocárdica, los cuales modifican elementos de la sangre así como en la región de tejido afectado y edema, mientras que los cambios a largo plazo pueden deberse a infiltración celular, fibrosis y otras características de la necrosis.
Las técnicas de retrodispersión del ultrasonido realmente fueron propuestas en la década pasada como útiles para el diagnóstico de viabilidad miocárdica, pero en la actualidad no tienen un empleo habitual en la clínica.
Doppler tisularEsta técnica consiste en modificar los parámetros de las señales Doppler para detectar las bajas velocidades originadas a partir del movimiento de la pared ventricular, eliminando con filtros las señales de alta velocidad provenientes de la circulación sanguínea (la velocidad de la sangre es de aproximadamente 100cm/s y las de la pared del corazón rondan los 10cm/s) y ajustando el límite de Nyquist en+20 −20cm/s. Esta tecnología se incorpora con facilidad en los equipos convencionales de ultrasonido y otorga información en vivo en un examen ecocardiográfico regular. Las velocidades pueden ser presentadas en forma de Doppler pulsado, ubicando la muestra en la pared ventricular que se desea investigar y se obtiene una imagen de manera espectral, en la que las señales se inscriben como ondas similares a las de los flujos sanguíneos o en Doppler color, ya sea modo-m o bidimensional con códigos de colores según la velocidad del tejido20.
El uso de Doppler tisular para la predicción de la viabilidad ha sido limitado por su falta de especificidad porque el segmento de interés puede ser tensionado o forzado por segmentos vecinos. Algunos parámetros como tiempo a pico de velocidad sistólica, velocidad sistólica pico y contracción isovolumétrica no han demostrado consistentemente predecir la recuperación funcional.
Sin embargo, la medición de Doppler tisular en la velocidad en el momento de preeyección, ha demostrado predecir viabilidad. El análisis de la velocidad miocárdica por Doppler tisular en reposo y durante la estimulación con dobutamina, podría permitir la evaluación de la viabilidad miocárdica21.
También se ha analizado la velocidad de Doppler pulsado del tejido en vistas apicales comparado con las velocidades sistólicas del tejido limitada a los segmentos basales. Este enfoque permite la evaluación de viabilidad para una pared entera ventricular del ápice a la base. Dichas velocidades diastólicas de tejido determinadas en reposo pueden ser suficientes para diferenciar miocardio viable de no viable, aunque puede estar afectado por la edad.
Chan et al., demostraron que el Doppler tisular puede usarse para distinguir infartos localizados en el subendocardio, que tienen mayor probabilidad de beneficiarse de revascularización, que los infartos transmurales22. Un aumento en la tasa de tensión sistólica máxima por más de 0,23/s con dobutamina respecto al reposo, mediante FDG PET, podría predecir viabilidad con una sensibilidad del 83% y especificidad de 84%23. Análisis de la función diastólica en los que se usa proyección de imagen de deformación miocárdica, pueden utilizarse para evaluar viabilidad miocárdica. Los segmentos disquinéticos pero viables aumentaron la tasa de deformación con una onda E temprana mayor, así como en la onda A tardía, mientras que los segmentos no viables eran menos sensibles a la estimulación con dobutamina
García-Fernández et al.24 analizaron 16 segmentos miocárdicos de sujetos normales y pacientes con cardiopatía isquémica. En los segmentos isquémicos la velocidad pico diastólica precoz E’ estuvo reducida (6,4±2,1 vs. 8,5±2,8) en comparación con los normales, la relación E’/A’ fue menor (0,95±0,3 vs. 1,5±0,6) y el tiempo de relajación isovolumétrica mostró prolongación (104±36,7ms vs. 69,6±30ms). Todos estos datos tuvieron diferencias estadísticamente significativas, demostrándose así que la función diastólica regional se encuentra empeorada en los segmentos isquémicos, aunque la contracción sistólica esté preservada.
La evaluación de la velocidad, desplazamiento, deformación (strain) y tasa de deformación (strain rate) mediante Doppler tisular, han mostrado ser promisorios como métodos clínicos cuantitativos útiles para la detección de isquemia y viabilidad. El estrés con dobutamina con Doppler tisular ha mostrado una exactitud comparable con la evaluación de la motilidad regional por expertos, en estudios aislados y multicéntricos.
Ecocardiografía por seguimiento de marcas o speckle trackingLa ecocardiografía por seguimiento de marcas, o speckle tracking, bidimensional, ha surgido como una técnica novedosa para la evaluación objetiva y cuantitativa de la función miocárdica general y regional, de manera independiente del ángulo de insonación miocárdica y de los movimientos de traslación. Los datos de deformación miocárdica (strain) se obtienen mediante una medición automática, fotograma a fotograma, de la distancia entre dos puntos de cada segmento del ventrículo izquierdo durante el ciclo cardiaco, en tres dimensiones (radial, circunferencial y longitudinal.
Además, la ecocardiografía con speckle tracking bidimensional puede usarse para evaluar la mecánica rotacional del ventrículo izquierdo. La rotación del ventrículo izquierdo puede medirse con proyecciones de eje corto bidimensionales obtenidas en la base y en los niveles apicales, para permitir el cálculo con y sin giro25.
El parámetro mejor evaluado es la deformación longitudinal global o strain longitudinal (GLS), que es más sensible que la fracción de eyección ventricular izquierda (FEVI) como una medida de la función sistólica y puede usarse para identificar la disfunción del LV subclínica en miocardiopatías. Es útil para evaluar viabilidad miocárdica; un strain longitudinal de −4,5% discrimina entre segmentos viables de aquellos con necrosis transmural26.
El strain postsistólico ha sido propuesto como un marcador de viabilidad, pero no debe utilizarse como un índice independiente ya que también puede ocurrir en el miocardio con necrosis transmural o cicatriz. En este último caso, existe un enlentecimiento sistólico típico y acortamiento postsistólico, debidos a retroceso pasivo por caída de presión del ventrículo izquierdo, durante el periodo de relajación isovolumétrica. Además, las interacciones dependientes de la carga en miocardio no isquémico pueden modificar el strain27.
El acortamiento postsistólico se atribuye a contracción activa y refleja miocardio viable; un segmento que es enteramente pasivo o aquinético durante las primeras horas después de la obstrucción coronaria, no siempre ha sido lesionado en forma irreversible y puede recuperarse con reperfusión.
En la fase crónica después de un infarto, sin embargo, una curva pasiva o totalmente plana de strain es un signo de cicatrización. Estos datos han sido demostrados en modelos experimentales pero hay datos clínicos limitados para corroborar dichos hallazgos.
A pesar de informes y resultados prometedores, se considera que esta tecnología todavía no está lista para la evaluación rutinaria de la viabilidad. En algunos casos, no obstante, la información y diagnóstico adicional que puede proporcionar pueden ser útiles, particularmente cuando otros exámenes no invasivos no han sido concluyentes. Pero incluso para este uso, las interpretaciones son subjetivas y es necesario adquirir mayor experiencia, que viene del uso frecuente de la tecnología28.
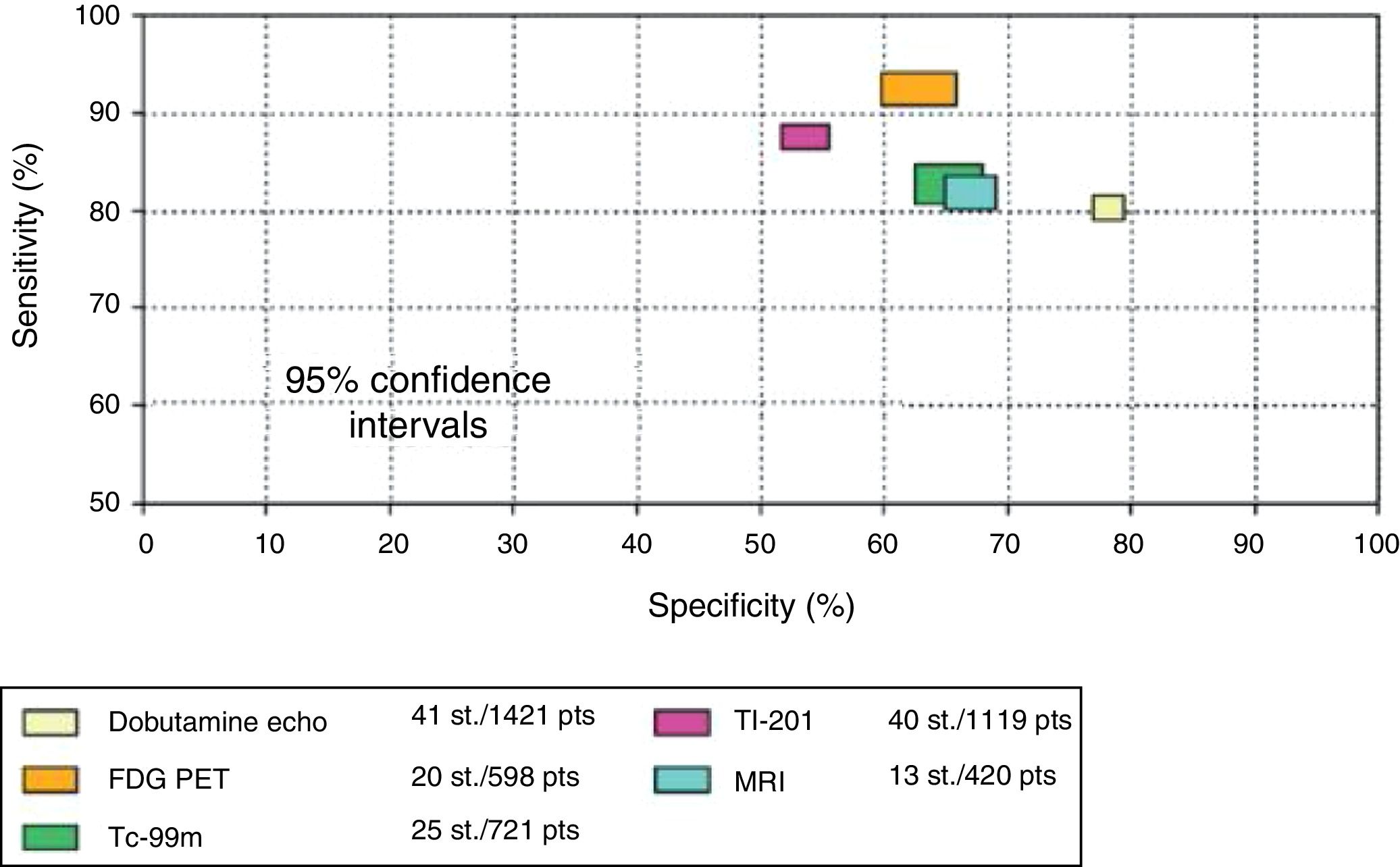
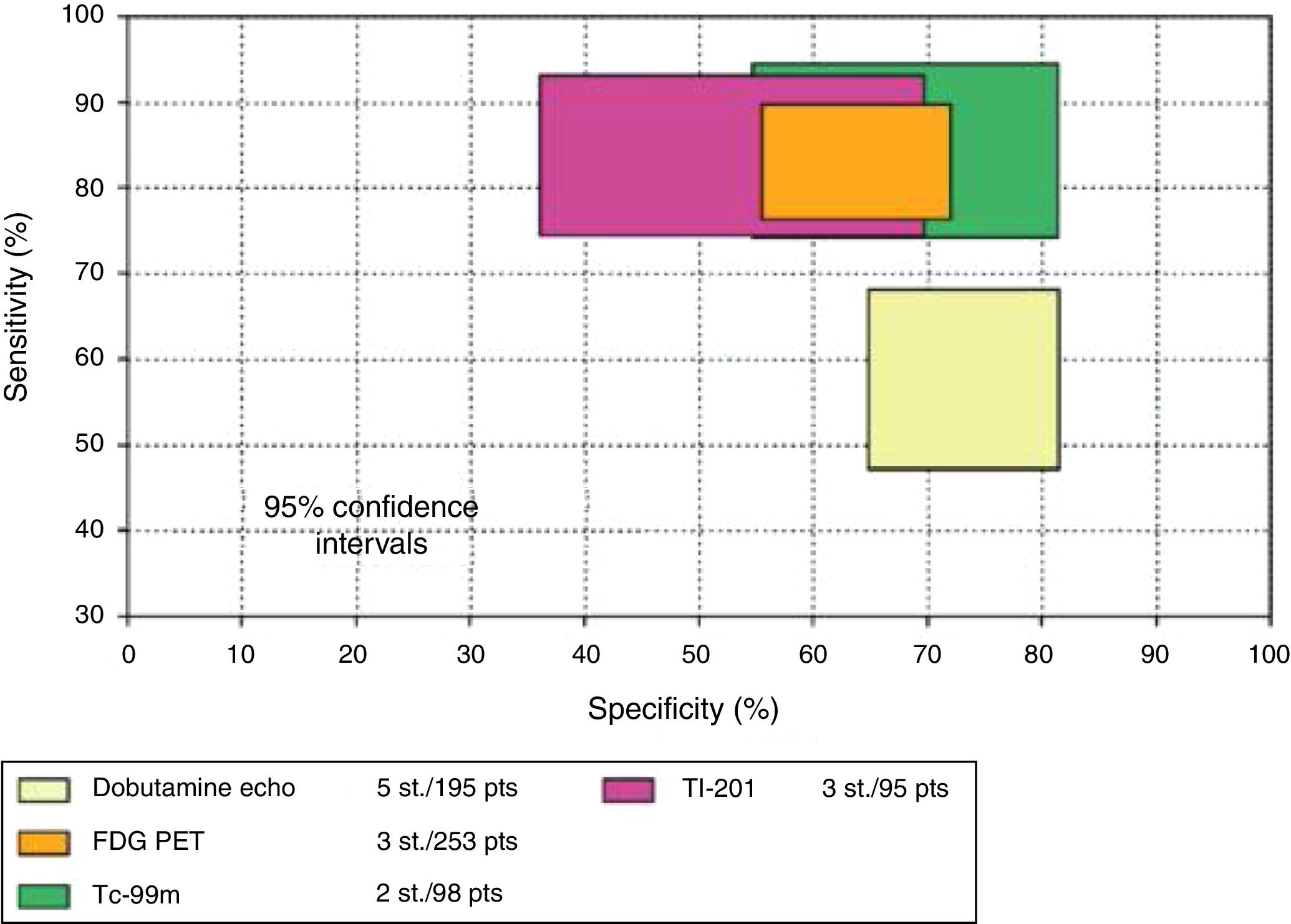
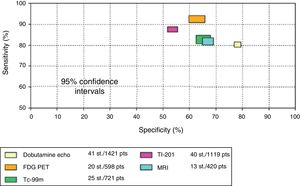
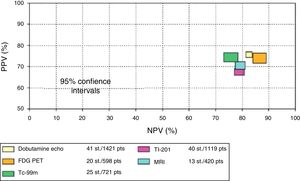
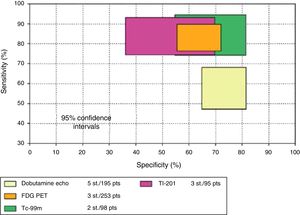
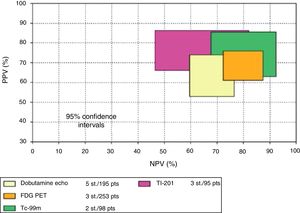
Valor pronóstico de la detección de viabilidad miocárdicaEl mayor valor de la detección de viabilidad miocárdica radica en la predicción de la recuperación de la función regional y global del ventrículo izquierdo luego de la revascularización coronaria quirúrgica o mediante intervencionismo percutáneo. En la tabla 1 y en las figuras 2 a 5 se resumen la sensibilidad, la especificidad y el valor predictivo de una prueba positiva y de una prueba negativa de las diferentes técnicas empleadas para la detección de viabilidad miocárdica29. Como puede observarse, el método que tiene mayor valor predictivo positivo es la PET-DFG y el de mayor valor predictivo negativo es el engrosamiento parietal con RM (fig. 4).
Respuesta de contractilidad regional al estímulo de la dobutamina a dosis bajas
| Interpretación | Reposo | Dosis inicial 5/10 mcg/kg min | Dosis máxima o pico 20 mc/kg min |
| Viabilidad | Miocardio hipocontráctil o aquinético | Miocardio hipocontráctil o aquinético | Miocardio hipercontráctil |
| Ausencia de viabilidad presencia de necrosis transmural | Miocardio hipocontráctil o aquinético | Miocardio hipocontráctil o aquinético | Sin variación |
| Respuesta bifásicaIndicativo de isquemia | Miocardio hipocontráctil o aquinético | Mejoría de la contractilidad. | Empeoramiento de la contractilidad |
| Isquemia en zonas nuevas | Miocardio hipocontráctil o aquinético | Miocardio hipocontráctil o aquinético | Aparición de nuevas zonas hipo- o aquinéticas. |
Comparación de sensibilidad y especificidad con intervalo del 95% de confianza de varias técnicas que miden la recuperación de la contractilidad regional (fig. 2) y global (fig. 3) después de revascularización. Eco estrés con dobutamina; FDG, fluorine18-deoxyglucose; MRI, resonancia nuclear magnética. PET, tomografía de emisión de positrones; Tc-99m, perfusión miocárdica; Tl-201, talio 201. Indican que pacientes con gran cantidad de tejido viable muestran mejoría en la clase funcional mientras que los que no tienen miocardio viable no tienen mejoría. Datos de Schinkel et al.39.
La ecocardiografía con dobutamina tiene una sensibilidad de 80% y una especificidad de 78%, porcentajes que indican que es el mejor método cuando se consideran simultáneamente estas dos propiedades (índice J de Youden: 79%) (tabla 2).
Diferentes técnicas de determinación de viabilidad por ecocardiografía
| Técnica determinante de viabilidad | Interpretación determinante de viabilidad |
| Eco dobutamina | Mejoría de la contractilidad reserva contráctil |
| Eco dipiridamol | Mejoría de la contractilidad reserva contráctil |
| Eco contraste | Presencia de contraste en el áreaMicrocirculación intacta |
| Caracterización de tejidos back scatter | Preservación de la caracterización y dispersión acústica de los tejidos |
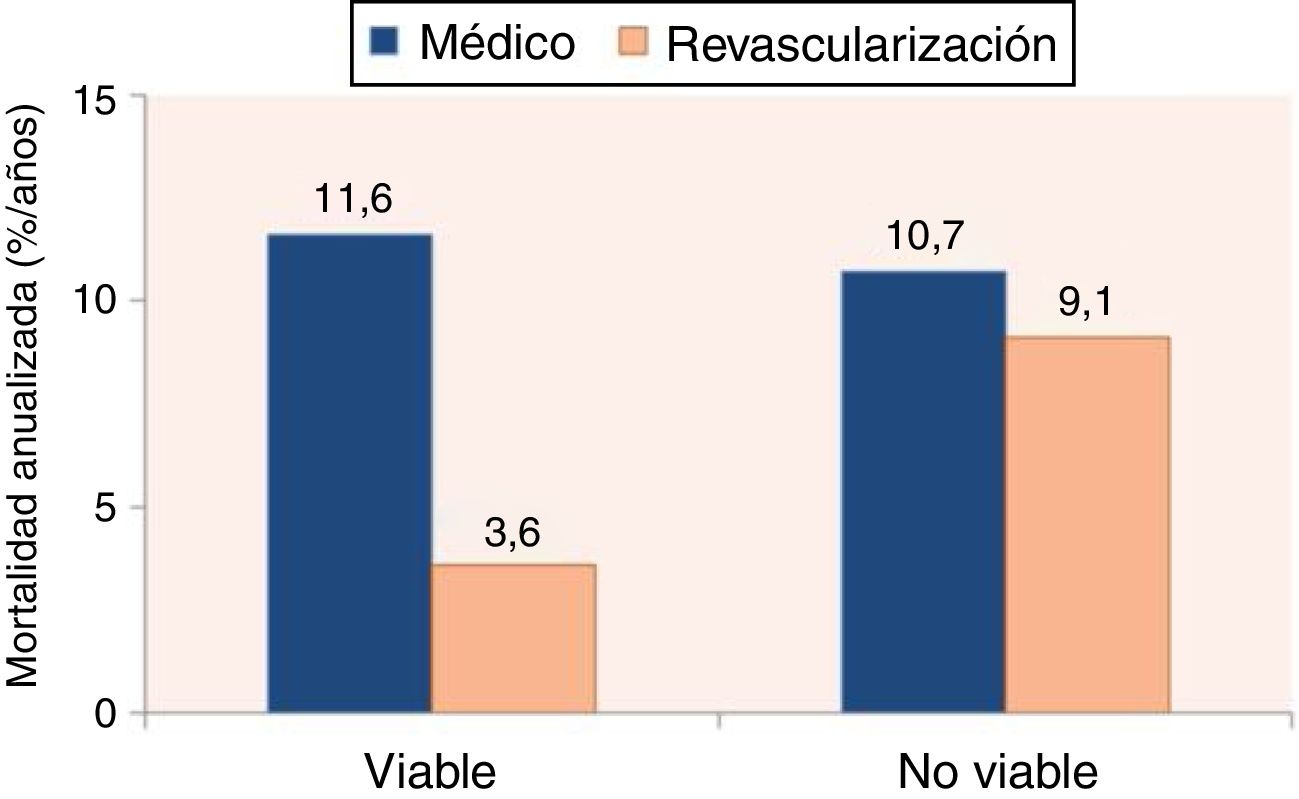
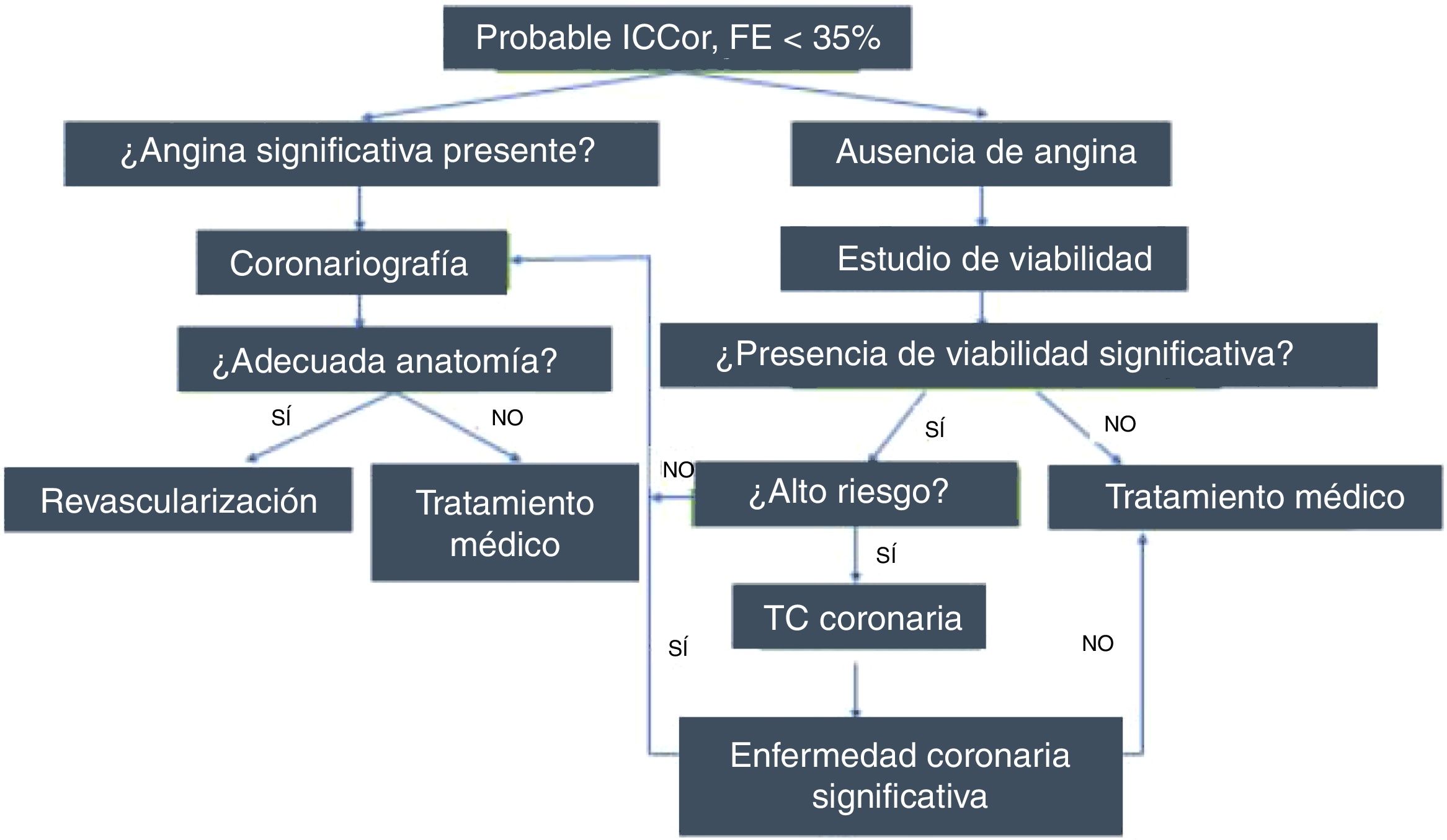
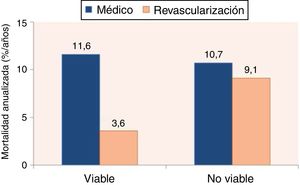
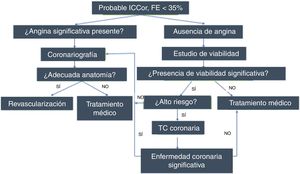
Probablemente, desde el punto de vista clínico tiene mayor relevancia la recuperación de la función global del ventrículo izquierdo que la regional. En este sentido se considera que se puede predecir la recuperación de la función global cuando por lo menos 25% de los segmentos disfuncionantes son viables1. Del mismo modo, esta mejoría se acompañaría de optimización en la capacidad funcional del paciente. Más importante aún es la demostración en estudios retrospectivos de una disminución en la mortalidad en aquellos pacientes que presentan viabilidad miocárdica y son revascularizados1 (fig. 6). Lamentablemente, el único estudio prospectivo, el STICH Trial, que analiza la utilidad de la detección de viabilidad miocárdica para establecer la estrategia terapéutica, resulta negativo30. Diversos autores han analizado y cuestionado los resultados de este estudio31–36. A pesar del resultado del estudio STICH, la detección de viabilidad miocárdica aún conserva prestigio y valor para muchos. Recientemente, Patel y colaborador propusieron un algoritmo para el manejo de pacientes con insuficiencia cardiaca crónica, que incluye en un rol protagónico la búsqueda de viabilidad miocárdica para la toma de decisiones clínicas37 (fig. 7).
Mortalidad anual de pacientes con y sin miocardio viable, de acuerdo con la estrategia de tratamiento escogido. Resultado del análisis de 28 estudios de pronóstico usando diferentes modalidades diagnósticas. Basado en el estudio Schinkel et al.29.
Algoritmo para el manejo de pacientes con insuficiencia cardiaca de probable origen isquémico; si no hay síntomas se procede a documentar viabilidad y de acuerdo con su presencia y el riesgo del paciente se define la modalidad de tratamiento. Patel et al.37.
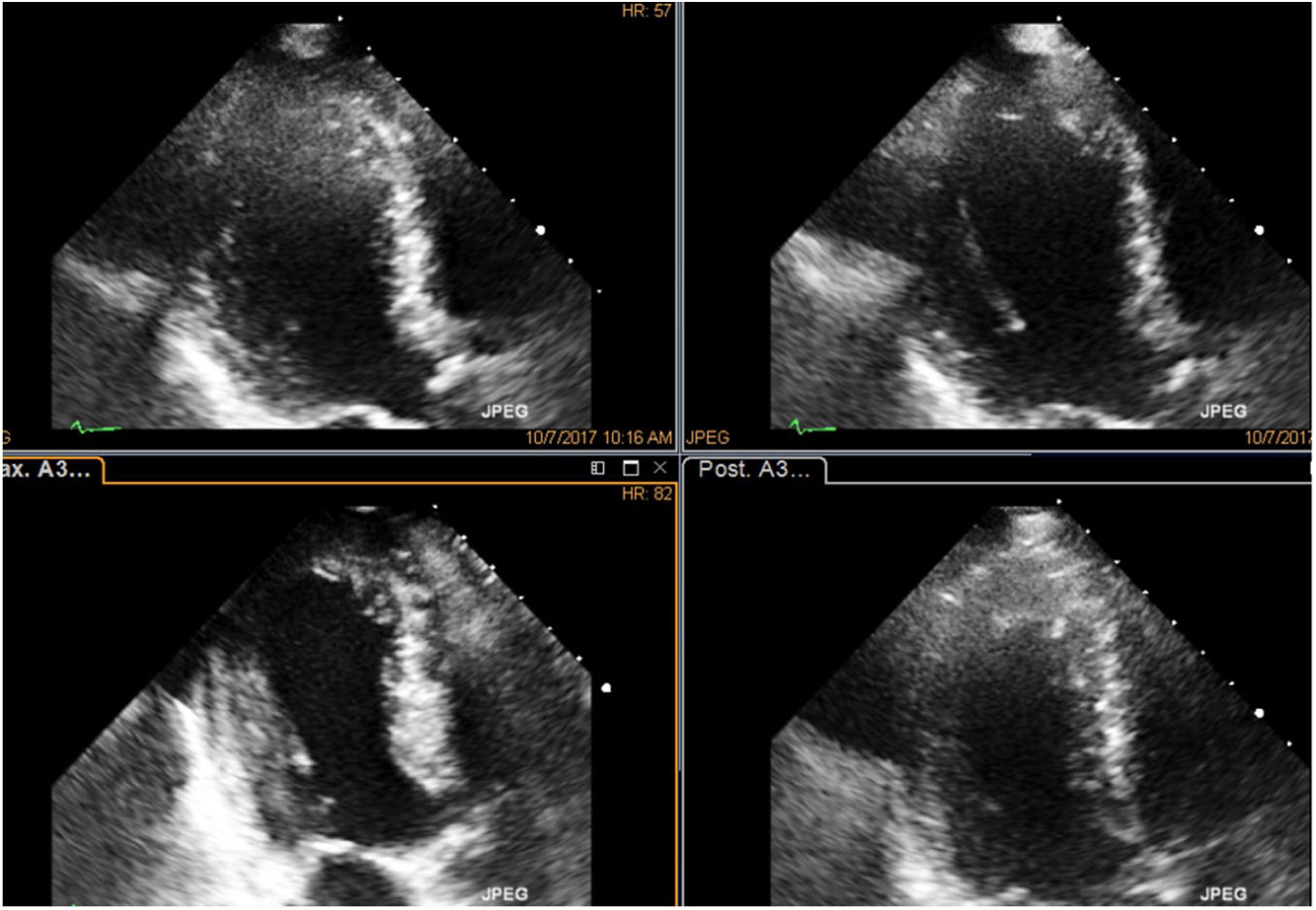
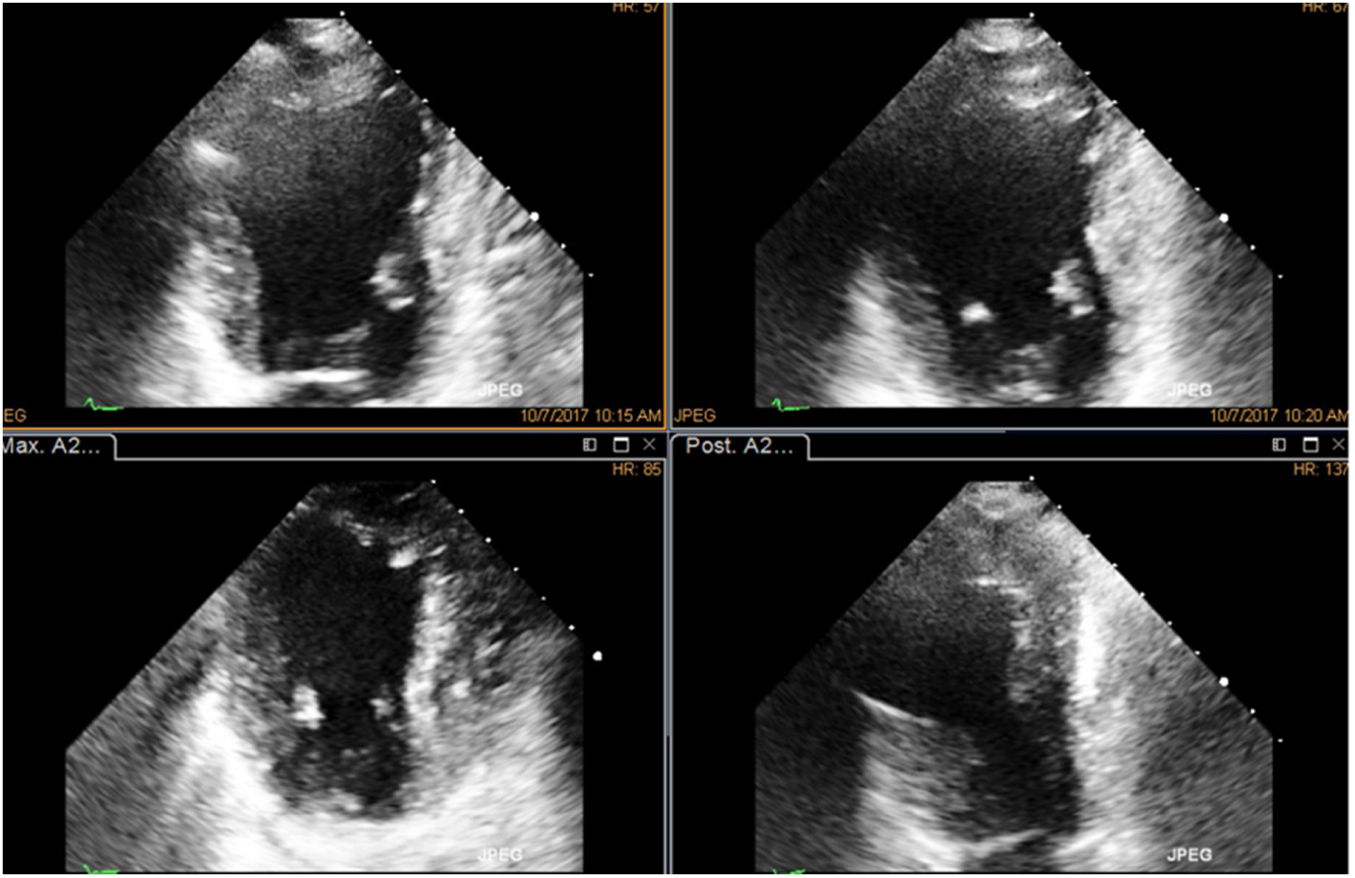
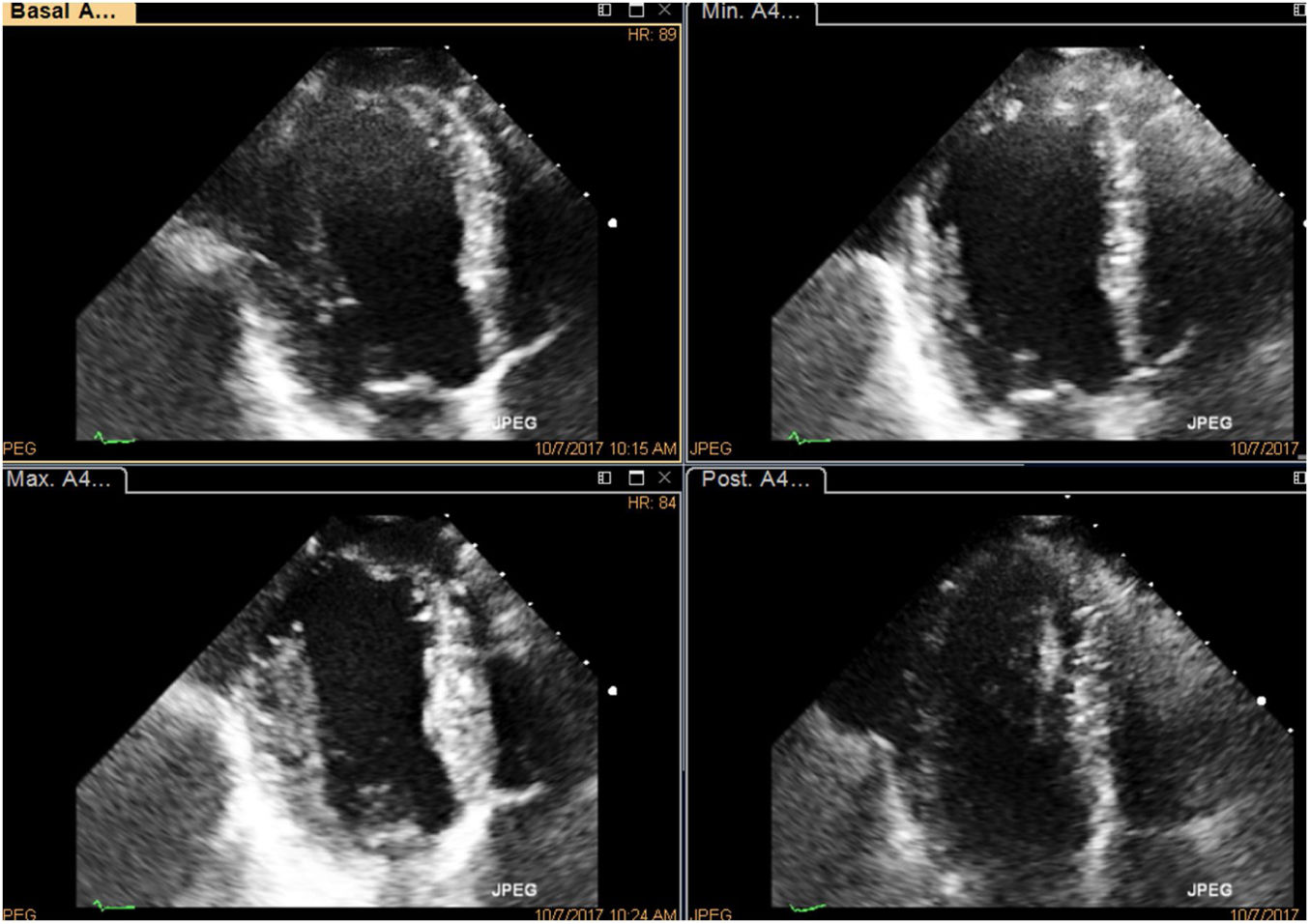
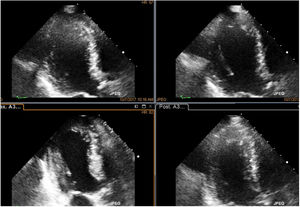
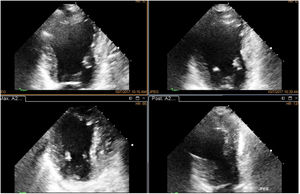
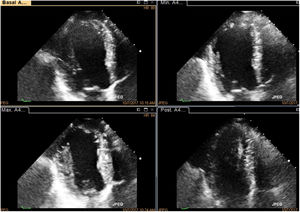
Paciente con enfermedad coronaria previa a compromiso severo de la función ventricular aquinesia apical, con mejoría notoria de la contractilidad en la fase de dosis máxima, proyección de 5 cámaras, quien fue llevado a revascularización y se logró recuperación evidente de su función ventricular en el postoperatorio. En la foto se observa el comparativo de cuatro imágenes simultáneas, en reposo en la primera imagen; la segunda corresponde a la dosis baja, la tercera a la dosis pico y la última a la dosis en recuperación, orden en que normalmente se hace un estudio.
El concepto de viabilidad miocárdica y su valor clínico han sido puestos en duda desde la aparición del estudio STICH. Los autores de este artículo consideran que:
- -
Existen nuevos estudios fisiopatológicos que brindan información básica sobre los mecanismos subyacentes a esta entidad clínica38–40.
- -
Hay un interés renovado en la clínica cardiológica por el estudio de la detección de viabilidad miocárdica, de su valor pronóstico y de su importancia para la decisión de revascularización de pacientes con insuficiencia cardiaca de etiología coronaria41–45.
- -
Existen desarrollos metodológicos nuevos y valiosos, tanto en técnicas nucleares como en RM46–48.
- -
El mayor aporte de las nuevas técnicas de la ecocardiografía son las imágenes de deformación y velocidad de deformación miocárdica28.
- -
Más allá del escenario clínico de la insuficiencia cardiaca crónica de etiología coronaria han aparecido nuevas situaciones clínicas en que la detección de viabilidad miocárdica podría ayudar en la toma de decisiones terapéuticas. Son ejemplo de ello los pacientes con oclusiones coronarias completas49, con síndrome de takotsubo50, con arritmias ventriculares complejas y terapia de resincronización, y con dispositivos de soporte ventricular.
Así mismo, consideran que el concepto fisiopatológico y clínico de viabilidad miocárdica está vigente y que el perfeccionamiento de los métodos tradicionales de su búsqueda y los nuevos desarrollos tecnológicos permitirán su uso para la optimización de las estrategias terapéuticas.
Conflictos de interésNinguno.