La hemorragia no compresible del torso es la principal causa de muerte asociada al trauma. Esto ha llevado al desarrollo de nuevos dispositivos para el control hemorrágico, y uno de estos es el balón de resucitación aórtico endovascular (REBOA).
ObjetivoRealizar una revisión no sistemática de la literatura con respecto al uso del REBOA en trauma.
Materiales y métodosSe realizó una búsqueda sistemática de la literatura en Medline, se seleccionaron los artículos relevantes para el logro de nuestro objetivo y con estos se realizó una síntesis cualitativa y narrativa de la literatura disponible.
ResultadosNuestra síntesis cualitativa y narrativa muestra que el REBOA podría ser una intervención segura y efectiva para el control de la hemorragia en trauma abdominopélvico. Su uso es controvertido en trauma torácico. Finalmente, el uso del balón de resucitación aórtico endovascular puede causar complicaciones relacionadas con su aplicación.
ConclusiónEl REBOA es una alternativa en la cirugía de control de daños que podría ser efectiva en el control de la hemorragia no compresible del torso de origen abdominopélvico. Al ser una intervención compleja, el REBOA se encuentra todavía en fase de desarrollo y la evidencia disponible no es suficiente para proveer recomendaciones fuertes.
Non-compressible torso haemorrhage is the leading cause of death in trauma cases. This has led to the development of new devices to control bleeding, including resuscitative endovascular balloon occlusion of the aorta (REBOA).
ObjectiveTo perform a non-systematic review of the literature on the use of REBOA in trauma.
Materials and methodsA systematic literature search through Medline was conducted. Articles relevant to our objective were selected. A qualitative and narrative synthesis of results is presented.
ResultsOur qualitative and narrative results show that REBOA could be a safe and effective intervention for the control of haemorrhage in abdomino-pelvic trauma. Its use is controversial in thoracic trauma. Finally, the performance of this intervention may cause complications.
ConclusionREBOA is an alternative that can be used in damage control surgery. It could be effective for early control of bleeding in patients with non-compressible torso haemorrhage. As a complex intervention, REBOA is in its development phase, and the evidence available preclude us from providing strong recommendations.
El trauma es un problema de salud pública a nivel global y ha sido calificado como la epidemia desatendida de los países en desarrollo1. Según datos del Global Burden of Disease Study2, para el 2013 unos 973 millones de personas sufrieron traumatismos que requirieron algún tipo de atención médica; de estos, 4,8 millones murieron y 56,2 millones requirieron cuidado hospitalario. Las causas de muerte relacionadas con el trauma fueron los accidentes de tránsito, los suicidios, las caídas y la violencia interpersonal2.
La injuria vascular es una de las principales causas de muerte en el trauma civil y militar3,4. La hemorragia secundaria a la injuria vascular puede provenir de sitios susceptibles a compresión directa, o de sitios no susceptibles a compresión directa; esta última se conoce como hemorragia no compresible del torso5.
La hemorragia no compresible del torso se define como sangrado masivo torácico, abdominal y/o pélvico de imposible control por medio de compresión directa. La mortalidad secundaria a esta condición puede llegar a ser tan alta como del 45%6, y se ha estipulado que la mayoría de estas muertes son potencialmente prevenibles.
El avance en el estudio del trauma ha llevado a la comprensión de los mecanismos fisiopatológicos del shock hemorrágico y al mejoramiento de la atención de los pacientes críticamente enfermos. Con esto, una mayor proporción de pacientes con hemorragia no compresible del torso sobreviven luego del ingreso hospitalario y logran llegar al quirófano para el control del sangrado7.
La investigación clínica y traslacional contemporánea en trauma se ha encaminado hacia el desarrollo de métodos y dispositivos para el mejorar el pronóstico de los pacientes con trauma grave8. Entre los nuevos dispositivos se encuentra el balón endovascular aórtico de resucitación (resuscitative endovascular balloon of the aorta [REBOA]). El REBOA podría ser una alternativa segura y efectiva a la toracotomía de emergencia en pacientes con shock hemorrágico secundario a hemorragia no compresible del torso.
El objetivo de este trabajo fue realizar una revisión no sistemática de la literatura con respecto al uso del REBOA en trauma.
MétodosSe realizó una búsqueda sistemática de la literatura en la base de datos Medline a través de la interfase OVID. Se construyó una fórmula de búsqueda basada en la condición de interés (trauma) y la intervención de interés (REBOA). La fórmula de búsqueda se encuentra en la tabla 1. Se seleccionaron los artículos que estudiaran el uso del REBOA en pacientes con trauma, y con estos se hizo una síntesis cualitativa y narrativa de la literatura.
Fórmula de búsqueda sistemática de la literatura en la base de datos Medline
| 1 | exp “Wounds and Injuries”/ |
| 2 | trauma.mp. |
| 3 | NCTH.mp. |
| 4 | noncompressible torso hemorrhage.mp. |
| 5 | exp Shock, Hemorrhagic/ |
| 6 | exp Shock, Traumatic/ |
| 7 | REBOA.mp. |
| 8 | “resuscitative endovascular balloon occlusion of the aorta”.mp. |
| 9 | 1 or 2 or 3 or 4 or 5 or 6 |
| 10 | 7 or 8 |
| 11 | 9 and 10 |
Fuente: Autor.
Como el REBOA es una técnica que se encuentra todavía en fase de desarrollo, no es posible realizar una revisión sistemática siguiendo una pregunta PICO típica. Por lo tanto, la siguiente revisión de la literatura responderá a la siguiente pregunta: ¿Qué ha sido descrito en la literatura sobre el uso del REBOA en pacientes con trauma?
Para responder a la pregunta descrita se incluyeron ensayos clínicos controlados, series de casos, estudios de cohorte y estudios de casos y controles que reportaran o estudiaran el uso del REBOA en pacientes con trauma. Se excluyeron estudios en los que el REBOA fuera usado en condiciones diferentes al trauma.
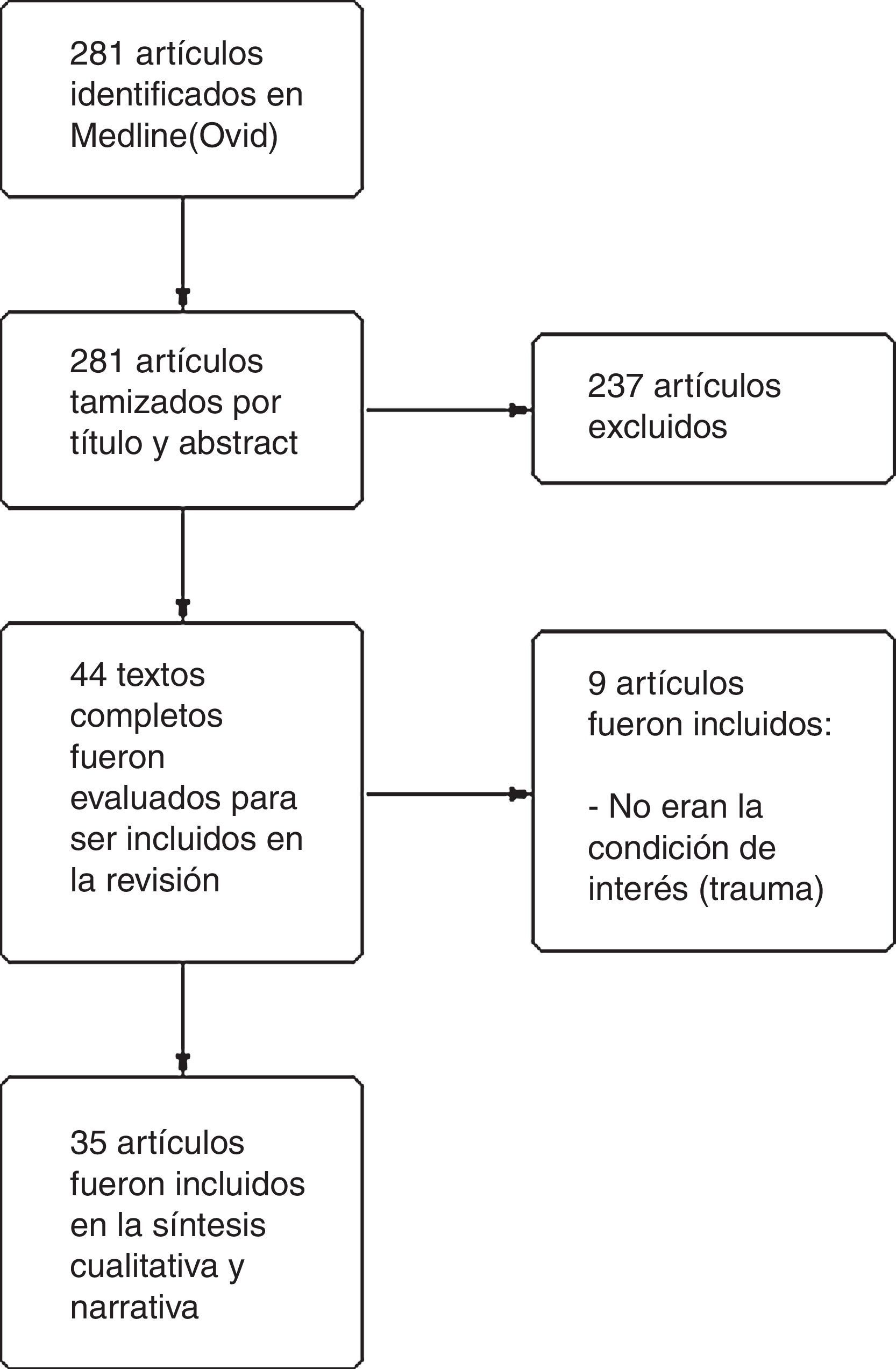
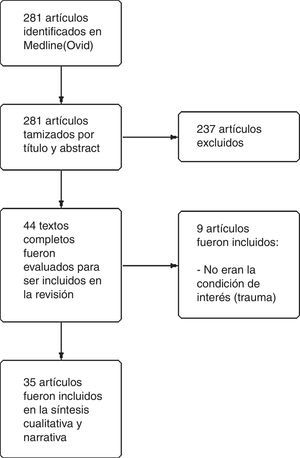
Resultados de la síntesis cualitativaLa búsqueda en Medline generó 281 resultados. Se excluyeron 246. Finalmente se incluyeron 35 artículos en la síntesis narrativa y cualitativa. La figura 1 describe el flujograma PRISMA para la selección de los artículos.
Evolución e historiaLa oclusión vascular para el control temporal del sangrado ha sido uno de los principios fundamentales de la cirugía de control de daños, especialmente en pacientes con shock secundario a hemorragia no compresible del torso5.
La toracotomía de emergencia es la técnica con la que tradicionalmente se ha realizado la oclusión aórtica directa9. Fue descrita por primera vez en humanos en 1880 por Paul Nihans. En 1967 Beall reportó su uso en pacientes agónicos, y en 1976 la práctica de este procedimiento en pacientes traumatizados se difundió cuando Ledgerwood et al.10 describieron el uso de la toracotomía pre-laparotomía para el manejo de la hemorragia masiva de origen abdominal.
La utilidad de la toracotomía de emergencia no se limita a la resucitación del paciente agónico mediante masaje cardiaco directo. Además, es útil en el control hemorrágico en las lesiones torácicas, facilitando el drenaje del hemopericardio cuando hay lesión cardiaca asociada. El pinzamiento de la aorta mediante toracotomía izquierda brinda algún grado de control hemorrágico en las lesiones abdominopélvicas e incrementa el flujo sanguíneo coronario y cerebral11. La toracotomía de emergencia con pinzamiento de la aorta es una intervención sencilla que, en manos expertas, puede realizarse rápidamente; sin embargo, es una técnica invasiva y cruenta que puede aumentar la morbimortalidad de los pacientes críticamente enfermos.
La oclusión aórtica endovascular mediante la técnica de REBOA en pacientes con hemorragia abdominal y pélvica, a riesgo de colapso cardiocirculatorio, es un método menos invasivo que la toracotomía de emergencia, con una historia que inició a mediados del sigloxx11,12. La primera descripción del uso de REBOA en pacientes con hemorragia fatal fue hecha por el coronel Hughes13 en el año 1954 durante la guerra de Corea. En este reporte la oclusión aórtica se realizó usando el balón Dotter-Lukas14; aunque los 3 pacientes intervenidos murieron, el uso del balón fue efectivo en la restauración de la presión arterial en un paciente.
A pesar de que los primeros reportes mostraron un restablecimiento efectivo de la presión arterial y control temporal de la hemorragia, esta técnica no obtuvo mayor atención ni tuvo una adopción clínica rutinaria por la carencia de tecnología endovascular de la época8 y las limitaciones para demostrar su efectividad15.
Con el desarrollo y la maduración de las técnicas endovasculares se despertó nuevamente el interés por REBOA8. Brenner et al.16 describieron 5 casos de trauma cerrado y 2 casos de trauma penetrante en los que se aplicó la oclusión aórtica endovascular para el control de la hemorragia. Los autores concluyeron que REBOA es una maniobra segura para la reanimación y el control hemorrágico en pacientes con hemorragia no compresible del torso.
Adicionalmente, este método ha sido reportado exitosamente en casos de manejo de sangrado no traumático, como hemorragia posparto17, cirugía pélvica oncológica18, cirugía ortopédica electiva y aneurismas rotos de aorta abdominal, siendo en este último utilizado de manera rutinaria en la actualidad8,19.
Principios fisiológicosLa reanimación del paciente en shock asociado a trauma tiene como objetivo restablecer el volumen intravascular, mantener el adecuado metabolismo celular y corregir las pérdidas sanguíneas20.
La oclusión aórtica, abierta o endovascular, en hemorragia abdominal o pélvica pretende redistribuir el volumen circulante y prevenir el paro circulatorio, incrementando la oportunidad para realizar el control definitivo del sangrado mediante cirugía o angioembolización.
La obstrucción del flujo aórtico mediante el uso de REBOA en pacientes en estado de shock y a riesgo de colapso cardiocirculatorio resulta en un cambio en la distribución del volumen y un aumento de la presión arterial18, mejorando la perfusión coronaria y carotídea21,22.
A pesar del beneficio de la redistribución del volumen circulante con el consecuente aumento en la perfusión cerebral y coronaria, el uso del REBOA puede traer como consecuencia la isquemia en los tejidos distales a la oclusión. Estudios de modelos animales con REBOA han mostrado que la oclusión aórtica prolongada tiene resultados fisiológicos deletéreos, como aumento de la acidosis, hipoxia y respuesta inflamatoria23. Sin embargo, esta alteración fisiológica parece ser menor con REBOA que con la oclusión aórtica tradicional por toracotomía23,24.
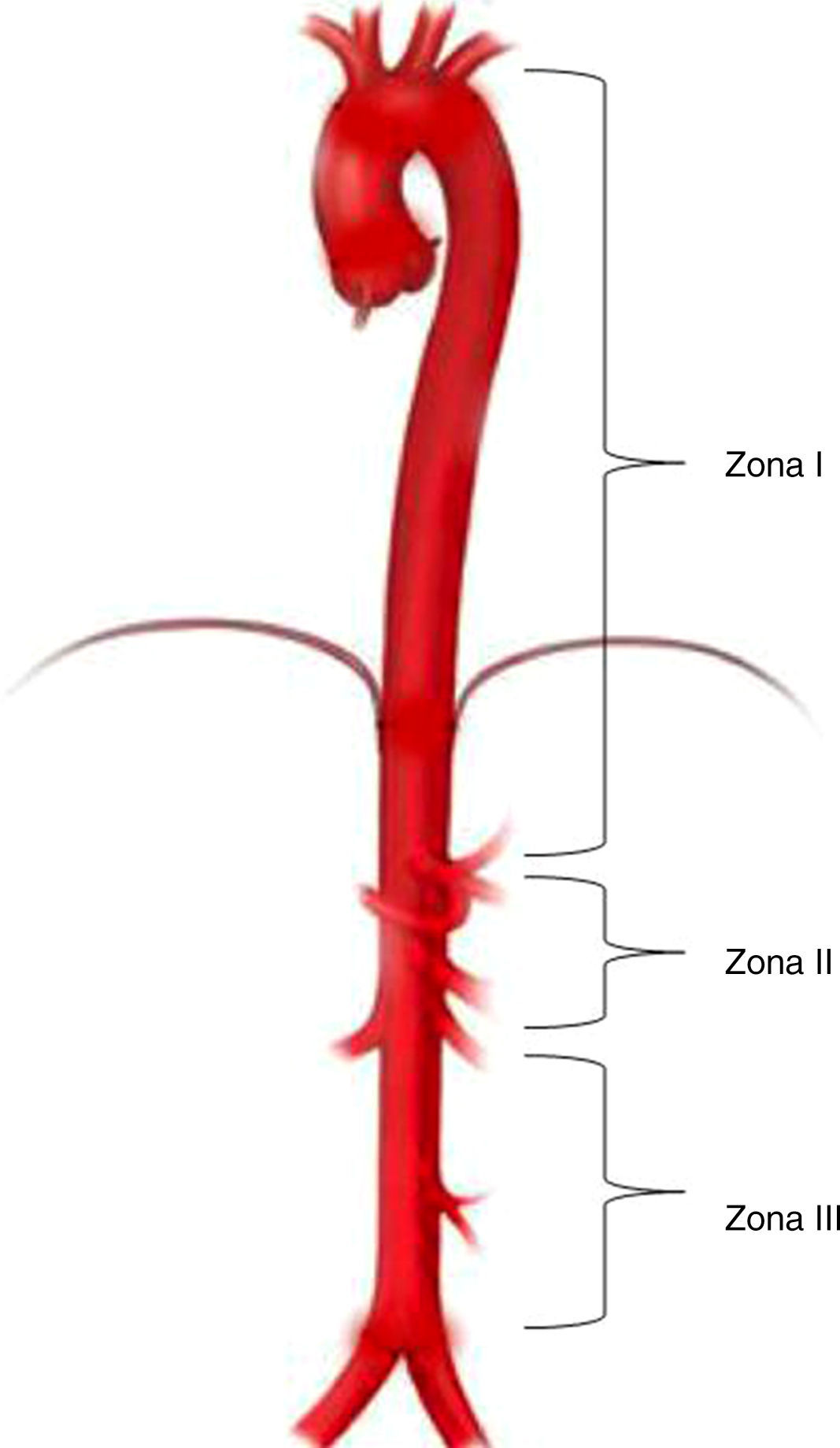
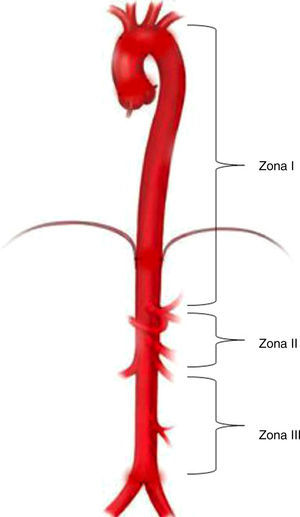
Zonas de oclusión aórticaEl nivel de la oclusión en REBOA depende de la indicación y del origen del sangrado. Se han identificado tres zonas anatómicas diferentes en la aorta para el despliegue del balón25. La zonai se encuentra entre la arteria subclavia izquierda y el tronco celiaco; la zonaii se caracteriza por ser una región de no oclusión que se extiende desde el tronco celiaco hasta la arteria renal más distal, y la zonaiii desde la arteria renal hasta la bifurcación de la aorta25 (fig. 2).
Indicaciones de REBOA en traumaLas indicaciones potenciales, basadas en estudios militares26, sugieren reservar el uso de REBOA para lesiones con una puntuación de 3 o más en la Escala abreviada de lesiones (Abbreviated injury scale [AIS]), equivalente a una lesión de combate severa que pone en riesgo inminente la vida del paciente26,27.
Se consideran indicaciones potenciales: a)el despliegue de REBOA en zonai en hemorragia abdominal secundaria a lesión severa (AIS≥3) de un órgano sólido, lesión mesentérica o de vasos proximales a la bifurcación de la aorta, y b)el uso de REBOA en zonaiii en hemorragia pélvica o inguinal con lesión severa (AIS≥3) del anillo pélvico asociada a fractura, amputación cercana a la articulación de la cadera o lesión vascular proximal a la arteria femoral26,27, ambos escenarios acompañados de una presión arterial sistólica inferior a 90mmHg en el momento de la llegada al hospital.
Los reportes clínicos existentes en civiles han corroborado que los pacientes con lesiones en abdomen o pelvis asociadas a shock hemorrágico con colapso circulatorio inminente conforman la población que más se beneficia del uso de REBOA en trauma12,28,29.
Con base en la evidencia disponible, tanto en militares como en civiles, Biffl et al.30 proponen un algoritmo para el control hemorrágico. En este sugieren considerar el uso de REBOA en pacientes con hemorragia no compresible abdominal y/o pélvica, en estado de shock hemorrágico, siempre y cuando se presenten aún con pulso palpable.
Hasta el momento no existe un consenso publicado que enumere las indicaciones para el uso de REBOA en trauma27. Al ser una intervención compleja, REBOA se encuentra todavía en fase de desarrollo y la evidencia disponible no es suficiente para proveer recomendaciones fuertes y contundentes sobre sus indicaciones y contraindicaciones18,31.
Trauma abdominalLas lesiones abdominales traumáticas contribuyen con un 15-20% de la mortalidad general en trauma32. El abdomen es una cavidad altamente vascularizada y los pacientes que sufren trauma abdominal severo tienen un alto riesgo de presentar hemorragia masiva, requiriendo reparación quirúrgica inmediata de las lesiones vasculares33.
El paciente con trauma abdominal, inestabilidad hemodinámica y sospecha de lesión intraabdominal debe ser llevado a laparotomía exploratoria para el control definitivo del sangrado y reparación de las lesiones o control de daños33,34. Muchos de estos pacientes requieren toracotomía con pinzamiento de la aorta, una técnica que inicialmente fue desarrollada bajo el concepto de toracotomía pre-laparotomía y cuyo objetivo era prevenir el colapso cardiocirculatorio y ayudar en el control de la hemorragia intraabdominal10. Sin embargo, estudios posteriores demostraron que la exploración simultánea de dos cavidades (toracotomía +laparotomía) es un predictor independiente de la mortalidad35. De ahí que surgiera la necesidad de opciones menos invasivas que la toracotomía tradicional para la oclusión aórtica.
En consecuencia, ante el trauma abdominal asociado a inestabilidad hemodinámica REBOA estaría indicado en los casos extremos, antes de la exploración abdominal, en reemplazo de la oclusión aórtica tradicional por toracotomía.
En los casos de shock hemorrágico en trauma abdominal, contuso o penetrante, se ha mostrado que el despliegue de REBOA en zonai podría contribuir a la estabilización hemodinámica de los pacientes y a la disminución del hemoperitoneo, facilitando la laparotomía de control de daños y la identificación de la fuente de sangrado25,36.
REBOA se ha utilizado en el manejo no operatorio del trauma abdominal cerrado asociado a inestabilidad hemodinámica. Ogura et al.37 reportaron una serie de 7 pacientes con estas características tratados con REBOA y angioembolización, con una sobrevida a 28días del 86%, concluyendo que la combinación de REBOA y angioembolización podría ser una alternativa efectiva en estos casos. También, una experiencia reciente con un caso de trauma hepático gradov asociado a hemorragia abdominal masiva mostró que REBOA es una intervención efectiva para el manejo del trauma abdominal severo38.
Trauma pélvicoAproximadamente el 15% de los pacientes con fracturas pélvicas se presentan con lesiones complejas de la pelvis, y de estos, el 4% tienen lesiones arteriales asociadas39. En estos pacientes la mortalidad es alta, y se ha demostrado que la cantidad de sangre transfundida es un predictor independiente de la mortalidad40, razón por la cual el control proximal de la hemorragia es un requisito fundamental para mejorar el pronóstico y la sobrevida.
La investigación traslacional demuestra que el uso de REBOA proporciona un mejor control de la pérdida sanguínea y se relaciona con menor mortalidad en modelos animales con hemorragia pélvica asociada a coagulopatía41. De igual manera, la investigación clínica ha corroborado los hallazgos de los modelos animales y ha evidenciado que REBOA podría ser una técnica efectiva para el control del sangrado en pacientes con fracturas pélvicas y shock hemorrágico18,42.
En pacientes con fractura pélvica e inestabilidad hemodinámica (PAS<90mmHg) la mortalidad prehospitalaria puede llegar a ser hasta del 78%29. En estos pacientes el shock hemorrágico es generalmente de origen arterial, por lo que el uso de REBOA asociado a empaquetamiento pre-peritoneal y/o angioembolización es una opción terapéutica a considerar29,43.
El paciente traumatizado con fractura pélvica severa e inestabilidad hemodinámica tiene indicación para ser llevado a control quirúrgico del sangrado y control de daños. Cuando hay marcada inestabilidad hemodinámica, debe considerarse REBOA para sostener la perfusión proximal mientras se logra el control de la hemorragia29,43. El despliegue de REBOA en la zonaiii, en presencia de fracturas del anillo pélvico con shock hemorrágico, podría ser una maniobra efectiva para el control hemorrágico en ausencia de sangrado abdominal18. Además, la oclusión aórtica infrarrenal tiene la ventaja de mantener la perfusión renal y visceral, disminuyendo las complicaciones posteriores al uso del balón.
Con relación a lo antes planteado, la Western Trauma Association incorporó en su guía de manejo de fracturas pélvicas asociadas a inestabilidad hemodinámica el uso de REBOA como un complemento o alternativa al empaquetamiento pélvico pre-peritoneal44.
ContraindicacionesCon base a la evidencia disponible, se ha propuesto que REBOA podría ser perjudicial en shock hemorrágico asociado a trauma cervico-torácico, contuso o penetrante, específicamente en casos de lesiones cardiacas y aórticas, ya que la oclusión en zonai podría exacerbar el sangrado y acelerar el colapso cardiocirculatorio8, por lo que los consensos actuales recomiendan que en estos escenarios los pacientes sean llevados directamente al quirófano para toracotomía de emergencia30.
Estudios comparativos de REBOAPocos estudios han sido desarrollados con el objetivo de estudiar la efectividad del REBOA, en comparación con la oclusión aórtica tradicional por toracotomía. Abe et al.45 compararon los desenlaces relacionados con el uso de REBOA y la oclusión aórtica tradicional en pacientes con trauma; en este estudio, el uso de REBOA se asoció con una menor mortalidad comparado con la oclusión aórtica tradicional por toracotomía. Adicionalmente, los pacientes que fueron sometidos a REBOA tuvieron una menor incidencia de complicaciones torácicas. En otros estudios, en los que se usó el score de propensión para estudiar el efecto de REBOA sobre la mortalidad, se encontró una asociación entre el REBOA y un exceso de mortalidad46,47.
ComplicacionesRelacionadas con la insuflación del balónLa preocupación principal con REBOA es la lesión isquémica en los tejidos distales a la oclusión. Al respecto, la investigación en modelos animales se ha centrado en establecer tiempos de oclusión seguros, donde el riesgo de alteraciones fisiológicas sea mínimo o reversible. Así pues, Avaro et al.21 estudiaron un modelo animal de shock hemorrágico y establecieron que 40min es un tiempo de oclusión aórtica seguro. En la misma línea, Scott et al.48 reportaron que 60min de oclusión aórtica con REBOA es un tiempo tolerable sin daños orgánicos irreversibles a pesar de las alteraciones fisiológicas evidenciadas. Por su parte, Markov et al.49 evaluaron la tolerancia fisiológica a la oclusión endovascular en trauma, encontrando que un tiempo de oclusión de 90min produce daños orgánicos irreversibles, como por ejemplo necrosis hepática e injuria renal aguda.
Estudios realizados en humanos han mostrado que el tiempo de oclusión aórtica con REBOA es mucho menor en los sobrevivientes, demostrando que la oclusión prolongada se asocia a un aumento de la mortalidad28,50,51. Adicionalmente, de todos los casos publicados sobre el uso de REBOA en humanos solo dos han sobrevivido a un tiempo de oclusión mayor a 90min37,51.
Además de la lesión hepática y renal, otras lesiones isquémicas podrían estar relacionadas con la oclusión aórtica prolongada. Entre ellas están: parálisis por isquemia de la médula espinal, amputación de miembros inferiores, isquemia intestinal y falla multiorgánica8,28,52,53.
Como se ha mencionado, la oclusión aórtica en trauma restablece la perfusión cardiaca y cerebral por periodos cortos de tiempo. Sin embargo, el aumento sostenido de la presión arterial podría ser nocivo para los órganos proximales al despliegue del balón54.
Con respecto a lo antes mencionado, Uchino et al.55 reportaron un caso de hemorragia intracraneal masiva secundaria al uso de REBOA. En este caso, REBOA fue usado para el control de la hemorragia secundaria a una fractura pélvica compleja. Después de la oclusión aórtica con REBOA y mientras se realizaba la angioembolización, la presión arterial sistólica alcanzó valores superiores a los 180mmHg. Este aumento suprafisiológico de la presión arterial se asoció a la aparición de hemorragia intracraneal masiva, no reportada al ingreso del paciente.
Por tanto, evitar la hipertensión suprafisiológica podría disminuir el riesgo de complicaciones desencadenadas por el aumento de flujo cerebral, cardiaco y pulmonar24,52,55,56.
Relacionadas con la descompresión del balónLa isquemia distal por oclusión endovascular prolongada altera la fisiología celular, disminuyendo la producción de energía y aumentando la de ácido láctico por la transición del metabolismo aeróbico a anaeróbico. El restablecimiento del flujo en estos tejidos causa la liberación de radicales libres y mediadores inflamatorios que generan una lesión por reperfusión54,56. La reacción inflamatoria asociada a la lesión de los tejidos por isquemia-reperfusión empeora el síndrome de respuesta inflamatoria sistémica, ya iniciado por la lesión traumática, y las intervenciones quirúrgicas para el control de daños25,54.
Kralovich et al.57 evaluaron en un modelo animal los efectos hemodinámicos de la oclusión aórtica en shock hemorrágico. En este estudio encontraron que durante el periodo de reanimación posterior al restablecimiento del flujo aórtico hubo alteraciones en la función ventricular izquierda, en el consumo de oxígeno y en la presión de perfusión coronaria. Por lo anterior, se debe tener precaución en el momento de desinflar el balón, principalmente por la combinación de la caída abrupta de la presión arterial, la disminución de la contractilidad miocárdica y la lesión por isquemia-reperfusión, que ponen al paciente a riesgo de colapso hemodinámico si el equipo no toma las medidas preventivas necesarias25,54. Inflar y desinflar intermitentemente el balón se ha recomendado para disminuir la intensidad de los efectos deletéreos relacionados con la descompresión de REBOA25.
Relacionadas con la técnicaEl procedimiento para la colocación del balón aórtico endovascular se resume en cinco pasos: el acceso arterial, el posicionamiento del balón, la inflación del balón, la descompresión del balón y la remoción de la camisa25. REBOA se realiza mediante la técnica de Seldinger58. Las complicaciones relacionadas con la técnica han sido evidenciadas, en su mayor parte, al realizar el acceso arterial y al introducir o remover la camisa50.
El acceso arterial se hace de manera percutánea a través de la arteria femoral común. Este paso también puede realizarse con la ayuda de ultrasonografía o mediante la identificación quirúrgica directa de la arteria25. Durante el acceso hay riesgo de lesión vascular por punción directa o al insertar el catéter. Dentro de las posibles complicaciones reportadas se encuentran: lesión de la arteria femoral, disección y perforación de la aorta, embolización, embolismo aéreo e isquemia periférica18,50. Sin embargo, se ha descrito que estas complicaciones son raras y se relacionan con múltiples intentos de punción52.
Posteriormente, se introduce la camisa a través de una guía25. Tradicionalmente, REBOA se hace con camisas grandes de 10-14Fr. Esto se ha relacionado con complicaciones severas como embolia con amputación de miembro inferior secundaria, disección, pseudoaneurisma y fístula arteriovenosa de la arteria femoral50,52,59.
Otra de las complicaciones reportadas es la rotura del balón. Matsuda et al.60 reportaron tres rupturas de balón en 125 pacientes con aneurisma de aorta abdominal.
El futuroEl objetivo a corto plazo es validar la seguridad, la efectividad y la viabilidad de REBOA en trauma para que este procedimiento sea adoptado universalmente. Los esfuerzos están siendo dirigidos a disminuir las complicaciones. El desarrollo de nuevos dispositivos, la disminución del tiempo de isquemia, el fortalecimiento de la técnica, el incremento de personal entrenado, entre otros, son factores que podrían reducir estas complicaciones.
El desarrollo de un dispositivo o kit diseñado para REBOA en trauma es una necesidad. Los catéteres para balón endovascular actualmente disponibles (CODA balloon catheter, Cook Medical, Bloomington, IN, Estados Unidos) son de gran tamaño (9 y 10Fr) y están diseñados para otras indicaciones diferentes a trauma. Un catéter más pequeño disminuye el contacto con la íntima, disminuyendo el riesgo de eventos tromboembólicos durante la remoción de la camisa59. El catéter de 7Fr (ER-REBOA, Prytime Medical Devices Inc., Boerne, TX, Estados Unidos) es uno de estos nuevos dispositivos que hasta el momento no se ha relacionado con lesiones vasculares, hematomas ni complicaciones embólicas. Su tamaño favorece la remoción del dispositivo y el cese del sangrado mediante compresión directa, sin la necesidad de hacer arteriotomía como se recomienda al utilizar las camisas más grandes59,61.
La preocupación con respecto a la isquemia prolongada y sus implicaciones ha hecho que surjan técnicas alternativas como el REBOA parcial (P-REBOA), que permite mantener algo de perfusión distal al no inflar el balón completamente54, y el REBOA intermitente (I-REBOA), donde se alterna entre periodos de oclusión completa y no oclusión8.
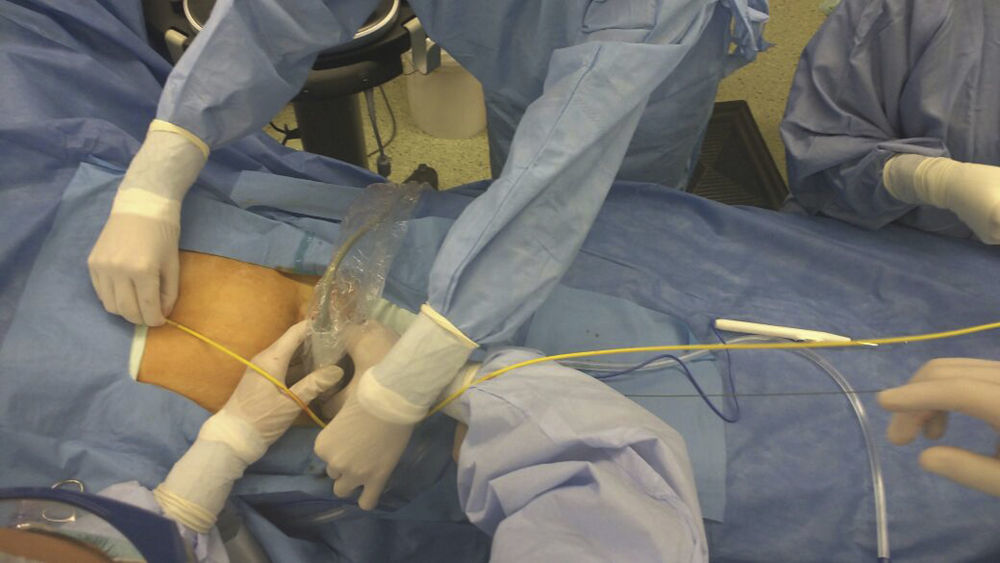
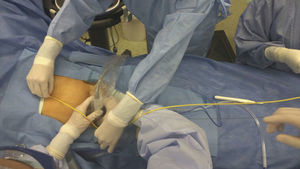
La verificación de la posición del balón es muy importante para prevenir complicaciones. A pesar de ser confiable, la utilización de fluoroscopia en urgencias puede tener desventajas relacionadas con la disponibilidad y el tiempo empleado en la verificación62. Por esta razón, se ha propuesto colocar el balón utilizando referencias anatómicas externas, sin necesidad de imágenes52. En este sentido, un estudio realizado en cadáveres por Linnebur et al.63 reportó un éxito del 100% en el despliegue de REBOA en zonai utilizando como referencia anatómica la distancia entre el sitio de punción y la mitad del esternón. En nuestra experiencia el uso de la medición por referencias anatómicas es un método confiable y seguro para la inserción de REBOA en zonai y zonaiii (fig. 3).
Para aumentar el éxito de REBOA en trauma y lograr que haga parte del protocolo estándar de reanimación se debe asegurar el acceso oportuno. Esto implica que el entrenamiento del personal de urgencias sea adecuado, estandarizado y acreditado15,62. De igual manera, se debe fortalecer la exposición a procedimientos endovasculares en los programas de residencia, idealmente implementándolo como parte del currículo académico64. Se ha demostrado que incluso la realidad de simulación virtual es efectiva en la adquisición de competencias para procedimientos endovasculares en control de daños65.
Probablemente el futuro también incluya el uso prehospitalario de REBOA en trauma. En este sentido, Sadek et al.66 reportaron el primer caso exitoso de oclusión aórtica prehospitalaria en un paciente con hemorragia no compresible de origen pélvico.
ConclusiónREBOA podría ser maniobra segura y efectiva para el control de la hemorragia y la prevención del colapso cardiocirculatorio en pacientes con trauma. Parece que su mayor utilidad se encuentra en pacientes con hemorragia no compresible del torso de origen pélvico y abdominal.
Existen dudas sobre su seguridad en pacientes con trauma torácico, por lo que se contraindica en trauma asociado a hemorragia no compresible en esta región corporal. En el futuro REBOA podría reemplazar a la toracotomía de emergencia en pacientes con hemorragia no compresible de origen abdominal y pélvico cuando esta se asocie a riesgo de colapso cardiocirculatorio. Sin embargo, es necesario que se realicen más estudios prospectivos y comparativos para probar su efectividad.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesNinguno. Los autores declaran que no tienen ningún interés comercial o asociativo que presente un conflicto de interés con el trabajo presentado.
Muchas gracias al Dr. Jesús Edigio Solís por sus recomendaciones en el transcurso de la escritura de este manuscrito.