El uso de expansor mamario, previo a la reconstrucción definitiva con prótesis, no está exento de complicaciones. Las mismas no solo tienen relación con la presencia de radioterapia perioperatoria, o factores propios de las pacientes, sino que también guardan relación con la cobertura muscular íntegra del expansor mamario.
Material y métodosRevisión retrospectiva de pacientes sometidas a reconstrucción mamaria diferida utilizando una modificación de la técnica del cierre de bolsillo submuscular con celulosa oxidada regenerada NU-KNIT® de expansor mamario. Entre el 1 de enero de 2014 y el 31 de diciembre de 2015 un solo cirujano plástico (J.V.) de la Unidad de Patología Mamaria de la Clínica Alemana de Santiago realizó reconstrucción con dicha técnica en 31 pacientes. Se describe la modificación de la técnica, así como los datos demográficos, histológicos y complicaciones de la fase de expansión de las mismas.
ResultadosSe realizaron 40 reconstrucciones mamarias en 31 pacientes. Se presentaron 11 seromas (27,5% del total de los expansores), 2 sufrimientos de colgajo cutáneo con dehiscencia de la herida (5% de los expansores) y una infección de la herida operatoria (2,5% de los expansores). Dos pacientes requirieron aseo quirúrgico por dehiscencia e infección. Una paciente requirió explantación del expansor (2,5% del total de los expansores).
DiscusiónLa modificación de la técnica quirúrgica representa una alternativa segura y reproducible para lograr un cierre total del bolsillo muscular y con ello la cobertura completa del expansor, evitando así algunas de las complicaciones descritas secundarias a una cobertura insuficiente del mismo.
The use of breast expander, prior to the final prosthetic reconstruction, is not exempt from complications. They not only relate to the presence of peri-operative radiation therapy, or patient-related issues; but also related to the muscle integrate coverage of the breast expander.
Material and methodsRetrospective review of patients undergoing deferred breast reconstruction using a modification of the technique of sub muscular pocket closing with oxidized regenerated cellulose NU-KNIT™ for the breast expander. Between January 1, 2014 and December 31, 2015 one plastic surgeon (J.V.), from the Breast Pathology Unit at Clínica Alemana de Santiago, performed reconstruction surgeries with this technique in 31 patients. In the present article, the technique modification, demographic data, histological data and the complications which arose during the expansion phase of the same, will be described.
Results40 breast reconstructions were performed in 31 patients. 11 seromas (27.5% of total expanders), 2 sufferings of skin flap wound dehiscence (5% expanders) and 1 wound infection (2.5% of expanders) were presented. Two patients required surgical debridement due to surgical dehiscence and infection. One patient required explantation of the expander (2.5% of total expanders).
DiscussionThe modification of the surgical technique represents a safe and reproducible alternative to achieve a complete closure of the muscular pocket and thus a complete coverage of the expander, consequently; avoiding some of the secondary complications drawn from an insufficient coverage of the expander.
La reconstrucción mamaria puede llevarse a cabo de forma inmediata después de la mastectomía o de forma diferida. Si bien existen distintos factores para elegir uno u otro timing, la necesidad de radioterapia tras la mastectomía es probablemente el factor más importante a considerar. De esta manera, en términos generales, se recomienda realizar una reconstrucción diferida en pacientes que van a recibir irradiación, mientras que en pacientes sin indicación de dicha adyuvancia, la reconstrucción inmediata es una buena alternativa.
Dentro de las técnicas de reconstrucción, existen 3 grandes grupos: las que utilizan materiales aloplásticos únicamente; las que utilizan tejidos autógenos, y las que usan ambos elementos. La decisión de cuál técnica utilizar estará influenciada por factores tanto de la paciente como del cirujano y del centro hospitalario.
La reconstrucción mamaria con implantes es la técnica más frecuentemente utilizada en nuestro país así como en el resto del mundo1-4. Si bien puede realizarse en prácticamente cualquier paciente, las mejores candidatas a este tipo de reconstrucción son aquellas con mamas de tamaño pequeño-mediano y con un bajo grado de ptosis5. En términos generales, la técnica de prótesis directa estaría indicada en pacientes con mamas pequeñas en las que existe piel y músculo suficientes con los que cubrir la gran mayoría de la superficie protésica. Si esto no es posible, se debe recurrir a la expansión.
Respecto al uso de prótesis y/o expansor, ya sea en forma inmediata o diferida, el sufrimiento de los colgajos cutáneos es tal vez la complicación más temida, puesto que trae consigo la exposición-infección del material aloplástico y sus consecuencias funcionales (dolor) y/o estéticas6. Durante los últimos años ha habido un interés creciente en el uso de matrices dérmicas acelulares en reconstrucción mamaria, las que han sido utilizadas para proporcionar cobertura al material aloplástico cuando el bolsillo submuscular no es capaz de cubrir por entero.
La celulosa oxidada regenerada fue desarrollada con fines hemostáticos y su uso se encuentra ampliamente documentado en la literatura médica7. Dadas las características comerciales de esta alga vegetal, que tiene tanto un rol hemostático como bacteriostático, su uso no está limitado a áreas cruentas sangrantes.
El presente trabajo tiene por objeto describir una variación de la técnica quirúrgica de reconstrucción mamaria con expansor, utilizando la celulosa oxidada (NU-KNIT®) como «pledget» en el cierre del bolsillo muscular. Junto con la descripción de dicha técnica, se presenta la casuística inicial de pacientes que han sido sometidas a esta modificación en el cierre del bolsillo muscular.
Material y métodoSe realizó una revisión retrospectiva a través de la ficha clínica electrónica y de los protocolos operatorios de la totalidad de pacientes sometidas a reconstrucción mamaria diferida con expansor mamario entre el 1 de enero de 2014 y el 31 de diciembre de 2015 por un solo cirujano plástico (J.V.) de la Unidad de Patología Mamaria de la Clínica Alemana de Santiago.
Después de la mastectomía, 31 pacientes fueron sometidas a reconstrucción mamaria utilizando la técnica modificada del cierre de bolsillo muscular con NU-KNIT®. El tamaño del expansor se eligió basándose en el peso y la talla (IMC), el contorno de la mama, el ancho de la pared torácica y el volumen de mama resecada.
Se evaluaron las complicaciones solo durante la etapa de expansión de tejido, las cuales incluyeron: necrosis de piel, contractura capsular, dehiscencia de la herida operatoria, infección, rotura del implante, seroma y hematoma. Se registraron los procedimientos de exploración no programada de expansores mamarios así como la necesidad de explantación de los mismos. La infección se definió como cambios inflamatorios locales que requirieron tratamiento antibiótico y/o intervención quirúrgica. La contractura capsular se definió según la clasificación de Baker.
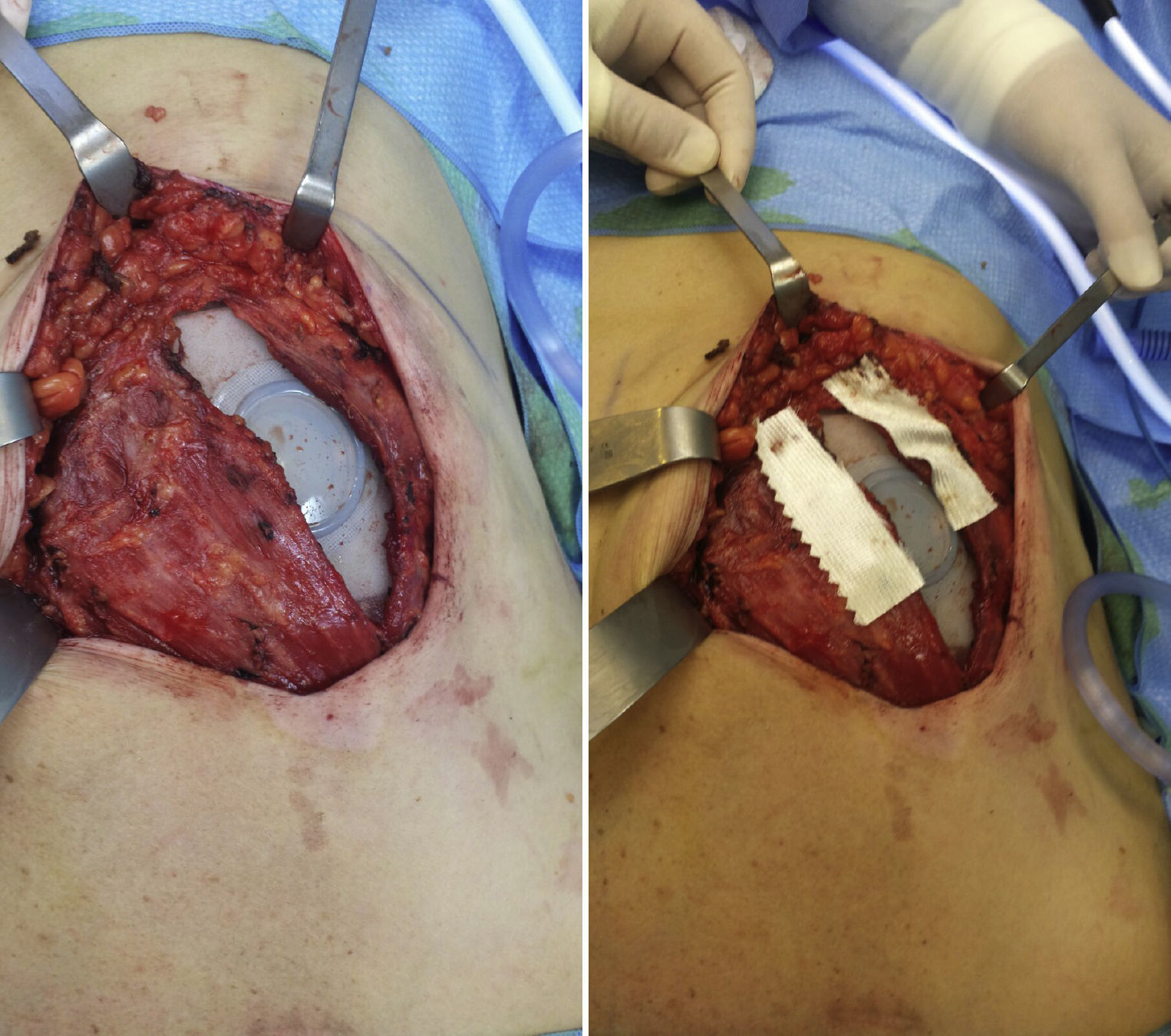
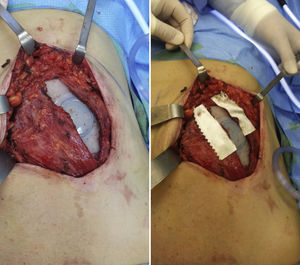
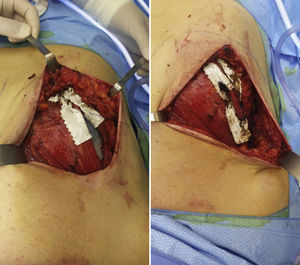
Modificación de la técnica quirúrgicaLa técnica quirúrgica de instalación del expansor no difiere mayormente de la publicada en la literatura8. Esta consiste en la elaboración de un bolsillo submuscular, con acceso a través del límite lateral del músculo pectoral mayor. Se realiza una disección medial e inferior para lograr la cobertura total del expansor tisular. El cierre del bolsillo muscular antes descrito, previa colocación del expansor, se realiza con material reabsorbible. Esto último no resulta siempre factible, o fácil de lograr, ya sea por lo delgado del pectoral mayor, o bien por la dificultad de la disección del mismo, momento en el cual se puede producir la rotura parcial del músculo o bien la desinserción a nivel costal del mismo. Dicha rotura o desinserción trae consigo sangrado y por tanto mayor dificultad técnica en la elaboración del bolsillo. Para logar la cobertura total del expansor, se hace necesario entonces la elaboración de un colgajo de músculo pectoral menor, recto abdominal, o serrato en el caso del borde lateral del expansor. Para evitar la elaboración de colgajos musculares distintos al pectoral mayor, hemos modificado la técnica de cierre del bolsillo muscular. La misma no tiene por objeto reemplazar el músculo pectoral mediante el uso de celulosa oxidada, sino que logra reforzar las propias fibras musculares evitando que las mismas se desgarren con la tracción necesaria durante el cierre hermético y la cobertura total del expansor subyacente. Utilizando la presentación comercial NU-KNIT®, se instalan 2 láminas de aproximadamente 2,5cm de ancho en cada uno de los bordes del abordaje del bolsillo muscular. Utilizando material reabsorbible, se procede al cierre del bolsillo, con puntos continuos tipo colchonero vertical a través de dichas láminas. De esta forma, se logra una adecuada hemostasia de los bordes musculares y el cierre hermético del bolsillo descrito. Se completa la cirugía con la instalación de un drenaje cerrado en la axila y, según la necesidad, un segundo drenaje cerrado en relación con el lecho mamario. Se realiza el cierre por planos de la mastectomía y la curación de la herida operatoria (figs. 1 y 2).
La expansión tisular se inicia de 3 semanas a un mes después de la cirugía con infiltraciones semanales de un 10% de la capacidad total del expansor hasta alcanzar un volumen acorde con las necesidades y deseos de reconstrucción del cirujano y de la paciente. Una vez alcanzado el volumen, se deja un periodo de aproximadamente una semana antes de sustituir el expansor por la prótesis mamaria definitiva. Tres meses más tarde, se realiza la reconstrucción del complejo aréola-pezón (CAP) y la cirugía de la mama contralateral para simetrización, cuando así lo desee la paciente.
ResultadosEntre el 1 de enero de 2014 y el 31 de diciembre de 2015, un total de 31 pacientes fueron sometidas a reconstrucción mamaria diferida con expansor por uno de los autores del presente artículo, en la Unidad de Patología Mamaria de la Clínica Alemana de Santiago.
Se realizaron un total de 22 reconstrucciones unilaterales y 9 reconstrucciones bilaterales, lo que constituye un total de 40 reconstrucciones mamarias diferidas con expansor. El tiempo de seguimiento promedio de las pacientes antes mencionadas fue de 16 meses (5-27 meses).
Los datos demográficos, la histología tumoral, así como la neoadyuvancia y/o adyuvancia de las pacientes reconstruidas se detallan en la tabla 1.
Antecedentes demográficos, histológicos y terapias complementarias
| Variable | Valor |
|---|---|
| Pacientes, n | 31 |
| Mama, n | 40 |
| Unilateral | 22 |
| Bilateral | 9 |
| Edad, años (media±DE) | 48,3±10,3 |
| Índice de masa corporal | 24,8±3,97 |
| Comorbilidades, n | |
| Tabaco | 8 |
| Hipertensión arterial | 2 |
| Diabetes mellitus | 0 |
| Histología tumoral, n | |
| Carcinoma ductal in situ | 8 |
| Carcinoma ductal infiltrante | 24 |
| Carcinoma lobulillar in situ | 6 |
| Carcinoma lobulillar infiltrante | 0 |
| Otros | 3 |
| Terapia neoadyuvante, n | |
| Quimioterapia | 5 |
| Radioterapia | 2 |
| Terapia adyuvante, n | |
| Quimioterapia | 17 |
| Radioterapia | 6 |
En la totalidad de las pacientes de nuestra serie, se realizó una mastectomía total (MT) sin conservación del CAP. Solo 2 pacientes fueron a la reconstrucción mamaria (instalación del expansor) en un tiempo diferente al de la mastectomía; vale decir que en las otras 29 pacientes, la instalación del expansor se llevó a cabo en el mismo tiempo de la mastectomía.
Respecto del tipo de procedimientos oncológicos asociados a la instalación del expansor, se realizaron 6 MT + expansor, 29 MT con linfonodo centinela (LNC) + expansor y 5 pacientes fueron a MT + disección axilar (DAX) + expansor.
Utilizando la modificación del cierre del bolsillo muscular antes descrito, se presentaron un total de 11 seromas (27,5% del total de los expansores), 2 sufrimientos de colgajo de mastectomía con dehiscencia de la herida (5% de los expansores) y una infección de la herida operatoria (2,5% de los expansores). No se registraron hematomas así como tampoco contracturas capsulares en la fase de expansión. Respecto a la necesidad de exploración quirúrgica no programada, 2 pacientes requirieron de aseo quirúrgico por dehiscencia e infección del expansor. Solo en una de estas pacientes hubo necesidad de retirar dicho expansor (2,5% del total de los expansores).
A 31 de diciembre de 2015, un total de 24 (77,4%) pacientes habían terminado su proceso de expansión. El volumen medio de expansión fue de 397ml, con una desviación estándar de 64ml.
DiscusiónLa reconstrucción mamaria diferida con el uso de expansor y posterior recambio a prótesis, como ya se ha dicho, es hoy por hoy el método de reconstrucción más utilizado en el mundo1-4. Si bien esta puede ser considerada una técnica «simple», comparada con aquellas que utilizan sólo tejido autógeno como base de reconstrucción, no está exenta de riesgos y potenciales complicaciones. Estas potenciales complicaciones representan un problema para el binomio médico-paciente, puesto que en casos determinados puede significar el cambio de estrategia reconstructiva. La literatura se ha hecho cargo de estas complicaciones, dividiéndolas en aquellas que se pueden observar en el postoperatorio inmediato y aquellas que se hacen presentes en el largo plazo. Dentro de las primeras, se describen el hematoma y seroma; ambas complicaciones per se no indicarían una exploración y subsecuente retiro del expansor. Ahora bien, la principal y más temida complicación de esta técnica es la exposición-infección del expansor. Es importante mencionar que la literatura habla de complicaciones de hasta un 50% en pacientes sometidas a radioterapia9-11.
Respecto a la casuística actualmente presentada utilizando la modificación del cierre muscular, la tasa de reexploración y pérdida del implante resultan considerablemente menores que las presentadas en la literatura, tanto en pacientes sometidas a radioterapia como en aquellas que no recibieron dicho tratamiento de adyuvancia o neoadyuvancia. La explicación a nuestra baja presentación de complicaciones, no responde necesariamente a la introducción de esta nueva técnica de cierre de colgajo muscular, siendo factible el bajo tamaño muestral como una de las respuestas a esta interrogante.
En nuestra experiencia, las complicaciones del postoperatorio inmediato son porcentualmente menores que las reportadas en la literatura. Un estudio retrospectivo en población taiwanesa presenta complicaciones en la etapa de expansión mamaria de un 16,3%. Las más frecuente son: necrosis de colgajo (4,9%) y dehiscencia de herida operatoria (4,1%) que llevaron al retiro del expansor en un 5,8% de los casos. Nos atrevemos a compararnos con este trabajo, puesto que la población estudiada de 238 pacientes (230 reconstrucciones unilaterales y 8 bilaterales) se asemeja demográficamente a nuestra casuística. Esto pues, las cifras de dicha población presentan promedios de IMC menores que la población caucásica de estudios norteamericanos, con edades de presentación del cáncer más tempranas y menores porcentajes de tabaquismo asociado12. Estos 3 últimos puntos la literatura los ha señalado, junto con la radioterapia, como los factores más importantes asociados a complicación en reconstrucción mamaria con expansor-prótesis4,13-19.
No cabe duda que la total cobertura muscular del expansor es fundamental para evitar complicaciones asociadas a su uso. Sin embargo, en el análisis de los resultados antes expuestos, resulta difícil separar las complicaciones derivadas de la nueva técnica descrita, respecto de las condiciones propias de las pacientes y/o de la mastectomía que den cuenta de dichas complicaciones. En la misma línea, y respecto al uso de matrices dérmicas acelulares en la reconstrucción mamaria que asegurarían la cobertura total del expansor o de la prótesis, algunos metaanálisis dan cuenta del mayor número de complicaciones asociadas al uso de matrices en la reconstrucción mamaria. Tal es el caso del trabajo de Hoppe et al., en el que se incluyen 7 trabajos comparativos entre el uso vs. no uso de matrices dérmicas acelulares en la reconstrucción mamaria, encontrando mayor riesgo de seroma, infección y explantación protésica20,21.
Por otra parte, respecto a la recomendación del uso de matrices acelulares en el primer tiempo de la reconstrucción con expansor-prótesis, la literatura menciona que la cobertura submuscular completa del expansor produciría un surco mamario mal definido, una reconstrucción amorfa y carente de la ptosis natural de la mama; sin embargo, algunos grandes estudios retrospectivos han encontrado excelentes resultados estéticos prescindiendo de las matrices acelulares21-25.
Lo anterior consideramos que resulta pertinente a la discusión, puesto que lograr la completa cobertura muscular del expansor es la clave para evitar las complicaciones asociadas al uso del mismo en la reconstrucción mamaria. Dicha cobertura, en muchas pacientes resulta dificultosa dadas las características anatómicas del músculo pectoral mayor o bien las condiciones de la pared torácica tras ser sometida a radioterapia.
En suma, consideramos que la modificación de la técnica quirúrgica presentada representa una alternativa segura y reproducible que ayuda al cirujano a lograr un cierre total del bolsillo muscular y con ello la cobertura completa del expansor, evitando así algunas de las complicaciones descritas secundarias a una cobertura insuficiente del mismo. La presentación de estudios prospectivos que consideren un mayor número de pacientes resulta fundamental para proponer este método como la alternativa al uso de otros colgajos musculares distintos al pectoral mayor o matrices dérmicas acelulares en la fase de expansión mamaria.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores del presente trabajo declaran no tener ningún tipo de conflicto de interés, así como tampoco subvención para la realización del mismo.
A la Unidad de Patología Mamaria de la Clínica Alemana de Santiago, a la Unidad de Patología Mamaria del Hospital Padre Alberto Hurtado y al Servicio de Cirugía Adultos del Hospital Padre Alberto Hurtado.