La neumonía herpética es una rara enfermedad que afecta casi con exclusividad a personas con un déficit de inmunidad. Con frecuencia tiene un desenlace fatal.
Su aparición está descrita en los primeros 2 meses luego del trasplante pulmonar, pero en nuestra experiencia se evidenció después de los 10 meses, 1 año y medio, 8 y 19 años.
Describimos los hallazgos tomográficos detectados en 4 pacientes con trasplantes pulmonares que cursaron neumonía herpética. Presentaban fiebre, tos, expectoración y disnea, con empeoramiento progresivo de su clase funcional, y todos fallecieron tras la aparición de la enfermedad. El diagnóstico histológico se realiza mediante lavado bronquioalveolar o biopsia transbronquial, con posterior tinción con hematoxilina-eosina y/o marcación inmunohistoquímica.
Los hallazgos tomográficos destacados fueron: opacidades en vidrio esmerilado de distribución parcheada, consolidación del espacio aéreo, derrame pleural y bronquiectasias.
Debido a su baja frecuencia y mal pronóstico, es importante conocer y tener presente esta entidad en personas trasplantadas de pulmón para no demorar el diagnóstico y actuar lo más rápidamente posible.
Herpetic pneumonia is a rare disease that mostly affects people with immune deficiency whose outcome is frequently fatal.
Its appearance is described in the first two months after surgery. In our experience it was evidenced in the post transplant apart since 10 months, 1 ½ years, 8 years and 19 years after the transplant.
We described the CT findings detected in 4 lung transplant recipient that had evolved with herpetic pneumonia. Patients presented fever, cough, sputum and dyspnea with progressive worsening of functional class, four died after the disease.
The histological diagnosis is made by bronchoalveolar lavage or transbronchial biopsy with subsequent staining with hematoxylin eosin and / or immunohistochemistry procedure.
The highlighted CT findings were ground-glass opacities patchy distribution, airspace consolidation, pleural effusion and bronchiectasis.
Due to its low frequency and poor prognosis is important to know this entity in lung transplant recipients to avoid a delayed diagnosis and treatment.
La neumonía por virus del herpes simple fue descrita por primera vez en 19491. Es considerada una rara entidad que afecta a pacientes con déficit inmunitario, especialmente a los trasplantados, oncológicos, virus de la inmunodeficiencia humana positivos y grandes quemados2,3. También puede presentarse en casos con injuria de la vía aérea, ya sea por intubación o por tabaquismo crónico3,4.
La enfermedad se produce por una reactivación endógena del virus. Las lesiones mucocutáneas del virus del herpes simple no siempre son visibles y, de serlo, se observan en cualquier momento en relación con las manifestaciones respiratorias2,5,6. La llegada del virus al tracto respiratorio inferior ocurre por pasaje directo desde la vía aérea superior o a través de la vía hematógena en caso de sepsis4,5.
Esta entidad se presenta con un cuadro de comienzo agudo/subagudo, caracterizado por disnea, fiebre, tos productiva y dolor torácico asociado a leucocitosis2,6. En los pacientes trasplantados de pulmón, la aparición de la enfermedad está descrita en los primeros 2 meses después de la cirugía, y el hallazgo adquiere una importancia adicional debido a su mala evolución y elevada mortalidad5,7,8. Por ello, ante la sospecha de esta patología, el lavado bronquioalveolar (BAL) más una biopsia transbronquial y el tratamiento precoz con aciclovir resultan de vital importancia9,10.
El estudio histológico de la lesión de la vía aérea se caracteriza por una necrosis epitelial y alveolar con exudado proteico asociado a un grado variable de respuesta por parte de los polimorfonucleares3,4.
El diagnóstico anatomopatológico de certeza está dado, en el BAL o material biopsiado, por la presencia de cuerpos de inclusión intranucleares en la tinción con hematoxilina-eosina (cuerpos Cowdry tipo A) y/o mediante la tinción inmunohistoquímica, que permite diferenciar los serotipos 1 y 23,4,6. Los hisopos para la demostración de las células de Tzank por medio de la tinción homónima se han dejado de lado debido a la superioridad de los otros métodos5. La serología tampoco resulta útil para diagnosticar la infección pulmonar aguda por virus herpes tipo 1, ya que hasta el 90% de las personas adultas tiene anticuerpos positivos6. En este sentido, cabe señalar que la neumonía herpética (NH) coexiste con otras infecciones bacterianas hasta en 1/3 de los casos4,11.
La broncoscopia puede arrojar un resultado normal o mostrar edema y/o eritema de la vía aérea, secreciones mucopurulentas, úlceras mucosas e, incluso, exudado fibrinoproteico (que en ocasiones forma membranas)4,6.
Los hallazgos tomográficos incluyen áreas de vidrio esmerilado de distribución parcheada, consolidación del espacio aéreo (que puede ser segmentario o subsegmentario) y engrosamiento septal asociado en algunos casos a derrame pleural y/o atelectasia3,4,12.
Descripción de los hallazgosEn nuestra institución se realizaron 280 trasplantes pulmonares y/o cardiopulmonares desde junio de 1994 hasta la fecha. Revisamos retrospectivamente los hallazgos tomográficos de los únicos 4 casos con diagnóstico anatomopatológico de neumonía por herpes simple tipo 1 mediante BAL y biopsia transbronquial con técnica de inmunohistoquímica. En estos, la broncoscopia para la obtención de las muestras se había llevado a cabo en las primeras horas del ingreso en nuestra institución, y el tiempo de obtención de los resultados no había excedido los 2 días.
Clínicamente, todos presentaron cuadros de inicio agudo con fiebre, tos, expectoración y disnea con empeoramiento de su clase funcional. Los 4 pacientes fallecieron, tras la infección.
Si bien ninguno de ellos tuvo infección bacteriana concomitante, cabe señalar que todos recibieron antibioticoterapia empírica, luego de la obtención de las muestras. Una vez confirmada la NH, los pacientes fueron tratados con aciclovir y oseltamivir endovenoso.
La enfermedad de base que motivó el trasplante fue una comunicación interventricular con hipertensión pulmonar (2 casos), una histiocitosis X (1 caso) y un enfisema (1 caso). En nuestros pacientes, la NH se presentó en el postrasplante a los 10 meses, 1 año y medio, 8 años y 19 años de la intervención.
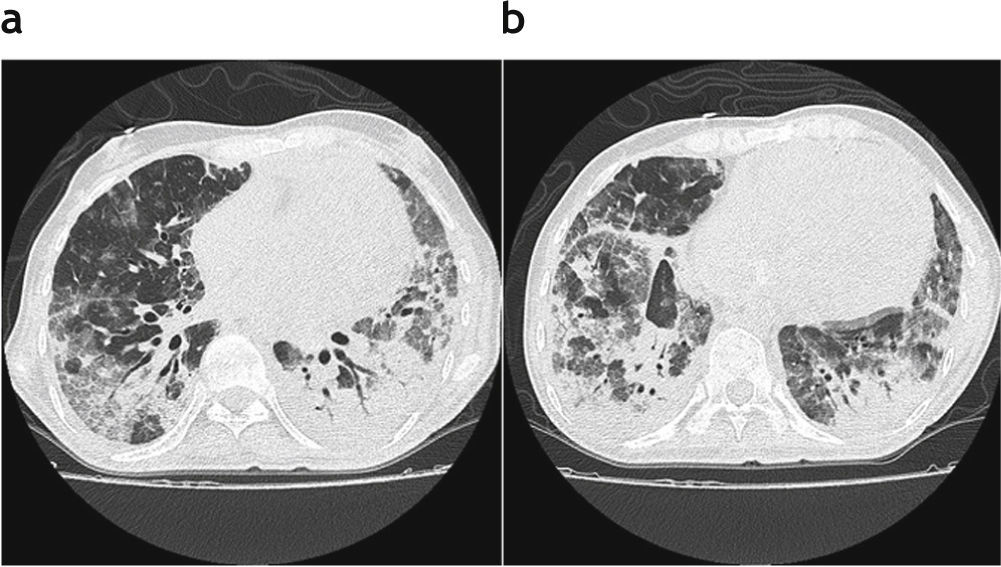
Los hallazgos tomográficos en estos pacientes mostraron opacidades en vidrio esmerilado de distribución parcheada y bilateral, predominantemente en las bases pulmonares, consolidación del espacio aéreo, engrosamiento septal y algunas bronquiectasias de tipo retráctil. En 2 pacientes se evidenció la presencia de un derrame pleural asociado (figs. 1-3, tabla 1).
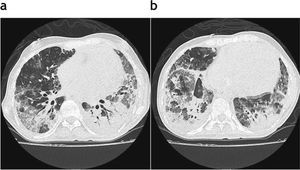
Paciente trasplantado bipulmonar por comunicación intraventricular e hipertensión pulmonar con diagnóstico de neumonía herpética a los 10 meses postrasplante. Corte axial de tomografía computada de alta resolución donde se visualizan múltiples opacidades en vidrio esmerilado de distribución difusa en ambas bases pulmonares con áreas de consolidación del parénquima pulmonar posterobasal bilateral a predominio izquierdo y algunas bronquiectasias de tipo retráctil.
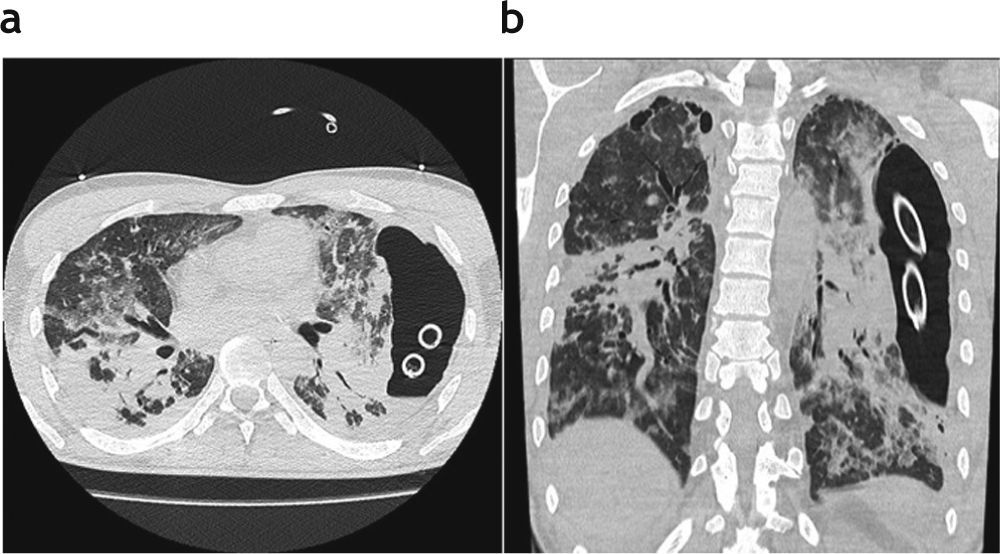
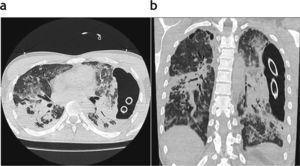
Paciente trasplantado bipulmonar por histocitosis X con diagnóstico de neumonía herpética a los 8 años postrasplante. (a) Corte axial de tomografía computada de alta resolución donde se visualizan áreas de consolidación y opacidades en vidrio esmerilado de distribución bilateral, derrame pleural y neumotórax con avenamiento pleural doble. (b) Reconstrucción coronal donde se aprecia el compromiso de todo el parénquima pulmonar y, además, se reconoce la presencia de bullas apicales derechas.
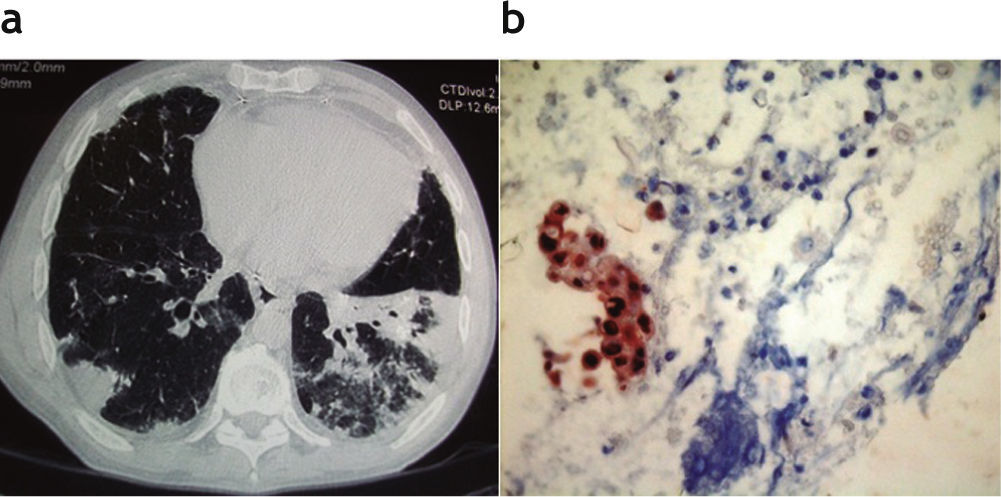
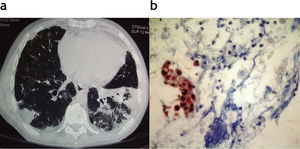
Paciente trasplantado cardiopulmonar por comunicación intraventricular e hipertensión pulmonar con diagnóstico de neumonía herpética a los 19 años postrasplante. (a) Corte axial de tomografía computada de alta resolución donde se visualizan opacidades en vidrio esmerilado a predominio basal izquierdo asociado a procesos consolidativos posteriores con base pleural y presencia de mínimo derrame pleural bilateral. (b) Estudio inmunohistoquímico de lavado bronquioalveolar del paciente, el cual demuestra positividad nuclear intensa para virus herpes tipo 1 en grupo de células epiteliales y en elementos celulares aislados.
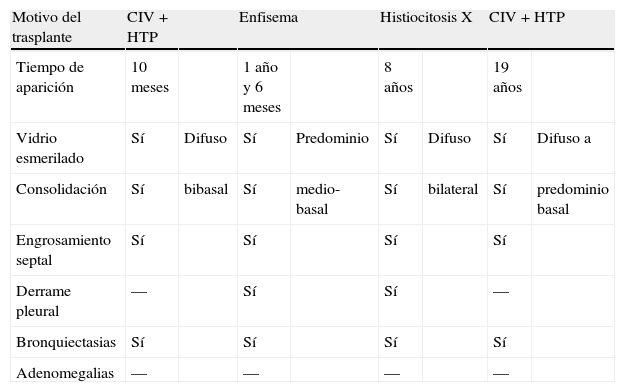
Hallazgos tomográficos y tiempo de aparición de la neumonía herpética en nuestros pacientes
| Motivo del trasplante | CIV + HTP | Enfisema | Histiocitosis X | CIV + HTP | ||||
| Tiempo de aparición | 10 meses | 1 año y 6 meses | 8 años | 19 años | ||||
| Vidrio esmerilado | Sí | Difuso | Sí | Predominio | Sí | Difuso | Sí | Difuso a |
| Consolidación | Sí | bibasal | Sí | medio-basal | Sí | bilateral | Sí | predominio basal |
| Engrosamiento septal | Sí | Sí | Sí | Sí | ||||
| Derrame pleural | — | Sí | Sí | — | ||||
| Bronquiectasias | Sí | Sí | Sí | Sí | ||||
| Adenomegalias | — | — | — | — | ||||
CIV: comunicación intraventricular; HTP: hipertensión pulmonar.
La NH es una entidad infrecuente altamente relacionada con el estado inmunológico y deterioro clínico significativo del paciente, y en muchos casos, provoca la muerte2,3,5. Si bien la bibliografía indica que su aparición es más frecuente en los primeros 2-3 meses postrasplante, en nuestra experiencia se evidenció en un lapso posterior (el más temprano a los 10 meses y el más lejano a los 19 años de la intervención)7,8.
Los hallazgos tomográficos en nuestros pacientes fueron similares, pero inespecíficos de NH, e incluyeron opacidades en vidrio esmerilado y una consolidación del espacio aéreo de distribución parcheada y difusa, que predominó en las bases de ambos pulmones. Además, se reconocieron aisladas bronquiectasias de tipo retráctil, y en 2 casos se observó un mínimo derrame pleural asociado.
La presencia de estos hallazgos en pacientes con trasplantes pulmonares suele generar sospecha de neumonía de etiología bacteriana, pero dada la baja frecuencia de NH, su alta mortalidad y la falta de signos imagenológicos específicos distintivos, es muy importante tener un bajo umbral de sospecha clínica y tomográfica de esta entidad y no demorar la realización de un BAL más biopsia transbronquial con marcación inmunohistoquímica para hacer el diagnóstico3,7,8. Con el resultado histológico positivo de NH, se debe efectuar su tratamiento con aciclovir endovenoso6,8.
Es importante señalar que esta entidad debe sospecharse también en aquellos pacientes con trasplante de pulmón portadores de neumonía bacteriana que, además de no responder a los esquemas antibióticos, presentan mala progresión clínica e imagenológica9.
ConclusiónEn nuestra experiencia, al igual que en la bibliografía, la NH demostró ser una entidad infrecuente y letal en pacientes con trasplante pulmonar. Sin embargo, a diferencia de la literatura (que señala una aparición inmediata luego del trasplante), nuestros pacientes presentaron la dolencia después de un largo lapso de tiempo (entre 10 meses y 19 años después de la cirugía).
Con base en nuestro estudio, concluimos que la aparición de la NH aparece más tardíamente por el aumento de la sobrevida de estos pacientes, el mayor número de trasplantes y la eficacia de las drogas inmunosupresoras.
Tanto las manifestaciones clínicas como los hallazgos tomográficos fueron inespecíficos de esta patología, pero su presencia, junto al antecedente de trasplante (con independencia del tiempo transcurrido), nos obliga a conocer y tener presente esta entidad para poder actuar en consecuencia.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.