Introducción
En los estudios sobre el coste beneficio de la terapéutica de las diversas patologías se ven implicados muchos aspectos de la estrategia sanitaria: la disponibilidad de recursos (personales, técnicos y materiales), los costes asistenciales, las repercusiones sociales (laborales, familiares, etc.) y múltiples factores más, de ahí que se hayan establecido diferentes índices de referencia para su valoración, entre otros, en los siguientes conceptos1: coste/beneficio (CBA) que valora en términos económicos los costes y beneficios de las terapéuticas aplicadas; coste/efectividad (CEA) que compara los costes de las terapias alternativas capaces de ofrecer similares resultados clínicos y sociales, coste/ utilidad (CUA) que compara los costes adicionales de una terapia que es capaz de mejorar algunos aspectos concretos como la calidad de vida o de la morbilidad; coste/oportunidad (COA) compara el beneficio obtenido con el mismo coste económico tratando diferentes patologías.
En este trabajo sólo pretendemos alcanzar una aproximación al CBA en el tratamiento anticoagulante oral (TAO).
Las indicaciones del tratamiento anticoagulante oral (TAO) se han ampliado en los últimos años tanto en el número de patologías como en pacientes de avanzada edad, dado el establecimiento de niveles de anticoagulación eficaces con mínimos riesgos iatrogénicos. En los países desarrollados, con incrementos anuales sobre el 10% de pacientes incluidos en esta terapéutica, la prevalencia de los enfermos anticoagulados se aproxima al 1% de la población2-5.
Pero esta terapéutica, con eficacia probada en patologías de riesgo tromboembólico, tiene un estrecho margen farmacológico, de ahí la necesidad de controles periódicos (clínicos y biológicos) para situarlos en los márgenes que ofreciendo beneficio superen el coste de las complicaciones hemorrágicas.
El incremento de la población en TAO y la gran cantidad de controles demandados han originado estrategias cambiantes de política sanitaria, y así las soluciones adoptadas son diferentes según los países, e incluso son diversas en cada uno de los territorios nacionales. En España, donde tradicionalmente el control del TAO está adscrito a la especialidad de Hematología, en los últimos años se discute y se propone la participación de otras especialidades, en concreto los consultorios de Medicina de Atención Primaria6, con o sin la coordinación y supervisión de hematólogos para esta labor asistencial. Ambas situaciones, control centralizado o descentralizado, tienen sus ventajas y sus inconvenientes, pero son los resultados clínicos los que han de evaluar la mejor opción. Esto hace imprescindible tener las referencias sobre la efectividad, morbimortalidad, repercusiones sociosanitarias y gastos del tratamiento. A estas conclusiones sólo se podrá llegar mediante amplios estudios que reúnan, bajo los mismos criterios, estas valoraciones.
Esta experiencia solamente puede ser obtenida y comparada entre hospitales que dispongan de Unidades de anticoagulación y que hayan realizado el pertinente seguimiento de sus pacientes.
Pacientes y métodos
Estudio clínico
El estudio incluye 20.347 pacientes en TAO controlados durante el año 2003 en 4 Unidades de anticoagulación de grandes hospitales del país (Ramón y Cajal de Madrid, Santa Creu y Sant Pau, Clinic y Provincial de Barcelona y La Fe de Valencia) que cubrían un área asistencial total con 1.641.000 usuarios. Los resultados biológicos (INR) junto a la dosis administrada y los episodios adversos (trombóticos o hemorrágicos),medicación concomitante y situaciones clínicas específicas fueron registrados en sistemas informáticos diseñados para el control de esta terapéutica. El interrogatorio y las órdenes clínicas fueron establecidos por especialistas de Hematología. Cuando ocurrieron situaciones que necesitaron ingreso hospitalario los informes clínicos de alta se archivaron codificados en el registro informático general del hospital. La morbilidad fue establecida mediante la clasificación de los episodios según el grado de severidad:
1. Leve: no requieren medidas sanitarias y se comunican al especialista en la visita habitual.
2. Moderada: precisan la visita al consultorio del TAO o Servicio de Urgencias y la aplicación de medidas específicas (acciones locales y medicación paliativa).
3. Grave: requieren tratamiento especial, como ingreso hospitalario o intervención quirúrgica o transfusión sanguínea por descenso de Hb>2 g/dl.
Todos estos episodios se relacionaron con el INR y la posible causa desencadenante.
Estas Unidades hospitalarias de anticoagulación funcionan de manera independiente de Atención Primaria para el control de sus pacientes, aunque se limitan a las cuestiones relacionadas con el TAO, control, preparación para maniobras quirúrgicas y asesoramiento en cuanto a la asociación de otros fármacos.
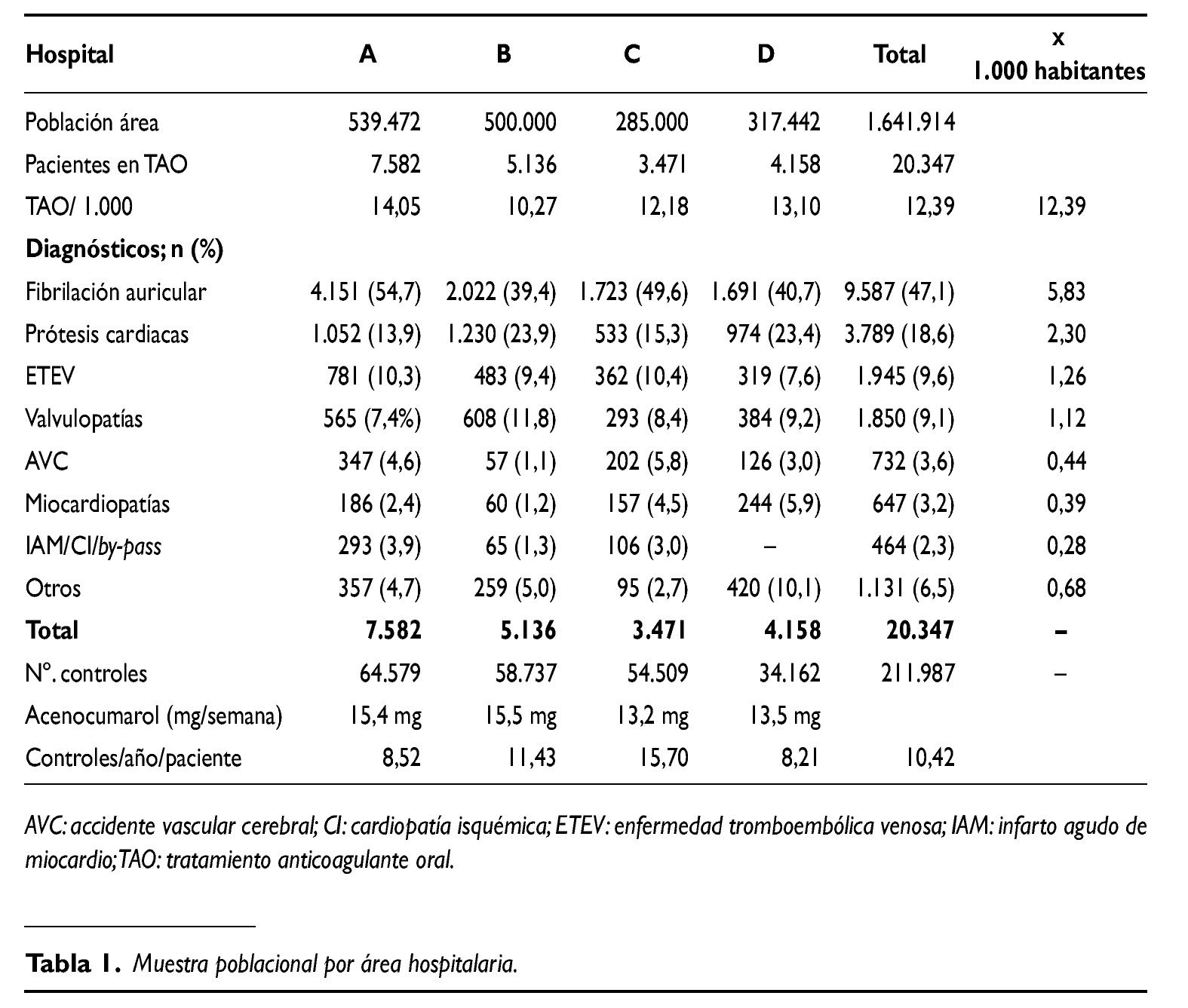
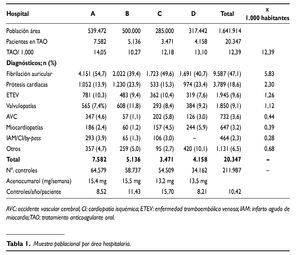
En este estudio los pacientes sometidos a TAO representaban el 12,19 por cada 1.000 habitantes de la población total. La principal causa de TAO fue la fibrilación auricular (FA) (47,1%), seguida por las prótesis cardíacas mecánicas (18,6%),las cardiopatías de origen reumático (12,4%), las secuelas de la enfermedad tromboembólica (ETE) (9,6%),las cardiopatías isquémicas (2,3%) y misceláneas (6,5%) (tabla 1).
Cálculo de costes
El cálculo de costes (tabla 2) se realizó según el baremo disponible en el Hospital Ramón y Cajal de Madrid durante el año 2003, tanto para los diferentes procesos según los grupos relativos de diagnóstico (GRD) y los gastos generados por el control clínico/analítico del TAO.
Coste unidad de complejidad hospitalaria (UCH) = 2.066 euros.
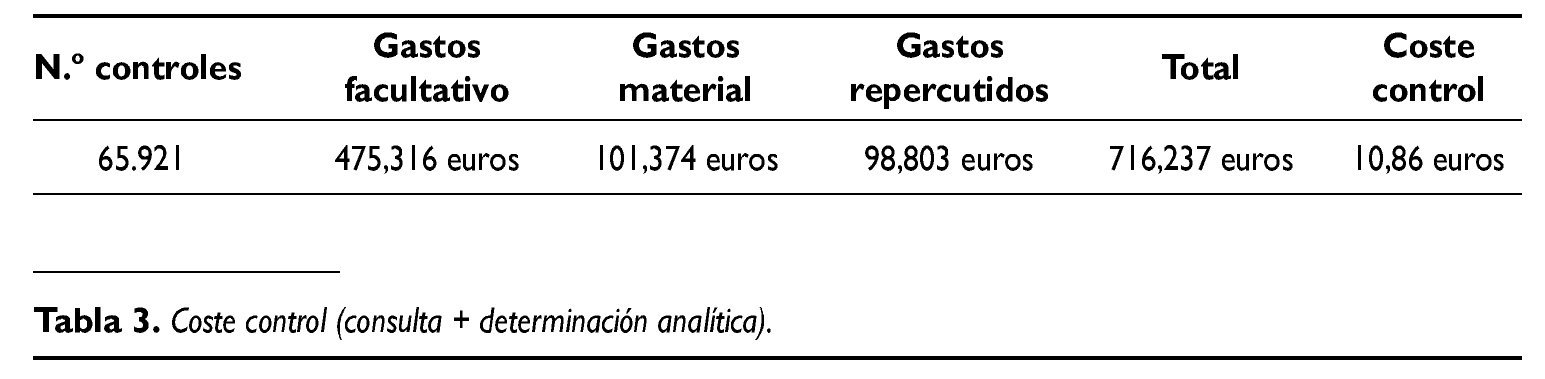
Gastos del tratamiento anti-coagulante oral (tabla 3)
Coste de la medicación
La dosis media es de 14 mg/semana/paciente y el precio del fármaco (Sintrom®) 0,03 euros/mg.
Resultados
Morbilidad y mortalidad
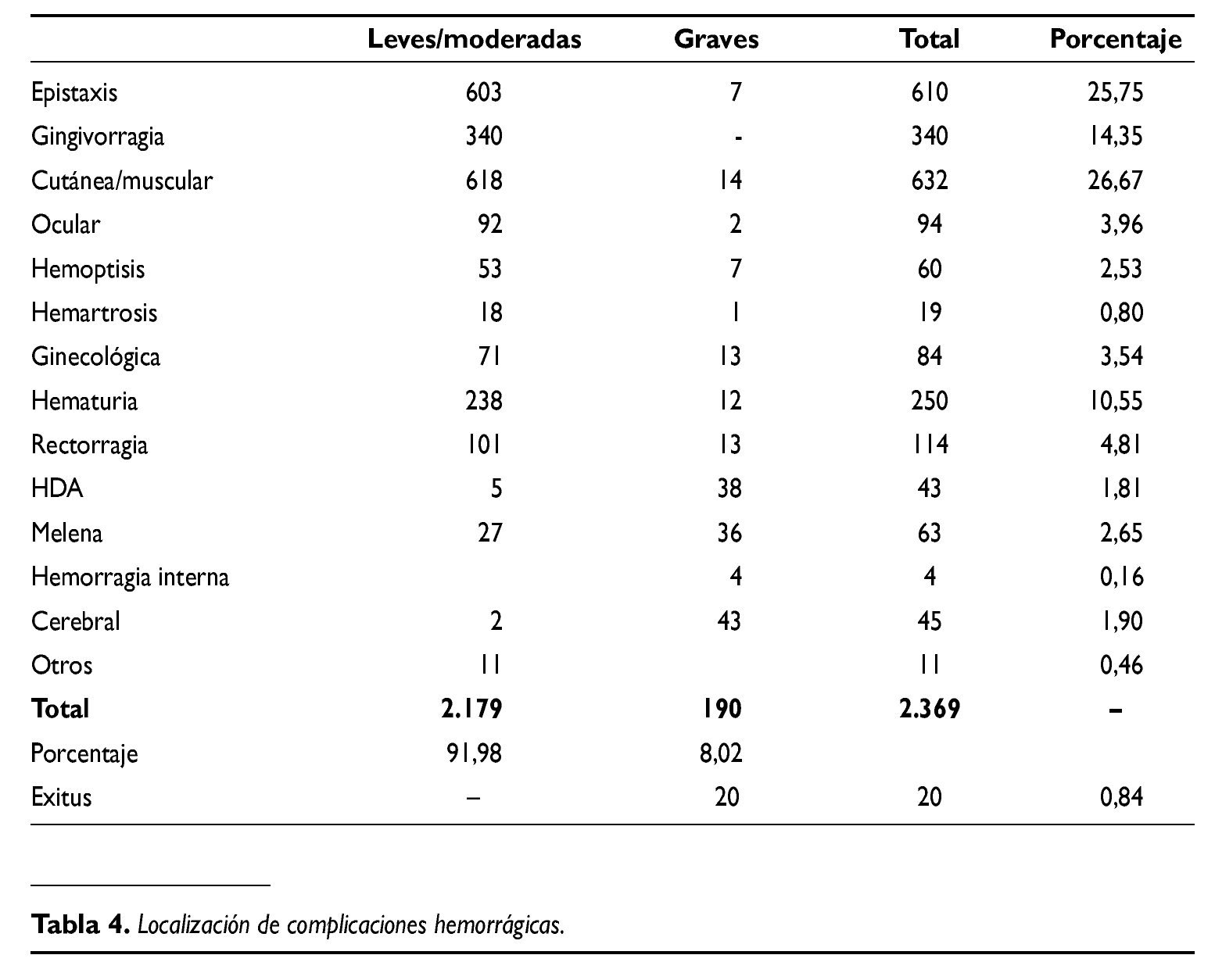
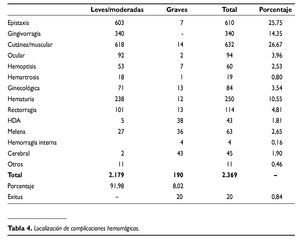
Los accidentes hemorrágicos se consignan según la severidad y localización en la tabla 4. Se detectaron un total de 2.369 eventos hemorrágicos (con 20 exitus), de los cuales el 82% fueron leves o moderados y el 8% fueron clasificados como graves.Según su ubicación la distribución de los principales eventos hemorrágicos correspondía a localización cutáneo-mucosa en más del 75%. Las del tracto digestivo fueron del 10%,similar a las de origen urinario y solamente el 1,8% se produjeron en el territorio cerebral.
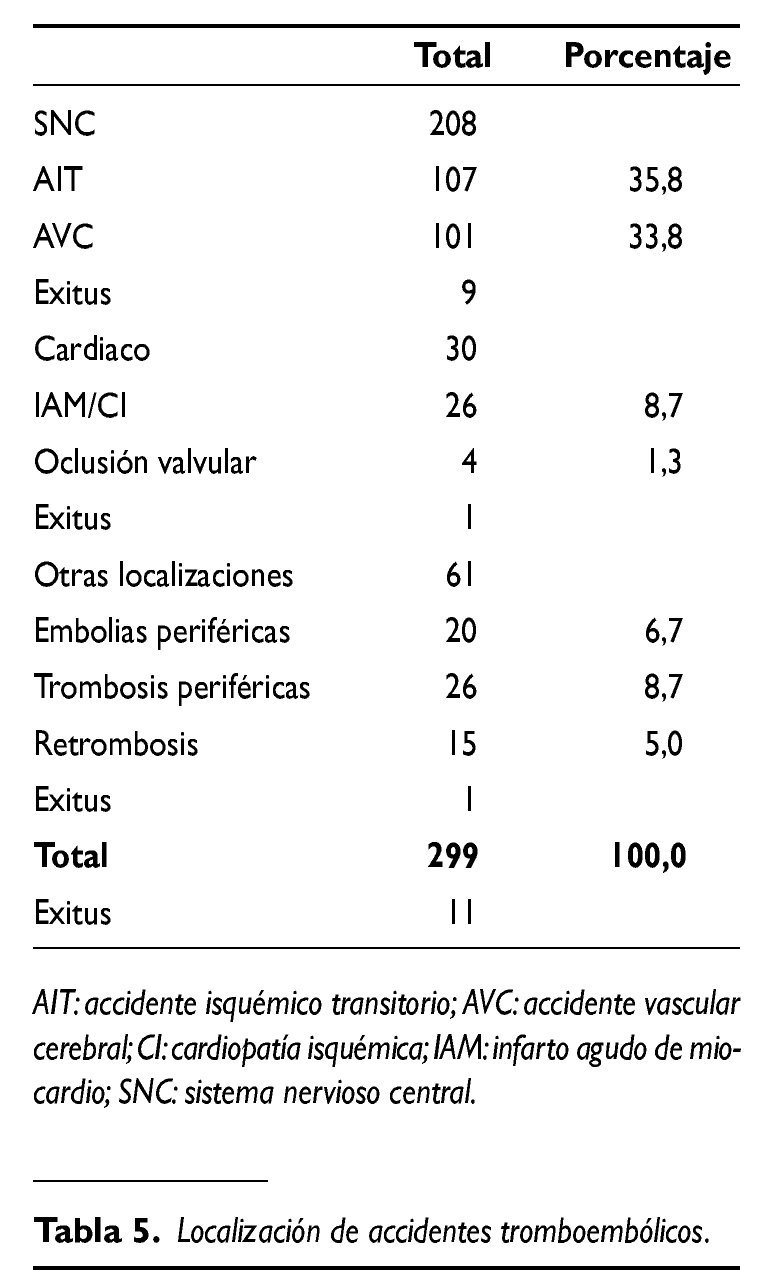
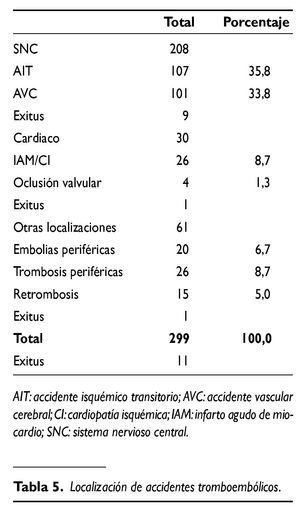
Los accidentes tromboembólicos se muestran en la tabla 5. Se registraron un total de 299 tromboembolias (con 11 exitus).La localización fue en el territorio cerebral en el 55% de los casos, 8% en localización cardiaca y 17% en los vasos periféricos.
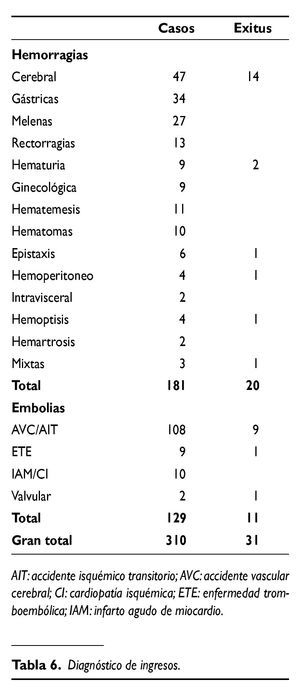
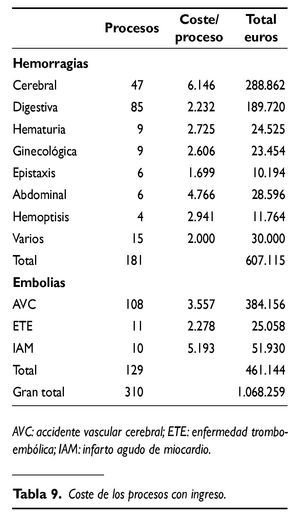
En la tabla 6 se establecen los episodios graves que requirieron ingreso hospitalario. Por causa hemorrágica fueron 181 (58%) y por causa tromboembólica 129 (42%), en total 310 procesos. Las principales localizaciones donde se produjeron las complicaciones que indicaron el ingreso fueron por causa cerebral en el 50% de los casos, y por hemorragias digestivas en el 25%.
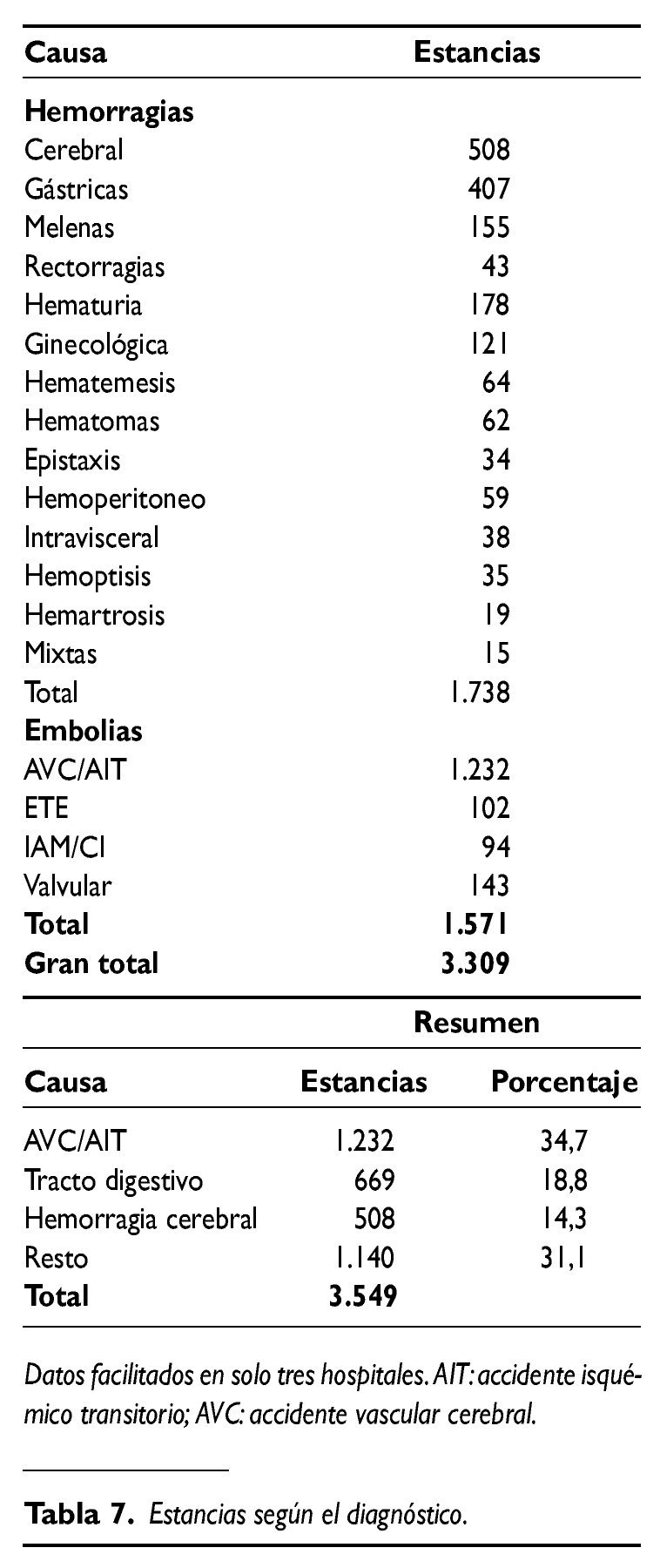
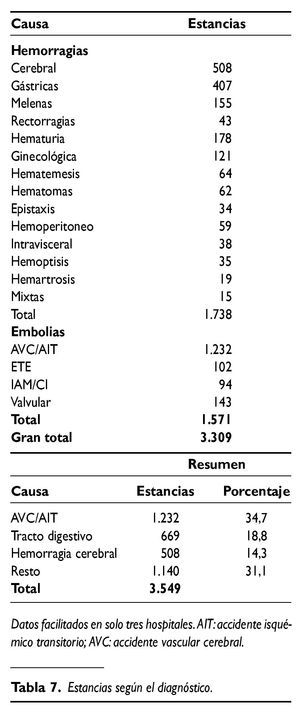
Solamente tres hospitales han facilitado el dato completo sobre las estancias hospitalarias. En ellos se han contabilizado 3.549 días de ingreso y su distribución por patologías se detalla en la tabla 7.
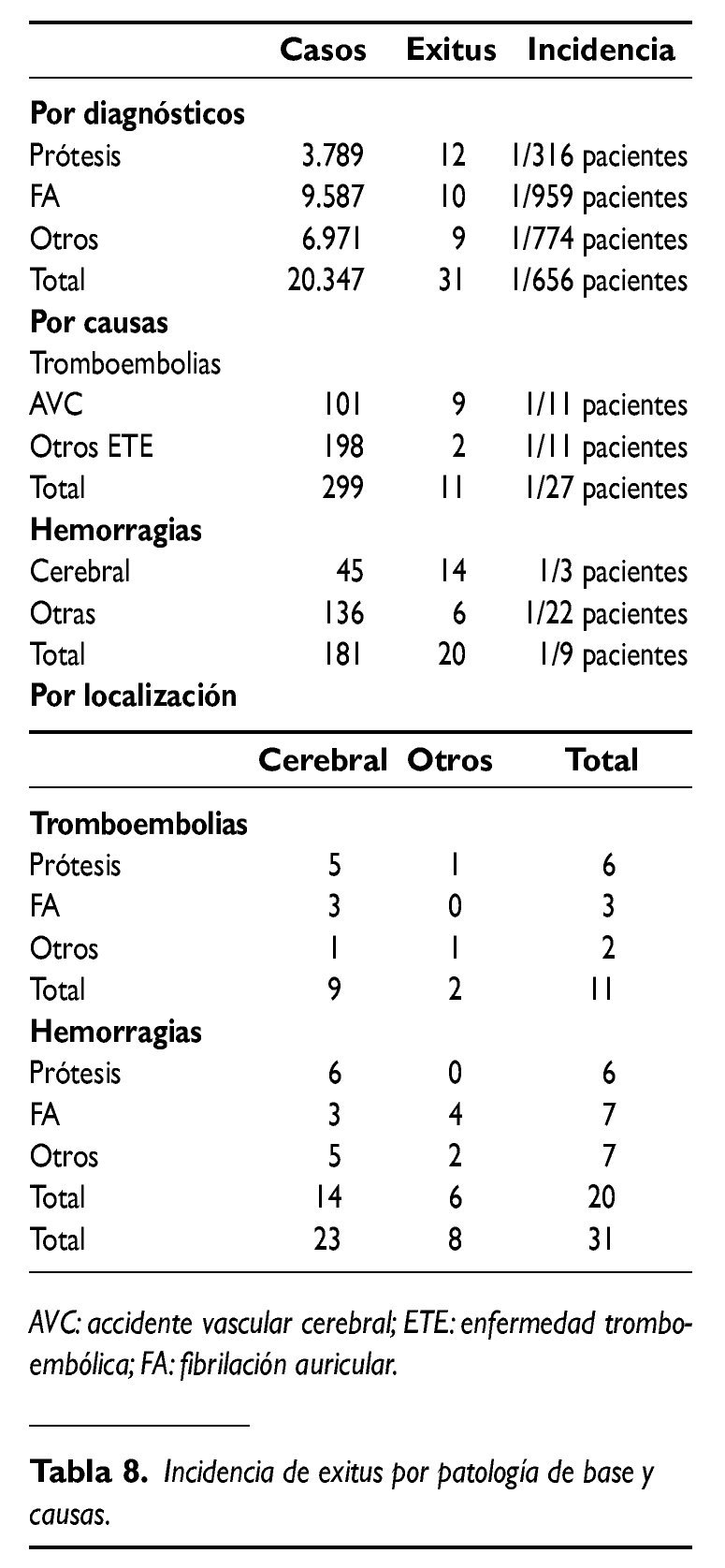
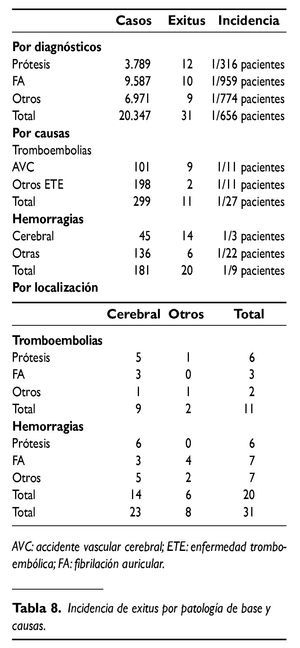
En la tabla 8 se relacionan los exitus con los diagnósticos de base y los procesos donde ocurrieron (sólo se hace mención a las muertes por las complicaciones posibles o inherentes al TAO y no a las debidas a otras causas). Del total de los 31 exitus consignados, 20 (64%) ocurrieron durantes episodios hemorrágicos y 11 (36%) en tromboembolismos; en conjunto 1 de cada 656 pacientes tratados, siendo tres veces más frecuentes en portadores de prótesis que en pacientes con FA. La localización más frecuente de los episodios que concurrieron en el exitus fue la cerebral con 23 casos (74%) y ocurrió en uno de cada tres pacientes afectados por hemorragia y en uno de cada 11 pacientes afectados por embolia cerebral.
Gastos estimados Hospitalización
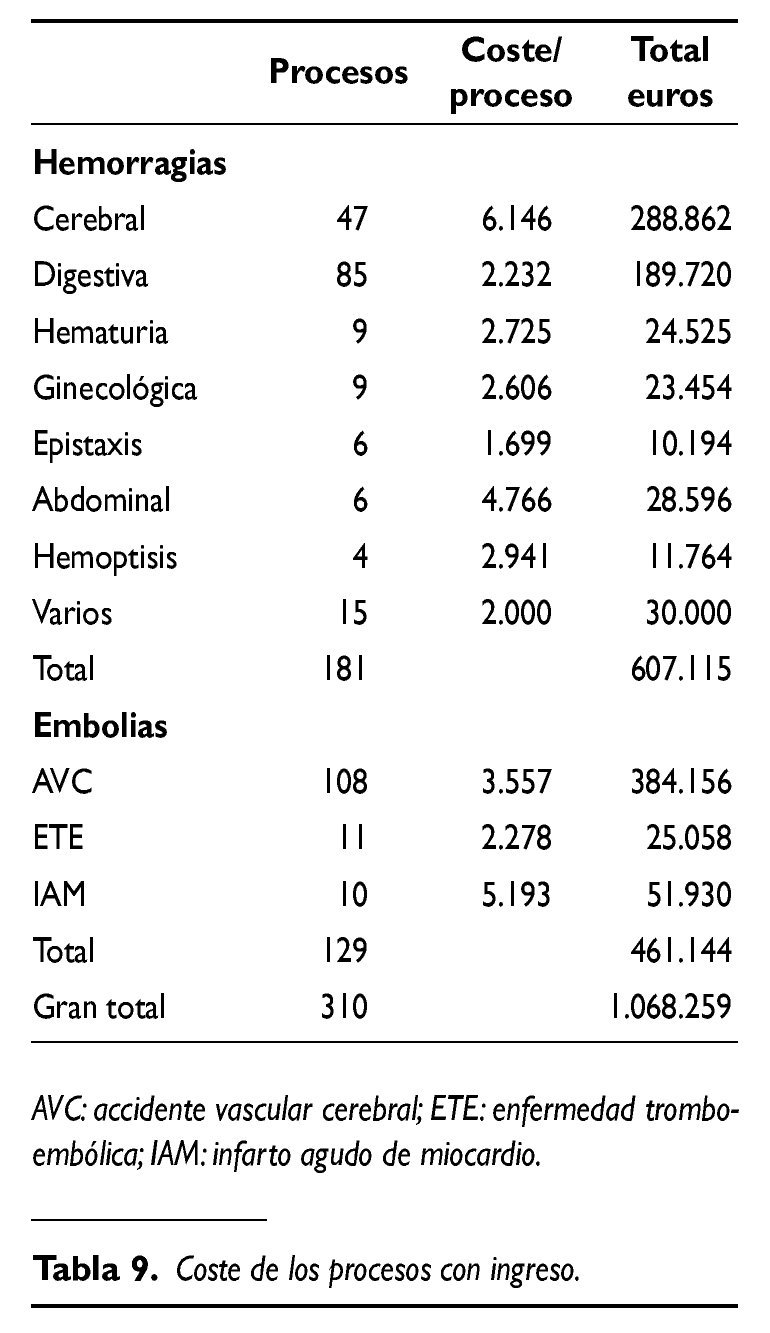
Según se detalla en la tabla 9 el conjunto de los 310 episodios que indicaron el ingreso hospitalario, aplicando la clasificación de los GRD, generaron un coste de 1.068.259 euros.
Control y tratamiento ambulatorio
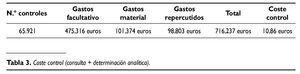
Coste control (consulta + determinación): coste control clínico/biológico 10,86 euros, promedio controles por paciente/año =10,5 y coste total /año/paciente 115 euros.
Coste medicación: precio fármaco (Sintrom®) 0,03 euros/mg, consumo medio anual por paciente:14 mg/semana, 730 mg/año/paciente y 22 euros/ año/paciente.
Por paciente: controles/paciente/ año 115 euros, medicación/paciente/año 22 euros, total 137 euros.
En el grupo estudiado (año 2003) por controles 2.302.179 euros, por medicación 447.634 euros; total 2.749.813 euros.
Gastos totales (a+b) 3.818.072 euros; coste medio paciente/año: 191 euros.
No se han contabilizado otros gastos sanitarios de difícil valoración ni los gastos sociales (trasporte, pérdida de tiempo laboral, impuestos no devengados, atención personal, etc.),ni la valoración de los años de vida salvados.
Discusión
El estudio incluyó pacientes de 4 Unidades de anticoagulación del país escogidas por ser representativas, utilizar criterios similares en el manejo de los pacientes en TAO y disponer de datos estadísticos de la población controlada en cuanto a diagnóstico, dosis administradas, morbilidad y mortalidad. Todas ellas funcionan de manera independiente de Atención Primaria para el control de sus pacientes, aunque se limitan a las cuestiones relacionadas con el TAO, control, preparación para maniobras quirúrgicas y asesoramiento en cuanto a la asociación de otros fármacos. Como se describe en la literatura las principales causas de TAO, fibrilación auricular, prótesis mecánicas cardíacas, enfermedad tromboembólica venosa y cardiopatías reumáticas coinciden en todos los centros, siendo los demás grupos diagnósticos menos frecuentes. Otros parámetros como son la dosis media semanal de acenocumarol recibida por los pacientes, así como el número de visitas anuales fueron también muy similares.
Población anticoagulada
Es importante, desde el punto de vista asistencial, saber si la población atendida está anticoagulada en la proporción que sus patologías lo demandan. Los pacientes susceptibles a este tratamiento pueden deducirse de las cifras publicadas y de acuerdo con las diferentes patologías.
Prótesis cardíacas mecánicas
En este estudio 3.789 pacientes eran portadores de prótesis cardiacas (2,3 por 1.000 habitantes),lo que debería ser el número real de pacientes con esta patología, dada la obligatoriedad del TAO al que deben ser sometidos. Esta cifra no ha de reflejar la incidencia media del país, ya que al ser hospitales de referencia pueden concentrar pacientes con este diagnóstico.
Cardiopatías
La más frecuente es la originada por la FA. Su prevalencia en la población general es el 8,0 por 1.000 habitantes7, por lo que puede haber 4.000 pacientes mayores de 65 años por millón de habitantes con este diagnóstico8-11. Estudios más detallados por estratos de edad han establecido que entre los 60-70 años de edad, la prevalencia de FA es del 5%, y en edades comprendidas entre 70-90 años se alcanza el 14%,siendo de más del 22% en mayores de 90 años12-14. Aunque paulatinamente se va instaurando la indicación del tratamiento, en algunos estudios solamente el 60% de los pacientes en FA que no tienen contraindicación para el TAO (40%) estaban recibiendo este tratamiento15-17, por lo que solamente se aplica en un tercio de estos pacientes18. Aplicando estas cifras a la población estudiada y distribuida según la pirámide poblacional (memoria del año 2003 del hospital Ramón y Cajal) el total de la población con este diagnóstico de FA y mayores de 60 años debe ser de 40.000 personas. De ellas en la actualidad reciben TAO 9.600 (5,8 por 1.000 habitantes), pero como esta indicación se ha instaurado recientemente y los incrementos en los últimos años son de más del 20% anual, es de esperar que se alcancen en el futuro inmediato al 50% de los pacientes en FA o su equivalente a los 20.000 pacientes. Posiblemente el dato más importante para conocer el grado de implantación de una correcta indicación del TAO es el número de pacientes con FA anticoagulados y referidos al número de habitantes.
La enfermedad tromboembólica
La trombosis venosa profunda (TVP) es una patología con importante morbilidad y con una incidencia de 0,5/1.000 habitantes/año, con un 5% de mortalidad y con secuelas postflebíticas del 5%19. La prevalencia del tromboembolismo pulmonar (TEP), estimando que sólo se diagnostican la mitad de los posibles, puede ser de 0,5/1.000 habitantes/año y como causa de muerte en 0,1/1.000 habitantes/año20.La sistemática aplicación de medidas profilácticas en las patologías y procedimientos de riesgo trombótico ha supuesto un extraordinario descenso de las TVP y TEP, principalmente en las áreas quirúrgicas21,22.Sin embargo, todavía se producen un importante número de casos que se refleja en ingresos hospitalarios, lo que supone un promedio de 600 casos nuevos anuales por millón de habitantes. En la población del presente estudio estaban siendo anticoagulados en el año referido 1.900 pacientes (tratamiento agudo y en fase crónica), lo que representa una prevalencia de este tratamiento de 1,15/1.000 habitantes/año.
Otras patologías justificarían el tratamiento de otros 2.500 pacientes/ año por millón de habitantes2.
Costes de los procesosPor ictus cerebrales
De varias referencias se pueden sacar algunas conclusiones: por cada año libre de ictus en pacientes con FA,se calcula un ahorro anual de más de 600 euros23.
En grandes cifras en Estados Unidos, que es el país donde mejor se ha estudiado, se producen 500.000 ictus/año que generan unos costes directos de 17.000 millones de dólares, e indirectos de 13.000 millones24. Los gastos de rehabilitación se calculan en 179.000 millones de dólares25 y generan una pérdida de calidad de vida del 30%26.
Resumiendo las cifras aportadas en varios países, un episodio de ictus tiene un coste estimativo de 15.000 euros en la fase aguda y de 48.000 euros en la fase subaguda, y unos gastos de 100.000 euros durante el resto de la vida27-35.
Por retrombosis
De las cifras de varios autores se puede estimar que en la fase aguda de TVP/TEP el coste es de 6.000 y 3.000 euros en la fase subaguda36,37. Entre el 17-50% desarrollan síndrome postflebítico38, que genera un coste anual de 1.800 euros (1.200 directos y 600 por pérdidas económicas laborales)39.
Estimación de complicaciones evitadas
De las múltiples complicaciones posibles en estas patologías sólo contemplaremos los ictus cerebrales y las retrombosis.
Ictus isquémicos cardioembólicos
Aunque hay un declinar en la mortalidad de ictus isquémicos a lo largo de los últimos años, todavía es la tercera causa de mortalidad en EE.UU., y en Europa es de 1-2/1.000 hombres y 0,7-1/1.000 mujeres40-42, aunque con gran diferencia entre países43. Según el estudio Manresa44 en España se alcanza una mortalidad de 88/100.000 habitantes y una morbilidad de 183/100.000 habitantes. En presencia de FA la mortalidad se incrementa en más del 25%45.
En pacientes con prótesis.
En pacientes con prótesis cardiacas artificiales sin TAO no hay estudios recientes, dado que habitualmente se anticoagulan sistemáticamente, pero aunque la técnica quirúrgica y la construcción de las prótesis han mejorado se podría deducir de experiencias previas que la incidencia de accidentes cerebrovasculares isquémicos sería del 8-10% de tasa anual45-47.
En pacientes con fibrilación auricular.
Más experiencia hay constatada sobre los riesgos tromboembólicos en los pacientes con FA mayores de 65 años y los que padecen alteraciones en las válvulas cardiacas. Para el conjunto de estas patologías se asume que la incidencia de complicaciones tromboembólicas cerebrales es del 5% por paciente/año, pero el riesgo de recidiva posteriormente alcanza el 20%48,49.
Para otras cardiopatías, en ausencia de TAO, la incidencia de procesos tromboembólicos puede estimarse en el 5% anual50-52.
RetrombosisLos pacientes que han sufrido estos episodios,si no se someten a TAO en los próximos 3-6 meses, cursan con un 30% de recidivas53.
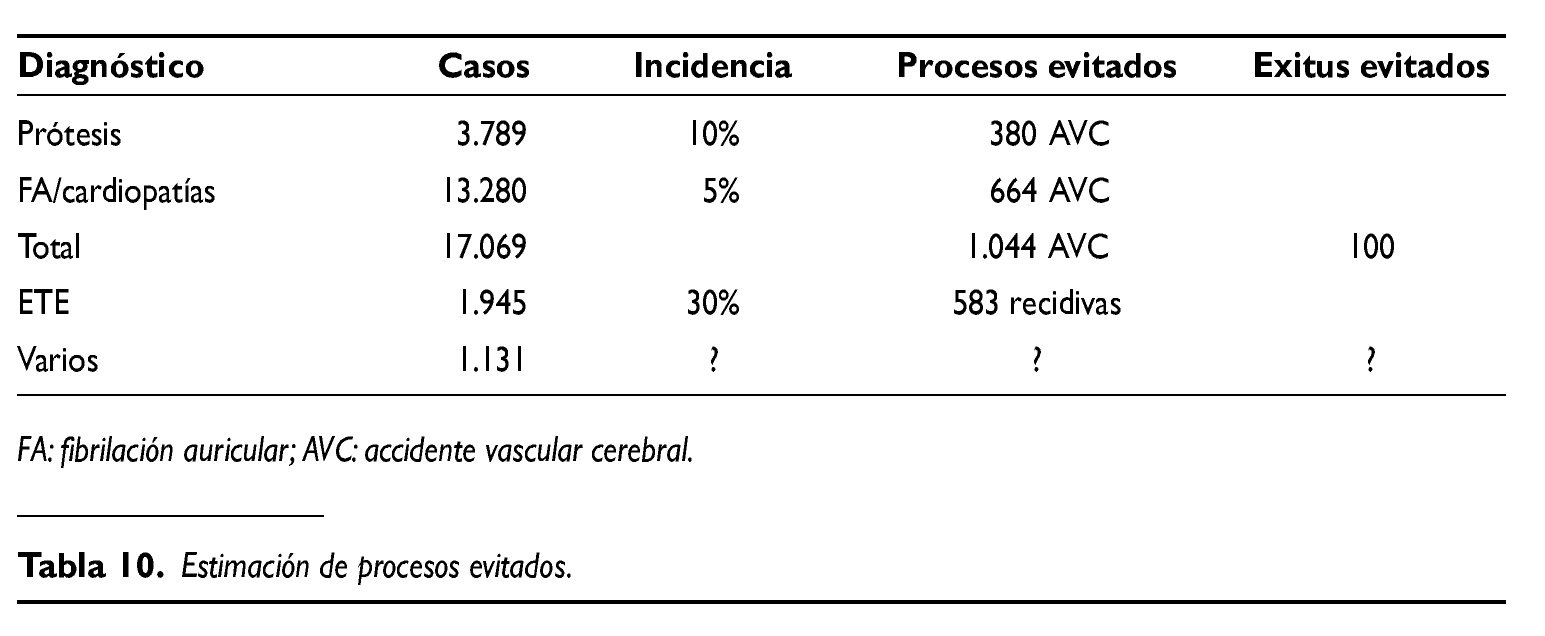
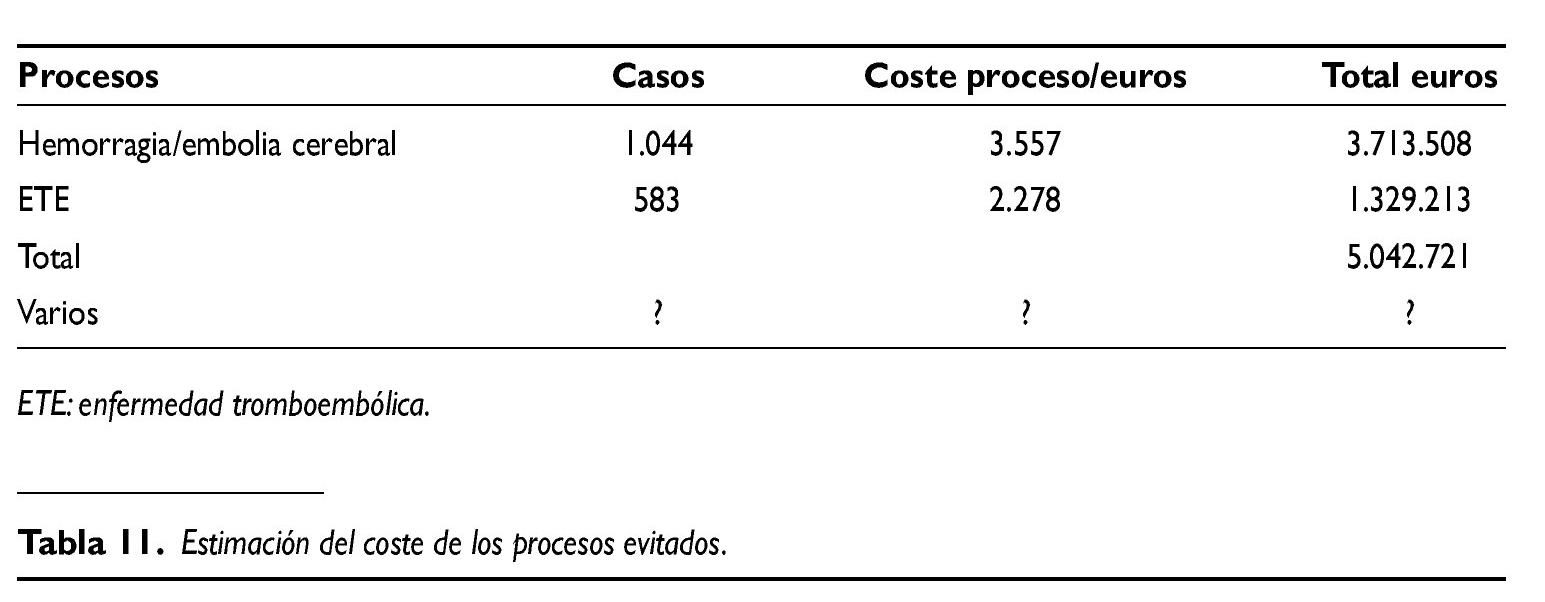
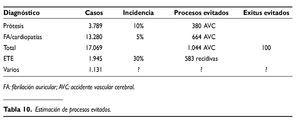
Con estos antecedentes,y basados en los datos del presente estudio, se puede deducir, como se detalla en la tabla 10, que en el conjunto de estos pacientes se han evitado más de 1.000 accidentes cerebrales isquémicos graves y 100 exitus por esta causa,y más de 500 recidivas trombóticas.
Valoración económica de las complicaciones evitadas
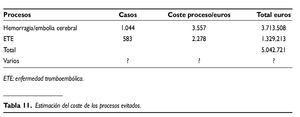
Aplicando los mismos criterios de valoración para los costes de las complicaciones ocurridas y las evitadas, con los datos de los apartados anteriores, se puede deducir, como se indica en la tabla 11,que al menos los gastos evitados sumarían 5.000.000 de euros y los costes ocasionados 3.800.000 euros.
Además, no se valoran los gastos originados por las secuelas: fase subaguda y crónica de un ictus cerebral (gastos sociosanitarios) 50.000 euros/paciente; fase crónica de episodios trombóticos (20% síndrome post-flebítico) 2.000 euros/paciente/año.
Conclusiones
Los fármacos antivitaminas K son actualmente la mejor opción terapéutica en la profilaxis de la enfermedad tromboembólica en diferentes patologías, algunas como la FA, de una importante prevalencia en la tercera edad.
Estos fármacos tienen un estrecho margen farmacológico y su actividad es susceptible a la influencia de variables como la dieta. Por ello los pacientes sometidos a este tratamiento necesitan controles periódicos para ajustar la dosis.
Los datos indican que el tratamiento se asocia a un riesgo de mortalidad y morbilidad no despreciable. Por ello, cualquier alternativa de seguimiento debe conocer los resultados de su gestión clínica.
Las Unidades de anticoagulación, una de las alternativas de seguimiento, manejan un número importante de enfermos, y sus estadísticas de reacciones adversas y mortalidad se ajustan a los datos publicados en otros países de similar desarrollo sanitario.
Cuando el seguimiento es adecuado el riesgo-beneficio entre la administración de los fármacos antivitamina K y la abstención terapéutica es muy favorable a esta medicación, tanto en los estudios clínicos como en los económicos.
En resumen, es deseable que se realicen estudios similares en otras variantes de aplicación de este tratamiento (autotratamiento, control en Atención Primaria, etc.) en los que reuniendo amplia casuística se puedan comparar los resultados clínicos y los económicos. Dada la gran divulgación de este tratamiento, la posibilidad de registros informáticos para su seguimiento, etc., es posible obtener resultados a corto plazo.
Pero independientemente de la adopción de las diferentes medidas para su aplicación y sus resultados, parece conveniente un seguimiento continuo y permanente que establezca la garantía del tratamiento óptimo, para lo cual será imprescindible la colaboración de la asistencia hospitalaria y Atención Primaria, en cuyo conjunto se encuentra el historial completo y el destino del paciente.
*Este trabajo ha sido financiado en parte por el Proyecto FISS. 03/10019.