Las porfirias constituyen un grupo de ocho enfermedades de baja prevalencia, causadas por defectos enzimáticos en la vía metabólica de la síntesis del grupo hem. Una de sus formas es la porfiria intermitente aguda; afecta a 1,5/100.000 personas año y se presenta con dolor abdominal, taquicardia, parestesias, constipación y vómito. La neuropatía porfírica es en esencia motora, simétrica y suele ser proximal. Se presenta el caso de una paciente de sexo femenino con neuropatía periférica, dolor abdominal y elevación de las transaminasas, en quien se documentó porfiria intermitente aguda. Después de instaurado el manejo, los síntomas se resolvieron.
Porphyrias are a group of eight low prevalence disorders of heme metabolism, each characterized by a defect in an enzyme required for the synthesis of heme. Acute intermittent porphyria, affecting 1.5 per 100.000 people per year manifesting with abdominal pain, tachycardia, paresthesia, constipation and vomiting, is one type of porphyria. Porphyric neuropathy is fundamentally motor, symmetrical and often has a proximal predilection. A case is presented in a female patient in whom acute intermittent porphyria was documented. Her symptoms included peripheral neuropathy, abdominal pain and elevation of transaminases. Her symptoms resolved after receiving treatment.
Las porfirias comprenden un grupo de ocho enfermedades que tienen como fundamento fisiopatológico defectos enzimáticos en la vía metabólica de la síntesis del grupo hem. Cada tipo de porfiria es el resultado de la acumulación de precursores metabólicos, responsables de los síntomas que presentan los pacientes1. Son entidades poco frecuentes pero se deben tener como diagnóstico diferencial en pacientes con neuropatía periférica. A continuación se hace referencia a un caso de ataque agudo de porfiria cuya presentación inicial fue con neuropatía periférica, dolor abdominal, hiponatremia y elevación de transaminasas.
Presentación del casoMujer de 27 años edad, natural del Cauca, residente en Bogotá, desempleada. Consultó por cuadro de 13 días de evolución de dolor progresivo, localizado en grupos musculares de la región posterior de ambas piernas, de leve intensidad, asociado con parestesias, temblor y disminución de la fuerza, que dificultaba la marcha y se caía con facilidad. Refiere también disminución de la fuerza en extremidades superiores, todo asociado con picos febriles no cuantificados, astenia, adinamia y dolor abdominal generalizado tipo cólico, intermitente. A la revisión por sistemas relata alteración del patrón de sueño por dolor, tos productiva de 4 días de evolución, orina colúrica intermitente. Como antecedentes personales refirió alergia a dipirona y butil bromuro de hioscina.
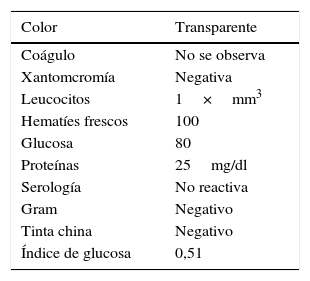
Al ingreso se encontraba en regulares condiciones generales, alerta, orientada en tres esferas mentales, deshidratada, escleras con tinte ictérico. Signos vitales con tensión arterial de 140/90mmHg, frecuencia cardíaca 128 latidos por minuto y 18 respiraciones por minuto, temperatura de 36,5°C. El examen neurológico mostró fuerza en extremidades superiores: distal 4+/5, proximal 5/5; extremidad inferior derecha 4/5, izquierda 4+/5. Reflejos miotendinosos: miembros superiores hiporreflexia, inferiores arreflexia, con marcha miopática. No presentaba alteraciones de los pares craneales, de la sensibilidad superficial o profunda, ni de la coordinación. Se toman paraclínicos (tabla 1) en donde es llamativa la leucocitosis con neutrofilia, la hiponatremia, que en el contexto del paciente es euvolémica e hipoosmolar (osmolaridad calculada: 270 mOsm/l) y la alteración de las transaminasas con un patrón hepatocelular. Fosfatasa alcalina, glucemia, bilirrubinas y pruebas de coagulación normales. Todo el perfil infeccioso es negativo. Se realizó punción lumbar (tabla 2) la cual no orientó hacia ningún factor etiológico.
Paraclínicos
| Hemograma | Leucocitos 18.200 |
| Neutrófilos 78% | |
| Linfocitos 13% | |
| Hemoglobina 13,1 | |
| Plaquetas 318.000 | |
| Función renal | Creatinina 0,9mg/dl |
| Nitrógeno ureico 23 | |
| Electrolitos | Sodio 129 mEq/l |
| Potasio 4,4 mEq/l | |
| Cloro 8,5 mEq/l | |
| Calcio 8,5 mEq/l | |
| Proteína C reactiva | < 0,5mg/dl |
| VSG | 20 |
| Función hepática | AST 199 |
| ALT 409 | |
| GGT 35 | |
| Fosfatasa alcalina 92 | |
| PT 11.5 | |
| PTT 27,6 | |
| Bilirrubina total 0,7mg/dl | |
| Bilirrubina directa 0,5mg/dl | |
| Albúmina 3g/l | |
| Creatinquinasa | 51 |
| Uroanálisis | Sin alteraciones |
| Infeccioso | HBsAg negativo |
| VHC negativo | |
| Hepatitis A IgM negativo | |
| VIH negativo | |
| IgM leptospira | |
| Serología negativa | |
| Glucemia | 84mg/dl |
Durante la hospitalización la paciente continuó sintomática, con persistencia de dolor abdominal localizado en epigastrio, sin signos de irritación peritoneal. Se decidió realizar electromiografía y velocidad de neuroconducción en miembros superiores e inferiores, las cuales fueron normales. La resonancia nuclear magnética no reveló hallazgos de mielopatía. La ecografía abdominopélvica reportó esteatosis hepática.
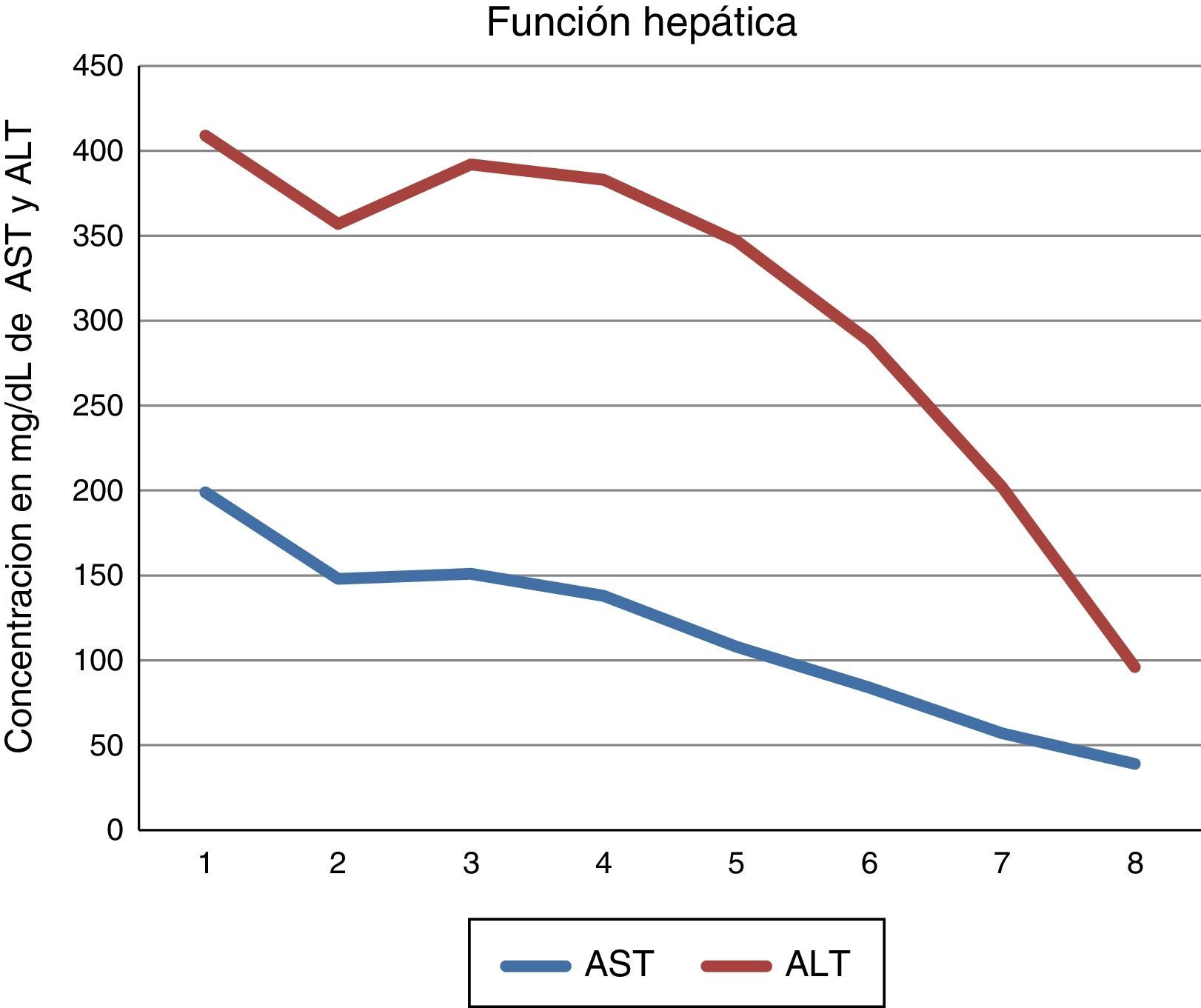
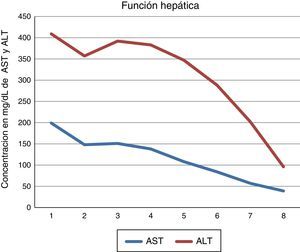
Ante ausencia de polineuropatía en la electromiografía, la resonancia nuclear magnética negativa para mielopatía y teniendo en cuenta la presencia de dolor abdominal sin hallazgos clínicos ni ecográficos que sugieran alguna etiología, la hiponatremia euvolémica y la orina colúrica, se plantea como diagnóstico un ataque agudo de porfiria. Se realizó exposición solar de la orina con cambio en su coloración. Se toma ácido delta aminolevulínico en orina el cual fue de 33,57mg/24 h (valor normal 1,5-7,5mg/24 h) y porfobilinógeno en orina positivo según descripción cualitativa. Se inició manejo con infusión de dextrosa y a los 2 días se administró hemina (3mg/kg/día) con clara mejoría sintomática tras 4 días de tratamiento, observando normalización de las transaminasas y los electrolitos. Ante la evolución clínica satisfactoria se decide dar de alta (fig. 1).
DiscusiónEl término porfiria viene del griego porphuros que significa púrpura y se refiere a un conjunto de enfermedades producto de alteraciones en las enzimas de la vía de síntesis del grupo hem. La mayoría tienen un patrón de herencia autosómico dominante, pero algunas pueden ser recesivas o esporádicas1.
Clásicamente se han dividido en porfirias hepáticas y eritropoyéticas, de acuerdo con el lugar donde se produzcan los precursores de porfirina, sin embargo esta no es una clasificación estricta pues algunas porfirias tienen ambos rasgos. Desde el punto de vista clínico es más práctico clasificarlas en porfirias agudas y no agudas2:
- •
Porfirias agudas.
- ∘
Porfiria por déficit de ácido delta aminolevunílico.
- ∘
Porfiria intermitente aguda.
- ∘
Coproporfiria hereditaria.
- ∘
Porfiria variegate.
- ∘
- •
Porfiria hepática no aguda.
- ∘
Porfiria cutánea tarda.
- ∘
Porfiria congénita eritropoyética.
- ∘
Protoporfiria eritropoyética.
- ∘
Porfiria hepatoeritropoyética.
- ∘
Las porfirias agudas tienen un patrón de herencia autosómico dominante y se caracterizan por presentar crisis con síntomas neuroviscerales y alteraciones electrolíticas, que en conjunto se han denominado ataques agudos. Son de difícil diagnóstico dado la heterogeneidad clínica y la baja penetrancia de la enfermedad en personas con el defecto enzimático. El 90% de los pacientes afectados nunca experimentan un ataque agudo de porfiria3.
La prevalencia de las porfirias agudas no se conoce con certeza, pero se calcula que es de 0,01% en la población general4. Se sabe que la intermitente aguda (PIA) es la más frecuente, es causada por mutaciones en la enzima porfobilinógeno deaminasa (también llamada hidroximetilbilano-sintetasa) y predomina en el sexo femenino. La prevalencia del portador del defecto enzimático es de 1 en 10.000 habitantes pero la prevalencia de casos con manifestaciones clínicas es de 1-5 por 100.000 habitantes5.
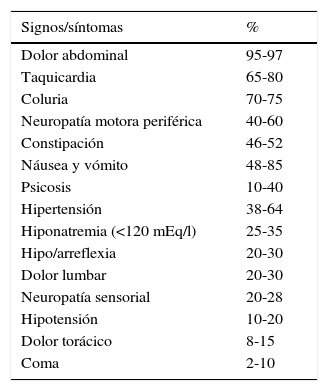
Entre las porfirias agudas la PIA se manifiesta solo con síntomas neuroviscerales, no así la variegate ni la coproporfiria hereditaria, que además tienen síntomas dermatológicos (fragilidad y erupciones bulosas). Las características clínicas de un ataque agudo se describen en la tabla 3.
Características clínicas de la PIA
| Signos/síntomas | % |
|---|---|
| Dolor abdominal | 95-97 |
| Taquicardia | 65-80 |
| Coluria | 70-75 |
| Neuropatía motora periférica | 40-60 |
| Constipación | 46-52 |
| Náusea y vómito | 48-85 |
| Psicosis | 10-40 |
| Hipertensión | 38-64 |
| Hiponatremia (<120 mEq/l) | 25-35 |
| Hipo/arreflexia | 20-30 |
| Dolor lumbar | 20-30 |
| Neuropatía sensorial | 20-28 |
| Hipotensión | 10-20 |
| Dolor torácico | 8-15 |
| Coma | 2-10 |
Tomada y modificada de Ventura et al.6.
Todas estas manifestaciones clínicas se dan por alteraciones en el sistema nervioso central, visceral, autonómico y periférico. Dada la prevalencia del dolor abdominal, la presentación clínica sin este síntoma hace muy poco probable el diagnóstico de porfiria y algunos autores recomiendan no considerarla7.
La hiponatremia se desarrolla en el contexto de un síndrome de secreción inadecuada de la hormona antidiurética (SIADH), ya que la acumulación de porfirinas produce alteración de las neuronas de los núcleos supraóptico y paraventricular en el hipotálamo, generando liberación de la hormona antidiurética, con la consecuente retención de agua y dilución del sodio5,8,9. Se han relacionado los ataques agudos de porfiria con carcinoma hepatocelular. Se sabe que la PIA, porfiria variegate, coproporfiria hereditaria, son factores de riesgo para su desarrollo e incluso se ha propuesto que la PIA sea una causa de hepatitis crónica, pues el 13% de los pacientes con PIA asintomáticos presentaron elevación de las transaminasas10,11. Al ingreso la paciente presentó elevación de las transaminasas que se normalizaron después de la instauración de la infusión de dextrosa y la hemina, sin embargo no se puede atribuir la transaminitis al ataque agudo de porfiria, ya que se documentó también esteatosis hepática, causa conocida de transaminitis, pero no deja de ser llamativo su descenso después del manejo del ataque.
El diagnóstico es un verdadero desafío pues se llega después de haber descartado numerosas patologías, debido a las variadas formas de presentación. Fue descrita por el profesor Jan Waldenström como la «pequeña imitadora» en contraste con la sífilis que era la «gran imitadora» al inicio del siglo XX12. Se debe sospechar un ataque agudo de porfiria en todo paciente entre los 20 y los 50 años con dolor abdominal, neuropatía, hiponatremia y cambios comportamentales. El diagnóstico oportuno es muy importante pues se ha documentado en grandes series una mortalidad entre 5-10%. Pero puede ser más alta como lo reportaron Latorre et al.13 quienes evaluaron 37 pacientes con PIA documentando una mortalidad de 33%. Cabe anotar que ninguno de estos pacientes recibió hemina.
La European Porphyria Initiative14 propuso unos criterios diagnósticos, los cuales incluyen el cuadro clínico característico, aumento significativo de PBG y ALA y porfirias en orina, pico de emisión de fluorescencia en plasma, cromatografía líquida de alta eficiencia de porfirinas e isómeros en heces, disminución de la actividad de la porfibilinógeno deaminasa y la confirmación genética. Sin embargo, en Colombia no es rutinario realizar todo el proceso diagnóstico propuesto y el diagnóstico se basa en la clínica y en la elevación de precursores de porfirina. Algo característico de la PIA (más que en otras porfirias agudas) es la coloración de la orina tras la exposición solar, la cual resulta de la polimerización del PBG urinario. El diagnóstico se basa en documentar la excreción aumentada de los precursores de porfirina en la orina o las heces según sea el caso15.
En el paciente con PIA la elevación del ALA y del PBG en la orina supera de 5 a 20 y de 20 a 50 veces el valor superior normal respectivamente. Se debe tener presente que la cuantificación anómala de las porfirinas puede presentarse en otras condiciones clínicas como las anemias hemolítica y sideroblástica, la ferropenia, intoxicación por plomo (porfirismo tóxico), falla renal, colestasis, enfermedad hepática y hemorragia intestinal2. Como la PIA es una condición que puede amenazar la vida, el diagnóstico y tratamiento oportunos son imperativos. Los pilares del tratamiento son:
- •
Identificar y controlar los eventos desencadenantes.
- •
Mejorar los síntomas.
- •
Disminuir la actividad de la ALA sintetasa.
Los factores desencadenantes pueden ser medicamentos (que inducen los citocromos), la desnutrición (que induce la ALA sintetasa), las infecciones y los factores hormonales (uso de anticonceptivos orales). En la paciente no fue posible identificar un factor desencadenante claro.
El control de los síntomas abdominales y comportamentales responde a clorpromazina, por el efecto inhibitorio que ejerce a nivel ganglionar autonómico. El dolor puede ser controlado con opiáceos. Las manifestaciones cardiovasculares (hipertensión y taquicardia) pueden manejarse con betabloqueadores, aunque los IECA y los ARAII también son seguros16.
La hidratación con soluciones dextrosadas contribuye a suprimir la actividad de la ALA sintetasa, por eso debe iniciarse un aporte elevado de glucosa (400g/día). La hemina a una dosis de 3-4mg/k/día inhibe adecuadamente la actividad de la ALA sintetasa, suele administrarse durante 4 días y es efectiva en la disminución del dolor, el riesgo de neuropatía severa y la morbimortalidad9.
Los nuevos enfoques terapéuticos se enfocan en un tratamiento curativo como la terapia de reemplazo enzimático y el trasplante hepático, el cual se ha documentado sobre todo en pacientes con PIA, con resultados alentadores pues disminuye la excreción de ALA y PBG urinario, mejora los síntomas neurológicos y mejora la calidad de vida2,3.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.