Propiedades farmacológicas generales de los anestésicos locales
Los anestésicos locales disponibles en el mercado rara vez contienen sólo un anestésico. Normalmente contienen aditivos como vasoconstrictores, tratándose en la mayoría de los casos de simpaticomiméticos, lo que obliga a incluir un sulfito como antioxidante. Los conservantes como el metilparabén se encuentran ya únicamente en viales multidosis. La farmacodinamia de los anestésicos locales se basa en el bloqueo de los canales de sodio y la interrupción consiguiente de la conducción del estímulo en las fibras nerviosas. En el caso de los simpaticomiméticos, los vasoconstrictores actúan tanto en los receptores α-adrenérgicos como en los receptores β-adrenérgicos, por lo que pueden desencadenar distintas reacciones.
Las propiedades farmacocinéticas proporcionan información sobre la distribución y el metabolismo de los medicamentos. En el caso de los anestésicos locales se debería prestar atención a su capacidad de unión a las proteínas, a la liposolubilidad, al metabolismo y a la semivida de eliminación. Cuanto mayor es la liposolubilidad, mayor es la eficacia, pero mayor es también la toxicidad del anestésico local. Y cuanto mayor es la capacidad de unión a las proteínas, menor es la toxicidad, menor es el paso de la barrera placentaria y menor también la incidencia de efectos adversos17,18,30,32. Los anestésicos disponen de dos vías metabólicas dependiendo del tipo de enlace del resto lipófilo con el resto hidrófilo. En el caso de un enlace éster en anestésicos locales de tipo éster, el metabolismo se produce a través del desdoblamiento catalizado por colinesterasas plasmáticas. Los anestésicos locales del tipo amida se metabolizan en el hígado por acción de las monooxigenasas y las carboxilesterasas. La metabolización por las colinesterasas en el plasma es un proceso relativamente rápido, mientras que en el hígado es más lento, lo que repercute en la semivida de eliminación de los anestésicos locales. Cuanto más tiempo permanece un fármaco en su forma activa en el organismo, más durará su efecto sobre el organismo en general10,11,16,32.
¿Qué son pacientes crónicos y qué son pacientes de riesgo?
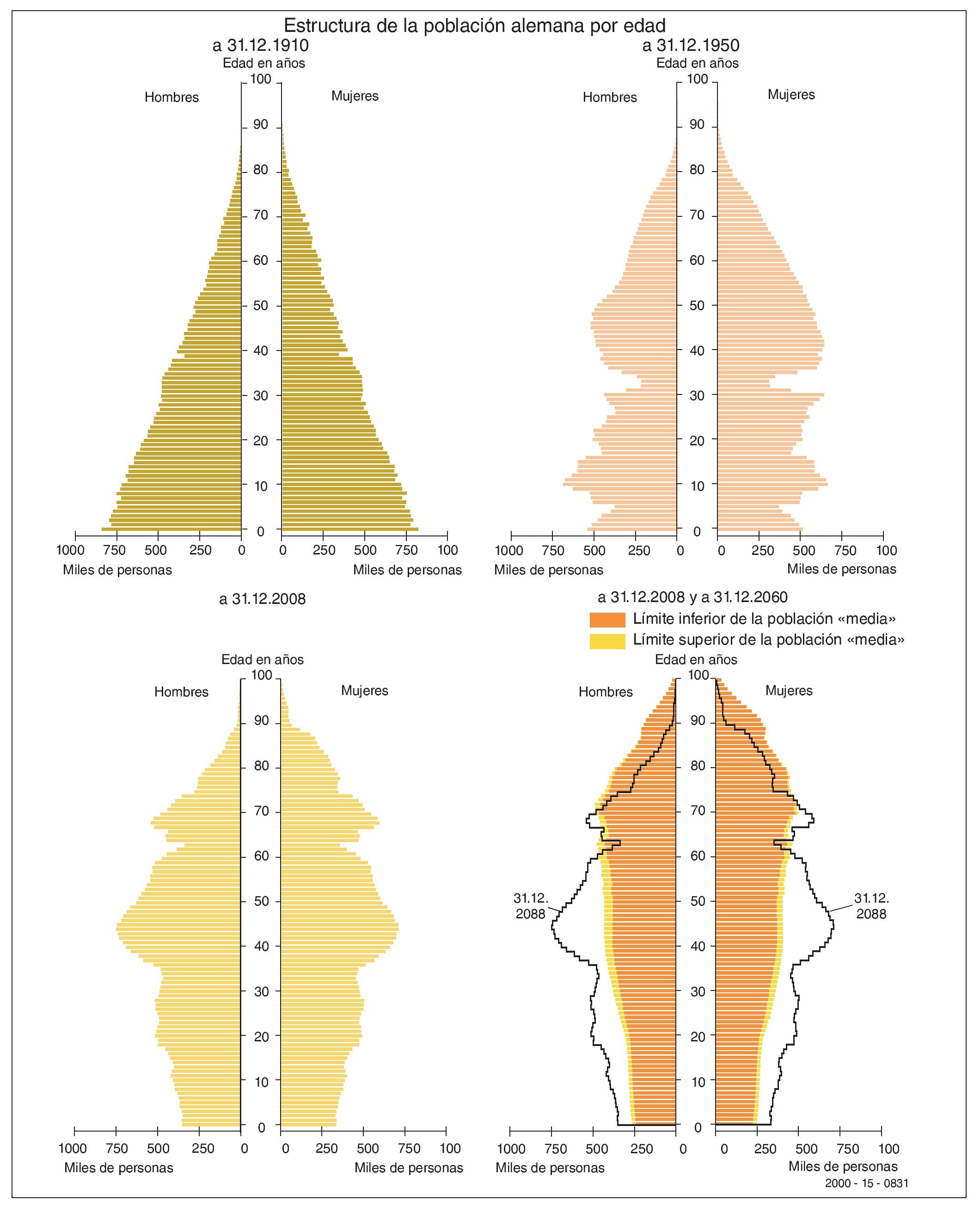
No todos los pacientes con enfermedades crónicas requieren medidas especiales ante el uso previsto de un anestésico local. Hará falta, por lo tanto, definir el concepto de paciente de riesgo en relación con las enfermedades crónicas. Se consideran pacientes de riesgo los pacientes en los que un proceso patológico crónico previo puede empeorar o evolucionar a acontecimientos críticos en caso de interacción con los anestésicos locales o con sus aditivos. Se han de tener en cuenta especialmente también las posibles interacciones con otros medicamentos. En este aspecto, los pacientes de edad avanzada merecen una atención especial por su mayor probabilidad de sufrir pluripatologías y estar sometidos a tratamientos farmacológicos crónicos (fig. 1).
Figura 1. Estructura por edad de la población alemana con proyección al año 2060 en una población cada vez más envejecida (Fuente: Statistisches Bundesamt 2009).
Los efectos sistémicos de los anestésicos locales
Los anestésicos locales influyen de diversas maneras en el organismo. Además del efecto local deseado, la inhibición de la conducción del estímulo puede repercutir, en determinadas circunstancias, sobre el sistema nervioso central y el sistema cardiovascular. Su metabolismo interfiere en la función hepática, la función renal y probablemente con otros medicamentos. En lo que se refiere al sistema nervioso central, es posible que la depresión de centros corticales inhibidores superiores lleve a la actividad incontrolada de centros inferiores. En un primer momento se produce una excitación y posteriormente una inhibición por un posible bloqueo selectivo inicial de neuronas inhibitorias. Se pueden considerar signos de alerta clínicos preconvulsionantes un sabor de boca metálico, disartria, sensación de mareo, somnolencia, tinnitus, alteraciones visuales, nistagmo y temblor muscular, más adelante se producen convulsiones generalizadas, coma y finalmente un paro respiratorio. Por lo tanto, en pacientes con enfermedades crónicas del sistema nervioso central aumenta el riesgo asociado a la anestesia local. En algunas enfermedades como la miastenia grave o la epilepsia se pueden agravar los síntomas y empeorar de este modo el estado general22,23,25,32. Las repercusiones sobre el sistema cardiovascular se deben a los efectos simpaticolíticos, ya sea directamente como resultado de la inhibición de la conducción de estímulos y de la contractilidad miocárdica o indirectamente a través del bloqueo de las fibras nerviosas autónomas cardiacas y de las fibras vasculares autónomas.
Los anestésicos locales también son vasodilatadores potentes (excepto ropivacaína y la cocaína). La vasodilatación provoca hipotensión, bradicardia sinusal, arritmias cardiacas y un inotropismo negativo por su efecto sobre la fosforilación oxidativa, como resultado de la cual disminuye la concentración intracelular de ATP15,19,32. Por lo tanto, las alteraciones graves de la generación y la conducción de estímulos en el corazón, la insuficiencia cardiaca aguda descompensada y la hipotensión grave constituyen contraindicaciones para la anestesia local. Los anestésicos locales que se metabolizan preferentemente en el hígado pueden experimentar un aumento de las concentraciones plasmáticas en presencia de medicamentos (como eritromicina, cimetidina6) que ralentizan su metabolismo. La disminución del aclaramiento renal (debido al tratamiento con propranolol, diltiazem y verapamilo12,28) puede prolongar la semivida de eliminación.
Efectos sistémicos de los vasoconstrictores
En la bibliografía se encuentran numerosas comunicacio nes de interacciones con los aditivos vasoconstrictores. En el momento de elegir un aditivo vasoconstrictor nos podemos decantar por un simpaticomimético o por un derivado de la vasopresina. Los simpaticomiméticos actúan sobre los receptores α-adrenérgicos y los receptores β-adrenérgicos. La afinidad de los distintos simpaticomiméticos disponibles por los receptores no es uniforme. Se ha constatado que, a diferencia de la adrenalina, la noradrenalina tiene bastantes más efectos adversos como cefaleas, aumento importante de la presión arterial y bradicardia. Los efectos adversos de los simpaticomiméticos suelen empeorar sobre todo las enfermedades cardiovasculares debido a su efecto sobre los receptores α y β-adrenérgicos23. Por lo tanto, los simpaticomiméticos están contraindicados en pacientes con taquicardia paroxística, taquiarritmias absolutas, en pacientes tratados con beta-bloqueantes no cardioselectivos (como propranolol, riesgo de aparición de una crisis hipertensiva o una bradicardia grave, entre otros) y en pacientes con hipertensión grave. Además, los simpaticomiméticos también están contraindicados en pacientes con hipertiroidismo, dado que las concentraciones plasmáticas altas de hormonas tiroideas en combinación con simpaticomiméticos pueden tener efectos cardiovasculares negativos. Esto se debe a una sobreestimulación del metabolismo cardiaco26,32. Los pacientes portadores de un feocromocitoma tampoco deben ser tratados con aditivos simpaticomiméticos debido a la producción tumoral de catecolaminas. En pacientes con glaucoma de ángulo cerrado, la activación del sistema simpático aumenta la producción de humor acuoso y disminuye su eliminación. En estos casos se puede producir un aumento espontáneo de la presión intraocular con el riesgo de desarrollo de un glaucoma agudo5.
Si bien las enfermedades cardiovasculares y los trastornos vasculares cerebrales no constituyen contraindicaciones para el uso de simpaticomiméticos, se ha de proceder con precaución en presencia de estas patologías. La vasoconstricción mediada por los receptores a1 puede empeorar la enfermedad de base existente o desencadenar una situación crítica en el peor de los casos. La enfermedad pulmonar crónica (como la EPOC) o el enfisema pulmonar resultante se acompañan a menudo de hipertensión pulmonar y de una insuficiencia cardiaca derecha. Las sustancias simpaticomiméticas que actúan sobre los receptores β2-adrenérgicos provocan una vasodilatación de los vasos pulmonares, a diferencia de las catecolaminas que inducen una vasoconstricción en el sistema vascular4,29. Los niveles plasmáticos altos de adrenalina pueden desencadenar una hiperglucemia en los pacientes diabéticos, debido a un aumento de la liberación de glucosa a la sangre mediada por la adrenalina23. Además, existe también la posibilidad de interacciones de los simpaticomiméticos con otros medicamentos. En el caso de los antidepresivos tricíclicos se ha demostrado que el bloqueo de la recaptación de los neurotransmisores (adrenalina, noradrenalina y serotonina) provoca un aumento de la concentración en el medio extraneuronal. En esta situación se puede producir una reacción hipertensiva accidental8. Se sospechó que las monoaminooxidasas, sustancias también pertenecientes al grupo de los antidepresivos, podían desencadenar un cuadro similar, si bien este efecto no se ha podido demostrar en estudios clínicos31.
Se ha de proceder con precaución al utilizar beta-bloqueantes no selectivos (como propranolol), dado que estos medicamentos no sólo bloquean los receptores α1-adrenérgicos, sino que también inhiben el efecto vasodilatador de los receptores β2-adrenérgicos. En estudios clínicos se observó un aumento de la presión sistólica y de la presión diastólica de 15 a 33 mmHg y de 14 a 21 mmHg, respectivamente, en pacientes hipertensos sometidos a tratamiento con propranolol durante una infusión intravenosa de 0,016 a 0,032 mg de adrenalina. Esto corresponde a una dosis de 2 ml de anestésico local (1:100.000)7. En pacientes con enfermedad de Parkinson tratados con inhibidores de la catecol-O-metiltransferasa, el bloqueo reversible de la catecol-O-metiltransferasa inhibe la inactivación de la levodopa. Dado que la adrenalina también es un sustrato de esta enzima, se puede producir un aumento de la concentración plasmática de adrenalina24. Como alternativa a los simpaticomiméticos se utilizan derivados de la hormona del lóbulo posterior de la hipófisis, la vasopresina (Felypressin), como aditivo vasoconstrictor. En pacientes con hipersensibilidad conocida a los sulfitos, la cual constituye una contraindicación absoluta para los simpaticomiméticos, los derivados de la vasopresina representan una buena alternativa. A nivel sistémico carecen de efectos adversos directos sobre el corazón, aunque pueden afectar al sistema cardiovascular a través de un aumento indirecto de la presión arterial. Están contraindicados en el embarazo dado que son inductores directos de las contracciones23.
Tratamiento de pacientes crónicos o de pacientes de riesgo con anestésicos locales
La anestesia local puede comportar un posible riesgo en las situaciones siguientes:
El anestésico local o los aditivos tienen efecto alergénico.
Administración intravascular rápida del anestésico local (precaución: anestesia de conducción, zona hiperémica), por lo que tiene un efecto sistémico directo.
El paciente se presenta con un «estado reactivo crítico» o lo padece durante el tratamiento (estrés).
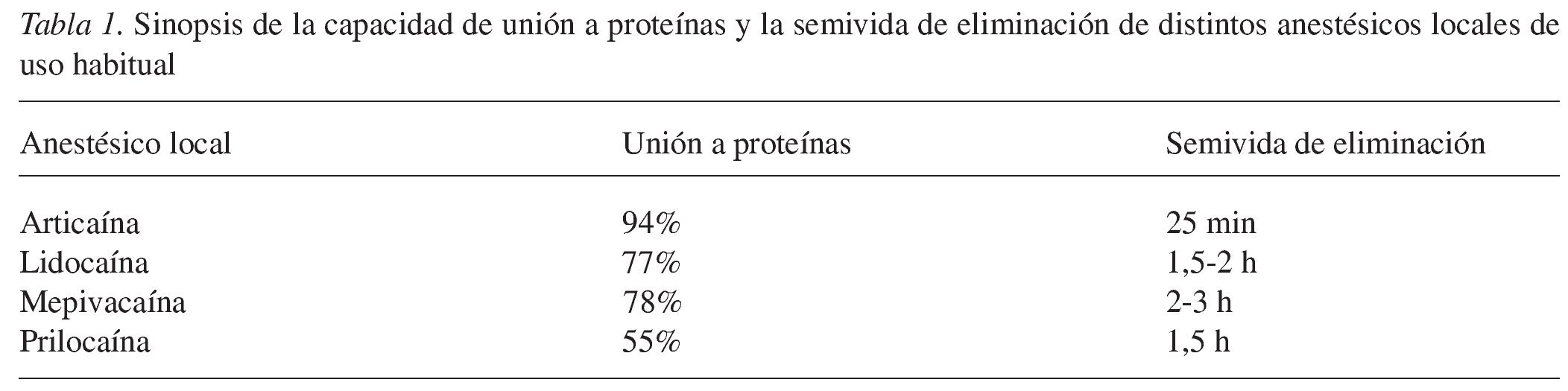
En pacientes con una anamnesis general poco clara es recomendable ponerse en contacto con el médico de cabecera o con el especialista correspondiente. Una técnica de aplicación segura con una aspiración adecuada minimiza el riesgo de administrar el anestésico en un vaso sanguíneo y, por lo tanto, el riesgo de interacciones sistémicas. En lo que se refiere a la elección del anestésico local hay que recordar que una capacidad de unión elevada a proteínas disminuye el riesgo de efectos adversos tóxicos sobre el sistema nervioso central y el paso de la barrera placentaria (tabla 1). Por el contrario, una liposolubilidad elevada aumenta la toxicidad, pero al mismo tiempo también la eficacia. Cuanto más corta es la semivida de eliminación, menor es la posibilidad de que el paciente padezca efectos cardiodepresores17,18,30,32. La semivida de eliminación de los anestésicos locales que se metabolizan por vía hepática a menudo es más larga que la de los anestésicos inactivados por colinesterasas plasmáticas32. La semivida corta de la articaína se explica por el hecho de que este anestésico de tipo amida posee un grupo éster, por lo que hasta el 90% de la sustancia es inactivada in situ (tabla 1).
Los vasoconstrictores aumentan la duración y la profundidad de la anestesia, disminuyen las concentraciones plasmáticas máximas y permiten reducir la dosis total del anestésico local23. El perfeccionamiento continuo y la introducción clínica de sustancias innovadoras con efecto anestésico local y una toxicidad cada vez menor han incrementado progresivamente la seguridad de la anestesia local. Esto se ha traducido en una disminución de la incidencia de acontecimientos sistémicos tóxicos en los últimos 35 años del 0,2% al 0,01%32. Al elegir el vasoconstrictor se debería dar preferencia a la adrenalina. La concentración de adrenalina debe ser la mínima imprescindible en pacientes de riesgo como, por ejemplo, pacientes con enfermedades cardiovasculares, enfermedades cerebrovasculares (ictus), bronquitis crónica o enfisema pulmonar, diabetes mellitus y trastornos de ansiedad graves21,23.
En 1964, la American Heart Association y la American Dental Association declararon en un documento conjunto que no existe contraindicación para el uso de vasoconstrictores en los anestésicos locales1. Malamed14, Bennett2 y Budenz3 sostienen que en pacientes con enfermedades cardiovasculares no se debe superar una dosis máxima de adrenalina de 0,04 mg para no comprometer la seguridad de los pacientes. Esto corresponde a 8 ml de una solución anestésica con adrenalina en una relación de 1:200.000. La liberación de cantidades importantes de catecolaminas endógenas como la que se puede producir en situaciones de tensión o de dolor durante un tratamiento odontológico provoca una estimulación intensa del sistema simpático. En estas circunstancias se liberan cantidades de adrenalina muy superiores a las dosis mínimas administradas de forma exógena en el marco del tratamiento odontológico13.
Las investigaciones siguientes permiten hacerse una idea acerca de la situación de equilibrio de la adrenalina en el organismo. La concentración media de adrenalina por ml de sangre en un sujeto sano en estado de reposo es, según Goldstein9, de 43 pg. Esta concentración puede aumentar hasta aproximadamente 180 pg/ml durante la inyección de un anestésico local con una concentración de adrenalina de 1:80.000, para volver a descender a alrededor de 80 pg/ml en el transcurso de la intervención quirúrgica odontológica. Wittstein et al.27 comprobaron que a concentraciones de adrenalina superiores a 1.264 pg/ml por término medio aumentaba la posibilidad de aparición de acontecimientos cardiológicos reversibles. Una situación de estrés emocional repentino podía actuar como factor desencadenante20. En el caso hipotético de administración intravenosa de una ampolla de Ultracain D-S con adrenalina en una relación de 1:200.000, se obtiene una concentración calculada de adrenalina de 1.200 pg/ml con el riesgo real de desencadenar efectos cardiológicos reversibles. Hay que recordar que la semivida biológica de la adrenalina es muy corta (< 1 min) debido a un proceso oxidativo, por lo que los efectos adversos sistémicos han de ser forzosamente de corta duración.
Aunque es evidente que el embarazo no puede ser considerado una enfermedad crónica, en las embarazadas se ha de elegir un anestésico local con una gran capacidad de unión a proteínas para disminuir el paso del anestésico de la madre al feto a través de la placenta y proteger de este modo al feto de posibles efectos tóxicos. La concentración del vasoconstrictor se debe reducir al mínimo imprescindible (1:200.000). Se recomienda utilizar adrenalina como vasoconstrictor23. La vasopresina está contraindicada en el embarazo por la posible inducción de contracciones.
Si el tratamiento odontológico con anestesia local entraña un riesgo para un determinado paciente por su estado general, de acuerdo con la información aportada por su médico de cabecera, se recomienda monitorizar al paciente con pulsioximetría y el control de la presión arterial. En determinados casos puede estar indicada también la presencia de un anestesista, por si fuera necesaria su intervención.
A continuación se resumen nuevamente los puntos más importantes que pueden contribuir a minimizar el riesgo de un acontecimiento anestésico:
Anamnesis completa/anamnesis farmacológica
Descartar hipersensibilidades
No acudir en ayunas, tomar la medicación habitual
Ejecución cuidadosa de la anestesia
Anestésico local con adrenalina (máximo 1:100.000)
Aspiración suficiente en las anestesias de conducción
Siempre que sea posible evitar las anestesias de conducción
Aplicación lenta
Monitorización si procede (pulsioximetría)
Conclusiones
La anestesia local forma parte desde hace más de 100 años de distintos procedimientos odontológicos. Los riesgos y los efectos adversos han ido disminuyendo y su aplicación es cada vez más segura gracias a la evolución continua, a la suma de experiencias y a la mejoría de las propiedades farmacológicas de los principios activos anestésicos. Sin embargo, antes de aplicar una anestesia local es imprescindible obtener una anamnesis completa y, en caso de duda, consultar con el médico de cabecera con el fin de determinar si una enfermedad crónica existente permite utilizar un anestésico local con adición de adrenalina, si el caso lo requiere. El anestésico local elegido debe tener la potencia suficiente con la mínima toxicidad posible. La adrenalina, como aditivo vasoconstrictor, es la que muestra menos efectos adversos, debiendo utilizarse a concentraciones bajas (máximo 1:100.000). De no poder descartar totalmente posibles situaciones de emergencia debido a un estado general deteriorado del paciente, se monitorizarán los parámetros circulatorios y respiratorios.
Correspondencia: C.K. Müller.
Theodor Stern-Kai 7, 60590 Fráncfort, Alemania.