Evaluar la eficacia y seguridad de 5 y 25mg de mifepristona en el tratamiento de la endometriosis.
DiseñoEnsayo clínico aleatorizado, doble ciego.
LugarHospital Eusebio Hernández, La Habana, Cuba.
SujetosVeintiséis mujeres con diagnóstico laparoscópico de endometriosis.
TratamientosGrupo I: una tableta oral diaria de 25mg de mifepristona, o grupo II: una tableta oral diaria de 5mg de mifepristona, durante 6 meses. Se realizó laparoscopia y biopsia endometrial pre y postratamiento.
Variable para evaluar eficaciaReducción de la intensidad de la dismenorrea medida por una escala visual análoga.
ResultadosEn ambos grupos las disminuciones de la intensidad de la dismenorrea y la dispareunia fueron muy significativas comparadas con los valores iniciales. Todas las mujeres estaban en amenorrea a los 45 días de tratamiento.
ConclusionesLa mifepristona, en dosis de 25 o 5mg, podría ser una alternativa para el tratamiento de la endometriosis.
To evaluate the safety and efficacy of 5mg and 25mg doses of mifepristone for the treatment of endometriosis.
DesignRandomized double-blind study.
SettingEusebio Hernández Hospital, Havana, Cuba.
SubjectsTwenty-six women laparoscopically diagnosed with endometriosis were included.
TreatmentGroup I received one tablet of 25mg mifepristone daily and group II received one tablet of 5mg mifepristone daily for 6 months. Laparoscopy and endometrial biopsy were performed before and after treatment.
Variable to evaluate efficacyReduction in the intensity of dysmenorrhea measured by a visual analogue scale.
ResultsIn both groups reductions in the intensity of dysmenorrhea and dyspareunia were highly significant compared with initial values (P<.001). All the women were amenorrheic after 45 days of treatment.
ConclusionsAt doses of 5mg or 25mg, mifepristone could be an alternative for the treatment of endometriosis.
Se estima que la endometriosis afecta al 10-15% de las mujeres en edad reproductiva y que del 25 al 40% de las mujeres infértiles presentan endometriosis1,2.
Los progestágenos y el danazol, debido a sus intensos efectos androgénicos, han ido siendo sustituidos en el tratamiento de esta afección por los análogos de la GnRH3-6.
Asimismo, debido a las intensas sintomatologías hipoestrogénicas que provocan los análogos de la GnRH y a la pérdida de densidad ósea que se produce cuando se emplean por largos periodos, su uso está sensiblemente limitado, aun cuando se asocie a terapia de apoyo7.
Por tanto, se necesitan nuevos fármacos que sean altamente efectivos y seguros en esta patología.
La mifepristona (RU-486) tiene actividad antiprogestagénica y antiglucorticoidea8. Al impedir que la progesterona actúe se está comprometiendo el normal desarrollo del endometrio, tanto el eutópico como el ectópico, de los focos endometriósicos, ya que en la fase secretora del ciclo menstrual es dependiente del progestágeno. La ausencia de acción progestágena en el endometrio provoca una disrupción de la maduración del mismo9,10. También se sabe que la mifepristona provoca retraso de la maduración folicular y anovulación con disminución del nivel de estrógenos11-13. Estas acciones nos indujeron a pensar, igual que al Dr. Kettel hace 15 años, que la mifepristona podría ser eficaz en el tratamiento de la endometriosis, ya que el endometrio ectópico también presenta receptores de progesterona y estrógenos.
Utilizada en monos, la mifepristona ha mostrado ser tan eficaz como los análogos de la GnRH en la reducción de las lesiones endometriósicas14.
Kettel et al., con dosis diarias de 100mg de mifepristona durante 3 meses consiguieron disminuciones significativas del dolor endometriósico, pero se produjo un efecto antiglucocorticoideo negativo15. Con dosis de 50mg diarios durante 6 meses consiguió una regresión de las lesiones endometriósicas del 55% de su extensión, similar mejoría clínica en el dolor y, además, desaparición del efecto antiglucocorticoideo16. Su último estudio utilizando dosis diarias de 5mg durante 6 meses consigue similar mejoría clínica en el dolor, pero en su estudio afirman que no hay cambios significativos en las lesiones endometriósicas17.
Otros moduladores de los receptores de la progesterona (MRP), como el asoprisnil (J867) o el CDB-4124 (Proellex), han demostrado eficacia en el tratamiento de la endometriosis18,19.
El objetivo del actual estudio es evaluar la eficacia y seguridad de dosis diarias de 5 y 25mg de mifepristona durante 6 meses en el tratamiento de la endometriosis.
Material y métodosDiseñoSe presenta un ensayo clínico aleatorizado, con doble cegamiento, para evaluar la eficacia y la seguridad de dosis diarias de 5 y 25mg de mifepristona durante 6 meses en el tratamiento médico de la endometriosis. El ensayo clínico se realizó en el Hospital Eusebio Hernández de La Habana, Cuba. El protocolo del estudio fue aprobado por el comité de investigaciones y ética del hospital. Todas las mujeres incluidas dieron consentimiento informado por escrito. El ensayo clínico fue realizado en concordancia con la versión revisada de la Declaración de Helsinki y con las normas de las buenas prácticas clínicas. El estudio comenzó en noviembre de 2008 y la última paciente incluida fue evaluada en mayo de 2010, 6 meses después de haber concluido el tratamiento con mifepristona.
SujetosMujeres voluntarias, entre 18 y 45 años de edad, sin otra enfermedad, con o sin diagnóstico de infertilidad, fueron elegibles para el estudio. Fueron enviadas 32 pacientes de la consulta de clasificación del hospital y evaluadas para su inclusión en el estudio. Criterios de inclusión: a) diagnóstico de certeza de endometriosis, de cualquier grado en correspondencia con la clasificación modificada de puntuación de la American Fertility Society (AFS) realizado por laparoscopia20; b) dismenorrea y/o dolor pélvico definido como sigue: dolor localizado dentro de la verdadera pelvis o entre y por debajo de las crestas iliacas anteriores, y/o dispareunia; c) aceptar el uso de métodos anticonceptivos de barrera durante el estudio. Criterios de exclusión: a) histerectomía, ooforectomía o salpingectomía previas; b) amenorrea de más de 3 meses de duración; c) lactancia; d) tratamiento hormonal o quirúrgico para la endometriosis menos de 4 meses antes de comenzar el estudio; e) enfermedades como diabetes, hipertensión arterial severa, hepatopatías, endocrinopatías o tratamientos con otras hormonas, incluidos los contraceptivos hormonales; f) patología endometrial, y g) cualquier contraindicación para el uso de antiprogestágenos.
TratamientosDespués de la evaluación inicial, las mujeres fueron asignadas a uno de los 2 grupos de tratamiento: grupo I: una tableta diaria, por vía oral, de 25mg de mifepristona, o grupo II: una tableta diaria por vía oral de 5mg de mifepristona, por un periodo de 6 meses en ambos grupos y comenzando entre el segundo y cuarto días de la menstruación. Las tabletas de 25 y 5mg de mifepristona eran iguales en aspecto, color y forma. En cada visita de control o evaluación de la paciente se le suministró el frasco con la cantidad de medicamento necesaria hasta la próxima visita y así sucesivamente hasta completar los 6 meses de tratamiento. La mifepristona fue adquirida en los Laboratorios Beijing ZIZHU PHARM Co. Ltd., China.
La asignación al tratamiento fue como sigue: se elaboró una lista aleatoria generada por una computadora. Personal ajeno al estudio, preparó sobres opacos sellados con un número de serie cada uno conteniendo una tarjeta que indicaba el grupo de tratamiento al que se asignaba la paciente. Las mujeres fueron asignadas a uno u otro grupo de tratamiento de manera aleatoria como sigue: una vez que se evaluó a la paciente según los criterios de inclusión y exclusión y firmado el consentimiento informado, se procedió a abrir el sobre correspondiente al número de orden de entrada de la paciente en el estudio y se le asignó al tratamiento indicado en la tarjeta que contenía el sobre «mifepristona A» o «mifepristona B» en que «A» correspondía a una de las dosis y «B» a la otra. Este código fue abierto después de finalizado el primer procesamiento de datos. Ni los médicos ni las pacientes conocieron a qué grupo de mifepristona se realizó la asignación. Este proceso fue controlado por el monitor del estudio.
Exámenes realizadosExamen ginecológico completo, ultrasonografía pélvica y laparoscopia diagnóstica (no terapéutica) antes del inicio del tratamiento mediante la que se determinaron la localización, la extensión y el grado de severidad de las lesiones endometriósicas y se asignó una puntuación (score) de acuerdo con la clasificación revisada de la AFS20.
Al finalizar el tratamiento, se realizó una laparoscopia diagnóstica-terapéutica, es decir, después que se calculó el score final de la AFS. Se tomó una muestra de sangre para estudios hematológicos y de la función hepática en cada visita de control. Se realizó una biopsia endometrial antes del tratamiento si había alguno de los siguientes criterios: a) grosor endometrial>8mm; b) episodios de sangrado vaginal de más de 10 días de duración; c) sangrado vaginal en las 3 semanas antes del inicio de la menstruación, y d) sangrado vaginal muy abundante. A todas las mujeres se les tomó una muestra para la biopsia endometrial al final del tratamiento.
Hubo visitas de control o evaluación cada 45 días hasta el fin del tratamiento. Una vez finalizado este, las mujeres fueron evaluadas 3 y 6 meses después. En el periodo de seguimiento no se suministró ningún otro tratamiento ni placebo para la endometriosis que pudiera enmascarar la evolución o los síntomas de la enfermedad. En las consultas de evaluación y seguimiento se entregó a las pacientes un modelo para registrar episodios de sangrado, los efectos de la mifepristona y cualquier otra información; estos modelos fueron devueltos por las pacientes en cada consulta de evaluación o seguimiento.
Variables para evaluar eficaciaLa variable principal para la evaluación de la eficacia fue la intensidad de la dismenorrea, medida esta por una escala visual análoga (EVA) con valores de 0 a 10, en que 0 significa la ausencia del síntoma y 10 su valor máximo en intensidad, y su reducción promedio con respecto al valor inicial fue la forma de evaluarla. Los valores de esta variable fueron señalados por la propia paciente y se midió antes del inicio del tratamiento y cada 45 días hasta el final del mismo y a los 3 y 6 meses después.
Otras variables para la evaluación de la eficaciaa) Cambios en la intensidad de la sintomatología atribuible a la endometriosis: dolor pélvico, dispareunia, alteraciones urinarias y trastornos intestinales; los síntomas se evaluaron por una EVA con metodología y frecuencia descritas para la dismenorrea, y b) porcentaje de reducción de la puntuación (o scores según AFS) de las lesiones endometriósicas con respecto al de antes del inicio del tratamiento con mifepristona. Esta variable se evaluó por laparoscopia antes del inicio del tratamiento y al final de este.
Variables para evaluar la seguridada) Cambios en el grosor endometrial medido por ultrasonografía (mm); se evaluó al inicio, en cada consulta intra-tratamiento, al final y a los 3 y 6 meses post tratamiento; b) efectos secundarios de la mifepristona: amenorrea, calores o sofocos, náuseas, mareos, vómitos, fatiga/cansancio; c) cambios en los valores de transaminasas hepáticas evaluadas antes del inicio del tratamiento y cada 3 meses hasta el final de este, y d) frecuencia de hiperplasia simple endometrial postratamiento o cambios endometriales asociados al uso de moduladores de los receptores de progesterona (PAEC, receptors modulators of progesterone associated with endometrial changes)21-23.
Número de pacientes que se deben incluirLa intensidad de la dismenorrea (EVA) fue la variable utilizada para calcular el número de pacientes a incluir en el estudio. Se asumió que después del tratamiento de mifepristona la intensidad promedio de la dismenorrea con 25mg sería 1,0±1,5 y que con 5mg de mifepristona ese valor sería 3,0±1,5. Esos promedios y las desviaciones estándar para ambas dosis fueron estimados sobre la base de un estudio piloto realizado en el hospital antes de que se iniciara el presente ensayo clínico. Un análisis de la potencia realizado con el Software GPower 3.0.10 indicó que se obtendría una potencia del 80% con α=0,05 con 12 mujeres en cada grupo de tratamiento en una hipótesis bilateral24.
Análisis estadísticoPara evaluar la homogeneidad de los 2 grupos de tratamiento se utilizó el test paramétrico de la t para diferencia de promedios, la prueba de la chi al cuadrado de Pearson y la probabilidad exacta de Fisher, pruebas no paramétricas para contrastar la hipótesis en tablas de contingencia de que las variables por filas y columnas son independientes, y la prueba no paramétrica de aproximación normal para comparar proporciones. Los cambios ocurridos en la intensidad de la dismenorrea y la dispareunia medidos por la EVA cada 45 días hasta el fin del tratamiento y 3 y 6 meses postratamiento se analizaron mediante un modelo de efectos fijos con medidas repetidas sin incluir covariables y se utilizó la t de Dunnett para las comparaciones con el valor inicial (prueba de comparación por parejas basada en el módulo máximo según la prueba de Student que es adecuada cuando las varianzas son desiguales). Este procedimiento se empleó para el análisis de los cambios del grosor endometrial en cada periodo de evaluación, comparando con el valor antes del tratamiento.
El análisis de los cambios en la puntuación de la AFS se realizó teniendo en cuenta solamente a las mujeres que tuvieron laparoscopia postratamiento y se utilizó el test no paramétrico para muestras relacionadas de Wilcoxon para comparar con los valores iniciales dentro de cada grupo de tratamiento. La comparación entre grupos se hizo usando la prueba no paramétrica de la U de Mann-Whitney. Los efectos secundarios de la mifepristona se presentan mediante estadígrafos descriptivos. En todos estos casos se consideró significativo un valor de p<0,05. Los datos fueron procesados con el SPSS 11.5. Los resultados se presentan como frecuencias, porcentajes, medias, desviaciones estándar e intervalos de confianza (IC) del 95% para promedios y porcentajes.
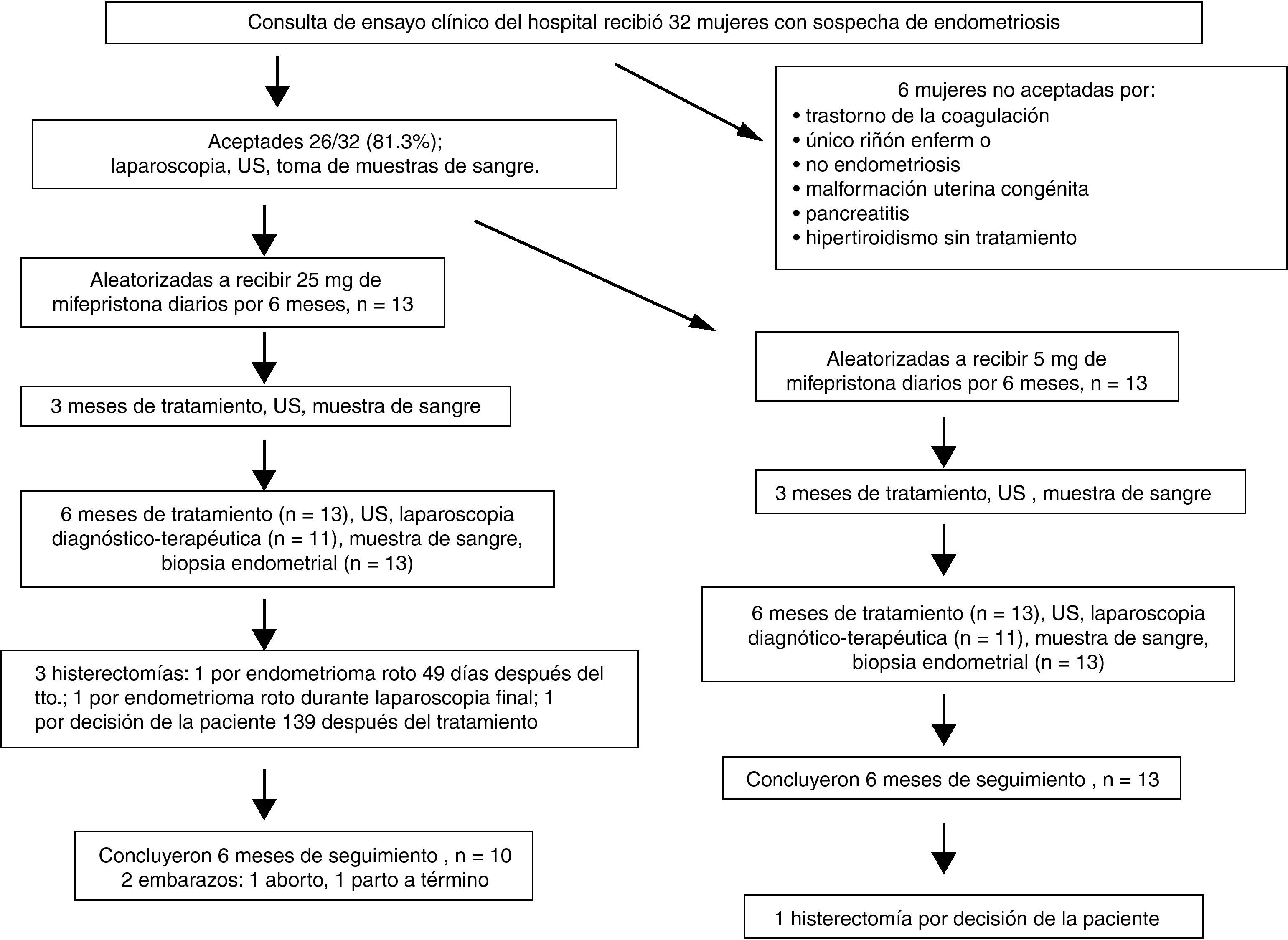
ResultadosInclusión y seguimientoSe incluyó a 26 mujeres, 13 en cada grupo de tratamiento, con endometriosis confirmada por laparoscopia previa al tratamiento con mifepristona. Del total de las 32 mujeres remitidas a la consulta del estudio no se incluyó a 6 (18,6%) por no reunir los requisitos de inclusión. Todas las mujeres completaron los 6 meses de tratamiento (fig. 1).
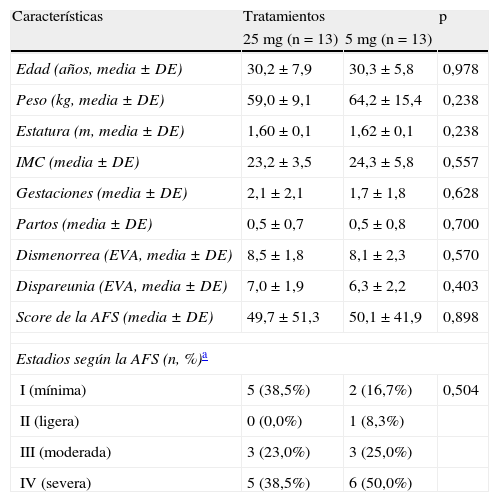
Variables iniciales y comparación entre grupos de tratamientoEn la tabla 1 se muestran las características generales de las mujeres incluidas según grupos de tratamiento con mifepristona. En total, 15/26 (57,8%) de las mujeres eran de raza blanca, 3/26 (11,5%) eran negras y 8/26 (30,7%) eran mestizas; no hubo diferencias significativas entre los grupos de tratamiento (p=0,231).
Características de las mujeres por grupos de tratamiento con mifepristona
| Características | Tratamientos | p | |
| 25mg (n=13) | 5mg (n=13) | ||
| Edad (años, media±DE) | 30,2±7,9 | 30,3±5,8 | 0,978 |
| Peso (kg, media±DE) | 59,0±9,1 | 64,2±15,4 | 0,238 |
| Estatura (m, media±DE) | 1,60±0,1 | 1,62±0,1 | 0,238 |
| IMC (media±DE) | 23,2±3,5 | 24,3±5,8 | 0,557 |
| Gestaciones (media±DE) | 2,1±2,1 | 1,7±1,8 | 0,628 |
| Partos (media±DE) | 0,5±0,7 | 0,5±0,8 | 0,700 |
| Dismenorrea (EVA, media±DE) | 8,5±1,8 | 8,1±2,3 | 0,570 |
| Dispareunia (EVA, media±DE) | 7,0±1,9 | 6,3±2,2 | 0,403 |
| Score de la AFS (media±DE) | 49,7±51,3 | 50,1±41,9 | 0,898 |
| Estadios según la AFS (n, %)a | |||
| I (mínima) | 5 (38,5%) | 2 (16,7%) | 0,504 |
| II (ligera) | 0 (0,0%) | 1 (8,3%) | |
| III (moderada) | 3 (23,0%) | 3 (25,0%) | |
| IV (severa) | 5 (38,5%) | 6 (50,0%) | |
AFS: American Fertility Society; DE: desviación estándar; EVA: escala visual análoga; IMC: índice de masa corporal.
La dismenorrea y la dispareunia estaban presentes en el 100% de las mujeres en ambos grupos de tratamiento. En total, 8/26 (30.8%) de las mujeres incluidas, 3/13 (23.1%) del grupo de 25 y 5/13 (38,5%) del de 5mg de mifepristona tenían infertilidad asociada a la endometriosis, p=0,198. Los trastornos intestinales fueron referidos por 6/26 (23,1%) mujeres, 3 en cada grupo de tratamiento, p=1,000. Los trastornos de la micción estaban presentes en el 23,1% de las pacientes incluidas en el grupo de 5mg de mifepristona (p<0,033) y ausentes en el grupo de 25mg.
Se realizó laparoscopia diagnóstica inicial (no terapéutica) al total de mujeres incluidas y en todas se confirmó la endometriosis, excepto en un caso en que no se ratificó endometriosis pélvica pero sí se hizo un diagnóstico de sospecha de endometriosis en la rafia de la episiotomía de un parto anterior. Este diagnóstico de sospecha se convirtió en diagnóstico de certeza por exclusión, ya que el intenso dolor que presentaba en la rafia cuando menstruaba desapareció con el tratamiento con mifepristona.
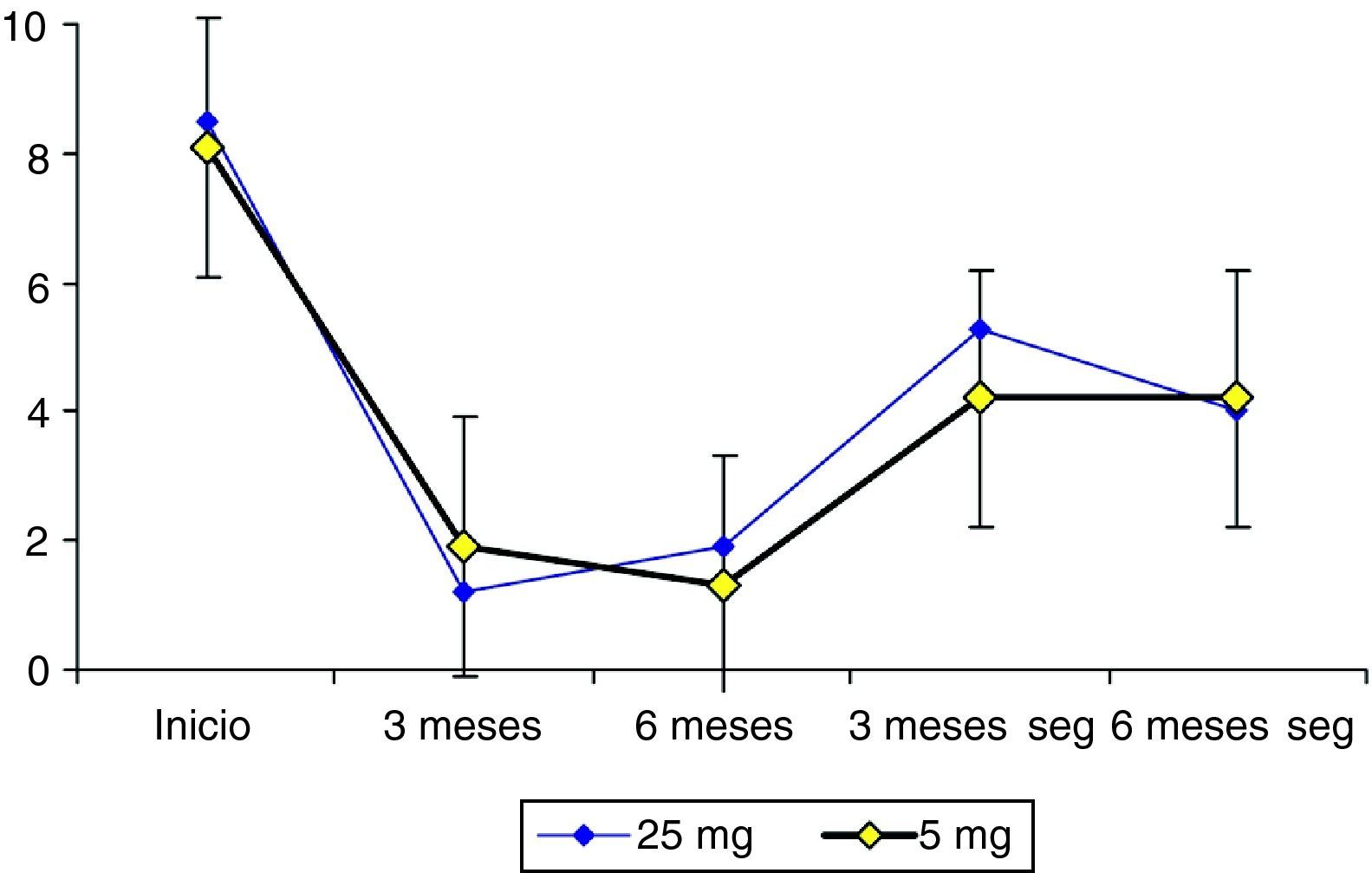
EficaciaDismenorreaLa figura 2 muestra las variaciones en la intensidad de la dismenorrea (EVA) en los periodos evaluativos del estudio. No hubo diferencias significativas entre los grupos de mifepristona. En cada grupo de tratamiento la disminución de la intensidad de la dispareunia en cada visita fue muy significativa cuando se comparó con los valores iniciales (fig. 3).
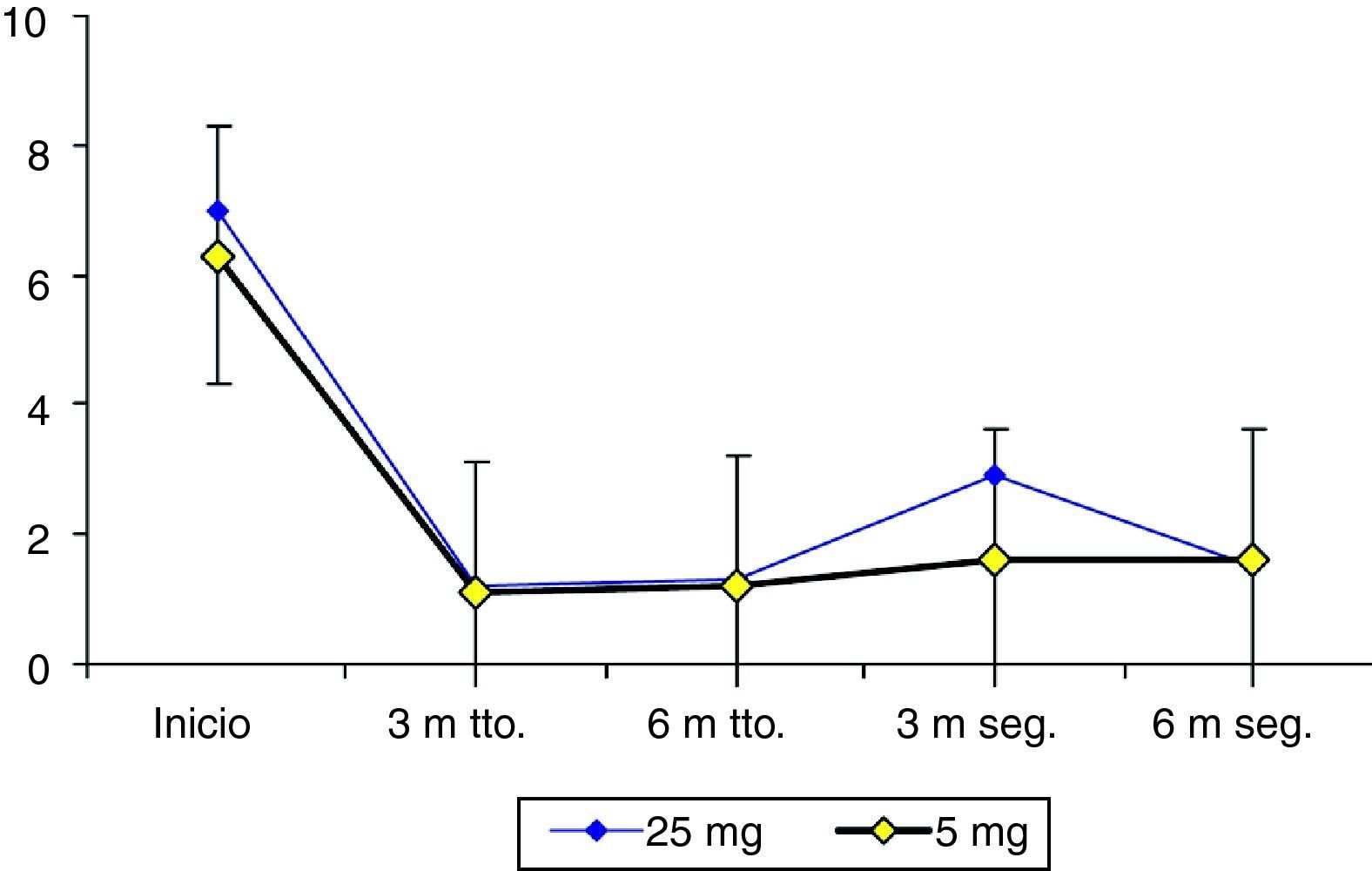
Otros síntomas de la endometriosisLa figura 3 muestra las variaciones en la intensidad de la dispareunia (EVA) en los consultas del estudio. No hubo diferencias significativas entre los grupos de mifepristona. En ambos grupos de tratamiento la disminución de la intensidad de la dispareunia fue significativa en cada visita cuando se comparó con los valores iniciales.
De las 9 mujeres que presentaban alteraciones urinarias o intestinales antes del tratamiento, solo 1 tenía trastornos intestinales 3 meses después de iniciado aquél, siendo negativo este caso al final del tratamiento.
Scores promedios de la AFSSe realizó laparoscopia evaluativa-terapéutica final a 22/26 (84,6%) participantes. En las 22 participantes con laparoscopia final, el score (AFS) inicial fue 58,2±51,5 (rango 2–134) y de 42,7±34,8 (rango 1-131) en los grupos de 25 y 5mg, y al final fue 23,7±32,1 (rango 0-81) y 10,5±13,0 (rango 0-34), es decir, se produjo una reducción significativa del 59,3%, p=0,033 (Wilcoxon) y de 75,4%, p=0,005 (Wilcoxon), respectivamente. La diferencia entre los grupos de mifepristona no fue significativa, p=0,765, con una potencia a posteriori de 80%.
Cambios en las magnitudes de los scores de la AFSEn el grupo de 25mg de mifepristona, en 9/11 (82%) mujeres hubo reducción del score de la endometriosis y en 2/11 (18%) pacientes hubo ligero aumento del mismo. En el grupo de 5mg de mifepristona, en 10/11 (91%) hubo disminución del score de la endometriosis y en 1/11 (9/%) la puntuación fue la misma que al inicio del tratamiento. La diferencia entre los grupos de tratamiento no fue significativa, p=1,000.
Estadios y tipos de endometriosisEn el grupo de 25mg de mifepristona, hubo 11/13 (85%) participantes con laparoscopia postratamiento: en 3/11 (27.3%) de ellas que al inicio estaban en el estadio I no se observaron lesiones endometriósicas al final del tratamiento; en 2/11 (18.2%) con estadio III antes del tratamiento 1/11 (9,1%) pasó al estadio II y 1/11 (9,1%) quedó en el mismo estadio, aunque con puntuación ligeramente menor. De las 6 que estaban en estadio IV, 4/11 (36,4%) quedaron en el mismo, aunque con puntuaciones inferiores la mayoría y 2/11 (18.2%) pasaron al estadio III.
En el grupo de 5mg hubo 11/13 (85%) mujeres con laparoscopia final; 3/11 (27,3%) que estaban en estadio I al inicio quedaron en el mismo; 2/11 (18,2%) con estadio III quedaron en el mismo con puntuaciones inferiores, de las 6 que estaban en estadio IV, 4/11 (36,4%) quedaron en el mismo aunque con puntuaciones menores y 2/11 (18,2%) pasaron al estadio III.
El 65% de los casos presentaban afectación peritoneal profunda y el 15% superficial. El 73% presentaba afectación ovárica profunda y el 18% superficial. El 34,5% de los casos hubo afectación pélvico-ovárica. Hubo afectación del saco de Douglas en el 31% de las mujeres. El 61% de los casos presentaba gruesas adherencias. Un caso no fue endometriosis pélvica ni ovárica, sino intramuscular en el lugar de la cicatriz de la episiotomía. No hubo diferencias significativas en la distribución de la endometriosis entre ambos grupos de tratamiento, p=0,574.
Cambios en las dimensiones de los endometriomasPor ultrasonografía, fueron observados endometriomas en 5 pacientes del grupo de 25mg y 4 del grupo de 5mg de mifepristona. Se observaron disminuciones no significativas (p>0,05), de las dimensiones de los endometriomas del 34 y el 48,4% a los 3 y 6 meses de tratamiento, respectivamente, en el grupo de 25mg con respecto a los valores iniciales. En el grupo de 5mg no hubo reducciones significativas (p>0,05), del 2,3 y el 18% a los 3 y 6 meses de tratamiento, respectivamente, en relación con los valores pretratamiento. En este grupo, la ultrasonografía no demostró evidencia de endometriomas en 2 pacientes al final del tratamiento. Al final del tratamiento no hubo diferencias significativas entre los grupos de tratamiento en cuanto a la disminución promedio del volumen de los endometriomas, p=0,176.
SeguridadEfectos secundarios de la mifepristonaAmenorreaLas participantes de ambos grupos de mifepristona estaban todas ya en amenorrea a los 45 días de tratamiento. A los 6 meses continuaban en amenorrea 11/13 (85%) y 10/13 (77%) de los grupos de 25 y 5mg, respectivamente, p=0,309. En total 5/26 (19,2%) presentaron sangrado intratratamiento. Dos mujeres del grupo de 25mg sangraron entre el quinto y sexto mes del tratamiento, 1 de ellas reportó dolor intenso durante el sangrado igual que al inicio del tratamiento (10 en la EVA) y en esta mujer el grosor endometrial al final del tratamiento era de 20mm; la otra refirió intensidad 1 en la dismenorrea cuando sangró. Las 3 mujeres del grupo de 5mg sangraron entre el quinto y sexto mes de tratamiento, solo 1 refirió dismenorrea de intensidad 6 (EVA), que era de 10 antes del tratamiento con mifepristona; las 2 mujeres restantes no reportaron dismenorrea con el sangrado. La duración promedio del spotting fue 5,0±2,3 y 3,0±2,0 días en los grupos de 25 y 5mg, respectivamente, p=0,261. El sangrado tuvo una duración promedio de 4,1±2,5 y 2,1±1,5 días en los grupos de 25 y 5mg, respectivamente, p=0,263.
SofocosReportaron sofocos 1/13 (8%) y 1/13 (8%) mujeres a los 45 días de tratamiento en los grupos de 25 y 5mg, respectivamente, p=0,500. A los 3 meses de tratamiento, los reportes de sofocos fueron 3/13 (23,1%) y 2/13 (15,4%) en los grupos de 25 y 5mg, respectivamente, p=0,309 y a los 6 meses en ninguna mujer del grupo de 25mg y en 1/13 (8%) del grupo de 5mg, p=0,154.
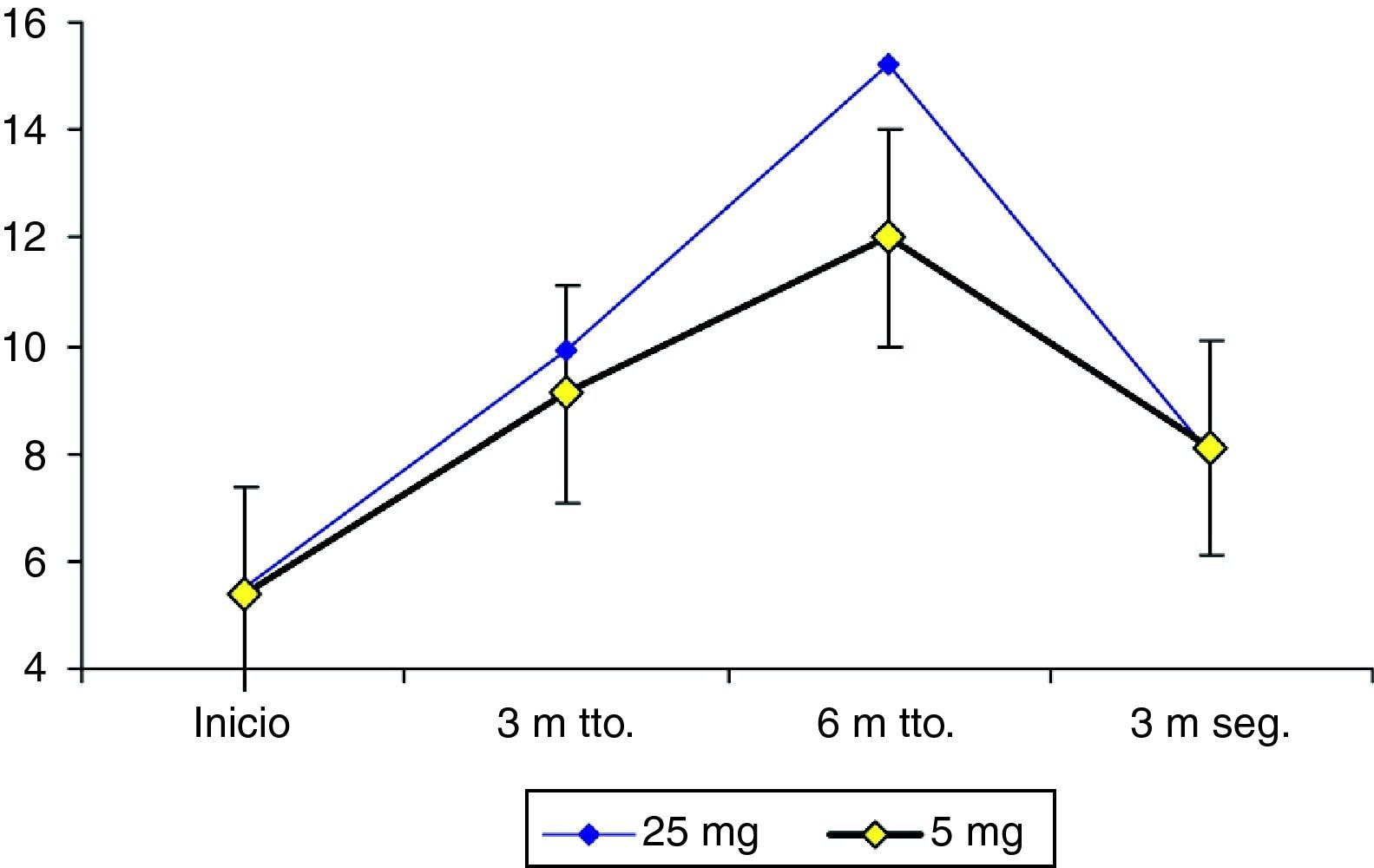
Grosor endometrial (mm)En la figura 4 están los valores del grosor endometrial a lo largo del estudio. Al final del tratamiento había 5/13 (38,5%) y 4/13 (30,7%) con valores de grosor endometrial menores o iguales que 8mm, en los grupos de 25 y 5mg, respectivamente, p=0,34, y había 4/13 (30,8%) y 5/13 (38,5%) con valores de grosor endometrial superior a 20mm en los grupos de 25 y 5mg, respectivamente. Tres meses después de concluido el tratamiento con mifepristona, el grosor endometrial había regresado a 8,0±3,3 y 8,1mm±2,4, p=0,993, en los grupos de 25 y 5mg, respectivamente.
Transaminasas hepáticasA los 3 meses de tratamiento, hubo 2/13 (15.4%) del grupo de 25mg de mifepristona con elevaciones de las transaminasas hepáticas: a) 71 U y 80 U, ASAT y ALAT, respectivamente, (valores de referencia 46 y 49 U para ASAT y ALAT, respectivamente), y b) 48 U y 57 U, ASAT y ALAT, respectivamente. Esas pacientes continuaron en el estudio después de ser evaluadas por el médico y en la visita de los 6 meses de tratamiento los valores de las transaminasas eran normales. En el grupo de 5mg no hubo valores elevados de las transaminasas hepáticas en ninguno de los periodos de evaluación.
Biopsia endometrialNo hubo diagnóstico de hiperplasia endometrial en las biopsias realizadas al inicio y al final del tratamiento con 25 o 5mg de mifepristona.
Retorno de la menstruaciónLa menstruación retornó entre 25 y 35 días después del cese del tratamiento con mifepristona, y no hubo diferencias entre los grupos de mifepristona, p>0,05.
SeguimientoCuatro mujeres (2 de cada grupo de mifepristona) se negaron a realizarse la laparoscopia final pero completaron las consultas de seguimiento. Dos de estas 4 mujeres quedaron embarazadas una vez concluido los 6 meses de seguimiento: 1 tuvo un aborto diferido a las 13 semanas de gestación y la otra ya había tenido un parto transpelviano de un recién nacido femenino a término sano en el momento de escribir este trabajo; ambas tenían diagnóstico de infertilidad asociada a la endometriosis. No asistieron a consultas de seguimiento 2 mujeres: una del grupo de 25mg a la se le realizó histerectomía en el tercer mes después de finalizado el tratamiento con mifepristona por rotura espontánea de un endometrioma y otra del grupo de 5mg, que fue operada al final del tratamiento porque en la laparoscopia final había un endometrioma en el ovario derecho de aproximadamente 7cm3, con una fisura por donde drenaba líquido achocolatado y se decidió realizar histerectomía total. Por decisión propia, a otras 2 pacientes se les realizó histerectomía a los 90 y 139 días postratamiento, respectivamente. Estas pacientes presentaban endometriomas que no pudieron ser tratados quirúrgicamente en la laparoscopia realizada al final del tratamiento. La paciente con endometriosis en la rafia decidió operarse a los 3 meses después del tratamiento y la anatomía patológica dio como resultado endometriosis.
DiscusiónEste estudio da indicios de que la mifepristona en cualquiera de las dos dosificaciones utilizadas podría ser una opción en el tratamiento de esta afección dados: a) la gran disminución en la intensidad de la sintomatología que se observó en el total de las mujeres (es decir, no hubo ni un solo caso que no tuviera una notable mejoría clínica), ya que esta disminución de intensidad fue del 77,6 y el 84,7% en la dismenorrea y del 81,4 y el 81% en la dispareunia en los grupos de 25 y 5mg, respectivamente, gracias a la amenorrea producida en la mayoría de los casos, y b) la gran disminución del tamaño y número de los implantes endometriósicos, que alcanzó disminuciones del score del 52,3 y el 79%, en los grupos de 25 y 5mg, respectivamente.
Hay que tener en cuenta que el cálculo de los porcentajes finales de disminución de las lesiones endometriósicas se excluyeron aquellos casos a los que no se les realizó el second-look laparoscópico: 4 mujeres, 2 de las cuales quedaron embarazadas después del tratamiento.
Es posible que el tratamiento esté en la base de los dos embarazos que se produjeron en el grupo de 25mg al finalizar el periodo de seguimiento de 6 meses, teniendo en cuenta que además no se beneficiaron del second-look laparoscópico y no podemos saber que puntuación de la AFS tenían postratamiento, aunque se trataba de 2 casos en estadio I con puntuaciones de 2 y 4. Una muestra de la eficacia del tratamiento es la gran adhesión a este que manifestó el 100% de las pacientes, que se traducía en la petición de las mujeres de querer continuar tomado el tratamiento ya que asimilaban mentalmente que la finalización del mismo significaba empeoramiento de su enfermedad.
Aun teniendo en cuenta que la ultrasonografía no es una ciencia diagnóstica exacta en materia de endometriosis, hay que resaltar que disminuyó tanto el número de endometriomas como el volumen de estos en mayor o menor medida según que grupo de tratamiento, aunque estas disminuciones no fueron significativas casi seguramente por el exiguo número de observaciones y la gran variabilidad de esos datos.
El caso de endometriosis en la rafia, obviamente no pudo ser valorado por laparoscopia, pero sí por la respuesta clínica que tuvo al tratamiento, con desaparición absoluta del dolor intramenstrual que siempre se presentaba en esa zona.
Respecto de los efectos secundarios, hay que señalar que náuseas, vómitos y fatiga, que supuestamente la mifepristona provoca, no tienen mayor frecuencia y significación clínica que los que se producen en otros tratamientos de larga duración por vía oral. Los sofocos no suponen ningún obstáculo para el uso de este tratamiento, ya que su frecuencia fue muy baja y su intensidad menor aun (muchísimo menor que los menopáusicos); no necesitaron tratamiento y ninguna mujer lo discontinuó por esta causa. Las elevaciones de las transaminasas a los 6 meses de tratamiento que ocurrieron en 2/13 (15,4%) mujeres del grupo de 25mg tienen escasa significación clínica debido a sus bajos valores y desaparecieron antes de finalizar el tratamiento.
Los 5 casos que tuvieron sangrado entre el cuarto y quinto mes del tratamiento presentan valores de grosor endometrial por encima de la normalidad: 20, 10, 23, 10, y 14mm, respectivamente. Sería factible pensar que el mecanismo de ese sangrado irregular, que la mayoría de las veces es un simple spotting, pudiera ser más debido al exceso de grosor endometrial que a factores hormonales.
Hay que señalar que los grosores endometriales alcanzados a los 6 meses de tratamiento en los dos tratamientos estudiados fueron similares, resaltando no obstante la gran diferencia que existe con el valor límite de la normalidad que es 8mm. Es interesante saber que, a pesar de este gran aumento del grosor endometrial promedio, aproximadamente un tercio de los casos a los 6 meses de tratamiento tenían valores de grosor endometrial normales (≤ 8mm) en ambos grupos de mifepristona.
En este estudio, al igual que en otros realizados con PRM, se producen significativos engrosamientos endometriales25. Nuestro estudio tiene similitudes con el realizado con CDB-4124 (Proellex), donde igualmente se produce sangrado entre el cuarto y el quinto mes de tratamiento en pacientes cuyo grosor endometrial está excesivamente aumentado19.
Se debe señalar que no hubo ningún caso de hiperplasia simple a los 6 meses de tratamiento con mifepristona en ninguno de los 2 grupos de dosis de esta, aunque ya se ha demostrado recientemente por un panel de expertos que los tratamientos de larga duración con dosis bajas de mifepristona no producen cuadros de hiperplasia simples sino modificaciones a nivel endometrial que se caracterizan básicamente por: dilataciones quísticas glandulares, alteraciones de la proporción estroma/tejido glandular, etc., que se agrupan bajo el nombre de PAEC (progesterone associated endometrial changes)21-23. Llama la atención poderosamente el hecho de que el engrosamiento endometrial solo se produce a nivel intrauterino, ya que los focos ectópicos endometriósicos no experimentan este fenómeno, sino al contrario, ya que en caso contrario no se produciría la desaparición de implantes o disminución de su tamaño comprobado a nivel laparoscópico en el second-look. Sería aconsejable la realización de biopsias postratamiento para estudiar las modificaciones celulares producidas por la mifepristona.
Después de la finalización del tratamiento, las menstruaciones se presentaron entre 4 y 5 semanas más tarde.
Este nuevo tratamiento, además de presentar una eficacia similar a otras alternativas terapéuticas como análogos de la GnRh, danazol, etc., tiene la ventaja de que no provoca los indeseables efectos secundarios de estas. Kettel et al. ya demostraron que la mifepristona como antigestágeno que es no altera el perfil lipídico ni la densidad ósea16.
Un aspecto negativo de este estudio es que en su diseño no se contempló valorar o medir el impacto de este tratamiento en la calidad de vida de las mujeres a través de sistemas o cuestionarios, como por ejemplo el Short Form-36 Health Survey (SF-36)26.
Otro aspecto negativo también fue el quizás excesivo número de laparoscopistas (4) que realizaron las mediciones de los scores de la AFS, lo cual podría explicar el hecho infrecuente de que varios casos de este estudio aumentaron su score y estadio de la enfermedad.
Otro aspecto negativo fue haber diseñado un periodo de seguimiento postratamiento tan largo (6 meses) ya que es sabido todas las endometriosis empeoran con la menstruación. En este sentido, no obstante, hay que señalar que la mejoría clínica producida intratratamiento persistió de manera significativa después de la finalización del mismo, ya que a los 6 meses postratamiento la dismenorrea presentaba disminuciones del 50% en su intensidad con respecto a los valores pretratamiento. Lo mismo ocurre con la dispareunia pero con porcentajes mayores de disminución.
A modo de conclusiones, podríamos decir que: a) la mifepristona podría ser una alternativa para el tratamiento farmacológico de la endometriosis tanto en su variante de 25mg como la de 5mg; b) a igualdad de eficacia, debería ser estudiada con mayor profundidad la dosis de 5mg; c) estudios multicéntricos con mayor casuística deberían ser realizados comparando este nuevo tratamiento con los estándares actuales: análogos de la GnRh, gestágenos (dienogest), etc., y/o con grupos placebo, y d) son necesarios estudios que lleguen a periodos largos de tratamiento (1-2 años) para conocer el potencial de este fármaco, dados su relativamente alto perfil de seguridad y eficacia, especialmente si se compara con las alternativas farmacológicas existentes en la actualidad.