INTRODUCCIテ哲
La combinaciテウn de marcadores bioquテュmicos y ecogrテ。ficos para el cribado del sテュndrome de Down (SD) en el primer trimestre fue motivo de diversos estudios retrospectivos a finales de los aテアos noventa del siglo pasado. La combinaciテウn mテ。s utilizada empleaba 2 marcadores bioquテュmicos de primer trimestre, la proteテュna plasmテ。tica A asociada al embarazo (PAPP-A) y la fracciテウn ホイ libre de la gonadotropina coriテウnica (fホイ-hCG), conjuntamente con la translucencia nucal (TN) y los resultados de cada uno de los marcadores modificaban el riesgo epidemiolテウgico basado en la edad materna1-5. Este mテゥtodo de cribado de trisomテュa 21 en el primer trimestre ha recibido el nombre de Test Combinado, y sus resultados se han publicado desde el aテアo 2000, cuando se ha aplicado prospectivamente en la poblaciテウn general6-15.
En nuestro centro, desde el aテアo 1991, se evaluaron retrospectivamente los marcadores bioquテュmicos de primer trimestre y la TN en la predicciテウn del riesgo de aneuploidテュa, en las gestaciones programadas para biopsia de corion16,17. En octubre de 1999 se iniciテウ en nuestra unidad un programa prospectivo de intervenciテウn para el cribado poblacional en el primer trimestre de la gestaciテウn basado en el Test Combinado18. Una caracterテュstica especテュfica de nuestro programa reside en la prテ。ctica de las determinaciones bioquテュmicas y ecografテュcas en edades gestacionales, diferenciadas basテ。ndose en un anテ。lisis previo de nuestros datos retrospectivos, mostrando que en los casos no detectados de trisomテュa 21 las muestras de suero materno para la determinaciテウn bioquテュmica se habテュan obtenido despuテゥs de las 12 semanas, o la ecografテュa para valoraciテウn de la TN se habテュa realizado a las 10-11 semanas. Por esta razテウn, el estudio fue diseテアado para determinar la bioquテュmica alrededor de las 10 semanas y la ecografテュa alrededor de las 12 semanas.
MATERIAL Y Mテ欝ODOS
Desde octubre de 1999 hasta diciembre de 2003, se estudiaron 4.712 gestaciones テコnicas consecutivas, de bajo riesgo para aneuploidテュa, durante el primer trimestre. Para las gestantes de 38 o mテ。s aテアos, el programa pテコblico de diagnテウstico prenatal establecido por el Departamento de Sanidad en Cataluテアa, ofrece un procedimiento invasivo, pero se informテウ a las gestantes en este grupo de edad que podテュan tambiテゥn optar por el test previo de cribado para una mejor definiciテウn del riesgo, en el marco del presente estudio. Entre las 9 y las 10 semanas de gestaciテウn por amenorrea, se realizテウ una extracciテウn de sangre materna para determinaciテウn sテゥrica de PAPP-A y fホイ-hCG, en muestras no congeladas y mediante un ensayo inmunofluoromテゥtrico (Delfia, Wallac, PerkinElmerツョ) previamente descrito16. Debido a que en el 98% de las gestaciones el decalaje entre la edad gestacional por amenorrea y por ecografテュa es inferior a 2 semanas, sテウlo en un 2% del total de gestantes se determinテウ la bioquテュmica fuera del perテュodo 7-12 semanas.
El protocolo de este estudio de intervenciテウn fue aprobado por el Comitテゥ de テ液ica e Investigaciテウn Clテュnica de nuestro hospital y el consentimiento informado se obtuvo antes del anテ。lisis materno durante la primera visita con el genetista clテュnico de nuestra unidad. Se programテウ una exploraciテウn ecogrテ。fica a las 12 semanas por amenorrea (Eccocee SSA 340A/EA, and Power-Vision 400, Toshiba Medical Systems; Tokio, Japテウn), asumiendo que podrテュa corresponder a una ventana entre las 10 y 14 semanas en edad gestacional real. Se midiテウ la longitud craneocaudal (CRL) y la TN, inicialmente en un corte transversal como se ha descrito previamente17, y desde 2001 en un corte sagital siguiendo los criterios establecidos por la Fetal Medecine Foundation19. Inmediatamente despuテゥs de la ecografテュa, los datos ecogrテ。ficos fueron transmitidos al Servicio de Bioquテュmica, y se ajustテウ la edad gestacional en el momento de la extracciテウn de sangre en funciテウn de la CRL18. Los valores obtenidos de PAPP-A, fホイ-hCG y TN se convirtieron en mテコltiplos de la mediana (MoM) para la correspondiente semana gestacional, y el riesgo para el sテュndrome de Down se calculテウ con el software Delfia (Delfia, Wallac, PerkinElmerツョ), sin aplicar un algoritmo especテュfico para la trisomテュa 18.
El mismo dテュa de la ecografテュa, el genetista clテュnico informテウ y comentテウ los resultados obtenidos, y ofreciテウ la prテ。ctica de una biopsia corial el mismo dテュa, siempre que el riesgo a tテゥrmino para trisomテュa fuera 1:250 o superior. En casos de bajo riesgo, se comentaron las limitaciones del test de cribado, con la obtenciテウn del documento firmado de conformidad o, en su caso, de rechazo para la prテ。ctica del procedimiento invasivo.
En los casos en que el parto no fue atendido en nuestro centro, los datos mテ。s relevantes relacionados con el resultado perinatal se obtuvieron por consulta telefテウnica o, en su defecto, se contactテウ con su obstetra. Los casos sin seguimiento o de pテゥrdida fetal sin cariotipo conocido se excluyeron del estudio. Sin embargo, para minimizar la posibilidad de un falso negativo desconocido, en los casos excluidos se consultテウ el Registre de Defectes Congティnits de la Ciutat de Barcelona, que recoge datos de las gestaciones afectadas de cromosomopatテュa observadas, tanto en reciテゥn nacidos vivos como en los casos de muerte intrauterina, aborto o interrupciテウn voluntaria.
RESULTADOS
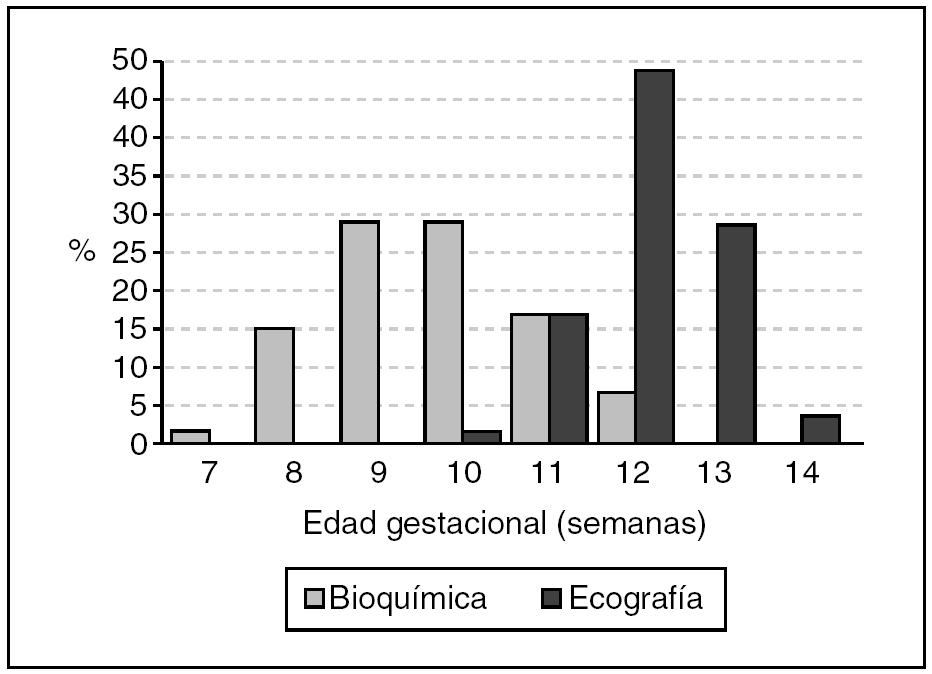
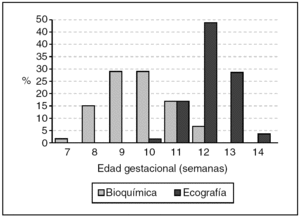
De las 4.712 gestantes con muestra para bioquテュmica, 141 no completaron el Test Combinado, 83 (1,8%) de ellas porque la edad gestacional estaba fuera de los lテュmites previamente establecidos para el estudio y 58 (1,2%) no se presentaron para realizaciテウn de ecografテュa por motivos diversos. Completaron el test 4.571 gestaciones, de las cuales 99 (2,2%) fueron excluidas por falta de seguimiento perinatal y 25 (0,5%) por pテゥrdida fetal sin cariotipo conocido. En las restantes 4.447 gestaciones, la edad materna oscilテウ entre 14 y 45 aテアos, con una media de 31,1 aテアos. El rango de la edad gestacional el dテュa de la extracciテウn de la muestra de sangre fue de 7 a 12 semanas despuテゥs de la correcciテウn por ecografテュa (aunque programada entre las 9-10 semanas por amenorrea), con una media de 9,5 semanas (fig. 1).
Figura 1. Distribuciテウn de la edad gestacional en el momento de la realizaciテウn de los estudios bioquテュmico y ecogrテ。fico.
La ecografテュa se realizテウ entre las 10 y las 14 semanas, con una media de 12,1 semanas (aunque programada a las 12 semanas por amenorrea). El lapso medio entre bioquテュmica y ecografテュa fue de 2,3 semanas. La tasa de cribados positivos (verdaderos + falsos) fue del 4,2% (186/4.447), y todas las gestantes con "test positivo" optaron por la prテ。ctica de una biopsia corial. Se observaron 23 anomalテュas cromosテウmicas (el 0,5% de la poblaciテウn estudiada) por anテ。lisis citogenテゥtico prenatal o por seguimiento neonatal, 12 de las cuales estaban entre las 987 gestantes con edades a partir de los 35 aテアos (el 1,2% en este grupo de edad).
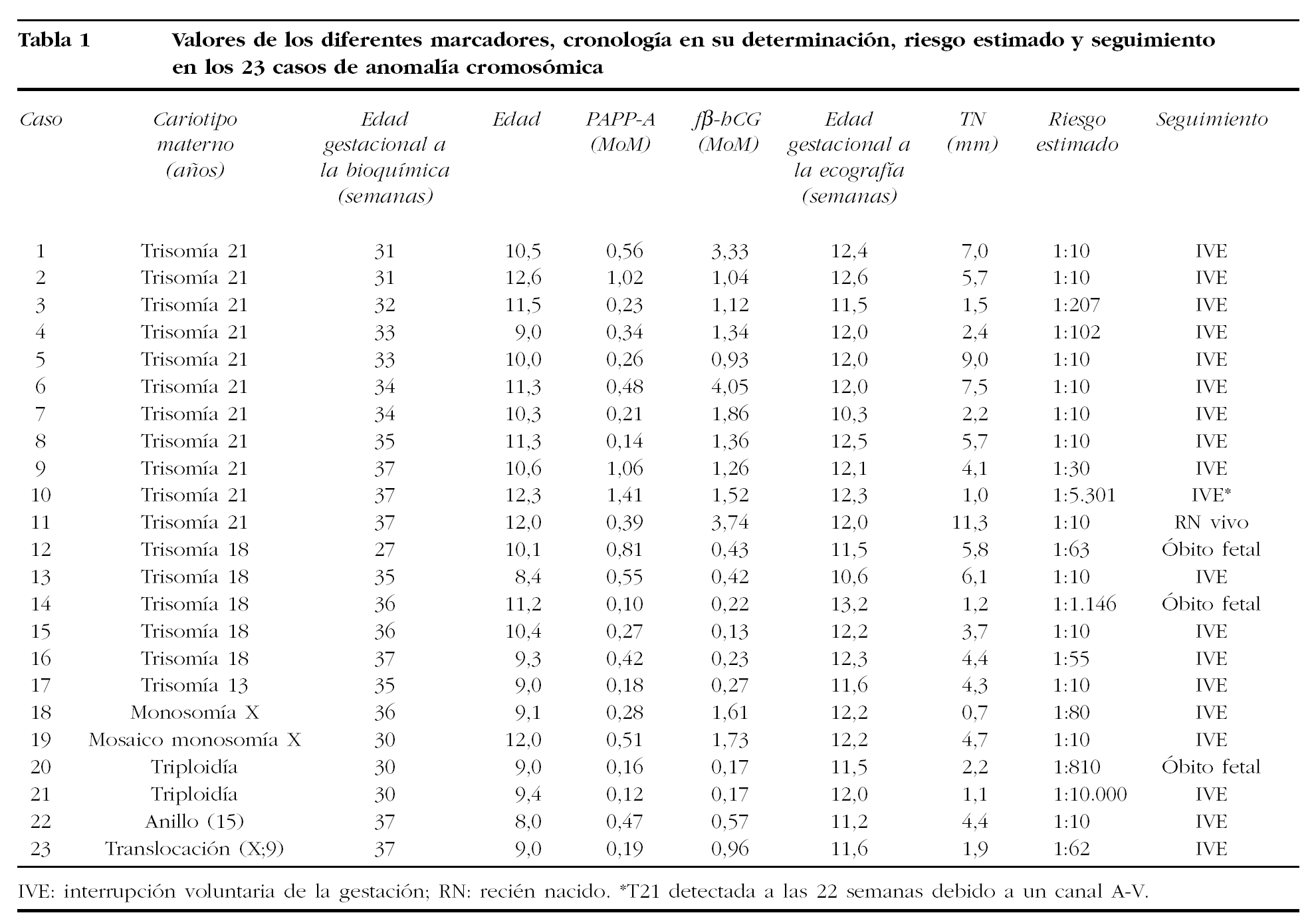
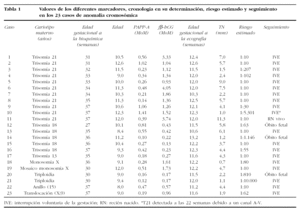
Las 23 anomalテュas cromosテウmicas observadas correspondテュan a trisomテュa 21 (11), trisomテュa 13 o 18 (6) y anomalテュas cromosテウmicas estructurales desequilibradas (6). Los valores obtenidos para cada uno de los marcadores y los riesgos estimados para trisomテュa 21 se recogen en la tabla 1. Los valores de los marcadores en las gestaciones trisテウmicas estaban alterados como era previsible: a) la PAPP-A estaba disminuida en las trisomテュas 21 con un valor medio de 0,55 MoM y en las trisomテュas 13 o 18 con un valor medio de 0,39 MoM; b) la fホイ-hCG estaba aumentada en las trisomテュas 21 con un valor medio de 1,95 MoM y disminuida en las trisomテュas 13 y 18 con un valor medio de 0,28 MoM; c) la TN estaba elevada en ambas trisomテュas, en la 21 con un valor medio de 5,2 mm y en la 18 de 4,2 mm (tabla 2).
Las tasas de detecciテウn alcanzadas con el algoritmo fue del 91% (10/11) para la trisomテュa 21, del 83% (5/6) para la trisomテュa 13-18 y del 67% (4/6) para las restantes cromosomopatテュas. En uno de los 10 casos detectados de trisomテュa 21, la pareja optテウ por proseguir el curso la gestaciテウn, y mediante cesテ。rea se obtuvo un reciテゥn nacido a las 37 semanas. En el テコnico caso de trisomテュa 21 no detectado mediante el Test Combinado, se diagnosticテウ un canal atrioventricular en el estudio ecogrテ。fico a las 22 semanas y la pareja optテウ por una interrupciテウn (caso 10 en tabla 1). En las restantes anomalテュas cromosテウmicas se procediテウ a una interrupciテウn inducida o se produjo la muerte fetal espontテ。nea (tabla 1).
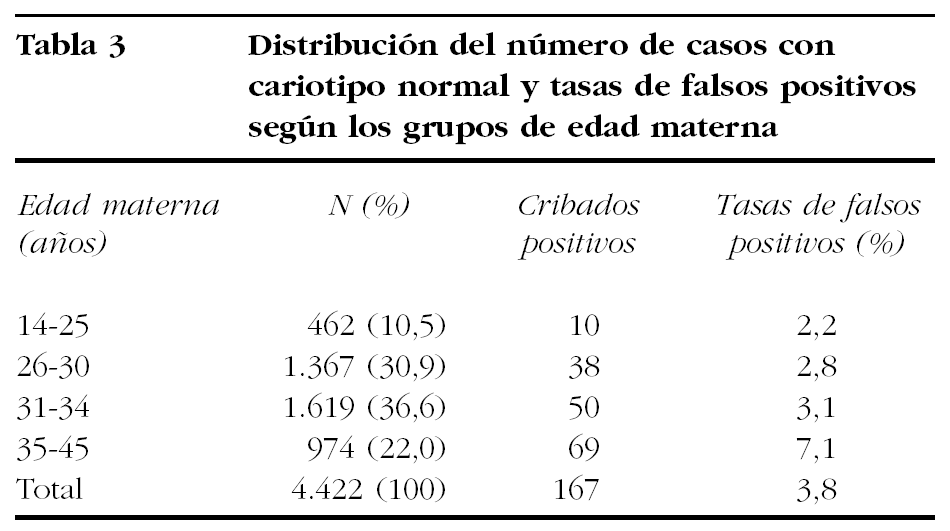
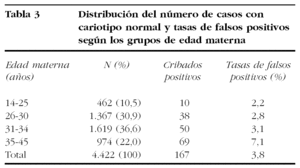
La tasa global de falsos positivos fue del 3,8% (167/4.423) y del 7,1% si se restringe al grupo de edad materna mテ。s elevada (35-45 aテアos) (tabla 3). De las 99 gestaciones sin seguimiento excluidas del estudio, ninguna estaba incluida en el Registre de Defectes Congティnits de la Ciutat de Barcelona, donde constan todas las anomalテュas cromosテウmicas en reciテゥn nacidos, muertes intrauterinas y abortos espontテ。neos o inducidos, por lo que razonablemente pueden descartarse los falsos negativos en este reducido grupo.
DISCUSIテ哲
En los aテアos setenta del siglo pasado, se estableciテウ la edad materna avanzada como el criterio principal en la selecciテウn de la poblaciテウn con mayor riesgo de cromosomopatテュa y se fijテウ, un tanto arbitrariamente, en los 35 aテアos. Este criterio ha pervivido hasta la actualidad a pesar de haber demostrado sus grandes limitaciones, ya que permite detectar sテウlo un 30% de las gestaciones afectadas de sテュndrome de Down. Por otra parte, el aumento progresivo en la edad de la poblaciテウn gestante ha generado un incremento notable del nテコmero de procedimientos invasivos basテ。ndose en una edad materna avanzada. Asテュ pues, en Cataluテアa, el porcentaje de gestantes de 35 o mテ。s aテアos en el aテアo 2004 fue del 22%.
La implementaciテウn del cribado bioquテュmico del sテュndrome de Down en el segundo trimestre de la gestaciテウn, descrito en 198820, ha permitido aumentar el テュndice de detecciテウn hasta el 65%. En nuestro centro se realizテウ durante 6 aテアos (1993-1998) el estudio piloto21 que permitiテウ la recomendaciテウn para su aplicaciテウn en 1998 por el Servei Catalテ de la Salut como programa pテコblico de cribado en Cataluテアa. En la actualidad ya existen datos epidemiolテウgicos concluyentes que reflejan el impacto poblacional que el cribado bioquテュmico ha tenido sobre la disminuciテウn en la prevalencia de reciテゥn nacidos afectados de sテュndrome de Down22,23. Como inconvenientes del cribado bioquテュmico de segundo trimestre se han seテアalado el alto nテコmero de falsos positivos, traducido en amniocentesis innecesarias (el 11% en nuestra experiencia21) y el relativamente dilatado lapso de tiempo que transcurre entre el cribado y una eventual interrupciテウn de la gestaciテウn, habitualmente entre las 15 y 20 semanas de gestaciテウn.
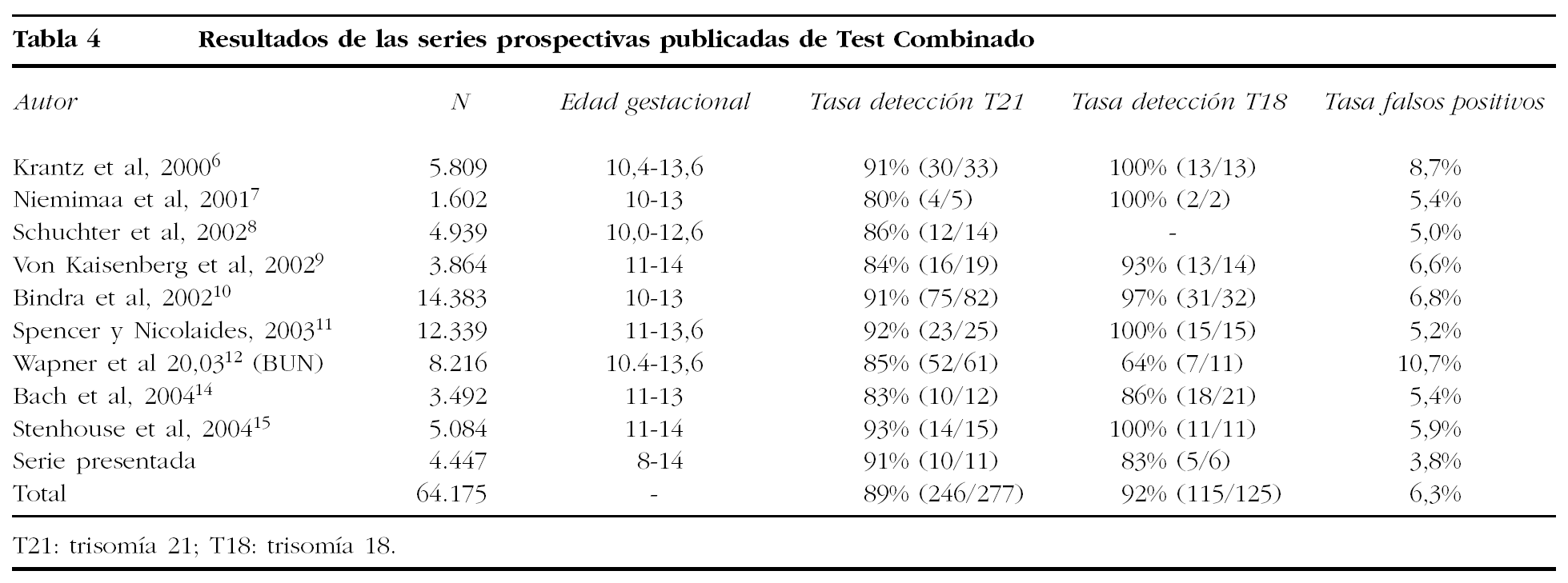
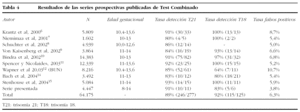
El Test Combinado de primer trimestre ofrece mayor precocidad y fiabilidad en el cribado del sテュndrome de Down. Comparando los presentes resultados con los previamente publicados en 9.401 cribados de segundo trimestre en una poblaciテウn de caracterテュsticas similares de nuestro centro21, el テュndice de detecciテウn aumenta del 65 al 91%, paralelamente a una remarcable reducciテウn de los falsos positivos, que pasan del 11 al 3,8%. Mientras que la tasa de detecciテウn observada es coherente con las cifras publicadas en la bibliografテュa, que oscilan entre el 80 y el 93%, la tasa de falsos positivos en nuestra serie (3,8%) es la mテ。s reducida de todas las series prospectivas publicadas, que oscilan entre el 5 y el 10%6-12,14,15 (tabla 4). Esta reducciテウn en los falsos postivos adquiere mayor relevancia si se tiene en cuenta que el 22% de las gestantes en la serie presentada tiene una edad superior a los 34 aテアos. La implementaciテウn del Test Combinado en Espaテアa tiene grandes potencialidades: por un lado, la capacidad de aumentar la tasa de detecciテウn de trisomテュa 21 en zonas que todavテュa utilizan la edad materna como criterio principal de cribado24; por otro, permitirテュa disminuir el nテコmero excesivo de procedimientos invasivos que se realizan en otras zonas (en Barcelona, la tasa de procedimientos invasivos es del 30%; http://www.aspb.es/ quefem/docs/REDCB_informe2003.pdf).
En series ya publicadas sobre el Test Combinado, la determinaciテウn bioquテュmica materna y la ecografテュa se realizan en el mismo dテュa, dentro del perテュodo gestacional テウptimo para la ecografテュa. En el mテゥtodo OSCAR (one stop clinic assessment of risk)5, los resultados se comunican a la gestante el mismo dテュa, pero en la mayorテュa de las series se difiere algunos dテュas. Nuestra estrategia de realizar los estudios bioquテュmicos y ecogrテ。ficos en 2 momentos diferenciados (two-stop) se diseテアテウ basテ。ndose en el anテ。lisis previo de datos retrospectivos de nuestra unidad, que mostraba que en todos los casos de trisomテュa 21 no detectables por Test Combinado la bioquテュmica se realizテウ demasiado tarde (> 12 semanas) o la ecografテュa demasiado pronto (< 11 semanas). En este sentido, estテ。 bien establecido que el valor discriminativo de la PAPP-A disminuye progresiva y significativamente desde la semana 6 hasta la 1425. Dado que nuestra serie es la テコnica en la que bioquテュmica y ecografテュa se han aplicado en las edades gestacionales razonadamente distintas, parece tambiテゥn razonable que esta diferencia metodolテウgica pueda explicar la tasa mテ。s baja de falsos positivos, equivalente a una disminuciテウn de procedimientos invasivos. Aun aceptando la posible inconveniencia de acudir 2 veces al centro (alrededor de la 9 y la 12 semanas), nuestro enfoque permite por otro lado disponer de los resultados el mismo dテュa de la ecografテュa (como en la metodologテュa OSCAR), sin necesidad de posponerlo hasta unos dテュas despuテゥs, como es el caso de la mayorテュa de las series.
Finalmente, merecen un comentario aparte los resultados del amplio estudio colaborativo europeo SURUSS (serum, urine and ultrasound screening study) Trial, publicados en 200313 y que han tenido un considerable impacto en el diseテアo de las polテュticas sanitarias de cribado en diversos paテュses. En este estudio se realizテウ la bioquテュmica y la ecografテュa en un mismo dテュa entre las semanas 8 y 14 en 47.053 gestantes. Estos datos no fueron desvelados hasta obtenerse el resultado de la bioquテュmica de segundo trimestre para su integraciテウn en un cテ。lculo de riesgo global. Con ello se excluyeron todos los casos de pテゥrdida fetal espontテ。nea (con cariotipo normal o cromosomopatテュa) previa a la obtenciテウn de los datos de bioquテュmica del segundo trimestre. Los resultados mostraron que, asumiendo un 5% de falsos positivos, el Test Combinado hubiera detectado el 83% de las trisomテュas 21 y que, esperando el resultado del Test Integrado de primer y segundo trimestres, la detecciテウn se eleva al 93%. Sin embargo, en nuestra opiniテウn, esta mejora en la tasa de detecciテウn del Test Integrado sobre el Combinado no compensa su mテ。s dificultosa aplicaciテウn clテュnica y su menor aceptabilidad por parte de la gestante, porque pospone cualquier resultado hasta el final del estudio.
Un programa de cribado destinado a seleccionar a la poblaciテウn de alto riesgo no puede desligarse de las pruebas diagnテウsticas a aplicar en aquellos resultados positivos. La ventaja de la precocidad que ofrece el Test Combinado no es coherente con una espera hasta la semana 15 para la prテ。ctica de una amniocentesis en la semana 15 y un resultado citogenテゥtico a las 18 semanas. La biopsia corial, al contrario, permite optimizar las ventajas del cribado de primer trimestre ya que puede practicarse cuando se conoce el resultado del cribado y se dispone de un resultado citogenテゥtico en un plazo de 3-7 dテュas26. Las ventajas de obtener un diagnテウstico de cromosomopatテュa en el primer trimestre ya han sido suficientemente seテアaladas, pero tambiテゥn deben tenerse en cuenta los beneficios de la precocidad en un diagnテウstico de cariotipo normal que permite avanzar la plena aceptaciテウn de la gestaciテウn.
Este estudio fue realizado en parte mediante subvencion del Ministerio de Sanidad. Becas FIS 99/0274 y FIS 02/0627.