Desde el año 1996, con la aprobación por parte de la FDA del primer alimento derivado de un cultivo genéticamente modificado, el tomate SavrFlavr®, con una maduración retrasada, el desarrollo de estos organismos ha crecido vertiginosamente, considerándose hoy en día la tecnología biotecnológica de más rápida adopción y crecimiento por área sembrada a nivel global. El desarrollo de la tecnología del ADN recombinante permitió progresos más eficientes y seguros: en la industria farmacéutica, para antibióticos, vacunas, hormonas, productos de diagnóstico e insulina humana recombinante; en la floricultura, para nuevas variedades; en la reparación de ambientes contaminados, y en la agricultura, para introducir rasgos de resistencia, en particular a herbicidas e insectos. Paralelamente con este proceso, ha surgido una inquietud sobre la seguridad y la inocuidad de los cultivos genéticamente modificados, y los alimentos derivados de estos, lo que ha llevado al desarrollo de sistemas de bioseguridad que buscan establecer las medidas apropiadas para la investigación, el uso, la manipulación, el transporte y la comercialización segura de los organismos genéticamente modificados (OGM). Este artículo describe la evolución de los procesos para el establecimiento de los sistemas de bioseguridad de OGM en el país, el sistema regulatorio vigente y los procedimientos utilizados; además, se detalla el proceso gradual de adopción y utilización de los cultivos genéticamente modificados.
Since 1996, with the approval by the FDA of the first food derived from a genetically modified crop, the tomato SavrFlavr®, which had a delayed maturation, development of genetically modified organisms (GMOs) has grown rapidly, being considered the biotechnology technique with the faster adoption and globally growth. The development of recombinant DNA technology allowed more efficient and safe developments, such as in the pharmaceutical industry for the production of antibiotics, vaccines, hormones, diagnostics, recombinant human insulin; in floriculture, for the development of new varieties; repair of contaminated environments and in agriculture, for introducing traits, in particular for herbicide tolerance and insects resistance. Parallel to these developments,concerns have arisen about the safety and harmlessness of genetically modified crops and foods derived from them, which has led to the development of biosafety systems that seek to establish appropriate measures for research, use, handling, transportation, safe marketing of GMOs. This paper describes the evolution of the development of biosafety systems for GMOs in this country, the current regulatory system, the procedures, and also describes the gradual process of adoption and use of GM crops.
Entre los principales desarrollos científicos y tecnológicos de las últimas décadas, la biotecnología y sus productos ocupan una posición prominente. Estas han impactado en casi todos los sectores de la economía debido al desarrollo de productos en importantes áreas industriales como en salud, con el desarrollo de sistemas para el diagnóstico temprano, vacunas y productos para el tratamiento de enfermedades; en agricultura, con el desarrollo de cultivos y alimentos mejorados; en usos no alimentarios de los cultivos como materiales biodegradables, aceites vegetales y biocombustibles; y en manejo ambiental a través de la biorremediación (reciclaje, tratamiento de residuos y limpieza de zonas contaminadas por actividades industriales)1. La base fundamental de estos avances es la biología molecular y la aplicación de las técnicas del DNA recombinante, que ha permitido la inserción de genes en el genoma de un organismo en sitios específicos y con características que el organismos receptor no presenta2. Su aplicación ha sido objeto de escrutinio público con amplias controversias y debates públicos y políticos, posiblemente por el desconocimiento que hay acerca del tema y por la desinformación que la sociedad en general ha recibido de los medios.
A pesar de su enorme potencial, hay muchas inquietudes públicas en relación con el impacto de los cultivos genéticamente modificados –GM- en la salud humana y animal y el ambiente, una vez estos son sembrados. Debe recordarse que cualquier tipo de agricultura ya sea convencional –de subsistencia, orgánica, intensiva- afecta al ambiente, por ello es de esperar que, en forma similar, el uso de nuevas tecnologías genéticas para los cultivos, lo afecte. Las consideraciones que giran alrededor de la aplicación de la tecnología de genes en los cultivos agrícolas involucran varias categorías que pueden ser agrupadas en forma amplia en aspectos de seguridad alimentaria, seguridad del alimento, seguridad ambiental, así como implicaciones éticas, culturales y de impacto socioeconómico1,3.
Cáncer, VIH-sida, alergias, efectos tóxicos, cambios en los patrones de uso y consumo, impactos a las especies silvestres, efectos nutricionales y hasta homosexualismo, son algunos de las preocupaciones que hay entorno al consumo de alimentos derivados de cultivos modificados genéticamente o comúnmente llamados: “alimentos transgénicos”. La introducción de ADN nuevo permite la síntesis de nuevas sustancias, las cuales pueden ser componentes convencionales de los alimentos como proteínas, carbohidratos o vitaminas, pero también podrían generar nuevos metabolitos que resultarían tóxicos para el ser humano.
Los alimentos derivados de los cultivos genéticamente modificados, son los alimentos obtenidos a partir de un organismo modificado genéticamente (OGM), o que contiene ingredientes que provienen de plantas que han sido modificadas por ingeniería genética. Lo que se modifica genéticamente es la planta, los microorganismos o el animal, NO el alimento. Un alimento puede contener ingredientes que provienen de OGM, (por ejemplo aceite de algodón, harina de maíz, salsa de soya), o pueden ser directamente OGM, por ejemplo, la mazorca o la papaya. Un OGM es cualquier organismo vivo que posea una combinación nueva de material genético, que se haya obtenido mediante la aplicación de la tecnología de ADN Recombinante, sus desarrollos o avances; así como sus partes, derivados o productos que los contengan, con capacidad de reproducirse o de transmitir información genética4.
Los sistemas mayormente empleados para la transferencia de genes son el Agrobacterium y la biolística o biobalística. Sin embargo, son diversos los métodos que hoy en día se emplean entre los que cabe mencionar la fusión de protroplastos, la metodología de whiskers5, el silenciamiento de genes, la electroporación o la microinyección entre otros.
La transformación mediada por Agrobacterium fue el primer sistema de transferencia de genes en producir una planta modificada genéticamente en 1983, cuando reportaron la transferencia de genes bacterianos a plantas y de una especie vegetal a otra6. Agrobacterium tumefaciens, es una bacteria perteneciente al género Agrobacterium, un agente patógeno vegetal que tiene la capacidad natural de transferir genes a las plantas que infecta (huéspedes). Estas bacterias ingresan al vegetal a través de una herida, inyectan su material genético al interior de la célula, y una pequeña porción se integra en el genoma de la célula huésped. El segmento de DNA transferido es conocido como la región T-DNA (DNA de transferencia) y se encuentra en el plásmido residente de la bacteria llamado plásmido Ti (inductor de tumores).
La construcción génica que se inserta tiene una composición molecular básica que permita la correcta expresión del gen insertado en la planta hospedera. Para lo cual se construye un casete de expresión que está constituido por una región promotora (promueve cuánta proteína producir y cuando producirla), una región codificante (codifica la información para la producción de una proteína), y una región terminadora (termina la expresión o producción de la proteína). Los promotores y terminadores son secuencias de genes de plantas, virus o bacterias. El casete de expresión se inserta en una molécula de ADN o vector de transformación. Los vectores más usados en la transformación de bacterias son los plásmidos, moléculas pequeñas, circulares de DNA, que se encuentran naturalmente en bacterias y cuyo tamaño varía entre 5 a 400 Kbp, que se encuentran fuera del cromosoma central bacteriano, navegando en el citoplasma. En la naturaleza, los plásmidos contienen genes que no son esenciales para el normal funcionamiento de la célula bacteriana, y pueden intercambiarse entre bacterias de la misma especie7.
En el caso de la transformación de plantas, es necesario combinar la actividad de por lo menos tres genes. Un gen que permita seleccionar las futuras plantas transgénicas, un gen que sirvan para seleccionar las bacterias recombinantes y otro de interés comercial o investigativo. El casete de inserción contiene entonces dos genes: un marcador de selección para plantas y el gene de interés.
El plásmido bacteriano con el casete de expresión se introduce en Agrobacterium, el cual se pone en contacto (cocultivo) con el tejido vegetal de la planta de interés. Después del cocultivo, los explantes se transfieren a los medios de regeneración que contienen un antibiótico para detener el crecimiento de la bacteria y un agente de selección. El agente de selección se utiliza para asegurarse que solo regeneren plántulas potencialmente transgénicas. Las plántulas que resultan regeneradas en un medio de selección, luego del cocultivo, deben ser caracterizadas molecularmente. Se debe demostrar la presencia del transgen en el genoma de la planta, y que se está transcribiendo y traduciendo correctamente. Posteriormente se realizan los ensayos biológicos en invernadero y en campo, para demostrar que la planta está expresando el fenotipo deseado.
La transformación de plantas por el método de biolísitca o La pistola de genes (fig. 1) fue uno de los métodos desarrollados para transferir genes a genomas vegetales en la década de los 80s del pasado siglo XX, proceso ideado por John Sanford, Theodore Klein, Edward Wolf y Nelson Allen de la Universidad de Cornell en los Estados Unidos8.
La biolística, permite orientar fragmentos de DNA desnudo hacia el interior de cualquier célula. Como es un método físico es aplicable prácticamente a todos los sistemas biológicos. El plásmido con el casete de inserción recubre microproyectiles de oro o tungsteno, que son disparados sobre el tejido vegetal de interés, Posteriormente las células bombardeadas se transfieren a medios de cultivo, donde se van a seleccionar y regenerar plántulas que son potencialmente transgénicas.
El desarrollo de una planta genéticamente modificada desde que se descubre el gen de interés y la característica deseada hasta su aprobación para los diferentes usos (consumo humano, animal, siembra) puede tomar cerca de 13 años y con un costo aproximado en dólares de 136 millones, de los cuales 3.6 millones se destinan al proceso regulatorio y los estudio implicados en el mismo9.
El contexto regulatorio y la evaluación del riesgo de los alimentos derivados de organismos genéticamente modificadosCon el fin de que sean realmente útiles, los productos de la transformación genética deben ser seguros para el usuario y para el ambiente, para lo cual se han desarrollado estrategias que regulan el uso y aplicación de los organismos genéticamente modificados, con el fin de obtener los máximos beneficios sociales de su utilización.
Considerables esfuerzos internacionales, regionales y nacionales buscan desarrollar los mecanismos para por un lado, garantizar el uso adecuado de los desarrollos biotecnológicos y, por otro, facilitar el acceso a sus beneficios para toda la sociedad a través de regulaciones sobre bioseguridad10. Con el fin de establecer el grado de inocuidad de los alimentos derivados de plantas genéticamente modificadas, se ha establecido el concepto de BIOSEGURIDAD, el cual establece el conjunto de medidas y acciones que se deben tomar para evaluar, evitar, prevenir, mitigar, manejar y/o controlar los posibles riesgos y efectos directos o indirectos que puedan afectar la salud humana, el medio ambiente y la biodiversidad, la productividad o producción agropecuaria, como consecuencia de la investigación, introducción, liberación, movimiento transfronterizo y producción de OGM.
Como instrumento a nivel mundial en términos de seguridad de las aplicaciones de la biotecnología moderna, se cuenta con el Protocolo de Cartagena de Seguridad de la Biotecnología, del cual Colombia es signatario, ratificado por la Ley 740 de 2002. El Protocolo de Cartagena de Bioseguridad se deriva de los compromisos del Convenio sobre Diversidad Biológica (CDB) y es un instrumento jurídicamente vinculante para los países signatarios que lo ratifican. Su objetivo principal es garantizar un nivel adecuado de protección para la transferencia, uso y aplicación segura de los organismos modificados genéticamente que puedan tener efectos adversos en la conservación y uso sostenible de la biodiversidad, o sobre la salud humana. Colombia fue uno de los países líderes en la formulación y negociación del Protocolo de Cartagena sobre seguridad de la biotecnología, así como del Protocolo de Nagoya-Kuala Lumpur sobre responsabilidad y compensación suplementario al Protocolo de Cartagena.
El marco regulatorio de la seguridad de la biotecnología en Colombia en relación con los cultivos genéticamente modificados tiene dos componentes básicos. El primero está compuesto por los mandatos constitucionales y los diferentes actos legislativos en relación con el medio ambiente, la biodiversidad, recursos genéticos y temas agropecuarios. Aunque ninguna de éstos trata directamente de cuestiones de seguridad de la biotecnología, constituyen el marco jurídico de los cultivos agrícolas modificados genéticamente en Colombia en los aspectos relacionados con principios, competencias generales, definiciones y conceptos, riesgos, responsabilidades, sanciones y prohibiciones, exportación, importación, comercialización, e introducción de especies, entre otros. El segundo componente hace referencia a la legislación específica en bioseguridad desarrollada, en su mayoría, como cumplimiento al Protocolo de Cartagena y los Acuerdos Internacionales de los cuales Colombia es país Parte1.
Las instancias involucradas en los aspectos de bioseguridad de OGM incluyen los Ministerios de Ambiente y Desarrollo Sostenible; de Agricultura y Desarrollo Rural; y de Salud y Protección Social conjuntamente con sus institutos adscritos: Instituto de Investigación en Recursos Biológicos Alexander von Humboldt IAvH; Instituto Colombiano Agropecuario ICA y el Instituto Nacional de Vigilancia de Medicamentos y Alimentos INVIMA respectivamente, los cuales interactúan también con los Ministerios de Comercio Exterior y el de Relaciones Exteriores (Cancillería).
El país cuenta con normatividad específica para bioseguridad de OGM y sus productos derivados para producción de alimentos para el consumo humano desde 1996 a través reglamentación expedida por el Ministerio de Salud y aplicada por el INVIMA, y para las áreas agrícola y pecuaria desde 1998 donde se designó al Instituto Colombiano Agropecuario, ICA del Ministerio de Agricultura como autoridad competente para los procedimientos relacionados con la introducción, producción, liberación y comercialización de Organismos Genéticamente Modificados (OGM) de uso agrícola y pecuario. El Sistema Nacional de Bioseguridad de OGM en Colombia es sólido y consistente con los avances científicos y jurídicos que se vienen dando.
Tras la ratificación del Protocolo de Cartagena por el país en el año 2002, y su entrada en vigor en Septiembre de 2003, se consideró necesaria la redefinición de la estructura del Sistema Nacional de Bioseguridad y las medidas para la implementación del mismo. En diciembre de 2005, los Ministerios de Agricultura, de Protección Social y de Ambiente, expidieron conjuntamente el Decreto 4525. Este decreto estableció la reglamentación marco para los OGM en relación con: las autoridades competentes, la autorización para desarrollar actividades con OGM, la evaluación y gestión de riesgos, la creación de los Comités Técnicos Nacionales de Bioseguridad (sectoriales), monitoreo y vigilancia, información, educación e investigación.
Las tres Autoridades Nacionales Competentes (ANC) designadas y sus respectivos Comités Técnicos Nacionales (CTN) son:
- •
Ministerio de Agricultura y Desarrollo Rural (MADR) a través del ICA es responsable de evaluar y autorizar los OGM exclusivamente para uso agrícola, pecuario, pesquero, plantaciones forestales comerciales y agroindustriales;
- •
Ministerio de Salud y Protección Social es responsable de evaluar y autorizar los OGM cuyo destino es el uso en alimentación humana o salud;
- •
Ministerio de Ambiente, Vivienda y Desarrollo Rural MAVDT (hoy Ministerio de Ambiente y Desarrollo Sostenible) es responsable de evaluar y autorizar los OGM de uso exclusivamente ambiental.
Los efectos en la salud humana de los alimentos derivados de plantas genéticamente modificadas, dependen del contenido específico del alimento y tienen el mismo potencial de tener riesgos o presentar beneficios como los alimentos convencionales. La evaluación de la inocuidad de los OGM se realiza caso a caso y paso a paso, lo que significa que cada evaluación es individual y específica para los criterios a evaluar y el uso específico teniendo en cuenta cada una de las etapas de su desarrollo y utilizando los siguientes criterios11:
- •
Concepto de equivalencia sustancial.
- •
Uso de un enfoque multidisciplinario, que incluye la evaluación de las características de la proteína nueva introducida, aspectos toxicológicos y alergénicos y análisis de la composición nutricional.
- •
Consultas con expertos nacionales e internacionales, así como las autoridades regulatorias de otros países.
- •
Fundamento científico.
- •
No existe riesgo cero.
Cuando se evalúa un alimento derivado de una planta genéticamente modificada, siempre se busca establecer que los riesgos no sean diferentes a los que tiene el mismo alimento convencional. Entonces, se analiza que no haya nuevos tóxicos o alérgenos, que las composición de nutrientes sea la misma o esté dentro de los rangos establecidos para el alimentos convencional y que como resultado de la instrucción de nuevos genes no se presenten cambios no deseados, de manera que el alimento derivado del OGM SEA TAN SEGURO COMO el alimento que conocemos y consumimos comúnmente.
Las plantas transgénicas podrían tener proteínas nuevas que sean alérgicas y por lo tanto una persona sensible presentar una reacción alérgica. Si bien los alimentos desarrollados en forma tradicional no se evalúan generalmente en cuanto a alergenicidad, los protocolos para pruebas de alimentos OGM han sido evaluados por la Organización de las Naciones Unidas para la Alimentación y la Agricultura (FAO) y la Organización Mundial de la Salud (OMS). Hasta la fecha no se han hallado efectos alergénicos en relación con los alimentos derivados de OGM que se encuentran actualmente en el mercado.
El concepto de equivalencia sustancial es parte esencial del marco de evaluación del riesgo de los alimentos derivados de OGM, basado en la idea de que existen alimentos que sirven como base para comparar las propiedades del OGM con una contraparte apropiada basada en su historial de uso seguro12 y reconociendo que los alimentos per se pueden contener muchos anti-nutrientes y tóxicos, los cuales a ciertos niveles de concentración pueden causar daños a la salud humana.
Los estudios para determinar la inocuidad de los alimentos derivados de los cultivos GM, incluye análisis de toxicidad aguda y subcrónica (cuando aplica) de acuerdo con la naturaleza y función de la nueva proteína expresada; potencial ocurrencia de efectos intencionados; evaluaciones para establecer la posible alergenicidad de la nueva proteína; estudios de composición nutricional en los que se analizan componentes esenciales, metabolitos y la elaboración de los alimentos13. Todos estos presentados y evaluados por las autoridades nacionales competentes.
Con base en que el país cuenta con un Sistema Nacional de Bioseguridad de los OGM, y que se adelantan las evaluaciones del riesgo requeridas para determinar la seguridad e inocuidad de los alimentos derivados de éstos, se desarrolló la reglamentación en materia de etiquetado de estos alimentos, Resolución 4254 de 2011 expedida por el Ministerio de la Protección Social (hoy de Salud y Protección Social).
En Colombia se etiquetan las diferencias que se generan por la modificación genética y que han sido determinadas en la evaluación del riesgo, que no representan un riesgo para la salud humana y por las cuales se ha determinado que no son sustancialmente equivalentes a su contraparte convencional con historia de uso seguro. Con base en lo anterior se han establecido cuatro (4) condiciones bajo las cuales un alimento se debe rotular o etiquetar todos los envases o empaques de alimentos derivados de OGM para consumo humano: “1. Los valores de la composición nutricional existentes en el alimento que contiene el OGM o que empleó materias primas que son OGM, no son sustancialmente equivalentes en comparación con el homólogo convencional o el producto alimenticio que se encuentra en el mercado. 2. La forma de almacenamiento, preparación o cocción del alimento que contiene el OGM o la utilización de materias primas que son OGM, difiere a causa de éste, en comparación con el homólogo convencional o el producto alimenticio equivalente existente en el mercado. 3. La presencia de un alérgeno introducido como resultado de la modificación genética en un alimento que contiene el OGM o que empleó materias primas que son OGM y que los consumidores no esperan que se presente. 4. La presencia de una diferencia en las propiedades organolépticas de un alimento, como consecuencia de la modificación genética, en comparación a su homólogo convencional.”14.
Adicionalmente, hay etiquetado voluntario para aquellos comercializadores de alimentos que deseen declarar en sus empaques o envases que un alimento “No contiene OGM”, o que es “libre de OGM”; podrá hacerlo siempre y cuando este en la capacidad de demostrar que dicha información es veraz a través de análisis de laboratorio o de sistemas de trazabilidad.
Organismos genéticamente modificados para cultivo y alimentación humana en Colombia y el mundoEl último informe de la ISAAA (International Service for the Acquisition of Agri-Biotech Applications) de 201415, indica que para diciembre de ese año se sembraron a nivel mundial 181,5 millones de hectáreas de cultivos biotecnológicos por 18 millones de agricultores en 28 países entre los que se encuentra Colombia, siendo considera la tecnología agrícola de más rápida adopción en los últimos 19 años.
De los 28 países, 20 son países en vías de desarrollo y 8 países industrializados, siendo Estado Unidos el primer productor, seguido por Brasil, Argentina, India y Canadá. Contrario a lo que se piensa cinco (5) países de la Unión Europea siembran cultivos GM (España, Portugal, República Checa, Eslovaquia y Rumania), y casi la totalidad de la EU importa alimentos derivados de los mismos.
Los cultivos que hoy en día se siembran son soya, maíz, algodón, canola, remolacha azucarera y papaya en Hawai. En el año 2014, se iniciaron las primeras siembras comerciales de Berenjena en la India, resultado de una iniciativa pública-privada. Es de resaltar que no son sólo las grandes multinacionales de semillas las que están desarrollando este tipo de cultivos, centros de investigación, Universidades públicas y privadas, alrededor del mundo están trabajando en investigaciones tendientes a desarrollar cultivos transgénicos en variedades propias de una región y para necesidades específicas. Las modificaciones genéticas que se encuentran comercialmente, corresponden a la introducción de genes que dan características de resistencia a insectos, tolerancia a herbicidas o las dos. Solo hasta el año pasado se hicieron las primeras siembras comerciales de maíces tolerantes a sequía, y aunque ya han sido aprobados por las autoridades de diferentes países, entre ellos Colombia, cultivos GM con mejoras nutricionales (mayor contenido de ácidos grasos Omega 3, Menor contenido de grasas, mayor contenido de vitaminas) aún no hay ninguna variedad que se esté sembrando y comercializando.
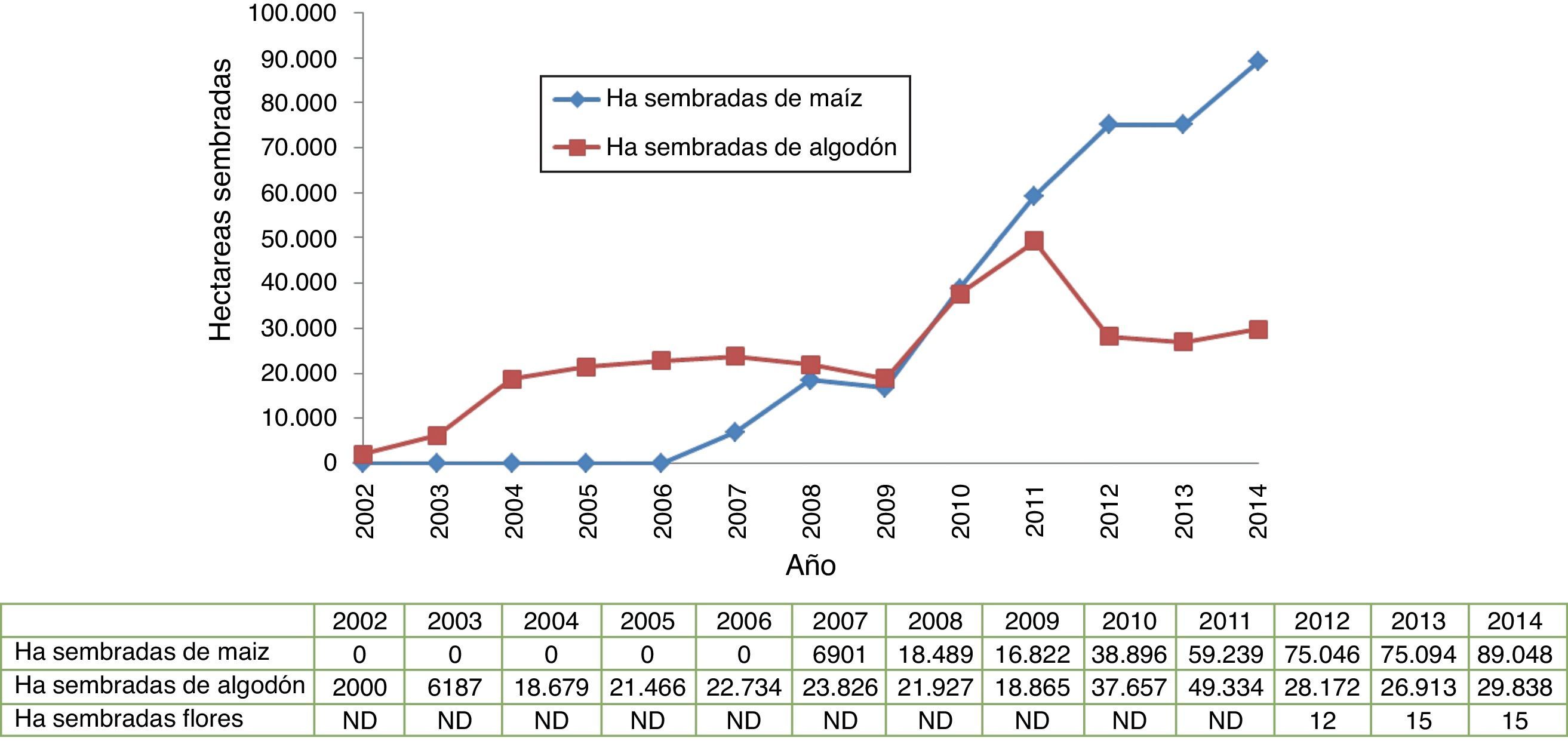
En Colombia a diciembre de 2014 se sembraron un total de 118.991 hectáreas de cultivos GM en 20 departamentos (fig. 2). En maíz GM se sembraron 80.048 hectáreas en siembras controladas, en algodón GM, 29.838ha y en cuanto a claveles y rosas, se sembraron 15ha, en medio confinado (invernadero de bioseguridad). Respecto a la soya, si bien la soya con tolerancia a herbicidas tiene autorización para siembra comercial desde 2010, no se encuentra en cultivo actualmente, y se encuentra autorizada tanto para el consumo humano como para el consumo animal.
Para el consumo humano, se encuentran autorizados en Colombia Maíz, Algodón, Soya, Remolacha Azucarera, Arroz y Trigo, no necesariamente su aprobación para el consumo humano o animal conlleva la aprobación para la siembra o viceversa. Muchos de estos cultivos están aprobados para el consumo humano, teniendo en cuenta las dinámicas comerciales de granos en el mundo y no necesariamente porque haya un interés de siembra en el territorio nacional.
ConclusionesEl debate en relación con los cultivos genéticamente modificados y los alimentos que de estos se derivan, se ha convertido en un frente de discusión de posiciones extremas en donde en ocasiones se desconoce la experiencia de casi 20 años de uso y consumo ininterrumpido, y de la aplicación de procesos regulatorios y de evaluación de riesgo resultado del consenso entre los países y del soporte científico para el desarrollo de los mismos, citando entre otros las guías de evaluación de riesgo de la OECD (Organización para la Cooperación y el Desarrollo Económico), los instrumentos de Bioseguridad de la FAO, los estándares del Codex Alimentarius (FAO/OMS), la guías y regulaciones nacionales (FDA, EFSA, FSANZ, SENASA, entre otros), consideradas para la toma de decisiones en relación con el uso de OGM para su siembra, consumo humano o consumo animal.
La FAO, la OMS, Asociaciones Científicas internacionales (Sociedad de Toxicología de los Estados Unidos, Asociación Médica de Gran Bretaña, Colegio Americano de Nutrición), Academias de Ciencias (Pontifica Academia de la Ciencias, Academia de Ciencias de China, Brasil, India, México, EE.UU), Agencias Sanitarias homologas (FDA en Estados Unidos, EFSA en Europa, SENASA en Argentina), la Academia Pontifica de la Ciencias, entre otras manifiestan que la evidencia disponible a la fecha, además de un consumo prolongado por más de 15 años, desde que se aprobó el primer OGM, indican que no hay indicios de que los organismos genéticamente modificados sean perjudiciales para la salud como resultado de su consumo. Sin embargo la evaluación previa a la puesta en el mercado debe seguir los principios científicos de evaluación del riesgo que busquen un nivel de certeza adecuado sobre la inocuidad de estos, como lo debe ser con cualquier producto que se destine al ser humano, independientemente del método que se haya empleado para su obtención.
Recientemente (2014), científicos italianos llevaron a cabo y publicaron en la revista científica “Critical Reviews in Biotechnology” una revisión y análisis de la literatura científica sobre la inocuidad de los cultivos transgénicos desarrollada durante los últimos 10 años, generando un listado de más de 1.780 publicaciones científicas que muestran la seguridad de los mismos para el consumo humano.
La estructura con la que actualmente cuenta el país, no solo para dar cumplimiento con el Protocolo de Cartagena, sino también para responder a los acuerdos internacionales que ha suscrito, es sólida y consistente con los avances de la tecnología, es tomada como punto de referencia por países de la región, sigue los lineamientos internacionales que en la materia se han generado, y se encuentra en permanente revisión y actualización de manera tal que las autoridades competentes puedan responder a la sociedad1.
Conflicto de interesesLos autores declaran no tener conflicto de intereses.