El Ministerio de Sanidad y Consumo, mediante la Orden SCO/3.215/2002, de 4 de diciembre, aprueba la incorporación de nuevos conjuntos homogéneos de presentaciones de especialidades farmacéuticas a los ya existentes y, a su vez, aprueba los precios de referencia aplicables a estos conjuntos homogéneos.
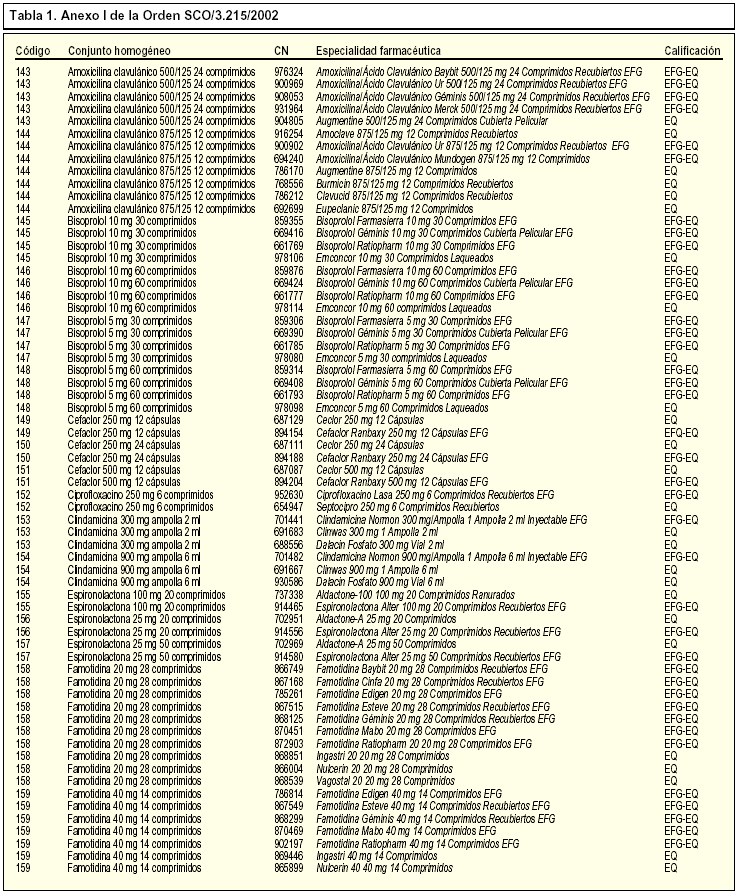
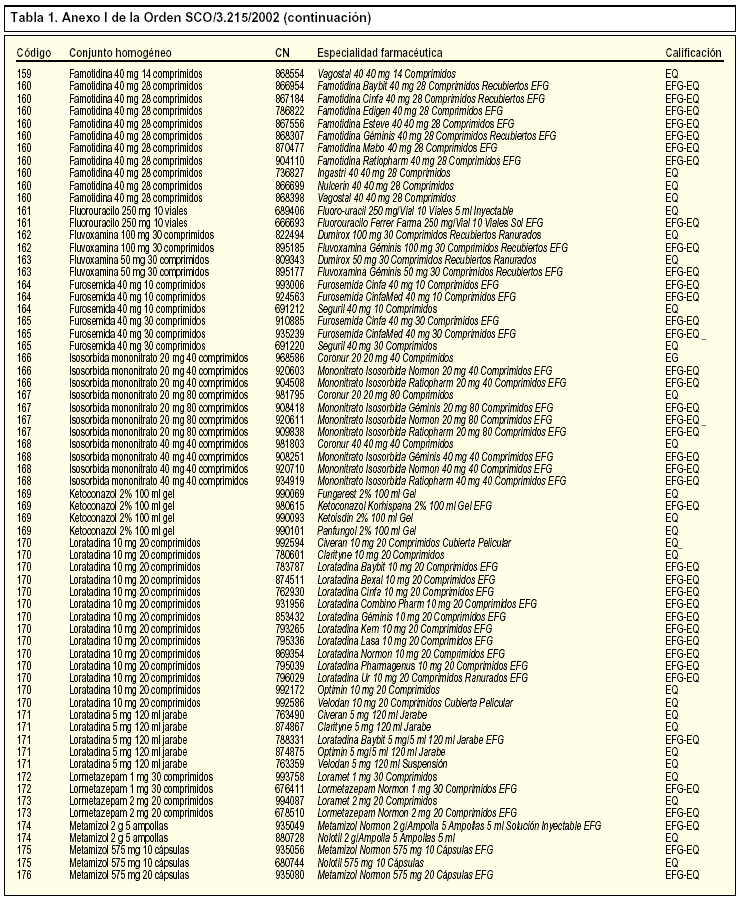
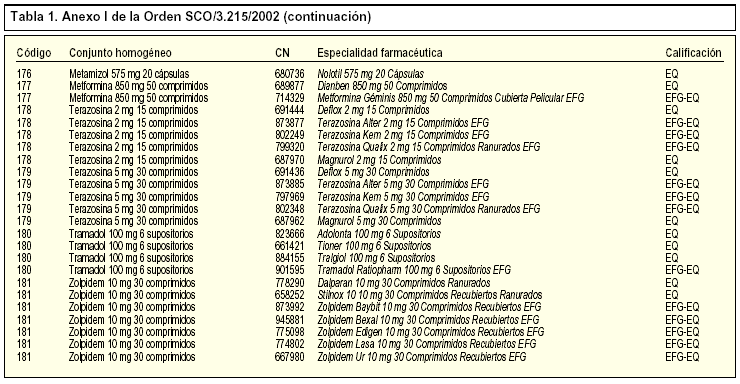
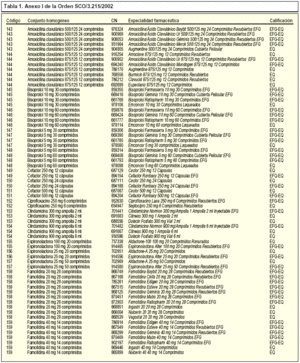
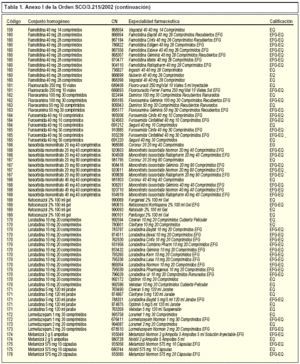
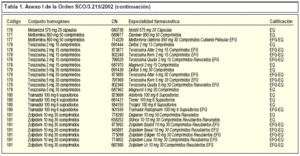
La Orden SCO/3.215/20021 incorpora, en concreto, 39 nuevos conjuntos homogéneos a los 142 existentes, por lo que en la actualidad contamos con un total de 181 conjuntos homogéneos. En la tabla 1 se incluye la relación de los nuevos conjuntos homogéneos con sus respectivos códigos y las especialidades farmacéuticas incluidas en cada uno de ellos.
A los conjuntos homogéneos de nueva creación se les asigna su correspondiente precio de referencia representados en la tabla 2.
Las presentaciones de las especialidades farmacéuticas que tienen la calificación de bioequivalentes y que están incluidas en un conjunto homogéneo deben llevar las siglas EQ en el cupón-precinto con tal de garantizar su correcta identificación y permitir su posible sustitución. Recordemos que las siglas EQ deben aparecer en el cupón-precinto situadas inmediatamente a continuación del nombre, forma farmacéutica, presentación y de las siglas EFG (si las llevara por tener esta condición). Las siglas EQ se encontrarán separadas por un guión y tanto el guión como las siglas se resaltarán en negrita.
Los laboratorios afectados por la inclusión de sus especialidades en los nuevos conjuntos homogéneos han de ajustarse a lo reglamentado; por ello, se les concede un plazo de 3 meses desde la fecha de entrada en vigor de esta Orden (finaliza el 19 de marzo de 2003) para la incorporación de las siglas EQ en el cupón precinto, mediante reetiquetado de las actuales con etiquetas adhesivas o bien utilizando nuevos cartonajes. A partir de la fecha establecida, los laboratorios sólo podrán suministrar a los almacenes de distribución y a las oficinas de farmacia las especialidades farmacéuticas con las siglas EQ en el cupón precinto.
A su vez, los titulares de presentaciones de especialidades farmacéuticas incluidas en un conjunto homogéneo deben actualizar el contenido de la ficha técnica y/o prospecto, con tal de asegurar la homogeneidad de información del conjunto.
Para las oficinas de farmacia se fija el 1 de mayo de 2003 como fecha a partir de la cual han de tener a disposición de los usuarios la relación actualizada de conjuntos homogéneos incluyendo los precios de referencia aplicables a cada uno de ellos. En esa misma fecha, comienza la obligación por parte del farmacéutico de sustituir la especialidad farmacéutica bioequivalente prescrita cuando supere la cuantía establecida como precio de referencia y deba financiarse con cargo a los fondos de la Seguridad Social o a fondos estatales afectos a la sanidad por una especialidad farmacéutica genérica del mismo conjunto homogéneo cuyo precio no supere el de referencia, salvo los supuestos previstos en los artículos 5.2 y 6.3 del RD 1.035/1999, de 18 de junio2.
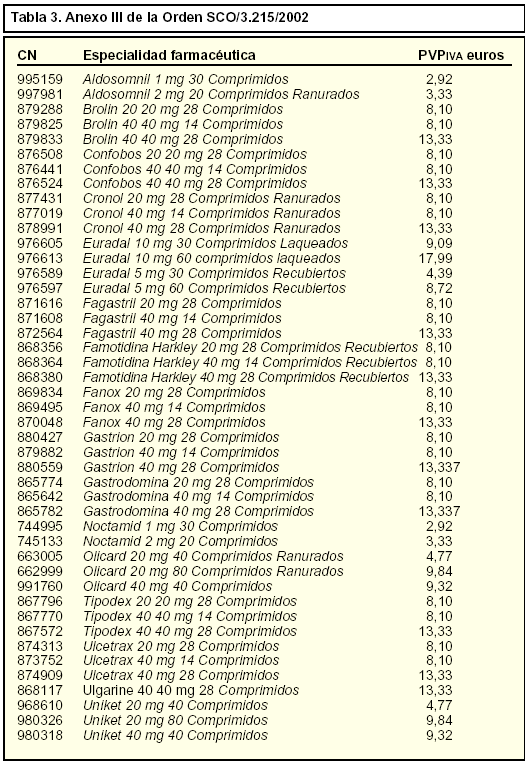
También cabe señalar que en aplicación del Real Decreto-Ley 12/1999, de 31 de julio3, cuando el precio de las presentaciones de especialidades farmacéuticas no bioequivalentes utilizadas para el cálculo del precio de referencia supere éste, se reducirá aquél hasta la cuantía fijada para el de referencia. La Orden de 4 de diciembre de 2002 incluye la relación de las presentaciones de especialidades farmacéuticas no calificadas como bioequivalentes cuyo precio supera al de referencia (de nueva creación) para que se suministren por los laboratorios al precio industrial que se corresponda con el de referencia. Las especialidades afectadas por esta medida no modifican su código nacional y se incluyen en la tabla 3.
A su vez, existe la posibilidad de que los laboratorios decidan voluntariamente comercializar las presentaciones de especialidades farmacéuticas a un precio inferior al autorizado para adecuarlo a un nivel igual o inferior al de referencia, sin modificar el código nacional; para ello deben comunicarlo al Ministerio de Sanidad y Consumo en el plazo de 30 días contados a partir del 19 de diciembre de 2002, fecha de la entrada en vigor de esta Orden.
A los laboratorios afectados por estas medidas se les concede un plazo de 3 meses desde la fecha de entrada en vigor de la presente Orden (finaliza el 19 de marzo de 2003) para suministrar las especialidades farmacéuticas con el nuevo precio y para efectuar la correspondiente modificación del cartonaje, mediante la utilización de etiquetas adhesivas o la fabricación de unos nuevos, pero recordemos que no supone modificación alguna del código nacional de la especialidad.
En las oficinas de farmacia, durante el tiempo en que coincidan especialidades farmacéuticas de precio antiguo con especialidades farmacéuticas de precio renovado correspondientes a las presentaciones de especialidades farmacéuticas no calificadas como bioequivalentes o las que de forma voluntaria decidieron reducir su precio; el cliente satisfará el importe de las mismas de acuerdo con el que figure en el envase exterior, pero si la dispensación se realiza con cargo al Sistema Nacional de Salud, MUFACE, ISFAS o MUGEJU, a partir del 1 de mayo de 2003, las cantidades que deba satisfacer el beneficiario se calcularán con base en los nuevos precios de facturación.
A su vez, el Sistema Nacional de Salud, MUFACE, ISFAS y MUGEJU, mantendrán a efectos de facturación hasta el 30 de abril de 2003, el precio anterior de las presentaciones de estas especialidades farmacéuticas. A partir del 1 de mayo de 2003, las facturaciones de todas las especialidades farmacéuticas afectadas por esta Orden se liquidarán con los nuevos precios.
Bibliografía y notas
1. Orden SCO/3.215/2002, de 4 de diciembre, por la que se determinan nuevos conjuntos homogéneos de presentaciones de especialidades farmacéuticas y se aprueban los correspondientes precios de referencia (BOE de 18 de diciembre de 2002).
2. RD 1.035/1999, de 18 de junio, por el que se regula el sistema de precios de referencia en la financiación de medicamentos con cargo a fondos de la Seguridad Social o a fondos estatales afectos a la sanidad (BOE de 29 de junio de 1999).
3. Real Decreto-Ley 12/1999, de 31 de julio, de medidas urgentes para la contención del gasto farmacéutico en el Sistema Nacional de Salud (BOE de 16 de agosto de 1999).