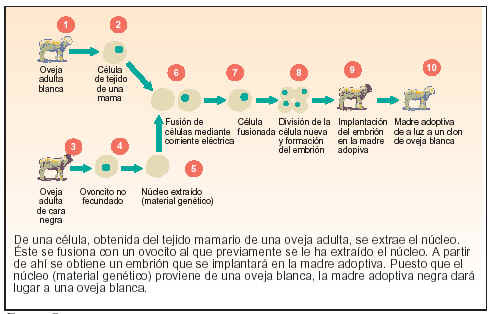
Desde que, en julio de 1996, los científicos del Instituto Roslin comunicaron el nacimiento de la oveja Dolly, la posibilidad de clonar seres vivos es un tema candente en nuestra sociedad. Los éxitos parciales en la clonación de embriones humanos han suscitado muchos debates éticos. Pero, ¿y la clonación de otros mamíferos? ¿Es simplemente un capricho? Está claro que no. Constituye el punto de partida de una nueva era: la del uso de las técnicas de la clonación para usos biomédicos.
Producir organismos genéticamente idénticos a otros no es algo nuevo en la naturaleza. Muchos seres vivos utilizan esta forma de reproducción asexual para perpetuarse.
El término «clon» procede del griego y significa «rama». Desde hace millones de años las plantas pueden reproducirse por clonación mediante esquejes. Basta cortar un tallo o una rama y plantarlo. Cuando el esqueje enraíza, se obtiene un individuo nuevo genéticamente idéntico a la planta original.
Las bacterias también se pueden reproducir de forma asexual, ya que una única bacteria puede dar lugar a miles de millones de descendientes idénticos, como si se tratara de una clonación a escala industrial. Sin embargo, también las bacterias, al igual que las plantas, pueden reproducirse de forma «sexual». Intercambian material genético entre ellas mediante la conjugación. Este proceso es imprescindible para aportar la diversidad genética necesaria para su supervivencia.
También son clónicos los gemelos univitelinos u homocigotos. Son genéticamente idénticos puesto que proceden de la división de los primeros estadios del embrión.
Sin embargo, de los 2 millones, aproximadamente, de especies descritas hasta ahora, sólo alrededor de 2.000 se reproducen habitualmente de forma asexual. A la vista de estas cifras, la pregunta es ¿por qué la mayoría de animales ha elegido la reproducción sexual para perpetuar su especie? La respuesta es muy simple: porque la principal ventaja de la reproducción sexual es aportar diversidad genética a la descendencia y conferir ventajas adaptativas y evolutivas.
Conociendo las ventajas de la reproducción sexual respecto a la asexual, resulta difícil entender por qué existen algunas especies que se reproducen de forma asexual, mediante «clonación natural». La verdad es que las especies facultativas (con capacidad de reproducción sexual y asexual) saben aprovechar muy bien ambos tipos de reproducción dependiendo de las condiciones ambientales de cada momento.
Esto es lo que están haciendo los científicos. Aunque saben que la mejor opción para la perpetuación de una especie es la reproducción sexual, la técnica de la clonación animal puede ofrecer ventajas en aspectos muy concretos que vamos a comentar más adelante.
Técnicas de clonación animal
A finales de la década de los setenta y principios de los ochenta, los científicos ya consiguieron obtener ovejas, vacas, caballos y otros animales genéticamente iguales. Desarrollaron experimentalmente lo que ocurre de forma natural cuando se originan los gemelos univitelinos.
Esta técnica consiste en dividir un embrión y los productos de esta división se introducen en el útero donde se desarrollan los gemelos. Así se pueden obtener dos, cuatro y hasta ocho individuos clónicos (gemelos), pero de este modo, el número de clónicos se limita al número de células que se puede dividir el embrión. La alternativa es la clonación por transferencia nuclear, puesto que permite producir un número ilimitado de clones. Esta técnica consiste en fusionar una célula donante con un ovocito anucleado al que se le ha extraído el núcleo previamente.
Fig. 1. Clonación por transferencia nuclear.
Se realizó con éxito por primera vez en 1952 con anfibios. Desde entonces, se ha utilizado de forma habitual para estudiar el desarrollo embrionario de éstos. Así, se demostró la totipotencia (células capaces de originar cualquier linaje celular adulto) de las células resultantes de la primera división del ovocito.
Sin embargo, la transferencia nuclear en mamíferos es mucho más compleja. La investigación en el campo de la transferencia nuclear en especies estabuladas y, en particular, en el ganado vacuno ha sido alentada por los beneficios económicos que se derivan de la multiplicación --ilimitada-- de embriones con un «interés especial», como por ejemplo, obtener de forma ilimitada animales transgénicos.
A mediados de los años ochenta varios grupos de investigación habían conseguido clonar ovejas y otras especies de ganado vacuno transfiriendo directamente núcleos de embriones muy tempranos. Sin embargo, para lograr una «substitución dirigida de genes» (para obtener animales modificados genéticamente) en especies estabuladas se debía de producir animales vivos a partir de células procedentes de cultivos in vitro (en el laboratorio).
No fue hasta 1996 cuando lo consiguieron. En el Instituto Roslin lograron el nacimiento de dos ovejas --Megan y Morgan-- engendradas mediante transferencia nuclear de células de embriones tempranos cultivadas in vitro durante varios meses.
Éste fue el inicio de las investigaciones con distintos tipos celulares derivados de embriones con estadios más tardíos. Y en febrero de 1997 se publicó en la prestigiosa revista Nature el nacimiento de un cordero clonado por transferencia nuclear a partir de una célula mamaria adulta, la oveja Dolly. Se confirmó su origen por medio del análisis de marcadores de ADN.
Paradigma de la reprogramación nuclear
El nacimiento de Dolly cuestiona uno de los principios fundamentales de la biología evolutiva, puesto que la mayoría de los científicos creían que la diferenciación celular era irreversible; es decir, se creía que una vez las células embrionarias totipotentes inician la diferenciación a un linaje celular específico, el proceso ya no es reversible. El nacimiento de una oveja a partir de una célula adulta puso en entredicho esta teoría. A partir de este experimento muchos investigadores han demostrado que existen distintos linajes celulares, como las células epiteliales o las células neuronales capaces de ser reprogramadas y originar otro tipo celular distinto.
El caso de la oveja Dolly ha abierto nuevas líneas de investigación, quizá más interesantes que la propia clonación, como conocer cómo afectan las mutaciones somáticas en el proceso de envejecimiento e incluso el desarrollo de los tumores.
Entender los procesos de «reprogramación» podrá aportar nuevos datos sobre el control de la expresión génica en células diferenciadas y abrir nuevas perspectivas en la terapia celular.
Clonar animales transgénicos
El instituto Roslin es también líder en el desarrollo de la tecnología de animales transgénicos. A mediados de los años ochenta, el Dr. Clark y sus colaboradores demostraron que era posible dirigir la expresión de un gen humano en la glándula mamaria de otro mamífero.
Este éxito y la síntesis de una oveja transgénica, Tracy, que secretaba 35 g de una proteína humana, la alfa-1-antitripsina (AAT) en cada litro de leche, proporcionó la creación de PPL Therapeutics.
PPL se dedica hoy a la producción de proteínas recombinantes humanas, entre ellas la AAT sintetizada a gran escala por animales transgénicos. Esta molécula se está probando en ensayos clínicos para el tratamiento de la fibrosis quística.
En un principio, la única manera de conseguir animales de granja modificados genéticamente era mediante el método de la inyección pronuclear. Consiste en inyectar directamente en óvulos recién fecundados de 200 a 300 copias del gen que se desea transferir. Posteriormente, las células microinyectadas se implantan en madres adoptivas. Pero sólo el 2-3% de los animales que nacen son transgénicos de línea germinal (es decir, transmiten el gen incorporado a la siguiente generación) y además, sólo una pequeña proporción de éstos, muestran valores suficientemente altos de expresión del gen transmitido para ser comercialmente interesantes.
La inyección pronuclear es simplemente una metodología para incorporar genes. En cambio, la manipulación genética de células en cultivo permite realizar modificaciones mucho más complejas, como la substitución o deleción de genes concretos.
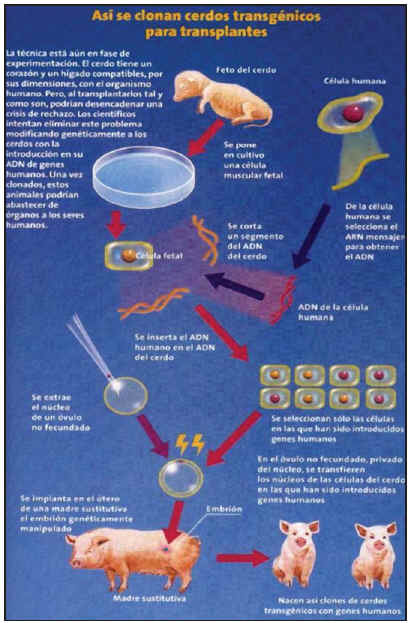
Fig. 2. Xenotransplantes.
La metodología de «substitución dirigida de genes», conocida como gene targeting, se utiliza de forma rutinaria en células madre embrionarias de ratón. Pero el Instituto Roslin ha sido pionero en la transferencia nuclear con objeto de diseñar una ruta alternativa al gene targeting en ganado.
Finalidades biomédicas
La industria biotecnológica parece que, de momento, es la más beneficiada del conocimiento de las técnicas de transferencia nuclear, puesto que proporciona métodos más fiables para conseguir animales transgénicos y reducir el número de animales necesarios para establecer una línea transgénica.
Los científicos del Instituto Roslin, usando células embrionarias clónicas en cultivo, lograron incorporarles el gen del factor IX humano, proteínas de la coagulación sanguínea usadas para el tratamiento de la hemofilia B. Así, nacieron, en 1997, las primeras ovejas clónicas transgénicas, como Polly.
Estas ovejas son capaces de segregar esta proteína humana como si fuera un componente normal de su leche. Ello demostró que mediante la clonación se pueden introducir genes específicos de otros mamíferos y, también, la posibilidad de obtener verdaderos rebaños portadores y capaces de expresar los genes exógenos.
A partir de ahí empezó una carrera, llena de obstáculos, para conseguir otros animales de ganado vacuno y porcino mediante la técnica del gene targeting y la transferencia nuclear, puesto que los beneficios pueden ser enormes, tal como veremos a continuación.
Una de las posibilidades que ofrece la técnica de la clonación por transferencia nuclear son los xenotrasplantes. Las reacciones inmunitarias hiperagudas imposibilitan, por ahora, los trasplantes de órganos de origen animal. Mediante las técnicas de manipulación genética se pretende eliminar la reacción autoinmunitaria. A partir de ahí, se podrían obtener animales clónicos, como el cerdo, con órganos trasplantables a pacientes humanos.
Otra de las posibilidades de la clonación es la obtención de modelos animales con enfermedades humanas. En ocasiones la inserción de mutaciones específicas en ratones ha resultado ser de gran utilidad para la creación de modelos de enfermedades genéticas humanas como la fibrosis quística o la obesidad. La transferencia nuclear permite aumentar el abanico de modelos animales para experimentar terapias para los hombres.
Otra posibilidad es la terapia celular. Actualmente, se utilizan células de dadores para tratar enfermedades como la leucemia o la enfermedad de Parkinson, pero además, normalmente, para evitar el rechazo deben ser de parientes próximos. La idea es obtener clones del propio paciente para obtener la estirpe celular necesaria para la terapia y evitar los rechazos de las células exógenas.
Finalmente, ya en un marco distinto del biomédico, la clonación por transferencia nuclear está abriendo nuevas perspectivas para los animales de granja (con el fin de mantener linajes que tienen características como la alta producción de leche), la clonación de animales de compañía e incluso la clonación de especies en extinción.
Obstáculos en la clonación
Aunque cada semana escuchamos los logros en distintos centros de investigación de la obtención de un clon de vacuno, un clon de caballo o un clon de gato, lo cierto es que aún quedan muchos problemas técnicos por resolver. Los investigadores aún se mueven, en gran parte, de modo empírico, con numerosas tentativas de ensayo y error para mejorar los protocolos.
Por un lado, se da una alta incidencia de nacimientos muertos y abortos. Wilmut et al han descrito que existe un patrón de muertes durante el desarrollo embrionario y fetal, llegando al término sólo 1-2% de los embriones. Por otro lado, también se dan malformaciones y anomalías en el desarrollo. En el ganado bovino los intentos de clonación se saldan, a menudo, con gestaciones complicadas, abortos y nacimientos de terneros con tamaño anormalmente grande. De los terneros clónicos de tamaño anormal, muchos presentan hipercalemia (alta concentración de potasio) y pulmones poco maduros.
También se ha planteado la cuestión de la «edad biológica» de los clones. ¿Qué edad genética tiene el clon? ¿Corresponde a la edad de la célula dadora? ¿Supone esto un mayor peligro de acumulación de mutaciones y de envejecimiento celular? Hay informes sobre estas anomalías, como el acortamiento de los telómeros, lo que parece un indicio de edad celular.
Parece ser que uno de los mayores problemas está en los genes que se conocen como «genes de impresión». Estos genes son indispensables para la expresión génica en el desarrollo embrionario.
El grupo de investigación del Centro de Investigación Biomédica del Instituto Whitehead observó que clones que parecían normales presentaban graves anomalías que afectan a la expresión genética y que no se manifiestan en las características externas. Estos investigadores se han centrado en analizar los mecanismos de la escasa supervivencia y el sobrecrecimiento de los animales clonados. Mediante ratones clonados obtenidos a partir de células embrionarias, monitorizaron la actividad de estos genes impresores. El estudio sirvió para discernir si los problemas de los clones venían dados por alteraciones en las células donantes o en el procedimiento de la clonación. Y observaron que muchos de los problemas procedían de las células madre donantes, puesto que provenían de cultivos extremadamente inestables.
En definitiva, la clonación aún no es una técnica eficaz, pero parece que puede ofrecer importantes oportunidades médicas. Como sociedad, debemos adoptar actitudes críticas ante los cambios que se nos avecinan, pero, por otro lado, no debemos desaprovechar las posibilidades que nos ofrece la ciencia para mejorar nuestra calidad de vida y la de las generaciones futuras.
Bibliografía general
Casado M. González-Duarte R. Los retos de la genética en el siglo xxi: genética y bioética. Barcelona: Universidad de Barcelona, 1999; p. 203-13.
Cloning uses and ethics [consultado 29/08/2003]. Disponible en: http:// www.klsnet.com/clone.html
El proceso de la clonación [consultado 29/08/03]. Disponible en: http://www. geocities.com/CapeCanaveral/Hangar/9713/clon4.htm
Esponda P. Aspectos biológicos de los animales clónicos [consultado 29/08/03]. Disponible en: www.ciencia.cl/CienciaA1Dia/volumen5/numero1/articulos/articulo3.html
Iañez E. Seguridad en las clonaciones [consultado 29/08/03]. Disponible en: www.ugr.es/einez/Biotecnologia/clonseg.htm
Xenotrasplantes [consultado 29/08/03]. Disponible en: http://www.angelfire.com/ scifi/xenofermi/transgenicos.htm