Sepa cómo cuidar de un paciente que requiere tratamiento por proteinosis alveolar pulmonar.
La proteinosis alveolar pulmonar (PAP) es una enfermedad poco frecuente que se caracteriza por una acumulación excesiva de surfactante que altera el intercambio de gases. Se puede tratar mediante lavado broncopulmonar completo, que requiere la participación de un equipo multidisciplinar tanto en el quirófano como durante el postoperatorio. En este artículo describimos la PAP y veremos cuál es su tratamiento y lo que usted debe saber para apoyar y proporcionar educación sanitaria al paciente.
Un diagnóstico difícil
La PAP es una enfermedad que suele afectar a ambos pulmones y que se caracteriza por la acumulación de surfactante, una sustancia insoluble, en los alvéolos. Esta acumulación reduce la capacidad pulmonar del paciente, altera el intercambio de gases y desencadena una respuesta inflamatoria con fibrosis pulmonar.
La PAP de origen no hereditario afecta con mayor frecuencia a varones de 20 a 50 años de edad. Su causa es desconocida, aunque se ha puesto en relación con trastornos de inmunodeficiencia; exposición a polvo, sílice u óxido de aluminio, y tumores malignos hematológicos. Los estudios de investigación más recientes también apuntan otra posibilidad: los autoanticuerpos, que inhiben el factor estimulante de colonias de granulocitos y macrófagos (GM-CSF) y que alteran la capacidad de los macrófagos alveolares para eliminar el surfactante.
Los síntomas de la PAP son disnea de esfuerzo progresiva con tos mínimamente productiva y fatiga. Algunos pacientes desarrollan acropaquías en los dedos de las manos o cianosis, aunque ello es poco frecuente. En la radiografía de tórax se observa generalmente una afectación alveolar importante con infiltración e imágenes intersticiales llamativas. En la gasometría en sangre arterial (GSA) se detecta hipoxemia.
Puede ser difícil el diagnóstico diferencial entre la PAP y enfermedades como la neumonía, la sarcoidosis, la tuberculosis, la alveolitis o la carcinomatosis linfangítica. El diagnóstico se puede establecer mediante biopsia transbronquial y tomografía computarizada (TC).
La evolución de la enfermedad es variable. En hasta el 33% de los pacientes se produce una resolución espontánea del cuadro. En algunos estudios de pequeña envergadura se ha observado que en los pacientes con deficiencia de surfactante puede ser útil la administración de este factor. En la mayor parte de los pacientes restantes es necesaria una intervención terapéutica de carácter mecánico mediante lavado broncopulmonar completo.
La PAP es una enfermedad que suele afectar a ambos pulmones y que se caracteriza por la acumulación de surfactante, una sustancia insoluble, en los alvéolos. Esta acumulación reduce la capacidad pulmonar del paciente, altera el intercambio de gases y desencadena una respuesta inflamatoria con fibrosis pulmonar.
Lavado de los pulmones
El único tratamiento que se muestra eficaz de manera constante en la PAP sintomática es el lavado broncopulmonar completo, que representa el estándar terapéutico. Durante el procedimiento, que se realiza mientras el paciente permanece bajo anestesia general, se realiza el lavado de uno de los pulmones con una solución de cloruro sódico al 0,9% hasta que el líquido que se obtiene tras el lavado es limpio. Mientras tanto, se realiza ventilación mecánica en el otro pulmón. (En cada procedimiento sólo se puede efectuar el lavado de uno de los pulmones; véase el cuadro anexo Equipo para el lavado broncopulmonar.) El lavado broncopulmonar elimina las acumulaciones de lipoproteínas alveolares, interrumpe el proceso patológico y restablece la función de los macrófagos.
El equipo humano que lleva a cabo el lavado broncopulmonar está constituido por un neumólogo, que realiza el lavado con una solución de cloruro sódico al 0,9%, un anestesista, 2 profesionales de enfermería y un fisioterapeuta respiratorio. Durante el lavado broncopulmonar, este equipo debe mantener la ventilación del paciente, así como su oxigenación, perfusión, temperatura corporal y balance hídrico. La monitorización intraoperatoria incluye la oximetría de pulso, el control de la presión hemodinámica mediante un catéter en la arteria radial, la vigilancia de la presión venosa central (PVC), la monitorización cardíaca continua, el control de la temperatura y el mantenimiento del dióxido de carbono al final de la respiración corriente.
Presentación de un caso
David M., de 39 años de edad, acude al servicio de urgencias (SU) debido a que presenta un cuadro de disnea progresiva con sintomatología de tipo catarral desde hace 4 meses. Además, el paciente presenta tos seca que aparece cuando realiza ejercicio, habla o se ríe, pero que no le despierta por la noche. No tiene antecedentes de cuadros alérgicos ni de tuberculosis, asma, diabetes o problemas cardíacos; realiza ejercicio de manera regular y no fuma.
La auscultación pulmonar es normal, tanto en reposo como en la espiración forzada. La frecuencia respiratoria es de 14, con ritmo regular; la SpO2 es del 92% mientras respira aire ambiente, y el resto de sus signos vitales es normal. El paciente no presenta dolor torácico, fiebre, escalofríos ni sudación excesiva. No se detectan acropaquías ni cianosis.
En la radiografía de tórax se observan zonas parcheadas de densidad aumentada diseminadas en ambos campos pulmonares inferiores, con reforzamiento del patrón intersticial. Se establece un diagnóstico de posible neumonía y al Sr. David M. se le prescriben antibióticos.
Sin embargo, en las semanas siguientes tiene lugar un deterioro de su estado. Vuelve de nuevo al SU debido a que muestra disnea progresiva y tos seca.
En el estudio diagnóstico efectuado en este momento se observan un pH de 7,4, una PaCO2 de 40 mmHg y una PaO2 de 59 mmHg en aire ambiente. Su capacidad pulmonar total es el 60% de la esperada, lo que indica un problema restrictivo grave. En la radiografía de tórax se observa un aumento en el número de zonas de incremento de la densidad, con una consolidación marcada que es más importante en el lóbulo inferior derecho.
Las pruebas diagnósticas descartan tuberculosis, Legionella e infección por neumococos y por hongos. Tras confirmarse la PAP mediante una biopsia transbronquial y una TC, al Sr. David M. se le prepara para la realización de un lavado broncopulmonar completo en el pulmón derecho.
Durante el lavado, la presión arterial (PA) del Sr. David M. muestra labilidad, de manera que la PA sistólica disminuye hasta 70 mmHg cuando se introduce el líquido y vuelve a presentar los valores normales de 110-120 mmHg cuando se realiza el drenaje del líquido. Para el mantenimiento de una PA sistólica estable de 100 mmHg durante el procedimiento se precisa la administración de un bolo intravenoso de efedrina y la realización de una perfusión de dopamina.
La PVC del Sr. David M. es elevada durante todo el procedimiento, con cifras de 18 mmHg. Esta inestabilidad hemodinámica puede reflejar la existencia de desplazamientos mediastínicos o de alteraciones en el llenado ventricular izquierdo, complicaciones que tienen lugar a menudo cuando el pulmón se llena de líquido.
Posibles problemas
El principal efecto adverso causado por el lavado bronco pulmonar completo es la hipoxemia. Durante la introducción del líquido disminuye el flujo sanguíneo en el pulmón en el que se realiza debido a que tiene lugar una compresión de los vasos sanguíneos pulmonares. Durante el drenaje del líquido, la reperfusión del pulmón en el que se realiza el lavado da lugar a una situación de derivación con el pulmón ventilado, con desaturación. Durante el lavado del pulmón derecho, la presión excesiva que tiene lugar sobre la tráquea puede dar lugar a la entrada de líquido en el pulmón izquierdo ventilado, lo que causa hipoxemia. La corrección del problema requiere la aplicación inmediata de medidas de aspiración y el mantenimiento escrupuloso tanto de la ventilación como de la oxigenación.
Durante el lavado broncopulmonar del Sr. David M. se utilizan aproximadamente 20 l de solución de cloruro sódico al 0,9%, hasta que el líquido que se obtiene en el drenaje es relativamente limpio. El lavado final se lleva a cabo manteniendo al Sr. David M. en posición de Trendelenburg con objeto de facilitar el drenaje. En el pulmón en el que se efectúa el lavado se realiza una aspiración concienzuda y finalmente se aplica ventilación mecánica en ambos pulmones con oxígeno al 100% durante 15 min.
Tras la desaparición de la anestesia, el Sr. David M. se despierta en el quirófano, es extubado sin dificultad y trasladado a la unidad de reanimación posquirúrgica (URPQ).
Recuperación rápida
Tras su llegada a la URPQ, se administra oxígeno al 100% mediante mascarilla y el paciente es colocado en posición semi-Fowler. La SpO2 es del 93%; la frecuencia respiratoria, de 24; la PA, de 110/70; la frecuencia cardíaca, de 88, y la PVC, de 9 mmHg. La respiración es ligeramente dificultosa pero regular; en la auscultación pulmonar se observan sibilancias inspiratorias leves.
Los cuidados durante el postoperatorio se centran en la ventilación óptima. Se realiza fisioterapia torácica cada 2 h y se efectúan 3 tratamientos de broncodilatación con albuterol cada 2 h. Al paciente se le recomienda que realice inspiraciones profundas frecuentes, con tos y con espirometría a demanda. (En algunos pacientes es necesario proceder a la ventilación mecánica durante un período breve de tiempo en el postoperatorio, generalmente durante menos de 2 h, para el restablecimiento de la función pulmonar adecuada).
La monitorización postoperatoria incluye la oximetría de pulso continua, el control de los parámetros cardíacos y respiratorios, la vigilancia de los parámetros hemodinámicos y la valoración de los signos vitales cada 15 min. La GSA del Sr. David M. se comprueba cada 2 h. Una vez que los valores de la misma son estables, se retira la ventilación mecánica y se administra oxígeno mediante cánula nasal a una tasa de 3 l/min.
Normalmente, los infiltrados alveolares desaparecen a las 24 h del lavado. La primera radiografía que se le realiza en el postoperatorio al Sr. David M. muestra una pequeña cantidad de líquido residual con persistencia del patrón intersticial y con alteraciones alveolares en el pulmón derecho y una zona importante de consolidación en el pulmón izquierdo. En una nueva radiografía torácica efectuada 3 h después se evidencia una mejoría importante en el pulmón derecho.
Mediante el conocimiento de esta enfermedad infrecuente y de su tratamiento, el profesional de enfermería puede ayudar al paciente a mantener una mejor calidad de vida.
Tras 6 h de permanencia en la URPQ, el Sr. David M. es dado de alta a la unidad de cirugía. El SpO2 a lo largo de la noche se mantiene en el 96% respirando aire ambiente. Al cabo de 1 h de estancia en la unidad de cirugía puede caminar por el vestíbulo de la misma sin presentar una disnea significativa. Recibe el alta a la mañana siguiente, después de que la GSA y la radiografía de tórax muestren una resolución significativa de la consolidación pulmonar derecha. Dos semanas después, el mismo equipo asistencial realiza el lavado broncopulmonar del pulmón izquierdo y el Sr. David M. recibe el alta la noche siguiente.
En más del 50% de los pacientes sólo es necesario efectuar el lavado broncopulmonar completo inicial. Sin embargo, en algunos es necesario el lavado broncopulmonar completo cada pocos meses.
Mediante el conocimiento de esta enfermedad infrecuente y de su tratamiento, el profesional de enfermería puede ayudar al paciente a mantener una mejor calidad de vida.
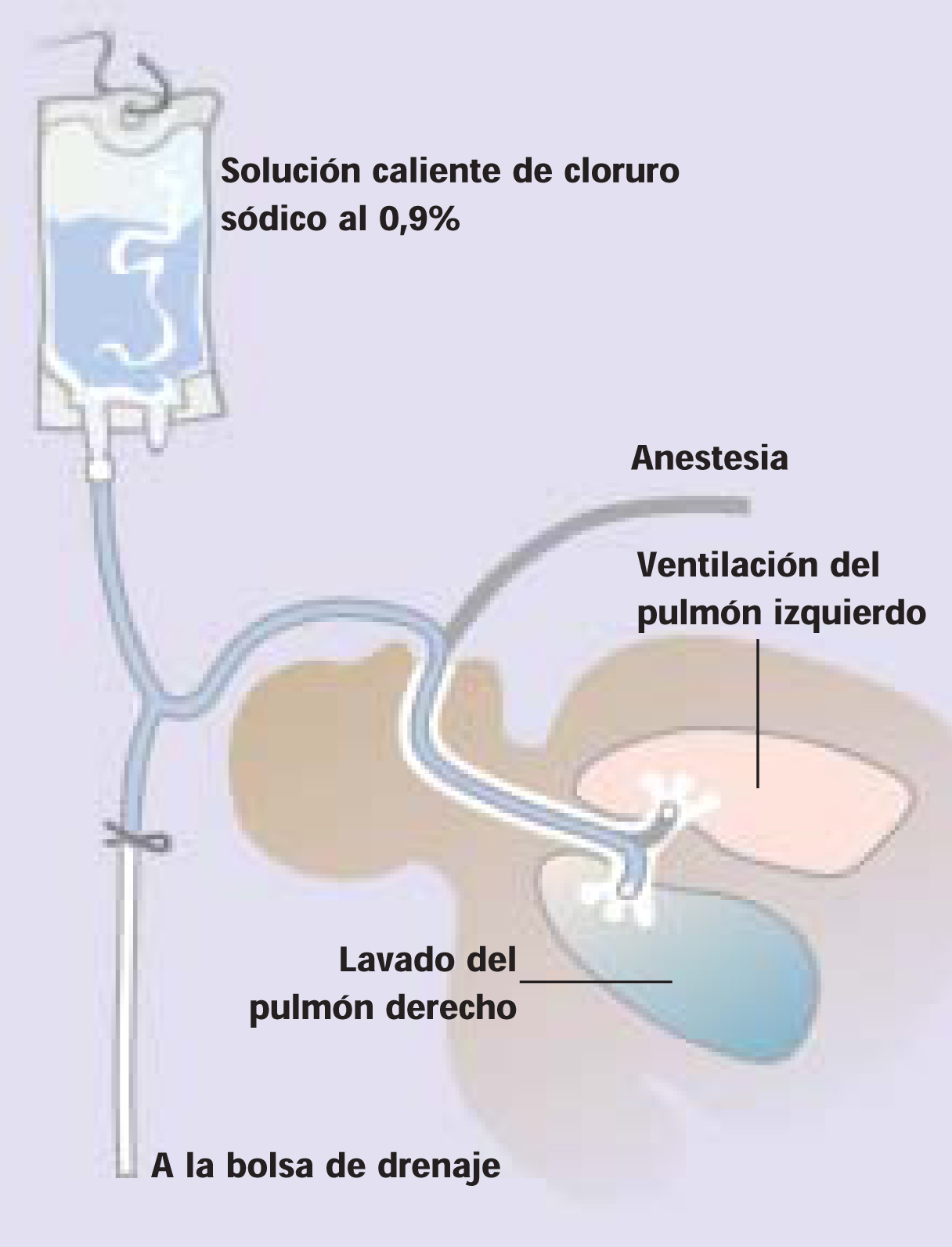
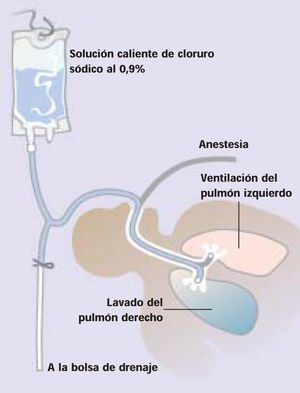
Equipo para el lavado broncopulmonar
Mientras se efectúa la ventilación del pulmón izquierdo del paciente, se lleva a cabo el lavado del pulmón derecho a través de un tubo endotraqueal de luz doble, tal como se muestra en el esquema: la solución de cloruro sódico al 0,9% se calienta hasta 37 °C y se coloca 30 cm por encima del tórax. El contenedor de drenaje conectado mediante un sistema en Y se sitúa 30 cm por debajo del tórax. La solución caliente se introduce en el pulmón y sale del mismo por efecto de la gravedad. El líquido de aspecto lechoso que se obtiene inicialmente es característico de la proteinosis alveolar pulmonar.
Debbie Lacheur es coordinadora de pacientes y profesional de enfermería clínica y educadora en la unidad de reanimación del Royal Columbian Hospital en New Westminster, British Columbia, Canadá.
BIBLIOGRAFÍA SELECCIONADA
Bussieres, J.: "Whole Lung Lavage," Anesthesiology Clinics of North America. 19(3):543-558, September 2001.
Seymour, J., and Presneill, J.: "Pulmonary Alveolar Proteinosis: Progress in the First 44 Years," American Journal of Respiratory and Critical Care Medicine. 166(2):215-235, July 15, 2002.
Wasserman, K.: "Pulmonary Alveolar Proteinosis," in Textbook of Respiratory Medicine, 3rd edition, J. Murray, et al. (eds). Philadelphia, Pa., W.B. Saunders Co., 2000.