Los meningiomas son los tumores primarios más frecuentes del sistema nervioso central y son de consulta frecuente en neurooncología.
MétodosSe realizó una revisión bibliográfica extensa y actualizada con el objetivo de favorecer el mejor abordaje de esta patología.
ResultadosLos meningiomas son tumores extraaxiales originados a partir de las células de la aracnoides y representan el 36,4% de los tumores primarios intracraneanos. Los meningiomas pueden ser incidentales, pequeños y de lento crecimiento, o masas extensas y/o de crecimiento progresivo. La primera alteración genética descripta fue la pérdida del cromosoma 22; en los últimos años se han descripto diversas mutaciones genéticas, tales como las mutaciones del promotor de transcriptasa reversa de la telomerasa (TERT), implicadas en la progresión maligna. Las neuroimágenes suelen tener características distintivas en la tomografía computarizada y la resonancia magnética. Por anatomía patológica se los clasifica en grados i, ii y iii de la Organización Mundial de la Salud y existen diversos subtipos con diferentes características, evolución y pronóstico. La neurocirugía y el grado de resección son el pilar del tratamiento y el predictor de progresión. En pacientes seleccionados se podría considerar la embolización prequirúrgica. La radioterapia puede ser adyuvante o como tratamiento único en los irresecables; al igual que en los grados ii y anaplásicos. En relación con la terapia farmacológica, solo bevacizumab, sunitinib y vatalinib han mostrado una potencial actividad clínica.
ConclusionesDescribimos en detalle las características más relevantes, la evaluación y las opciones terapéuticas disponibles para pacientes con meningiomas.
Meningiomas are the most common central nervous system tumors, and as such, they are frequently encountered in neuro-oncology practice.
MethodsWe conducted an extensive and up-to-date literature review on meningiomas aimed at describing the best approach to this pathology.
ResultsMeningiomas are extra-axial tumors originated from arachnoid cells. They represent 36.4% of the primary intracranial tumors. Meningiomas may be incidental, small, and slow growing tumors, or extensive and/or progressive growing masses. The first genetic alteration described in these tumors was the loss of chromosome 22; in recent years many other genetic mutations have been described, such as mutations of the TERT promoter (telomerase reverse transcriptase), which are involved in malignant progression. Meningiomas usually have distinctive features in computed tomography and magnetic resonance imaging. From the histological standpoint, the World Health Organization classifies meningiomas into grade i, ii or iii. There are several histological subtypes, which are linked to different clinical courses and prognoses. Tumor resection is the main treatment for these tumors, and the extent of resection is a predictor of progression-free survival. In selected patients, preoperative embolization could be considered. Radiation therapy may be used as an adjuvant therapy or, in non-resectable meningiomas, as a neo-adjuvant therapy. Regarding systemic therapy, bevacizumab, sunitinib and vatalinib have shown potential clinical activity in a small subset of patients.
ConclusionsIn this review, we present a detailed description of the most important characteristics, diagnosis and treatment options available for patients with meningiomas.
Los meningiomas son tumores extraaxiales originados a partir de las células de la aracnoides y son los tumores primarios más frecuentes del sistema nervioso central (SNC). Representan el 36,4% de los tumores intracraneanos1.
Abarcan un amplio espectro que va desde lesiones pequeñas de lento crecimiento y de hallazgo incidental y que requieren solo observación, a masas extensas y/o de crecimiento progresivo que afectan áreas vitales, como el tronco cerebral y nervios craneales, en ocasiones, con pocas expectativas u opciones terapéuticas2.
La incidencia de los meningiomas se incrementa con la edad y la mayoría son diagnosticados en los adultos, aumentando significativamente a partir de los 65 años de edad; predominan en el sexo femenino (relación fem:masc>2:1) y en la raza negra. El 98,6% son benignos —grado i—; el resto son los meningiomas atípicos —grado ii— y mucho más infrecuentes son los malignos o anaplásicos —grado iii1,3.
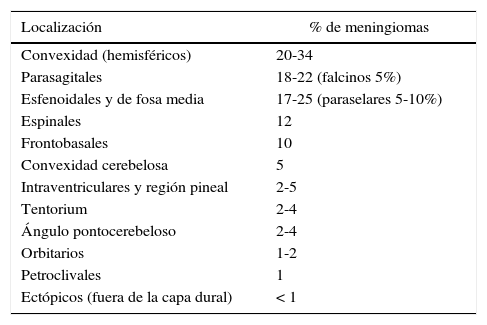
Las localizaciones más frecuentes de los meningiomas son la convexidad y parasagital, ala del esfenoides y fosa media craneana, espinales, surco olfatorio, etc. (tabla 1)4,5.
Incidencia global de los meningiomas (%) basado en la localización
| Localización | % de meningiomas |
|---|---|
| Convexidad (hemisféricos) | 20-34 |
| Parasagitales | 18-22 (falcinos 5%) |
| Esfenoidales y de fosa media | 17-25 (paraselares 5-10%) |
| Espinales | 12 |
| Frontobasales | 10 |
| Convexidad cerebelosa | 5 |
| Intraventriculares y región pineal | 2-5 |
| Tentorium | 2-4 |
| Ángulo pontocerebeloso | 2-4 |
| Orbitarios | 1-2 |
| Petroclivales | 1 |
| Ectópicos (fuera de la capa dural) | < 1 |
Las radiaciones ionizantes están implicadas en la génesis de tumores sólidos como los meningiomas, entre otros6,7. Dado que las radiaciones ionizantes son un factor de riesgo modificable conocido para tumores de SNC, sería importante aclarar la relación entre las radiaciones ionizantes/tumores del SNC para proporcionar antecedentes etiológicos y la implementación de estrategias preventivas. En general, se encontró que la exposición a la radiación se asoció con un mayor riesgo para todos los tumores del SNC, gliomas, meningiomas y sarcomas, y que la radiación tuvo un mayor efecto sobre el riesgo de desarrollar meningiomas en comparación con gliomas8. El riesgo de desarrollar tumores secundarios a radiación oscila entre el 1 y el 3%.
Los estudios mencionan la radioterapia (RT) en la niñez para la tiña capitis y otras patologías9-12.
Diversas teorías se postulan sobre el desarrollo de tumores secundarios a la radiación:
- a.
La generación de alteraciones genéticas con disrupción del ADN en genes PTEN o P53.
- b.
Inestabilidad cariotípica ocasionada por aberraciones cromosómicas inducidas por la RT.
- c.
Alteraciones en la pared vascular que induce la liberación de factores prooncogénicos como PDGF, factor de crecimiento del endotelio vascular (VEGF, vascular endotelial growth factor), FGF-B13,14.
Los tumores deben cumplir ciertos criterios para considerarse secundarios a la RT, a saber:
- 1.
El tumor no estaba presente previo a la RT.
- 2.
El tumor se encuentra dentro del campo irradiado.
- 3.
Existe un intervalo razonable entre la RT y la aparición del tumor (años).
- 4.
Hay diferencias histológicas entre el tumor irradiado y los subsecuentes.
- 5.
El paciente no debe presentar otra patología que favorezca el desarrollo de otros tumores como neurofibromatosis u otra enfermedad genética que incremente el riesgo de desarrollar un meningioma.
El período de latencia entre la RT y el desarrollo de meningiomas abarca de 1,2 a 63 años y el promedio de latencia para altas dosis de RT (> 20Gy) es de 19,5 a 24,6 años7,15.
Telefonía inalámbrica/celularLa telefonía inalámbrica y celular (ondas electromagnéticas de baja frecuencia) podrían estar implicadas en la génesis de tumores del SNC, entre ellos los meningiomas16. La clasificación de la Organización Mundial de la Salud (OMS) y la Agencia Internacional para la Investigación del Cáncer introdujo los campos electromagnéticos de radiofrecuencia emitidos por los dispositivos de telefonía inalámbrica como posiblemente carcinógeno para los humanos —grupo 2B— (última actualización abril del 2015)17.
Obesidad y sedentarismoRecientemente, un metaanálisis sugiere que el mantenimiento de un índice de masa corporal normal y la participación en la actividad física se asocia con un menor riesgo de desarrollo de meningioma. El gran desconocimiento de otros factores de riesgo modificables para evitar el desarrollo de meningiomas, y la alta prevalencia de aumento de la masa corporal a nivel mundial y del sedentarismo, hacen que estos hallazgos puedan ser relevantes en las estrategias a nivel individual y de salud pública dirigidas a reducir el riesgo de meningioma18.
Cáncer de mama y meningiomaLa asociación entre cáncer de mama y meningioma ha sido reportada en la literatura; sin embargo, existe bibliografía discordante al respecto. Un estudio retrospectivo de Criscitiello et al. con más de 12.000 pacientes con cáncer de mama y un seguimiento promedio de 7 años no encontró asociación significativa entre el desarrollo de meningioma y el cáncer de mama19.
Genética de los meningiomas y enfermedades asociadasLa primera alteración genética descripta en los meningiomas fue la pérdida del cromosoma 22 (Cr22), que persiste como hallazgo más frecuente en los meningiomas. Posteriormente, se identificó un gen en el cromosoma 22 (schwannomina/merlina) responsable del síndrome hereditario neurofibromatosis tipo 2 (NF2). Si bien los schwannomas bilaterales son la característica del síndrome, aproximadamente la mitad de los pacientes desarrolla meningiomas (generalmente múltiples), lo que indica el papel del gen NF2 en el desarrollo de los meningiomas. Estas alteraciones moleculares a nivel del gen NF2 ocurren además en el 50% de los meningiomas esporádicos20-22.
A partir del 2013, se comunicaron diversas mutaciones genéticas en una pequeña proporción de meningiomas, tales como TRAF7, KLF4, AKT1 y SMO. De estos se destaca la mutación en AKT1 que también se encuentra en el cáncer de mama, ovario y colorrectal; en los meningiomas predomina en los subtipos tumorales meningotelial y transicional. Las mutaciones en TRAF7 ocurren en un alto porcentaje (93-100%) en el subtipo meningioma secretor y son mutuamente excluyentes de las mutaciones del gen NF223,24.
Tanto las deleciones de los cromosomas 1p, 6q, 10q, 14q y 18q, como las adiciones de cromosomas 1q, 9q, 12q, 15q, 17q y 20q, han sido relacionadas con la progresión y recurrencia de los meningiomas22,25.
La mayoría de los meningiomas muestran neoangiogénesis y regulación positiva de las vías angiogénicas, como el receptor del VEGF26.
El mantenimiento de la longitud de los telómeros es un proceso clave en la progresión maligna y las mutaciones en el promotor de la transcriptasa reversa de la telomerasa (TERT) han sido recientemente identificadas en diversos tumores. Una elevada incidencia de mutaciones del promotor de TERT ha sido encontrada en meningiomas que recaen con progresión histológica maligna. Los tumores recaídos sin progresión histológica (malignización) no mostraron ninguna mutación del promotor de TERT. Las mutaciones del promotor de TERT son alteraciones genéticas cruciales implicadas en la progresión maligna de meningiomas, y esto podría ser utilizado como un biomarcador para identificar aquellos pacientes con meningiomas y riesgo de malignización27.
Existen cuadros clínicos que se asocian con meningiomas; incluyen la meningioangiomatosis, el síndrome de Gorlin, la enfermedad de Castleman y el síndrome Rubenstein-Taybi, entre otros28,29.
ClínicaLa presentación clínica de los meningiomas dependerá de la localización del tumor. Como los meningiomas son de crecimiento lento, los síntomas de inicio suelen ser insidiosos30. Se clasifican en sintomáticos e incidentales o asintomáticos.
Meningiomas sintomáticosLa sintomatología depende de la localización y de la velocidad de crecimiento tumoral. La cefalea de reciente comienzo es un síntoma de presentación común y en ocasiones no asociado a síntomas de hipertensión endocraneana; esto refleja el lento crecimiento de estos tumores. También puede recabarse una historia de epilepsia parcial, así como cambios en la personalidad (usualmente confundidos con depresión o demencia) en algunos pacientes con meningiomas de la convexidad o con meningiomas extensos frontobasales31. La convexidad y la región parasagital son los lugares de asiento más frecuentes, produciendo cefalea y cambios en la personalidad, que constituyen la presentación clínica más habitual32,33.
En el caso de los meningiomas del foramen magno, los síntomas más frecuentes son la cefalea y la cervicobraquialgia34.
Dada la multiplicidad topográfica de los meningiomas y sus variadas formas de presentaciones clínicas, se sugiere al lector consultar sobre este tema en tratados de neurología y neurocirugía.
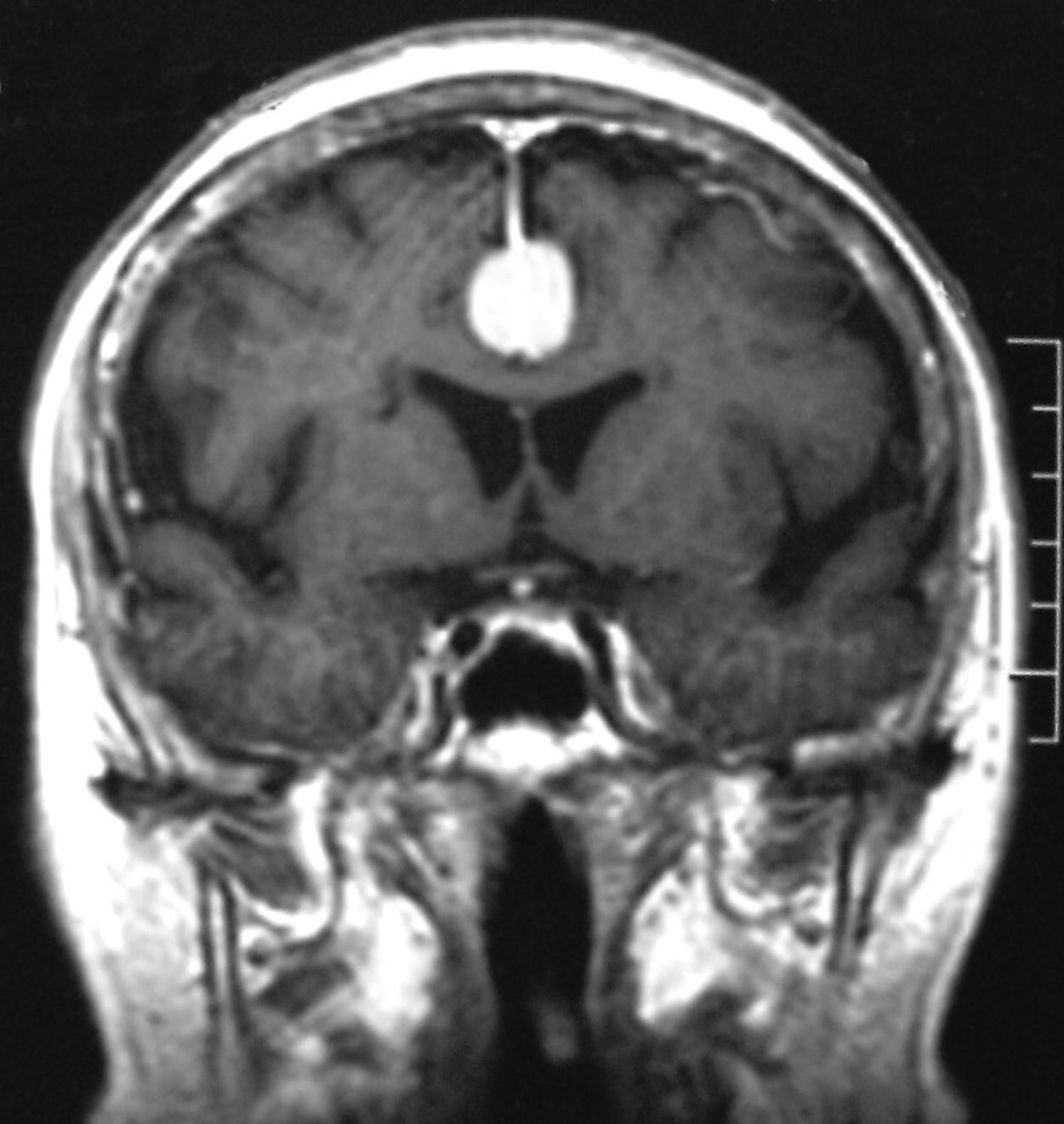
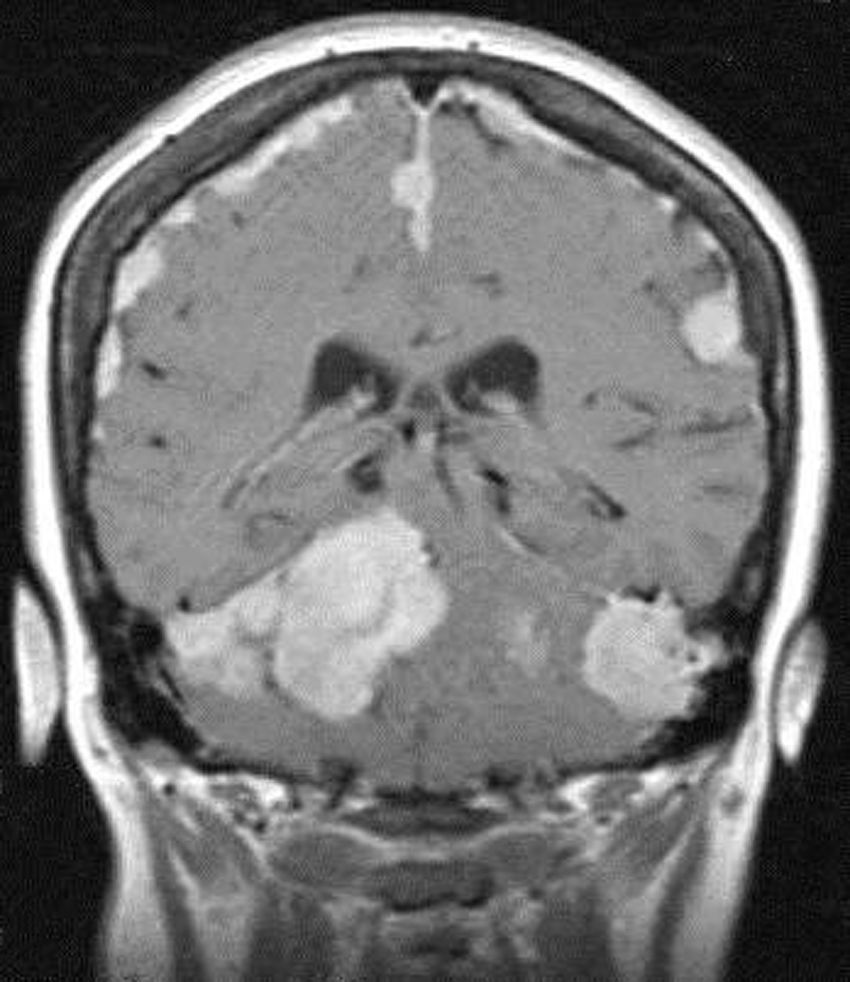
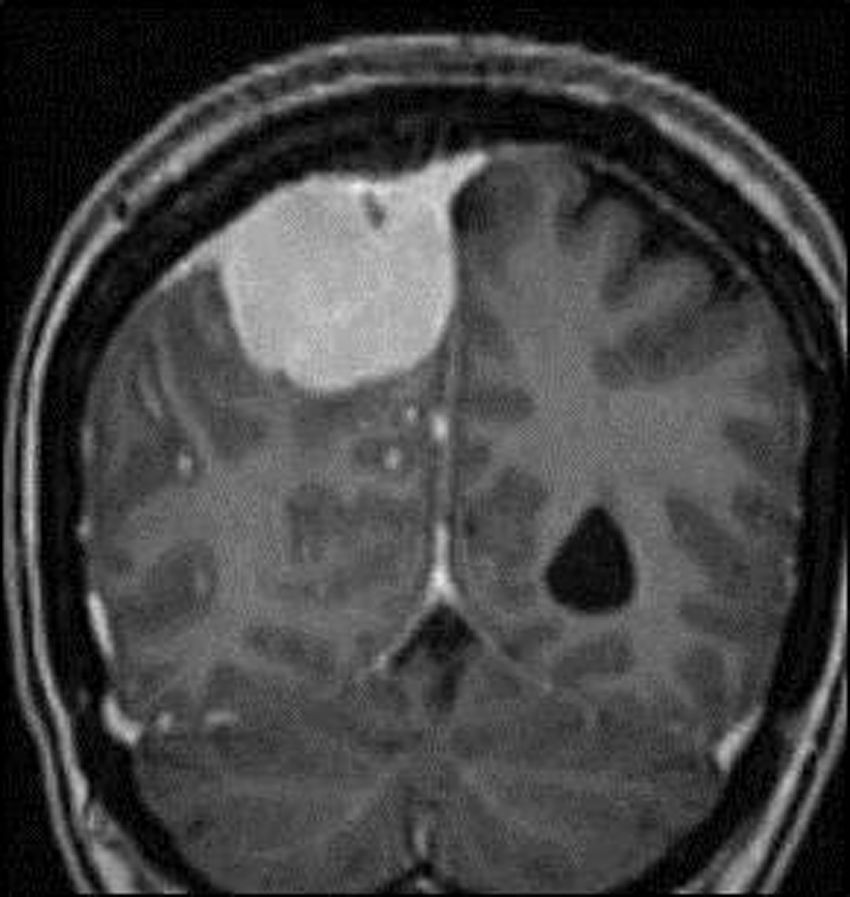
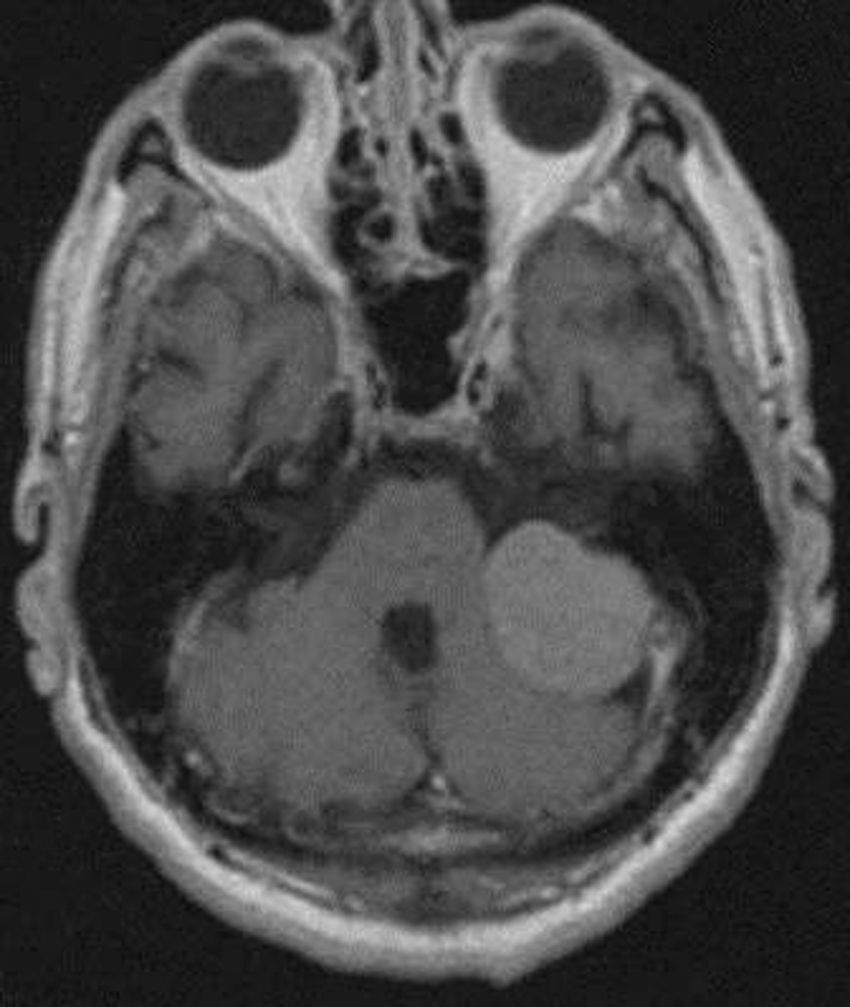
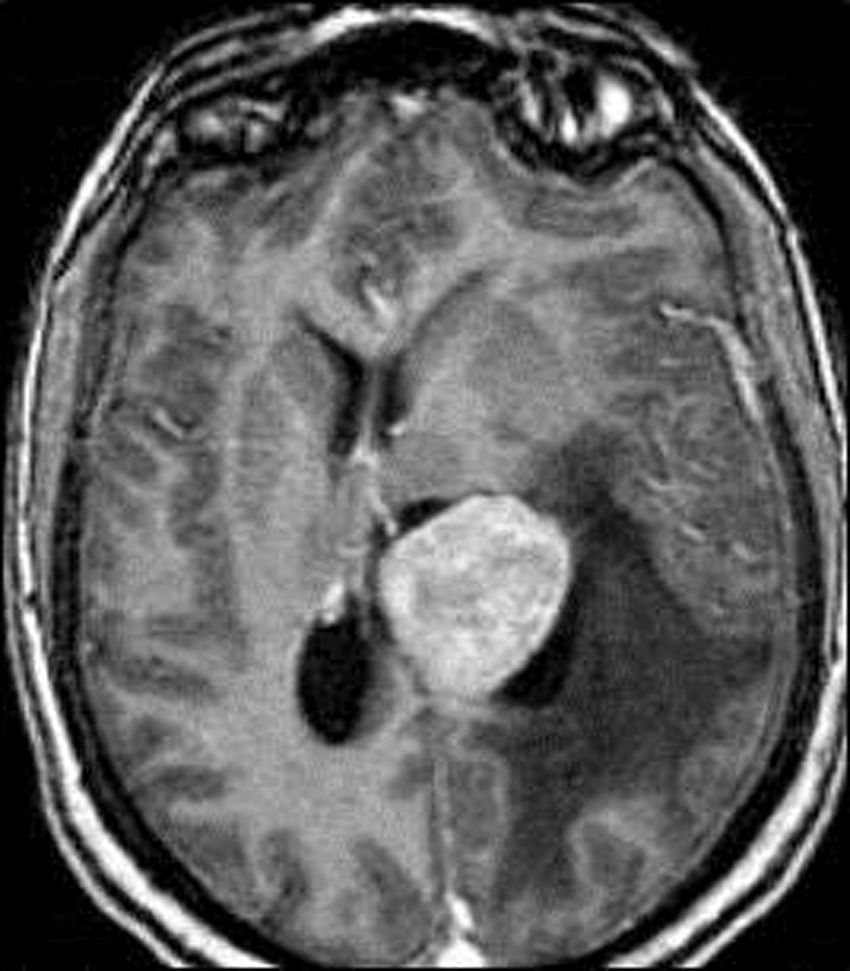
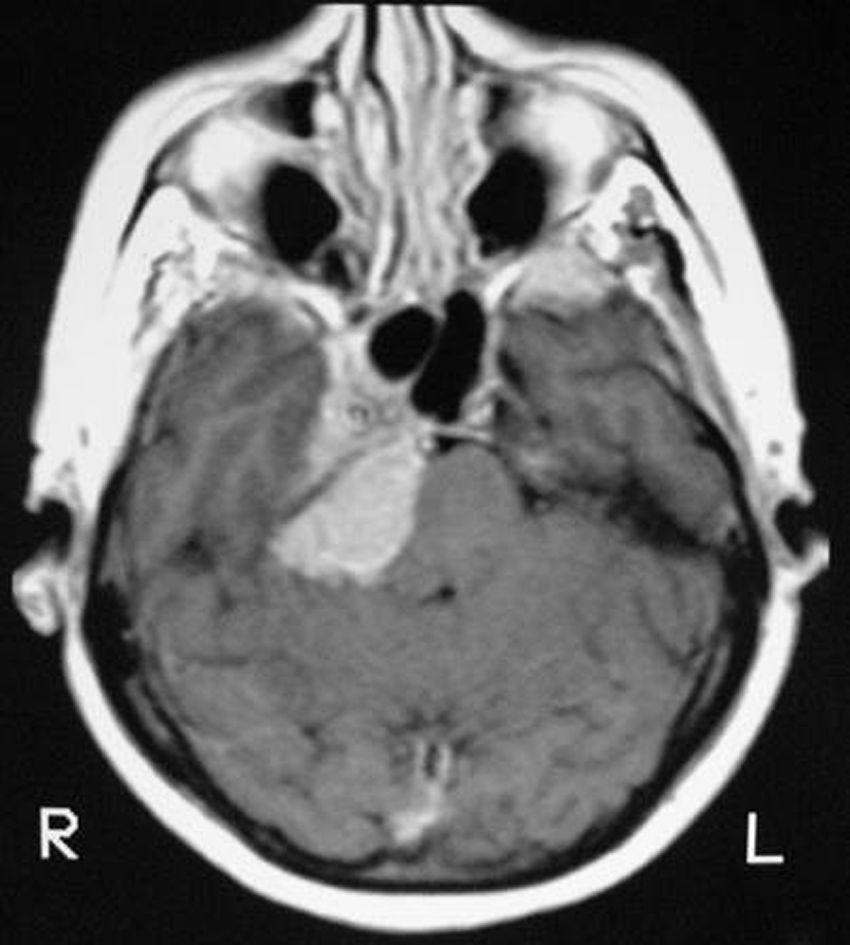
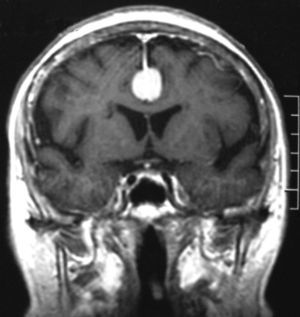
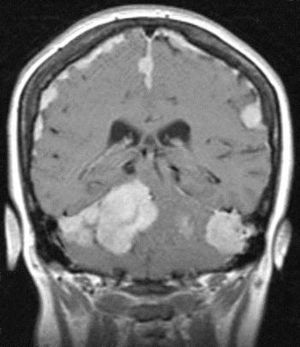
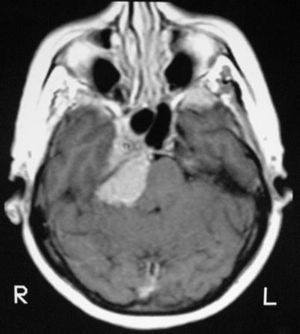
Meningiomas incidentales (asintomáticos)Dentro de los tumores primarios del SNC de hallazgo incidental, el tumor benigno más común es el meningioma y su detección incidental es más frecuente en personas añosas y de sexo femenino (fig. 1)1. Es común que los casos incidentales sean detectados durante el estudio de otras patologías del SNC, como el ataque cerebral, enfermedades degenerativas, traumatismo de cráneo y otras.
La detección incidental es mucho más frecuente en personas de edad avanzada que en jóvenes. Es razonable prever que con el aumento del uso de técnicas avanzadas de neuroimágenes aumentará el hallazgo de meningiomas incidentales o asintomáticos35,36. Asimismo, el aumento de población longeva; en estudios post mortem se ha reportado una cifra tan alta como el 3%36,37.
La mayoría de los meningiomas incidentales, incluidos los pacientes jóvenes, permanecen asintomáticos y tienen un crecimiento muy lento o una tasa de crecimiento cero luego de períodos de seguimiento que varían entre 21 meses a 8,8 años38.
Sin embargo, la edad del paciente ≤ 60 años, el tamaño tumoral inicial>25mm, la ausencia de calcificaciones, la señal hiperintensa en T2 y la presencia de edema peritumoral son factores predictivos que se correlacionan positivamente con el crecimiento tumoral. Su evolución clínica también dependerá de otras variables, tales como la localización y/o la compresión de estructuras vecinas33,37,39.
En pacientes añosos ≥ 70 años debe prestarse atención a las neuroimágenes; la presencia de calcificaciones no se relacionan con crecimiento tumoral, mientras que un tamaño ≥ 30mm es predictivo de crecimiento tumoral, aunque también pueden serlo el sexo masculino y la presencia de hiperintensidad tumoral en T240.
Neuroimágenes de los meningiomasLos meningiomas se distinguen de otros tumores intracraneanos por su localización extraaxial con base de implantación dural y su rica vascularización4.
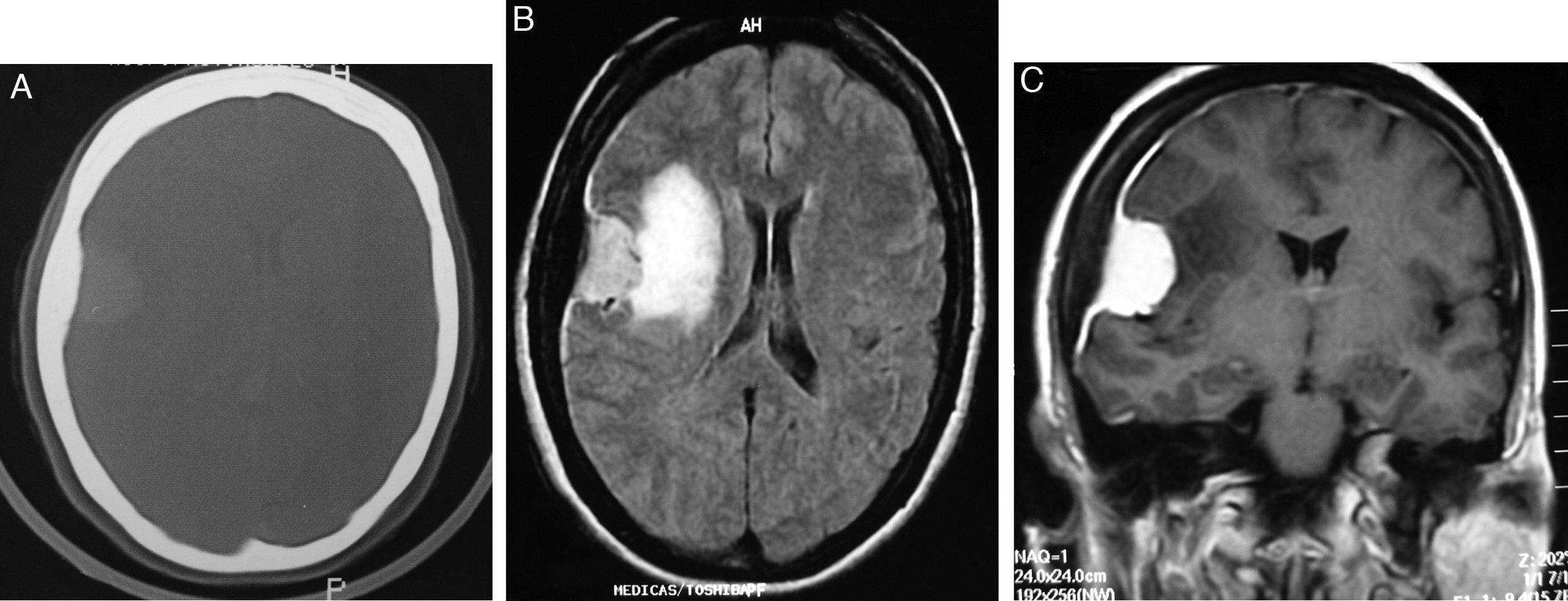
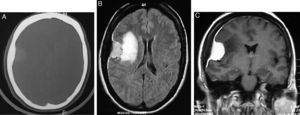
En la tomografía computarizada (TC) de cerebro se comportan isodensos (25%) o ligeramente hiperdensos (75%) respecto al parénquima cerebral, con presencia de calcificaciones en un 15-20%. Luego de la administración del contraste por vía IV, realzan en forma homogénea e intensa en aproximadamente el 90% de todos los meningiomas. En el hueso adyacente se pueden encontrar signos de hiperostosis (es importante la ventana ósea) (fig. 2A-C)4,41,42.
A) TC con ventana ósea: lesión nodular con realce y engrosamiento óseo adyacente. B) RM axial Flair: lesión extraaxial hiperintensa con signos de edema vasogénico, efecto de masa sobre el ventrículo, engrosamiento dural e hiperostosis. C) RM coronal T1 con gadolinio: realce intenso y homogéneo con cola dural. Dx: meningioma e hiperostosis con afección fronto-insular.
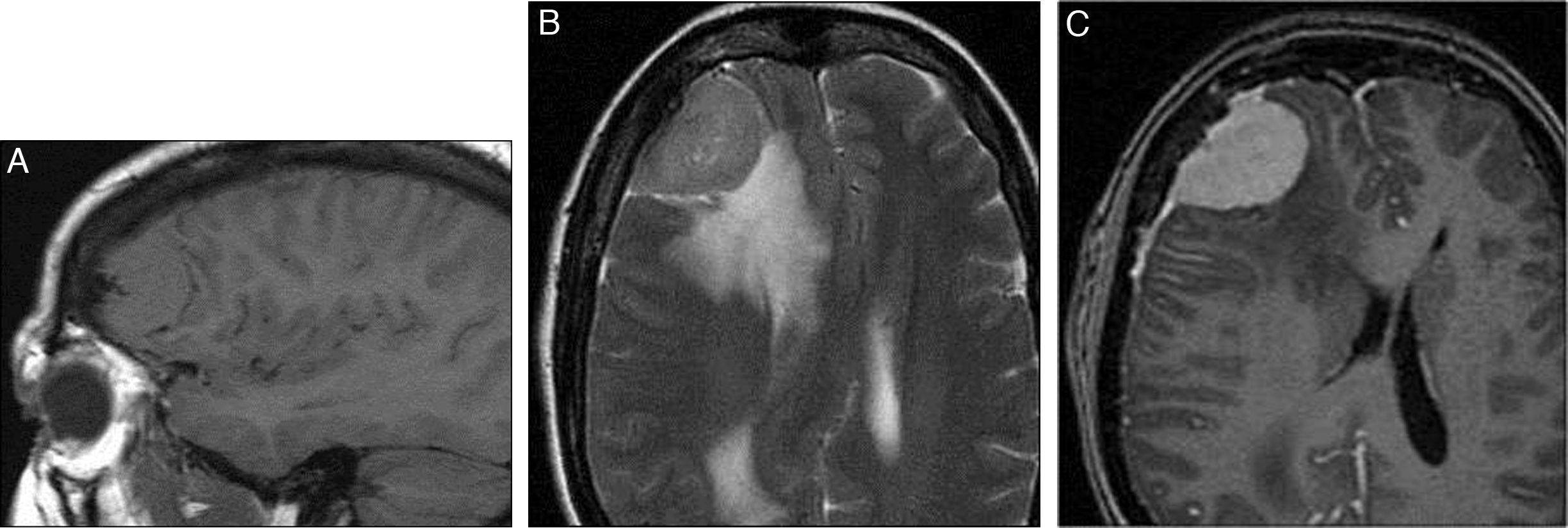
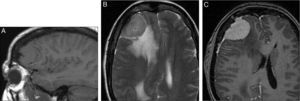
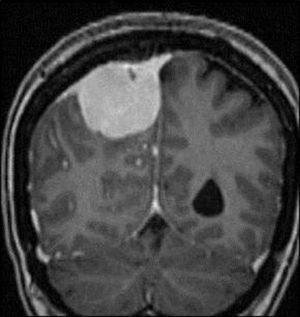
En la resonancia magnética (RM) se comportan de forma variable; en T2 son generalmente hiperintensos o isointensos con respecto al parénquima, e isointenso o levemente hipointenso en T1. Tras la administración de gadolinio, el 95% de los casos muestra un realce intenso y homogéneo. Un signo muy característico pero no patognomónico es el de la cola o coleta dural (fig. 3A-C)43,44. La prevalencia de la cola dural oscila entre el 52 y el 78%45,46. En la RM, la secuencia más sensible para poner en evidencia las posibles calcificaciones es la de ecogradiente. Pueden acompañarse de signos de edema vasogénico (60%)6,42.
A) RM sagital T1: lesión frontal extraaxial isointensa. B) Axial T2: misma lesión discretamente hiperintensa con signos de edema vasogénico adyacente, efecto de masa y desviación de la línea media. C) Axial T1 con gadolinio: realce intenso y homogéneo y refuerzo dural (signo de la cola dural). Dx: meningioma frontal derecho.
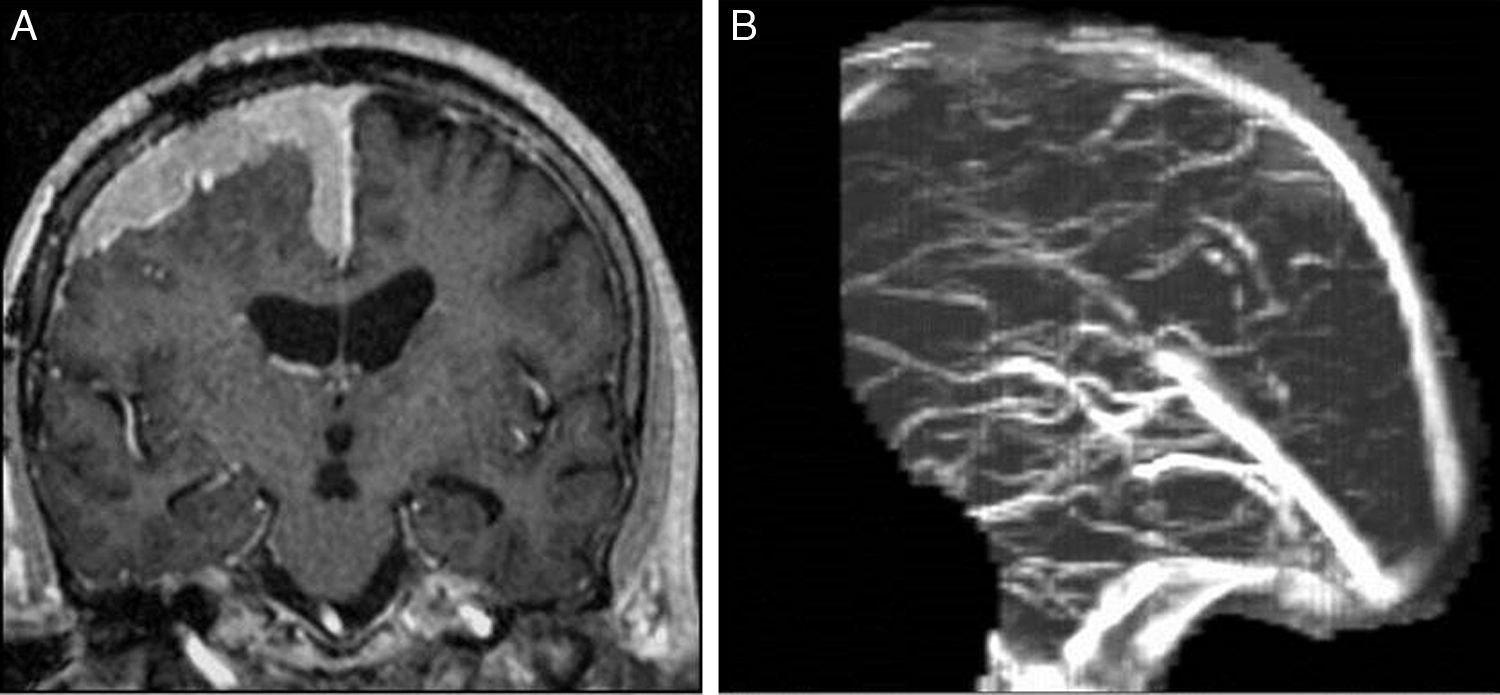
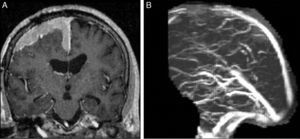
Se debe evaluar la indemnidad de los senos durales contiguos con secuencias convencionales y angiográficas (fig. 4A-B). Los vasos arteriales englobados por el meningioma se encuentran típicamente reducidos de calibre.
A) RM Coronal T1 con gadolinio: lesión extraaxial con crecimiento en placa y realce intenso y homogéneo en la convexidad y la hoz cerebral. B) Angio-RM en tiempo venoso: pérdida de señal en el sector anterior del seno longitudinal superior. Dx: meningioma de la convexidad con compromiso del seno venoso.
En la secuencia de espectroscopia con tiempo de eco (TE) corto se describe un típico pico de alanina en la franja de 1,3 a 1,5 ppm47.
Otros casos especiales e infrecuentes son4,48:
- a.
Lipoblástico: con componente de tejido adiposo, y por lo tanto unidades Hounsfield (UH) negativas en la TC e hiperintensos en T1.
- b.
Fibroblástico: se comporta hipointenso en T2.
- c.
Psamomatoso: se muestra marcadamente calcificado.
- d.
Con degeneración quística.
- e.
Atípico o maligno: hay evidencia de invasión local con áreas de necrosis, extenso edema periférico y destrucción ósea. La mayoría de los meningiomas atípicos o malignos son hiperintensos en secuencias de difusión, con valores de coeficiente de difusión aparente significativamente más bajos que los meningiomas típicos o que la sustancia blanca normal.
- f.
Con crecimiento en placa.
- g.
Intraóseo: lesión hiperostótica, osteolítica o formas mixtas.
La terminología meningiomas intracraneales múltiples debe ser utilizada solo cuando 2 o más meningiomas se producen de forma simultánea o secuencialmente en diferentes lugares. La falta de solución de continuidad se denomina meningiomatosis (fig. 5).
- 1.
Aproximadamente en el 60% de los casos de meningiomas con cola dural, esta presenta invasión tumoral (fig. 6)44.
- 2.
Los criterios que definen la cola dural son:
- a.
Se observa en al menos 2 cortes consecutivos en la RM y en más de un plano.
- b.
El grosor es mayor adyacente al tumor y al alejarse de este, decrece.
- c.
Refuerza más con el gadolinio que el mismo tumor45.
- a.
- 3.
La cola dural se observa más en meningiomas con edema peritumoral.
- 4.
La inmunohistoquímica con VEGF y CD34 tienen mayor expresión en la cola dural invadida por tumor que en el tumor mismo (VEGF es un marcador positivo para la angiogénesis tumoral. El CD34 se relaciona con una elevada densidad microvascular).
- 5.
La cola dural de aspecto liso orienta a un grado i, mientras que si es irregular o con nódulos orienta a un grado mayor44.
Es conocido que los meningiomas presentan una alta densidad de receptores para somatostatina y esta cualidad permite el uso de la gammagrafía cerebral con octreótido para delinear la extensión de la enfermedad; también puede ser útil para el diagnóstico diferencial de otras lesiones extraaxiales (p. ej., metástasis, granulomas), con escasos falsos positivos. La formación de imágenes de octreótido con indio radiomarcado, o más recientemente galio, puede ser particularmente útil para distinguir residuo tumoral de cicatrización postoperatoria en meningiomas parcialmente resecados o recurrentes49,50.
Diagnósticos diferencialesComo diagnóstico diferencial del meningioma, debemos tener en cuenta diferentes etiologías6:
- 1.
Metástasis durales: suelen ser multifocales y con infiltración de la calota craneana.
- 2.
Hemangiopericitoma: puede ser indistinguible del meningioma. No suelen encontrarse calcificaciones ni hiperostosis, y sí erosión ósea y vacíos de flujo.
- 3.
Tumor fibroso solitario: muy infrecuente, indistinguible por neuroimágenes del meningioma.
- 4.
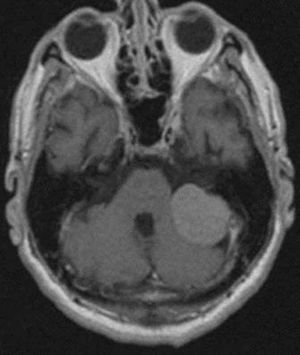
Neurinoma del acústico vs. meningioma del ángulo pontocerebeloso: el primero centrado en el CAI con o sin crecimiento extracanalicular. El meningioma es una masa excéntrica al poro acústico con base de implantación dural con o sin cola dural (fig. 7).
- 5.
Meningioma atípico o maligno: los diagnósticos diferenciales posibles son el osteosarcoma, el sarcoma de Ewing y el sarcoma meníngeo primario.
Cuando la lesión meningiomatosa está en una ubicación típica, con los hallazgos radiológicos característicos, el diagnóstico es relativamente sencillo. Sin embargo, existen un espectro de localizaciones y características morfológicas atípicas. Dada la naturaleza común de estas neoplasias, es importante tener presente estas características engañosas a fin de evitar diagnósticos erróneos4,42.
Edema peritumoral en meningiomasEn más de la mitad de los casos de meningiomas puede observarse un leve a moderado edema peritumoral. La dificultad diagnóstica surge cuando el edema vasogénico está fuera de proporción con el tamaño del meningioma. Existe controversia en cuanto a la causa del edema peritumoral asociado con meningiomas. Algunas teorías sugieren una lesión mecánica a través de la compresión directa, o de una lesión isquémica secundaria al compromiso de arterias corticales y/o participación de los senos durales. También se ha postulado la producción directa de líquido tumoral (figs. 2B, 3B y 8)27. La presencia de edema peritumoral adyacente a un meningioma no implica necesariamente la invasión intraaxial y no ayuda a graduar los meningiomas no invasivos5,27.
El VEGF es ampliamente conocido por ser un potente inductor de la permeabilidad vascular tumoral y es 1.000 veces más potente que la histamina en la inducción de la permeabilidad capilar27,51. Asimismo, el VEGF demostró ser un factor crítico en la formación del edema peritumoral cerebral en los meningiomas, el cual es una complicación más y desempeña un importante papel en la fisiopatología44,52,53.
Se ha sugerido que la expresión de VEGF y sus receptores Flt-1 (VEGFR1) y Flk-1 (VEGFR2) están involucrados en la progresión tumoral, además de incrementar la permeabilidad vascular y, subsecuentemente, el edema cerebral54. El edema peritumoral en los meningiomas responde pobremente a la terapia corticoidea55.
Anatomía patológicaLa mayoría de los meningiomas biopsiados y resecados corresponden al grado i (OMS). Ciertos subtipos histológicos se asocian a una evolución menos favorable y corresponden a grados ii y iii. La clasificación histopatológica se basa, en primera instancia, de acuerdo con el grado de atipia nuclear y la presencia de figuras mitóticas. Características adicionales incluyen hipercelularidad, aumento del índice núcleo-citoplasma, nucléolo prominente, crecimiento en empalizada y necrosis. Por definición, los subtipos histológicos atípicos, a células claras y cordoide, y aquellos con invasión de parénquima cerebral son clasificados como grado ii; los subtipos papilar, rabdoide y anaplásico (maligno) son clasificados como grado iii (tablas 2 y 3)3,56◊.
Tumores de las meninges (código OMS)
| Meningioma | 9530/0 |
| Meningotelial | 9531/0 |
| Fibroso (fibroblástico) | 9532/0 |
| Transicional (mixto) | 9537/0 |
| Psamomatoso | 9533/0 |
| Angiomatoso | 9534/0 |
| Microquístico | 9530/0 |
| Secretor | 9530/0 |
| Rico en linfoplasmocitosis | 9530/0 |
| Metaplásico | 9530/0 |
| Cordoide | 9538/1 |
| A células claras | 9538/1 |
| Atípico | 9539/1 |
| Papilar | 9538/3 |
| Rabdoide | 9538/3 |
| Anaplásico (maligno) | 9530/3 |
Tomado de Louis et al.3.
Meningiomas agrupados según grado (OMS) y riesgo de recurrencia tumoral
| Meningiomas con bajo riesgo de recurrencia y/o crecimiento agresivo | |
| Meningotelial | I |
| Fibroso (fibroblástico) | I |
| Transicional | I |
| Psamomatoso | I |
| Angiomatoso | I |
| Microquístico | I |
| Secretor | I |
| Rico en linfoplasmocitos | I |
| Metaplásico | I |
| Meningiomas con mayor probabilidad de recurrencia y/o comportamiento agresivo | |
| Atípico | II |
| A células claras (intracraneal) | II |
| Cordoide | II |
| Papilar | III |
| Rabdoide | II |
| Anaplásico (maligno) | III |
| Meningiomas de cualquier subtipo o grado con alto índice de proliferación (Ki 67) y/o invasión cerebral | |
Tomado de Perry et al.56.
En un estudio que analizó 368 muestras por inmunohistoquímica, los pacientes con un índice Ki67 ≥ 5% fueron significativamente más propensos a tener meningiomas atípicos y anaplásicos que aquellos pacientes con un índice Ki67<5%. Además, el porcentaje de pacientes con meningiomas con un índice Ki67 ≥ 5% fue mayor en los que presentaron meningiomas de la convexidad cerebral que aquellos con una ubicación fuera de esta. Esto indicaría que los meningiomas de la convexidad representan un factor de riesgo para meningiomas atípicos y anaplásicos57. Además, la actividad de telomerasa, que indica expansión clonal y potencial de crecimiento, se encontró en el 95% de los meningiomas atípicos y malignos. La frecuencia de positividad de la telomerasa es mucho menor en meningiomas benignos58,59.
Por otra parte, los meningiomas pueden expresar receptores de estrógenos y progesterona60,61. Los estudios de inmunohistoquímica mostraron que el 88% de los meningiomas expresan receptores de progesterona y el 40% receptores de estrógenos, casi un 40% receptores androgénicos y hasta un 60% receptores de prolactina61-63. Los meningiomas pueden modificar su tamaño durante la fase lútea del ciclo menstrual, como también durante el embarazo64.
El uso de hormonas exógenas por las mujeres pareciera no vincularse con el desarrollo de meningiomas65. Sin embargo, un estudio prospectivo sobre un millón de mujeres posmenopáusicas y en reemplazo hormonal mostró un riesgo levemente aumentado en comparación con quienes no recibieron tratamiento hormonal64. El riesgo en los hombres solo se observó con dosis altas y terapias a corto plazo (< 1 año)65. Con respecto al uso de anticonceptivos orales y meningiomas con receptores progesterona, continúa la controversia66.
Como fuera mencionado, el VEGF está relacionado con la angiogénesis y se observa incrementado con el aumento del grado tumoral. Los meningiomas de crecimiento rápido y los meningiomas anaplásicos tienden a expresar niveles más altos de VEGF que su contrapartida benignos, de crecimiento más lento67,68.
TratamientoLa resección neuroquirúrgica y el grado de la misma son el pilar del tratamiento y el predictor de progresión. Cuando esta es incompleta se observa recidiva a los 5 a 10 años, según la agresividad del tumor. La radiocirugía posoperatoria podría ser de ayuda en los pacientes con resección tumoral incompleta69.
En los meningiomas asintomáticos la viabilidad de la cirugía debe evaluarse cuidadosamente sobre la base del control clínico-neurológico y por neuroimágenes valorando la aparición de síntomas y el crecimiento tumoral; por ello, algunos autores recomiendan control periódico por neuroimágenes36,37,70. En los pacientes añosos, las mismas pueden efectuarse 2 o 3 meses luego del diagnóstico inicial, y si hay ausencia de malignidad, pueden realizarse controles cada 6 o 12 meses41.
La tarea del neurooncólogo está orientada al diagnóstico y el tratamiento de los síntomas, el control posterior a la neurocirugía y/o RT/quimioterapia y sus potenciales complicaciones3,50,56,60,71-73.
Tratamiento quirúrgico de los meningiomasEl tratamiento quirúrgico de un meningioma requiere de un balance entre el tratar definitivamente el tumor y evitar el daño neurológico del propio tratamiento. Así, factores específicos del paciente (edad, presencia o ausencia de síntomas, comorbilidades) y factores específicos del tumor (localización, tamaño, características histológicas del mismo) son importantes a la hora de determinar el tratamiento óptimo de un meningioma. De esa manera, la terapia inicial de un paciente con un meningioma de características benignas puede consistir en: a) cirugía; b) cirugía+RT; c) solo RT, y d) solo observación71,74.
Muchos pacientes con pequeños meningiomas asintomáticos pueden observarse de forma segura; se indica tratamiento solo si el tumor crece significativamente o se vuelve sintomático37,40,75.
Los meningiomas sintomáticos o asintomáticos que crecen, pacientes con edades ≤ 60 años, diámetro inicial ≥ 25mm, ausencia de calcificaciones, o los que infiltran o están asociados a edema a su alrededor, deberían ser resecados, si esto es posible34. Una resección completa es preferible cuando el meningioma se ubica en un área accesible, ya que la completa exéresis tumoral y de la inserción dural suelen proporcionar un tratamiento curativo74. Estudios observacionales han reportado que una resección completa, cuando es posible, está asociada significativamente con una sobrevida prolongada comparada con una resección parcial76-78.
Se sigue utilizando la graduación de Simpson (Simpson i-v) para describir la extensión de la resección quirúrgica76:
- –
Grado 1: resección completa, incluida la inserción dural y el hueso anormal.
- –
Grado 2: resección completa, con coagulación de la inserción dural.
- –
Grado 3: resección completa, sin resección o coagulación de la inserción dural.
- –
Grado 4: resección subtotal.
- –
Grado 5: solo descompresión tumoral.
El neurocirujano busca, habitualmente, una resección completa en tumores localizados en sitios como la convexidad, el surco olfatorio, el tercio anterior del seno sagital, al igual que algunos meningiomas del tentorio y la fosa posterior74. Sin embargo, para los meningiomas grado i de la OMS, al analizar el beneficio entre una resección Simpson 1 y 2, la diferencia podría ser insignificante. Por ello, ante un riesgo remoto pero posible de complicaciones (lesión vascular y cerebral, fístula del líquido cefalorraquídeo) al intentar remover el hueso hiperostótico y la duramadre adyacente, es preferible ser conservador79. Una resección subtotal es, en general, más apropiada para tumores menos accesibles, por ejemplo, los meningiomas localizados en la parte posterior del seno sagital, la región petroclival (fig. 9) o el tercio interno del ala del esfenoides74.
La mayoría de los meningiomas se pueden resecar en forma completa. Cuáles no: del seno cavernoso, 1/3 interno del ala del esfenoides (con invasión carotídea), petroclivales, parasagitales (con invasión del seno sagital) y meningiomas en placa. Entonces, en algunos casos la resección completa del meningioma es imposible y la recurrencia se produce en aproximadamente el 70% de los pacientes con resección subtotal seguidos por más de 15 años80.
Una biopsia o el tratamiento adyuvante sin diagnóstico histopatológico son realizados en casos muy selectos de tumores inaccesibles, como por ejemplo el meningioma del seno cavernoso74.
En general, los meningiomas son tumores vascularizados, por lo tanto, en algunos casos seleccionados, es necesario la utilización de embolización preoperatoria81-84. Sin embargo, desde un punto de vista de técnica quirúrgica, es importante comprender la irrigación arterial del tumor, principalmente producida por arterias meníngeas, para poder planificar correctamente el abordaje85.
En los casos con meningiomas del foramen magno (fig. 10), debido a la complejidad de la región, la terapéutica y la estrategia quirúrgica deberán decidirse según el caso35.
La incidencia de déficit neurológico postoperatorio varía entre el 2 y el 30%, y depende fundamentalmente de la localización del tumor y de la extensión de la resección74. La mortalidad varía ampliamente entre una serie y otra; sin embargo, podemos identificar los factores asociados a un aumento de la mortalidad:
- a.
Mala condición clínico-neurológica preoperatoria del paciente.
- b.
Compresión encefálica tumoral.
- c.
Edad avanzada.
- d.
Resección tumoral incompleta.
- e.
Hematoma intracraneano que requiere evacuación77.
La embolización preoperatoria endovascular de los meningiomas se utiliza desde hace más de 40 años86,87. Con cierta frecuencia, los meningiomas son embolizados preoperatoriamente con el objetivo de reducir el flujo sanguíneo tumoral a través de la eliminación de una o más arterias tributarias.
La embolización preoperatoria reduce88-90:
- –
La pérdida de sangre intraoperatoria.
- –
La necesidad de transfusión.
- –
El tiempo de la cirugía.
- –
Hace que el tumor sea más blando o friable.
- –
La resección es más sencilla y segura.
Generalmente, son embolizados aquellos meningiomas de tamaño grande y dependientes de la arteria carótida externa91. Sin embargo, el papel de la embolización preoperatoria para meningiomas es controvertido92. La práctica de la embolización de meningiomas varía significativamente en diferentes centros neuroquirúrgicos. En algunos hospitales, la embolización se realiza en todos los meningiomas que técnicamente sea posible; en otros lugares, la embolización se usa muy poco88. La tasa de complicaciones del procedimiento es del 4,3%93.
El momento de la cirugía después de la embolización varía de un día a más de una semana84,88,89,94,95. En la mayoría de los casos, la neurocirugía se realiza durante el mismo tiempo de estancia hospitalaria y dentro de las 72 h de la embolización.
Como norma general, podemos afirmar que la embolización preoperatoria de los meningiomas es efectiva para producir necrosis tumoral y mejorar los resultados de la cirugía en meningiomas intracraneales cuando puede realizarse de forma agresiva, obstruyendo la mayor parte de las arterias aferentes.
¿Qué pacientes se beneficiarían más con la embolización prequirúrgica?
- 1.
Tumores>de 5cm en general son de cirugía más dificultosa y por ello se beneficiarían más con la embolización.
- 2.
La localización en el ala del hueso esfenoides, fosa media craneana, paraselares o aquellos que comprometan senos durales o hueso.
- 3.
Irrigación del meningioma a partir de la carótida externa, en forma exclusiva o dominante.
- 4.
Hipervascularización mayor que en los tejidos adyacentes.
- 5.
Diámetro suficiente para el microcatéter y ausencia de irrigación a los pares craneanos o de la arteria carótida interna92,93,96.
En algunos casos, cuando el riesgo de la cirugía es muy alto o la hace no recomendable, se ha utilizado como tratamiento primario; se han descripto mejorías o alivio de los síntomas tras la embolización y también disminución en la recurrencia tumoral78,84,97-100.
Finalmente, es importante tener en cuenta que los meningiomas embolizados antes de la resección pueden cambiar su apariencia microscópica y hacer más difícil el análisis histológico. Los cambios isquémicos y citológicos asociados luego de la embolización pueden confundir con la histopatología observada en los meningiomas de más alto grado101.
Tratamiento radiante de los meningiomasRadioterapiaEl papel de la RT en el tratamiento de los meningiomas depende de factores asociados al paciente, como las comorbilidades y su preferencia, y factores asociados al tumor, como el tamaño tumoral, la resecabilidad y particularmente el grado histológico. La RT se recomienda, generalmente, en los meningiomas luego de una cirugía inicial (adyuvante), o como tratamiento único en los irresecables102. También luego de una resección de un meningioma maligno (grado iii de la OMS), porque la supervivencia libre de progresión a 5 años es de 80% comparado con la cirugía sola (15%)103. La RT ha demostrado reducir la carga tumoral además de prevenir la recurrencia104,105.
En los meningiomas atípicos (grado ii de la OMS), el tiempo óptimo de la RT no está del todo claro, especialmente luego de una resección completa. Estudios retrospectivos han demostrado que la RT adyuvante temprana en los meningiomas («no benignos») mejora la supervivencia libre de progresión, pero la mayoría evaluó a pacientes con meningiomas grado ii y iii conjuntamente, y el beneficio podría deberse a un sesgo en la selección103,106-108. Los objetivos del tratamiento evolucionaron, buscando optimizar los resultados funcionales y minimizar la toxicidad relativa al tratamiento; así, se prefiere «la observación» luego de una resección macroscópica completa de un meningioma grado ii. Si la resección fue incompleta y/o ante una recurrencia, se pueden ofrecer distintas opciones de tratamiento radiante, que incluyen la radiocirugía y la RT fraccionada, dependiendo del tamaño tumoral y su localización109.
Para los meningiomas grado i de la OMS, existe una controversia aún mayor; las opciones incluyen observación, cirugía sola, radiocirugía sola, RT fraccionada sola o la combinación de cirugía con radiocirugía postoperatoria o RT fraccionada. Luego de una resección, puede optarse entre la RT temprana o posponer la misma hasta la recurrencia. Los datos apoyan, para un mejor control local, la RT adyuvante inmediata en comparación con la cirugía sola, especialmente luego de una resección parcial110. En contraste, una RT que se pospone hasta la recurrencia puede ayudar a evitar la toxicidad de la RT en una proporción de pacientes que no experimentarán recurrencia111.
RadiocirugíaLa radiocirugía puede entregarse con diferentes dispositivos, incluyendo el Gamma Knife, CiberKnife y un acelerador lineal69. Generalmente se utilizan dosis o fracciones únicas con una dosis marginal de 10 a 15 Gy112,113. Estas técnicas se ofrecen a pacientes con tumores pequeños y que no se encuentren en la proximidad de estructuras críticas como el quiasma óptico114.
En un estudio multicéntrico con 254 pacientes con meningiomas petroclivales tratados de inicio con radiocirugía (140 pacientes) o con radiocirugía después de la cirugía (144 pacientes), las tasas de supervivencia libre de progresión fueron de 93 y el 84%, a 5 y 10 años, respectivamente115.
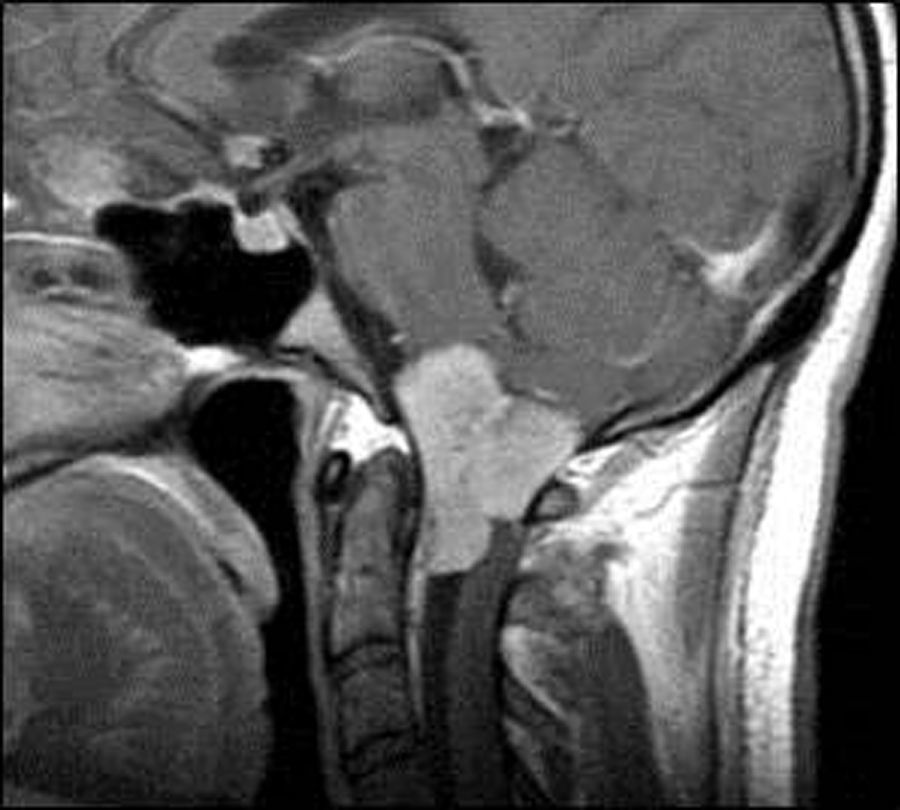
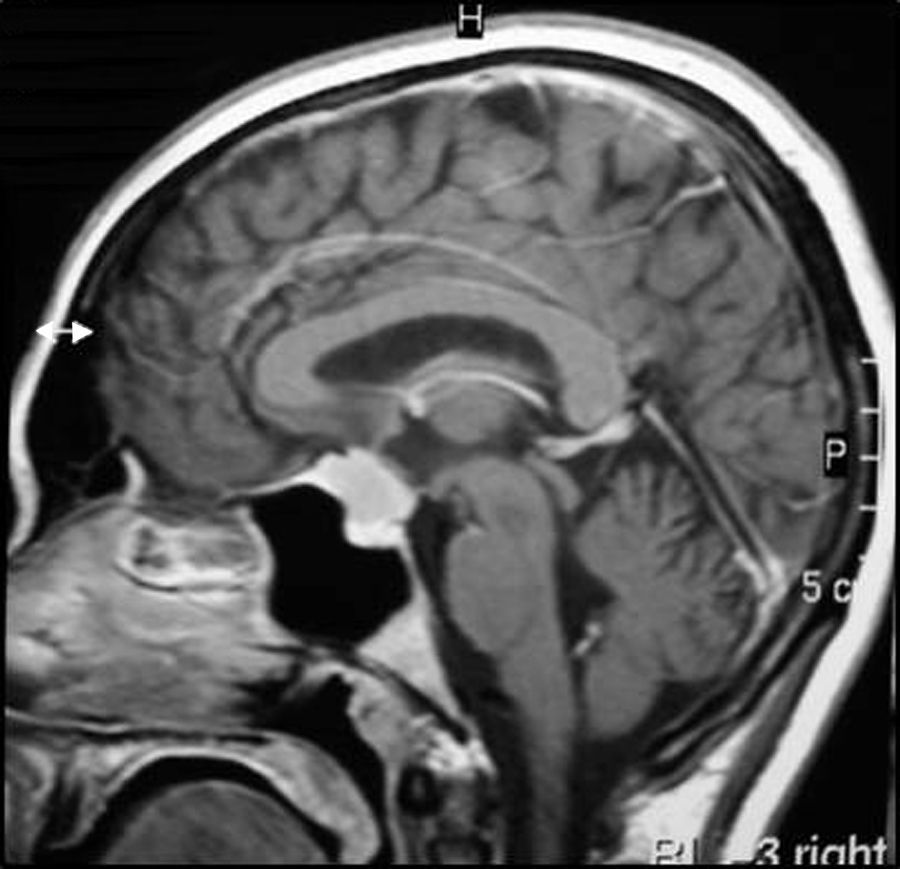
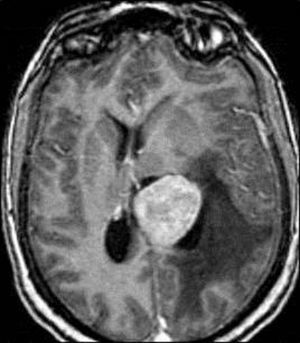
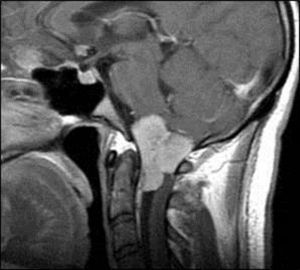
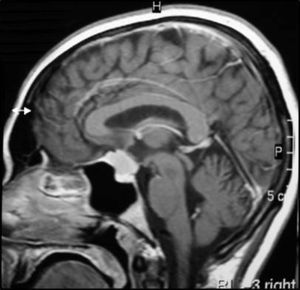
Asimismo, para meningiomas selares y paraselares (fig. 11), aplicando radiocirugía con una dosis media de 13Gy (rango de 5 a 30Gy), se obtuvo un control tumoral similar, con tasas de supervivencia libre de progresión a 5 y 10 años del 95 y el 92%, respectivamente116.
Radioterapia fraccionadaLa RT fraccionada se puede entregar con técnicas estereotácticas o guiada por imágenes para optimizar la precisión de la RT, entregada en combinación con técnicas de intensidad modulada para mejorar la conformación de la dosis alrededor de blancos complejos en proximidad de estructuras normales críticas69,117. En los meningiomas benignos, la RT fraccionada se utiliza para tumores de gran volumen o para aquellos que se encuentran muy cercanos a estructuras críticas, como el quiasma óptico. El volumen a tratar consiste en todo el tumor que realce con el contraste, con un mínimo de margen. La dosis varía entre 50 y 56Gy en fracciones de 1,8 o 2Gy/día. Con una mediana de seguimiento de 43 meses (rango entre 2 y 144 meses), Solda et al. reportaron tasas de control local muy similares para RT fraccionada como para radiocirugía, el 93 y el 86% a 5 y 10 años, respectivamente117. Para meningiomas de alto grado existe una gran preocupación por la posibilidad de extensión al parénquima cerebral; por esto, al blanco terapéutico se le agrega un margen adicional de entre 1 y 2cm por la posibilidad de diseminación microscópica. Por la mayor agresividad biológica, en los meningiomas de alto grado se requieren dosis mayores, en el rango de 60 a 66 Gy103,117,118.
Tratamiento farmacológicoUna variedad de fármacos han sido estudiados para el tratamiento de los meningiomas. Estos incluyen hidroxiurea, temozolomida, irinotecan, interferón-α, mifepristona, análogos del octreótido, acetato de megestrol, bevacizumab, sunitinib, vatalinib, imatinib, erlotinib y gefitinib. Desafortunadamente, la mayoría de estos agentes no han mostrado ninguna o muy poca actividad en el tratamiento de los meningiomas. Sobre la base de una reciente y amplia revisión de la literatura, solo bevacizumab, sunitinib y vatalinib han mostrado una potencial actividad clínicamente relevante119.
Ciertamente, los agentes antiangiogénicos parecen una oportunidad para proporcionar un tratamiento racional hacia los meningiomas120; ejemplo de ello es la regulación positiva de las vías angiogénicas repetidamente descriptas en estos tumores121-123.
El vatalanib es un inhibidor oral de VEGFR1 (Flt-1), VEGFR2 (KDR) y VEGFR3 (Flt-4), y tiene propiedades antiangiogénicas. Este fármaco se administró por vía oral a pacientes con meningioma con una dosis de 500mg 2 veces al día, todos los días y por tiempo prolongado124.
Sunitinib es un inhibidor de la tirosina-cinasa con blanco en los receptores de VEGF, los receptores de los factores de crecimiento derivado de las plaquetas (PDGFR) y c-KIT. Se administra por vía oral en pacientes con tumores meníngeos, con una dosis de 50mg/día durante 4 semanas de cada 6 semanas (descansa 2 semanas)125.
El bevacizumab es un anticuerpo monoclonal humanizado que inhibe el VEGF. Tiene una marcada actividad contra el edema peritumoral con mejoría de los síntomas producidos por este, y con menor requerimiento de corticoides, hecho observado en diversos tipos tumorales, entre estos los gliomas, las metástasis cerebrales y meningiomas. La dosis es de 5-10mg/kg IV c/2 semanas o 15mg/kg IV c/3 semanas126-128.
Si el meningioma crece rápidamente, y los meningiomas anaplásicos son más vascularizados y expresan niveles más altos de VEGF, la respuesta al tratamiento con bevacizumab de algunos meningiomas parece lógica, ya que este anticuerpo monoclonal es un anticuerpo anti-VEGF y, por ende, produce el bloqueo de la angiogénesis.
Wilson et al. comunicaron un caso con resección subtotal de un meningioma grado i de ubicación en seno cavernoso izquierdo, que recibió tratamiento con paclitaxel y bevacizumab. Al año de iniciado el tratamiento combinado, la RM cerebral mostró regresión del meningioma. Un nuevo control un año después de la regresión, la regresión se mantuvo estable129.
Corresponde aclarar que los estudios clínicos que utilizaron vatalanib y sunitinib fueron con pocos pacientes, de fase 2 y con meningiomas refractarios. Respecto del bevacizumab, es simplemente una revisión retrospectiva. El uso de cualquiera de estos fármacos en meningiomas es off label y su uso se debería considerar solamente en casos refractarios y luego de una discusión caso por caso.
La identificación de un régimen farmacológico efectivo en los meningiomas sería un avance significativo en el arsenal terapéutico disponible para los pacientes y los médicos que deben lidiar con el tipo tumoral más frecuente del sistema nervioso.
PronósticoLa recurrencia y la progresión tumoral dependen de las características individuales del tumor, así como de las modalidades y los resultados de los tratamientos aplicados.
La histología predice la mortalidad y la recurrencia; se han reportado tasas de recaída en el grado i de la OMS (benignos)/ii (atípicos)/iii (malignos) del 7, el 40 y el 80%, respectivamente, y la media de supervivencia en estos estudios fue>10, 11,5 y 2,7 años, respectivamente130,131. Es de destacar que, incluso en ausencia de los criterios celulares de grado ii, la invasión cerebral califica para el grado ii de la OMS, porque las tasas de recurrencia y mortalidad son similares a los meningiomas atípicos132. También los meningiomas que se presentan con invasión ósea muestran peores resultados en comparación con los tumores no invasores130.
Los tumores grado iii de la OMS que incluyen los meningiomas malignos son más invasivos y tienen mayor recurrencia local luego del tratamiento inicial, incluyendo aquellos con resección «completa». El pronóstico empeora cuanto más indiferenciado es el tumor133,134. La tasa mitótica elevada y un pobre Karnofski son factores pronósticos significativos135. Esto conduce a una supervivencia más corta en comparación con los pacientes con tumores grado i y ii.
En un estudio de 1.098 pacientes tratados quirúrgicamente, 40 fueron clasificados como atípicos y 24 como anaplásicos. Las tasas de supervivencia a 10 años y de supervivencia libre de recurrencia para los pacientes con tumores atípicos grado ii de la OMS fue del 90 y el 87%, respectivamente. En contraste, los pacientes con tumores anaplásicos grado iii de la OMS, las tasas de supervivencia libre de recurrencia a 3 y 5 años fueron del 50 y el 29%, respectivamente131.
Aparte del grado tumoral de la OMS, la antigüedad y la extensión de la resección (véase el apartado Tratamiento quirúrgico) también representan factores pronósticos importantes76,136.
La resección de Simpson grado 1 se puede realizar de forma fiable en los meningiomas de la convexidad y, con independencia de los hallazgos histológicos malignos, puede mejorar el pronóstico78,133. El pronóstico es también peor para tumores con resección subtotal en comparación con los resecados por completo. En un estudio de 581 pacientes, las variables: edad<40 años, sexo masculino, la resección subtotal y un alto índice mitótico se asociaron de forma independiente con una menor supervivencia libre de progresión78. Sin embargo, aunque muchos pacientes con meningiomas grado i completamente resecados pueden ser considerados como curados, se han observado recidivas tardías incluso después de 20 años137.
Por otra parte, un estudio de seguimiento sobre los meningiomas incidentales no operados mostró que el 26% de los tumores de la base del cráneo mostraron una tasa de crecimiento relativo del 6,8% por año, mientras que el 95% de los tumores que no son de la base del cráneo crecen más rápidamente con una tasa de crecimiento relativo del 13,8%/año, con un tiempo promedio de observación de 49 meses138. En línea con esta observación, otro estudio cohorte de 378 meningiomas operados (82% grado i de la OMS, de los cuales el 56% estaban localizados en la base del cráneo y 44% fuera de la base del cráneo) mostró que los pacientes con lesiones fuera de la base del cráneo eran significativamente más propensos a tener meningiomas atípicos o malignos139.
Para entender mejor las diferencias pronósticas entre los meningiomas atípicos y malignos, y la influencia de la extensión de la extirpación quirúrgica en el postoperatorio, se estudiaron 42 casos con meningiomas atípicos y 29 pacientes con meningiomas malignos. La supervivencia de los meningiomas atípicos y malignos a los 5 y 10 años fue del 95 y el 79%, y el 64,3 y el 34,5%, respectivamente. La supervivencia libre de recurrencia y la media de tiempo hasta la recurrencia también fueron significativamente más extensas en pacientes con meningiomas atípicos que en los pacientes con tumores malignos: 11,9 vs. 2 años y 5 vs. 2 años, respectivamente. Seis de los meningiomas atípicos (26%) se malignizaron. La resección grado 1 de Simpson y la ubicación en la convexidad cerebral, estrechamente relacionadas, se asociaron con un curso clínico significativamente mejor en toda la serie. Después de una resección quirúrgica subtotal, los pacientes con meningiomas atípicos tuvieron una mejor evolución que los pacientes con meningiomas malignos, pero la diferencia no fue estadísticamente significativa. Este estudio demostró que la extirpación completa y los hallazgos histológicos estuvieron significativamente relacionados con una supervivencia prolongada133. En otro estudio, el análisis multivariado determinó que la edad<60 años, la resección quirúrgica completa, y el grado histológico ii (vs. grado iii) fueron factores pronósticos independientes de supervivencia140.
Otro estudio analizó las terapias combinadas para los meningiomas grados ii y iii y abordó el papel de la RT adyuvante después de la resección quirúrgica de estos tumores. En los meningiomas grado iii se observó una tendencia hacia una mayor supervivencia en comparación con los tratados solo con cirugía141.
Respecto de los marcadores de proliferación Ki-67 y el índice MIB-1, estos se correlacionan con el grado tumoral de la OMS y, por lo tanto, con el pronóstico142. En un estudio que incluyó 60 casos de meningiomas grado i de las OMS, la invasión ósea y de tejidos blandos, la expresión de p53 y un índice de proliferación Ki-67 elevado identificaron meningiomas con características histológicas benignas pero con evolución clínica desfavorable143. La frecuencia de positividad de la telomerasa es mayor en los meningiomas grados ii y iii58,59. Los meningiomas benignos telomerasa-positivos pueden mostrar recurrencia temprana, incluso después de la resección completa58.
También la expresión de los receptores de hormonas sexuales se correlaciona con el grado tumoral y afectan el pronóstico. Los receptores de progesterona son más frecuentes en los meningiomas benignos y se corresponden con una tasa de recurrencia media del 5%. Los meningiomas que expresan receptores de estrógenos, o tumores que carecen de receptores de hormonas sexuales, pertenecen con mayor frecuencia a los grados ii y iii de la OMS y se asocian con tasas de recurrencia de hasta el 30%144.
En conclusión, los factores pronósticos descriptos pueden ayudar a planificar una mejor estrategia de tratamiento a través de la embolización, la cirugía, la RT y farmacológico.
Meningioma y maternidadLa incidencia de meningiomas durante el embarazo es baja, pero aumenta con la edad, y en la actualidad las mujeres suelen posponer el deseo de embarazo para edades más avanzadas145. Los meningiomas pueden aumentar su tamaño en el curso del embarazo64.
Los cambios hormonales y hemodinámicos del embarazo pueden acelerar el crecimiento tumoral. El mecanismo podría explicarse por la retención de líquidos, la congestión vascular, los cambios hormonales y los factores de crecimiento; posterior al parto, puede observarse alguna mejoría. Estudios observacionales mostraron un crecimiento anual de 2,4-3,6mm, y muchos autores no recomiendan tratamientos en meningiomas asintomáticos146-151.
El tratamiento debe ser individualizado considerando el estado clínico de la paciente y sus deseos, la edad gestacional y el tamaño tumoral151.
Durante el embarazo no se recomienda realizar una neurocirugía durante el primer trimestre, para así disminuir el riesgo de aborto; el procedimiento se considera «seguro» durante el segundo y tercer trimestre145.
La neurocirugía de urgencia se reserva para los casos de hidrocefalia activa, signos de herniación o de déficit neurológico progresivo; en estos casos, el riesgo de muerte materna no está aumentado en relación a las mujeres no embarazadas152,153.
La decisión de realizar una cesárea electiva pretérmino se basa en el riesgo de aumento de la presión intracraneana y la necesidad de disminuir la fuerza realizada durante la segunda etapa del parto147. De todas maneras, si la paciente se encuentra clínicamente estable y luego de una cuidadosa discusión sobre los riesgos y el crecimiento tumoral, en casos seleccionados se puede considerar llevar el embarazo a término, así como un eventual parto vaginal145-151.
Los tiempos de los diferentes tratamientos deben ser considerados en cada caso individual por un equipo multidisciplinario, basado en la evidencia científica y en la experiencia145.
ConclusiónLos meningiomas son los tumores intracraneanos más frecuentes del SNC y en su gran mayoría son benignos. La radiación ionizante es el único factor de riesgo reconocido como causante de meningiomas.
Debido a la falta de ensayos prospectivos, es muy difícil desarrollar guías de tratamiento estándar. Siempre que sea posible, la exéresis completa es la conducta de elección seguida de observación. Existe controversia respecto al tratamiento adyuvante luego de una resección subtotal, particularmente si realizar el mismo inmediatamente, o a la progresión. La radiocirugía como la RT externa puede ser una alternativa en la mayoría de los casos.
El tratamiento farmacológico queda relegado para pacientes en progresión luego de cirugía y RT.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
A la Sra. Agustina Casas, por la edición de las imágenes.
En el momento de la publicación de este trabajo, la OMS publicó la nueva clasificación de los tumores del Sistema Nervioso Central (2016). La tabla con la nueva clasificación de meningiomas está disponible en www.sna.org.ar (grupo de trabajo de Neurooncología).