En ausencia de hechos clínicos o de una prueba diagnóstica específica, el diagnóstico de esclerosis múltiple continúa basándose en criterios que incluyen la demostración de lesiones en el sistema nervioso central diseminadas en tiempo y espacio y en la exclusión de otros diagnósticos alternativos.
ObjetivosEfectuar consideraciones acerca de los criterios de diagnóstico vigentes para esclerosis múltiple.
DesarrolloLos criterios de McDonald en su revisión 2005 fueron diseñados con el objetivo de simplificar y acelerar el diagnóstico, y son los más utilizados en la actualidad tanto para la práctica clínica como para la inclusión de pacientes en estudios de investigación. La resonancia magnética es la herramienta paraclínica más importante dentro de los actuales criterios de diagnóstico, aportando evidencias para la demostración de la diseminación en el tiempo y en el espacio. La presencia de bandas oligoclonales y/o un incremento en el índice IgG en el líquido cefalorraquídeo, así como anormalidades en los potenciales evocados, representan herramientas menos consideradas en estos criterios.
ConclusionesSi bien los criterios de mantienen una adecuada sensibilidad y especificidad, pueden inducir una sobrestimación del valor de la resonancia magnética que lleve al error diagnóstico o a un sobrediagnóstico de la enfermedad. La identificación de “banderas rojas”, tanto clínicas como de imágenes, puede alertar al clínico sobre la posibilidad de un diagnóstico alternativo y por lo tanto complementar los criterios para, de este modo, alcanzar un diagnóstico más preciso y fiable.
In the absence of clinical features or a specific diagnostic test, the Multiple Sclerosis diagnosis is still based on criteria that include the demonstration of lesions in the Central Nervous System disseminated in time and space and the exclusion of alternative diagnoses.
ObjectiveMake considerations about the current diagnostic criteria for Multiple Sclerosis.
MethodsThe 2005 Revision of McDonald Criteria, which were designed with the objective of simplifying and accelerating the diagnosis, are currently the most frequently used both in clinical practice and in the inclusion of patients in clinical trials. Magnetic Resonance Image (MRI) is the most important paraclinical tool in the current diagnostic criteria, providing evidence for the demonstration of dissemination in time and space. The presence of oligoclonal bands and/or the increase in the IgG index in cerebrospinal fluid as well as Evoked Potential abnormalities represent less considered tools in these criteria.
ConclusionsAlthough McDonald Criteria maintain an adequate sensibility and specificity, an overestimation of the importance of MRI results may lead to misdiagnosis or overdiagnosis of the disease. The identification of both clinical and imagenological “red flags” can warn the physician about complementing the criteria in order to reach a more accurate and reliable diagnosis.
La esclerosis múltiple (EM) es una enfermedad progresiva que afecta al sistema nervioso central (SNC) y se inicia en etapas tempranas de la adultez1. En los últimos años se han producido avances muy importantes en el conocimiento de las bases fisiopatológicas y también en el tratamiento de esta enfermedad. Sin embargo, ante la ausencia de una prueba diagnóstica específica, el diagnóstico de esta entidad continúa basándose en “criterios" que brindan pautas o guías para avanzar en el problema, pero no lo resuelven de manera definitiva. Por otra parte, la disponibilidad de tratamientos, aunque parcialmente eficaces, determina la necesidad de llegar a un diagnóstico de la forma más precisa y precoz posible.
El diagnóstico de EM se realiza fácilmente, por lo general en adultos jóvenes con manifestaciones clínicas recurrentes referidas a diferentes áreas del SNC. Resulta más difícil en aquellos pacientes con inicio reciente de su enfermedad o que se presentan con un curso progresivo desde el comienzo.
Las dificultades existentes en el diagnóstico de EM se ven reflejadas en que aún hoy, a pesar de los adelantos en métodos complementarios, la demora en alcanzar un diagnóstico se mantiene entre 4 y 5 años. Este es un tiempo considerable si tenemos en cuenta que el pronóstico de la enfermedad en cuanto a discapacidad se determina justamente en los primeros años de evolución. Sabemos actualmente que el daño axonal y la atrofia se manifiestan desde el comienzo de la enfermedad y conforman el sustrato mismo de la discapacidad2,3.
Criterios de diagnósticoEl diagnóstico de EM ha sido una verdadera preocupación para los pacientes y para los médicos. Para los primeros porque el diagnóstico preciso permite superar un periodo de incertidumbre y prepararse para enfrentar una enfermedad crónica con un significativo impacto en muchos aspectos de la vida. Para los segundos porque la ausencia de una prueba diagnóstica específica suele resultar en un arduo proceso en búsqueda de evidencias en favor y en contra de la enfermedad. A lo largo de los años, y de acuerdo con el conocimiento y las disponibilidades diagnósticas, se han ido elaborando pautas o criterios en un intento de sistematizar el diagnóstico de EM. Un número de criterios formales han sido desarrollados con el fin de unificar conceptos en torno a determinar qué es EM y qué no.
A partir de los criterios de Schumacher4, conceptos considerados esenciales para el diagnóstico son la demostración de dos o más lesiones en el SNC diseminadas en el tiempo y en el espacio, y la necesidad de excluir otras patologías que puedan manifestarse con un cuadro clínico similar.
En 1983 fueron diseñados los criterios de Poser5, que estuvieron vigentes durante casi 20 años y que aún hoy siguen siendo considerados. Si bien estos criterios fueron establecidos para ser implementados en ensayos clínicos, también se utilizaron para la práctica clínica. Evidencias paraclínicas como los potenciales evocados y la neuroimágenes fueron consideradas como herramientas diagnósticas, del mismo modo que la presencia de bandas oligoclonales (BOC) en el líquido cefalorraquídeo (LCR) o la producción intratecal de IgG. A pesar de que estos criterios resultan confusos en algunas áreas y han sido criticados, su enorme aporte al diagnóstico de la EM no puede ser ignorado.
Los criterios de McDonald 2001 y la revisión 2005En julio de 2000 un Panel Internacional liderado por Ian McDonald se reunió bajo el auspicio de la National Múltiple Sclerosis Society y la Múltiple Sclerosis International Federation con el objeto de revisar los criterios de diagnóstico de EM y adecuarlos a los progresos realizados en esa área. Los resultados fueron publicados en julio de 20016.
Los principales objetivos del Panel fueron crear criterios diagnósticos que pudieran ser utilizados por los neurólogos en su práctica cotidiana y que pudieran, además, adaptarse para su implementación en ensayos clínicos. Otros objetivos fueron lograr la integración de la resonancia magnética (RM) en el esquema diagnóstico e incluir criterios de diagnóstico para EM primaria progresiva (EMPP) que no estaban contemplados en los criterios de Poser.
Desde su aparición en 2001, los criterios de McDonald han sido ampliamente utilizados y también sujetos a evaluaciones y debates acerca de su utilidad y practicidad de implementación. En los últimos años han aparecido distintas publicaciones confirmando la posibilidad de efectuar un diagnóstico de EM de una forma más precoz y con un adecuado nivel de sensibilidad y especificidad7,8. Del mismo modo, otras publicaciones apuntaron a efectuar eventuales modificaciones a partir de optimizar los criterios de imágenes y de reevaluar el papel del LCR para el diagnóstico de la EMPP9,10. Basados en estos conceptos, un Panel Internacional se reunió en marzo de 2005 con el objeto de adecuar los Criterios de McDonald a los nuevos conocimientos en el terreno del diagnóstico de la EM.
Estos últimos criterios, conocidos como Revisión 2005 de los Criterios de McDonald11, establecen que para sostener un diagnóstico de EM se mantiene el concepto de eventos separados en el tiempo y en el espacio con la condición de que no exista una mejor posibilidad diagnóstica. La utilidad de los potenciales evocados (PE) (a excepción del visual) y del estudio del LCR, salvo para el caso de la forma primaria progresiva, resultan menos relevantes. Por el contrario, la RM como herramienta diagnóstica alcanza una importancia significativa hasta llegar a considerarse casi como un sustituto del ataque clínico.
Los criterios de McDonald presentan 5 escenarios con sus correspondientes requerimientos a cumplir para alcanzar un diagnóstico de EM. De acuerdo con el grado de satisfacción de dichos requerimientos se concluirá que el paciente padece efectivamente EM cuando se cumplen la totalidad de los requisitos, o se trata de una “EM posible” en el caso de que no se cumplan totalmente los requisitos o se requieran más estudios con persistencia de un elevado índice de sospecha de la enfermedad. Por último, se define como “no EM” al paciente que no cumple criterios de diseminación en tiempo y espacio o presenta un mejor diagnóstico alternativo.
El Panel McDonald propone una serie de definiciones con el objetivo de unificar conceptos a los fines del diagnóstico.
Ataque clínico (recaída o exacerbación)Episodio de disturbios neurológicos del tipo de los vistos en la EM, cuando estudios clínico-patológicos establecen una causa inflamatoria y desmielinizante en su origen. La duración de los síntomas no debe ser menor de 24 horas y la confirmación de una recaída requiere de la objetivación de cambios clínicos. El reconocimiento de ataques separados requiere de 30 días desde el inicio del primer evento y el inicio del segundo. Un pseudoataque se reconoce por la agravación de signos y síntomas previos, determinado por la presencia de infección o hipertermia y su reconocimiento tiene implicancias terapéuticas.
Anormalidades en estudios paraclínicosResonancia magnéticaEl uso de esta herramienta diagnóstica para la determinación de diseminación en el tiempo y el espacio constituye un elemento clave de los criterios de McDonald en su revisión 2005.
Para la diseminación en el tiempo (tabla 1) se consideran dos formas que demuestran diseminación en tiempo a través de las imágenes:
- 1.
Detección de refuerzo con el gadolinio al menos tres meses después del comienzo del evento clínico inicial y con una topografía diferente a la de dicho evento.
- 2.
La presencia de una nueva lesión en T2, ocurrida en algún momento después del estudio referencial efectuado al menos 30 días después del inicio del cuadro clínico, también es considerada suficiente para sostener un criterio de imágenes de diseminación en tiempo. Esta nueva lesión en T2 deberá ser suficientemente consistente en cuanto a tamaño, localización y características para ser aceptada como tal, debiéndose tener en cuenta además aspectos técnicos (artificios, características del corte) que pudieran inducir a errores de apreciación. Por estas razones, el Panel recomienda la evaluación de las imágenes por parte de un profesional con adecuada experiencia, así como la implementación de estudios debidamente estandarizados.
Criterios de diseminación en tiempo (McDonald - revisión 2005)
|
Para demostrar la presencia de criterios de diseminación en el espacio por imágenes (tabla 2) deben cumplimentarse tres de los siguientes 4 criterios: a) la presencia de una lesión que refuerza con gadolinio o 9 lesiones hiperintensas en T2 si no existe una lesión que refuerza; b) al menos una lesión infratentorial; c) al menos una lesión yuxtacortical; d) al menos tres lesiones periventriculares. Adicionalmente, una lesión espinal puede ser considerada equivalente a una lesión cerebral infratentorial; una lesión espinal que refuerza es considerada equivalente a una lesión cerebral que refuerza y lesiones medulares pueden contribuir, junto con lesiones cerebrales, a alcanzar el número requerido de lesiones en T2.
Criterios de diseminación en espacio para resonancia magnética (McDonald - revisión 2005)
Tres de los siguientes cuatro criterios
|
Una lesión espinal puede ser considerada equivalente a una lesión cerebral infratentorial; una lesión espinal que refuerza es considerada equivalente a una lesión cerebral que refuerza y lesiones medulares pueden contribuir, junto con lesiones cerebrales, a alcanzar el número requerido de lesiones en T2.
Los criterios de McDonald 2005 continúan basándose en los estudios de Barkhof y Tintoré12,13 para la determinación de criterios de diseminación en el espacio por imágenes; sin embargo, reconsidera el valor de la RM espinal proponiendo una guía relacionada con las lesiones medulares:
- 1.
Las lesiones medulares pueden resultar de gran utilidad para el diagnóstico diferencial de EM14.
- 2.
En un paciente con diagnóstico probable de EM con imágenes encefálicas que no califican para diseminación en espacio, la presencia de imágenes medulares con características típicas de EM resulta de gran utilidad9–15.
- 3.
Una lesión medular es equivalente y puede sustituir a una lesión cerebral infratentorial, pero no a una periventricular o yuxtacortical. Una lesión medular que realza con gadolinio es equivalente a una lesión que realza en el encéfalo, además de ser también considerada como una lesión infratentorial. El número de 9 lesiones en T2 requerido puede ser alcanzado por la sumatoria de lesiones tanto encefálicas como medulares.
- 4.
Las lesiones medulares deberán ser focales. A pesar de aceptarse la posibilidad de cambios de señal difusos en la médula, en especial en EMPP, estas no son consideradas suficientemente fiables para ser incorporadas en los criterios de diagnóstico.
- 5.
A efectos de demostrar diseminación en tiempo, sólo se recomienda la reiteración de RM en búsqueda de lesiones medulares ante la presencia de eventos clínicos que permitan sospechar cambios a ese nivel.
De este modo, la Revisión 2005 de los criterios de McDonald parece ubicar en un plano más apropiado la RM espinal, reconociendo su valor como elemento diagnóstico y también al momento de considerar diagnósticos diferenciales.
En 2006, un estudio realizado por Swanton et al en pacientes con un primer episodio clínico o síndrome clínicamente aislado (SCA) propuso nuevos criterios de diagnóstico para RM que podrían resultar más fáciles de aplicar en la práctica clínica16. Este estudio considera como evidencia de diseminación en el tiempo la sola presencia de una nueva lesión en T2 en una RM de seguimiento, independientemente del momento en que se haya efectuado el estudio basal. La evidencia de diseminación en el espacio lo constituye la presencia de al menos una lesión asintomática en T2 en, como mínimo, 2 de 4 localizaciones características (periventricular, yuxtacortical, fosa posterior, espinal). Estos nuevos criterios de imágenes no requieren la administración de gadolinio, ya que los autores consideran que esto implica menores costes y una mayor seguridad para el paciente y que, además, lesiones que refuerzan con gadolinio sólo implican actividad y no localización. Sin embargo, un aspecto negativo de la no utilización de gadolinio lo constituye una cierta pérdida en la posibilidad de efectuar diagnósticos diferenciales. Los criterios de Swanton demostraron poseer una mayor sensibilidad en relación con los criterios de McDonald 2005 (72 frente a 60%) mientras que mantienen una similar alta especificidad (87 frente a 91%)17. Deberá notarse que los criterios de McDonald y Swanton para RM han probado utilidad para suministrar un diagnóstico fiable de EM durante el primer año después del inicio de un SCA y no a partir de un examen retrospectivo de casos de EM definida18.
Líquido cefalorraquídeoLas anormalidades encontradas en el LCR resultan la evidencia de un compromiso inmune e inflamatorio en el SNC. Las mismas consisten en el hallazgo de BOC de IgG, las cuales deberán ser evaluadas preferentemente utilizando la técnica de enfoque isoeléctrico, y deberán hallarse sólo en LCR y no en suero19. En la EM clínicamente definida (EMCD) se demostró que en más del 90% de los pacientes es posible identificar BOC cuando se utiliza enfoque isoeléctrico20. De manera adicional una elevación en el índice de IgG resulta un dato con similar significación. Asimismo, puede existir pleocitosis linfocitaria, que no debería exceder de los 50 elementos por milímetro cúbico. La presencia de un LCR anormal, con las características descritas, puede resultar de utilidad para alcanzar un diagnóstico de EM como complemento de la RM para la evidencia de diseminación en el espacio en el caso de un SCA, y eventualmente en apoyo del diagnóstico de EMPP11. De igual modo, un estudio de LCR puede ser necesario ante la presencia de imágenes que se prestan a dudas o pierden especificidad (individuos mayores de 50 años) o en caso de cuadros neurológicos atípicos.
Potenciales evocados visualesLa utilización de los PE en el diagnóstico de la EM tiene como objetivo básico evidenciar manifestaciones subclínicas de la enfermedad. Los criterios de McDonald sólo consideran como elemento diagnóstico neurofisiológico a los PE visuales (PEV)21. El hallazgo de una onda prolongada con buena conformación se considera una información suplementaria a la clínica para proveer de evidencia objetiva de una segunda lesión.
Esquemas diagnósticosLos criterios de McDonald analizan las distintas posibilidades diagnósticas que pudieran llegar a presentarse, y consideran los pasos a seguir para llegar a un diagnóstico de EM. Se consideran 5 presentaciones clínicas de menor a mayor complejidad (tabla 3).
- 1.
Dos o más ataques; evidencia clínica objetiva de 2 o más lesiones. La presencia de dos o más ataques separados en el tiempo y el espacio resultarán evidencia suficiente para sostener un diagnóstico clínico de EM. Si bien no se requieren estudios adicionales, se trata de un escenario diagnóstico que puede plantear dudas con otras entidades que también presentan evidencia de diseminación temporoespacial. Por esta razón el Panel recomienda la implementación de algún estudio adicional y tener en cuenta la ausencia de una mejor explicación para sostener el diagnóstico.
- 2.
Dos o más ataques; evidencia clínica objetiva de una lesión. Esta forma de presentación requiere la evidencia de una segunda lesión que demuestre diseminación en el espacio con el objeto de alcanzar un diagnóstico de EM. Dicha evidencia puede ser provista por la RM o, en su defecto, la presencia de al menos dos lesiones en RM consistentes con EM sumadas a un LCR anormal. Alternativamente, la aparición de un nuevo ataque clínico con una topografía lesional diferente completaría los criterios de diseminación en el espacio.
- 3.
Un ataque; evidencia clínica objetiva de dos lesiones. Este esquema plantea la necesidad de demostrar diseminación en el tiempo, que puede objetivarse a través de RM o como consecuencia del desarrollo de un segundo ataque clínico.
- 4.
Un ataque; evidencia clínica objetiva de una lesión. Se trata en este caso de la presentación de un SCA o evento monofásico. Este escenario diagnóstico constituye uno de los puntos más relevantes, teniendo en cuenta que uno de los objetivos principales de los criterios de McDonald es alcanzar el diagnóstico de EM de una manera rápida. Para su diagnóstico se requieren: a) evidencia de diseminación en el espacio a través de RM o al menos dos lesiones en RM consistentes con EM con un LCR positivo; b) evidencia de diseminación en el tiempo demostrada por RM o la aparición de un segundo ataque clínico con diferente topografía lesional.
- 5.
Progresión neurológica insidiosa sugestiva de EM. Esta presentación se refiere a la forma primaria progresiva de la enfermedad y también constituye uno de los objetivos principales del Panel. En este caso, se reconoce que determinar diseminación temporoespacial resulta más dificultoso. Se establece como condición la presencia de una enfermedad progresiva durante un año (determinada prospectiva o retrospectivamente) y dos de los siguientes requisitos adicionales: a) RM positiva (9 o más lesiones en T2 o 4 o más lesiones en T2 con un PEV positivo); b) RM espinal positiva (dos lesiones focales en T2) y c) LCR positivo.
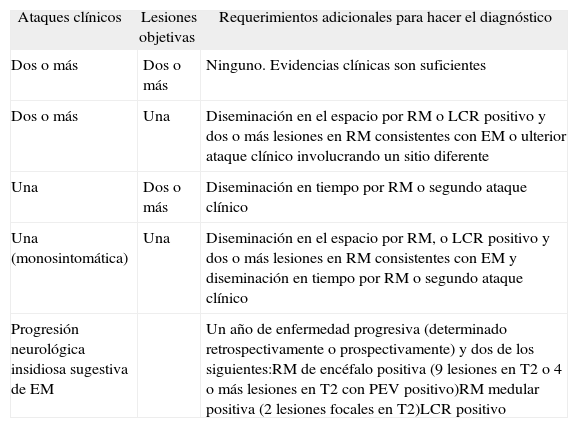
Criterios de McDonald - revisión 2005
| Ataques clínicos | Lesiones objetivas | Requerimientos adicionales para hacer el diagnóstico |
| Dos o más | Dos o más | Ninguno. Evidencias clínicas son suficientes |
| Dos o más | Una | Diseminación en el espacio por RM o LCR positivo y dos o más lesiones en RM consistentes con EM o ulterior ataque clínico involucrando un sitio diferente |
| Una | Dos o más | Diseminación en tiempo por RM o segundo ataque clínico |
| Una (monosintomática) | Una | Diseminación en el espacio por RM, o LCR positivo y dos o más lesiones en RM consistentes con EM y diseminación en tiempo por RM o segundo ataque clínico |
| Progresión neurológica insidiosa sugestiva de EM | Un año de enfermedad progresiva (determinado retrospectivamente o prospectivamente) y dos de los siguientes:RM de encéfalo positiva (9 lesiones en T2 o 4 o más lesiones en T2 con PEV positivo)RM medular positiva (2 lesiones focales en T2)LCR positivo |
EM: esclerosis múltiple; LCR: líquido cefalorraquídeo; RM: resonancia magnética; PEV: potenciales evocados visuales.
Los criterios de McDonald han resultado un aporte significativo, especialmente en lo concerniente a acelerar el diagnóstico de la EM con vistas a un tratamiento más precoz, y sin duda son la mejor herramienta con la que contamos en la actualidad para realizar el diagnóstico de esta entidad de una manera segura y fiable. A pesar de ello, estos criterios no han estado exentos de críticas por parte de diversos autores y siguen resultando algo complejos y difíciles de aplicar en la práctica diaria.
Uno de los cuestionamientos a los criterios de McDonald es la no consideración de referencias históricas de la enfermedad (recaídas) ante la falta de evidencias objetivas en el examen neurológico. Esto significa que un dato obtenido del interrogatorio, y que puede correlacionar con una recaída de la enfermedad, no puede ser considerado como tal si no se acompaña de hallazgos en el examen neurológico consistentes con dicho episodio. Sin embargo, es conocido el hecho de que una recaída puede resolverse sin dejar secuelas, en especial en los primeros estadios de la enfermedad. Si bien puede aceptarse que el no reconocimiento de referencias históricas le agrega una mayor rigurosidad al diagnóstico, muchas de estas referencias pueden tener una alta especificidad en un contexto clínico apropiado (parestesias, vértigo, diplopía, signo de L'Hermitte) y la falta de reconocimiento de ellas puede llegar a significar una demora en el diagnóstico22.
En la actualidad está ampliamente generalizado el concepto erróneo de que la RM constituye la base esencial para el diagnóstico de la EM, mientras que aspectos clínicos como un interrogatorio minucioso y la adecuada valoración de los hallazgos del examen neurológico tienden a ser menos valorados. Si bien el impacto de la RM sobre el proceso diagnóstico no puede ser cuestionado, los nuevos criterios de diagnóstico ubican este método complementario prácticamente como un sustituto del ataque clínico con el riesgo de sobrestimación del método, e inclusive con la probabilidad de que el neurólogo llegue a fundamentar el diagnóstico de la EM exclusivamente por los hallazgos de RM18. Adicionalmente, esta sobrevaloración de la RM como herramienta diagnóstica también puede expresarse a través del radiólogo, quien, en no pocas oportunidades, informa “lesiones compatibles con EM” en lugar de limitarse a un informe descriptivo de los hallazgos en las imágenes.
Los criterios de Barkhof y Tintoré12,13 fueron establecidos originalmente para predecir el desarrollo de EM en pacientes con SCA, brindando elementos cuantitativos y anatómicos, pero sin ahondar en aspectos cualitativos de las imágenes, como por ejemplo la alta especificidad diagnóstica que representa la presencia de lesiones en el cuerpo calloso23,24. Llamativamente los criterios de McDonald sí establecen comentarios muy valiosos en torno a las características cualitativas que deben tener las lesiones medulares para ser consideradas como compatibles con EM y en lo que concierne a su diferenciación con otras patologías desmielinizantes, en especial la neuromielitis óptica.
DiscusiónLa característica de “diseminación en el tiempo y el espacio” no es patrimonio exclusivo de la EM, y muchas otras entidades pueden llegar a cumplimentar este requerimiento. Si bien los criterios vigentes establecen claramente el concepto de exclusión de otras entidades que puedan simular EM como paso ineludible en el procedimiento diagnóstico, no se han establecido pautas claras dentro de los criterios de McDonald que consideren guías para el diagnóstico diferencial con otras patologías.
Un exhaustivo análisis del diagnóstico diferencial de la EM con otras entidades excede el objetivo de esta revisión, no obstante resulta necesario efectuar algunos comentarios en ese sentido. Desafortunadamente la tasa de error diagnóstico indicando una enfermedad distinta a EM se estima entre un 5 y un 10% y hasta un 35%, según los autores25,26.
Algunas implicaciones a tener en cuenta como consecuencia de un error diagnóstico incluyen: a) un significativo impacto en la vida del paciente; b) en muchas ocasiones la implementación de un tratamiento innecesario y de alto coste; c) la no implementación de terapias para otras enfermedades potencialmente tratables y d) la posibilidad de incluir a pacientes con otros diagnósticos en estudios clínicos para la EM.
Particular interés reviste el diagnóstico diferencial con el grupo de las llamadas “enfermedades desmielinizantes inflamatorias idiopáticas", como la encefalomielitis aguda diseminada monofásica o recurrente, la neuritis óptica recurrente, la mielitis transversa y la neuromielitis óptica, las cuales pueden reunir elementos para sospechar un diagnóstico de EM, pero son consideradas entidades separadas27.
Aportes muy significativos surgen de publicaciones recientes en torno a satisfacer el requerimiento de “no mejor explicación" establecido en los criterios de McDonald ante una presentación clínica sospechosa de la EM.
En 2006, un panel convocado por el Comité Asesor Internacional sobre Ensayos Clínicos en EM, aportó guías para el diagnóstico diferencial de la enfermedad28. Este grupo de expertos identificó una lista de “banderas rojas” categorizadas como mayores, intermedias y leves que podrían indicar un diagnóstico distinto a EM. Este listado provee una guía muy útil de diagnósticos alternativos cuando se presentan hechos no característicos de esa enfermedad. En el mismo sentido, Trojano et al revisaron las patologías más frecuentemente consideradas en pacientes evaluados por sospecha de EM25. En sus conclusiones los autores consignan signos de alerta considerados como indicadores de posibles diagnósticos alternativos: a) inicio de los síntomas antes de los 20 o después de los 50 años; b) prominente historia familiar; c) curso atípico (curso gradualmente progresivo desde el inicio, particularmente en un paciente joven o con manifestaciones distintas a una mielopatía); d) desarrollo abrupto de síntomas; e) manifestaciones unifocales; f) manifestaciones neurológicas inusuales para la EM; g) manifestaciones sistémicas asociadas; h) resultados normales en la RM, LCR y PE e i) respuesta atípica al tratamiento (ausencia o rápida respuesta a corticoides o terapias modificadoras de la enfermedad).
La limitada especificidad de los hallazgos en la RM convencional puede aumentar la probabilidad de diagnóstico de EM en pacientes afectados por otras patologías29.
Si bien resulta muy importante establecer pautas radiológicas sugestivas de EM, también puede ser valioso determinar características no sugestivas de EM que pudieran aplicarse al momento de desarrollar el proceso diagnóstico. El grupo europeo MAGNIMS (Magnetic Resonance Network in Múltiple Sclerosis)30 definió una serie de “banderas rojas” de RM que podrían alertar a los médicos con el fin de reconsiderar el diagnóstico de EM ante la presencia de alguna de ellas, o cuando la aplicación de los criterios vigentes de RM no resuelve el diagnóstico de una manera fiable. Estas “banderas rojas” son numerosas e incluyen lesiones que comprometen la sustancia blanca, la sustancia gris cortical, la sustancia gris profunda, la médula espinal y otras regiones. Es esperable que en los próximos años técnicas no convencionales de RM, como la espectroscopia31, difusión y tensor de difusión32,33, transferencia de magnetización34 y RM 3T aporten mayor especificidad a las imágenes, permitiendo una mejor precisión diagnóstica.
ConclusionesLos actuales criterios de diagnóstico pueden resultar algo complejos, en especial para el neurólogo sin una dedicación especial en la EM. La particular heterogeneidad de esta entidad, la ausencia de métodos más específicos de diagnóstico radiológico, así como la carencia de marcadores inmunológicos más precisos hacen que por el momento este problema no pueda ser completamente resuelto.
En los casos en que no es posible llegar a un diagnóstico de certeza, la consulta con un profesional con más experiencia puede resultar de utilidad. Eventualmente la alternativa de aguardar a que la enfermedad defina un perfil más característico siempre será preferible antes que aventurar un diagnóstico basado en pruebas insuficientes.