La estimulación del nervio vago (ENV) se ha mostrado como una terapia complementaria al tratamiento farmacológico en pacientes con epilepsia refractaria. Nuestro objetivo es evaluar la eficacia de la ENV en relación con la disminución del número, intensidad y duración de las crisis, con la reducción del número de fármacos antiepilépticos y con la mejoría de la calidad de vida.
Material y métodosSe analizó la evolución de 70 pacientes con epilepsia refractaria, tratados mediante ENV en el Hospital General Universitario de Alicante y en el Hospital Clínico de Valencia. Se recogieron variables pre- y postoperatorias. La diferencia en la frecuencia tras la estimulación vagal se clasificó mediante la escala de McHugh. También se recogieron los cambios en la duración e intensidad de las crisis y la disminución de la medicación junto con la modificación de la calidad de vida.
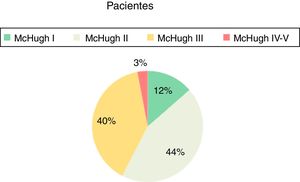
ResultadosEl 12,86% de los pacientes se clasificaron como McHugh I, el 44,29% como ii, el 40% como iii y el 2,86% como iv-v. Un 57,15% de los pacientes presentaron una reducción superior al 50% en la frecuencia de las crisis. Un 88% de los pacientes presentaron una mejoría en la duración de las crisis, en el 68% disminuyó la intensidad, un 66% toman menos fármacos y en el 93% mejoró la calidad de vida.
ConclusionesLa ENV ha mostrado disminuir la frecuencia de las crisis, así como la duración, la intensidad y el consumo de fármacos, ofreciendo además una mejoría en la calidad de vida de nuestros pacientes.
Vagus nerve stimulation (VNS) is used as a complementary therapy to pharmacological treatment in patients with refractory epilepsy. This study aims to evaluate the efficacy of VNS in reducing seizure frequency, severity, and duration; reducing the number of antiepileptic drugs administered; and improving patients’ quality of life.
Material and methodsWe analysed the clinical progression of 70 patients with refractory epilepsy treated with VNS at Hospital Universitario de Alicante and Hospital Clínico de Valencia. Data were collected before and after the procedure. The difference in seizure frequency pre- and post-VNS was classified using the McHugh scale. Data were also collected on seizure duration and severity, the number of drugs administered, and quality of life.
ResultsAccording to the McHugh classification, 12.86% of the patients were Class I, 44.29% were Class II, 40% were Class III, and the remaining 2.86% of patients were Class IV-V. A≥50% reduction in seizure frequency was observed in 57.15% of patients. Improvements were observed in seizure duration in 88% of patients and in seizure severity in 68%; the number of drugs administered was reduced in 66% of patients, and 93% reported better quality of life.
ConclusionsVNS is effective for reducing seizure frequency, duration, and severity and the number of antiepileptic drugs administered. It also enables an improvement in patients’ quality of life.
Se considera epilepsia refractaria a la persistencia de las crisis epilépticas no provocadas, diagnosticadas con certeza, que se repiten con una frecuencia que interfiere en las actividades de la vida diaria, sociofamiliares, laborales, educacionales y que producen insatisfacción personal, a pesar de haber seguido tratamiento con 2 fármacos antiepilépticos de elección en las dosis máximas toleradas y con un cumplimiento impecable, durante un período mínimo de 2 años1–3.
La epilepsia refractaria representa un importante problema sociosanitario, ya que hasta un tercio de los pacientes con epilepsia no responden a tratamientos médicos con antiepilépticos. De estos, el 25-40% no son buenos candidatos para cirugía resectiva1,4. Ante este problema, Penry y Dean4 realizaron el primer implante de un dispositivo de estimulación vagal en un ser humano en 1988. Posteriormente, en 1997, la FDA aprobó el uso de estimulación del nervio vago (ENV) como tratamiento adyuvante para epilepsia médicamente refractaria. Desde entonces, la ENV se ha presentado como una terapia complementaria segura para los pacientes con epilepsia que sufren una respuesta insuficiente al tratamiento médico y que no presentan criterios para realizar tratamiento quirúrgico mediante técnicas resectivas, lesivas o de desconexión5,6.
La técnica consiste en la colocación de un dispositivo similar a un marcapasos (generador) que se implanta en un bolsillo subcutáneo, el cual es capaz de estimular el nervio vago de forma retrógrada a través de un electrodo, que se dispone alrededor del tramo cervical del nervio. El generador estimula al nervio de forma intermitente con una intensidad, frecuencia y duración que puede variar según los parámetros introducidos a través de un cabezal telemétrico. Además, el paciente puede activar el equipo mediante un pequeño imán cuando note una crisis inminente7.
La ENV es un tratamiento con múltiples interrogantes. Hay una gran variedad de artículos sobre la eficacia de esta técnica, los cuales presentan resultados bastante heterogéneos y con un bajo tamaño muestral8,9. Aunque si bien es cierto que todas las fuentes están de acuerdo en que es una técnica segura (los efectos adversos más frecuentes consisten en alteraciones en la frecuencia cardiaca, ronquera, cambios de voz, dolor cervical, disfonía y tos)10,11, hay discrepancias en cuanto a la eficacia del tratamiento.
Los resultados de un metaanálisis realizado en 2013 por Chambers y Bowen12 muestran que la ENV reduce la frecuencia de crisis epilépticas a la mitad en hasta un cuarto de los pacientes. En contraste con este metaanálisis, últimamente se han publicado nuevos estudios donde se aprecia un aumento en la eficacia de la ENV. Por ejemplo, el metaanálisis realizado por Connor et al.13 muestra una reducción de más de un 50% de la frecuencia de las crisis en hasta un 50,9% de los pacientes.
Asimismo, no hay consenso sobre qué síndromes epilépticos presentan una mayor tasa de éxito con la realización de esta técnica, por lo que sería interesante estudiar dicho aspecto.
También hay disparidad de opiniones sobre si la edad de implantación del dispositivo de estimulación vagal influye en la eficacia. Algunos autores defienden que existe mejoría significativa de la eficacia en niños menores de 12 años14,15, mientras que hay otros que concluyen que no la hay16,17.
Por otra parte, se ha observado en algunos estudios que la ENV no solo reduce la frecuencia de las crisis, sino que además disminuye la duración, la intensidad de estas y la toma de fármacos18–20. Lamentablemente, son pocos los artículos que han estudiado dichos efectos, ya que la mayoría únicamente se centran en la disminución del número de crisis.
Aunque el control de las crisis ha sido prácticamente el único parámetro investigado en ensayos experimentales y clínicos durante las últimas décadas, el efecto de la ENV en la calidad de vida ha ganado recientemente una gran cantidad de interés clínico, siendo necesario incluir dicho efecto en los nuevos estudios que se realicen.
Por todo esto, parece necesario realizar nuevas investigaciones sobre la ENV que tengan en cuenta tanto los cambios en la frecuencia de las crisis como la mejoría de la intensidad y la duración de estas, la reducción del consumo de fármacos y la mejora de la calidad de vida.
ObjetivosEl objetivo principal de este estudio ha sido evaluar la eficacia de la ENV en relación con la disminución del número, intensidad y duración de las crisis, con la reducción de la toma de antiepilépticos y con posibles cambios en la calidad de vida de nuestros pacientes.
Además, nos hemos planteado valorar la eficacia de la ENV según el tipo de crisis, la etiología de las mismas y la edad de los pacientes, así como determinar la seguridad de la técnica teniendo en cuenta los principales síntomas adversos (alteraciones en la frecuencia cardiaca, ronquera, infecciones, dolor cervical, disfonía y tos).
Material y métodosEste trabajo se ha planteado como un estudio clínico retrospectivo no aleatorizado. Se han incluido 70 pacientes tratados mediante ENV en el Servicio de Neurocirugía del Hospital General Universitario de Alicante y en el Hospital Clínico de Valencia.
El análisis se ha llevado a cabo mediante la revisión retrospectiva de las historias clínicas de los pacientes intervenidos con ENV, recogiéndose los datos en los 3 meses previos a la intervención y tras un año desde el inicio de la estimulación.
Se ha empleado el estimulador vagal intermitente Cyberonics modelo 103. Se ha programado el dispositivo de modo que produzca descargas con una intensidad de 0,5μA, una frecuencia de 30Hz, una amplitud de onda de pulso de 500ms y manteniendo una intermitencia de 30s de estimulación cada 10min durante las 24h del día.
Cada una de las variables clínicas ha sido recogida por un familiar y/o el propio paciente en un diario de crisis.
Parámetros recogidosVariables clínicas y demográficasSe ha recogido el sexo, edad de los pacientes, fecha de implantación del dispositivo, tipos de crisis que presentaban y etiología de las mismas.
Frecuencia de las crisisSe ha medido la reducción de la frecuencia de las crisis (media semanal), en los diferentes tipos de epilepsia, según la etiología de las mismas y en función de la edad de los pacientes (mayores y menores de 12 años). Para cuantificar la reducción de la frecuencia de la crisis se ha escogido la clasificación de McHugh. Esta se basa en las respuestas de los pacientes y/o familiares a las preguntas formuladas sobre la frecuencia de convulsiones en el momento de la encuesta (un año tras la intervención) en comparación con las respuestas previas al implante del dispositivo. De este modo, se recoge el número de crisis antes y después de la intervención. Esta clasificación tiene mayor concordancia interobservador (medida mediante el coeficiente kappa) que las demás escalas empleadas hasta la fecha21. Se clasifica a un paciente como McHugh clase i cuando ha presentado una reducción mayor o igual del 80% en la frecuencia de las crisis, clase ii si ha sido del 50-79%, clase iii si ha sido inferior al 50%, clase iv si solo ha notado mejoría cuando se ha estimulado con el imán y como McHugh clase v si no ha presentado mejoría alguna. Además, los resultados en cuanto a la disminución de las crisis, también se dividieron atendiendo a la clasificación de Engel.
Duración de las crisisSe ha clasificado a los pacientes según hayan presentado una reducción de la duración del 0-33% (reducción baja), 33-66% (reducción media) y 66-100% (reducción alta). La duración se ha medido en tiempo (minutos y segundos) referidos por los familiares/acompañantes, contados desde el inicio de la misma hasta la recuperación completa o parcial del nivel de conciencia, y/o cese de los movimientos involuntarios.
Intensidad de las crisisSe ha pedido a los pacientes/familiares que cataloguen la intensidad de sus crisis en alta, media o baja antes y tras la cirugía de ENV. De este modo se ha objetivado en cuántos pacientes ha habido una mejoría tras la intervención.
Cantidad de fármacos antiepilépticosSe ha calculado el porcentaje de reducción del número de fármacos tras la estimulación vagal. Se ha clasificado a los pacientes según hayan presentado una reducción del 0-33% en la cantidad de fármacos antiepilépticos (reducción baja), del 33-66% (reducción media) y del 66-100% (reducción alta).
Efectos adversos tras la cirugíaSe han recogido las alteraciones en la frecuencia cardiaca (palpitaciones, detección de alteraciones en la frecuencia por el médico de atención primaria y/o medicina de urgencias), ronquera, cambios de voz, dolor cervical, infecciones, disfonía y tos. Todas estas variables se recogieron en la consulta atendiendo a la información proporcionada por la familia y/o el paciente, al ser preguntados de forma directa por las mismas. Es decir, se anotaron como complicaciones aquellas en las que la respuesta a dichas preguntas fue positiva.
Calidad de vida pre- y postimplantación de estimulación del nervio vagoSe ha medido mediante el cuestionario quality of life in epilepsy (QOLIE-10) modificado (tabla 1). Para ello se ha llamado telefónicamente a los pacientes para realizarles el cuestionario una vez que ha pasado un año de la intervención. Dicha escala no se encuentra validada.
Según la puntación obtenida, se ha clasificado a los pacientes en el grupo i si tienen entre 19 y 25 puntos (peor calidad de vida); en el grupo ii si presentan entre 12 y 18 puntos y en el grupo iii si tienen entre 5 y 11 puntos (mejor calidad de vida).
Análisis estadísticoPara realizar el estudio estadístico se ha empleado el programa Epidat 3.5 de la Junta de Galicia y el programa Excel. Se ha realizado mediante la prueba exacta de Fisher (para el estudio de la frecuencia) y con la prueba de McNemar (para el estudio de la calidad de vida).
ResultadosPacientes del estudioDe los 70 pacientes incluidos en el estudio, el 53% fueron hombres y el 47% mujeres. El rango de edad de los pacientes fue de 8-69 años, con una media de 30 años. El rango de edad de implantación es de 4-58 años, siendo la edad media de 23 años. De los pacientes estudiados, 21 eran menores de 12 años, mientras que el resto (49 pacientes) superaban dicha edad.
Las diferentes causas que han provocado las crisis se resumen en la tabla 2. Los distintos tipos de crisis encontradas se resumen en la tabla 3.
Diferentes causas responsables de la aparición de las crisis en los pacientes analizados
| Etiología | Porcentaje (%) | Número de pacientes |
|---|---|---|
| Idiopáticas | 37 | 26 |
| Meningoencefalitis | 14 | 10 |
| Postraumáticas | 10 | 7 |
| Sufrimiento fetal | 10 | 7 |
| Isquémica | 10 | 7 |
| Esclerosis tuberosa | 7 | 5 |
| Síndrome de Lennox-Gastaut | 4 | 3 |
| Displasia cortical | 4 | 3 |
| Síndrome de Aicardi | 1,5 | 1 |
| Hematoma intracraneal | 1,5 | 1 |
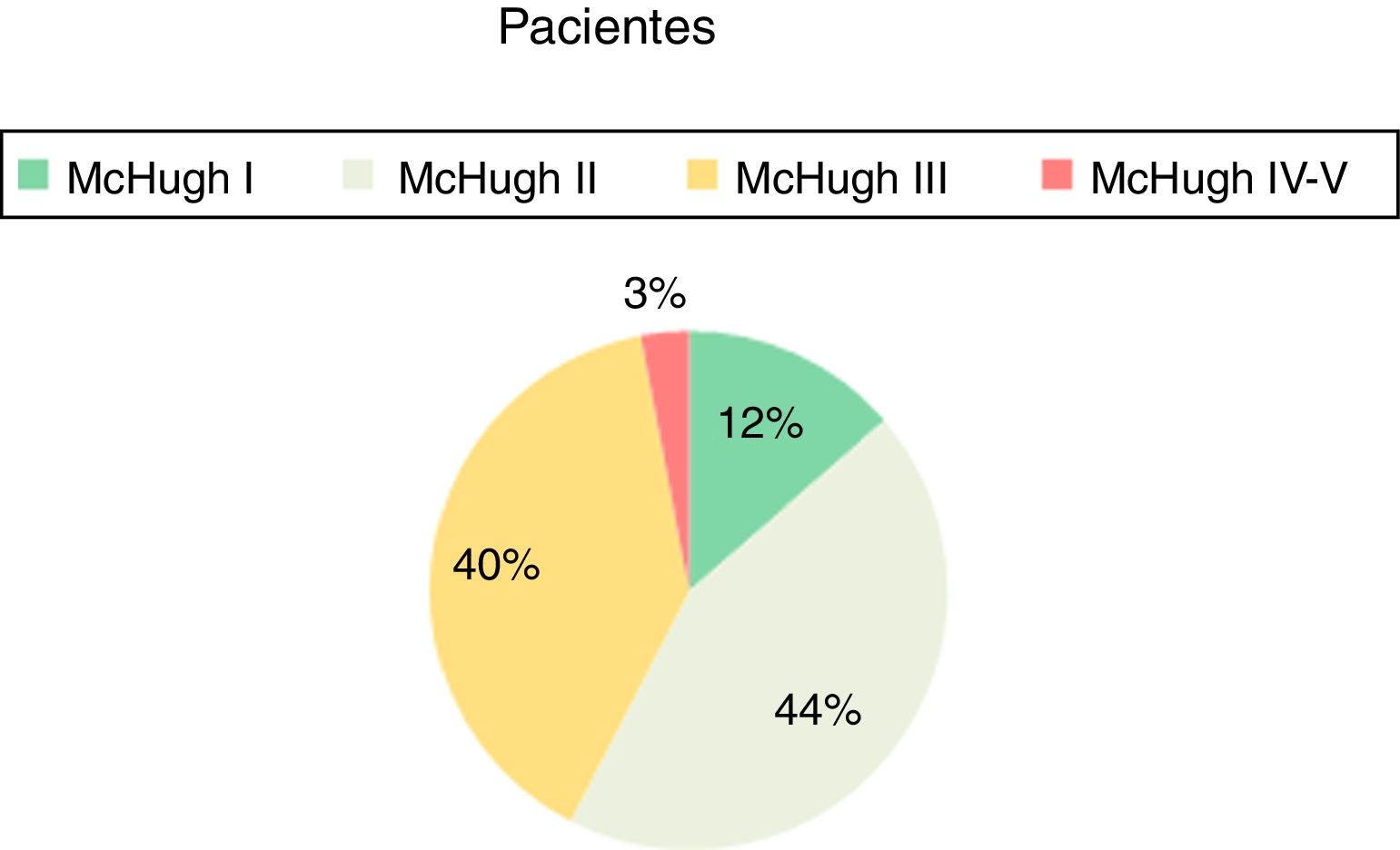
(fig. 1) La frecuencia crítica basal media de los pacientes era de 15 crisis/semana. Tras la intervención, el 12,86% de los pacientes se han clasificado como McHugh clase i, el 44,29% como ii, el 40% como iii y el 2,86% como clases iv-v. Es decir, un 57,15% (pacientes catalogados como clase i y ii) ha presentado una reducción en la frecuencia de las crisis, superior al 50%. La reducción media de la frecuencia tras la ENV fue del 53%. Ninguno de nuestros pacientes ha conseguido mantenerse completamente libre de crisis tras la implantación.
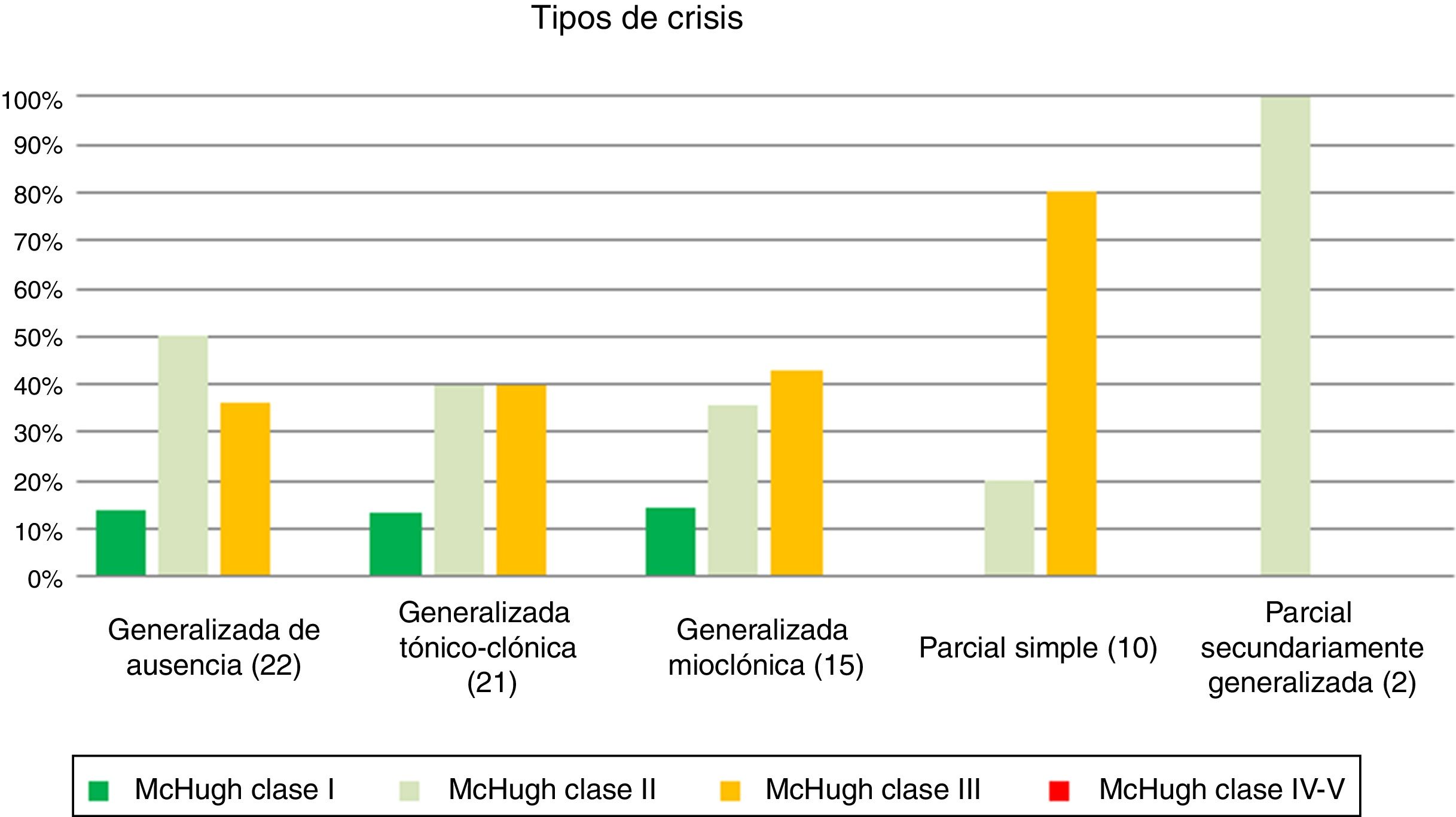
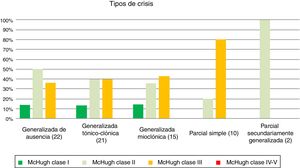
En cuanto a la disminución de la frecuencia en función del tipo de crisis, los resultados se muestran en la tabla 4 y en la figura 2 (p=0,32). Los pacientes con crisis generalizadas tónico-clónicas han sido los que más han reducido la frecuencia de las crisis tras la ENV.
Disminución de la frecuencia en función del tipo de crisis (p>0,05)
| Tipo de crisis (n) | McHugh I (%) | McHugh II (%) | McHugh III (%) | McHugh IV-V (%) |
|---|---|---|---|---|
| Generalizada de ausencia (22) | 13,64 | 50 | 36,36 | 0 |
| Generalizada tónico-clónica (21) | 19,05 | 47,62 | 28,57 | 4,76 |
| Generalizada mioclónica (15) | 13,33 | 40 | 40 | 0 |
| Parcial simple (10) | 0 | 20 | 80 | 0 |
| CPSG (2) | 0 | 100 | 0 | 0 |
Dado el gran número de variables para el tamaño muestral del estudio, se ha comparado la disminución en la frecuencia de las crisis según el tipo de las mismas como se resume en la tabla 5. Un 63% de los pacientes con crisis generalizadas han presentado una reducción superior al 50% en la frecuencia, mientras que tan solo el 20% de los pacientes con crisis parciales presentaron dicha mejoría alcanzando significación estadística (p=0,01).
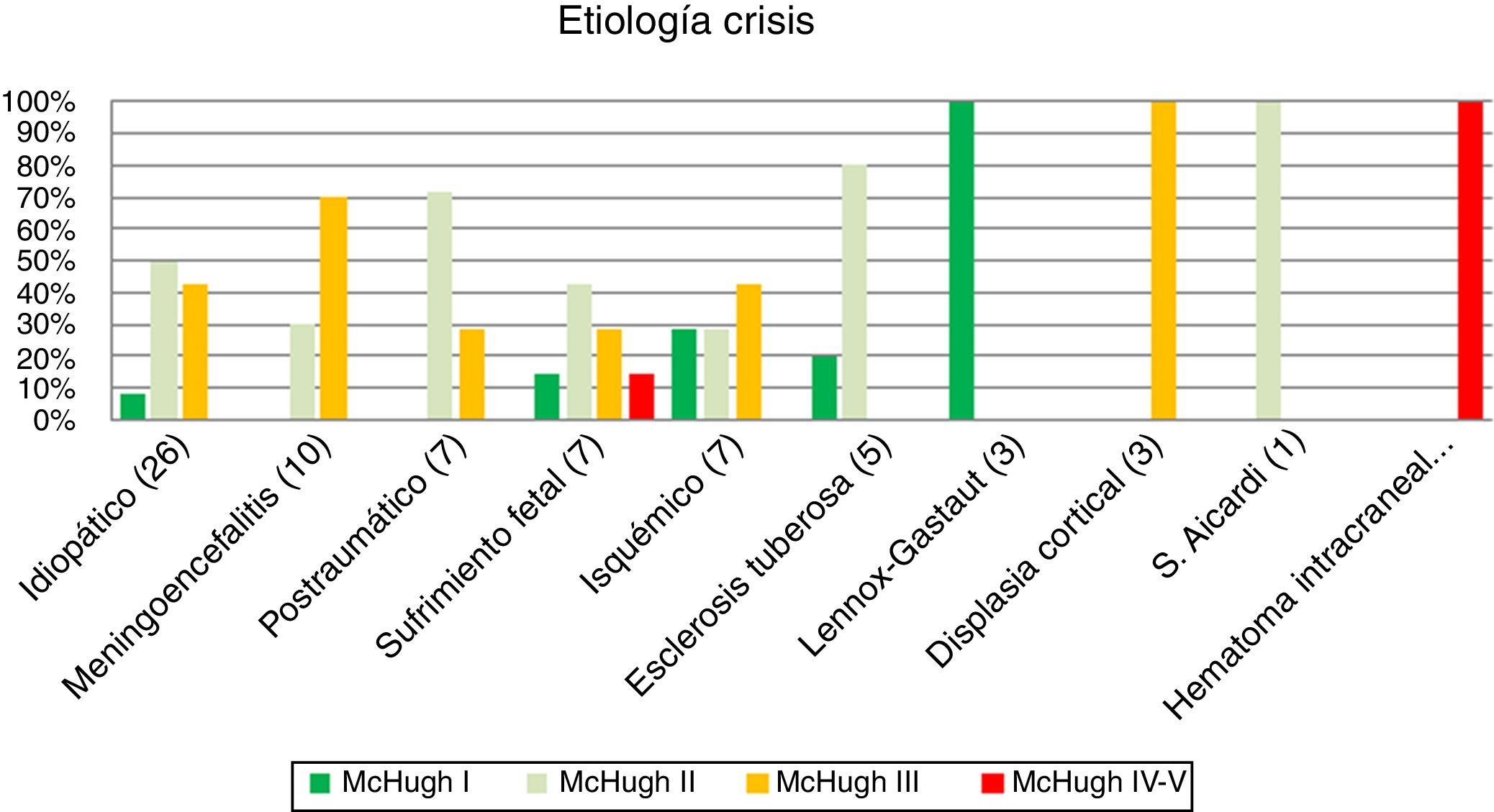
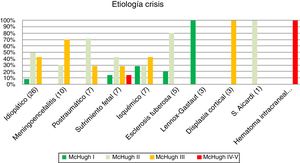
Teniendo en cuenta la etiología de las crisis, se han obtenido los resultados según se resume en la figura 3 (p>0,05). Destacan de forma notable los buenos resultados en pacientes con Lennox-Gastaut, crisis de etiología postraumática, así como pacientes con el diagnóstico de esclerosis tuberosa.
Estratificando la reducción de la frecuencia en función de la edad se han obtenido los resultados detallados en la tabla 6. El 66% de los pacientes menores de 12 años han presentado una disminución en la frecuencia de las crisis por encima del 50%, resultados que tan solo alcanzaron el 53% de los pacientes mayores de 12 años (p=0,21).
Atendiendo a la clasificación de Engel, el 15,7% de los pacientes (11/70) se clasificaron como clase i, el 45,7% (32/70) como clase ii, el 35,7% (25/70) como clase iii, mientras que tan solo el 2,9% (2/70) se agruparon como clase iv.
Duración de las crisisUn 88% de los pacientes presentaron una disminución en la duración de las crisis. De estos, en el 19% fue baja, media en el 46% y alta en el 35%.
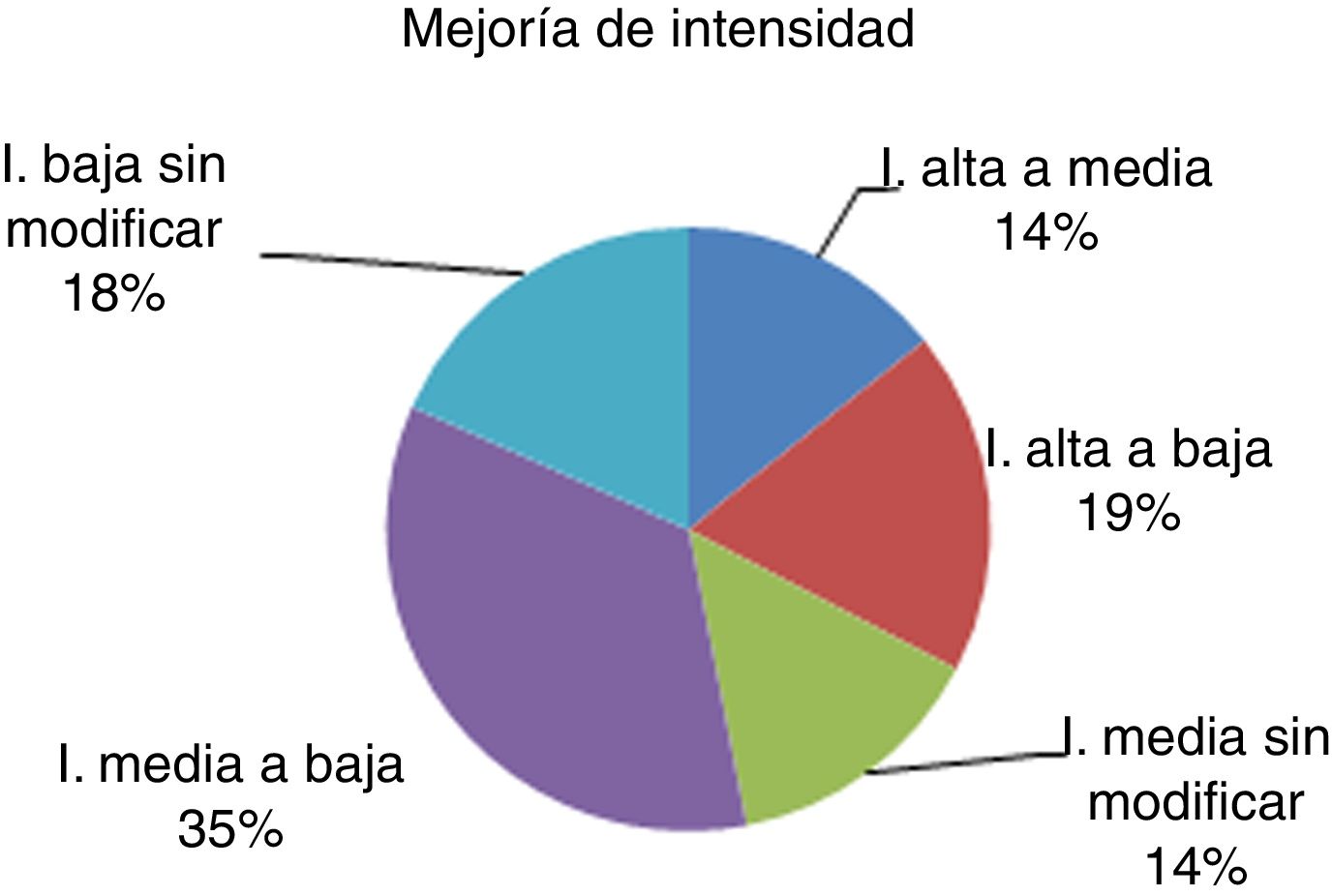
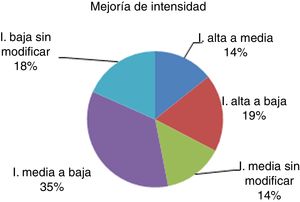
Intensidad de las crisis(fig. 4) Un 14% de los pacientes han pasado de tener crisis de intensidad alta a intensidad media; un 19% bajaron de intensidad alta a baja y en un 34% las crisis han disminuido en intensidad de media a baja. El resto de los pacientes no han presentado cambios en la intensidad de sus crisis (un 14% de los pacientes continúan con crisis de intensidad media y un 18% siguen teniendo sus crisis con intensidad baja). Todos los pacientes con crisis de intensidad alta han mejorado.
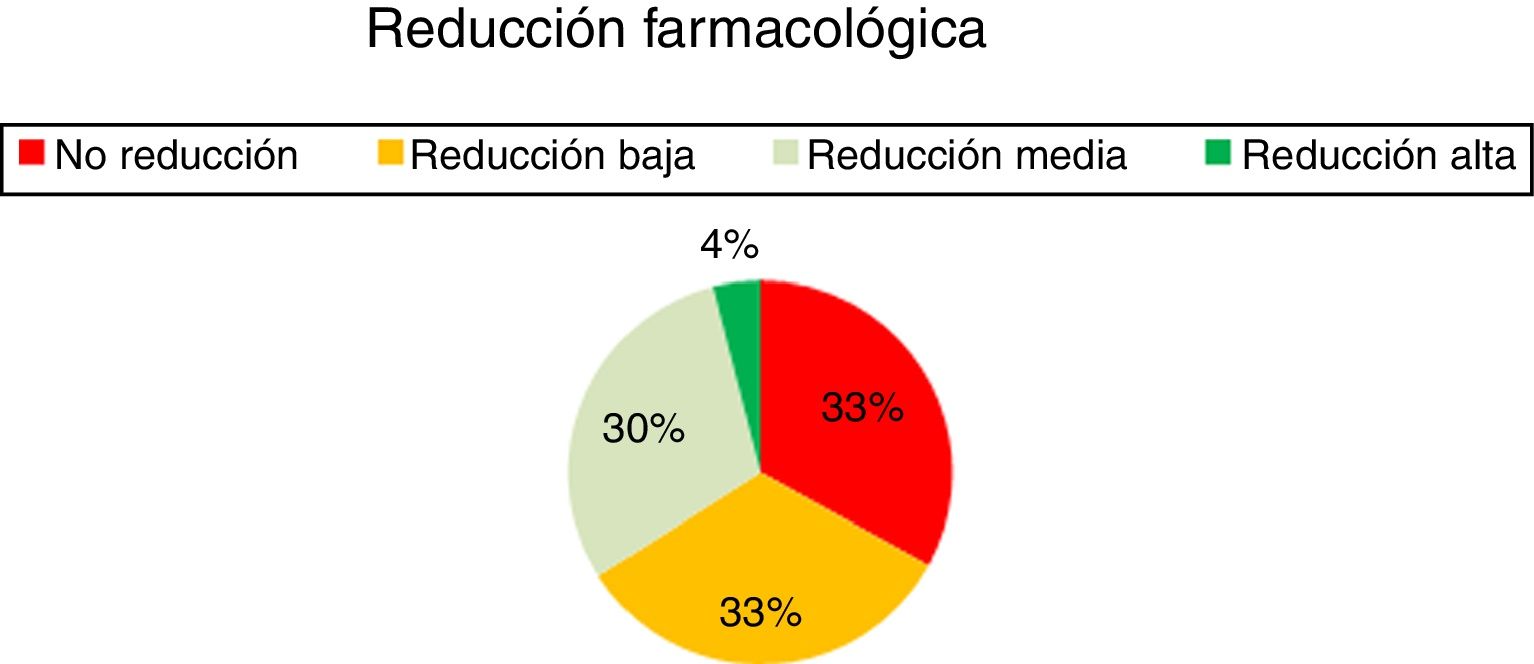
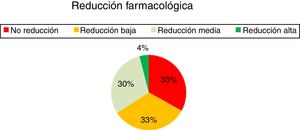
Cambios en la posología de los fármacos antiepilépticos(fig. 5) En un 33% de los pacientes se ha alcanzado una reducción baja del consumo de fármacos, media en un 30% y alta en un 4%. El 33% restante no han obtenido una reducción del número de fármacos. No se han introducido nuevos fármacos antiepilépticos tras la implantación del dispositivo.
Efectos adversosUn 21% de los pacientes refirieron efectos adversos. Un 4,55% disfonía, un 10,61% tos, un 4,55% presentaron tos y disfonía, y un 3% disestesias cervicales. No se recogieron cambios en la frecuencia cardiaca en forma de palpitaciones o alteraciones registradas por los profesionales de atención primaria y/o medicina de urgencias. Tampoco se anotaron ronquera ni infecciones del dispositivo implantado en ninguno de nuestros pacientes.
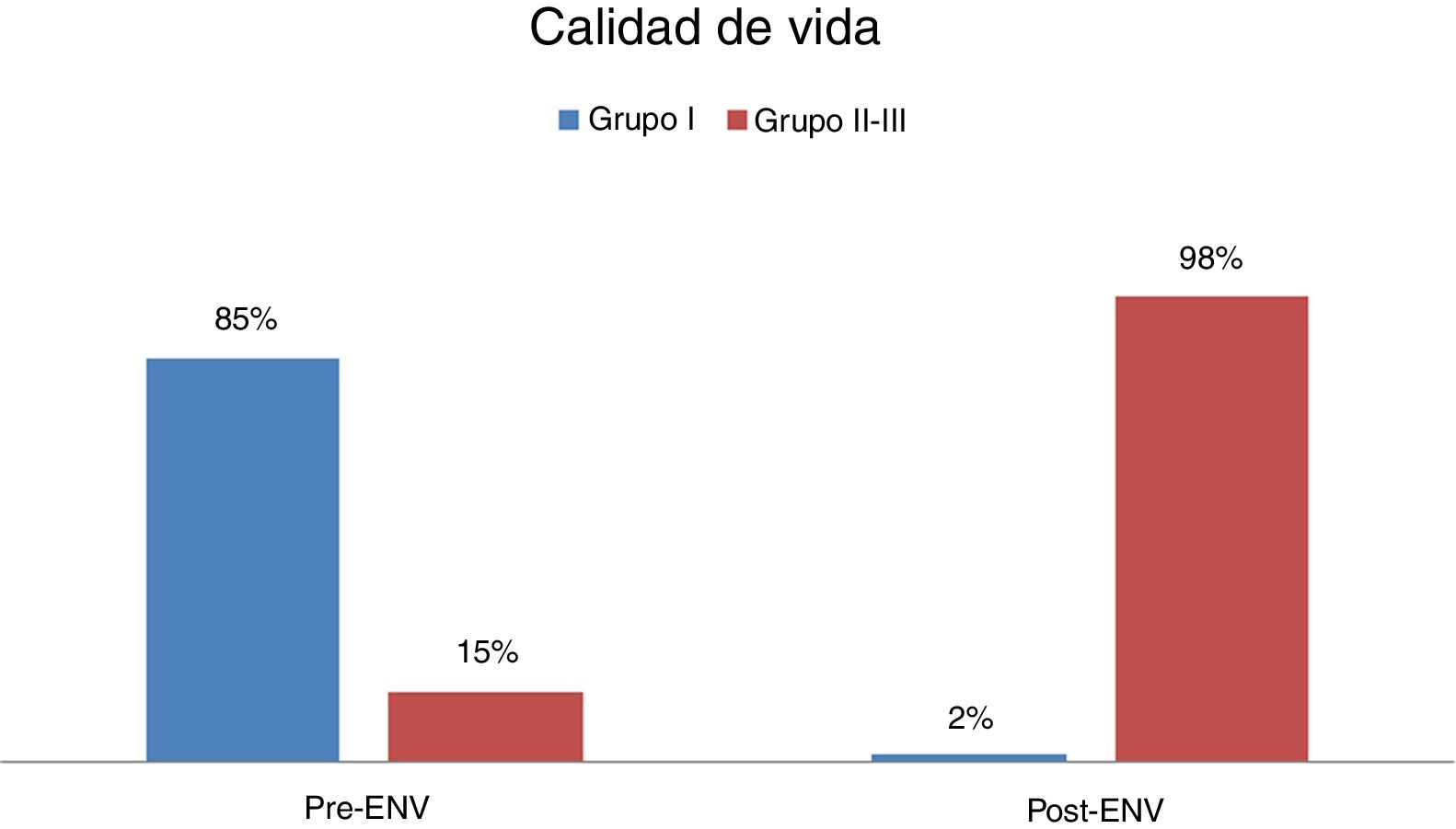
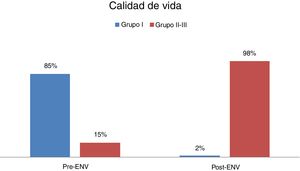
Cambios en la calidad de vida(fig. 6) Antes de la estimulación vagal, un 85% de los pacientes pertenecían al grupo i (peor calidad de vida), un 15% estaban en el grupo ii y ningún paciente se encontraba en el grupo iii (mejor calidad de vida). Tras la estimulación vagal, tan solo un 2% de los pacientes permanecen en el grupo i, un 59% están en el grupo ii y un 39% se encuentran en el grupo iii. Tras la ENV, tan solo un 2% de los pacientes pertenecen al grupo i, mientras que el 98% de los pacientes están en el grupo ii-iii, alcanzando este análisis la significación estadística (p=<0,001).
La media de reducción del QOLIE fue de un 8,45 con una desviación estándar de ±7,2.
DiscusiónLa ENV parece una buena alternativa al tratamiento farmacológico en pacientes con epilepsia refractaria en varios estudios previos. Sin embargo, y aunque son muchos los estudios que han evaluado la eficacia de la técnica con resultados bastante heterogéneos hasta el momento, dichos estudios evalúan fundamentalmente la disminución de la frecuencia, dejando de lado parámetros tan importantes como son la intensidad de las crisis, su duración, la disminución de la medicación o la calidad de vida. Esto se debe en gran medida a la dificultad para recoger dichas variables en estudios retrospectivos22-24.
Un elevado porcentaje de nuestros pacientes han reducido de forma significativa el número de crisis totales (un 57% de los pacientes alcanzaron una disminución superior al 50%). En el metaanálisis realizado por Connor et al.13 se evidencia que un 50,9% de los pacientes presentan una reducción superior al 50%. Meng et al.25 clasifican a 94 de sus pacientes con la escala de McHugh, observando que un 35,1% de los pacientes son clase i, un 28,7% clase ii, un 21,3% clase iii y un 14% son clases iv-v (por lo que se evidencia una reducción superior al 50% en el 63,8%). Otro de los trabajos que presenta resultados similares es el estudio de Wasade et al.26. En este estudio, en el que participan 152 personas intervenidas de ENV, se ha objetivado una reducción superior al 50% en el 68% de los pacientes.
En el metaanálisis publicado en 2013 por Chambers y Bowen12, tan solo un cuarto de los pacientes obtuvo una reducción superior al 50%. Sin embargo, esto pudo deberse a que la mayoría de los estudios incluidos en el metaanálisis recogieron los datos a los 3 y 6 meses post-ENV. En este sentido, se ha observado un aumento significativo de la eficacia con el tiempo (por la desactivación crónica del tálamo)25, por lo que dichos resultados pueden deberse a la poca duración del tratamiento.
Los resultados en cuanto a la disminución de la frecuencia entre los 5 tipos de crisis epilépticas o entre las diferentes etiologías, aunque muestran cierta tendencia, no han alcanzado significación estadística, probablemente debido a que el tamaño muestral no ha sido suficiente para el número de variables estudiadas. Sin embargo, sí se ha alcanzado significación estadística al comparar la reducción del número de crisis parciales frente a generalizadas. Un 63% de las crisis generalizadas han obtenido una reducción superior al 50% mientras que tan solo un 20% de las crisis parciales han alcanzado dicha reducción. Apenas hay trabajos que comparen la eficacia de la ENV entre estos 2 tipos de eventos comiciales, y los que se han realizado presentan un tamaño muestral muy reducido.
Al comparar la disminución de la frecuencia en pacientes mayores y menores de 12 años, no encontramos diferencias estadísticamente significativas entre ambos grupos de edad. Estos datos concuerdan con los obtenidos en el estudio retrospectivo realizado por Elliott et al.16. En dicho estudio, en el que se incluyen 141 pacientes pediátricos, los autores concluyen que la eficacia y seguridad de la ENV es similar en los niños menores y mayores de 12 años. En el estudio de Murphy et al.17 tampoco se encontraron diferencias significativas.
En contraposición, el estudio de Lagae et al.14, en el que se analizaron 70 pacientes, pone de manifiesto que la edad temprana de implantación es un factor de buen pronóstico. Sin embargo, únicamente lograron demostrar una diferencia estadísticamente significativa entre niños mayores y menores de 5 años a la hora de conseguir la ausencia total de crisis (3 de los 4 pacientes que presentan una reducción del 100% en la frecuencia de las crisis tienen menos de 5 años); no obstante, no logran evidenciar una mayor tasa de respuesta global entre los diferentes grupos de edad.
Sin embargo, aunque no exista significación estadística, es probable que la tendencia objetivada en nuestro estudio apoye una mejor respuesta con implantaciones más tempranas tras el inicio de la enfermedad. Hecho que podría ser analizado en futuros estudios.
Por otra parte, y con respecto a la reducción de la duración de las crisis, hasta un 88% de los pacientes han experimentado una clara mejoría. De estos, un 85% han obtenido una reducción moderada-alta.
También se ha evidenciado una reducción significativa en la intensidad de las crisis, ya que hasta un 66% de los pacientes la han alcanzado. Teniendo en cuenta que un 18% de los pacientes ya presentaba intensidad baja antes de la ENV, únicamente un 14% de los pacientes no se ha beneficiado en este aspecto. Además, un 52% han pasado de tener intensidad alta-media a intensidad baja, por lo que se puede decir que los resultados adquiridos son muy satisfactorios.
En cuanto a la reducción de los fármacos, un 33% de los pacientes no ha presentado disminución alguna en el número de fármacos. En los demás pacientes (67%) se ha observado en mayor o menor medida una reducción del número de fármacos significativa.
Como ya hemos comentado, son pocos los estudios que analizan estos 3 últimos parámetros. Uno de ellos es el estudio retrospectivo con 347 niños de Orosz et al.18, donde objetivan una disminución de la duración en el 42,9% de los pacientes, una disminución de la intensidad en el 34-42% y una disminución de la cantidad de fármacos en un 50,4%. Son necesarios nuevos estudios que se centren en dichos parámetros y que confirmen los resultados obtenidos, ya que influyen significativamente en la calidad de vida de los pacientes.
De igual importancia es la seguridad de la técnica. En este estudio únicamente se han encontrado efectos adversos en un 21% de los pacientes, siendo todos banales (disfonía, tos y disestesias cervicales). Estos resultados concuerdan con la bibliografía consultada. En la cohorte realizada por Ramsay et al.27, en la que se estudia los efectos adversos de la ENV en 68 pacientes, se apreciaron efectos adversos en el 25,8% de los pacientes, siendo la mayor parte poco importantes (únicamente un paciente presentó parálisis de la cuerda vocal izquierda; no hubo alteraciones en la función cardiaca).
Todos estos parámetros influyen en la calidad de vida de los pacientes. En nuestra serie se ha evidenciado una mejoría estadísticamente significativa de la calidad de vida de los pacientes. Una gran proporción de pacientes han pasado de clase i a clases ii y iii. Tras la ENV casi un 40% de los pacientes están en el grupo con mejor calidad de vida. Podemos considerar la mejoría en la calidad de vida como una de las variables más importantes para mediar la eficacia de la ENV, pues en mayor o menor medida es un reflejo de la mejoría del resto de los parámetros.
En el ensayo de Ryvlin et al.28, se compara la mejoría de la calidad de vida en pacientes con ENV y tratamiento farmacológico con la mejoría observada solo con el tratamiento farmacológico usado la escala QOLIE-89. La media de reducción en la escala QOLIE-89 con el tratamiento combinado es de 5,5 (±7,2) mientras que la media de reducción con el tratamiento farmacológico aislado es de 1,2 (±7,9). En dicho estudio concluyen que la ENV junto con el tratamiento farmacológico se asocia a una mejoría significativa de la calidad de vida en comparación con el tratamiento farmacológico aislado.
En este estudio hay varias limitaciones. La primera de ellas es que se trata de un estudio retrospectivo, en el que no se han estandarizado los parámetros de estimulación (aunque refleja la práctica clínica). El diseño retrospectivo del estudio no permite la inclusión de un grupo control, aunque, en vista de la duración del estudio, no habría sido ético. Por tanto, no se ha podido objetivar el efecto placebo. Otra limitación del estudio es el pequeño tamaño de las muestras para algunas de las comparaciones, especialmente para la medición de la eficacia en las diferentes etiologías de las crisis. También hay que tener en cuenta que se ha empleado una escala de valoración de la calidad de vida modificada con menor cantidad de preguntas. Para realizar un análisis más amplio de la calidad de vida, es necesario emplear otras escalas como el QOLIE-10, QOLIE-39 o el QOLIE-89. Además, otra limitación en cuanto al análisis de la calidad de vida es que los datos respecto a la percepción de la misma se recogieron de forma transversal al año del inicio de la estimulación. De esta forma, no fuimos capaces de analizar las posibles fluctuaciones temporales, que seguro existieron, durante este período de tiempo. Por último, hay que tener en cuenta que las variables clínicas han sido recogidas por un familiar y/o el propio paciente en un diario de crisis. Esta forma de recoger los datos puede sobrevalorar la respuesta a la ENV, ya que algunas de las crisis han podido pasar desapercibidas (sobre todo tras la reducción de la intensidad y de la duración de las mismas), especialmente en el caso de crisis mioclónicas y de ausencias.
ConclusionesLa ENV es una técnica eficaz, que no solo contribuye a la disminución en la frecuencia de las crisis epilépticas, sino que también reduce la duración, la intensidad y el consumo de fármacos. Es además una técnica segura, habiéndose registrado pocos efectos adversos, siendo estos banales. No se ha registrado complicación alguna que haya puesto en riesgo la vida de ninguno de nuestros pacientes, ni que haya obligado a finalizar el tratamiento.
Se ha observado una mayor eficacia de la ENV en las crisis generalizadas en comparación con las crisis parciales, siendo, no obstante, necesarios nuevos estudios para confirmar dichos resultados.
En consonancia con los trabajos publicados, no se han observado diferencias significativas entre pacientes en edad pediátrica y pacientes adolescentes y adultos, hecho que requiere de un estudio multivariable y con mayores tamaños muestrales.
La ENV se ha mostrado por tanto como una técnica quirúrgica eficaz en el tratamiento de ciertos pacientes con epilepsia refractaria, y que además produce una mejoría significativa en la calidad de vida de estos pacientes.
Conflicto de interesesDeclaramos la inexistencia de conflictos de interés por parte de ninguno de los autores en relación con el material remitido.