Las espinas dendríticas representan los principales sitios de contactos sinápticos de tipo excitador. Además, presentan respuestas plásticas a diferentes estímulos propios de la actividad sináptica o daño, que van de un aumento o disminución de su número total a una redistribución a lo largo de las dendritas progenitoras o variaciones en su tamaño o forma. Sin embargo, las espinas pueden permanecer estables durante tiempos largos.
FuentesEl uso de modelos experimentales ha reportado que distintas moléculas de unión a los F-actina y vías de señalización están estrechamente relacionadas con el desarrollo, el mantenimiento y la plasticidad de las sinapsis de tipo excitador, lo que podría influir en el número, tamaño y la forma de las espinas dendríticas; mecanismos que afectan y depende el reordenamiento del citoesqueleto de actina.
DesarrolloSe ha propuesto que los filopodios son los precursores de espinas dendríticas. Drebrina es una proteína de unión a los F-actina y es la responsable de concentrar los F-actina y PSD-95 en los filopodios que guiarán la formación de la nueva espina.
ConclusionesLos mecanismos específicos de regulación de la actina son parte integral en la formación, maduración y plasticidad de espinas dendríticas en correlación con diversas proteínas de unión al citoesqueleto de actina. Además, de las vías de señalización mediadas por pequeñas GTPasas, así como la relación entre la G-actina y F-actina.
Dendritic spines are the main sites of excitatory synaptic contacts. Moreover, they present plastic responses to different stimuli present in synaptic activity or damage, ranging from an increase or decrease in their total number, to redistribution of progenitor dendritic spines, to variations in their size or shape. However, the spines can remain stable for a long time.
BackgroundThe use of experimental models has shown that different molecules of the F-actin binding and signalling pathways are closely related to the development, maintenance and plasticity of excitatory synapses, which could affect the number, size and shape of the dendritic spines; these mechanisms affect and depend on the reorganisation of the actin cytoskeleton.
DevelopmentIt is proposed that the filopodia are precursors of dendritic spines. Drebrin is an F-actin binding protein, and it is responsible for concentrating F-actin and PSD-95 in filopodia that will guide the formation of the new spines.
ConclusionThe specific mechanisms of actin regulation are an integral part in the formation, maturing process and plasticity of dendritic spines in association with the various actin cytoskeleton-binding proteins The signalling pathways mediated by small GTPases and the equilibrium between G-actin and F-actin are also involved.
Las conexiones y los circuitos neuronales que establece el cerebro subyacen a diferentes tipos de conductas, pensamientos, emociones y recuerdos. La capacidad de las neuronas de funcionar dentro de los circuitos neuronales es mediada a través sitios de contacto denominados sinapsis. Las sinapsis químicas regulan la comunicación eléctrica dentro de las redes neuronales y transmiten información desde la terminal axónica presinápticas a regiones dendríticas post-sinápticas. La construcción de los circuitos neuronales durante el desarrollo del cerebro requiere del control preciso para que la actividad de la red neuronal funcione de manera adecuada. La mayoría de las sinapsis de tipo excitador en el cerebro de mamífero se establecen sobre pequeñas protuberancias dendríticas, llamadas espinas dendríticas1. Experimentalmente se ha demostrado que la eficacia sináptica puede inducir cambios morfológicos en el número de espinas dendríticas2. Además, se sabe que el almacén de información en el cerebro está dado por el fortalecimiento o el debilitamiento de las sinapsis existentes, así como por la aparición o eliminación de las espinas dendríticas. Estos cambios funcionales y estructurales en las espinas y las sinapsis se cree son la base del aprendizaje y la memoria3. Las espinas dendríticas son minúsculas protuberancias protoplasmáticas que revisten la superficie de muchas neuronas4 y representan el sitio de contacto sináptico excitador en neuronas del hipocampo, la neocorteza y otras regiones cerebrales. Fueron descritas inicialmente por Ramón y Cajal (1888), quien propuso que estas se conectan por axones y dendritas, y que son elementos estructurales del sistema nervioso5. Por otro lado, diversos estudios han demostrado que las proteínas de unión al citoesqueleto de actina son fundamentales en la formación, eliminación, motilidad, estabilidad, tamaño y forma de las espinas dendríticas6,7. Además, en las sinapsis, el citoesqueleto de actina no solo contribuye a la estructura morfológica de la neurona, sino también participa en la organización de proteínas presentes en la densidad post-sináptica, así como en el anclaje de diferentes tipos de receptores post-sinápticos necesarios para la recepción del mensaje y la transmisión de la información sináptica8.
El objetivo de esta revisión es mostrar evidencias actuales acerca de los mecanismos que regulan la morfogénesis de las espinas dendríticas. Además, describir la participación del citoesqueleto de actina sobre la organización y estructura de las espinas dendríticas, así como las vías de señalización que regulan la formación las espinas dendríticas mediante la formación de filopodios.
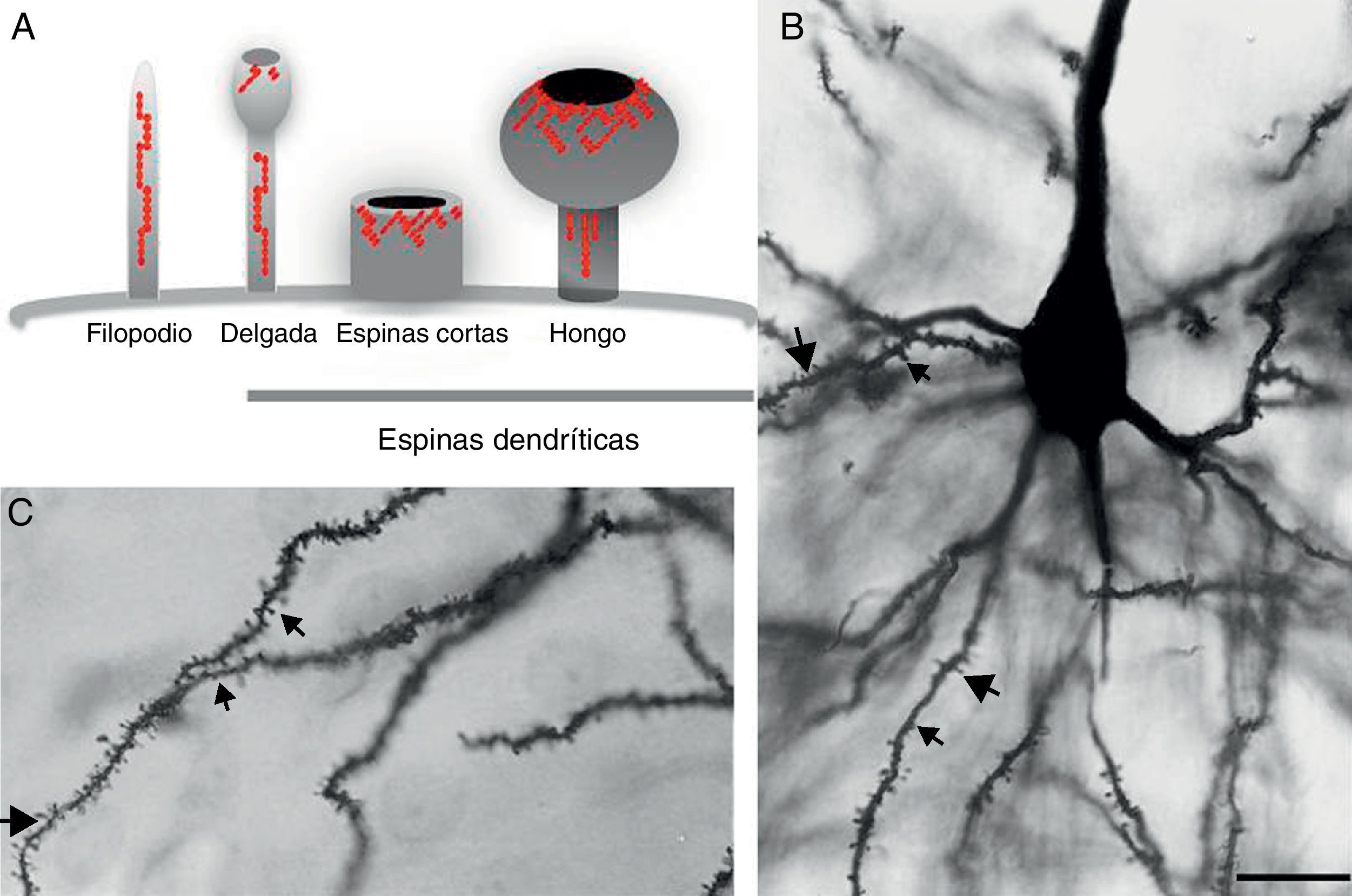
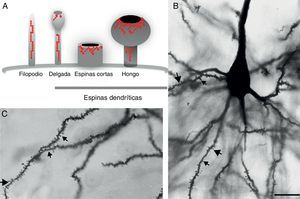
DesarrolloEspinas dendríticas: estructura y funciónLas espinas dendríticas son minúsculas protuberancias protoplasmáticas que revisten la superficie de muchas neuronas y representan el sitio de contacto sináptico de tipo excitador por excelencia. La densidad de estas va de 1 a 10 por micrómetro a lo largo de la longitud de la dendrita. Algunas neuronas como las del hipocampo contienen miles de espinas a lo largo de la arborización dendrítica9. Su estructura consta de tres elementos básicos: a) la base en el cruce con el eje dendrítico, b) el cuello, y c) la cabeza que puede hacer contacto con el axón. Su forma y tamaño es variable. Su longitud va de 0,2 a 2μm, con un volumen de 0,001 a 1μm3. En base a la morfología que presentan se clasifican en: espinas delgadas, espinas cortas sin cuello y espinas con cabeza ancha denominadas espinas hongo1 (fig. 1A y B fig. 2 y B). Lo interesante de estas estructuras es que no son estáticas, su morfología cambia continuamente, incluso a lo largo de la edad adulta, lo que refleja la naturaleza de la plasticidad de las conexiones sinápticas10. Se ha reportado que la morfología de las espinas puede ser modificada por la actividad neuronal in vitro e in vivo por la experiencia11. Los patrones de actividad que inducen la potenciación a largo plazo (del inglés LTP), son uno de los principales mecanismos celulares que subyacen al aprendizaje y la memoria e inducen el alargamiento de las espinas y se ha sugerido que estos cambios son fundamentales en la formación de los trazos de memoria12.
A) Representación esquemática de los filopodios y las espinas dendríticas: delgada, corta sin cuello y hongo. Modificado de Sekino et al.24, 2007. B y C) Fotomicrografía de una neurona piramidal de tercera capa de la corteza cerebral prefrontal de la rata. En la cual se muestra las diferentes formas de espinas dendríticas a lo largo de la dendrita basal. (
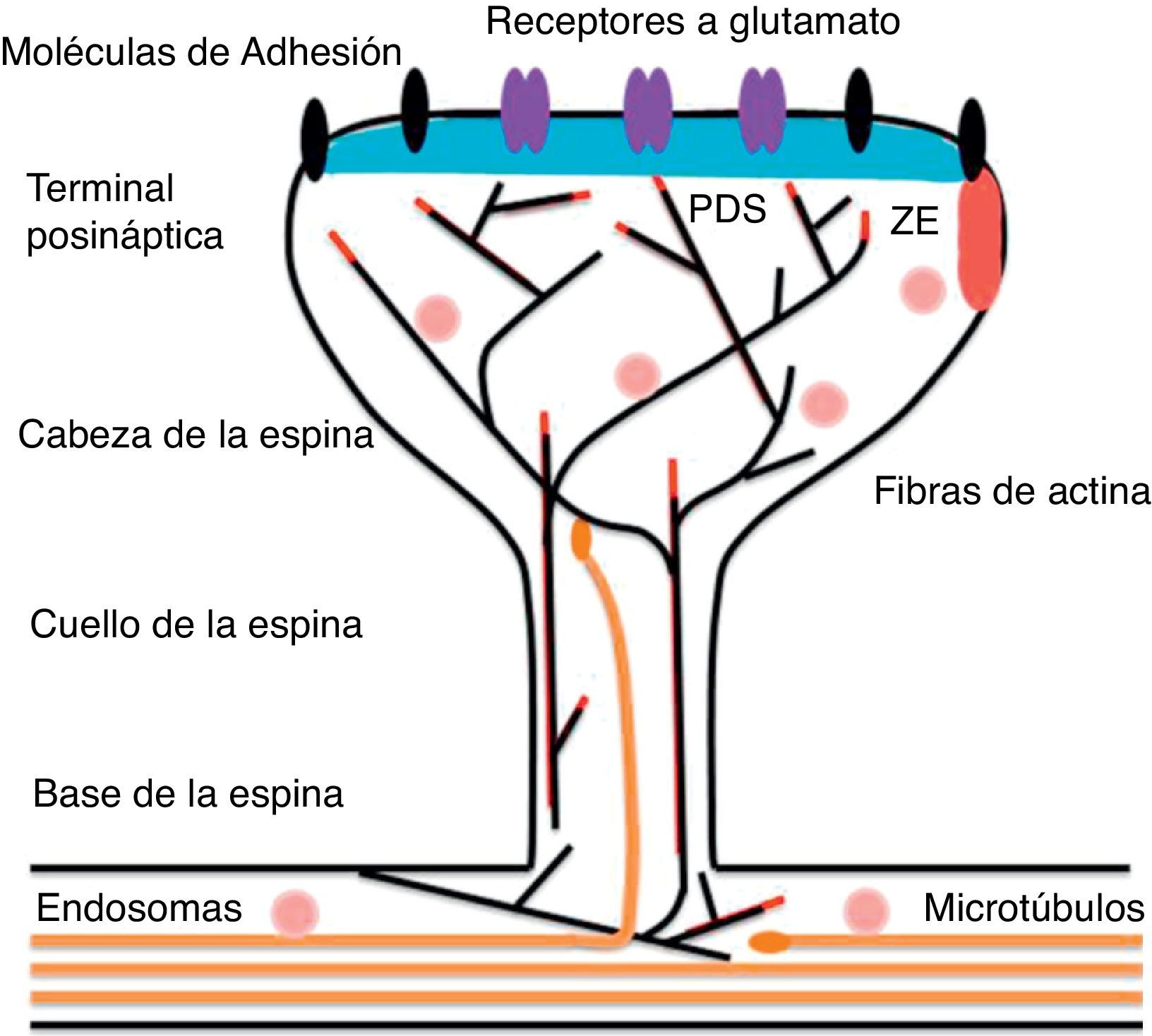
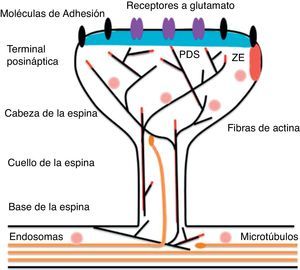
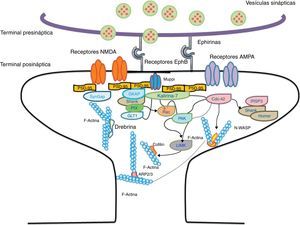
Representación esquemática de una espina en forma de hongo en la que se muestra la maquinaria post-sináptica necesaria para la trasmisión del impulso nervioso. Modificado de Hotulainen y Hoogenraad23, 2010.
Las espinas dendríticas contienen la maquinaria post-sináptica necesaria para la trasmisión del impulso nervioso; incluyen receptores a glutamato, proteínas de densidad post-sináptica (PDS) y el citoesqueleto de actina, así como una amplia variedad de organelos del sistema de endomembranas (retículo endoplasmático liso, mitocondrias y endosomas)13 (fig. 2). La zona de la PDS se encuentra generalmente en parte posterior de la cabeza de la espina dendrítica frontal a la zona activa presináptica. El PDS funciona como una estructura organizadora de diferentes grupos de receptores, moléculas de adhesión y canales iónicos. Une una gran variedad de moléculas de señalización en la membrana posináptica14. La mayoría de las vías de señalización intracelular parecen controlar la forma de las espinas y además convergen de manera directa en el citoesqueleto de actina.
Organización de la actinaLa actina es una proteína monomérica (G-actina) que regula la motilidad y la estructura celular. La fuerza en la motilidad es regulada por la actividad de la ATPasa de la miosina (enzima que hidroliza trifosfato de adenosina) o por la modulación de la propia polimerización y despolimerización de los filamentos de actina (F-actina). Es la principal proteína del citoesqueleto presente en las espinas dendríticas15, forma redes cortas y ramificaciones largas presentes en el cuello de las espinas dendríticas, así como en la cabeza justo por debajo de la PDS (fig. 2). La principal función de las proteínas post-sinápticas en las espinas maduras es la de estabilizar y modular la estructura de la cabeza. Estudios con espectrometría de masas de fracciones de PDS ha reportado que las proteínas; calcio calmodulina dependiente proteína cinasa IIβ (CaMKIIβ), cortactina, drebrina y neurabina I están presentes en esta zona16. Este trabajo ha señalado que la regulación de estas proteínas reduce la formación y la maduración de espinas dendríticas17 y al parecer son cruciales para la plasticidad sináptica y la formación de algunos tipos de memoria18.
Se ha demostrado que el reordenamiento de la actina tiene efectos sobre la formación y/o la pérdida de espinas dendríticas, así como cambios morfológicos (forma y número de espinas). Tanto la forma monomérica (G-actina) como polimérica (F-actina) están presentes en espinas y el grado de polimerización de actina (y, por lo tanto, la relación G-actina/F-actina) influye en la morfología de las espinas dendríticas. Se ha reportado que la inducción del LTP cambia la relación G-actina/F-actina hacia F-actina e incrementa el volumen de las espinas dendríticas. Mientras que la inducción de la depresión a largo plazo (DLP) cambia la relación G-actina/F-actina hacia G-actina (disminución de filamentos de actina) y provoca la contracción de las espinas dendríticas19,20.
Espinas dendríticas y filopodiosLas dendritas inmaduras o en desarrollo se caracterizan por la presencia de pequeñas y finas protuberancias citoplasmáticas filamentosas sin cabeza de más de 3μm de longitud presentes en neuronas inmaduras denominados filopodios, los cuales forman contactos sinápticos que recubren gran parte de las extensiones dendríticas de las neuronas en desarrollo21, el cual puede ser remplazado por espinas maduras y estables.
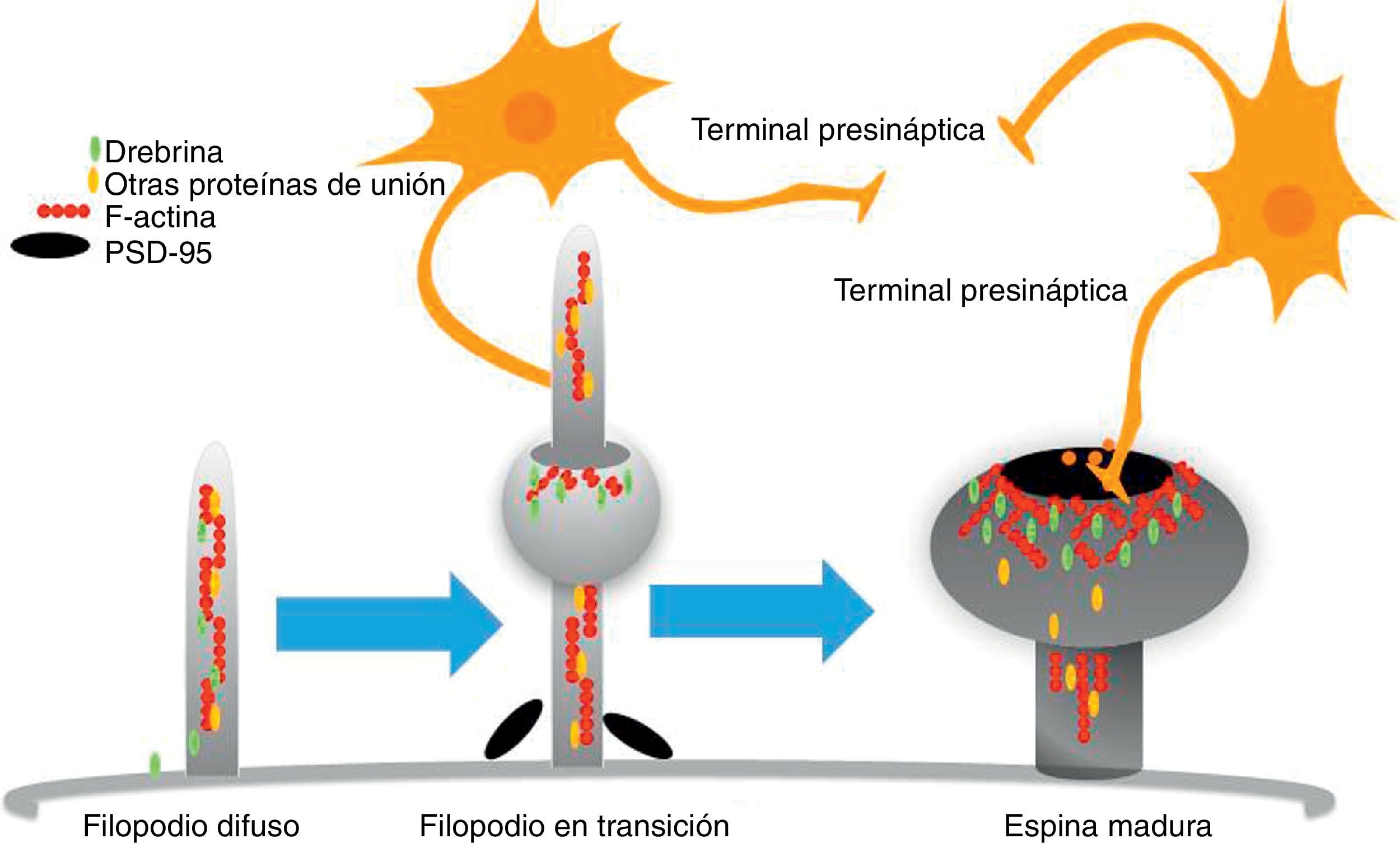
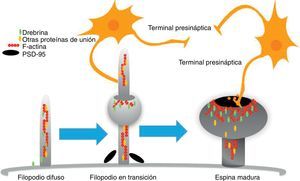
La motilidad de los filopodios y de las espinas depende de F-actina en el citoesqueleto presentes en las espinas. En este sentido, se ha sugerido que la transición de un filopodio a una espina madura involucra la regulación de la actina22. A pesar de que los filopodios desaparecen conforme las espinas maduran, no se ha observado una relación proporcional entre la cantidad de filopodios que se retraen y la cantidad de espinas que se forman; teoría que hasta la fecha es la más aceptada. Al respecto, se ha reportado que los filopodios podrían elongarse y retraerse directamente mediante un contacto sináptico en cualquier sitio de su estructura longitudinal, y se ha propuesto que los filopodios podrían constituir una guía anatómica relacionada con la formación de espinas23 (fig. 3).
Esquema que muestra la formación una espina dendrítica. Las dendritas presentan muchos filopodios en los que se distribuye una proteína de unión al citoesqueleto denominada drebrina. Después de que una terminal axónica establece contacto con los filopodios, se forma un complejo con drebrina y F-actina en un sitio de contacto post-sináptico. El complejo drebrina-actina es esencial para la maduración de espinas dendríticas. Modificado de Sekino et al.24, 2007.
Debido a que los filopodios y las espinas son similares en términos de la presencia de pequeñas protuberancias (0,5-8μm) en el eje dendrítico24, en ocasiones hay confusión entre un filopodio dendrítico y una espina dendrítica. En este sentido, el término filopodio se aplica a todas aquellas protuberancias finas sin cabeza y el término espina dendrítica se aplica al resto de las protuberancias presentes en el eje dendrítico. En general, se asume que los filopodios y las espinas son ambos intrínsecamente diferentes de otros tipos de protuberancias, y que el papel de los filopodios dendríticos es capturar axones y establecer sinapsis tempranas, más que transformarse en espinas (fig. 1).
Proteínas de unión a la actina y espinas dendríticasVarias proteínas de unión a actina han sido identificadas en las espinas dendríticas, como Arp2/3, cortactina, ADF/cofilina, profilina, gelsolina, drebrina y neurabina25, las cuales tienen una participación esencial en la regulación de la organización del F-actina. Una de las proteínas que regulan la longitud de F-actina (mediante corte de los filamentos) es la denominada gelsolina calciodependiente; proteína clave en el ensamblaje y desensamblaje de F-actina. La rotura de F-actina es el paso inicial y directo para acortar la F-actina. La actividad de esta proteína se incrementa por activación del receptor tipo NMDA (N-Metil-D-aspartato) y la consecuente entrada de iones calcio (Ca2+)26.
Otra de las proteínas que se unen a F-actina es la ADF/cofilina, que junto con profilina y gelsolina despolimerizan y regulan la longitud de los F-actina. La cofilina es miembro de la familia ADF/cofilina y poseen una homología del 70% de secuencia de aminoácidos con ADF (actin-depolymerizing factor, factor que despolimeriza la actina). Esta proteína despolimeriza el extremo (–) de los microfilamentos e impide el reensamblado; por ello crea más extremos (+) en los fragmentos de filamentos. Cofilina/ADF realiza una función de corte de F-actina y los monómeros resultantes pueden ser reciclados por la profilina, otra proteína asociada a actina que facilita el cambio de adenosina difosfato (ADP) a adenosina trifosfato (ATP) de los monómeros de actina, lo cual facilita su polimerización27. La profilina es una proteína multifuncional de unión a la actina involucrada en el equilibrio de G-actina/F-actina. Particularmente, incrementa el intercambio de ADP por ATP unido a la actina, lo cual promueve la polimerización de la F-actina28. El cambio de G-actina controlado por la profilina inhibe la polimerización de la F-actina. Por otro lado, se ha demostrado en neuronas del hipocampo en cultivo que la profilina II es la responsable de estabilizar la morfología de las espinas dendríticas. Además, la profilina II puede regular la organización de los F-actina mediante la unión de pequeñas GTPasas (RhoA)29. Por su parte, el complejo Arp2/3 induce la ramificación y entrecruzamiento de los F-actina. Por lo tanto, los F-actina nacientes cuyos extremos están cubiertos por el complejo Arp2/3 están relacionados con la formación de las espinas dendríticas30 (fig. 4).
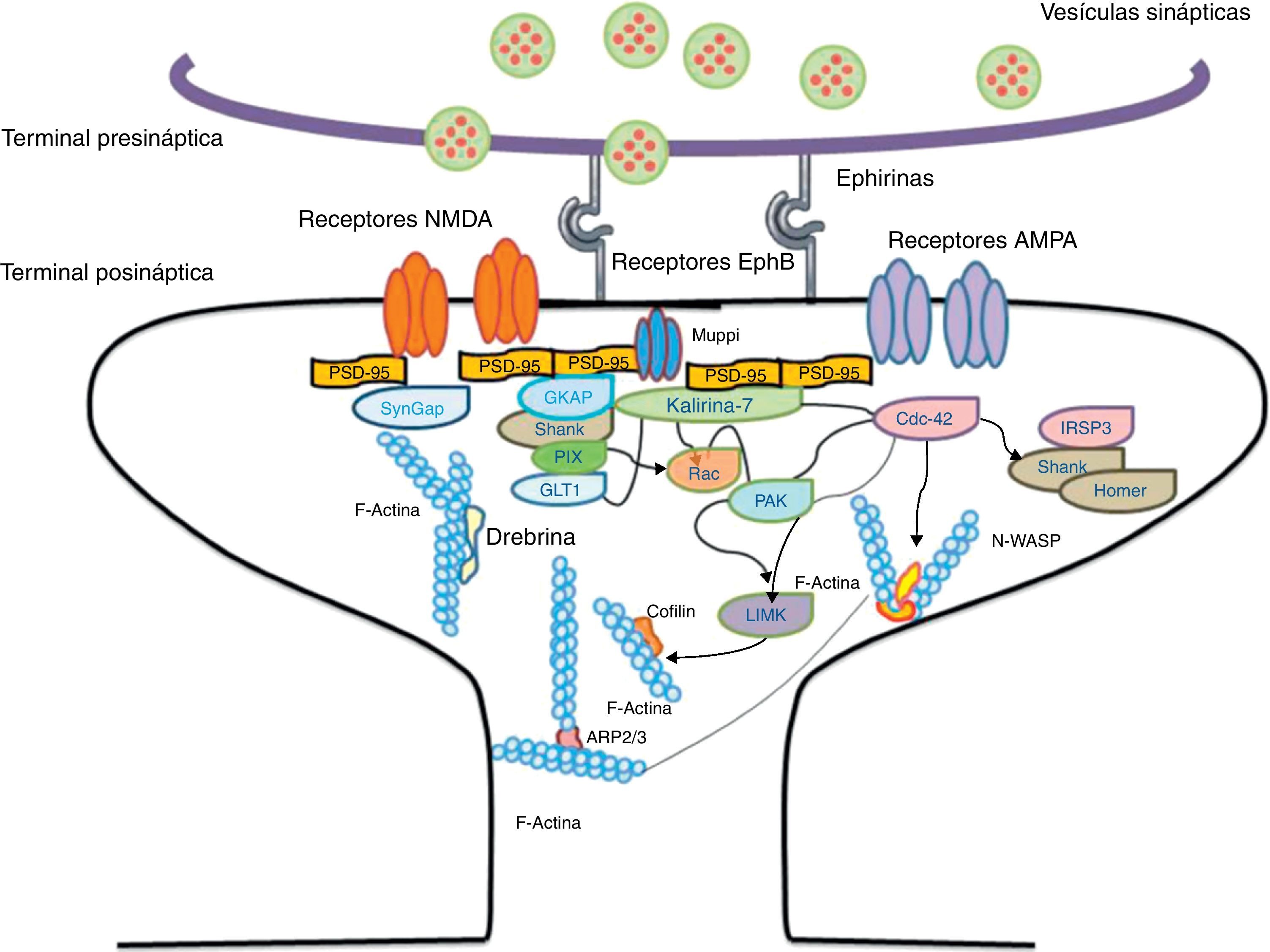
Representación de la cascada de señalizaciones de Rac y Cdc42 activados por los receptores EphB vía kalirina-7. Cdc42 puede promover la polimerización de la actina mediante el complejo IRSp53 (localizado en las espinas conocido como regulador del citoesqueleto de actina). La activación de las vías da inicio al ensamblaje y agrupación de los F-actina esenciales para la formación de los filopodios.
Drebrina ha sido una de las proteínas más ampliamente estudiadas debido a su marcada expresión tanto en espinas como en los filopodios, además de su estrecha relación con los F-actina y por ende su participación en la morfogénesis de las espinas dendríticas31. Esta una proteína de unión al citoesqueleto de actina y es expresada en la mayoría de las neuronas. Diversos estudios han demostrado que se expresa preferentemente en los sitios de contacto post-sinápticos de las dendritas. Inicialmente fue descrita como una proteína reguladora del cerebro cuya expresión máxima ocurre durante la embriogénesis y disminuye en la edad adulta31. Se pueden distinguir dos isoformas; drebrina E en la fase embrionaria y drebrina A en la fase adulta. Esta última, se expresa abundantemente en el cerebro anterior, la corteza cerebral e hipocampo con baja expresión en la corteza cerebelosa, bulbo raquídeo y médula espinal, su expresión es detectada a partir de la cuarta semana después del nacimiento y mantiene un nivel de expresión bajo durante 10 semanas después del nacimiento17. Esto sugiere una rápida conversión de las isoformas de drebrina durante la fase de formación de espinas y de contactos sinápticos. La drebrina A se encarga de regular las fases de maduración de las proto-espinas después del establecimiento de la morfología de estas31. En neuronas maduras drebrina A predomina su localización en las espinas dendríticas, en el soma y en el eje dendrítico, pero nunca en las terminales presinápticas17,31. Un estudio de microscopía inmunoelectrónica in vivo revela que aproximadamente en un 70% de las espinas es posible detectar niveles bajos de drebrina; sin embargo, la inhibición aguda de los receptores tipo NMDA incrementa significativamente el número de espinas positivas a drebrina lo que lleva a postular que drebrina A es regulada por la actividad de este tipo de receptores32. Además, se ha demostrado que drebrina A se acumula en la región submembranosa del sitio de contacto axo-dendrítico, por lo que se ha sugerido que está involucrada en el paso inicial para la unión de drebrina a los F-actina (DBF) para la formación de un filopodio.
Vías de señalización y citoesqueleto de la actinaSe sabe que las vías de señalización intracelular relacionadas con la morfología de las espinas dendríticas son reguladas principalmente por receptores a glutamato de tipo NMDA y AMPA (ácido α-amino-hidrixi-5-metil-4-isoxazolepropiónico). Los receptores tipo NMDA regulan en citoesqueleto de actina mediante: a) la regulación del flujo de iones calcio hacia las neuronas post-sinápticas; lo que modula la actividad de algunas proteínas de unión a la actina, por ejemplo, CaMKIIβ y gelsolina, y b) por la unión directa de la actina o regulación de proteínas, por ejemplo, CaMKII, α-actinina33. Además, varios receptores de tirosina cinasas, como miembros del Trk (receptor BDNF) y las familias de la EphB/ephrina, así como moléculas de adhesión las cuales han demostrado ser importantes en la regulación de la actina en las espinas34.
Receptores EphBLos receptores EphB son una familia de moléculas de adhesión intercelular que controlan aspectos relacionados con el desarrollo neuronal, tales como la formación y maduración de sinapsis, así como la plasticidad sináptica estructural y funcional. Los receptores EphB se encuentran ligados a proteínas cinasas localizadas en la terminal post-sináptica, los cuales son activados por la ephrina localizada en el axón35. Este grupo de moléculas fue caracterizado inicialmente en el sistema nervioso del embrión; las cuales están constituidas por un grupo de receptores denominados Eph y sus ligandos llamados ephirinas, ambos anclados a la membrana extracelular (fig. 4). Se ha reportado que la señalización mediada por estos receptores es esencial para la formación de espinas en el hipocampo36. El uso de ratones transgénicos con doble y triple mutante para los receptores EphB1, EphB2 y EphB3ha demostrado que, en ausencia de los tres receptores, falla la formación de espinas en células de hipocampo (cultivo celular). Por otro lado, se ha reportado in vivo que la densidad de las espinas disminuye cerca de un 25%; sin embargo, la arborización dendrítica es normal y la cabeza de las espinas disminuye. Por último, reportan que la polimerización de los F-actina tanto in vivo como in vitro no se modifican36.
GTP asas y Rho GTPasasLas GTPasas (guanosina trifosfatasa) son una familia de enzimas con más de 100 proteínas estructuralmente relacionadas y que regulan diversas funciones biológicas. Son enzimas de tipo hidrolasa que pueden unirse e hidrolizar la molécula guanosín trifosfato (GTP). Todas las GTPasas poseen un mecanismo común que les permite activar o desactivar la transducción de señales por medio de un cambio unidireccional de la GTPasa activa a la forma inactiva GDP (guanosina difosfatada), este cambio se efectúa por la hidrólisis del GTP por medio de la actividad intrínseca de la misma GTPasa logrando inactivar la cascada de señalización. Esta reacción es iniciada por proteínas específicas denominadas proteínas activadoras de GTPasas (GAP). La inactivación de las GTPasas puede ser revertida por la acción de las GEF (factor de cambio de nucleótidos de guanina) facilitando que la GTP sea remplazada por una GDP37. Proteínas como Rac, Cdc42, Rnd1 y RhoA pertenecen a la familia de las Rho GTPasas y se ha reportado que son importantes reguladores del citoesqueleto de actina, influyen en la morfogénesis de las espinas, además tienen la función de promover el crecimiento y/o estabilización de las espinas dendríticas; cuando RhoA es expresada en altas concentraciones pueden inhibir o contraer las espinas hasta eliminarlas38. Por otro lado, Cdc42 está involucrada en la polimerización de los F-actina; proceso necesario para que un filopodio logre extenderse y elongarse para formar una espina madura. Además, Cdc42 junto con Rac conducen a un reordenamiento de los F-actina en la cabeza de las espinas38 (fig. 4).
Rnd1 puede actuar como un regulador de las espinas dendríticas en las neuronas del hipocampo. Su expresión se incrementa durante el periodo de sinaptogénesis e induce la elongación de las espinas, en tanto que una disminución en su expresión se relaciona con una reducción ligera de la densidad de las espinas39. Diferentes GEF y la activación de proteínas tipo GTPasa parecen controlar la función de las Rho GTPasas.
La activación de RhoA en las espinas dendríticas ha demostrado ser necesario para la expresión de LTP mediante la inactivación cofilina40. En fibroblastos, Cdc42 induce la formación de filopodio y en las espinas dendríticas induce el crecimiento de la cabeza de la espina38. RhoA es importante para inhibir la actividad cofilina y la consecuente estabilización de los F-actina y la espina dendrítica. Rac y Cdc42 regulan formación de cabeza, principalmente por la activación del complejo Arp2/3 e inhibiendo la despolimerización de actina mediante cofilina. Cabe mencionar que la familia Rho GTPasa Rif (Rho en filopodio) es un importante regulador de la formación de filopodio41.
Kalirina-7Es una proteína que pertenece a la familia de las RhoGTPasa GEF, es la más abundante en el cerebro de adultos y participa como regulador de la morfogénesis de neuronas piramidales y en la plasticidad estructural fundamental para el aprendizaje y la memoria42. Funciona como un centro de regulación de múltiples vías de señalización que controlan diversos aspectos de la plasticidad en las espinas. Se le considera como un GEF para Rac, Cdc42 y Rnd1, el cual se expresa en las espinas dendríticas e induce un alargamiento en las espinas con una gran variedad morfológica. Además, puede cumplir la función única de propagación de las señales desde los receptores a la membrana sináptica de actina, ya que cada molécula de kalirina-7 activa varias moléculas de Rac1 y proporciona un paso importante en la cascada de señalizaciones. Además, regula la estructura de las espinas y la expresión sináptica de receptores tipo AMPA42. Por otro lado, se sabe que kalirina-7 es rápidamente fosforilada por proteínas CaMKII en respuesta a la estimulación de los receptores tipo NMDA; mecanismo esencial para el alargamiento y mantenimiento de las espinas43. Asimismo, puede regular el anclaje a la membrana del citoesqueleto celular de los receptores tipo AMPA a través del citoesqueleto. Esto es posible ya que la señalización de kalirina-7 influye en el blanco o diana de dichos receptores, a través de interacciones con proteínas transmembranales (TARP), que son esenciales para el anclaje de receptores AMPA. Todo lo anterior indica que kalirina-7 puede tener un papel central en la transmisión de señales desde los receptores tipo NMDA al citoesqueleto de actina y al transporte de AMPA; base fundamental de la plasticidad sináptica desde el punto de vista estructural y funcional44 (fig. 4). Se ha señalado que la activación de EphB cataliza la fosforilación de tirosinas cinasas de kalirina-7, la cual entra en contacto con Rac1 GDP y esta cataliza el cambio de GDP a GTP cuando se activa Rac1. Kalirina-7 se encuentra concentrada en la densidad posináptica, donde puede interaccionar con diferentes proteínas incluyendo PSD-9545. De manera particular, se ha reportado que la activación de Rac1 por kalirina-7 es mediada por la activación de receptores EphB; necesaria para la formación de espinas en neuronas de hipocampo en cultivo. En este sentido, se ha señalado que la sobreexpresión de kalirina-7 bloquea los efectos de los ligandos de EphB y por ende la formación de espinas42.
Se ha reportado que kalirina-7 se puede asociar con proteínas N-caderinas a través de interacciones con el dominio PDZ de AF-6/afadin. AF-6 es una proteína de unión regulada por GTPasa-Rap. La unión de estas inducen un alargamiento de las espinas involucrando Rac1 y PAK y proporciona la capacidad a las moléculas para regular el reordenamientos post-sinápticos de actina, por lo que esta vía puede ser la base para la rápida coordinación de unión sináptica durante la maduración y plasticidad sináptica, pero también puede garantizar la estabilidad de las espinas en neuronas maduras46.
Karilina-7 interacciona con varias proteínas de PSD, como son PSD-95, SAP102, SAP97 cuya función es transportar receptores de glutamato o ensamblar estos receptores45. Se ha reportado que kalirina-7 puede ser regulada por GTPasa Arf6 y que junto con el activador EFA6 (factor de cambio para Arf6 relacionado con el reciclamiento de membrana y remodelación del citoesqueleto) regula la transición de filopodios a espinas maduras y estables47.
Otro GEF que se encuentra implicado en la morfogénesis de las espinas dendríticas es PIX el cual también por otra vía puede activar a Rac y a Cdc4248. Cdc42 es una de las principales vías de señalización que promueve la ramificación de las cabezas de las espinas dendríticas por la activación de N-WASP (proteína neuronal del síndrome Wiscott-Aldrich). La polimerización de la actina está mediada por el complejo Arp2/3. Se han descrito dos familias de proteínas que activan a N-WASP; así la activación de Arp2/3 polimeriza la actina y conduce al alargamiento de las cabezas de las espinas49 (fig. 4). Ras es otra proteína de la familia de las GTPasas la cual puede también activar algunas Rho y Ras activadores de GTPasas (GEF) y las inhibidoras (GAP), las cuales han mostrado ser fundamentales en la morfología y el crecimiento neuronal 50. Un importante inhibidor post-sináptico de señalización Ras es GAP sináptico (Syn-GAP) localizado en la PSD. La eliminación de Syn-GAP en ratones ha mostrado incrementar en el número de espinas en forma de hongo en neuronas del hipocampo51. Las mutaciones en la familia varios Rho y Ras GEF se han relacionado con el retraso mental52.
En cambio Rap GTPasas está estrechamente relacionada a Ras, pero parecen tener una función opuesta a la plasticidad sináptica. Ras y Rap actúan antagónicamente en el compartimiento post-sináptico sobre la regulación de la morfología de las espinas53.
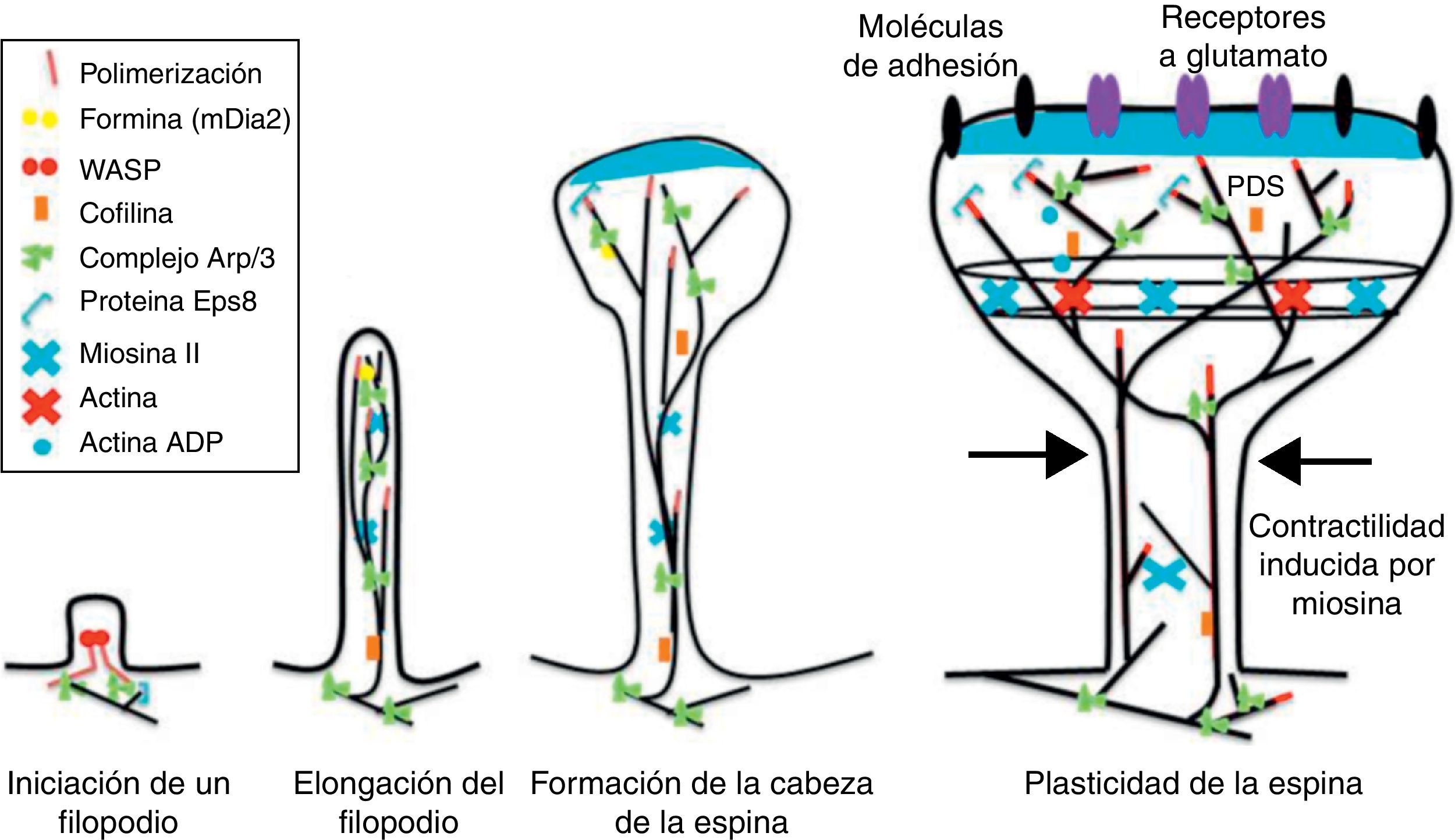
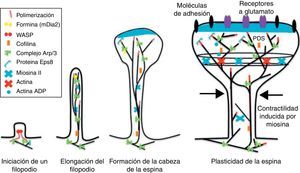
Iniciación y alargamiento de los filopodios dendríticosLos mecanismos moleculares involucrados en la iniciación de los filopodios dendríticos son poco conocidos. Los filopodios inician en el eje dendrítico, a menudo a partir de pequeñas agrupaciones de actina ramificada o de los llamados lamelipodios20. Se ha propuesto un modelo de iniciación de forma azarosa e inducido por una señal de iniciación. Se ha demostrado que el glutamato liberado desde la terminal presináptica tiene influencia sobre la iniciación y elongación del filopodio54. Se han descrito los posibles mecanismos implicados en el proceso de iniciación y elongación: a) la proteína denominada Ena/VASP une los filamentos generados por el complejo de Arp2/3 con lo cual podría iniciar la elongación del filamento; b) una proteína llamada formina tipo DRF3/mDia2 es importante para la correcta formación del filopodio. Es posible que otras proteínas de la familia formina participen en la polimerización de filamentos de actina y se de la iniciación y elongación de los filopodios; c) se ha propuesto que la miosina podría iniciar la formación del filopodio y que el movimiento lateral de la miosina en los extremos de los filamentos de actina produce la base del filopodio; d) los F-actina con frecuencia residen en los microtúbulos del eje dendrítico. De esta forma, grupos de F-actina asociada a los microtúbulos inician el filopodio; e) microtúbulos y F-actina unidos a la proteína septina 7 polimerizan filamentos hetero-trimétricos y forma pequeñas estructuras en forma de anillo. Con esto podrían iniciar la formación del filopodio y funcionar como una «barrera de difusión» en la maduración de las espinas dendríticas, y f) la iniciación de los filopodios podría producirse a través de la deformación de la membrana y de los dominios proteicos denominados I-BAR (del inglés inversa Amphiphysin/Bin/Rvs). Las interacciones electrostáticas entre los extremos cargados positivamente de los dominios I-BAR y de los grupos hidrofóbicos del fosfatidil-inositol-4-bi-fosfato [PI (4,5) P2] cargados negativamente inducen la generación de un curvatura de membrana debido a la geometría convexa de la interfaz de enlace de los lípidos. En neuronas en cultivo el abatimiento de proteínas I-BAR ha demostrado afectar morfogénesis espina dendrítica21 (fig. 5).
Mecanismos reguladores de actina durante el desarrollo las espinas dendríticas. Modificado de Hotulainen y Hoogenraad23, 2010.
Una vez formado el filopodio dendrítico y realizado el establecimiento del contacto axonal, la motilidad disminuye gradualmente y se estabiliza la estructura de la espina dendrítica35. Las espinas recién formadas normalmente son delgadas, largas y de cabeza pequeña. El complejo de Arp2/3 es necesario para crecimiento de cabeza espina. De forma alterna, los microtúbulos de espinas dendríticas puede inducir la activación del complejo Arp2/3. Se ha demostrado que los microtúbulos están asociados con los cambios morfológicos transitorios relacionados con la formación de la cabeza de la espina y el crecimiento de la espina dendrítica55. Los microtúbulos pueden inducir una cascada de señalización que afectan a la dinámica de actina a través de la proteína EB355. Un estudio de proteómica para patrones de unión a EB en las neuronas del hipocampo mostraron que p140Cap era una proteína que interacciona con SNAP-25 (proteína tipo PSD abundante en las espinas)55 y que además era importante regulador de tirosinas cinasas Src. El factor p140Cap también puede interaccionar con una proteína denominada cortactina que en un momento dado podría activar el complejo de Arp2/3 y estabilizar y promover la formación espinas en forma de hongo55. Es probable que la asociación entre EB3 enlazados a los extremos de los microtúbulos y p140Cap controlen la actividad del Src cinasa y regule la función de la cortactina, que podría conducir a la activación del complejo Arp2/3 y al crecimiento de la cabeza de la espina. De esta forma, los microtúbulos en las neuronas maduras pueden funcionar como señal local en la reorganización del citoesqueleto de actina y regular el tamaño de la cabeza de la espina.
Por su parte, la actividad de la miosina II modifica el tamaño y la forma de espinas; proceso importante en morfogénesis de la espina dendrítica. Por otro lado, se ha demostrado que la actina junto con proteínas como CaMKIIβ, neurabina y drebrina A participan en la modificación y estabilización de la cabeza de las espinas dendríticas17. La actividad de cofilina es importante en la morfología y estabilización de las espinas41. Además, se ha mencionado que la plasticidad sináptica se ha asociado con una rápida y persistente reorganización del citoesqueleto de actina en la espina.
Espinas dendríticas y alteración de la función cerebralLas espinas dendríticas pueden responder morfológicamente a una gran variedad de estímulos fisiológicos. Las respuestas a diferentes condiciones de estimulación o de daño, van desde aumento o disminución de su número total, una redistribución a lo largo de las dendritas progenitoras o variaciones en su tamaño o forma geométrica. Se ha reportado que en la denervación parcial de una vía neural, los axones remanentes pueden presentar una multiplicación de sus ramificaciones, fenómeno conocido como rebrote axonal56. Así, el grado de longitud y la ramificación dendrítica, así como de la densidad, forma y distribución de las espinas dendríticas, parecen estar influidos por una gran diversidad de factores medioambientales como la desnutrición, la privación sensorial, el estrés, la denervación y por procesos de aprendizaje, entre otros57.
Se ha demostrado que la lesión farmacológica del núcleo del rafe dorsal (NRD) con 5,7-Dihidroxytriptamina (5,7-DHT) en la rata provoca una disminución en el contingente de fibras serotoninérgicas a la corteza cerebral prefrontal58 y produce modificaciones en la citoarquitectura de neuronas piramidales de dicha región correlativamente con alteraciones en la ejecución de una tarea que requiere de la evocación de recuerdos adquiridos en el corto plazo, así como un incremento en el número y forma de espinas dendríticas59, además de un incremento en el número de receptores a serotonina tipo 5-HT2A, así como incremento en la expresión de drebrina58,60. En este sentido, se sugiere que la activación de diferentes tipos de receptores podría inducir la movilidad de proteínas de unión al citoesqueleto como drebrina y modular los cambios morfológicos antes mencionados como respuesta plástica que el SNC pone en marcha bajo el paradigma de lesión del NRD. Pero no hay que descartar la participación de otras proteínas de unión al citoesqueleto o bien otros mecanismos intracelulares.
Por otro lado, existen reportes en la literatura los cuales han relacionado las alteraciones morfológicas de las espinas dendríticas con algunos trastornos psiquiátricos y neurológicos61. Al respecto se sabe que mutaciones en la proteína sináptica denominada Shank3 y de moléculas adhesión como neuroligina3 y neuroligina4 están relacionadas con el autismo62. Otro estudio sugiere que varios trastornos de la memoria están directamente relacionados con defectos en la regulación del citoesqueleto de actina53. Por otro lado, la disminución de los niveles de PAK3 se ha relacionado con alteraciones en la transmisión sináptica en la enfermedad de Alzheimer. Experimentalmente, la inhibición de PAK3 en ratones provoca deterioro en memoria, lo que se ha correlacionado con una probable y potencial participación causal de PAK en la disminución de la memoria en la enfermedad de Alzheimer63. Más estudios desde el punto de vista de la genética identificarán nuevas mutaciones que podrían estar afectando el reordenamiento del citoesqueleto de actina de las espinas dendríticas. Además, el estudio de los mecanismos biológicos a nivel celular que subyacen a desarrollo de las espinas dendríticas conducirá a una mejor comprensión de la plasticidad sináptica, función cerebral y enfermedades neurológicas.
ConclusionesUn gran número de moléculas y vías de señalización está involucrado en la morfogénesis de espinas dendríticas, debido quizás a que estas son el principal sitio de contacto de tipo excitador. Se han reportado varios mecanismos que afectan al desarrollo, el mantenimiento y la plasticidad de las sinapsis de tipo excitador, lo que podría influir en el número, el tamaño y la forma de las espinas dendríticas. Por otro lado, el uso de modelos experimentales, tanto in vivo como in Vitro, acerca de la función del citoesqueleto y su relación con las espinas dendríticas ha reportado datos importantes relacionados con el entendimiento de los mecanismos moleculares que subyacen a los cambios plásticos relacionados con la morfogénesis de las espinas dendríticas. Dada la relación que existe entre la disfunción cerebral y las anormalidades de las espinas dendríticas, se ha pensado que la morfología de las espinas es importante para el entendimiento de la función sináptica y, por ende, de las funciones cerebrales superiores. Se sabe que los cambios morfológicos de las espinas son instantáneos y se deben a la dinámica del citoesqueleto actina de la espina dendrítica. Además, se ha demostrado que proteínas de unión a la actina, como drebrina A, es la responsable de la formación de los F-actina y PSD-95 en los filopodios, lo que da como resultado la formación de las espinas dendríticas. Drebrina, al ser una de las primeras proteínas de unión a la actina, controla la asociación de otras proteínas de unión a F-actina. Por lo tanto, existen trabajos que apoyan a las proteínas de unión a la actina como las responsables de regular los cambios morfológicos de las espinas dendríticas. Cabe mencionar que a la fecha la función precisa de algunas proteínas reguladoras de la actina es poco conocida, por lo que el estudio detallado de las proteínas de unión a la actina, así como la interacción de las vías de señalización de las espinas dendríticas, proporcionarán un avance importante sobre la comprensión de los mecanismo de regulación de la organización de los F-actina y su asociación con las funciones cognitivas (aprendizaje y memoria). Por otro lado, aplicación de técnicas moleculares en modelos de plasticidad cerebral tanto in vivo como in vitro permitirán en un futuro identificar los factores que regulan el crecimiento y densidad de las espinas dendríticas, así como los fenómenos plásticos que el cerebro pone en marcha durante la formación de nuevas conexiones neuronales bajo condiciones normales como patológicas. Dado que anormalidades en la morfología de las espinas dendríticas se han asociado con diversas enfermedades neurodegenerativas y de aquellas relacionadas con el retraso mental.
Conflictos de interesesLos autores declaran no tener ningún conflicto de intereses.
El presente trabajo se realizó durante el periodo de apoyo al proyecto PS-2009-610 otorgado por Consejo Estatal de Ciencia y Tecnología de Estado de Jalisco a la Universidad de Guadalajara (COECyTJal-UdG) y al primer autor.