El modafinilo es un fármaco estimulante del sistema nervioso central con mecanismo de acción diferente al de otros fármacos de su clase, que tiene su principal indicación en el tratamiento de la somnolencia excesiva por diversas causas. Además se ha utilizado para aliviar astenia en pacientes con enfermedades neurodegenerativas con resultados positivos.
Siguiendo la tendencia de utilización de psicoestimulantes (metilfenidato, p.e.) para alivio de problemas sintomáticos en Cuidados Paliativos, hay un creciente interés por el modafinilo como fármaco potencialmente eficaz para alivio de la astenia.
Con la finalidad de explorar la utilidad potencial de modafinilo para tratar astenia en enfermos con cáncer avanzado, hemos realizado una puesta al día. Se analizan los trabajos publicados en los últimos diez años sobre modafinilo, dedicando particular atención a los aspectos prácticos de su uso (perfil de los enfermos, pautas de inicio y mantenimiento, efectos secundarios, etc.) y a los estudios prospectivos y aleatorizados en astenia en pacientes con cáncer.
El perfil farmacológico del modafinilo parece adecuado para enfermos con cáncer avanzado. Cuatro estudios prospectivos y tres aleatorizados han explorado su uso, todos realizados desde el año 2005.
De los 157 pacientes tratados prospectivamente con 200mg de modafinilo, entre un 46-90% mejoraron significativamente la astenia. En dos de los tres trabajos aleatorizados, se encontró una mejoría significativa de la astenia. En todos el modafinilo resultó bien tolerado. Estos resultados justifican nuevos estudios con modafinilo para tratamiento de la astenia en los pacientes con cáncer avanzado y mientras tanto el modafinilo puede ser considerado una alternativa para el tratamiento de astenia por cáncer.
Modafinil is a psychostimulant with a different mechanism of action to other similar drugs. It is approved for the treatment of excessive daytime sleepiness in relation with several causes. It has also been used in neurology illness- related fatigue with positive results. There is an increasing interest in modafinil as a potentially effective drug to improve fatigue.
Following the trend to use other psychostimulants (e.g.,methylphenidate) to improve symptomatic problems in Palliative Care, we performed a review with the aim of exploring the use of modafinil to alleviate cancer - related fatigue.
We analysed modafinil articles published in the last ten years, with particular attention to the practical aspects of its use (type of patient, dose, secondary effects, etc.), as well as prospective studies and randomised trials on cancer-related fatigue.
The pharmacological profile of Modafinil is appropiate for advanced cancer patients. Four prospective studies and three randomised trials have examined its use since 2005.
Between 46-90% of the 157 patients treated with 200mg of modafinil had a significant improvement in fatigue. There were significant improvements in fatigue in two of the three randomised trials. Modafinil had a good tolerance in all of them. These results justify further research into the treatment of cancer-related fatigue, and meanwhile modafinil could be considered as an alternative for cancer - related fatigue.
El modafinilo es un fármaco estimulante del sistema nervioso central que difiere en la estructura y en el mecanismo de acción de otros psicoestimulantes como la anfetamina y el metilfenidato. Fue sintetizado a finales de 1970 a partir del adrafenilo, un compuesto que se usó de manera experimental en el tratamiento de la narcolepsia. Ha sido empleado para promover la vigilia en profesiones en las que es más probable que se altere el ciclo circadiano1,2 y es conocido su uso entre los estudiantes para mejorar el rendimiento en época de exámenes.
FarmacologíaEl modafinilo es una sustancia racémica con enantiómeros R y S que muestran propiedades farmacocinéticas diferentes. La absorción oral del modafinilo es rápida; las concentraciones máximas en plasma se alcanzan a las 2-4 horas aunque la presencia de comida en el tracto intestinal puede enlentecer la velocidad de absorción. La semivida plasmática es de 10-12 horas. La situación de equilibrio se alcanza en 2-4 días. El modafinilo es una molécula lipofílica con una unión a proteínas plasmáticas (principalmente a la albúmina) cercana al 60%. La mayor parte del modafinilo se elimina por metabolismo hepático mediado por el citocromo P450. El modafinilo induce varias enzimas del citocromo P450, como CYP1A2, CYP2B6 y CYP3A4, con lo que puede alterar la concentración plasmática de otros fármacos como etinilestradiol, triazolam o ciclosporina. También puede inhibir la CYP2C19, lo que incrementaría las concentraciones de diazepam y fenitoína3. Se conocen dos metabolitos inactivos del modafinilo, ácido modafinílico y modafinil-sulfona, que se eliminan por vía renal. Menos del 10% de la dosis administrada se elimina como fármaco activo sin metabolizar. La eliminación está enlentecida en individuos ancianos o con insuficiencia hepática o renal4.
El armodafinilo es el enantiómero R del modafinilo. Sus propiedades farmacológicas son similares a las del modafinilo; de hecho tiene las mismas aprobaciones que el modafinilo por la Food and Drug Administration (FDA) desde el año 2007. Sin embargo, aunque la semivida plasmática es similar a la de la forma racémica, presenta unas concentraciones a largo plazo (horas) algo más elevadas5,6. Además, el armodafinilo no induce al CYP1A2, aunque es un inductor moderado del CYP3A4 y un inhibidor moderado del CYP2C19 en sujetos sanos7. Aún no hay evidencia de su eficacia en el tratamiento de la astenia8.
El mecanismo de acción del modafinilo no se conoce aún con detalle. Los estudios in vitro sugieren distintos efectos neuroquímicos. Los neurotransmisores centrales que parecen relacionados con el modafinilo son los transportadores de dopamina y noradrenalina a los que inhibe de forma significativa con las dosis usadas clínicamente. Además, el modafinilo eleva los niveles extracelulares de dopamina, noradrenalina, serotonina, histamina, glutamato y disminuye los de GABA9. Sus efectos se producen principalmente en el hipotálamo anterior, un área específicamente involucrada en la regulación del sueño10. Algunos estudios sugieren que el modafinilo aumenta el acoplamiento electrotónico neuronal que subyace a la liberación de los neurotransmisores en las sinapsis corticales11,12. Este aumento del acoplamiento electrotónico parece asociarse a una reducción de la actividad en las neuronas gabaérgicas cuya función normal es reducir la liberación de neurotransmisores en otras células13. Por otra parte, el modafinilo también se emplea en la narcolepsia, un problema caracterizado por una deficiencia severa de orexinas. Se ha supuesto un cierto efecto del modafinilo en la activación de las neuronas de orexina que se encuentran en el hipotálamo y se proyectan a varias áreas del cerebro que regulan la vigilia mediante el aumento de los niveles de dopamina y noradrenalina en estas áreas, que se asocia a la activación de neuronas histaminérgicas14.
Usos clínicosEl modafinilo se ha utilizado en trastornos asociados con somnolencia, alteraciones cognitivas, abusos de drogas y astenia15. En 1998 recibió la aprobación de la FDA para su uso en el tratamiento de la somnolencia diurna en pacientes con narcolepsia, en los trastornos del sueño por turnos de trabajo y en el síndrome de apnea obstructiva del sueño (SAOS) con somnolencia excesiva residual a pesar del uso óptimo de presión positiva continua (CPAP). En estos casos se aprecia una mejoría de la somnolencia, el comportamiento, el estado funcional y la calidad de vida de los pacientes16,17. En Francia el uso de modafinilo fue admitido en 1994 para el tratamiento de somnolencia excesiva por narcolepsia. Esta indicación está admitida actualmente en más de 30 países. En el 2002 se ampliaron las aprobaciones en Reino Unido para la somnolencia diurna en pacientes con SAOS. Esta indicación se aceptó en Alemania e Irlanda en 2010. Además se ha empleado en el tratamiento de la somnolencia diurna asociada a patologías como enfermedad de Parkinson18,19, distrofia miotónica20,21, lesión cerebral traumática22 y depresión23, así como para el control de somnolencia por opioides en dolor no oncológico24.
El modafinilo es eficaz en el trastorno por déficit de atención con hiperactividad en niños y adolescentes mejorando sus síntomas y conducta.25,26 Hay estudios que muestran beneficio del modafinilo en la función cognitiva en pacientes con patología psiquiátricas tipo esquizofrenia27, déficit de atención por hiperactividad en adultos28 y trastorno bipolar29. También ha mostrado eficacia en el tratamiento de adicciones (cocaína, metanfetamina30). Disminuye la autoadministración de cocaína y atenúa la euforia y sus efectos cardiovasculares; además, los pacientes tratados tienen más probabilidades de lograr la abstinencia prolongada31.
Modafinilo y asteniaModafinilo puede ser útil en el tratamiento de la astenia en patologías tan diversas como cirrosis biliar primaria32, fibromialgia33, enfermedad Charcot-Marie-Tooth34 o tras la sedación por anestesia35. La eficacia y seguridad del modafinilo en el tratamiento de astenia en la esclerosis múltiple se ha evidenciado en dos estudios comparativos con distribución aleatoria36,37. Un tercer estudio no llegó a confirmar este dato38, pero el ensayo presenta limitaciones metodológicas en cuanto a dosis, pauta y valoración que limitan la validez de los resultados39,40. También hay estudios en astenia en enfermos con esclerosis lateral amiotrófica (ELA)41,42. En los accidentes cerebrovasculares el modafinilo obtiene cierto efecto en los casos de afectación diencefálica y del tronco cerebral43. En pacientes con VIH, se ha empleado en astenia y función cognitiva44,45. En psiquiatría se ha estudiado modafinilo en el trastorno depresivo mayor, que con frecuencia se asocia a astenia46, y se ha empleado como adyuvante de los inhibidores selectivos de la recaptación de serotonina y como en terapia de reemplazo en respondedores parciales a estos fármacos47–49.
La astenia en relación con el cáncer es una sensación subjetiva de cansancio inusual y persistente relacionada con el cáncer o su tratamiento y que interfiere con la funcionalidad habitual50 y es uno de los síntomas que más influye en la calidad de vida51. La astenia afecta a la gran mayoría de los enfermos oncológicos que reciben quimioterapia y/o radioterapia52 y para muchos constituye uno de los problemas más limitantes incluso meses después de finalizar el tratamiento53. En programas de cuidados paliativos la prevalencia de astenia supera el 80% de los enfermos54.
La estrategia terapéutica incluye el tratamiento de las causas potencialmente reversibles como anemia55, infección, fiebre, deshidratación, desequilibrios electrolíticos y hormonales, alteraciones del ánimo o del sueño o la toma de fármacos. Dentro del tratamiento específico se incluyen medidas no farmacológicas como el ejercicio físico56. No existe consenso sobre el manejo farmacológico en el control sintomático de la astenia aunque hay una clara tendencia al empleo de psicoestimulantes. El metilfenidato es el mejor estudiado. Hay datos de metaanálisis que sugieren cierto beneficio del metilfenidato en comparación con placebo57. La dextroanfetamina y la pemolina se han mostrado eficaces en enfermos con VIH58,59, pero no han alcanzado aún el mismo perfil en pacientes oncológicos. Una nueva vía de investigación es el modafinilo que presenta un perfil farmacodinámico diferente.
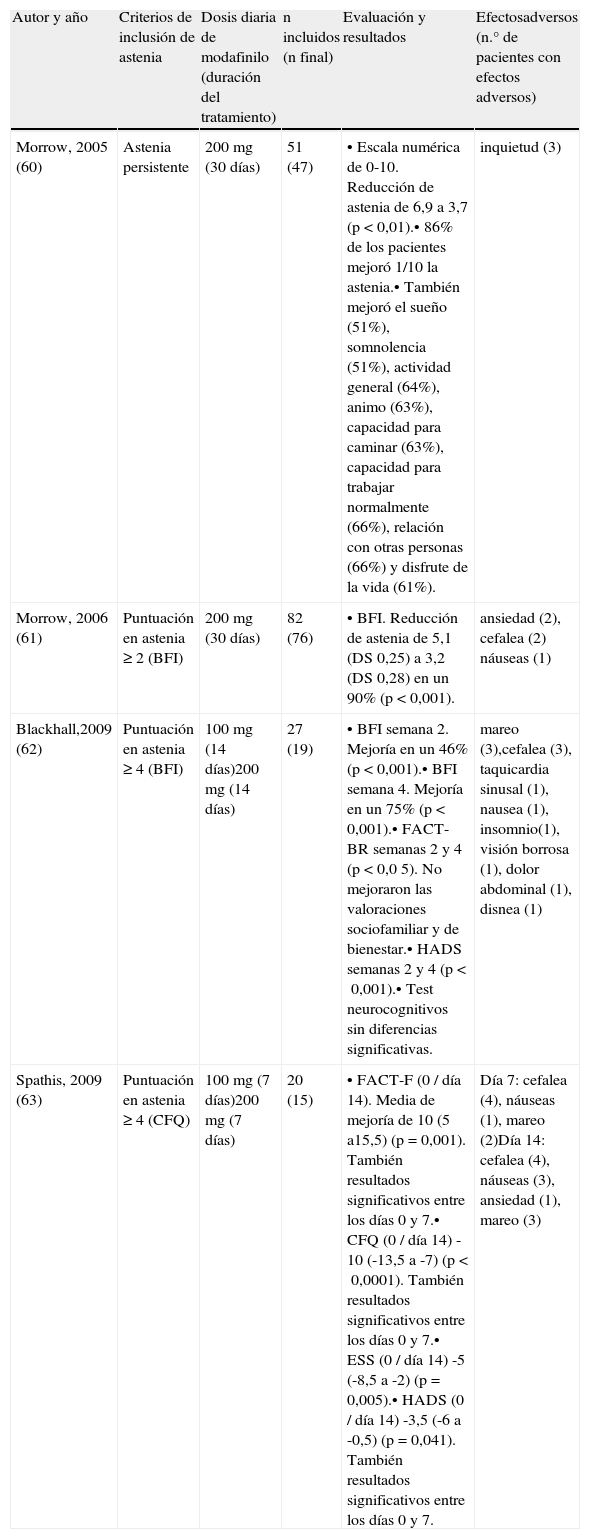
Estudios prospectivos de modafinilo en astenia por cáncerEl primer estudio con modafinilo en el tratamiento de astenia por cáncer se publicó en 2005 (tabla 1). Es un estudio prospectivo con 51 pacientes con astenia persistente a pesar de haber concluido el tratamiento complementario con quimioterapia un promedio de 24 meses antes. La astenia se valoró mediante una escala numérica de 0 a 10. Las pacientes fueron tratadas con modafinilo 200mg diarios en el desayuno a lo largo de un mes. La media de astenia se redujo de 6,9 a 3,7; el 86% tuvo una mejoría en astenia de al menos 1 punto. También se observaron efectos favorables sobre la actividad, el estado de ánimo, la relación con otras personas o la calidad del sueño. Tres (6%) pacientes abandonaron el estudio por inquietud psicomotriz60. Este estudio se complementó con un nuevo ensayo con pacientes con cáncer de mama que habían concluido la radioterapia al menos un mes antes. La astenia se evaluó mediante la Brief Fatigue Inventory (BFI). Setenta y seis pacientes completaron el estudio, de ellas, el 90% refirió mejoría de la astenia. Cinco (7%) abandonaron el estudio por intolerancia el estudio (ansiedad, cefalea o náuseas)61.
Estudios prospectivos sobre el uso de modafinilo en astenia en pacientes con cáncer avanzado
| Autor y año | Criterios de inclusión de astenia | Dosis diaria de modafinilo (duración del tratamiento) | n incluidos (n final) | Evaluación y resultados | Efectosadversos (n.° de pacientes con efectos adversos) |
| Morrow, 2005 (60) | Astenia persistente | 200mg (30 días) | 51 (47) | • Escala numérica de 0-10. Reducción de astenia de 6,9 a 3,7 (p<0,01).• 86% de los pacientes mejoró 1/10 la astenia.• También mejoró el sueño (51%), somnolencia (51%), actividad general (64%), animo (63%), capacidad para caminar (63%), capacidad para trabajar normalmente (66%), relación con otras personas (66%) y disfrute de la vida (61%). | inquietud (3) |
| Morrow, 2006 (61) | Puntuación en astenia≥2 (BFI) | 200mg (30 días) | 82 (76) | • BFI. Reducción de astenia de 5,1 (DS 0,25) a 3,2 (DS 0,28) en un 90% (p<0,001). | ansiedad (2), cefalea (2) náuseas (1) |
| Blackhall,2009 (62) | Puntuación en astenia≥4 (BFI) | 100mg (14 días)200mg (14 días) | 27 (19) | • BFI semana 2. Mejoría en un 46% (p<0,001).• BFI semana 4. Mejoría en un 75% (p<0,001).• FACT-BR semanas 2 y 4 (p<0,0 5). No mejoraron las valoraciones sociofamiliar y de bienestar.• HADS semanas 2 y 4 (p<0,001).• Test neurocognitivos sin diferencias significativas. | mareo (3),cefalea (3), taquicardia sinusal (1), nausea (1), insomnio(1), visión borrosa (1), dolor abdominal (1), disnea (1) |
| Spathis, 2009 (63) | Puntuación en astenia≥4 (CFQ) | 100mg (7 días)200mg (7 días) | 20 (15) | • FACT-F (0 / día 14). Media de mejoría de 10 (5 a15,5) (p=0,001). También resultados significativos entre los días 0 y 7.• CFQ (0 / día 14) -10 (-13,5 a -7) (p<0,0001). También resultados significativos entre los días 0 y 7.• ESS (0 / día 14) -5 (-8,5 a -2) (p=0,005).• HADS (0 / día 14) -3,5 (-6 a -0,5) (p=0,041). También resultados significativos entre los días 0 y 7. | Día 7: cefalea (4), náuseas (1), mareo (2)Día 14: cefalea (4), náuseas (3), ansiedad (1), mareo (3) |
BFI: Brief Fatigue Inventory; CFQ: Chalder Fatigue Questionnarie; FACT- BR: Functional Assessment of Cancer Therapy – Brain; FACT- F: Functional Assessment of Cancer Therapy – Fatigue; HADS: Hospital Anxiety and Depression Scale; ESS: Epworth Sleepiness Scale.
En 2009 se publicó un estudio piloto con 27 pacientes oncológicos que referían astenia (≥4 en el BFI) en que se descartaron causas reversibles como anemia, hipotiroidismo o hipercalcemia. Los pacientes fueron tratados con modafinilo en dosis diarias de 100mg durante dos semanas, y posteriormente con 200mg las dos semanas siguientes. Las evaluaciones se realizaron al inicio del estudio y al cabo de dos y cuatro semanas. Diecinueve pacientes completaron el tratamiento. La astenia (BFI) mejoró en el 46% de los pacientes a las dos semanas y en el 75% a las cuatro semanas. También mejoraron los niveles de ansiedad (Hospital Anxiety and Depression Scale, HADS) y el estado general (Eastern Cooperative Oncology Group, ECOG). Los efectos secundarios más comunes fueron mareo y cefalea. Solo un paciente interrumpió el tratamiento por toxicidad62.
También de 2009 es el estudio piloto con 20 pacientes con cáncer de pulmón no microcítico avanzado. La astenia se evaluó mediante la subescala de astenia Functional Assessment of Cancer Therapy (FACT-Fatigue) y el cuestionario Chalder Fatigue Questionnaire (CFQ). El estudio duró 14 días. El modafinilo fue administrado en una dosis fija diaria de 100mg los primeros siete días y de 200mg los siete días siguiente. Las evaluaciones se realizaron al inicio del estudio y los días 7 y 14. Completaron el estudio 15 pacientes. La puntuación media del FACT-F mejoró significativamente respecto a la inicial los días 7 y 14. Los efectos secundarios más frecuentes fueron cefalea, mareo y náuseas. Diez de los pacientes optaron por continuar el tratamiento con modafinilo una vez concluidos los 14 días previstos del estudio63.
Estudios controlados de modafinilo en astenia por cáncerHasta la fecha se han publicado tres estudios clínicos comparativos con distribución aleatoria con modafinilo en enfermos oncológicos (tabla 2).
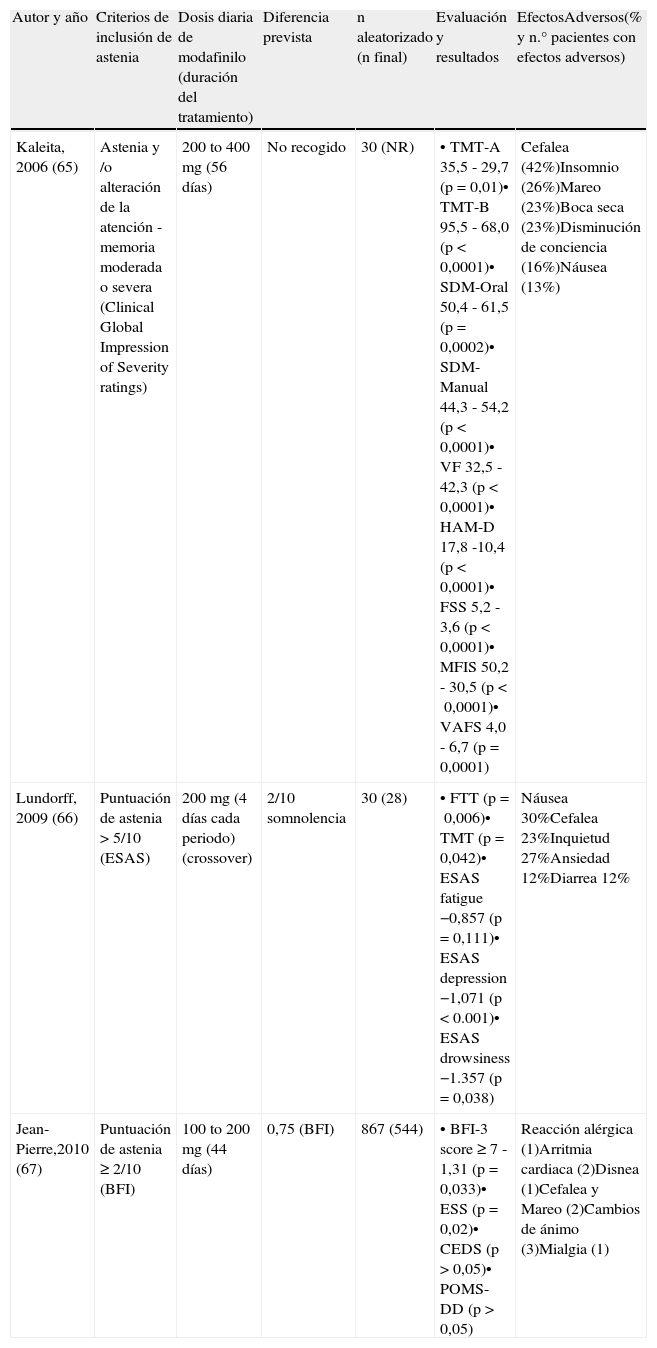
Estudios aleatorizados sobre el uso de modafinilo en astenia en pacientes con cáncer.
| Autor y año | Criterios de inclusión de astenia | Dosis diaria de modafinilo (duración del tratamiento) | Diferencia prevista | n aleatorizado (n final) | Evaluación y resultados | EfectosAdversos(% y n.° pacientes con efectos adversos) |
| Kaleita, 2006 (65) | Astenia y /o alteración de la atención - memoria moderada o severa (Clinical Global Impression of Severity ratings) | 200 to 400 mg (56 días) | No recogido | 30 (NR) | • TMT-A 35,5 - 29,7 (p=0,01)• TMT-B 95,5 - 68,0 (p<0,0001)• SDM-Oral 50,4 - 61,5 (p=0,0002)• SDM-Manual 44,3 - 54,2 (p<0,0001)• VF 32,5 - 42,3 (p<0,0001)• HAM-D 17,8 -10,4 (p<0,0001)• FSS 5,2 - 3,6 (p<0,0001)• MFIS 50,2 - 30,5 (p<0,0001)• VAFS 4,0 - 6,7 (p=0,0001) | Cefalea (42%)Insomnio (26%)Mareo (23%)Boca seca (23%)Disminución de conciencia (16%)Náusea (13%) |
| Lundorff, 2009 (66) | Puntuación de astenia>5/10 (ESAS) | 200mg (4 días cada periodo) (crossover) | 2/10 somnolencia | 30 (28) | • FTT (p=0,006)• TMT (p=0,042)• ESAS fatigue −0,857 (p=0,111)• ESAS depression −1,071 (p<0.001)• ESAS drowsiness −1.357 (p=0,038) | Náusea 30%Cefalea 23%Inquietud 27%Ansiedad 12%Diarrea 12% |
| Jean-Pierre,2010 (67) | Puntuación de astenia≥2/10 (BFI) | 100 to 200 mg (44 días) | 0,75 (BFI) | 867 (544) | • BFI-3 score≥7 -1,31 (p=0,033)• ESS (p=0,02)• CEDS (p>0,05)• POMS-DD (p>0,05) | Reacción alérgica (1)Arritmia cardiaca (2)Disnea (1)Cefalea y Mareo (2)Cambios de ánimo (3)Mialgia (1) |
BFI: Brief Fatigue Inventory; CEDS: Center for Epidemiological Study-Depression; ESAS: Edmonton Symptom Assessment System; ESS: Epworth Sleepiness Scale; FSS: Fatigue Severity Scale; FTT: Finger Tapping Test; HAM-D: Hamilton Depression Scale; MFIS: Modified Fatigue Impact Scale; POMS-DD: Depression-Dejection subscale of the Profile of Mood States; TMT: Trial Making Test; SDM: Symbol Digit Modalities; VAFS: Visuals Analogue Fatigue Scale; VF: Verbal Fluency.
Kaleita en el 2006 realizó un estudio con 30 pacientes con tumores cerebrales tratados con cirugía, quimioterapia y/o radioterapia. La astenia se valoró mediante una escala visual analógica (EVA), Fatigue Severity Scale (FSS) y Modified Fatigue Impact Scale (MFIS), la función cognitiva por el Trail Making Test (TMT) y el ánimo mediante el HADS. El estudio se estructuró en tres semanas iniciales, una de lavado y ocho de tratamiento. La dosis empleada osciló entre 200 y 400mg diarios. Se objetivó una mejoría significativa de la astenia con modafinilo, así como del ánimo y la capacidad cognitiva64. Los efectos adversos fueron cefalea, insomnio, mareo, xerostomía, reducción del nivel conciencia y náuseas.
Lundorff publicó en 2009 un ensayo clínico con distribución aleatoria, doble ciego y cruzado, con modafinilo en la disfunción psicomotriz y la alteración de la atención en 28 pacientes con cáncer avanzado. La intensidad de la astenia debía ser ≥5 (escala de 0 a 10). El día 1 los pacientes fueron asignados a recibir 200mg por vía oral de modafinilo o placebo y en el día 4 se cruzaron al tratamiento alternativo. Se realizó una evaluación del Finger Tapping Test (FTT), TMT y Edmonton Symptom Assessment System (ESAS) antes de la toma del fármaco y a las cuatro horas. La puntuación de FTT y TMT, los datos de depresión y somnolencia y las pruebas cognitivas de velocidad psicomotora y atención mejoraron de forma estadísticamente significativa. No hubo diferencias en la frecuencia e intensidad de los efectos secundarios en ambos brazos65. En este estudio no se apreció una mejoría estadísticamente significativa de la astenia si bien resultó positivo en la atención, velocidad psicomotora y la depresión y somnolencia.
Jean-Pierre publicó en 2010 un ensayo multicéntrico con distribución aleatoria, doble ciego y controlado con placebo que incluía 867 pacientes con cáncer en tratamiento con quimioterapia de los que 544 completaron el estudio. Se compararon 200mg de modafinilo y placebo. El tratamiento comenzaba el día 5 del ciclo 2 y finalizaba el día 7 del ciclo 4. La astenia se valoró mediante la escala BFI, la somnolencia mediante ESS y la depresión mediante las escalas Center for Epidemiological Study-Depression (CEDS) y Depression-Dejection subscale of the Profile of Mood States (POMS-DD). El modafinilo mejoró significativamente la astenia en los pacientes con astenia basal severa (BFI≥7). También mejoró la somnolencia. No hubo diferencias significativas en cuanto a depresión66. Este estudio sugiere que el modafinilo puede ser más eficaz en los pacientes con astenia severa, lo que podría ser importante en la selección de pacientes.
DiscusiónEl modafinilo es un fármaco bien tolerado. Aunque están descritos como efectos secundarios taquicardia, cefalea, excitación, nerviosismo, agresividad, insomnio, anorexia, náuseas, hipersalivación, euforia, agitación psicomotriz y discinesia bucofacial, los más relevantes observados en los estudios publicados son cefalea, náusea, nerviosismo, mareo e insomnio. Esto se debe a que a diferencia de otros psicoestimulantes como el metilfenidato, que actúa en distintas áreas cerebrales induciendo una excitación general, el modafinilo lo hace en áreas cerebrales específicas que regulan el ritmo sueño-vigilia. Además no actúa directamente sobre los receptores de noradrenalina y dopamina sino que inhibe a los transportadores de dichos neurotrasmisores. Por otro lado, disminuye los niveles de GABA involucrado en la inhibición de la liberación de otros neurotransmisores excitadores. Todo ello evita una mayor excitabilidad. La falta de actividad sobre los receptores de dopamina hace que el potencial de abuso sea menor.
En general, los efectos positivos se consiguen con dosis de 200mg y se describe menos desarrollo de tolerancia que en otros psicoestimulantes, convirtiéndolo en un fármaco adecuado en estadios iniciales de la enfermedad oncológica. Entre un 46-90% de los 157 pacientes tratados prospectivamente con 200mg de modafinilo mejoraron significativamente la astenia. Además, mejoraron otros síntomas como somnolencia, ánimo y cognición, poniendo de relieve la multidimensionalidad del síntoma astenia, en el que podríamos distinguir distintos aspectos físicos, cognitivos y emocionales. De los tres trabajos aleatorizados, dos encontraron una mejoría significativa de la astenia. En dos de ellos además, mejoraron significativamente los niveles de depresión y la capacidad cognitiva y en dos mejoró la somnolencia. Del análisis de los resultados del estudio aleatorizado más importante (544 pacientes en tratamiento con quimioterapia) se deduce que en el subgrupo con astenia basal severa, modafinilo mejora significativamente la astenia, sugiriendo que este factor puede ser importante en la selección de pacientes para el tratamiento de astenia con modafinilo, coincidiendo con los resultados de otro estudio aleatorizado realizado con metilfenidato de reciente publicación67. En todos los trabajos el modafinilo resultó bien tolerado. No obstante, se justifican nuevos estudios enfocados al alivio de astenia moderada-severa en pacientes con cáncer avanzado.
Hasta la fecha, era el metilfenidato el psicoestimulante más estudiado y con resultados más positivos para tratar astenia por cáncer. Sin embargo, el modafinilo podría presentar algunas ventajas como menor excitabilidad, menor tolerancia y mínimo potencial de abuso, frente a este último. Hay que añadir además un menor número de contraindicaciones, ya que puede emplearse en hipertiroidismo y glaucoma. Puede por tanto, considerarse otra opción en el tratamiento de astenia por cáncer. La posibilidad de uso de distintos psicoestimulantes en astenia por cáncer permite disponer de más opciones terapéuticas en aquellos casos en los que por distintos motivos un psicoestimulante no es efectivo, o produce efectos secundarios68. En el momento actual, su precio elevado y la necesidad de utilizarse solo como uso compasivo (fuera de indicación aprobada) son obstáculos para su uso más frecuente en astenia por cáncer.
FinanciaciónEste trabajo forma parte del proyecto de investigación 50/2010 promovido por el Departamento de Salud del Gobierno de Navarra, que también cuenta con una ayuda complementaria del Plan de Investigación de la Universidad de Navarra 2010.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.