Presentamos el caso de una paciente de 57 años de edad, que presentaba un cáncer epidermoide de canal anal metastásico. En su evolución presentó un intenso dolor glúteo somático con crisis de dolor irruptivo sacras 8/10 controladas con oxicodona oral. A pesar de la impresión inicial, la etiología de las crisis resultó ser secundaria, en parte, a secuelas de tratamiento radioterápico previo. Posteriormente, la aparición de metástasis cerebelosas condicionó la presencia de vómitos de difícil manejo, finalmente controlados con antihistamínicos y olanzapina parenterales. Por este mismo motivo, se procedió a la rotación de la vía de administración a oxicodona en perfusión subcutánea continua. La oxicodona parenteral se mantuvo durante 43 días, a dosis de 300mg/día, y en la perfusión se combinaron diversos fármacos (haloperidol, metoclopramida, escopolamina, midazolam, butilbromuro de escopolamina). Esta perfusión resultó claramente eficaz para el control de la sintomatología, sin que se evidenciaran problemas de incompatibilidad en la combinación de fármacos. Se observó una discreta reacción cutánea a partir de la semana de infusión, fácilmente controlable rotando el punto de inserción de la palomilla
We report the case of a 57 year-old patient with a metastatic anal epidermoid cancer. She progressively developed severe somatic pain in her buttocks, with breakthrough pain crises 8/10 located in the sacrum, which were well managed with oral oxycodone. Despite initial impressions, the pain crises were found to be partially related to radiotherapy side effects. She subsequently had intractable vomiting related to metastases in the cerebellum which was controlled with parenteral antihistamines and olanzapine. For this same reason, a switch in the route of administration to continuous subcutaneous infusion of oxycodone was performed. Parenteral oxycodone was maintained for 43 days at a dose of 300mg/day, and was combined with several drugs (haloperidol, metoclopramide, hyoscine hydrobromide, midazolam, hyoscine butylbromide). The infusion was found to be quite effective in dealing with the symptoms, and no problems of incompatibility were detected with the co-administration of the various drugs. A skin reaction was detected one week after starting the infusion, which was easily managed by rotation of the injection site
La reciente comercialización en España de la oxicodona en formulación parenteral ha permitido acceder a un nuevo opioide para su administración por esta vía1. Las presentaciones de opioides parenterales potentes disponibles hasta la fecha se reducían en la práctica a: morfina, fentanilo y metadona. Por diversos motivos, que incluyen la dificultad de la rotación opioide, tanto el fentanilo como la metadona no suelen considerarse los opioides de primera elección para la vía parenteral2. Por otro lado, no disponemos de experiencia acumulada sobre el empleo continuado de altas dosis de oxicodona parenteral.
Se presenta un caso de dolor basal somático glúteo en una paciente que presentaba crisis de dolor irruptivo (DI) intensas sacras y refractarias al manejo con la mayoría de los opioides potentes disponibles en la actualidad. En su evolución, el cuadro doloroso se controló adecuadamente, y durante tiempos prolongados mediante la administración de oxicodona por vía subcutánea.
Caso clínicoEn enero de 2005, la paciente, de 57 años de edad, fue diagnosticada de un carcinoma epidermoide de canal anal y fue tratada en el Hospital Clínico San Carlos (HCSC) con raspado. Entre sus antecedentes personales merece la pena destacar hábito tabáquico importante y la presencia de crisis de ansiedad. Desde abril a julio de 2005 recibió quimioterapia y posterior radioterapia en el HCSC. En octubre de 2005 se demostró recidiva a nivel anal y en enero de 2006 fue tratada con cirugía de resección rectal con amputación perineal y cierre del canal anal con colostomía izquierda. En mayo de 2006 se diagnosticaron metástasis pulmonares que fueron tratadas con quimioterapia con respuesta parcial.
En esta fecha, se derivó a la paciente a la Unidad de Cuidados Paliativos (UCP) del HCSC. Desde mayo de 2008 hasta agosto de 2009 requirió múltiples ingresos en esta unidad por colección anal con fístula y dolor secundario que requirió tratamiento con oxicodona oral en altas dosis de 160 mg/12 h (la paciente había experimentado fracaso terapéutico previo con todos los opioides mayores disponibles). Además, se observó progresión de las metástasis pulmonares con abscesos en región del canal anal y fístula interglútea. La paciente fue valorada por el Servicio de Cirugía, el cual no consideró indicado tratamiento quirúrgico.
En septiembre de 2009 la paciente ingresó nuevamente en la UCP del Hospital Clínico por infección microbiana y cuadro depresivo, y con posterioridad recibió tratamiento desde el 14 de octubre al 4 de noviembre de 2009 en la UCP del Hospital General Universitario Gregorio Marañón (HGUGM). Durante su estancia se confirmó la presencia de metástasis pulmonares, hepáticas, cistocele con neocavidad y una metástasis hemicerebelosa izquierda. Se efectuó biopsia de la lesión de canal anal que fue positiva para carcinoma epidermoide. Además, la paciente rechazó tratamiento con radioterapia paliativa holocraneal, por lo que fue tratada con esteroides y oxicodona oral.
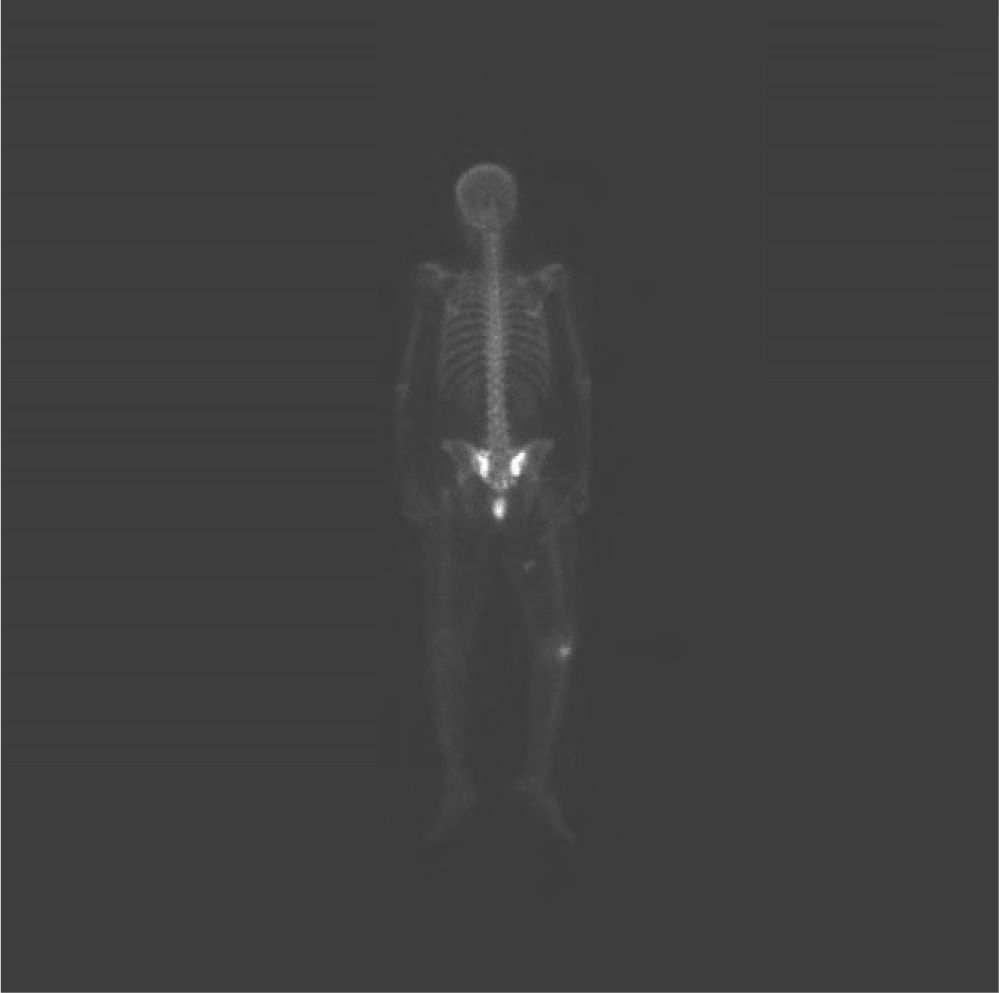
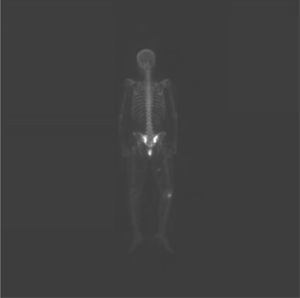
Desde noviembre de 2009 a enero de 2010, la paciente fue tratada con quimioterapia paliativa sin respuesta local. A finales de enero de 2010 comenzó con lumbalgia y presentó un hallazgo de captación a nivel de ambas sacroilíacas en el rastreo óseo (fig. 1).
En febrero de 2010 la paciente hubo de ingresar en el Servicio de Oncología Médica del HGUGM por trombosis secundaria a port-a-cath en vena cava superior, por lo cual se retiró la vía central y se procedió a anticoagulación con heparina de bajo peso molecular. Además la paciente recibió tratamiento con bisfosfonatos. En este contexto, fue ingresada de nuevo en nuestra unidad para tratamiento de Di óseo sacro de intensidad 2-8/10, y de probable etiología metastásica.
A su ingreso en la UCP, la exploración física mostraba una mujer madura con estigmas cushingoides y buen estado general con un Palliative Performance Scale3 (PPS) del 70%. Destacaba la presencia de progresión tumoral local en forma de fístula interglútea.
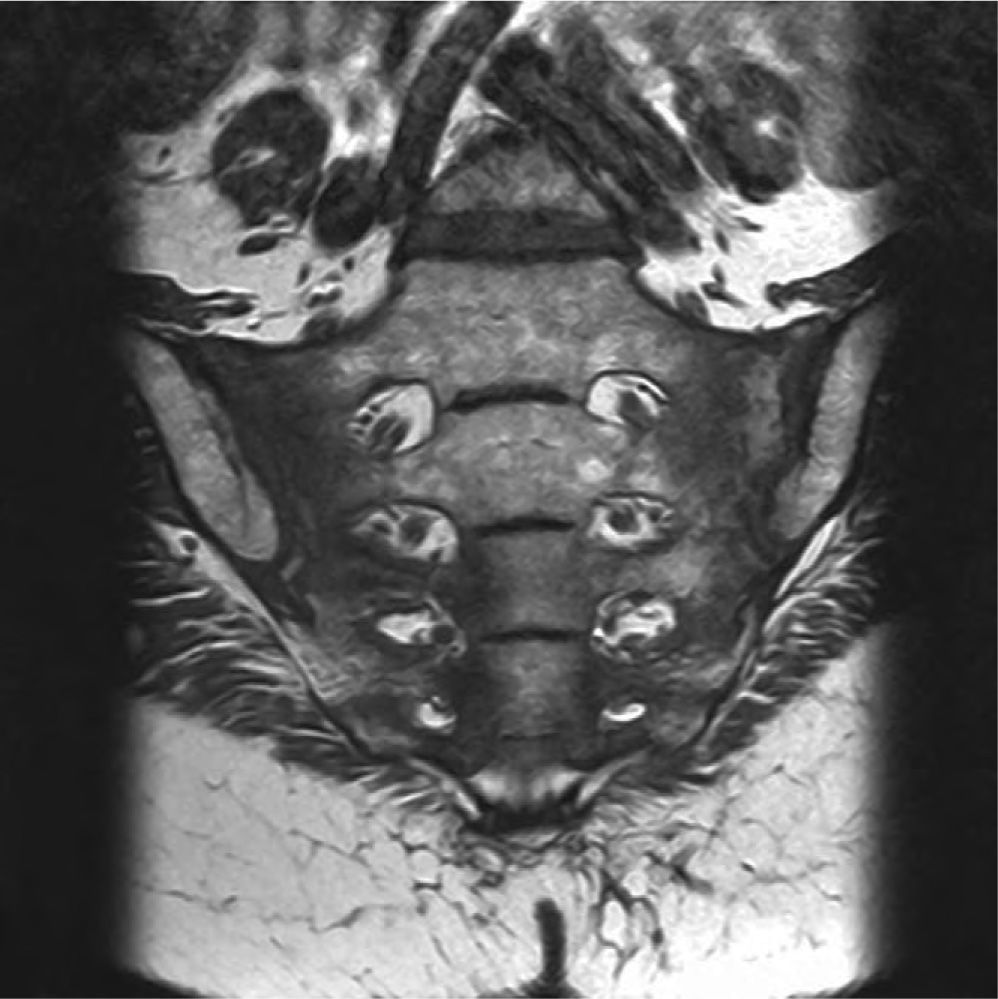
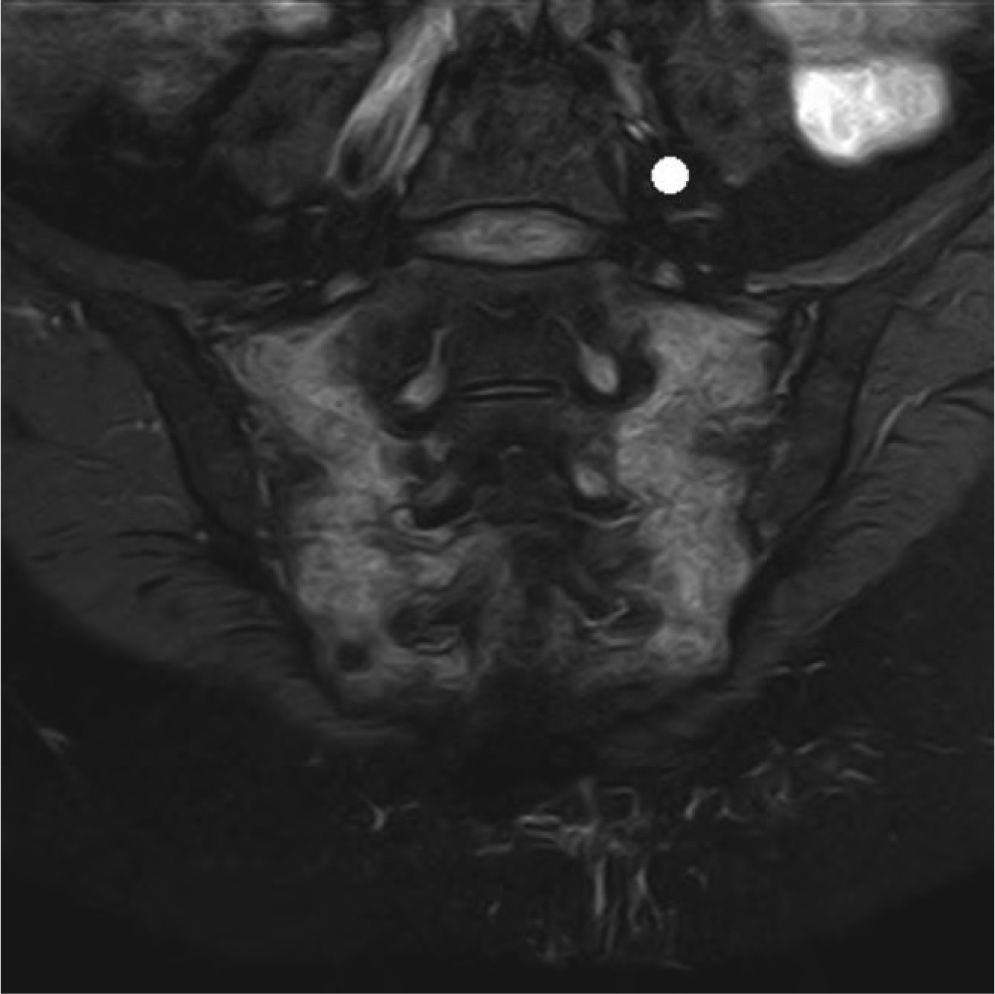
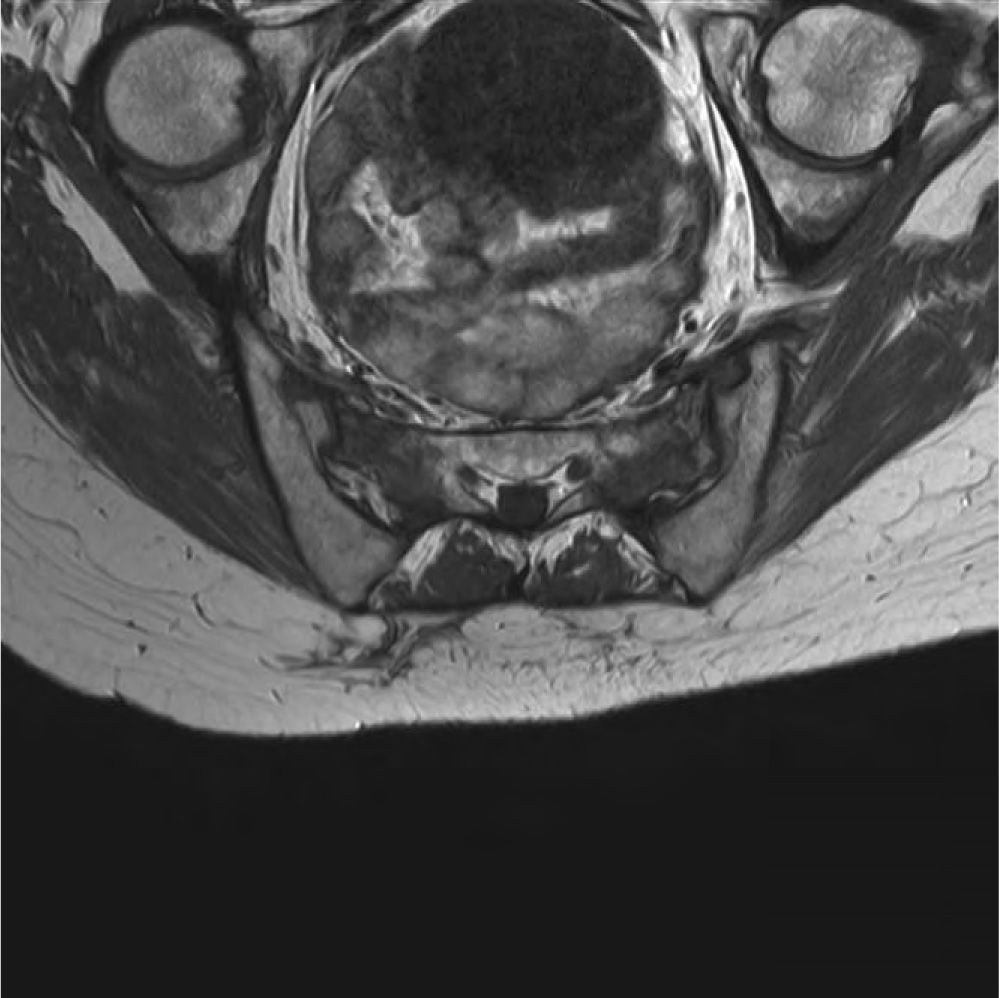
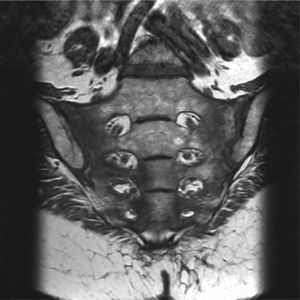
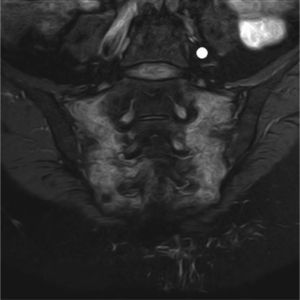
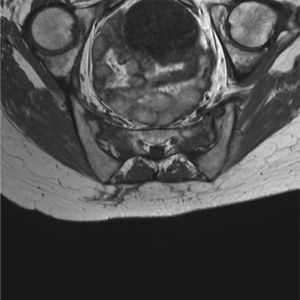
Entre las exploraciones complementarias efectuadas, se realizó una resonancia magnética que confirmó la existencia de secuelas de radioterapia en ambas sacroilíacas, así como en ambos huesos ilíacos (figs. 2–4).
Una vez descartada la existencia de metástasis óseas a nivel sacroilíaco, la paciente tomó la decisión de no continuar con quimioterapia por la mala evolución de la fístula interglútea. Durante su estancia con nosotros se controló adecuadamente el DI óseo mediante un abordaje multimodal que incluyó: optimización de opioides y adyuvantes, sedestación en una trona, deambulación en descarga con bastón y andador, faja lumbar blanda, TENS y anestésicos tópicos locales (crema EMLA). La paciente rechazó la analgesia espinal y los rescates para DI con formulaciones de fentanilos rápidos4. Gracias a este abordaje, la paciente recuperó capacidad de deambular y la independencia para las actividades de vida diaria, y se le dio de alta a domicilio el 9 de marzo de 2010 bajo supervisión de su médico de atención primaria, y equipo domiciliario de la Asociación Española Contra el Cáncer del Área 5. El tratamiento en ese momento incluía, entre otros medicamentos: dexametasona 2 mg/12 h, ibuprofeno 600 mg/8 h, oxicodona 160 mg/12 h, pregabalina 150 mg/12 h y diazepam 5 mg/ 24 h. Los rescates para DI se efectuaban con oxicodona de liberación rápida 40 mg/4 h a demanda.
Al cabo de una semana, la paciente acudió a urgencias del Hospital La Paz, remitida por su equipo domiciliario, tras haberla encontrado en la visita con un nivel de conciencia bajo. Valorada por el Equipo de Soporte Hospitalario del Hospital La Paz, la paciente ingresó en la UCP de dicho hospital, y posteriormente fue trasladada a la UCP de agudos del HGUGM. A su ingreso se observó un nuevo DI por sobrecarga muscular, linforrea secundaria a edema por esteroides y antiinflamatorios no esteroideos, y sobredosis por benzodiacepinas sin aparente intención suicida (confirmada en valoración psiquiátrica).
En las semanas posteriores presentó dificultades en el control analgésico y precisó oxicodona oral en dosis altas y crecientes. A principios de abril de 2010, se manifestó un episodio de somnolencia, desorientación, náuseas y vómitos con intolerancia oral, todo ello secundario a hipertensión intracraneal por metástasis hemicerebelosa izquierda conocida. En repetidas ocasiones, la paciente rechazó la posibilidad de radioterapia holocraneal, por lo que se controló el cuadro con esteroides por vía parenteral, antieméticos específicos (anti-H1 y olanzapina) y rotación de vía de administración a oxicodona parenteral en dosis altas. En este contexto, la situación se estabilizó nuevamente, por lo que, de acuerdo con la paciente y su familia, se trasladó a nuestra UCP de subagudos el día 27 de abril de 2010 para rehabilitación.
En las semanas siguientes, la paciente realizó ejercicios de rehabilitación salvo durante los episodios de vértigos sintomáticos secundarios a las metástasis cerebelosas. Las dosis empleadas de oxicodona en perfusión por vía subcutánea continua con bomba fueron muy elevadas y mantenidas (300 mg/24 h) durante 43 días. La oxicodona se combinó alternativamente con varios fármacos en la perfusión subcutánea: haloperidol (2 mg/día), bromuro de butilescopolamina (60 mg/día) y metoclopramida (20 mg/día), sin que se observaran problemas apreciables5. La enfermera responsable de la paciente observó irritación de la piel con la administración prolongada a partir de la primera semana, pero ello no impidió continuar con la perfusión gracias a la rotación del punto de inserción de la palomilla.
En los últimos días se observó progresión tumoral local muy importante con signos de fístula vesiculocutánea y deterioro progresivo de la paciente, quien entró en situación de agonía y falleció el día 1 de junio de 2010. El tratamiento en las últimas 24 h consistió en: oxicodona 300 mg + haloperidol 2 mg + escopolamina 1 mg + midazolam 30 mg en bomba de perfusión subcutánea continua, dexametasona 6 mg/8 h por vía subcutánea, metronidazol y crema EMLA tópicos, dexclorfeniramina 2,5 mg/8 h por vía subcutánea, olanzapina 10 mg/12 h por vía intramuscular a demanda y oxicodona 20–40 mg/4 h por vía subcutánea a demanda.
DiscusiónLa oxicodona, un potente opioide agonista mu y kappa, ha demostrado su utilidad en el manejo del dolor oncológico neuropático, somático y visceral. Además, se diferencia de otros opioides en aspectos importantes que lo convierten en una alternativa adecuada a la morfina6,7.
No obstante, la experiencia acumulada en nuestra población sobre la administración de oxicodona por vía parenteral, y en altas dosis, es bastante limitada. En un estudio de Maddocks et al8, se administró oxicodona en perfusión continua por vía subcutánea a 13 pacientes, con dosis de hasta 180 mg/día y por un máximo de 6 días, en un contexto de rotación opioide (RO) desde morfina parenteral. En otro estudio de Gagnon et al9, se administró oxicodona en pulsos por vía subcutánea mediante el inyector de Edmonton a 63 pacientes, con dosis de hasta 660 mg/día y durante un máximo de 49 días, también en un contexto de RO desde otros opioides potentes.
También hay otro tipo de evidencia más indirecta de la eficacia de la oxicodona parenteral y su seguridad en la administración a altas dosis. Desde hace unos años en Japón se viene empleando con buenos resultados una asociación de oxicodona inyectable con hidrocotarnina, un alcaloide derivado del opio no narcótico10,11. Por otro lado, los trabajos publicados con altas dosis de oxicodona por vía oral pueden resultar interesantes. Por ejemplo, Ferrarese et al12 han comunicado dosis medias de 221,84 mg/día de oxicodona oral, con seguimientos medios de 37,24 días, obteniéndose buenos resultados y tolerancia. Por su lado, Bercovitch y Adunsky13 han comunicado dosis medias de 231,1 mg/día, también con buenos resultados.
En nuestra paciente, las dosis alcanzadas y el tiempo de empleo fueron ambos bastante elevados, pero todavía inferiores a los comunicados en el trabajo de Gagnon et al9. En este mismo estudio se menciona la presencia de reacciones cutáneas en 2 de 63 pacientes, y en ambos casos se emplearon concentraciones de oxicodona superiores a 50 mg/ml (la solución inyectable se preparó a partir de polvo de oxicodona). En el trabajo de Maddocks et al8, se empleó una solución inyectable de 25 mg/ml de oxicodona sin que se apreciasen reacciones cutáneas. Es llamativa la presencia en nuestra paciente de intolerancia cutánea con la concentración comercializada en España de la solución inyectable, que es tan sólo de 10 mg/ml1. Sin embargo, es importante señalar que la reacción cutánea apareció siempre tras una semana de exposición al fármaco por vía subcutánea, si bien es cierto que el personal de enfermería observó poco cuidado de la hipodermoclisis por parte de la propia paciente (tirones).
En nuestra paciente no se observaron problemas de incompatibilidades en la combinación de fármacos administrada mediante una bomba para perfusión continua subcutánea: oxicodona + haloperidol, oxicodona + metoclopramida, oxicodona + bromuro de butilbuscapina, oxicodona + haloperidol + escopolamina + midazolam. En este sentido, nuestra experiencia avala los estudios previamente publicados de compatibilidad5.
Por último, señalar que no se efectuaron controles electrocardiográficos en la paciente para descartar la posibilidad de una prolongación sintomática del QT14.
ConclusionesLa oxicodona parenteral refuerza significativamente nuestras opciones de manejo del dolor intenso con opioides potentes por esta vía de administración. Nuestra experiencia clínica con este caso confirma su utilidad, facilidad de empleo y seguridad en altas dosis por tiempos prolongados.
AgradecimientosA la Dra. isabel Barreiro del Servicio de Radiología del Hospital General Universitario Gregorio Marañón. A los compañeros responsables de los cuidados de la paciente en el equipo domiciliario de la Asociación Española Contra el Cáncer (AECC) y Equipo de Soporte Hospitalario/Unidad de Cuidados Paliativos del Hospital La Paz.
Conflicto de interesesEl Dr. Núñez Olarte ha realizado investigación y/o formado parte de comités científicos para los laboratorios siguientes: Wyeth, Pfizer, Nycomed, Cephalon, Ferrer, Prostrakan, Mundipharma, Roxane, Asta, Grunenthal.
La Dra. Sánchez Sobrino ha realizado investigación y/o formado parte de comités científicos para los laboratorios siguientes: Wyeth, Ferrer, Cansen, Nycomed, Mundipharma.
La Dra. Viloria Jiménez ha realizado investigación y/o formado parte de comités científicos para los laboratorios siguientes: Pfizer, Wyeth, Lundbeck, Novartis, Jansen, Grunenthal, Eisai.