Se denomina trombocitopenia inducida por heparina (TIH) a una reacción adversa protrombótica, mediada por activación de anticuerpos antiplaquetarios (mayoritariamente IgG) contra el complejo formado por el factor plaquetario4 y la heparina, en individuos en tratamiento con este fármaco. Estos inmunocomplejos resultantes activan plaquetas y monocitos, y esta activación aumenta la generación de trombina.
El aumento de la trombina, no la trombocitopenia, se considera una de las principales causas de los problemas clínicos1.
Cuando los anticuerpos están presentes pueden causar trombosis venosa y/o arterial en un tercio a la mitad de los pacientes que manifiestan TIH. Este riesgo persiste hasta la completa metabolización de la heparina y hasta que otro anticoagulante no heparínico es iniciado. Cuando la trombosis está presente denominamos a esta entidad «trombocitopenia inducida por heparina con trombosis» (TTIH).
Gran parte de los casos pueden ser de gravedad clínica considerable, conduciendo a un desenlace fatal2. Dado que para el diagnóstico es necesaria la conjugación de criterios clínicos y patológicos, podría considerarse un síndrome clínico-patológico consecuente a una complicación grave después de la exposición a la heparina3.
La heparina no fraccionada (HNF) y la heparina de bajo peso molecular (HBPM) son los anticoagulantes más utilizados en pacientes hospitalizados. La incidencia de TIH en esos pacientes se estima entre <0,1% y el 7%, dependiendo de la duración de la exposición a la heparina, del tipo de heparina (HNF o HBPM) y del tipo de ingreso, si es de causa médica o quirúrgica4.
La mayor incidencia de este síndrome está relacionada con algunos factores de riesgo, y es más frecuente en mayores de 60años, después de exposición a la HNF en relación con la HBPM, en los procedimientos quirúrgicos en relación con los médicos, y en el sexo femenino.
El desarrollo de esta entidad ocurre entre el quinto y el décimo día después del inicio de heparina5 en pacientes que reciben heparina por primera vez y en pacientes con exposición previa. En los sujetos que recibieron heparina en los 90días anteriores, y sobre todo en los 30días anteriores, la TIH puede aparecer abruptamente cuando se re-exponen a heparina por la probable persistencia de anticuerpos antifactor plaquetario4 (anti PF4)/heparina; se considera que los anticuerpos circulantes desaparecen después de 50-85días, y la regeneración de anticuerpos requiere por lo menos 5días. En estos casos la TIH a veces se complica con una reacción anafiláctica tan solo 30min después del bolus de heparina6.
Existen casos de pacientes que desarrollan TIH o incluso empeoran la TIH cuando la heparina es descontinuada (TIH de inicio tardío). Estos pacientes pueden presentar trombosis hasta 3semanas después de la exposición a la heparina7.
Se presenta el caso clínico de una mujer de 74años con antecedentes personales de obesidad, hipertensión arterial, diabetes mellitus tipo2 y dislipidemia con buen control metabólico, que ingresa en el servicio de Traumatología y Ortopedia para ser sometida a cirugía programada de colocación de prótesis total de la rodilla derecha. A la llegada al hospital, en el estudio analítico realizado previo a la intervención presentaba un valor de plaquetas de 156,0×109/l, fue operada sin complicaciones y al día siguiente de la cirugía, según protocolo, inició tratamiento con HBPM en dosis de 40mg/día y se solicitó estudio analítico postoperatorio, en el que se detectó una anemia con Hb9,9g/dl y una trombocitopenia ligera de 126,0×109/l; los días siguientes presentó buena evolución clínica, y no se realizó ningún control analítico hasta pasados 6días (el octavo día de ingreso), cuando la paciente se quejó de dolor súbito e intenso (que cuantificaba como 7 sobre 10) en el miembro inferior derecho, que a la exploración se presentó con edema y rubor. Se solicitaron análisis, que manifestaron trombocitopenia de 39,0×109/l, y ante la sospecha de poder tratarse de una trombosis venosa profunda se pidió ecografía doppler, que confirmó la trombosis aguda de venas musculares del gemelo interno con extensión a la vena poplítea a pesar de estar realizado profilaxis con HBPM, por lo que se decidió aumento de dosis de HBPM, con 60mg/día, ante el nuevo hallazgo de trombosis venosa profunda. Los días siguientes mantuvo el control analítico con plaquetas ∼50,0×109/l.
Dos días después (undécimo día de ingreso) inició disnea súbita, taquicardia e hipersudoración. Por empeoramiento clínico se solicitó la colaboración de Medicina Interna, que después de observar a la paciente y realizar las pruebas pertinentes consideró como sospecha diagnóstica más probable la de tratarse de tromboembolismo pulmonar agudo (TEP) en paciente con factores de riesgo, por lo que se solicitó angio-TAC, que confirmó el TEP de la arteria pulmonar derecha (tabla 1).
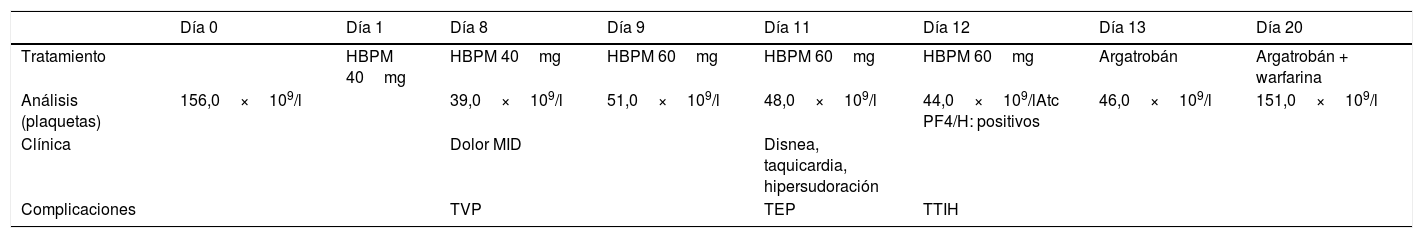
Evolución analítica
| Día 0 | Día 1 | Día 8 | Día 9 | Día 11 | Día 12 | Día 13 | Día 20 | |
|---|---|---|---|---|---|---|---|---|
| Tratamiento | HBPM 40mg | HBPM 40mg | HBPM 60mg | HBPM 60mg | HBPM 60mg | Argatrobán | Argatrobán + warfarina | |
| Análisis (plaquetas) | 156,0×109/l | 39,0×109/l | 51,0×109/l | 48,0×109/l | 44,0×109/lAtc PF4/H: positivos | 46,0×109/l | 151,0×109/l | |
| Clínica | Dolor MID | Disnea, taquicardia, hipersudoración | ||||||
| Complicaciones | TVP | TEP | TTIH |
Atc PF4/H: anticuerpos anti factor planetario 4/heparina; HBPM: heparina de bajo peso molecular; MID: miembro inferior derecho; TEP: tromboembolismo pulmonar; TTIH: trombocitopenia inducida por heparina con trombosis; TVP: trombosis venosa profunda.
En ese momento, ante una paciente con descenso de plaquetas y eventos trombóticos en tratamiento con HBPM y con reciente aumento de dosis, la sospecha de TIH era muy elevada, y se efectuó el cálculo del Score4T, como se recomienda, con puntuación de 8 (tabla 2). A pesar de que el cribado de rutina para detección de anticuerpos anti PF4-heparina no está indicado en todos los pacientes en tratamiento con HNF o HBPM con trombocitopenia, los pacientes con riesgo alto o intermedio (calculado a través del score4T) deben realizarlo, por lo que en este caso fue solicitado el anticuerpo anti PF4/heparina, con resultado fuertemente positivo8.
Probabilidad previa de trombocitopenia inducida por heparina (Score 4T)
| Trombocitopenia |
| El recuento de plaquetas cae >50% y nadir ≥20.000/μl (2puntos) |
| El recuento de plaquetas cae 30 a 50% o nadir 10 a 19.000/μl (1punto) |
| El recuento de plaquetas cae <30% o nadir <10.000/μl (0puntos) |
| Tiempo de disminución del recuento de plaquetas |
| El inicio claro entre los días 5 y 10 de exposición a la heparina o el recuento de plaquetas disminuye a ≤1día si exposición previa a heparina en los últimos 30días (2puntos) |
| Consistente con la caída en el recuento de plaquetas a los 5 a 10días, pero no está claro (p.ej., falta el recuento de plaquetas), o se inicia después del día 10, o cae ≤1día con exposición previa a heparina entre los 30 y los 100días anteriores (1punto) |
| El recuento de plaquetas disminuye a <4días sin exposición reciente a heparina (0puntos) |
| Trombosis u otras secuelas |
| Trombosis nueva confirmada, necrosis de la piel o reacción sistémica aguda después de un bolo de heparina no fraccionado intravenoso (2puntos) |
| Trombosis progresiva o recurrente, lesiones cutáneas no necrosantes (eritematosas) o sospecha de trombosis no demostrada (1punto) |
| Ninguno (0puntos) |
| Otras causas de trombocitopenia presentes |
| Ninguna aparente (2puntos) |
| Posible (1punto) |
| Definida (0puntos) |
| Interpretación |
| ≤3 puntos: baja probabilidad de HIT (≤5% en el estudio original, <1% en el metaanálisis) |
| 4-5 puntos: probabilidad intermedia (∼14% de probabilidad de HIT) |
| 6-8 puntos: alta probabilidad (∼64% de probabilidad de HIT) |
| Puntuación de nuestra paciente: 8 |
El tratamiento con heparina fue inmediatamente suspendido y se inició inhibidor directo de la trombina, perfusión de argatroban 250mg (2,5ml) diluido en 250cc de suero fisiológico a 2μg/kg/min con control de APTT para el ajuste posterior de la dosis.
Posteriormente se inició warfarina en sobreposición a argatrobán durante 5días, con buena evolución clínica sin recidiva trombótica y recuperación progresiva del recuento de plaquetas (tabla 1).
Los anticoagulantes anti vitaminaK deben ser administrados siempre en sobreposición con anticoagulante alternativo y nunca hasta que la TIH esté resuelta (recuento de plaquetas por encima de 150.000/μl y valor estable por lo menos durante 2días consecutivos).
Es conocido que el uso de antagonistas de la vitaminaK está asociado inicialmente con un estado protrombótico por depresión de anticoagulantes naturales. Este efecto se hace más evidente en la TIH, dado que la inducción de warfarina sin cobertura de inhibidores de la trombina se ha asociado con un aumento del riesgo de gangrena de los miembros9.
En caso de TIH confirmada complicada con trombosis (TTIH) o aguda sin trombosis, las recomendaciones actuales aconsejan suspender la heparina e iniciar un anticoagulante no heparínico8.
La elección del anticoagulante dependerá de varios factores: disponibilidad en el hospital, coste, facilidad de monitorización, vía de administración, riesgo hemorrágico y estabilidad clínica8.
Existen actualmente varios anticoagulantes aprobados: argatrobán, danaparoid, bivalirudina o fundaparinux; los anticoagulantes orales directos (ADO) dabigatrán, ribaroxabán y apixabán ya forman parte de las opciones de tratamiento8.
La transfusión de plaquetas profiláctica debe ser evitada en pacientes con TIH, una vez que el riesgo de sangrado es muy bajo, pues cada transfusión aumenta el riesgo de trombosis10.
Llamamos la atención a la importancia de la monitorización del recuento plaquetario regular. Atendiendo al intervalo de tiempo típico de esta entidad, un control analítico en los días 5, 7 y 9 permitiría un diagnóstico precoz para la mayoría de los pacientes11. La posterior realización de escores diagnósticos —el más extensamente utilizado es el 4T12— orientará hacia la identificación de pacientes de alto y medio riesgo de una forma simple y precoz, señalando individuos en los que el clínico deberá estar alerta para proceder a la suspensión y sustitución del fármaco y continuar estudio con test inmunológico que permita detectar anticuerpos. Estas medidas podrán evitar consecuencias fatales.
Las mejoras en el reconocimiento rápido y el tratamiento han ayudado a que las tasas de mortalidad de esta entidad hayan disminuido del 20% a menos del 2% en los últimos años13.
Este caso puede ser importante para, una vez más, resaltar el hecho de que la colaboración continua entre Medicina Interna y otras especialidades, a través de programas como cogestión o apoyo continuado de internistas en pacientes ingresados de otras áreas (sobre todo quirúrgicas), podrá llevar a diagnósticos más tempranos y tratamientos menos costosos y más efectivos, beneficiando al paciente y al sistema.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.