En 2015 se inició el Global HPP Registry, un registro observacional, prospectivo y multinacional de los pacientes con hipofosfatasia (HPP) (NCT02306720; EUPAS13514). El objetivo de este estudio es evaluar la sintomatología e impacto de la enfermedad en los pacientes incluidos en el registro nacional.
MétodosSe analizaron las características basales de los pacientes incluidos en el registro por los centros nacionales (5/11/2015-4/03/2024).
ResultadosDe los 83 pacientes, 16 (19,3%) eran menores de 18 años y 67 (80,7%) adultos. El tiempo (mediana) hasta el diagnóstico fue de 4,8 (mínimo: 0; máximo: 49,9) años. En los pacientes pediátricos, la edad (mediana) al inicio de síntomas fue de 4 (mínimo: 1,2; máximo: 11,8) años y los más prevalentes fueron dentales (37,5%), neurológicos (25%) y esqueléticos (18,8%). El 23,7% de los adultos comenzó con síntomas relacionados con HPP antes de los 18 años, y los más frecuentes fueron el dolor (64,2%), los dentales (50,7%) y los esqueléticos (32,8%). El 96,3% de los pacientes mostraron variantes en ALPL en heterocigosis, y las más frecuentes fueron c.343_348dup, c.334G>C y c.407G>A. En los pacientes adultos, los resultados informados por el paciente (mediana [Q1; Q3]) en el cuestionario para la valoración de la calidad de vida (SF-36v2) (escalas de 0-100) fueron de 44,8 (34,5;50,2) para el componente físico y de 50,4 (38,9;56,5) para el mental.
ConclusionesExiste un retraso significativo en el diagnóstico de la HPP. Las manifestaciones más frecuentes fueron dentales en los pacientes pediátricos y el dolor en adultos, con un impacto relevante en la calidad de vida.
The Global HPP Registry, an observational, prospective, multinational registry of patients with hypophosphatasia (HPP) (NCT02306720; EUPAS13514), was initiated in 2015. The aim of this study is to assess the symptomatology and impact of the disease in patients included in the national registry.
MethodsBaseline characteristics of patients included in the Registry by national centres were analysed (5/11/2015-4/03/2024).
ResultsOf the 83 patients, 16 (19.3%) were under 18 years of age and 67 (80.7%) were adults. Median time to diagnosis was 4.8 (minimum: 0; maximum: 49.9) years. In paediatric patients, median age at symptom onset was 4 (minimum: 1.2; maximum: 11.8) years and the most prevalent symptoms were dental (37.5%), neurological (25%), and skeletal (18.8%). 23.7% of adults started with HPP-related symptoms before the age of 18 years and the most frequent symptoms were pain (64.2%), dental (50.7%), and skeletal (32.8%). Heterozygous ALPL variants were found in 96.3% of patients and the most frequent were c.343_348dup, c.334G>C, and c.407G>A. In adult patients, patient-reported outcomes (median [Q1; Q3]) on the quality of life questionnaire (SF-36v2) (scales 0-100) were 44.8 (34.5;50.2) for the physical component and 50.4 (38.9;56.5) for the mental component.
ConclusionsThere is a significant delay in the diagnosis of HPP. The most frequent manifestations were dental in paediatric patients and pain in adults, with a relevant impact on quality of life.
La hipofosfatasia (HPP) es una enfermedad del metabolismo mineral óseo que se caracteriza por la presencia de niveles bajos de fosfatasa alcalina (FA) debido a variantes patogénicas del gen ALPL (1p36.1-p34) que codifica la FA no específica de tejido (FANET), expresada mayoritariamente en hueso, hígado y riñón1. Esta enzima desempeña un papel fundamental en el desarrollo y mantenimiento del tejido mineral óseo y el metabolismo del calcio y fosfato en el organismo. El espectro fenotípico de la HPP es variable. Se ha descrito mayor gravedad y peor pronóstico en las formas de inicio precoz, generalmente durante las etapas perinatal y del lactante (antes de los 6 meses de edad) (OMIM #241500)2, con la posible presencia de convulsiones, insuficiencia respiratoria secundaria a malformaciones de la caja torácica y raquitismo3,4. La HPP infanto-juvenil aparece después de los 6 meses de vida, como un continuum de la forma del lactante (OMIM #241510)5. Otras manifestaciones de la enfermedad incluyen la pérdida dentaria precoz, osteomalacia, seudofracturas de fémur, fracturas de estrés de metatarsianos, dolor musculoesquelético y debilidad muscular. En el adulto (OMIM #146300)6, la enfermedad ha sido menos caracterizada, dado que la sintomatología es generalmente más leve que la observada en los pacientes pediátricos7. Sin embargo, también puede observarse una alta carga de enfermedad8, y la sintomatología relacionada con la HPP puede cambiar con el tiempo9.
Para mejorar la caracterización de la enfermedad, en 2015 se creó el Global HPP Registry, un estudio observacional, prospectivo y multinacional (NCT02306720; EUPAS13526), patrocinado por Alexion, AstraZeneca Rare Disease (Boston, MA, EE. UU.) y supervisado por un comité científico de expertos en HPP, que recoge los datos relacionados con el diagnóstico, el curso clínico, los síntomas y la carga de la enfermedad de los pacientes de todas las edades con HPP en condiciones de práctica clínica rutinaria10. El objetivo de este estudio es describir las características sociodemográficas, las manifestaciones clínicas, la repercusión en el dolor, la calidad de vida y la discapacidad de la enfermedad en la cohorte española de los pacientes con HPP incluidos en el Global HPP Registry.
MétodosSe analizaron las características de los pacientes con HPP registradas en el momento de su inclusión en el Global HPP Registry. El estudio se realizó de acuerdo con los principios éticos de la Declaración de Helsinki y las guías de buena práctica clínica y fue aprobado por el comité ético (o equivalente local) de los centros participantes. Antes de participar, los pacientes y/o sus padres/tutores legales dieron su consentimiento informado por escrito.
PacientesSe analizaron los datos de pacientes de cualquier edad con diagnóstico de HPP, de acuerdo con los criterios del registro (niveles bajos de FA para edad y sexo y/o al menos una variante patogénica en ALPL), pertenecientes a la cohorte española del Global HPP Registry incluidos desde el 5 de noviembre de 2015 hasta el 4 de marzo de 2024. Todos los resultados presentados provienen exclusivamente de los pacientes no tratados con tratamiento enzimático sustitutivo.
Recogida y tratamiento de los datosLos datos se obtuvieron de la práctica clínica habitual y se registraron mediante un formulario electrónico de notificación de casos (eCRF). Tras su revisión, se solicitó información adicional a los centros para intentar alcanzar la máxima homogeneidad y cantidad de datos registrados.
VariablesSe analizaron las siguientes variables recogidas en la visita inicial del registro: 1) fecha de reclutamiento y características sociodemográficas (edad al momento de la inclusión, sexo, raza y etnia); 2) estudio molecular (número de pacientes con variantes en ALPL, número total y tipo de variantes así como su patogenicidad, atendiendo a las directrices del Colegio Americano de Genética Médica y Genómica [ACMG]11); 3) variables relacionadas con el retraso del diagnóstico (edad de inicio de la primera manifestación, edad al diagnóstico y tiempo transcurrido hasta el mismo); 4) manifestaciones clínicas características de HPP categorizadas según los siguientes sistemas orgánicos: dolor (dolor óseo y muscular crónicos, dolor corporal generalizado y fibromialgia), síntomas y signos dentales, esqueléticos, reumáticos (periartritis calcificante, seudogota, condrocalcinosis, calcificaciones ectópicas), renales, neurológicos, constitucionales/metabólicos, musculares y respiratorios (ver material suplementario 1 para más información relacionada con las manifestaciones de HPP incluidas en cada sistema orgánico o corporal); 5) historial de fármacos relacionados con la afectación esquelética (bisfosfonatos, análogos de la hormona paratiroidea [PTH], vitamina D) y analgésicos; 6) resultados informados por el paciente (patient-reported outcomes [PRO]) en adultos (≥18 años), para lo que se empleó el Cuestionario Breve para la Evaluación del Dolor (Brief Pain Inventory Short Form [BPI]), el Índice de Discapacidad del Cuestionario de Evaluación de la Salud (Health Assessment Questionnaire Disability Index [HAQ-DI]) y el Cuestionario de Calidad de Vida Relacionada con la Salud Versión 2 (36-Item Short-Form Health Survey Version 2, SF-36-v2). Ver más detalles sobre los PRO y los cuestionarios empleados en el material suplementario 2.
Métodos estadísticosSe presenta un estudio descriptivo transversal de las características basales y los antecedentes médicos de los pacientes con HPP atendiendo al grupo de edad en el momento del reclutamiento (pediátricos: <18 años; adultos: ≥18 años). Las variables cuantitativas se presentan mediante la media (desviación estándar [DE]) y la mediana (mínimo [mín] y máximo [máx] o intervalo intercuartílico [Q1;Q3]) y las variables categóricas, mediante frecuencias y porcentajes.
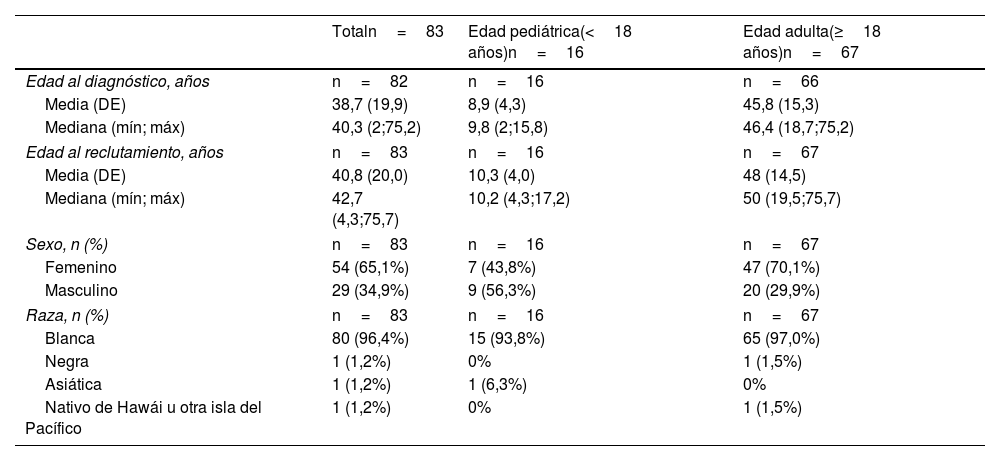
ResultadosCaracterísticas demográficas basalesLa población estudiada incluyó a 83 pacientes, de los cuales 16 (19,3%) eran pediátricos y 67 (80,7%) adultos. La edad (mediana [mín;máx]) al reclutamiento de los pacientes pediátricos fue de 10,2 (4,3;17,2) años. La mayoría de los niños de este grupo eran varones (56,3%), mientras que en el grupo de adultos hubo un predominio de mujeres (70,1%). La edad mediana al reclutamiento de los pacientes adultos fue de 50 (19,5;75,7) años. Se dispuso del estudio genético molecular de 82 pacientes (16 pacientes pediátricos y 66 adultos), que presentaron un total de 85 variantes. Las características demográficas basales de los pacientes se detallan en la tabla 1. La distribución de los centros participantes por comunidades autónomas es la siguiente: 4 en Cataluña (40%), 4 en la Comunidad de Madrid (40%), uno en Navarra (10%) y uno en Baleares (10%).
Características demográficas de los pacientes analizados
| Totaln=83 | Edad pediátrica(<18 años)n=16 | Edad adulta(≥18 años)n=67 | |
|---|---|---|---|
| Edad al diagnóstico, años | n=82 | n=16 | n=66 |
| Media (DE) | 38,7 (19,9) | 8,9 (4,3) | 45,8 (15,3) |
| Mediana (mín; máx) | 40,3 (2;75,2) | 9,8 (2;15,8) | 46,4 (18,7;75,2) |
| Edad al reclutamiento, años | n=83 | n=16 | n=67 |
| Media (DE) | 40,8 (20,0) | 10,3 (4,0) | 48 (14,5) |
| Mediana (mín; máx) | 42,7 (4,3;75,7) | 10,2 (4,3;17,2) | 50 (19,5;75,7) |
| Sexo, n (%) | n=83 | n=16 | n=67 |
| Femenino | 54 (65,1%) | 7 (43,8%) | 47 (70,1%) |
| Masculino | 29 (34,9%) | 9 (56,3%) | 20 (29,9%) |
| Raza, n (%) | n=83 | n=16 | n=67 |
| Blanca | 80 (96,4%) | 15 (93,8%) | 65 (97,0%) |
| Negra | 1 (1,2%) | 0% | 1 (1,5%) |
| Asiática | 1 (1,2%) | 1 (6,3%) | 0% |
| Nativo de Hawái u otra isla del Pacífico | 1 (1,2%) | 0% | 1 (1,5%) |
ALPL: gen de la fosfatasa alcalina no específica de tejido; DE: desviación estándar; HPP: hipofosfatasia.
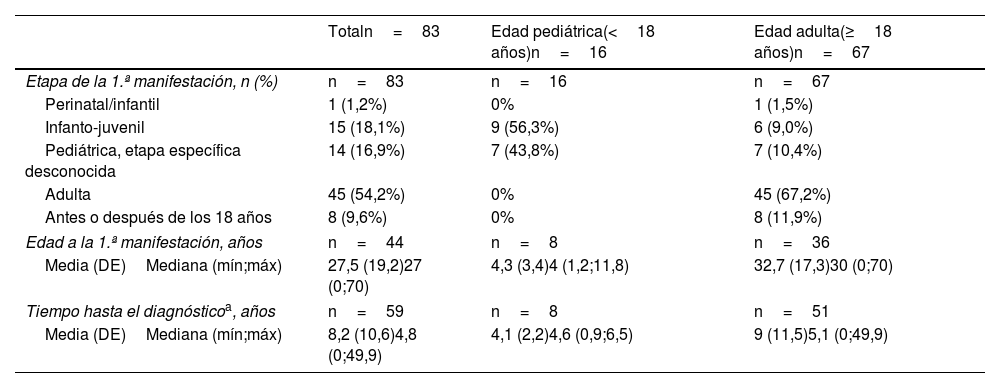
El número de sistemas afectados fue de (mediana [mín;máx]) uno (1;5) en niños y 2 (1;5) en adultos. Los datos cronológicos relacionados con el inicio de los síntomas, el diagnóstico y las principales manifestaciones clínicas observadas en los subgrupos de pacientes se detallan en las tablas 2 y 3, respectivamente.
Variables cronológicas relacionadas con el inicio de los síntomas y el diagnóstico
| Totaln=83 | Edad pediátrica(<18 años)n=16 | Edad adulta(≥18 años)n=67 | |
|---|---|---|---|
| Etapa de la 1.ª manifestación, n (%) | n=83 | n=16 | n=67 |
| Perinatal/infantil | 1 (1,2%) | 0% | 1 (1,5%) |
| Infanto-juvenil | 15 (18,1%) | 9 (56,3%) | 6 (9,0%) |
| Pediátrica, etapa específica desconocida | 14 (16,9%) | 7 (43,8%) | 7 (10,4%) |
| Adulta | 45 (54,2%) | 0% | 45 (67,2%) |
| Antes o después de los 18 años | 8 (9,6%) | 0% | 8 (11,9%) |
| Edad a la 1.ª manifestación, años | n=44 | n=8 | n=36 |
| Media (DE)Mediana (mín;máx) | 27,5 (19,2)27 (0;70) | 4,3 (3,4)4 (1,2;11,8) | 32,7 (17,3)30 (0;70) |
| Tiempo hasta el diagnósticoa, años | n=59 | n=8 | n=51 |
| Media (DE)Mediana (mín;máx) | 8,2 (10,6)4,8 (0;49,9) | 4,1 (2,2)4,6 (0,9;6,5) | 9 (11,5)5,1 (0;49,9) |
DE: desviación estándar; HPP: pacientes con hipofosfatasia; máx: máximo; mín: mínimo.
Manifestaciones clínicas basales relacionadas con los HPP
| Tipo de signos/síntomas | Total(n=83) | Edad pediátrica(<18 años)(n=16) | Edad adulta(≥18 años)(n=67) | Edad adulta(≥18 años)Inicio pediátrico(n=14) | Edad adulta(≥18 años)Inicio adulto(n=45) |
|---|---|---|---|---|---|
| Relacionados con el dolor, n (%) | 45 (54,2%) | 2 (12,5%) | 43 (64,2%) | 9 (64,3%) | 29 (64,4%) |
| Dolor óseo crónico | 39 (47,0%) | 2 (12,5%) | 37 (55,2%) | 6 (42,9%) | 27 (60,0%) |
| Dolor corporal generalizado | 9 (10,8%) | 0 (0%) | 9 (13,4%) | 2 (14,3%) | 6 (13,3%) |
| Fibromialgia | 3 (3,6%) | 0 (0%) | 3 (4,5%) | 2 (14,3%) | 1 (2,2%) |
| Dolor muscular crónico | 14 (16,9%) | 0 (0%) | 14 (20,9%) | 4 (28,6%) | 9 (20,0%) |
| Dentales, n (%) | 40 (48,2%) | 6 (37,5%) | 34 (50,7%) | 10 (71,4%) | 20 (44,4%) |
| Pérdida prematura dentadura deciduala | 8 (9,6%) | 3 (18,8%) | 5 (7,5%) | 5 (35,7%) | 0 (0%) |
| Otrosb | 36 (43,4%) | 3 (18,8%) | 33 (49,3%) | 9 (64,3%) | 20 (44,4%) |
| Esqueléticos, n (%) | 25 (30,1%) | 3 (18,8%) | 22 (32,8%) | 6 (42,9%) | 13 (28,9%) |
| Raquitismo (por rayos X) | 0 (0%) | 0 (0%) | 0 (0%) | 0 (0%) | 0 (0%) |
| Osteomalacia (por biopsia) | 1 (1,2%) | 0 (0%) | 1 (1,5%) | 0 (0%) | 1 (2,2%) |
| Inflamación crónica/edema médula ósea | 12 (14,5%) | 0 (0%) | 12 (17,9%) | 2 (14,3%) | 7 (15,6%) |
| Deformidad ósea | 8 (9,6%) | 2 (12,5%) | 6 (9,0%) | 3 (21,4%) | 3 (6,7%) |
| Fracturas/seudofracturas por cualquier causa, n (%)/n.° de fracturas | 24 (28,9%)/33 | 1 (6,3%)/3 | 23 (34,3%)/30 | 4 (28,6%)/4 | 19 (42,2%)/26 |
| Fracturas recurrentes y con difícil consolidación/seudofracturas | 6 (7,2%) | 1 (6,3%) | 5 (7,5%) | 2 (14,3%) | 3 (6,7%) |
| Reumatológicos, n (%) | 16 (19,3%) | 0 (0%) | 16 (23,9%) | 3 (21,4%) | 13 (28,9%) |
| Periartritis calcificante | 10 (12,0%) | 0 (0%) | 10 (14,9%) | 3 (21,4%) | 7 (15,6%) |
| Seudogota | 1 (1,2%) | 0 (0%) | 1 (1,5%) | 0 (0%) | 1 (2,2%) |
| Condrocalcinosis | 5 (6,0%) | 0 (0%) | 5 (7,5%) | 0 (0%) | 5 (11,1%) |
| Calcificaciones ectópicas | 3 (3,6%) | 0 (0%) | 3 (4,5%) | 0 (0%) | 3 (6,7%) |
| Renales, n (%) | 10 (12,0%) | 0 (0%) | 10 (14,9%) | 2 (14,3%) | 7 (15,6%) |
| Hipercalcemia/hipercalciuria/hiperfosfatemiaÚnicamente hiperfosfatemiaHiperfosfatemia e hipercalciuriaHipercalcemia e hipercalciuriaÚnicamente hipercalciuria | 8 (9,6%)5 (6,0%)1 (1,2%)1 (1,2%)1 (1,2%) | 0 (0%)0 (0%)0 (0%)0 (0%)0 (0%) | 8 (12,0%)5 (7,5%)1 (1,5%)1 (1,5%)1 (1,5%) | 2 (14,3%)1 (7%)0 (0%)1 (7,0%)0 (0%) | 5 (11,0%)4 (8,9%)0 (0%)0 (0%)1 (2,2%) |
| Nefrocalcinosis | 2 (2,4%) | 0 (0%) | 2 (3,0%) | 0 (0%) | 2 (4,4%) |
| Litiasis renal | 4 (4,8%) | 0 (0%) | 4 (6,0%) | 0 (0%) | 4 (8,9%) |
| Neurológicos, n (%) | 5 (6,0%) | 4 (25,0%) | 1 (1,5%) | 1 (7,1%) | 0 (0%) |
| Convulsiones | 1 (1,2%) | 1 (6,3%) | 0 (0%) | 0 (0%) | 0 (0%) |
| Craneosinostosis | 1 (1,2%) | 0 (0%) | 1 (1,5%) | 1 (7,1%) | 0 (0%) |
| Aumento de la presión intracraneal | 0 (0%) | 0 (0%) | 0 (0%) | 0 (0%) | 0 (0%) |
| Retraso cognitivo/retraso del desarrollo | 4 (4,8%) | 3 (18,8%) | 1 (1,5%) | 1 (7,1%) | 0 (0%) |
| Constitucional/metabólico, n (%) | 4 (4,8%) | 2 (12,5%) | 2 (3,0%) | 0 (0%) | 1 (2,2%) |
| Fallo de crecimiento | 1 (1,2%) | 1 (6,3%) | 0 (0%) | 0 (0%) | 0 (0%) |
| Fatiga | 3 (3,6%) | 1 (6,3%) | 2 (3,0%) | 0 (0%) | 1 (2,2%) |
| Musculares, n (%) | 3 (3,6%) | 1 (6,3%) | 2 (3,0%) | 2 (14,3%) | 0 (0%) |
| Retraso de la motricidad gruesa | 1 (1,2%) | 0 (0%) | 1 (1,5%) | 1 (7,1%) | 0 (0%) |
| Debilidad | 1 (1,2%) | 0 (0%) | 1 (1,5%) | 1 (7,1%) | 0 (0%) |
| Deambulación anómalac | 1 (1,2%) | 1 (6,3%) | 0 (0%) | 0 (0%) | 0 (0%) |
| Respiratorios, n (%) | 3 (3,6%) | 0 (0%) | 3 (4,5%) | 2 (14,3%) | 0 (0%) |
| Fallo respiratorio | 1 (1,2%) | 0 (0%) | 1 (1,5%) | 1 (7,1%) | 0 (0%) |
| Neumonía | 2 (2,4%) | 0 (0%) | 2 (3,0%) | 1 (7,1%) | 0 (0%) |
| N.° de signos/síntomas por paciente* | |||||
| Media (DE) | 2,53 (1,81) | 1,5 (1,17) | 2,74 (1,85) | 3,5 (2,70) | 2,6 (1,60) |
| Mediana (mín;máx) | 2 (1;9) | 1 (1;5) | 2 (1;9) | 2 (1;9) | 2 (1;7) |
| N.° de sistemas corporales afectados por paciente** | |||||
| Media (DE) | 2,07 (1,20) | 1,5 (1,20) | 2,20 (1,20) | 2,70 (1,40) | 2,00 (1,00) |
| Mediana (mín;máx) | 2 (1;5) | 1 (1;5) | 2 (1;5) | 2 (1;5) | 2 (1;4) |
| Signos/síntomas más afectados por orden de frecuencia | DentalNeurológicoEsquelético | DolorDentalEsquelético | DentalDolorEsquelético | DolorDentalEsquelético | |
DE: desviación estándar; HPP: pacientes con hipofosfatasia; máx, máximo; mín: mínimo.
El número de pacientes de los grupos incluidos (población total, pacientes pediátricos, adultos, adultos con formas de inicio pediátrico y adultos como formas de inicio en la etapa adulta) de los que se dispone del número de signos y síntomas y del número de sistemas corporales afectados por paciente es de n=73, n=12, n=61, n=13 y n=41.
En el grupo de edad pediátrica, la mitad de los pacientes comenzaron con síntomas en la etapa infanto-juvenil (56,3%), a una edad (mediana [mín;máx]) de 4 (1,2;11,8) años. La mediana de edad al diagnóstico fue de 9,8 (2;15,8) años, con un retraso del diagnóstico de 4,6 (0,9;6,5) años. Las manifestaciones dentales fueron las más frecuentes (37,5%), destacando la pérdida prematura de la dentadura decidual (18,8%). Las manifestaciones neurológicas (25,0%) constituyeron la segunda en frecuencia (el 18,8% presentó retraso cognitivo o del desarrollo y el 6,3%, convulsiones), seguidas por las esqueléticas (18,8%), de las cuales el 12,5% cursaron con deformidades óseas y el 6,3% con fracturas recurrentes. El dolor óseo crónico y los síntomas constitucionales (como el fallo de medro y la fatiga) se observaron en el 12,5% de los pacientes pediátricos y un paciente presentó deambulación anómala. Ninguno presentaba complicaciones respiratorias, renales o reumatológicas. En relación al tratamiento, 3 (18,8%) pacientes pediátricos habían recibido suplementos de vitamina D y ninguno bisfosfonatos o análogos de la PTH. Un paciente precisó de analgesia de primer escalón.
En los pacientes adultos, la primera manifestación se produjo a una edad (mediana [mín;máx]) de 30 años (0;70). La edad al diagnóstico fue de 46,4 (18,7;75,2) años y se registró un retraso en el mismo de 5,1 (0;49,9) años. El 23,7% de adultos con edad conocida al inicio de los síntomas comenzaron a presentar síntomas relacionados con HPP antes de los 18 años y el 76,3%, en la edad adulta. La manifestación clínica más frecuente en este grupo fue el dolor (64,2%), que era crónico en la mitad de los pacientes y generalizado en el 13,4%. La segunda manifestación más prevalente fue la dental (50,7%): el 49,3% sufrieron pérdida de dentadura permanente, dentición pobre e hipodoncia o precisaron de implantes, uso de puentes dentales o de prótesis extraíble. Además, el 7,5% de los pacientes presentó perdida dentaria decidual precoz. El 32,8% de los adultos mostraron signos y síntomas esqueléticos, la tercera manifestación en frecuencia. Concretamente, las fracturas o seudofracturas por cualquier causa estuvieron presentes en un tercio de los pacientes y fueron recurrentes y de difícil consolidación en el 7,5%. El 17,9% tuvo inflamación crónica/edema de médula ósea diagnosticada por resonancia magnética; el 9% mostró deformidades óseas y una paciente fue diagnosticada de osteomalacia mediante biopsia ósea. Las manifestaciones reumatológicas estuvieron presentes en un cuarto de los adultos y entre ellas destacó la periartritis calcificante (14,9%) y la condrocalcinosis (7,5%). Las manifestaciones menos frecuentes fueron las renales (14,9%), respiratorias (4,5%), musculares (3%), constitucionales (3%) y neurológicas (1,5%). En el grupo de adultos, 2 pacientes recibieron bisfosfonatos antes del diagnóstico de HPP y 3 fueron tratados con análogos de la PTH. El 70,1% de los adultos precisaron de fármacos analgésicos, que en el 13,4% fueron opiáceos.
El grupo de adultos se clasificó según el inicio de los síntomas tabla 3). La edad (mediana [mín;máx]) de aquellos en los que se iniciaron en la edad pediátrica (n=6) fue 10,4 (0;16,6) años y la de aquellos que comenzaron con síntomas a una edad ≥ 18 años (n=30) fue de 36,1 (mín: 18; máx: 70) años. La prevalencia de manifestaciones dentarias y esqueléticas fue mayor en el primer grupo respecto al segundo (71,4 vs. 44,4% y 42,9 vs. 28,9%), con más fracturas recurrentes y seudofracturas en el grupo de inicio pediátrico (14,3 vs 6,7%). Sin embargo, las prevalencias en términos de dolor fueron similares en ambos grupos (64,3 vs. 64,4%). En los adultos con inicio de síntomas en la infancia también se detectaron síntomas neurológicos, musculares y respiratorios, no objetivados en el otro grupo, mientras que en los de inicio en etapa adulta, se registraron síntomas constitucionales o metabólicos que no se evidenciaron en los de inicio pediátrico. El número de sistemas corporales afectados por paciente (mediana) fue de 2 en ambos grupos.
Cuestionarios informados por el paciente y carga de la enfermedadLos PRO analizados para esta publicación se limitan a la población adulta. En la visita de inclusión en el registro, en el cuestionario BPI (escala de 0-10 en la que una menor puntuación indica menos dolor e interferencia en la función diaria) se obtuvo una puntuación mediana (Q1;Q3) de la gravedad del dolor (BPI-S) de 3 (0,9;4,8) y una media (±DE) de 3±2,4, mientras que la puntuación mediana de la interferencia en la función diaria (BPI-I) fue 1,6 (Q1:0,3; Q3:4) y la media de 2,4±2,5. La puntuación mediana registrada en el HAQ-DI (escala de 0 a 3 en la que una mayor puntuación indica mayor discapacidad) fue 0,13 (0;0,6) con una media de 0,3±0,5. El cuestionario SF-36v2 (escala de 0-100 en la que menor puntuación indica peor estado de salud) mostró una puntuación mediana del componente sumario físico (PCS) de 44,8 (34,5;50,2) con una media de 43,2±11,4 y del mental (MCS) de 50,4 (38,9;56,5) con una media de 47,7±10,3. La figura 1 muestra los resultados basales de los cuestionarios BPI, HAQ-DI y SF-36v2.
Cuestionarios sobre dolor (BPI), discapacidad (HAQ-DI) y calidad de vida (SF-36v2) en la población adulta con HPP.
A) Puntuación mediana (mínimo, máximo e intervalo intercuartílico) en la visita basal del Cuestionario Breve para la Evaluación del Dolor (Brief Pain Inventory Short Form [BPI]) que valora la gravedad (BPI-S) y la interferencia (BPI-I) del dolor (escala de 0-10 en la que una menor puntuación indica menos dolor/interferencia con actividades cotidianas). La puntuación de BPI-S estaba disponible en 56 pacientes y la del BPI-I en 54 pacientes. B) Puntuación del Índice de Discapacidad del Cuestionario de Evaluación de la Salud (Health Assessment Questionnaire Disability Index [HAQ-DI]) mediante una escala de 0-3 (menor puntuación indica menor discapacidad). BPI y HAQ-DI se recogen en los pacientes ≥18 años. La puntuación de HAQ-DI estaba disponible en 59 pacientes. C) Puntuación mediana (mínimo, máximo e intervalo intercuartílico) en la visita basal del Cuestionario de Calidad de Vida Relacionada con la Salud o Salud Percibida (36-Item Short Form Survey Instrument [SF-36v2]). Escala 0-100, menor puntuación indica peor estado de salud. Se representan los 8 dominios de la salud (gris claro) que se agregan para calcular las puntuaciones del componente sumario físico (PCS) (gris claro) y la del mental (MCS) (gris oscuro). Los datos se recogen en los pacientes ≥18 años de edad. La puntuación de HAQ-DI estaba disponible en 59 pacientes.
CSF: componente sumario físico; CSM: componente sumario mental; DC: dolor corporal; FF: funcionamiento físico; FS: funcionamiento social; RE: rol emocional; RF: rol físico; SG: percepción de la salud general; SM: salud mental; VT: vitalidad.
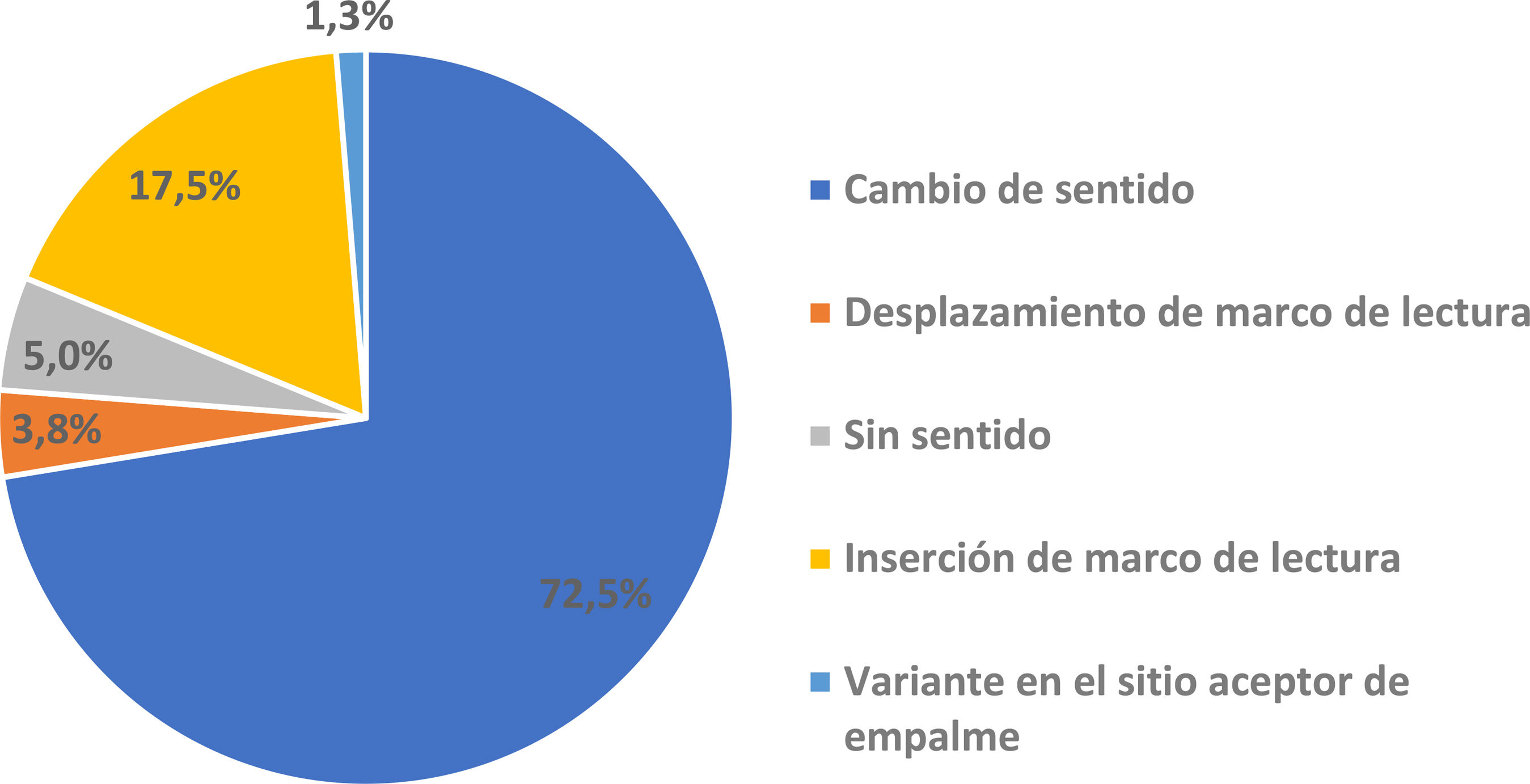
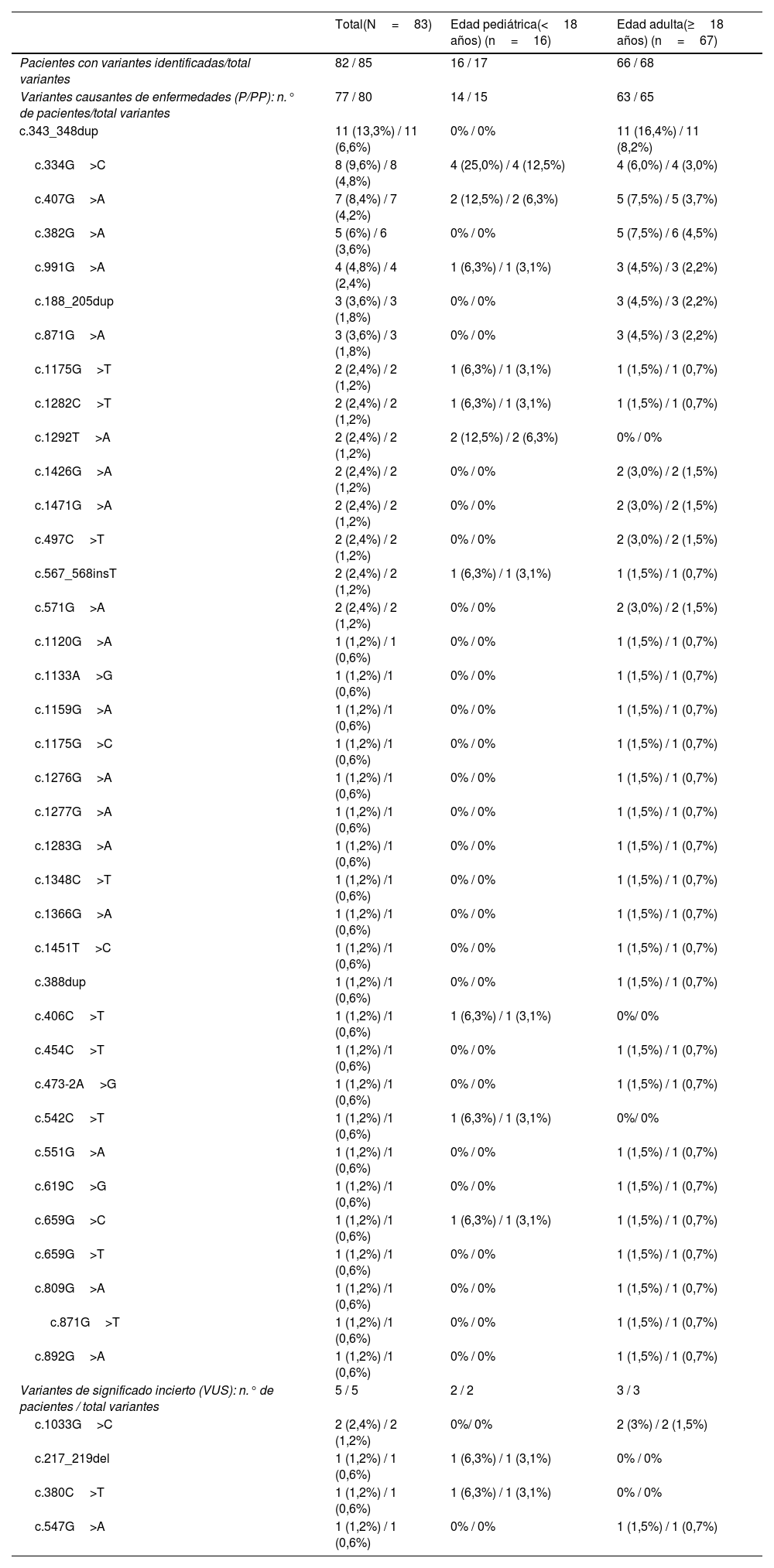
En el grupo de los pacientes menores de 18 años, 15/16 (93,8%) pacientes mostraron variantes en ALPL en heterocigosis y un paciente (6,2%) en heterocigosis compuesta. En los adultos, 64/66 (97%) presentaron variantes en ALPL en heterocigosis, un paciente en homocigosis (1,5%) y otro (1,5%) en heterocigosis compuesta. Se detectaron 85 variantes (94,1% causantes de enfermedad y 5,9% de significado incierto), la mayoría por cambio de sentido (missense) (82,4% en niños y 70,6% en adultos). La figura 2 recoge el tipo y frecuencia de variantes causantes de enfermedad en ALPL y la tabla 4 las variantes de la población estudiada.
Variantes genéticas en ALPL en la población estudiada
| Total(N=83) | Edad pediátrica(<18 años) (n=16) | Edad adulta(≥18 años) (n=67) | |
|---|---|---|---|
| Pacientes con variantes identificadas/total variantes | 82 / 85 | 16 / 17 | 66 / 68 |
| Variantes causantes de enfermedades (P/PP): n.° de pacientes/total variantes | 77 / 80 | 14 / 15 | 63 / 65 |
| c.343_348dup | 11 (13,3%) / 11 (6,6%) | 0% / 0% | 11 (16,4%) / 11 (8,2%) |
| c.334G>C | 8 (9,6%) / 8 (4,8%) | 4 (25,0%) / 4 (12,5%) | 4 (6,0%) / 4 (3,0%) |
| c.407G>A | 7 (8,4%) / 7 (4,2%) | 2 (12,5%) / 2 (6,3%) | 5 (7,5%) / 5 (3,7%) |
| c.382G>A | 5 (6%) / 6 (3,6%) | 0% / 0% | 5 (7,5%) / 6 (4,5%) |
| c.991G>A | 4 (4,8%) / 4 (2,4%) | 1 (6,3%) / 1 (3,1%) | 3 (4,5%) / 3 (2,2%) |
| c.188_205dup | 3 (3,6%) / 3 (1,8%) | 0% / 0% | 3 (4,5%) / 3 (2,2%) |
| c.871G>A | 3 (3,6%) / 3 (1,8%) | 0% / 0% | 3 (4,5%) / 3 (2,2%) |
| c.1175G>T | 2 (2,4%) / 2 (1,2%) | 1 (6,3%) / 1 (3,1%) | 1 (1,5%) / 1 (0,7%) |
| c.1282C>T | 2 (2,4%) / 2 (1,2%) | 1 (6,3%) / 1 (3,1%) | 1 (1,5%) / 1 (0,7%) |
| c.1292T>A | 2 (2,4%) / 2 (1,2%) | 2 (12,5%) / 2 (6,3%) | 0% / 0% |
| c.1426G>A | 2 (2,4%) / 2 (1,2%) | 0% / 0% | 2 (3,0%) / 2 (1,5%) |
| c.1471G>A | 2 (2,4%) / 2 (1,2%) | 0% / 0% | 2 (3,0%) / 2 (1,5%) |
| c.497C>T | 2 (2,4%) / 2 (1,2%) | 0% / 0% | 2 (3,0%) / 2 (1,5%) |
| c.567_568insT | 2 (2,4%) / 2 (1,2%) | 1 (6,3%) / 1 (3,1%) | 1 (1,5%) / 1 (0,7%) |
| c.571G>A | 2 (2,4%) / 2 (1,2%) | 0% / 0% | 2 (3,0%) / 2 (1,5%) |
| c.1120G>A | 1 (1,2%) / 1 (0,6%) | 0% / 0% | 1 (1,5%) / 1 (0,7%) |
| c.1133A>G | 1 (1,2%) /1 (0,6%) | 0% / 0% | 1 (1,5%) / 1 (0,7%) |
| c.1159G>A | 1 (1,2%) /1 (0,6%) | 0% / 0% | 1 (1,5%) / 1 (0,7%) |
| c.1175G>C | 1 (1,2%) /1 (0,6%) | 0% / 0% | 1 (1,5%) / 1 (0,7%) |
| c.1276G>A | 1 (1,2%) /1 (0,6%) | 0% / 0% | 1 (1,5%) / 1 (0,7%) |
| c.1277G>A | 1 (1,2%) /1 (0,6%) | 0% / 0% | 1 (1,5%) / 1 (0,7%) |
| c.1283G>A | 1 (1,2%) /1 (0,6%) | 0% / 0% | 1 (1,5%) / 1 (0,7%) |
| c.1348C>T | 1 (1,2%) /1 (0,6%) | 0% / 0% | 1 (1,5%) / 1 (0,7%) |
| c.1366G>A | 1 (1,2%) /1 (0,6%) | 0% / 0% | 1 (1,5%) / 1 (0,7%) |
| c.1451T>C | 1 (1,2%) /1 (0,6%) | 0% / 0% | 1 (1,5%) / 1 (0,7%) |
| c.388dup | 1 (1,2%) /1 (0,6%) | 0% / 0% | 1 (1,5%) / 1 (0,7%) |
| c.406C>T | 1 (1,2%) /1 (0,6%) | 1 (6,3%) / 1 (3,1%) | 0%/ 0% |
| c.454C>T | 1 (1,2%) /1 (0,6%) | 0% / 0% | 1 (1,5%) / 1 (0,7%) |
| c.473-2A>G | 1 (1,2%) /1 (0,6%) | 0% / 0% | 1 (1,5%) / 1 (0,7%) |
| c.542C>T | 1 (1,2%) /1 (0,6%) | 1 (6,3%) / 1 (3,1%) | 0%/ 0% |
| c.551G>A | 1 (1,2%) /1 (0,6%) | 0% / 0% | 1 (1,5%) / 1 (0,7%) |
| c.619C>G | 1 (1,2%) /1 (0,6%) | 0% / 0% | 1 (1,5%) / 1 (0,7%) |
| c.659G>C | 1 (1,2%) /1 (0,6%) | 1 (6,3%) / 1 (3,1%) | 1 (1,5%) / 1 (0,7%) |
| c.659G>T | 1 (1,2%) /1 (0,6%) | 0% / 0% | 1 (1,5%) / 1 (0,7%) |
| c.809G>A | 1 (1,2%) /1 (0,6%) | 0% / 0% | 1 (1,5%) / 1 (0,7%) |
| c.871G>T | 1 (1,2%) /1 (0,6%) | 0% / 0% | 1 (1,5%) / 1 (0,7%) |
| c.892G>A | 1 (1,2%) /1 (0,6%) | 0% / 0% | 1 (1,5%) / 1 (0,7%) |
| Variantes de significado incierto (VUS): n.° de pacientes / total variantes | 5 / 5 | 2 / 2 | 3 / 3 |
| c.1033G>C | 2 (2,4%) / 2 (1,2%) | 0%/ 0% | 2 (3%) / 2 (1,5%) |
| c.217_219del | 1 (1,2%) / 1 (0,6%) | 1 (6,3%) / 1 (3,1%) | 0% / 0% |
| c.380C>T | 1 (1,2%) / 1 (0,6%) | 1 (6,3%) / 1 (3,1%) | 0% / 0% |
| c.547G>A | 1 (1,2%) / 1 (0,6%) | 0% / 0% | 1 (1,5%) / 1 (0,7%) |
P: patogénicas; PP: probablemente patogénicas.
El Global HPP Registry constituye la mayor recopilación de datos de los pacientes con HPP procedentes de la práctica clínica rutinaria. En este artículo se analizan pormenorizadamente los datos de los pacientes pediátricos y adultos de centros españoles que fueron incluidos en dicho registro, los cuales reflejan que se trata de una enfermedad con una variedad de manifestaciones amplia, susceptible de afectar a varios sistemas orgánicos y que puede conferir una carga de enfermedad importante, condicionando una mayor puntuación en índices de discapacidad y deterioro de calidad de vida.
De manera similar a lo descrito en otras enfermedades minoritarias, en el registro nacional de HPP también se ha constatado un retraso importante en el diagnóstico. En la cohorte pediátrica nacional, el tiempo hasta el diagnóstico fue de 4,6 años, superior al publicado por Högler et al. en los pacientes de menos de una semana de vida: 0,1 meses (0-11,5 años) y a partir del año: 8,5 meses (0-10,7 años)10.
Las manifestaciones clínicas más frecuentes en los pacientes pediátricos fueron dentarias, neurológicas y esqueléticas. En el Global HPP Registry10, los pacientes pediátricos (n=121) comenzaron a presentar síntomas más precozmente y también la sintomatología más prevalente fue la dental (48,2%), que en España se identificó en el 37,5%. Las manifestaciones dentales de la enfermedad incluyen la exfoliación prematura, alteraciones estructurales de la dentadura, la hipoplasia del esmalte, las caries graves, pérdida de hueso alveolar y el agrandamiento de cámaras pulpares. Además, aunque la dentadura decidual es la más frecuentemente afectada, también pueden producirse alteraciones en la dentición permanente, por lo que se requiere un asesoramiento e intervenciones tempranas7. Las manifestaciones esqueléticas constituyeron la segunda manifestación en frecuencia en el Global HPP Registry (44,2%), con una prevalencia superior a la nacional de deformidades óseas (32,5 vs. 12,5%) y raquitismo (18,3 vs. 0%), mientras que la prevalencia de fracturas recurrentes y de difícil consolidación fue similar en ambas cohortes. Por otra parte, la clínica neurológica también fue frecuente, tanto en el Global HPP registry como en España y destacó la presencia de retraso cognitivo y del desarrollo y la presencia de convulsiones10. Ningún paciente de la cohorte española desarrolló complicaciones respiratorias, renales o reumatológicas, a diferencia de la serie internacional (18,6, 23,5 y 21%, respectivamente), en la que el 18,6% de niños precisaron de soporte respiratorio10. En conjunto, los datos obtenidos muestran que el subgrupo de pacientes de la cohorte pediátrica nacional se caracterizó por un inicio más tardío de síntomas y manifestaciones más leves que las observadas en el Global HPP Registry, datos que pueden condicionar la presencia de un mayor retraso diagnóstico en la cohorte nacional10.
En los pacientes adultos, los síntomas se iniciaron, fundamentalmente, con una edad ≥18 años (76,3%). Nuestros resultados están en consonancia con otras series que describieron un inicio frecuente de síntomas en la edad media de la vida12. Sin embargo, en la cohorte internacional (n=304) el porcentaje con formas de inicio en el adulto fue menor (44,6%). El sesgo de memoria, la falta de conocimiento de la enfermedad y una menor concienciación sobre sus manifestaciones menos críticas no nos permiten descartar que algunos de los pacientes clasificados como HPP de inicio en el adulto sean, en realidad, formas pediátricas no diagnosticadas. No obstante, trabajos previos no han observado diferencias en la carga de enfermedad atendiendo a la edad de inicio de los síntomas, poniendo de manifiesto las posibles limitaciones que ofrece la nosología actual8.
El registro español evidenció un retraso en el diagnóstico de hasta 5,1 años en adultos, hallazgo que pudiera estar en relación con el elevado porcentaje de pacientes con inicio en edad adulta. Las manifestaciones clínicas más frecuentes en el paciente adulto, por orden decreciente, fueron el dolor osteomuscular (64,2%), los signos y síntomas dentales (50,7%) y los esqueléticos (32,8%). También el Global HPP Registry mostró resultados similares (67,3, 54,3 y 43,3%, respectivamente)8. Estudios internacionales que incluyeron pacientes adultos con HPP mostraron una elevada prevalencia de dolor, que osciló entre un 41 y 95%10,12–14. Datos de series españolas constataron también una prevalencia significativa, que varió entre el 52,215 y el 79,5%16. En el historial médico de los pacientes del Global HPP Registry, el dolor también fue una manifestación frecuente, con una proporción de adultos que recibían analgésicos 3 veces superior a la de los niños, posiblemente debido a mayores dificultades para manifestar el dolor en edad pediátrica y la infraestimación de su gravedad por padres y facultativos10.
Por otra parte, Weber et al., tras realizar una encuesta a los pacientes con la enfermedad, encontró que en un 76% de los pacientes adultos el dolor era lo suficientemente significativo como para limitar sus actividades habituales13, y estudios previos han demostrado su repercusión en la función física y calidad de vida10,13,17. En este trabajo se ha evidenciado una repercusión discreta en términos de dolor (BPI-SF), similar a la observada por Seefried et al.8, y una repercusión significativa en el índice de discapacidad, ya que fue superior a la media de 0,25 descrita para la población general18. En la valoración de calidad de vida mediante el cuestionario SF-36v2, la media de las puntuaciones de los dominios de la cohorte española fue inferior a la media de la población general19. Estos datos son concordantes con los encontrados en el Global HPP Registry por Dahir et al., en los que se demostró una carga de enfermedad grave en adultos con HPP, independiente de la edad de inicio o de la presencia de afectación esquelética manifiesta20. También Santurtún et al., en una serie nacional, evaluaron los resultados de los PRO en los pacientes con niveles disminuidos de FA y encontraron peores puntuaciones en dolor corporal y otras dimensiones de calidad de vida (SF-36v2) en comparación con controles sanos21.
En lo que respecta a la afectación dentaria, segunda manifestación en frecuencia, también se ha observado una prevalencia similar, tanto en estudios españoles (28,6-46%)15,16,22 como internacionales (14-47%)12,14,23. Con frecuencia, estas manifestaciones pueden pasar inadvertidas en la práctica clínica. Sin embargo, muchos pacientes recuerdan haber presentado manifestaciones odontoestomatológicas que comenzaron en la edad pediátrica, por lo que resulta fundamental prestar atención a esta sintomatología en el proceso diagnóstico de la enfermedad17.
Las fracturas de estrés recurrentes en metatarsianos y seudofracturas de fémur son manifestaciones esqueléticas clásicas de la HPP24. En el registro nacional encontramos un porcentaje elevado de adultos con antecedentes de fracturas y seudofracturas (34,3%). Además, 2 recibieron tratamiento con bisfosfonatos antes del diagnóstico. Estudios españoles han encontrado una prevalencia similar de fracturas en adultos con HPP cercana al 40%16,22, que fueron múltiples en el 5%16. También, cohortes internacionales han registrado un porcentaje significativo de fracturas del 39-54%, con fracturas múltiples en el 15,8-36% de los pacientes12,14. Asimismo, Högler et al., en el Global HPP Registry, detectaron que un 36,5% de los adultos cursaron con fracturas recurrentes y de consolidación difícil, y que los bisfosfonatos habían sido prescritos hasta en un 17,6% de los pacientes en la cohorte internacional, probablemente antes de su diagnóstico10. Estos datos alertan de la importancia de vigilar los niveles de FA y considerar un posible diagnóstico de HPP previo antes de comenzar a administrar bisfosfonatos ante esta anomalía bioquímica25,26.
Las manifestaciones reumatológicas, como la periartritis calcificante y la condrocalcinosis, fueron más prevalentes en los adultos de la cohorte española (23,9%) que en la internacional (13,3%)8. Las calcificaciones periarticulares también han sido descritas en series de casos de adultos con HPP12,16,27,28. Además, la presencia de condrocalcinosis se ha objetivado en otras cohortes de pacientes con HPP con una frecuencia variable del 5-40%12,14,16,22,29. La afectación renal (14,9 y 15%) y respiratoria (4,5 y 4%) mostraron una prevalencia similar en la cohorte nacional e internacional, respectivamente. Por el contrario, en nuestra cohorte española se detectaron menos síntomas neurológicos (1,5%), musculares (3%) y constitucionales (3%) en comparación con los presentados por los adultos en el Global HPP Registry (11,4, 28,7 y 33,2%, respectivamente). Estas discrepancias no parecen explicarse por diferencias en variables demográficas o bioquímicas, como los niveles de FA, que fueron comparables en ambas cohortes8. Sin embargo, en la valoración clínica de los pacientes y los resultados obtenidos puede influir la variabilidad de especialidades médicas y/o quirúrgicas que atendieron a los pacientes.
Las manifestaciones dentarias y esqueléticas, como las fracturas, han sido más frecuentes en los adultos con formas de inicio pediátrico. Sin embargo, en las formas de inicio en el adulto, su prevalencia ha sido también significativa. Además, el dolor ha estado presente en casi dos tercios de los pacientes en ambos grupos y el número de sistemas corporales afectados fue de 2, similar en ambos grupos. Estos datos están en consonancia con los publicados en el Global HPP Registry, en el que los adultos con HPP frecuentemente presentaron dolor y alta carga de enfermedad, independientemente de la edad de inicio de los síntomas8,20, y cuya gravedad se ha relacionado con la necesidad de terapia enzimática sustitutiva20.
Las variantes en ALPL más frecuentes en nuestra cohorte fueron c.343_348dup, c.334 G>C y c.407G>A, c.382G>A y c.991G>A (tabla 4). Sin embargo, en el Global HPP Registry, la más prevalente fue c.571G>A, presente también en 2 pacientes del registro nacional, seguida de las variantes c.1250A>G y c.1159 del, que no fueron detectadas en la cohorte española. De forma similar, la mayoría de las variantes fueron por cambio de sentido, las más frecuentes según la base de datos de variantes del gen ALPL de la Johannes Kepler University Faculty of Medicine 202430. Por otra parte, gran parte de los pacientes del registro español mostraron variantes en ALPL en heterocigosis. Al respecto, cabe destacar que el estado genético podría influir en las diferencias clínicas observadas en la cohorte pediátrica entre el Global HPP Registry, con formas infantiles más graves y una prevalencia mayor de pacientes con 2 variantes en el gen ALPL, respecto al registro nacional10. Estas diferencias, por el contrario, no se observaron en adultos. El espectro de la enfermedad en individuos heterocigotos sigue siendo un tema relevante y los estudios de correlación genotipo-fenotipo pueden ser útiles para profundizar en este aspecto.
Como limitaciones, este estudio puede estar sujeto a determinados sesgos de selección en relación con los centros que reclutan pacientes, interesados en la investigación clínica de la HPP. Además, al tratarse de un registro multicéntrico en el que participan varias especialidades, las diferencias de práctica clínica entre centros y/o profesionales de formación diversa pueden haber afectado a la homogeneidad de datos. Asimismo, el sesgo de recuerdo puede haber influido en la recogida de datos históricos. Por otra parte, la exclusión de los pacientes fallecidos antes del reclutamiento puede infraestimar la gravedad en el subgrupo pediátrico y la menor presencia de varones adultos afectar a la caracterización en el sexo masculino. Además, no disponemos de acceso a los resultados genéticos individualizados, lo que impide establecer correlaciones genotipo-fenotipo en nuestra cohorte. Cabe destacar que esta correlación constituye un desafío particular en la HPP, caracterizada por una elevada heterogeneidad clínica, incluso entre miembros de una misma familia portadores de variantes en ALPL idénticas31,32, así como por la posible influencia de otros genes, mecanismos epigenéticos y factores ambientales, que podrían modular la expresividad de la enfermedad33.
Entre las principales fortalezas, destaca la metodología empleada y la inclusión de pacientes diagnosticados de HPP, con confirmación genética en su mayoría. El diseño del estudio y el tamaño muestral, considerable para una enfermedad minoritaria, ha facilitado la recogida de datos de manera sistematizada y consistente, permitiendo alcanzar un mayor conocimiento de la HPP tanto en pacientes adultos como pediátricos. Por otro lado, los futuros análisis de datos longitudinales obtenidos en el registro nacional permitirán conocer la evolución clínica y posibles complicaciones de los pacientes con HPP.
ConclusionesEl registro nacional de HPP constituye una herramienta de utilidad para caracterizar mejor la historia natural de la enfermedad en nuestro país. Los datos obtenidos confirman la existencia de un retraso significativo en el diagnóstico de la enfermedad y que se trata de una enfermedad sistémica con una amplia variedad de manifestaciones clínicas donde destacan las dentales y esqueléticas, además de las neurológicas en la edad pediátrica y el dolor en los adultos. La carga de la enfermedad, reflejada en el impacto en los índices de discapacidad y calidad de vida, determinan que sea preciso implementar estrategias para un diagnóstico más precoz que permita alcanzar un manejo adecuado.
FinanciaciónEste estudio, así como el Global HPP Registry, está patrocinado por Alexion, AstraZeneca Rare Disease, Boston MA, EE. UU. Alexion Pharma Spain S.L. (AstraZeneca Rare Disease Unit) ha financiado la redacción médica de esta publicación.
Consideraciones éticasEl protocolo del Global HPP Registry fue aprobado por el consejo de revisión institucional (o equivalente) en cada uno de los países participantes y fue realizado de acuerdo con los principios éticos de la Declaración de Helsinki y las guías de buena práctica clínica de acuerdo con la normativa europea sobre medicamentos. Todos los pacientes o padres/tutores legales proporcionaron su consentimiento informado por escrito y aprobaron la publicación de los datos médicos contenidos en el registro.
Declaración de la ia generativa en la escritura científicaNo se utilizó ningún tipo de herramienta de IA para la redacción o edición de este artículo.
Conflicto de interesesCarolina Tornero ha recibido una beca para investigación de Alexion y honorarios de Amgen, Alexion, Abbvie, Theramex, UCB y Gedeon-Richter.
Gabriel Ángel Martos-Moreno ha desarrollado labores de consultoría; ha recibido honorarios de Alexion, AstraZeneca Rare Disease; y pertenece al comité científico asesor del registro internacional de hipofosfatasia.
Núria Guañabens ha recibido honorarios de Amgen, Theramex, Gedeon-Richter y UCB.
Helena Flórez ha recibido honorarios personales de Amgen, Theramex, UCB, Rubió, STADA, Grünenthal y Gedeon-Richter.
Anna Ribera es empleada de AstraZeneca Rare Diseases Unit.
Pilar Aguado ha recibido una beca para investigación de Alexion y honorarios personales de Abbvie, Alexion, Amgen, Faes, Gedeon-Richter, GP-Pharm, Kyowa Kirin, Lilly, Rubió, UCB y Theramex.
Los autores quieren agradecer a los pacientes, a sus familias, a los investigadores y a las personas de los diferentes hospitales participantes en el Global HPP Registry. Los autores agradecen especialmente a la Dra. Garzón del Hospital Universitario 12 de Octubre (Madrid), al Dr. Malouf del Hospital de la Santa Creu i Sant Pau (Barcelona), a la Dra. Bou del Hospital Sant Joan de Déu (Esplugues de Llobregat, Barcelona), al Dr. Camins del Hospital General de Granollers (Granollers, Barcelona), a la Dra. Cacheda del Hospital de Son Llàtzer (Palma, Mallorca), al Dr. Manrique del Complejo Hospitalario de Navarra (Pamplona, Navarra) y a la Dra. Ceñal del Hospital Universitario de Móstoles (Móstoles, Madrid) por la utilización de los datos correspondientes a sus pacientes incluidos en el Global HPP Registry.
El soporte de redacción del manuscrito ha sido proporcionado por Fernando Sánchez Barbero de Content Ed Net (Madrid, España) y financiado por Alexion, AstraZeneca Rare Disease, Boston, MA, USA.







![Cuestionarios sobre dolor (BPI), discapacidad (HAQ-DI) y calidad de vida (SF-36v2) en la población adulta con HPP. A) Puntuación mediana (mínimo, máximo e intervalo intercuartílico) en la visita basal del Cuestionario Breve para la Evaluación del Dolor (Brief Pain Inventory Short Form [BPI]) que valora la gravedad (BPI-S) y la interferencia (BPI-I) del dolor (escala de 0-10 en la que una menor puntuación indica menos dolor/interferencia con actividades cotidianas). La puntuación de BPI-S estaba disponible en 56 pacientes y la del BPI-I en 54 pacientes. B) Puntuación del Índice de Discapacidad del Cuestionario de Evaluación de la Salud (Health Assessment Questionnaire Disability Index [HAQ-DI]) mediante una escala de 0-3 (menor puntuación indica menor discapacidad). BPI y HAQ-DI se recogen en los pacientes ≥18 años. La puntuación de HAQ-DI estaba disponible en 59 pacientes. C) Puntuación mediana (mínimo, máximo e intervalo intercuartílico) en la visita basal del Cuestionario de Calidad de Vida Relacionada con la Salud o Salud Percibida (36-Item Short Form Survey Instrument [SF-36v2]). Escala 0-100, menor puntuación indica peor estado de salud. Se representan los 8 dominios de la salud (gris claro) que se agregan para calcular las puntuaciones del componente sumario físico (PCS) (gris claro) y la del mental (MCS) (gris oscuro). Los datos se recogen en los pacientes ≥18 años de edad. La puntuación de HAQ-DI estaba disponible en 59 pacientes. CSF: componente sumario físico; CSM: componente sumario mental; DC: dolor corporal; FF: funcionamiento físico; FS: funcionamiento social; RE: rol emocional; RF: rol físico; SG: percepción de la salud general; SM: salud mental; VT: vitalidad. Cuestionarios sobre dolor (BPI), discapacidad (HAQ-DI) y calidad de vida (SF-36v2) en la población adulta con HPP. A) Puntuación mediana (mínimo, máximo e intervalo intercuartílico) en la visita basal del Cuestionario Breve para la Evaluación del Dolor (Brief Pain Inventory Short Form [BPI]) que valora la gravedad (BPI-S) y la interferencia (BPI-I) del dolor (escala de 0-10 en la que una menor puntuación indica menos dolor/interferencia con actividades cotidianas). La puntuación de BPI-S estaba disponible en 56 pacientes y la del BPI-I en 54 pacientes. B) Puntuación del Índice de Discapacidad del Cuestionario de Evaluación de la Salud (Health Assessment Questionnaire Disability Index [HAQ-DI]) mediante una escala de 0-3 (menor puntuación indica menor discapacidad). BPI y HAQ-DI se recogen en los pacientes ≥18 años. La puntuación de HAQ-DI estaba disponible en 59 pacientes. C) Puntuación mediana (mínimo, máximo e intervalo intercuartílico) en la visita basal del Cuestionario de Calidad de Vida Relacionada con la Salud o Salud Percibida (36-Item Short Form Survey Instrument [SF-36v2]). Escala 0-100, menor puntuación indica peor estado de salud. Se representan los 8 dominios de la salud (gris claro) que se agregan para calcular las puntuaciones del componente sumario físico (PCS) (gris claro) y la del mental (MCS) (gris oscuro). Los datos se recogen en los pacientes ≥18 años de edad. La puntuación de HAQ-DI estaba disponible en 59 pacientes. CSF: componente sumario físico; CSM: componente sumario mental; DC: dolor corporal; FF: funcionamiento físico; FS: funcionamiento social; RE: rol emocional; RF: rol físico; SG: percepción de la salud general; SM: salud mental; VT: vitalidad.](https://static.elsevier.es/multimedia/00257753/0000016500000005/v1_202510310437/S0025775325003483/v1_202510310437/es/main.assets/thumbnail/gr1.jpeg?xkr=ue/ImdikoIMrsJoerZ+w96p5LBcBpyJTqfwgorxm+Ow=)



