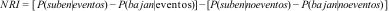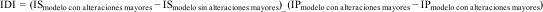Las alteraciones mayores del electrocardiograma (AMECG) son frecuentes en personas de mediana y avanzada edad, y podrían ser un factor importante en la predicción de eventos cardiovasculares (ECV).
ObjetivoAnalizar la asociación entre AMECG (clasificación de Minnesota) y ECV independientemente de los factores de riesgo cardiovascular (FRCV) clásicos y valorar si mejoran la predicción de la función de riesgo FRESCO-Función de Riesgo Española de Acontecimientos Coronarios.
MétodoSe incluyeron 1.752 participantes del estudio PREDIMED entre 55 y 80 años con RCV medio o alto, con una media de seguimiento de 5,1 años. Durante el periodo de seguimiento se ha estimado la incidencia acumulada de ECV por sexo y presencia de AMECG, y analizado la asociación entre AMECG y ECV mediante regresión multivariante de Cox ajustadas por grupo de aleatorización y RCV (FRESCO). Para analizar la mejora en la predicción se calcularon los índices C de Harrel's, Nam d’Agostino, Net Reclassification Improvement e Integrated Discrimination Improvement.
ResultadosAl inicio del estudio, un 25% de los participantes presentaron AMECG. Durante el seguimiento aparecieron 112 ECV (16 muertes cardiovasculares, 15 infartos agudo de miocardio, 38 anginas, 43 accidentes cerebrovasculares). Las AEMCG se asociaron a una mayor probabilidad de sufrir un ECV. En varones, las principales AMECG asociadas a la aparición de ECV fueron los criterios de hipertrofia de ventrículo izquierdo (HVE) con inversión de onda T (HR: 17,88; IC 95%: 5,51-58,03; p valor <0,001) y el alargamiento de QT (HR: 2,41; IC 95%: 1,38-4,21; p valor =0,002), y en mujeres la fibrilación auricular (HR: 5,7; IC 95%: 1,76-18,72; p valor =0,006) y el descenso del ST (HR: 3,24; IC 95%: 1,36-7,71; p valor <0,001). No se observó mejoría significativa en la capacidad predictiva de FRESCO al introducir las AMECG.
ConclusionesLas AMECG se asocian de manera independiente con los ECV, por lo que deben ser consideradas durante el curso del proceso clínico. Sin embargo, no ofrece una mejora adicional en la predicción del riesgo cardiovascular a la proporcionada por los factores de riesgo clásicos.
Major electrocardiogram abnormalities (MECG) are common in middle-aged and older individuals and could be an important factor in predicting cardiovascular events.
ObjectiveTo analyse the association between MECG (Minnesota classification) and CVE independently of classic cardiovascular risk factors (CVRF), and to assess whether they improve the prediction according to the Spanish Coronary Event Risk Function (FRESCO).
Method1.752 participants included in three nodes of the PREDIMED study aged between 55 and 80 years with medium or high CVRF. Mean follow-up time was 5.1 years. Cumulative CVE incidence was estimated by sex with and without MECG, and hazard ratios by sex were estimated using multivariate Cox regressions adjusted for randomization group and CCRF (FRESCO). Harrel's C Indices, Nam d’Agostino, Net Reclassification Improvement, and Integrated Discrimination Improvement were calculated.
ResultsAt baseline, 25% of the participants shows major electrocardiogram abnormalities (AMECG). During follow-up, there were 112 cardiovascular events (16 cardiovascular deaths, 15 acute myocardial infarctions, 38 anginas, 43 strokes). MECG were significantly associated with the onset of CVE. In men, left ventricular hypertrophy (LVH) criteria were associated with T-wave inversion (HR: 17.88, 95% CI: 5.51-58.03, pvalor<.001) and QT interval prolongation (HR: 2.41, 95% CI: 1.38-4.21, pvalor=.002); in women, atrial fibrillation (HR: 5.7, 95% CI: 1.76-18.72, pvalor=.006) and ST-segment depression (HR: 3.24, 95% CI: 1.36-7.71, pvalor<.001) were associated. No significant improvement in MECG prediction compared to FRESCO was observed.
ConclusionsMECG are independently associated with the occurrence of CVE, but do not improve risk prediction beyond traditional risk factors.
La enfermedad cardiovascular (ECV) continúa siendo la primera causa de muerte en los países de nuestro entorno1 siendo su prevención un objetivo prioritario de salud pública2. La cuantificación del riesgo individual de padecer la enfermedad, según la presencia de los factores de riesgo, permite individualizar la intensidad de acciones preventivas y es una estrategia preventiva de contrastada eficiencia3.
Diferentes funciones o ecuaciones de cálculo del riesgo cardiovascular (RCV) han sido desarrolladas a partir de estudios poblacionales longitudinales que permiten predecir la probabilidad de presentar ECV para cierta franja etaria en un período determinado de tiempo. La mayoría predicen el riesgo a los 10 años y en personas de 35 a 74 años4–6. La ecuación del Framingham Heart Study (FHS)7 ha sido validada en diferentes poblaciones diferentes de la original, entre ellas en España con datos del Registre Gironí del Cor (REGICOR)8. Más recientemente se diseñó y validó en nuestro país la ecuación de riesgo Función de Riesgo Española de Acontecimientos Coronarios (FRESCO) utilizando datos provenientes de 11 cohortes pertenecientes a siete comunidades autónomas9. Ambas ecuaciones, FRESCO y Framingham-REGICOR, estiman la aparición de ECV en una población del Sur de Europa, aunque la ecuación Framingham-REGICOR tiende a sobrestimar la aparición de ECV. A pesar de los intentos de adaptar las ecuaciones de RCV a poblaciones con una incidencia baja de ECV, alrededor de un 20% de los ECV ocurren en personas sin factores de RCV incluidos en las ecuaciones desarrolladas10.
Las alteraciones del electrocardiograma podrían tener importancia pronóstica en la detección de enfermedad cardiovascular subyacente. Las alteraciones del electrocardiograma se clasifican en alteraciones menores y mayores de acuerdo con la codificación internacional de Minnesota11. Siendo las alteraciones mayores del electrocardiograma (AMECG) las que han demostrado asociarse a un mayor RCV12–15. Las AMECG comprenden el descenso patológico del segmento ST (>0,05mV), la onda T invertida> de −0,5m, criterios de hipertrofia ventricular izquierda (HVE) con inversión de la onda T (patrón de sobrecarga), bloqueo de rama derecha del Haz de Hiss (BRDHH), el bloqueo de la rama izquierda del haz de Hiss (BRIHH), el alargamiento del intervalo QT, el bloqueo auriculoventricular avanzado (de segundo grado tipo Mobitz II o de grado 3.°), la alteración de la conducción intraventricular inespecífica (QRS>110ms), el flutter auricular y la fibrilación auricular.
Diferentes estudios han relacionado la presencia de alteraciones electrocardiográficas con la aparición de ECV fatales y no fatales16–18. Sin embargo, no ha sido evaluada de manera exhaustiva su posible contribución a la mejora de la predicción individual del RCV19,20.
La utilización de una técnica diagnóstica no invasiva, económica y ampliamente utilizada como es el electrocardiograma para mejorar la determinación del RCV podría tener gran relevancia en la prevención de la enfermedad, especialmente en población de riesgo moderado, donde se producen el mayor número absoluto de ECV al ser el segmento más numeroso de población. Sin embargo, su utilidad no ha sido estudiada en población mediterránea del riesgo moderado/alto, cuyo comportamiento respecto a la enfermedad cardiovascular tiene características singulares21.
Los objetivos de nuestro estudio son: a) analizar la asociación entre la presencia de AMECG, según la clasificación de Minnesota, y la aparición de ECV en una población de RCV moderado/alto, b) determinar si esta asociación es independiente de la presencia de factores de RCV clásicos (según FRESCO) y c) analizar su contribución a la mejora de la predicción de ECV.
MétodoDiseño y población de estudioEste estudio se ha realizado en una submuestra del estudio PREvención con DIeta MEDiterránea (PREDIMED)22,23, un ensayo clínico prospectivo multicéntrico aleatorizado que incluyó 7.447 pacientes de 55 a 80 años con RCV medio o alto y evaluó el efecto de la dieta mediterránea en la prevención primaria de la ECV en tres grupos de individuos: 1) con dieta mediterránea suplementada con aceite de oliva virgen extra (AOVE), 2) con dieta mediterránea suplementada con frutos secos y 3) un grupo control al que se le recomendaba seguir una dieta baja en grasas tanto de origen animal como vegetal. El estudio PREDIMED demostró la capacidad de la dieta mediterránea suplementada de reducir el riesgo de presentar ECV tras una mediana de 4,8 años de seguimiento. Los participantes elegibles para el estudio fueron varones de 55 a 80 años y mujeres de 60 a 80 años, con RCV medio o alto y sin enfermedad cardiovascular previa al momento de la inclusión y con ECG legible en los tres nodos que participaron. Los criterios de inclusión incluyeron individuos con diabetes mellitus tipo 2 o la presencia de al menos tres de los siguientes factores de riesgo: tabaquismo, hipertensión, altos niveles de colesterol de lipoproteínas de muy baja densidad y bajas de alta densidad, sobrepeso u obesidad, o antecedentes familiares de enfermedad coronaria prematura. El criterio de exclusión principal fue el haber presentado algún evento cardiovascular previamente. Una descripción más detallada de los criterios PREDIMED de inclusión y exclusión, así como los procedimientos utilizados han sido descritos previamente24.
En el presente estudio se incluyeron todos los participantes incluidos en PREDIMED en los nodos de Reus, Pamplona y Palma. La realización de ECG al inicio y durante el estudio se realizó en todos los nodos, se eligieron los pacientes de estos 3 nodos por ser los únicos que disponían de ellos de forma sistemática y accesible.
Identificación de la presencia de alteraciones electrográficas mayoresLa lectura de los ECG fue realizada por 3 de los autores de forma paralela (JPB, MJAA y MFS) siguiendo un formulario consensuado previamente por 2 de los cardiólogos autores (FAB y MFS), siendo revisados por el último (MFS). Se consideraron AMECG las codificadas según la clasificación de Minnesota: descenso del segmento ST superior a 0,05mV medido en el punto J horizontal o descendente, onda T invertida mayor o igual a −0,5mV, criterios de HVE (considerando alguno de: RI+SIII mayor de 25mm y/o S V1+RV5-6 mayor o igual a 35mV y/o R de aVL≥11mm o ≥16mm en presencia de hemibloqueo anterior) con inversión de onda T (patrón de sobrecarga), bloqueo avanzado de rama derecha, bloqueo avanzado de rama izquierda, alargamiento del intervalo QT (>470ms en mujeres y >450ms en varones), bloqueo auriculoventricular avanzado (de segundo grado tipo Mobitz II o de grado 3.°), alteración inespecífica de la conducción intraventricular (QRS>110ms), flutter auricular y fibrilación auricular.
Seguimiento y eventos cardiovascularesDefinimos evento cardiovascular como la presencia durante el estudio de infarto de miocardio, accidente cerebrovascular, angina y muerte por causas cardiovasculares. Los criterios para la adjudicación de los eventos y muerte cardiovasculares se describen detalladamente en Martínez-González et al.24.
Se utilizaron 4 fuentes de información para identificar los eventos: contactos repetidos con los participantes y sus médicos de familia, revisión anual de historia clínica y consulta del Índice Nacional de Defunciones. Un comité de expertos, cuyos miembros desconocían el grupo asignado al paciente, revisó la información referente al evento y decidían su adjudicación. Solo se incluyeron en los análisis los eventos confirmados por el comité de adjudicación y que ocurrieron entre el 25 de junio de 2003 y el 1 de diciembre de 2010.
Ecuación de riesgo FRESCOLa ecuación FRESCO de cálculo de RCV se desarrolló en 2014 a partir de un análisis conjunto de 11 estudios de cohortes de población española (1992-2005) incluyendo 50.408 participantes entre 35 y 79 años seguidos durante un periodo de 10 años a través de revisiones de sus historias clínicas, contactos telefónicos y el registro de mortalidad. Las variables utilizadas para predecir el RCV en la ecuación FRESCO son la presencia de tabaquismo, diabetes, los niveles de tensión arterial sistólica, el perfil lipídico y el índice de masa corporal. Se encuentran disponibles dos modelos de predicción para varones y mujeres: A (utilizando edad, tabaquismo e índice de masa corporal) y B (añadiendo los niveles de tensión arterial sistólica, colesterol total, colesterol HDL y la presencia de tratamiento antihipertensivo).
Métodos estadísticosSe analizó la distribución de las características clínicas y sociodemográficas en función de la presencia de AMECG en varones y mujeres. Se reportaron las variables cuantitativas como media y desviación estándar y las variables cualitativas como número y porcentaje.
Se calculó la incidencia acumulada de ECV en las personas con AMECG. Se realizaron modelos de riesgos proporcionales por sexo mediante regresiones multivariantes de Cox, ajustadas por el grupo de aleatorización del estudio PREDIMED y los factores de riesgo de la ecuación de RCV de FRESCO.
Comprobamos la proporcionalidad de riesgo de las variables incluidas usando la representación gráfica de los «residuos de Schoenfeld y el phtest». Una vez asumida la proporcionalidad de riesgos realizamos los modelos de regresión de Cox y reportamos los hazard ratio (HR) con los intervalos de confianza del 95% (IC 95%).
Utilizamos el índice C de Harrells para determinar la discriminación de nuestros modelos; valores de este índice de 0,50 a 0,75 indican concordancia baja, de 0,76 a 0,90 media y de 0,91 a 1 alta. El índice C de Harrells es conceptualmente análogo al área bajo la curva (AUC).
También evaluamos el estadístico de Nam D’Agostino como un indicador de la bondad de ajuste global de los modelos predictivos. Un valor más alto indica un mejor ajuste del modelo.
Reclasificación del riesgo cardiovascularLa reclasificación del riesgo de evento cardiovascular se evaluó comparando las estimaciones de RCV de los modelos de regresión de Cox incluyendo o no las AMECG. Se utilizaron el «Net Reclassification Improvement» (NRI) que evalúa las mejoras en la reclasificación del RCV sumando las mejoras de reclasificación de los individuos que experimentaron un ECV y los que no. Los individuos se clasifican según su riesgo en 4 categorías (0-4,99%, 5-9,99%, 10-19,99% y más 20%) y se determina la proporción de paciente que tras introducir las AMECG en el modelo pasan a otra categoría de riesgo en los pacientes con y sin evento. Se considera una mejora en la reclasificación un paciente que sufrió un evento cardiovascular y que hubiera aumentado de riesgo tras introducir las AMECG o en pacientes que no ha sufrido ningún evento cardiovascular que disminuyera de categoría de riesgo tras introducir las AMECG:
Net Reclassification Improvement:
También se calculó el «Integrated Discrimation Improvement» (IDI), que se define como la modificación de la probabilidad de presentar evento cardiovascular al considerar introducir un nuevo criterio. Se formula como:
Donde IS es la integral de la sensibilidad e IP es la integral de 1-especificidad sobre todos los posibles puntos de corte y calcula la variación de probabilidad de presentar ECV de los individuos que presentan AMECG.
Se realizaron análisis por subgrupos de varones, mujeres e individuos de riesgo CV medio. Se utilizaron los programas Stata (versión 15, StataCorp LLC, College Station, TX, EE. UU.) para los análisis estadísticos y la función ggplots de R Studio para las gráficas de incidencia acumulada (versión 11.0, RStudio, PBC, Boston, MA, EE. UU.).
ResultadosEl presente estudio ha sido realizado sobre 1.752 participantes (43,6 varones y 56,4% mujeres) del estudio PREDIMED (23,5% del total de personas incluidas en el estudio). El período de seguimiento en esta submuestra fue de 5,1 años (DE: 1,5 años) identificándose 112 ECV incidentes, 15 infartos agudo de miocardio (53,3% varones), 38 anginas (71,1% varones), 43 accidentes cerebrovasculares (55,8% varones) y 16 muertes por causas cardiovasculares (56,3% varones).
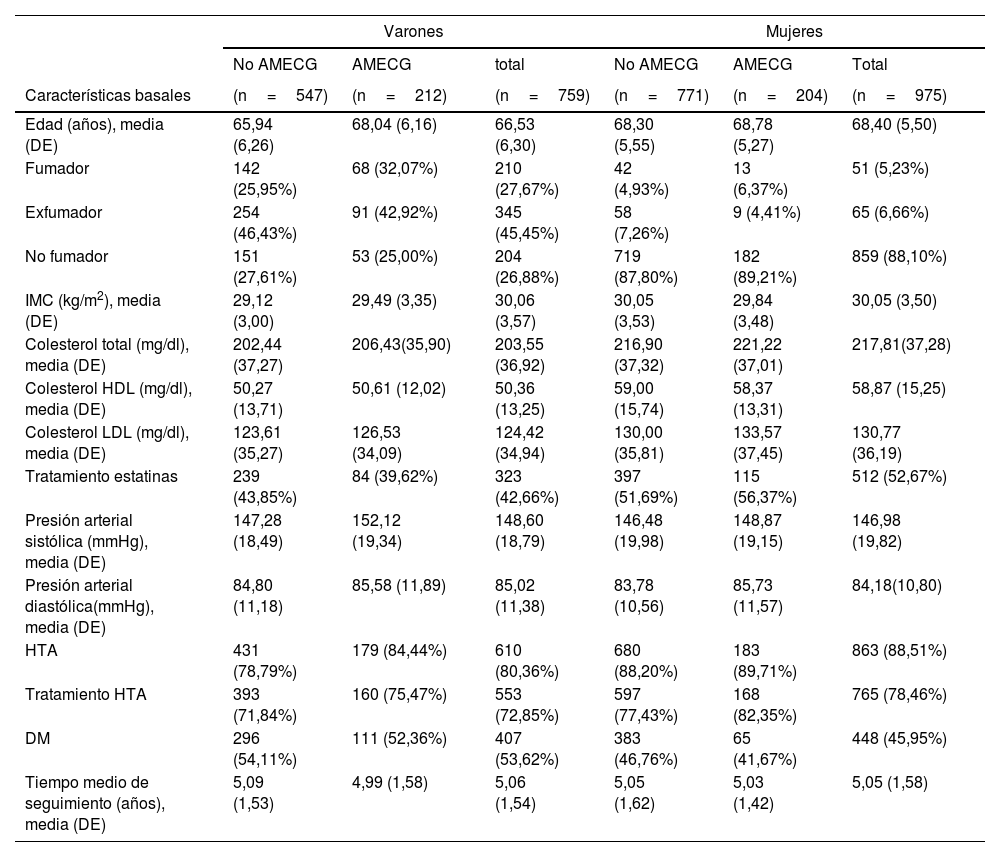
Las AMECG, fueron más frecuentes en los varones (27,9%) en comparación con las mujeres (20,9%). Entre los varones, se registró una mayor prevalencia de fumadores (27,67 frente al 5,23%), una menor incidencia de hipertensión (84,44 frente al 88,51%) y una mayor tasa de diabetes (53,63 frente al 45,95%) en comparación con las mujeres. Además, las mujeres presentaron niveles más elevados de colesterol total (217,81 frente a 203,43mg/dl en los varones) y colesterol HDL (58,87 frente a 50,36mg/dl), y fueron tratadas con mayor frecuencia con estatinas (52,67% frente al 42,66%) (tabla 1).
Características basales durante el seguimiento de los varones y de las mujeres con y sin AMECG incluidos en el estudio
| Varones | Mujeres | |||||
|---|---|---|---|---|---|---|
| No AMECG | AMECG | total | No AMECG | AMECG | Total | |
| Características basales | (n=547) | (n=212) | (n=759) | (n=771) | (n=204) | (n=975) |
| Edad (años), media (DE) | 65,94 (6,26) | 68,04 (6,16) | 66,53 (6,30) | 68,30 (5,55) | 68,78 (5,27) | 68,40 (5,50) |
| Fumador | 142 (25,95%) | 68 (32,07%) | 210 (27,67%) | 42 (4,93%) | 13 (6,37%) | 51 (5,23%) |
| Exfumador | 254 (46,43%) | 91 (42,92%) | 345 (45,45%) | 58 (7,26%) | 9 (4,41%) | 65 (6,66%) |
| No fumador | 151 (27,61%) | 53 (25,00%) | 204 (26,88%) | 719 (87,80%) | 182 (89,21%) | 859 (88,10%) |
| IMC (kg/m2), media (DE) | 29,12 (3,00) | 29,49 (3,35) | 30,06 (3,57) | 30,05 (3,53) | 29,84 (3,48) | 30,05 (3,50) |
| Colesterol total (mg/dl), media (DE) | 202,44 (37,27) | 206,43(35,90) | 203,55 (36,92) | 216,90 (37,32) | 221,22 (37,01) | 217,81(37,28) |
| Colesterol HDL (mg/dl), media (DE) | 50,27 (13,71) | 50,61 (12,02) | 50,36 (13,25) | 59,00 (15,74) | 58,37 (13,31) | 58,87 (15,25) |
| Colesterol LDL (mg/dl), media (DE) | 123,61 (35,27) | 126,53 (34,09) | 124,42 (34,94) | 130,00 (35,81) | 133,57 (37,45) | 130,77 (36,19) |
| Tratamiento estatinas | 239 (43,85%) | 84 (39,62%) | 323 (42,66%) | 397 (51,69%) | 115 (56,37%) | 512 (52,67%) |
| Presión arterial sistólica (mmHg), media (DE) | 147,28 (18,49) | 152,12 (19,34) | 148,60 (18,79) | 146,48 (19,98) | 148,87 (19,15) | 146,98 (19,82) |
| Presión arterial diastólica(mmHg), media (DE) | 84,80 (11,18) | 85,58 (11,89) | 85,02 (11,38) | 83,78 (10,56) | 85,73 (11,57) | 84,18(10,80) |
| HTA | 431 (78,79%) | 179 (84,44%) | 610 (80,36%) | 680 (88,20%) | 183 (89,71%) | 863 (88,51%) |
| Tratamiento HTA | 393 (71,84%) | 160 (75,47%) | 553 (72,85%) | 597 (77,43%) | 168 (82,35%) | 765 (78,46%) |
| DM | 296 (54,11%) | 111 (52,36%) | 407 (53,62%) | 383 (46,76%) | 65 (41,67%) | 448 (45,95%) |
| Tiempo medio de seguimiento (años), media (DE) | 5,09 (1,53) | 4,99 (1,58) | 5,06 (1,54) | 5,05 (1,62) | 5,03 (1,42) | 5,05 (1,58) |
AMECG; alteraciones mayores del electrocardiograma; Colesterol HDL: High Density Cholesterol; Colesterol LDL: Low density Cholesterol; DE: desviación estándar; DM: diabetes mellitus; HTA: hipertensión arterial; IMC: índice de masa corporal.
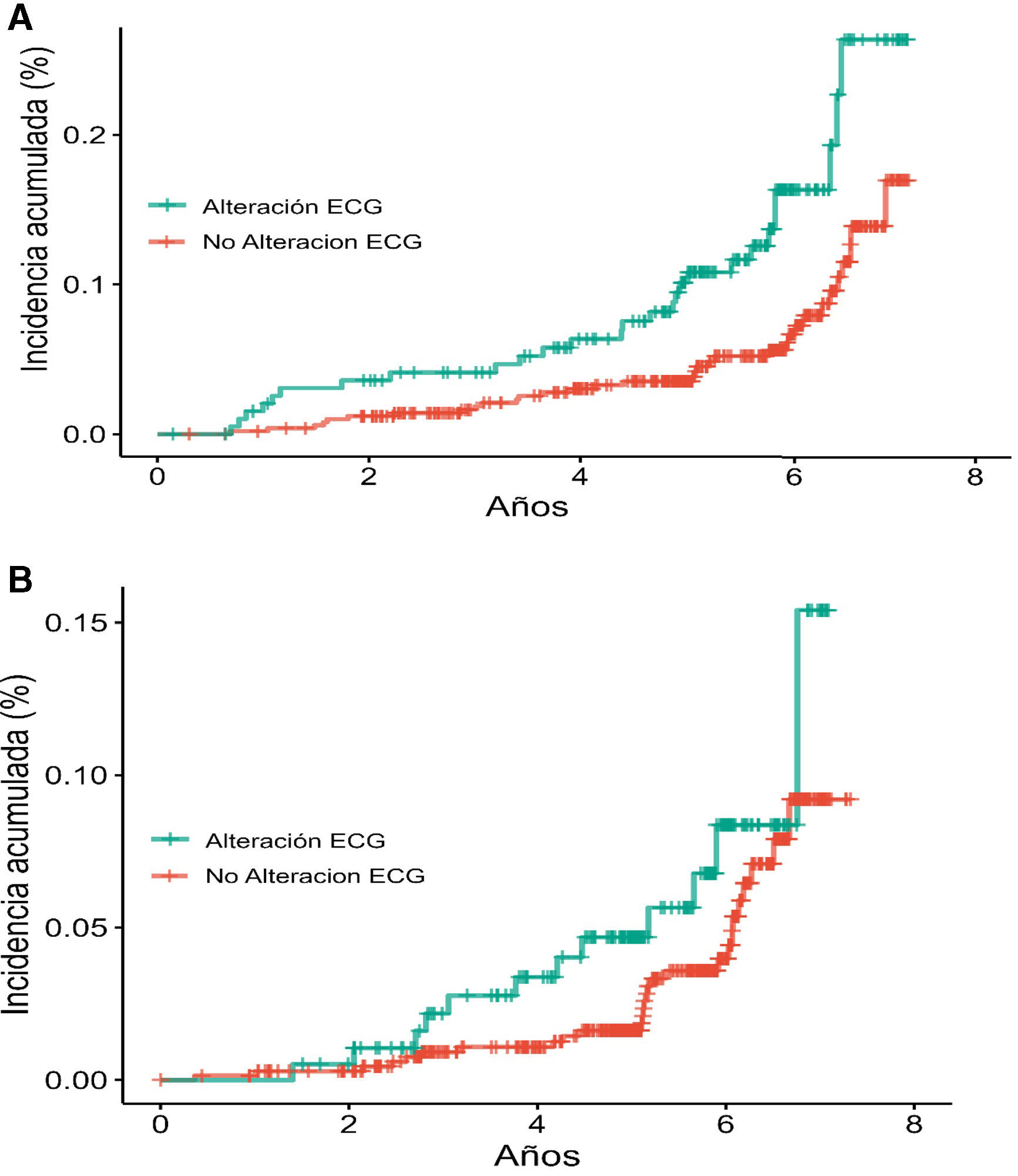
En general, tanto en varones como en mujeres, la prevalencia de AMECG fue mayor entre los fumadores (32,07 frente al 25,95% en varones y 6,37 frente al 4,93% en mujeres). La hipertensión fue más común en varones con AMECG (84,44 frente al 78,79%), mientras que en mujeres la prevalencia de hipertensión fue similar independientemente de la presencia de AMECG (89,71 frente al 88,20%). Observamos una mayor incidencia acumulada de aparición de ECV en los sujetos con AMECG desde el inicio del estudio tanto en varones como en mujeres (fig. 1), se observa una magnitud del efecto mayor en los varones.
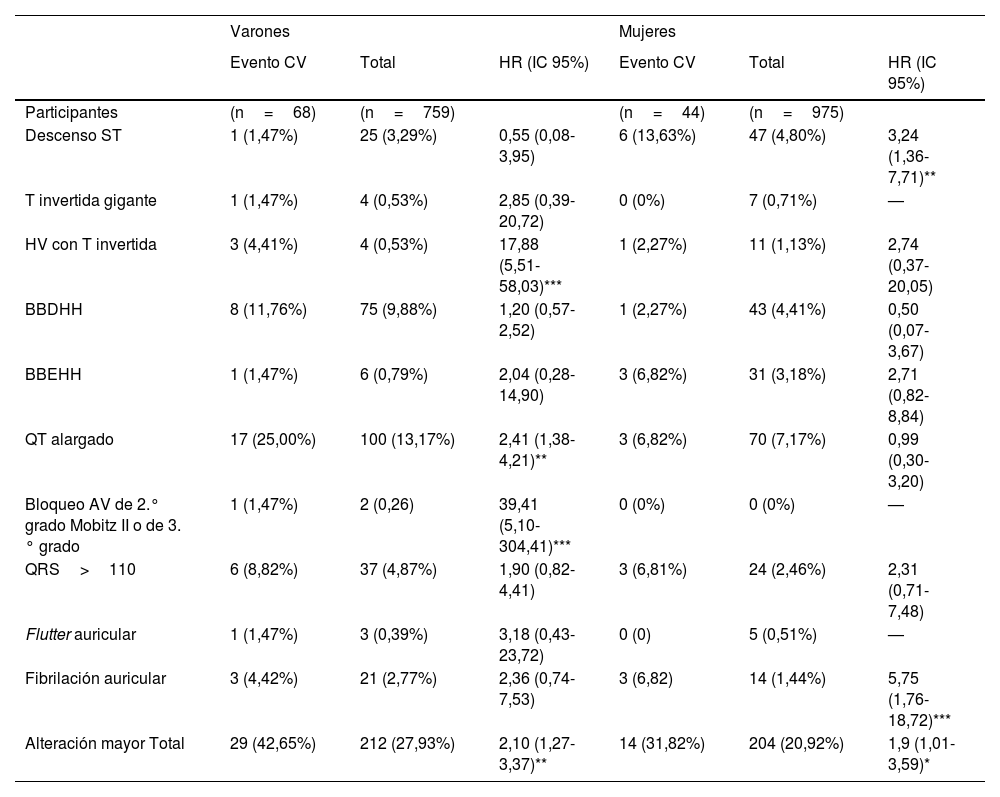
En varones, observamos una asociación estadísticamente significativa entre la presencia de AMECG y ECV tanto en el modelo ajustado solo por grupo intervención (HR: 2,10; IC 95%: 1,30-3,40) como en el modelo ajustados por otros factores de riesgo presentes en la ecuación FRESCO (HR: 2,10; IC 95%: 1,26-3,50). En mujeres, la presencia de AMECG se asocia con ECV en los modelos crudos (HR: 1,93; IC 95%: 1,02-3,64), pero pierde significación estadística al ajustar por otros factores de RCV (HR: 1,64; IC 95%: 0,83-3,25) (tabla 2).
Alteraciones mayores según codificación de Minnesota y aparición de eventos cardiovasculares
| Varones | Mujeres | |||||
|---|---|---|---|---|---|---|
| Evento CV | Total | HR (IC 95%) | Evento CV | Total | HR (IC 95%) | |
| Participantes | (n=68) | (n=759) | (n=44) | (n=975) | ||
| Descenso ST | 1 (1,47%) | 25 (3,29%) | 0,55 (0,08-3,95) | 6 (13,63%) | 47 (4,80%) | 3,24 (1,36-7,71)** |
| T invertida gigante | 1 (1,47%) | 4 (0,53%) | 2,85 (0,39-20,72) | 0 (0%) | 7 (0,71%) | — |
| HV con T invertida | 3 (4,41%) | 4 (0,53%) | 17,88 (5,51-58,03)*** | 1 (2,27%) | 11 (1,13%) | 2,74 (0,37-20,05) |
| BBDHH | 8 (11,76%) | 75 (9,88%) | 1,20 (0,57-2,52) | 1 (2,27%) | 43 (4,41%) | 0,50 (0,07-3,67) |
| BBEHH | 1 (1,47%) | 6 (0,79%) | 2,04 (0,28-14,90) | 3 (6,82%) | 31 (3,18%) | 2,71 (0,82-8,84) |
| QT alargado | 17 (25,00%) | 100 (13,17%) | 2,41 (1,38-4,21)** | 3 (6,82%) | 70 (7,17%) | 0,99 (0,30-3,20) |
| Bloqueo AV de 2.° grado Mobitz II o de 3.° grado | 1 (1,47%) | 2 (0,26) | 39,41 (5,10-304,41)*** | 0 (0%) | 0 (0%) | — |
| QRS>110 | 6 (8,82%) | 37 (4,87%) | 1,90 (0,82-4,41) | 3 (6,81%) | 24 (2,46%) | 2,31 (0,71-7,48) |
| Flutter auricular | 1 (1,47%) | 3 (0,39%) | 3,18 (0,43-23,72) | 0 (0) | 5 (0,51%) | — |
| Fibrilación auricular | 3 (4,42%) | 21 (2,77%) | 2,36 (0,74-7,53) | 3 (6,82) | 14 (1,44%) | 5,75 (1,76-18,72)*** |
| Alteración mayor Total | 29 (42,65%) | 212 (27,93%) | 2,10 (1,27-3,37)** | 14 (31,82%) | 204 (20,92%) | 1,9 (1,01-3,59)* |
BBDHH: bloqueo de rama derecha del Haz de Hiss; BBEHH: bloqueo de rama izquierda del Haz de Hiss; CV: cardiovascular; HR: hazard ratio; HVE: criterios de hipertrofia de ventrículo izquierdo; IC 95%: intervalo de confianza del 95%.
Hay diferencias entre sexos en las AMECG que de forma individual contribuyen a esta asociación (tabla 2). En varones son los criterios de HVE con T invertida (HR: 17,88; IC 95%: 5,51-58,03; p valor <0,001) (patrón de sobrecarga) y el alargamiento del QT (HR: 2,41; IC 95%: 1,38-4,21; p valor=0,002) y en mujeres el descenso patológico del ST (HR: 3,24; IC 95%: 1,36-7,71; p valor <0,001) y la fibrilación auricular (HR: 5,7; IC 95%: 1,76-18,72; p valor=0,006).
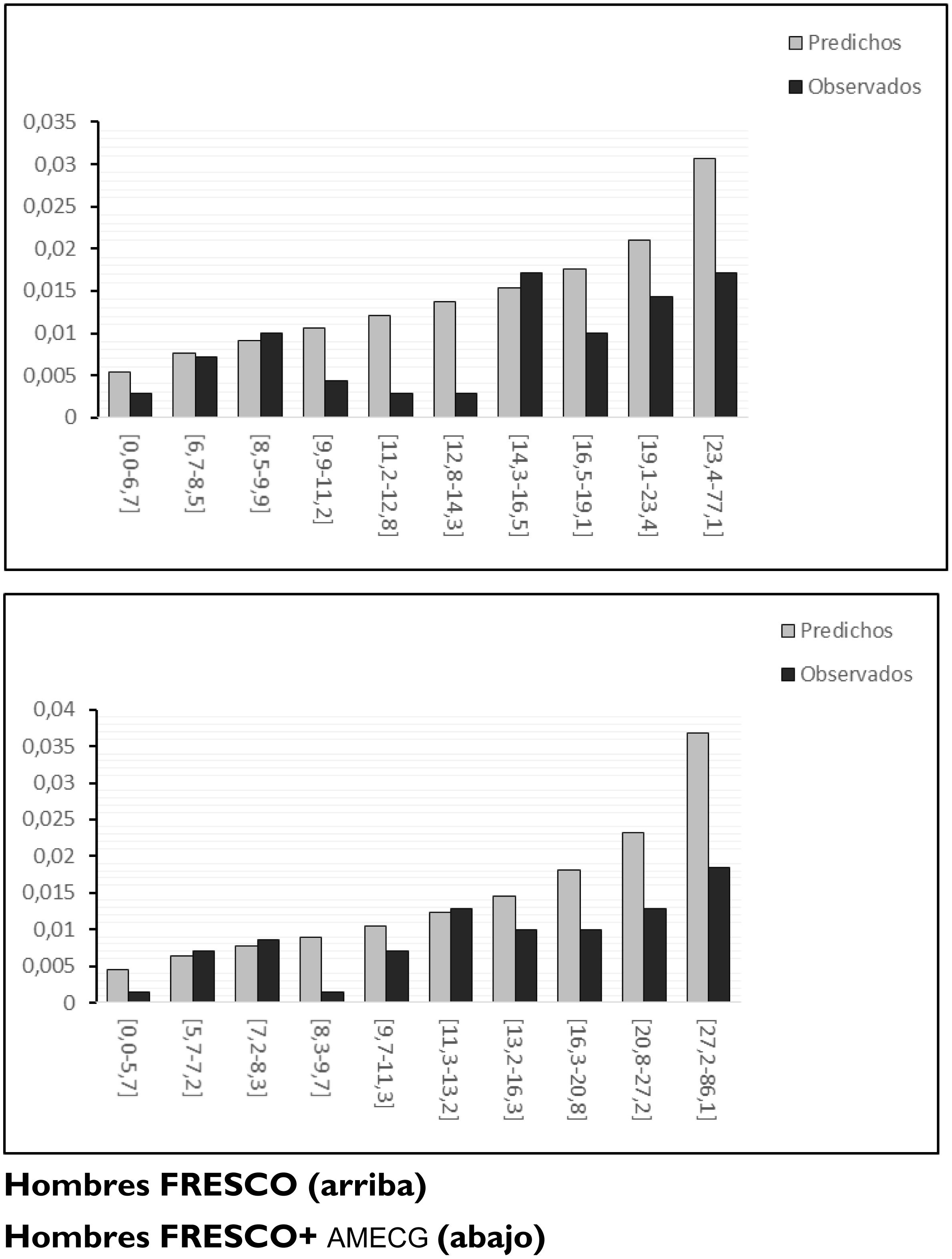
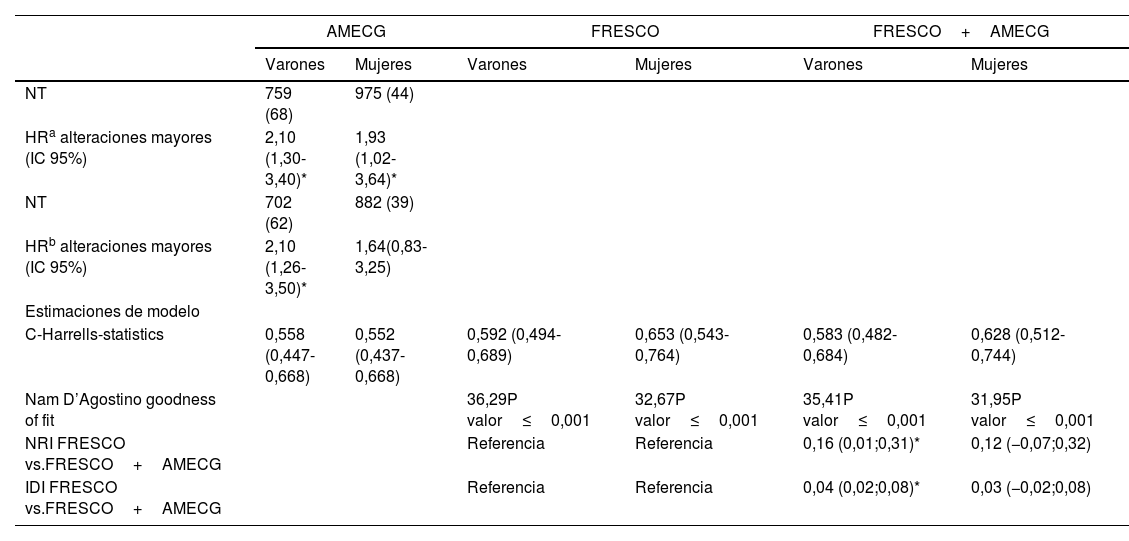
Podemos observar de manera gráfica la calibración de los modelos comparando los eventos predichos y observados para los diferentes deciles de riesgo (fig. 2). La prueba no paramétrica de Greenwood- Nam d’Agostino que evalúa la calibración de los modelos (comparación entre los eventos predichos y observados para los deciles de riesgo) fue estadísticamente significa tanto en varones como en mujeres para la función FRESCO (36,29 con p valor <0,001) y 32,67 con p valor <0,001) y para la función FRESCO y la aparición de AMECG (35,41 con p valor <0,001 y 31,95 con p valor <0,001) (tabla 3).
Incidencia de eventos cardiovasculares, asociación, poder de discriminación y reclasificación del riesgo en función de la presencia de AMECG
| AMECG | FRESCO | FRESCO+AMECG | ||||
|---|---|---|---|---|---|---|
| Varones | Mujeres | Varones | Mujeres | Varones | Mujeres | |
| NT | 759 (68) | 975 (44) | ||||
| HRa alteraciones mayores (IC 95%) | 2,10 (1,30-3,40)* | 1,93 (1,02-3,64)* | ||||
| NT | 702 (62) | 882 (39) | ||||
| HRb alteraciones mayores (IC 95%) | 2,10 (1,26-3,50)* | 1,64(0,83-3,25) | ||||
| Estimaciones de modelo | ||||||
| C-Harrells-statistics | 0,558 (0,447-0,668) | 0,552 (0,437-0,668) | 0,592 (0,494-0,689) | 0,653 (0,543-0,764) | 0,583 (0,482-0,684) | 0,628 (0,512-0,744) |
| Nam D’Agostino goodness of fit | 36,29P valor≤0,001 | 32,67P valor≤0,001 | 35,41P valor≤0,001 | 31,95P valor≤0,001 | ||
| NRI FRESCO vs.FRESCO+AMECG | Referencia | Referencia | 0,16 (0,01;0,31)* | 0,12 (−0,07;0,32) | ||
| IDI FRESCO vs.FRESCO+AMECG | Referencia | Referencia | 0,04 (0,02;0,08)* | 0,03 (−0,02;0,08) | ||
AMECG: alteraciones mayores del electrocardiograma; FRESCO: Función de Riesgo Española de Acontecimientos Cardiovasculares; HR: hazard ratio; IC 95%: intervalo de confianza del 95%; IDI: Integrated Discrimnitacion Improvement; NRI: Net Reclasification Improvement; NT: número total de eventos.
El poder de discriminación, índice C de Harrels, considerando aisladamente la presencia de AMECG fue en varones de 0,558; IC 95%: 0,447-0,668 y de 0,552; IC 95%: 0,494-0,689 en mujeres, en ambos casos el valor es bajo sin ser estadísticamente significativo. El poder de discriminación de la función FRESCO fue en nuestra muestra fue de 0,592, IC 95%: 0,494-0,689 en varones y de 0,653, IC 95%: 0,543-0,764 en mujeres; valores moderados/bajos sin alcanzar la significación estadística. No se observa una mejora en la predicción al considerar conjuntamente la función FRESCO y las AMECG: índice C de Harrels 0,583, IC 95%: 0,482-0,684 en varones y 0,628; IC 95%: 0,512-0,774 en mujeres (tabla 3).
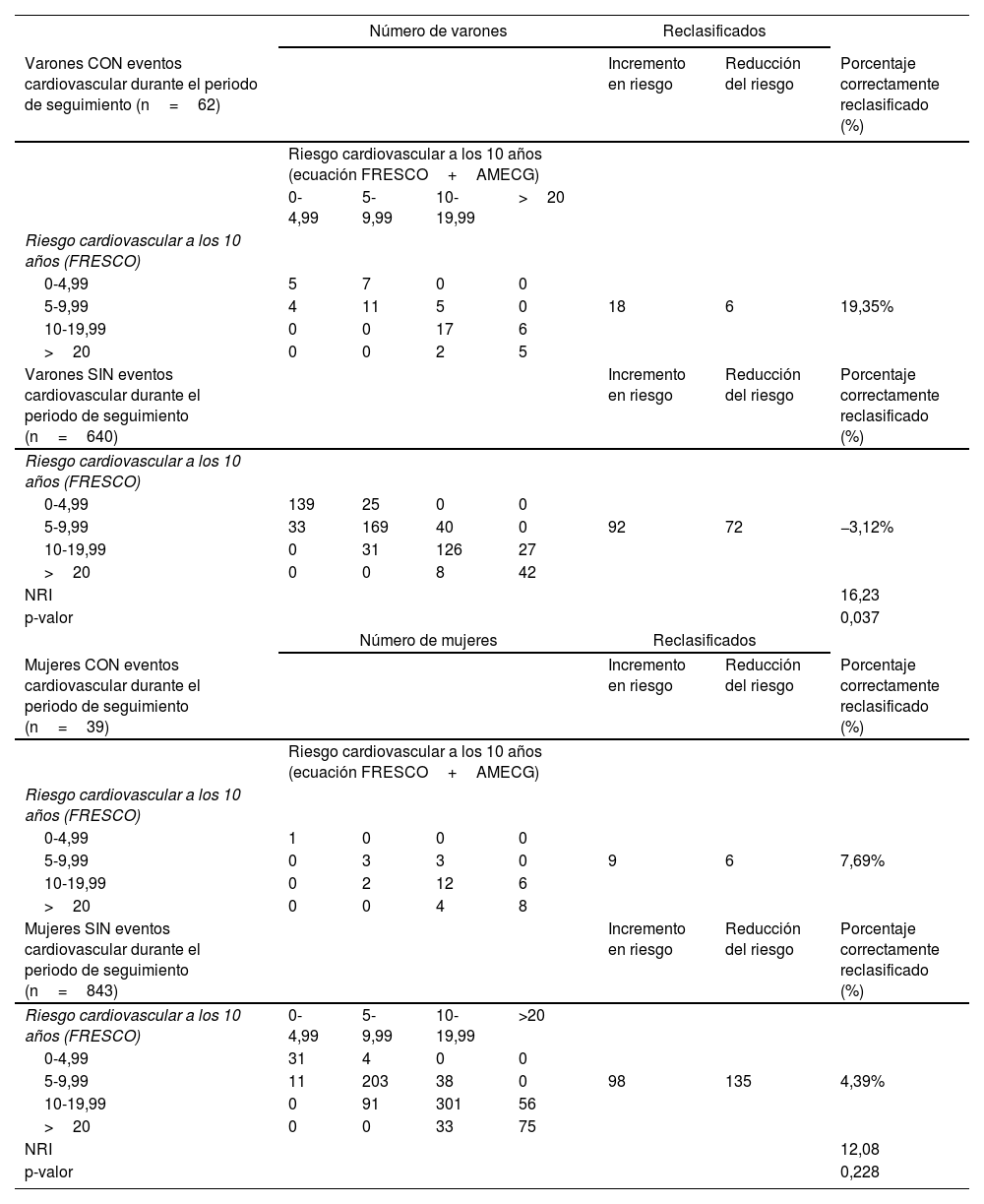
Reclasificación del riesgo y mejora del poder discriminatorioUtilizando el índice NRI, en varones observamos una mejora en la reclasificación de los sujetos que han sufrido un ECV (tabla 4), sin embargo, también se observa un incremento en el riesgo en sujetos que no lo han sufrido y la mejora neta en la reclasificación tras introducir la presencia de AMECG es de un 16,23% (IC 95%: 0,01-0,31) siendo estadísticamente significativo. En mujeres se observa una mejora en la reclasificación de un 12,84% (IC 95%: 0,07-0,32) y sin alcanzar la significación estadística. La mejora en el poder de discriminación IDI de la función FRESCO tras introducir la aparición de AMECG en varones es de IDI: 0,04; IC 95%: 0,02-0,08 y 0,03; IC 95%: −0,02-0,08 en mujeres, siendo solo estadísticamente significativo en varones.
Predicción y reclasificación de riesgo cardiovascular en varones y mujeres mediante ecuación FRESCO con y sin AMECG
| Número de varones | Reclasificados | ||||||
|---|---|---|---|---|---|---|---|
| Varones CON eventos cardiovascular durante el periodo de seguimiento (n=62) | Incremento en riesgo | Reducción del riesgo | Porcentaje correctamente reclasificado (%) | ||||
| Riesgo cardiovascular a los 10 años (ecuación FRESCO+AMECG) | |||||||
| 0-4,99 | 5-9,99 | 10-19,99 | >20 | ||||
| Riesgo cardiovascular a los 10 años (FRESCO) | |||||||
| 0-4,99 | 5 | 7 | 0 | 0 | |||
| 5-9,99 | 4 | 11 | 5 | 0 | 18 | 6 | 19,35% |
| 10-19,99 | 0 | 0 | 17 | 6 | |||
| >20 | 0 | 0 | 2 | 5 | |||
| Varones SIN eventos cardiovascular durante el periodo de seguimiento (n=640) | Incremento en riesgo | Reducción del riesgo | Porcentaje correctamente reclasificado (%) | ||||
| Riesgo cardiovascular a los 10 años (FRESCO) | |||||||
| 0-4,99 | 139 | 25 | 0 | 0 | |||
| 5-9,99 | 33 | 169 | 40 | 0 | 92 | 72 | −3,12% |
| 10-19,99 | 0 | 31 | 126 | 27 | |||
| >20 | 0 | 0 | 8 | 42 | |||
| NRI | 16,23 | ||||||
| p-valor | 0,037 | ||||||
| Número de mujeres | Reclasificados | ||||||
| Mujeres CON eventos cardiovascular durante el periodo de seguimiento (n=39) | Incremento en riesgo | Reducción del riesgo | Porcentaje correctamente reclasificado (%) | ||||
| Riesgo cardiovascular a los 10 años (ecuación FRESCO+AMECG) | |||||||
| Riesgo cardiovascular a los 10 años (FRESCO) | |||||||
| 0-4,99 | 1 | 0 | 0 | 0 | |||
| 5-9,99 | 0 | 3 | 3 | 0 | 9 | 6 | 7,69% |
| 10-19,99 | 0 | 2 | 12 | 6 | |||
| >20 | 0 | 0 | 4 | 8 | |||
| Mujeres SIN eventos cardiovascular durante el periodo de seguimiento (n=843) | Incremento en riesgo | Reducción del riesgo | Porcentaje correctamente reclasificado (%) | ||||
| Riesgo cardiovascular a los 10 años (FRESCO) | 0-4,99 | 5-9,99 | 10-19,99 | >20 | |||
| 0-4,99 | 31 | 4 | 0 | 0 | |||
| 5-9,99 | 11 | 203 | 38 | 0 | 98 | 135 | 4,39% |
| 10-19,99 | 0 | 91 | 301 | 56 | |||
| >20 | 0 | 0 | 33 | 75 | |||
| NRI | 12,08 | ||||||
| p-valor | 0,228 | ||||||
AMECG: alteraciones mayores del electrocardiograma; FRESCO: Función de Riesgo Española de Acontecimientos Cardiovasculares; NRI: Net Reclasification Improvement.
Las AMECG se asociaron con un mayor riesgo de eventos de ECV tanto en varones como en mujeres. Sin embargo, no se evidencia una mejora significativa en la capacidad predictiva de la ecuación FRESCO tras la inclusión de las AMECG como factor predictor.
Existen diferencias en la frecuencia de aparición de las AMECG entre varones y mujeres. La prevalencia de AMECG fue mayor en los varones, con un 27,9%, en comparación con el 20,9% en mujeres. La mayoría de los estudios observan una mayor prevalencia de AMECG en varones19,25, aunque algunos evidencian una mayor prevalencia en mujeres26,27. En nuestro estudio, la prevalencia de AMECG total fue de un 24%. Esta prevalencia es superior a la reportado en otros estudios15–18. Estas diferencias podrían ser explicadas por la variabilidad en las poblaciones de estudio, nuestra población de estudio es de mayor edad y mayor RCV, que otros estudios.
Nuestros resultados demuestran que, en una población de riesgo moderado y alto sin enfermedad cardiovascular preexistente, las anomalías mayores en el ECG se asocian con un mayor riesgo de ECV. De manera similar, las AMECG se han asociado a una mayor incidencia de infarto de miocardio y accidente cerebrovascular2, así como a una mayor mortalidad por enfermedad cardiovascular26. Sin embargo, no todos los estudios encuentran resultados concluyentes; por ejemplo, Terho et al.27 observaron que las AMECG se relacionaban con una mayor mortalidad cardíaca, pero no con un aumento en la ECV.
Un aspecto muy importante es el efecto diferencial de estas anomalías en la aparición de ECV entre varones y mujeres. Liao et al., en el «Chicago Heart Association Detection Project», identificaron una mayor prevalencia de anomalías menores en el ECG en mujeres, pero una mayor asociación de estas anomalías con ECV en varones25. Nuestro estudio también revela un comportamiento diferencial entre varones y mujeres: en mujeres, las alteraciones más fuertemente asociadas a la aparición de ECV son la presencia de descenso ST y la fibrilación auricular en las mujeres, mientras que en varones son la HVE con inversión de onda T y el alargamiento del intervalo QT. Estos resultados destacan la necesidad de un enfoque personalizado en la evaluación y manejo del riesgo cardiovascular.
Estos resultados reafirmaron nuestra intención de presentar los resultados de la predicción de la ecuación FRESCO y las AMECG, separadas por sexo. Observamos una mejora modesta en la predicción de ECV y en la reclasificación de riesgo en varones. Sin embargo, en mujeres, las AMECG no añaden valor predictivo en la predicción del riesgo cardiovascular. Estos hallazgos son similares a los reportados por Auer et al.28, quienes encontraron que las AMECG estaban asociadas con un mayor riesgo de ECV y a una mejora modesta en la predicción de ECV. En este estudio la inclusión de las anomalías en el ECG reclasificó al 13,6% de los participantes, un valor similar al de nuestro estudio, pero solo en varones. En nuestra opinión, estos resultados respaldan la afirmación de Pencina et al.29 de que los índices NRI e IDI son más sensibles a pequeñas variaciones en la discriminación que otros indicadores tradicionales de valoración de la predicción.
Estos resultados negativos observados en la predicción de riesgo en mujeres, se hacen patentes al comparar el número de ECV predichos y los observados, tanto utilizando la función FRESCO como considerando también la presencia de AMECG. Esto sugiere una sobreestimación del RCV en mujeres y que no mejorar al incorporar las AMECG. En términos generales, a pesar de la identificación de nuevos predictores o biomarcadores, la integración de estos nuevos factores de RCV es limitada, principalmente debido a que no aportan mejoras sustanciales en la predicción en comparación con los predictores clásicos30.
El estudio presenta algunas limitaciones, ya que se llevó a cabo únicamente en individuos de tres nodos del estudio PREDIMED y en personas con RCV moderado y alto. Aunque el estudio PREDIMED recogía datos de ECG de todos los pacientes de manera basal, solo tres nodos tenían los ECG accesibles y disponibles para ser leídos. Además, en el estudio PREDIMED solo se incluyeron participantes con RCV moderado y alto. La elección de esta población se hizo para asegurar una cantidad adecuada de eventos y garantizar un poder estadístico suficiente para detectar efectos en los predictores estudiados.
No obstante, no se debe descartar la relevancia de detectar alteraciones electrocardiográficas mayores en la predicción del RCV en poblaciones de bajo riesgo. Un estudio reciente ha mostrado que las personas de bajo riesgo con tales alteraciones tienen el doble de probabilidad de experimentar muerte cardiovascular. Entre las principales alteraciones predictivas se incluyen dilatación de la aurícula izquierda, la fibrilación auricular, la HVE, anomalías importantes en la onda Q y anomalías mayores en el segmento ST31.
Por otra parte, el tamaño de la muestra ha podido limitar el poder estadístico para observar diferencias en los análisis por subgrupos, especialmente en mujeres donde la incidencia de ECV era menor, pero también en los análisis de AMECG de forma individualizada, sobre todo en las menos frecuentes. Estudios con mayor muestra y de mayor duración podrían aportar tal vez resultados más concluyentes. Las fortalezas del estudio son: su diseño longitudinal, calidad en la recogida de datos, especialmente ECG y ECV, y ser un estudio pionero en la utilización de índices de mejora en la predicción de las AMECG en ecuaciones de riesgo CV.
El ECG es una técnica segura, accesible y de bajo coste. Sin embargo, las recomendaciones de la US Preventive Services Task Force desaconsejan la utilización del screening con ECG en reposo o esfuerzo de manera asilada para la prevención del RCV en personas con riesgo bajo32,33, principalmente, por no haber demostrado un claro balance entre el beneficio y el riesgo de realización de pruebas más invasivas. En nuestro estudio con población de riesgo intermedio o alto hemos podido observar una mayor incidencia de ECV en los participantes con AMECG. Sin embargo, y debido a la escasa mejora que aporta a las ecuaciones que incorporan los factores de riesgo clásicos, no podemos recomendar la utilización del ECG como apoyo en el cálculo del riesgo cardiovascular. No obstante, dada la asociación que hemos podido observar de algunas AEMCG y la aparición posterior de ECV, deberíamos prestar especial atención a la presencia de descenso ST y fibrilación auricular en las mujeres y en varones la HVE con inversión de onda T (patrón de sobrecarga) y el alargamiento del intervalo QT por su mayor probabilidad de desarrollar eventos.
ConclusionesLa presentación de AMECG se asocia en población mediterránea de medio y alto riesgo con la presentación posterior de ECV, en varones y mujeres. Observamos un comportamiento diferente entre por sexos en cuanto a las alteraciones que individualmente contribuyen a esta asociación, en varones los criterios electrocardiográficos de HVE con inversión de onda T y alargamiento del QT y en mujeres el descenso del ST, bloqueo de rama izquierda y fibrilación auricular se asocian en mayor medida con los ECV. A pesar de que los resultados de este estudio no permiten recomendar el uso del ECG añadido a las funciones de cálculo de RCV (FRESCO), el aumento de riesgo que implican aconseja el estudio individualizado de las alteraciones mayores en él decurso del proceso clínico.
FinanciaciónInstituto de Salud Carlos III. El ensayo PREDIMED contó con el apoyo del Instituto de Salud Carlos III (ISCIII), la agencia oficial de financiamiento para la investigación biomédica del gobierno español, a través de subvenciones otorgadas a redes de investigación específicamente desarrolladas para el ensayo (RTIC G03/140, a Ramón Estruch durante 2003-2005; RTIC RD 06/0045, a Miguel A. Martínez-González durante 2006-2013 y a través del Centro de Investigación Biomédica en Red de Fisiopatología de la Obesidad y Nutrición [CIBEROBN]), y mediante subvenciones del Centro Nacional de Investigaciones Cardiovasculares (CNIC 06/2007), Fondo de Investigación Sanitaria-Fondo Europeo de Desarrollo Regional (PI04-2239, PI 05/2584, CP06/00100, PI07/0240, PI07/1138, PI07/0954, PI 07/0473, PI10/01407, PI10/02658, PI11/01647, P11/02505, PI13/00462 y JR17/00022) financiadas por el Ministerio de Economía y Competitividad, Instituto Carlos III y también contó con el apoyo de fondos proporcionados por la Red de Atención Primaria y promoción de la Salud (RICAPPS) RD21/0016/0009, cofinanciado con fondos de Next Generation EU, que financian las actuaciones del Mecanismo de Recuperación y Resiliencia (MRR), Ministerio de Ciencia e Innovación (AGL-2009-13906-C02, AGL2010-22319-C03, AGL2011-23430 y SAF2016–80532-R), Fundación Mapfre 2010 (sin participación en el diseño, implementación, análisis o interpretación de los datos), Consejería de Salud de la Junta de Andalucía (PI0105/2007), División de Salud Pública del Departamento de Salud de la Generalitat de Cataluña, Generalitat Valenciana (PROMETEO 17/2017 y PROMETEO 21/2021), Fundació La Marató-TV3 (subvenciones 294/C/2015 y 538/U/2016, sin participación en el diseño, implementación, análisis o interpretación de los datos)), Agencia Canaria de Investigación, Innovación y Sociedad de la Información-EU FEDER (PI 2007/050 y CS2011-AP-042), y Gobierno Regional de Navarra (P27/2011). El estudio metabolómico recibió el respaldo de la subvención de investigación NIDDK-R01DK 102896. Las donaciones de aceite de oliva, nueces, almendras y avellanas fueron realizadas, respectivamente, por la Fundación Patrimonio Comunal Olivarero y Hojiblanca (Málaga, España), California Walnut Commission (Sacramento, California), Borges (Reus, España) y Morella Nuts (Reus, España). El Prof. Jordi Salas-Salvadó cuenta con el apoyo parcial de ICREA, en el marco del programa ICREA Academia.
Consideraciones éticasLos autores declaran ha seguido fielmente los principios de la Declaración de Helsinki, las directrices ICH de Buena Práctica Clínica (ICH/GCP) y en plena conformidad con las autoridades legales pertinentes. El protocolo y todos los documentos requeridos han sido sometidos a evaluación por parte del Comité Ético y de Investigación (CEI). Todas las modificaciones sustanciales de los documentos originales han sido enviadas para su evaluación y conformidad al CEI y a las entidades competentes. Se ha recogido consentimiento informado escrito y verbal de todos los pacientes tras ser informados (según la Ley Orgánica de Protección de Datos de Carácter Personal).
La Comisión de Ética de Investigación de la Clínica Universitaria de la Facultad de Medicina de la Universidad de Navarra (código 50/2005), el Comité Ético de Investigación Clínica de las Islas Baleares (código 491/05), y el Comité Ético de Investigación Clínica del Hospital Universitario Sant Joan de Reus (código 0306196proj3) han participado en la evaluación ética de este estudio.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses