La inmunodeficiencia variable común (IDVC) es una enfermedad heterogénea caracterizada por una disminución de los valores absolutos de los linfocitos B de memoria en la sangre periférica. A pesar de que esta disminución se ha atribuido previamente a un posible defecto en el desarrollo del centro germinal, las causas permanecen en gran medida desconocidas. Por otro lado, la apoptosis aumentada de los linfocitos B ha sido implicada en la patogénesis de diversas enfermedades. Hasta ahora, sin embargo, no se ha descrito un balance negativo entre apoptosis/supervivencia de los linfocitos B de memoria en los pacientes con IDVC y por ello nos preguntamos si una apoptosis aumentada podría ser relevante en la IDVC. En este estudio determinamos la apoptosis espontánea e inducida de los linfocitos B de memoria de pacientes con IDVC y controles sanos mediante citometría de flujo. La apoptosis se cuantificó mediante la expresión de la anexina v tras un cultivo de 24h en presencia o ausencia de un anticuerpo monoclonal proapoptótico anti-CD95. Además, desarrollamos un método nuevo y sensible que utiliza 7-amino-actinomicina D (7-AAD) para detectar linfocitos B apoptóticos en sangre completa. Nuestros resultados indican claramente una disminución del valor absoluto de linfocitos B de memoria y una apoptosis incrementada en los pacientes con IDVC con respecto a los controles sanos (p<0,01). Además, demostramos que el aumento de la apoptosis de esta población celular no está mediado por la molécula CD95.
Common Variable Immunodeficiency (CVID) is a heterogeneous disease characterised by low memory B cell counts in peripheral blood (PB). Although previous reports have attributed memory CD27+ B cell decrease to a possible defective germinal centre development, the cause of this defect remains basically unknown. On the other hand, increased apoptosis has been implicated in the pathogenesis of several diseases, and could be another factor that contributes to explain memory B cell reduction. However, a negative balance between apoptosis/survival of memory B cells in CVID patients has still not been documented. Therefore, we asked whether increased apoptosis was relevant in CVID. To test this concept, total and memory B cells from CVID patients and healthy controls were studied by flow cytometry to determine spontaneous and induced apoptosis. Apoptosis was measured by Annexin-V expression after a 24 hour culture with and without anti-CD95 proapoptotic monoclonal antibody. We also developed a new and sensitive method that uses 7-amino-actinomycin D (7-AAD) to measure very low numbers of apoptotic cells in whole PB. Our results clearly indicate diminished absolute counts and higher apoptosis in memory B cells from CVID patients than in healthy controls (P<.01). Moreover, we also demonstrate that CD95 is not implicated in regulating memory B cell apoptosis.
La inmunodeficiencia variable común (IDVC) es una enfermedad que se caracteriza por hipogammaglobulinemia y alteraciones en la respuesta inmune humoral1,2 que conducen a una respuesta defectuosa ante un estímulo antigénico, incluida la respuesta a vacunaciones3. Se han descrito diversas formas de clasificación de la enfermedad. Inicialmente, la mayoría de los estudios clasificaron a los pacientes con IDCV atendiendo a la capacidad mostrada por los linfocitos B para la producción in vitro de inmunoglubulinas4. Posteriormente, la clasificación se basó en el número de linfocitos B de memoria (CD27+)5,6, una población esencial en la generación y el mantenimiento de una respuesta inmune humoral adecuada7. Según esta clasificación, los pacientes con IDVC se dividen en distintos grupos atendiendo al número absoluto de células B de memoria detectados en la sangre periférica (SP).
Como ya se ha citado, en la gran mayoría de los pacientes con IDVC el número de células B de memoria se encuentra disminuido con respecto al encontrado en los individuos sanos. Los mecanismos que conducen a la depleción de esta subpoblación de células B no son conocidos hasta el momento. Fas (CD95), una molécula asociada con claridad a la apoptosis en células T8,9 y en mucha menor medida a la muerte celular programada de los linfocitos B, ha demostrado tener un papel en la viabilidad de algunas subpoblaciones B en diferentes enfermedades, tal y como se ha descrito en pacientes HIV10 o en pacientes con enfermedades autoinmunes11.
En este trabajo demostramos que el número reducido de células B circulantes de memoria en pacientes con IDVC se debe, al menos en parte, a una apoptosis aumentada de células B CD27+ con respecto a los controles sanos. Este aumento se verificó tanto en cultivos de 24h, mediante la técnica de la anexina, como en la SP recién extraída y sin ningún tipo de manipulación, determinada según un método ideado en nuestro laboratorio. Este aumento de células apoptóticas no fue dependiente de CD95.
Material y métodosPacientesSe estudiaron 15 pacientes con IDCV, 12 de ellos en tratamiento sustitutivo con inmunoglobulina intravenosa (IGIV). El rango de edad de los pacientes se encontraba entre 28 y 77 años (edad media de 49±15 años; media±ESM). De los 15 pacientes, 3 estaban siendo tratados en el momento en que se realizó el estudio: una paciente con artritis reumatoide en tratamiento con glucocorticoides, una paciente infectada con VIH (estadio B3) en tratamiento antirretroviral y un paciente con trasplante de hígado en tratamiento con ciclosporina. Cuatro de los pacientes con antecedentes de enfermedad linfoproliferativa se encontraban en remisión completa y sin tratamiento en el momento del estudio (enfermedad de Hodking, LNH B, LNH MALT y linfoma de la zona marginal). Los 8 pacientes restantes se encontraban sin ningún tratamiento adicional a la IGIV.
Participaron 7 voluntarios como controles sanos con edades comprendidas entre los 28 y los 50 años.
Obtención de las muestrasTras el consentimiento informado aprobado por el Comité Ético de Investigación del Hospital Universitario Ramón y Cajal se realizó una extracción de sangre en tubos heparinizados de 10ml. En todos los casos la extracción se realizó previamente a la infusión de IGIV.
Estudio de subpoblaciones linfocitarias por citometría de flujoEl estudio inmunofenotípico de las subpoblaciones linfocitarias se realizó en la SP completa. Para ello, la SP total (50μl) se incubó con diferentes anticuerpos monoclonales (AcMo) conjugados a diferentes fluorocromos durante 20min a temperatura ambiente y en oscuridad. Pasado este tiempo las muestra fueron lisadas con el reactivo FACS lysing solution 1X (BD Biosciences, San José, CA) durante un periodo de 10min. Tras 2 lavados con suero salino las células fueron analizadas en un citómetro de flujo FACScan (o FACSCanto II) (BD Biosciences, San José, CA). Se utilizaron los siguientes AcMo: anti-CD45-FITC, anti-CD19-PE (Beckman-Coulter, Hialeah, FL), anti-CD95-PE, anti-CD27-PE, anti-CD27-FITC, anti-CD45-PerCP y anti-CD19-PE-Cy5 (BD Biosciences, San José, CA). El número absoluto de células/μL de cada una de las poblaciones celulares estudiadas (células B totales y células B de memoria CD27+) se obtuvo aplicando el porcentaje obtenido de cada población en el análisis por citometría de flujo al número absoluto de linfocitos/μL obtenido en un hemograma realizado ese mismo día para cada uno de los pacientes y controles sanos.
Cultivos celulares y determinación de apoptosis espontánea e inducidaLas células se cultivaron inicialmente a una concentración de 5x105 en 100(L de medio completo (RPMI suplementado con 10% de suero de ternera fetal, glutamina y gentamicina) y en tubos de fondo cónico durante 2h en presencia o en ausencia del AcMo proapoptótico anti-CD95 (clon CH11) (Beckman-Coulter, Hialeah, FL) a una concentración de 200ng/mL (concentración previamente ensayada y que se mostró óptima en la inducción de la apoptosis de la línea celular Jurkat con respecto a un tubo de control de esta misma línea celular en ausencia de anti-CD95). Pasado este tiempo las células fueron depositadas en placas de 12 pocillos tras la adición de 900μL de medio completo. Sin lavar, las células fueron incubadas otras 22h a 37°C. Las células fueron lavadas y más tarde incubadas con diferentes combinaciones de AcMo con el fin de explorar el porcentaje de apoptosis espontánea e inducida en las diferentes poblaciones linfocitarias. La incubación con estos AcMo se realizó durante 20min a 4°C. Tras 2 lavados en suero salino las células fueron resuspendidas en un tampón de unión (Annexin V binding buffer) conteniendo Ca2+ (140mM NaCl, 2,5mM CaCl2, 10mM HEPES) por ser este catión indispensable para la unión de la anexina al fosfatidilinositol traslocado a la cara externa de la membrana citoplásmica. Posteriormente, se añadió anexina V-FITC (Caltag, Sweden, SE) durante 15min a temperatura ambiente. Como control negativo de este marcaje se utilizó PBS en vez del tampón de unión, pues la ausencia de Ca2+ en el PBS impide la unión de la anexina a la membrana. Se realizó entonces la adquisición y el análisis de las muestras por citometría de flujo y se determinó la apoptosis espontánea e inducida de cada subpoblación. Se consideraron células apoptóticas aquellas que expresaron anexina en la membrana con intensidad intermedia-alta a alta.
Detección por citometría de flujo y en sangre completa de células apoptóticas determinadas como células 7-amino-actinomicina D+Se incubaron 50μL de sangre completa durante 20min con las siguientes combinaciones de AcMo: CD45-FITC/CD19-PE o CD19-FITC/CD27-PE. Pasado este tiempo las células se incubaron con 2ml (dilución 1/10) de la solución lisante de hematíes Pharma-Lyse® (BD Biosciences, San José, CA), una solución que contiene NH4Cl pero que carece de cualquier agente fijador/permeabilizador (al contrario que la mayoría de soluciones lisantes que habitualmente se utilizan para lisar los glóbulos rojos). Este tipo de lisis mantiene la viabilidad de las células nucleadas. Tras la realización de un lavado las células se resuspendieron en 400μL de solución salina. Se añadieron entonces 50μL (20μg) del colorante vital fluorescente 7-amino-actinomicina D (7-AAD) (BD Biosciences, San José, CA) y se incubó durante 20min a 4°C y en oscuridad. Sin lavar, las células se adquirieron y analizaron por citometría de flujo. Se consideraron como células no viables aquellas que habían intercalado la 7-AAD en su ADN (células 7-AAD+).
Análisis estadísticoLas comparaciones estadísticas de los datos numéricos se realizaron utilizando la prueba no paramétrica U de Mann-Whitney, considerándose como diferencia significativa entre 2 grupos si la p<0,05.
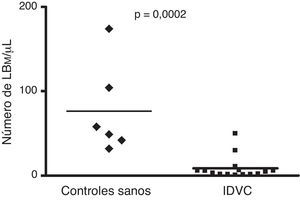
ResultadosNúmero absoluto de linfocitos B de memoria en pacientes con inmunodeficiencia variable común y en controles sanosTal y como muestra la figura 1 el número absoluto de linfocitos B en nuestro grupo de pacientes con IDVC (94±27 células/μL; n=15) (media±ESM) fue significativamente distinto al registrado en los controles sanos (225±54 células/μL) (p=0,02). A su vez, el número absoluto de células B de memoria también fue claramente inferior en los pacientes con respecto a los controles sanos. Como puede observarse en la figura 2, en pacientes con IDVC el número absoluto de linfocitos B de memoria fue de 8,7±3,4/μL (n=15), mientras que en los controles sanos ese número alcanzó la cifra de 76,5±22/μL (n=6) (p<0,0002).
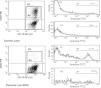
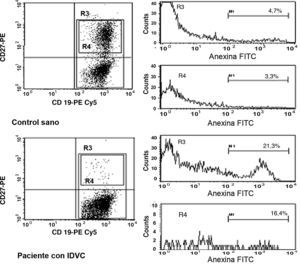
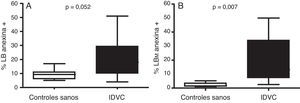
A continuación, pasamos a explorar la posibilidad de que el descenso en el número de linfocitos B de memoria en la IDVC pudiera estar relacionado con una mayor susceptibilidad a la apoptosis en estas células. En la figura 3 se muestra un ejemplo representativo en el que se observa cómo tanto las células B totales como las células B de memoria de los pacientes con IDCV experimentan apoptosis en un grado mayor que el experimentado por estas mismas células en un control sano. Esta diferencia se observó en todos los pacientes estudiados con IDVC, en los que tanto la apoptosis espontánea de las células B totales CD19+ (20,6±3,3% de células anexina+) como de las células B de memoria CD19+CD27+ (9,8±2,2%) estuvo significativamente aumentada con respecto a las células B totales (9,4±1,5%) o de memoria (1,1±0,5%) de individuos sanos (p=0,052 y p=0,007, respectivamente) (fig. 4).
Ejemplo representativo de la apoptosis espontánea observada en las células B totales y en las células B de memoria CD27+ en un control sano (histogramas superiores) y en un paciente con IDVC (histogramas inferiores). Tras la adquisición en el citómetro de flujo el análisis se realizó sobre las células CD19+. Se crearon entonces 2 ventanas de análisis: la ventana R3 que engloba a la totalidad del porcentaje de los linfocitos B (CD27- y CD27+) y la ventana R4 que engloba al porcentaje con respecto a solo los linfocitos B de memoria CD27+. El marcador M1 (canal a partir del cual se consideró a una célula como anexina+) se estableció con las células que fueron incubadas con anexina-FITC en PBS.
Diferente susceptibilidad a la apoptosis espontánea en los linfocitos B totales (A) o en los linfocitos B de memoria (LBM) CD27+ (B) en sujetos sanos y en pacientes con IDCV. Las células B totales y de memoria se detectaron con la combinación de los AcMo anti-CD19-PE-Cy5 y anti-CD27-PE. Los box-plots muestran el porcentaje de células apoptóticas en la fracción B total o en la fracción B de memoria determinadas como células anexina v+ con intensidad intermedia a intermedia-alta en el citómetro de flujo. El valor de la comparación estadística entre ambos grupos se consideró significativa si p<0,05.
A continuación, quisimos investigar la posible contribución de la molécula CD95 a este proceso. Con este fin, la apoptosis de células mononucleares se determinó en cultivos de 24h sin la adición de ningún estímulo exógeno (apoptosis espontánea) o incubadas con el AcMo anti-CD95 inductor de apoptosis (clon CH11) (apoptosis inducida). Las células apoptóticas fueron determinadas como células anexina+. En la práctica totalidad de los pacientes con IDVC, salvo alguna excepción, tanto las células B totales como las células B de memoria no respondieron al efecto inductor de apoptosis del AcMo anti-CD95. Tal y como se muestra en la tabla 1, en ninguno de los 15 casos de IDVC ni tampoco en los controles sanos el porcentaje de células B totales anexina+ en el ensayo de apoptosis espontánea difirió significativamente con respecto al ensayo de apoptosis inducida por CH11 (p>0,1). En las células B de memoria, 11 de 13 pacientes no respondieron al efecto inductor del anticuerpo anti-CD95 (p>0,1). En 2 pacientes no pudo determinarse la apoptosis espontánea y/o inducida de las células B de memoria CD27+ por el extremadamente bajo número de las mismas tras 24h de cultivo.
Comparación de la apoptosis espontánea e inducida con anticuerpos anti-CD95 (clon CH11) en controles sanos y en pacientes con IDVC
| A | %Linfocitos B totales anexina+ | |||
| Controles sanos | Pacientes IDVC | |||
| Espontánea | Inducida | Espontánea | Inducida | |
| 1 | 5 | 5 | 10 | 10 |
| 2 | 8 | 7 | 25 | 30 |
| 3 | 17 | 16 | 7,4 | 4,7 |
| 4 | 11,2 | 12 | 4 | 2 |
| 5 | 9 | 9,5 | 23 | 18,3 |
| 6 | 7 | 8 | 29 | 28,4 |
| 7 | 6 | 6 | 16 | 12 |
| 8 | 14 | 14 | ||
| 9 | 26 | 29 | ||
| 10 | 30 | 26 | ||
| 11 | 29 | 29 | ||
| 12 | 18 | 18 | ||
| 13 | 4 | 2 | ||
| 14 | 33 | 34 | ||
| 15 | 14,5 | 13,7 | ||
| B | %Linfocitos B memoria anexina+ | |||
| Controles sanos | Pacientes IDVC | |||
| Espontánea | Inducida | Espontánea | Inducida | |
| 1 | 3 | 2,5 | 4 | 7,3 |
| 2 | 2,5 | 2 | 25 | 28 |
| 3 | 0,8 | 1,2 | 7,2 | 7,1 |
| 4 | 1,5 | 1,8 | 17 | 15,7 |
| 5 | 2 | 1,3 | 6,6 | 6,8 |
| 7 | 2 | 2 | 6,2 | 5,3 |
| 8 | 17 | 19 | ||
| 9 | 19 | 23,6 | ||
| 10 | 4,2 | 3,4 | ||
| 11 | 1,2 | 0.9 | ||
| 12 | 3,2 | 22 | ||
| 13 | 15,5 | 18 | ||
Las células mononucleares se incubaron 24h en ausencia (apoptosis espontánea) o en presencia (apoptosis inducida) del AcMo anti-CD95 inductor de apoptosis. El porcentaje de células apoptóticas en la población de linfocitos B totales (A) y en la población de linfocitos B de memoria CD27+ (B) se determinó por citometría de flujo como células anexina+ con intensidad intermedia a intermedia-alta. En el análisis se utilizaron las mismas ventanas referidas en la figura 3.
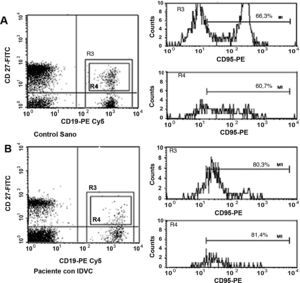
Estos hallazgos se vieron corroborados con los estudios de expresión en la membrana del antígeno CD95. En este sentido, y tal y como se muestra en un ejemplo representativo en la figura 5, aunque el porcentaje de células B totales o de memoria que expresó la molécula CD95 fue habitualmente mayor en los pacientes con IDVC que en los controles sanos, estas diferencias no fueron estadísticamente significativas (datos no mostrados).
Expresión de CD95 en linfocitos B totales y de memoria de un control sano y de un paciente con IDVC. Las células fueron incubadas con los AcMo anti-CD27-FITC, anti-CD95-PE y anti-CD19-PE-Cy5. Las poblaciones CD19+ (linfocitos B totales) (A) y CD19+CD27+ (linfocitos B de memoria) (B) fueron seleccionadas con las ventanas de análisis R3 y R4, respectivamente, y se determinó en cada una de ellas la expresión del antígeno CD95 en un histograma uniparamétrico.
La determinación de células apoptóticas en cultivos requiere de la separación previa de las células con un gradiente de densidad y varias horas de incubación, un método que conduce a un rendimiento limitado en la obtención de células. De hecho, tal y como hemos referido en el punto anterior de resultados, en 2 de los 15 pacientes con IDVC no pudimos determinar la apoptosis espontánea e inducida debido al muy escaso número de células B de memoria tras el cultivo de 24h. Con el fin de evitar al máximo la manipulación de la muestra para, por un lado, mantener casi intactas las condiciones fisiológicas en que circulan las células B y, por el otro, para aumentar la sensibilidad en la detección de la apoptosis, desarrollamos un nuevo método capaz de detectar la célula apoptótica ex vivo, método que se describe de forma pormenorizada en la sección de Materiales y métodos.
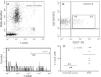
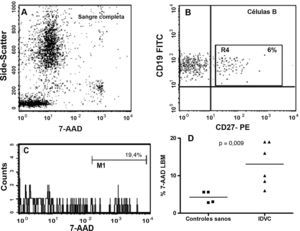
La figura 6A indica cómo el porcentaje de células B de memoria no viables de los pacientes con IDVC era manifiestamente mayor que el detectado en sujetos sanos (células 7-AAD+: 13,1±2,3% versus 4,3±1,3%, respectivamente; p=0,03). A su vez, se incluyen las imágenes de citometría de flujo de un ejemplo representativo (fig. 6B y C) con el objeto de mostrar la fuerte señal fluorescente emitida por las células no viables al incorporar la 7-AAD.
Detección de células apoptóticas en sangre completa. (A) Ejemplo representativo de una sangre lisada e incubaba con distintos AcMo y con 7-AAD en el que se muestran todas las poblaciones leucocitarias en un dot-plot de SSC/7-AAD. Se consideró señal positiva para 7-AAD la de aquellas células con una señal cercana al canal 103 de fluorescencia. (B y C) Se muestra un ejemplo representativo de un paciente con IDCV en el que tan solo un 6% de sus linfocitos B mostraron un fenotipo compatible con la célula B de memoria (ventana R4). El 19,4% de estas células B CD27+ se contabilizaron como células apoptóticas al emitir una fuerte señal para 7-AAD. (D) Representación gráfica del porcentaje de células B de memoria 7-AAD+ de todos los casos estudiados: controles sanos (n=4) y pacientes con IDVC (n=6).
Una de las alteraciones celulares características de la IDVC es la disminución del número absoluto de células B de memoria12. Por el contrario, aun cuando la disminución del porcentaje y el número absoluto de linfocitos B totales (naive + memoria) suele ser un hallazgo común en esta enfermedad, tal número puede ser muy heterogéneo, hasta el punto de ser equiparable, en un número limitado de pacientes, al de los controles sanos12. Nuestro trabajo, realizado con 15 pacientes diagnosticados de IDCV, ha corroborado el descenso muy significativo del número absoluto de células B de memoria. Además, en cultivos de corta duración (24h) nuestros hallazgos demuestran que las células B de memoria de los pacientes con IDCV experimentan espontáneamente apoptosis en un porcentaje significativamente mayor que el observado en sujetos sanos. Aun cuando el escaso porcentaje de células B de memoria en estos enfermos dificulta en ocasiones una adquisición en el citómetro de flujo que resulte estadísticamente representativa, el marcaje con anexina, capaz de detectar células apoptóticas ya en las fases más tempranas de este proceso13,14, demostró ser un método sensible en la mayoría de los casos estudiados. A nuestro juicio, esta es la primera vez que se demuestra que un incremento en la apoptosis de las células B de memoria en la IDCV pueda explicar su descenso numérico in vivo. En lo que respecta a la molécula que media en este proceso amplificado de apoptosis nuestros experimentos de apoptosis inducida mostraron que la contribución de la molécula CD95 no es relevante en la mayoría de los casos. Un resultado que, a su vez, era compatible con el hecho de que tanto el porcentaje como, en especial, la IMF de CD95 en las células B de memoria en IDCV fuera similar al registrado en las células B de memoria de la población sana. Por otro lado, se encontraron hallazgos similares al analizar la población B total en pacientes y controles: una mayor susceptibilidad al proceso apoptótico en los pacientes con IDCV, si bien con una significación inferior a la registrada al comparar exclusivamente la población B de memoria. Esta significación no tan evidente quizá pueda estar asociada a la demostrada heterogeneidad en el número de las células B con que cuenta cada paciente, tal y como se ha citado previamente. Estos hallazgos distancian a la fisiopatología de la respuesta humoral en la IDCV de la descrita en pacientes HIV10 en la que se ha demostrado un evidente aumento cuantitativo en la expresión del antígeno CD95 en las células B de memoria con capacidad para mediar la señal proapoptótica vehiculada por el ligando fisiológico de este receptor de membrana (CD95 ligando/CD178)15. En este momento estamos explorando la contribución de otras moléculas a este fenómeno, en especial TRAIL y sus receptores, pues tales moléculas han demostrado tener un papel importante en la fisiopatología de la supervivencia de los linfocitos B16,17.
Parece evidente que uno de los motivos que explican la ausencia de trabajo experimental, razonando el claro descenso de linfocitos B de memoria en estos pacientes, sea precisamente su muy escaso número, hasta el punto de que estudios funcionales que requieren contar con un número mínimo de células (estudios de apoptosis espontánea o inducida, estudios de proliferación, etc.) no pueden realizarse en estos enfermos. Además, estos cultivos raramente requieren de la obtención de las células tras un gradiente de densidad que no solo implica pérdida celular en cada uno de los pasos del proceso (el propio gradiente, los lavados), sino que puede, precisamente, eliminar una parte de las células apoptóticas contenidas en la muestra fresca, pues, como se sabe, las células linfoides apoptóticas poseen una densidad superior a los linfocitos viables. Por este motivo, consideramos que podría resultar interesante desarrollar un método que determinara el porcentaje (y número absoluto) de células B de memoria apoptóticas ex vivo en muestras mínimamente manipuladas. La lisis de la sangre completa con cloruro amónico, sin ningún gradiente celular posterior, nos ha permitido el análisis de un número de células de memoria claramente superior al conseguido con los métodos tradicionales de separación celular. En este caso, sin embargo, no pudimos utilizar la anexina como molécula capaz de detectar a las células apoptóticas, pues, de manera inesperada, el cloruro amónico elevó el «fondo» de la señal hasta dificultar sobremanera la interpretación de los resultados. Por el contrario, la 7-AAD, un colorante vital fluorescente, dio excelentes resultados arrojando, además, un dato muy revelador: una fracción relevante de células B de memoria en los pacientes con IDCV, claramente superior a la observada en controles sanos, tiene, muy probablemente, la señal de apoptosis dada ya in vivo. Otro dato más, inédito hasta el momento, que explicaría el descenso de estas células en la IDVC.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.