Obtener la concordancia de técnicas diagnósticas y confirmar el diagnóstico de los casos probables de tos ferina captados por inmunofluorescencia directa (IFD) durante un brote en 2013 en el departamento de Antioquia.
Materiales y métodosSe analizaron los datos demográficos, clínicos, epidemiológicos y de resultados de laboratorio de casos probables de tos ferina confirmados por IFD en un pico de tos ferina en 2013 en el departamento de Antioquia. Las muestras de aspirado nasofaríngeo y suero fueron recolectadas y recibidas entre los periodos epidemiológicos IV-VII de 2013. Todos los pacientes confirmados por IFD fueron confirmados por PCR o ELISA. El análisis de concordancia se realizó por índice kappa.
ResultadosDe las 180 muestras procesadas en el LSP de Antioquia, 134 (74%) fueron positivas por la técnica de IFD, de las cuales se confirmaron por PCR 109 muestras con 24 (22%) positivas para B. parapertussis, 3 (2,8%) para B. pertussis, 17 (15,6%) para Bordetella spp. y 18 (16,5%) con infección mixta por B. pertussis y B. parapertussis. De 81 casos que se confirmaron por ELISA, 31 (38,3%) fueron positivos. En el municipio de La Estrella la edad media de los casos confirmados fue de 6,6 años y la mediana de 3 años (rango: 2-4 años). Con respecto a los casos del municipio de Medellín, la edad media fue de 28,7 años y la mediana de 25 años (rango: 12-42 años). En su mayoría, en los síntomas no hubo diferencias significativas, excepto para la tos paroxística entre los casos confirmados de B. parapertussis y B. pertussis (p=<0,04) del municipio de La Estrella. De acuerdo con el índice kappa, los resultados mostraron una fuerza de concordancia pobre y sin grado de acuerdo con los resultados de las pruebas de PCR y ELISA comparados con IFD, índice kappa: (IFD/PCR: K = 0,0944) y (IFD/ELISA: K = −0,4533).
ConclusionesDurante este análisis, en el 2013 la población de Antioquia fue afectada por la circulación de B. parapertussis y B. pertussis en población adolescente y adulta en Medellín y en la población de 2-4 años en La Estrella. Actualmente, la PCR y la ELISA son las técnicas adecuadas para el diagnóstico de tos ferina. La IFD por su subjetividad y baja concordancia se encuentra en desuso.
To determine the correlation between diagnostic techniques and to confirm the diagnosis of probable cases of whooping cough captured by direct immunofluorescence (DIF) during an outbreak in 2013 in the department of Antioquia.
Materials and methodsWe analysed the demographic, clinical, and epidemiological data and the laboratory results of probable cases of whooping cough confirmed by DIF at a peak of whooping cough in 2013 in the department of Antioquia. The nasopharyngeal aspirate and serum samples were collected and received between the epidemiological periods IV-VII of 2013. All patients confirmed by DIF were confirmed by polymerase chain reaction (PCR) and/or enzyme-linked immunosorbent assay (ELISA). The analysis of agreement was performed using the kappa index.
ResultsOf the 180 samples processed in the public health laboratory of Antioquia, 134 (74%) were positive using the DIF technique of which 109 samples were confirmed by PCR, with 24 (22%) samples positive for B. parapertussis, 3 (2.8%) for B. pertussis, 17 (15.6%) for Bordetella spp. and 18 (16.5%) for mixed infection by B. pertussis and B. parapertussis. Of the 81 cases confirmed by ELISA, 31 (38.3%) were positive. In the municipality of La Estrella, the mean age of the confirmed cases was 6.6 years, and the median was 3 years (range, 2–4 years). For the municipality of Medellin, the mean age was 28.7 years, and the median was 25 years (range, 12–42 years). For most of the symptoms, there were no significant differences, except for paroxysmal cough among the confirmed cases of B. parapertussis and B. pertussis (p=<.04) in the municipality of La Estrella. According to the kappa index, the results showed poor correlation strength and no agreement with the results of the PCR and ELISA tests compared with DIF, kappa index: (DIF/PCR: K = 0.0944) and (DIF/ELISA: K = −0.4533).
ConclusionsDuring this analysis in 2013, Antioquia was affected by the circulation of B. parapertussis and B. pertussis in the adolescent and adult population in Medellin and the 2–4 year-old population in La Estrella. Currently, PCR and ELISA are the recommended techniques for diagnosing whooping cough. Due to its subjectivity and low correlation, DIF is in disuse.
La tos ferina es una enfermedad prevenible por vacuna, altamente contagiosa, causada por Bordetella pertussis (B. pertussis), un cocobacilo gramnegativo no fermentador, de requerimientos nutricionales especiales, que afecta exclusivamente al humano, que es el único reservorio1. La enfermedad tiene un amplio espectro de manifestaciones clínicas que depende de la edad del diagnóstico, estado de vacunación, previa infección con el microorganismo, transferencia pasiva de anticuerpos, tratamiento antimicrobiano, entre otras2–6.
La infección causada por B. parapertussis produce un cuadro que se distingue por manifestaciones clínicas menos severas que las de la tos ferina y que se presenta con menor frecuencia que B. pertussis7,8. Las infecciones causadas por B. pertussis, B. parapertussis, entre otros agentes bacterianos y virales que causan síndrome coqueluchoide, pueden ser indistinguibles y, por tanto, el diagnóstico por técnicas de laboratorio es necesario para especificar el agente etiológico9.
Las metodologías actualmente utilizadas para la detección de B. pertussis y B. parapertussis son el cultivo y la reacción en cadena de la polimerasa (PCR)10,11. El ensayo por inmunoabsorción ligado a enzimas (ELISA) con sueros pareados para la detección del isotipo IgG contra la toxina pertussis es útil para el diagnóstico de tos ferina causada por B. pertussis, sin embargo, se necesitan sueros pareados (lapso de 15 días) para obtener un resultado12. En casos especiales, se puede realizar un ELISA utilizando un solo espécimen; no obstante, se debe tener en cuenta las restricciones de su uso como diagnóstico, a menos que estos análisis se realicen en un contexto de brote, principalmente cuando estén involucradas las poblaciones adolescente y adulta13,14. La inmunofluorescencia directa (IFD) es un ensayo observador dependiente que actualmente no se recomienda como diagnóstico para tos ferina debido a la baja sensibilidad y especificidad comparadas con las técnicas actualmente avaladas: PCR, ELISA y cultivo15,16.
La vigilancia de la tos ferina en Colombia se realiza a través de la notificación individual de casos probables y a través de las búsquedas secundarias como la búsqueda activa institucional, la cual se define como la notificación de un caso positivo desde el Laboratorio de Salud Pública (LSP) con el fin de evaluar las búsquedas trimestrales de las instituciones de salud en donde se atendió el caso en los registros de atención, y como la búsqueda activa comunitaria, la cual consiste en la indagación o rastreo intencionado de casos probables de tos ferina que puedan estar ocurriendo o pudieron haberse presentado en la comunidad y que no hayan consultado a una institución de salud17–19.
Como medida de prevención se cuenta con la vacuna de DPT (difteria, Bordetella pertussis de célula entera y tétanos) y, de acuerdo con el esquema nacional de vacunación del Programa Ampliado de Inmunización (PAI) del Ministerio de Salud y Protección Social (MSPS), se cuenta también con la aplicación de la vacuna pentavalente (difteria, tétanos, pertussis, hepatitis B recombinada y Haemophilus influenzae tipo b) a los 2, 4 y 6 meses de edad con 2 refuerzos a los 18 meses y a los 5 años con la vacuna de DPT. Para el 2013 la cobertura fue del 91% en Colombia para las 3 primeras dosis17. Como medida de tratamiento antimicrobiano, los medicamentos recomendados son la claritromicina y la eritromicina, y aunque el medicamento recomendado para los menores de un año es la azitromicina, en el 2013 no se encontraba cubierto por el Plan Obligatorio de Salud para el tratamiento de tos ferina.
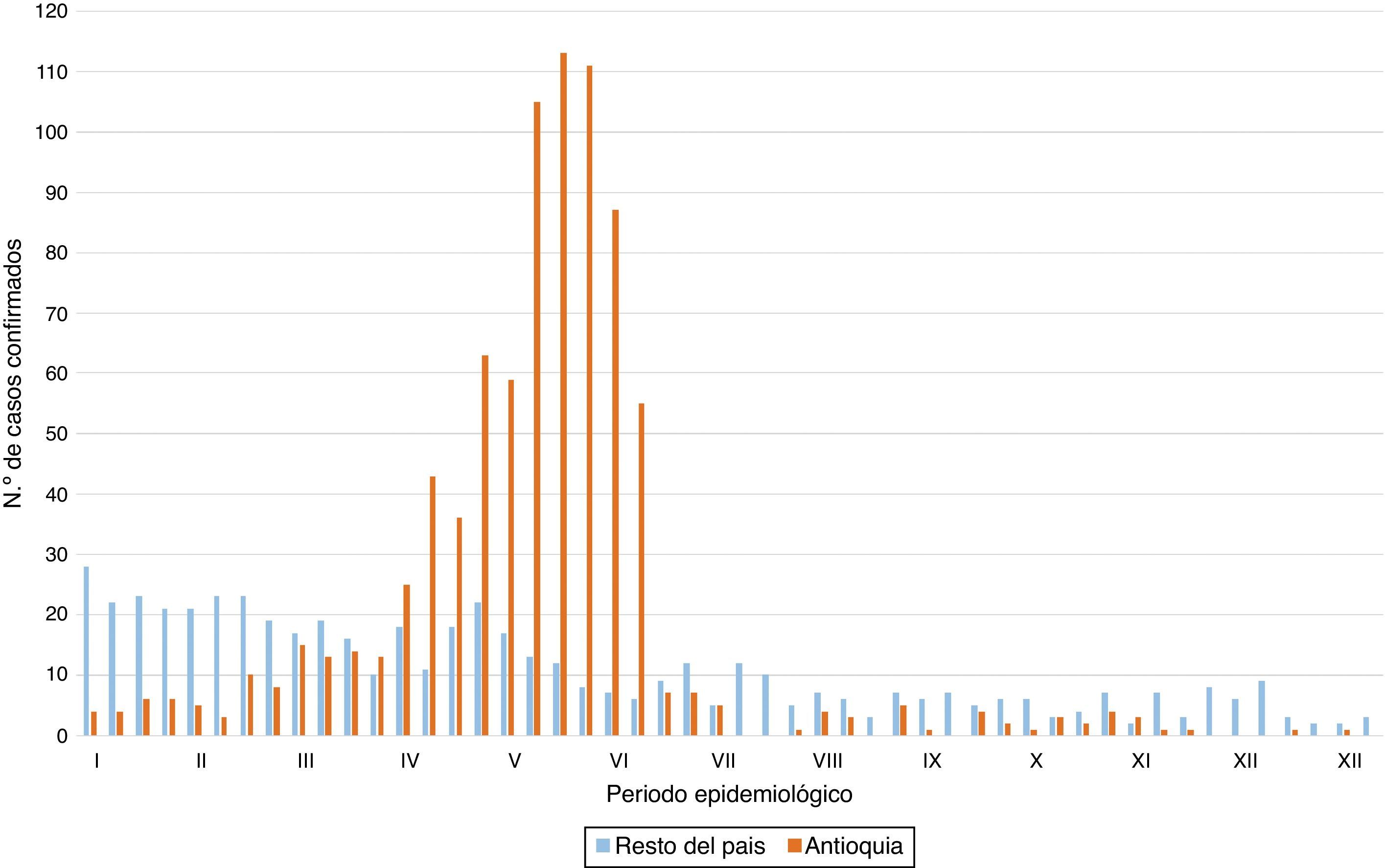
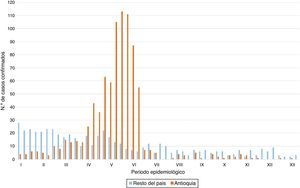
En Colombia han existido múltiples brotes de tos ferina, sin embargo, pocos se publican y reportan como diagnóstico la PCR en tiempo real. No obstante, algo parecido se reportó en un brote de 2006 en Cesar, donde los casos confirmados pertenecían a una comunidad indígena en la que la PCR de formato convencional para la detección única de IS481 detectó un mayor número de casos positivos comparada con la IFD: 6 casos que fueron positivos para PCR pero negativos para IFD20. En el 2012, la Organización Panamericana de la Salud emitió una alerta epidemiológica para Colombia, Canadá, Argentina, Chile y los Estados Unidos, la cual contenía un llamado de atención para que estuvieran preparados en la prevención, control y diagnóstico de tos ferina debido al aumento de los casos confirmados21. En 2013, la Secretaría Seccional de Salud y Protección Social de Antioquia detectó un aumento de casos confirmados en el departamento por B. pertussis en el periodo epidemiológico iv al vii22,23 (ver fig. 1), el aumento fue detectado a través de los resultados por IFD realizados por el LSP de Antioquia y reportado al Grupo de Inmunoprevenibles y Grupo de Microbiología del Instituto Nacional de Salud22 (INS). Con el fin de caracterizar con técnicas sensibles y específicas (PCR en tiempo real y ELISA) la situación del departamento, el objetivo del estudio fue obtener la concordancia entre técnicas diagnósticas, y confirmar el diagnóstico de los casos probables de tos ferina captados por IFD durante un pico de tos ferina en 2013.
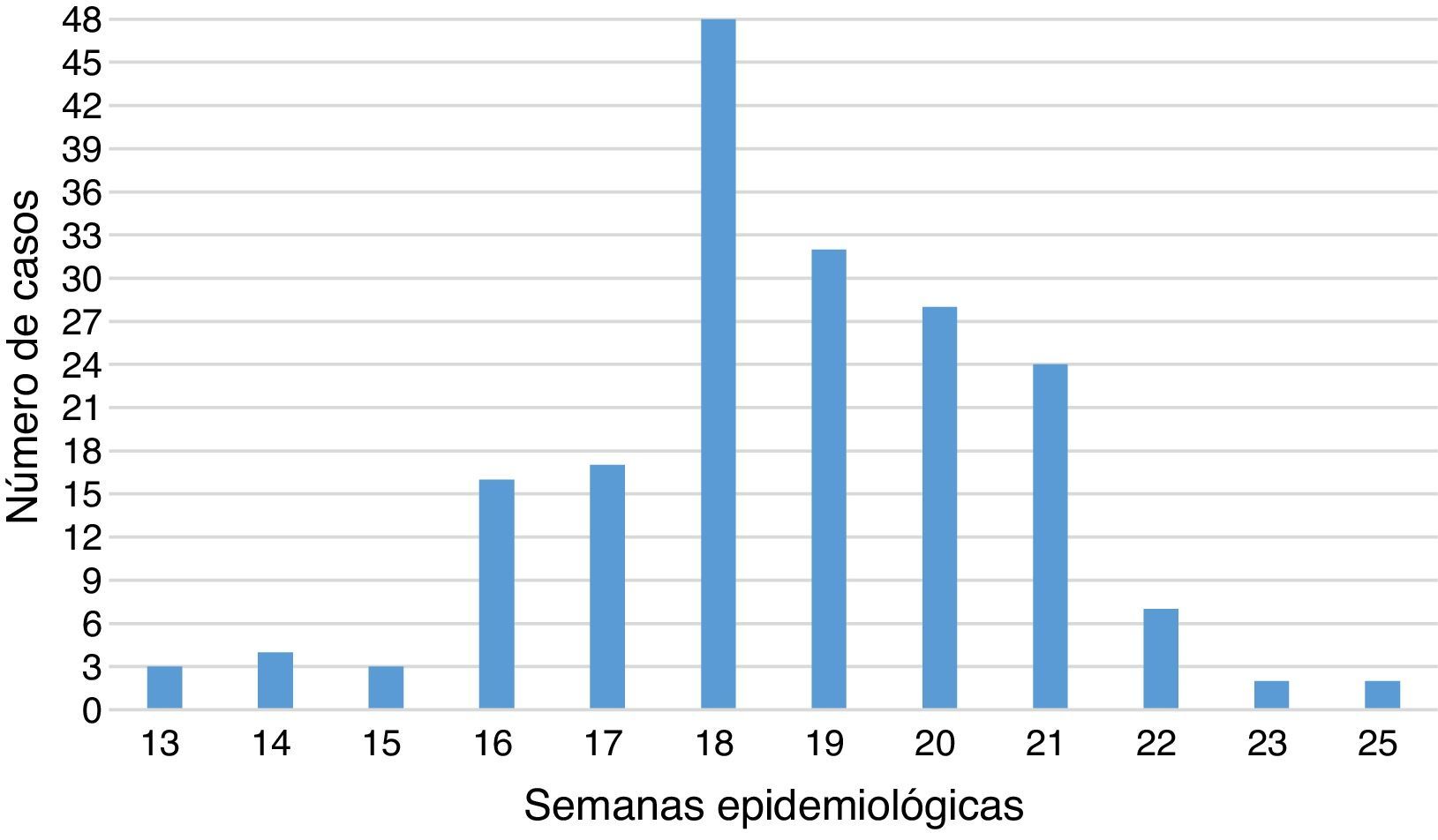
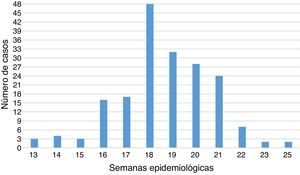
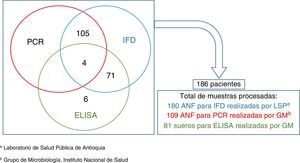
Materiales y métodosMuestrasSe recolectaron muestras de aspirados a través de la búsqueda activa comunitaria de contactos sintomáticos de pacientes con resultados positivos para IFD y de la búsqueda activa institucional a través de la revisión mensual de bases de datos del Sivigila de tos ferina del 2013 por el Grupo de Inmunoprevenibles del INS. En total se procesaron 180 aspirados nasofaríngeos por la técnica de IFD realizado por el LSP entre la semana epidemiológica 13 a la semana 25. Las muestras fueron enviadas al Grupo de Microbiología para confirmación de PCR en tiempo real, transportadas a 4 ¿C y mantenidas a -20 ¿C antes de su procesamiento. De las 180 muestras 109 cumplieron con los criterios de procesamiento por PCR en tiempo real de acuerdo a los lineamiento nacionales24. A las 71 muestras rechazadas para el procesamiento por PCR en tiempo real se solicitó toma de muestras de suero para realizar la confirmación de tos ferina por la técnica de ELISA. Los criterios de inclusión para la toma de muestras de suero fueron: pacientes que hubieran comenzado el tratamiento antimicrobiano, y que durante la toma de muestras hubiesen estado dentro de la ventana de los 15 días hasta los 3 meses a partir del inicio de los síntomas, pacientes mayores de 10 años sin antecedente de aplicación de vacuna o con un mínimo de 2 años entre el inicio de síntomas y la aplicación de la última dosis de DPT14,25. En la figura 2 se muestra por semana epidemiológica de acuerdo con la fecha de inicio de síntomas de los casos probables analizados.
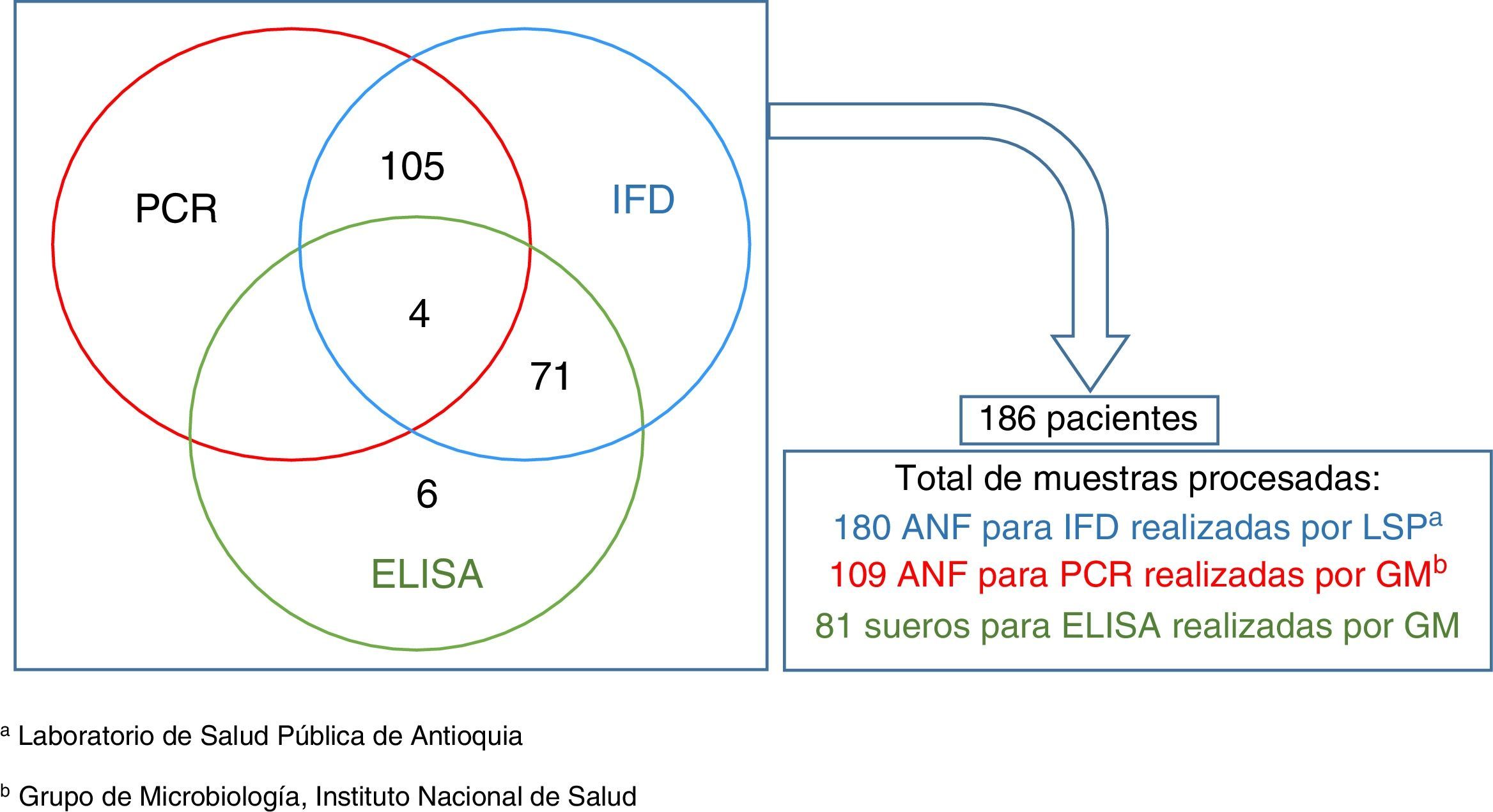
Consecuentemente, la Secretaría de Salud de Antioquia envió los 71 sueros para la confirmación por ELISA y adicionalmente envió 6 sueros de contactos sintomáticos que habían iniciado tratamiento profiláctico y no habían tenido resultado de IFD ni muestra nasofaríngea. Agregado a lo anterior, también recolectaron 4 sueros de pacientes que habían sido analizados por IFD y PCR, pero que en el momento de la toma del aspirado nasofaríngeo habían comenzado el tratamiento antimicrobiano, por lo cual se analizaron 81 muestras de suero para ELISA. En total se procesaron 370 muestras para diagnóstico y confirmación de B. pertussis con las técnicas de IFD, PCR y ELISA que pertenecían a 186 casos probables (ver fig. 3).
Obtención de datos demográficos, clínicos, epidemiológicos y de laboratorioSe realizó un estudio descriptivo transversal retrospectivo. Se analizaron los datos de la fecha de inicio de síntomas, dosis de vacuna, síntomas, duración de la tos y resultados de laboratorio recolectados de la base de datos de Sivigila 2013, de la base de datos del laboratorio de Antioquia y de la base de datos del Grupo de Microbiología. Los especímenes recolectados pertenecían a casos de los municipios de La Estrella (n: 94; 50,5%), Medellín (n: 62; 33,3%), San José de la Montaña (n: 16; 8,6%), Itagüí (n: 6; 3,2%), Pueblorrico (n: 3; 1,6%), Girardota (n: 2; 1,1%), Sabaneta (n: 2; 1,1%) y Rionegro (n: 1; 0,5%).
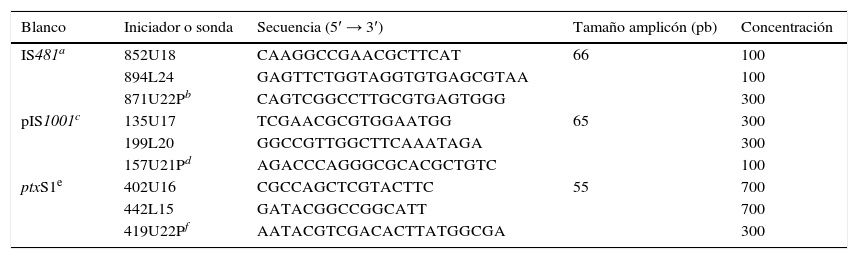
Ensayo de reacción en cadena de la polimerasaA las 109 muestras de aspirado nasofaríngeo se les realizó la extracción de ADN con el kit de Qiamp DNAmini kit (Qiagen, Alemania) a partir de 200μl de muestra y siguiendo las recomendaciones del fabricante; los eluidos obtenidos fueron almacenados a 4°C hasta su posterior procesamiento. Las secuencias de iniciadores y las sondas usadas en el análisis fueron las reportadas por Tatti et al.9 con modificación en los fluoróforos, quencher, concentración de sonda para IS481 y la ausencia de sondas e iniciadores para B. holmesii (ver tabla 1).
Secuencias de iniciadores y sondas utilizadas por el Grupo de Microbiología del Instituto Nacional de Salud para el ensayo de PCR dúplex
| Blanco | Iniciador o sonda | Secuencia (5′ → 3′) | Tamaño amplicón (pb) | Concentración |
|---|---|---|---|---|
| IS481a | 852U18 | CAAGGCCGAACGCTTCAT | 66 | 100 |
| 894L24 | GAGTTCTGGTAGGTGTGAGCGTAA | 100 | ||
| 871U22Pb | CAGTCGGCCTTGCGTGAGTGGG | 300 | ||
| pIS1001c | 135U17 | TCGAACGCGTGGAATGG | 65 | 300 |
| 199L20 | GGCCGTTGGCTTCAAATAGA | 300 | ||
| 157U21Pd | AGACCCAGGGCGCACGCTGTC | 100 | ||
| ptxS1e | 402U16 | CGCCAGCTCGTACTTC | 55 | 700 |
| 442L15 | GATACGGCCGGCATT | 700 | ||
| 419U22Pf | AATACGTCGACACTTATGGCGA | 300 |
Fuente: Modificado de Tatti et al., 2011.
a Acceso a GenBank número M28220.
b Sonda 5′ unida con 6-carboxifluoresceína (FAM) y 3′ unida con minor grove binder (MGB).
c Acceso a GenBank número X66858.
d Sonda 5′ unida con 4,7,2′-tericloro-7′-fenil6-carboxifluoresceína (VIC) y 3′ unida con minor grove binder (MGB).
e Acceso a GenBank número M14378.
f Sonda 5′ unida con 6-carboxifluoresceína (FAM) y 3′ unida con minor grove binder (MGB).
La PCR dúplex fue diseñada para la búsqueda de B. parapertussis y Bordetella spp. usando en la misma reacción los blancos pIS1001 e IS481. Se realizó una PCR singleplex para la búsqueda de la toxina pertussis (ptxS1) con el fin confirmar la presencia de B. pertussis cuando el resultado era positivo para IS481. Las dos PCR se realizaron en un volumen final de 25μl con adición de 4μl de ADN a una concentración de 2X de máster mix TaqMan Gene Expression (Applied Biosystems). Las condiciones de ciclado para los blancos IS481 y pIS1001 fueron 2 min a 50°C para activación de la enzima uracilo N-glicosilasa (UNG), denaturación inicial de 10min a 95°C y 45 ciclos con denaturación de 15 s a 95°C y anillamiento de 1min a 60°C. El ensayo con ptxS1 se realizó con las mismas condiciones anteriormente descritas, excepto por la temperatura de anillamiento que fue de 57°C26.
Interpretación de la PCREl resultado del ensayo de PCR se consideró negativo si el valor de Ct fue mayor o igual a 40. Una muestra es positiva para B. pertussis si el valor de Ct para los blancos IS481 y ptxS1 son menores a 40; se consideró como B. spp. las muestras que presentaban un valor de Ct mayor o igual a 35 e igual o inferior a 40 para IS481 y negativo para ptxS1. Si una muestra es positiva para pIS1001 con un valor de Ct ≤ 40 con resultado positivo o negativo para ptxS1, se consideró B. parapertussis9.
Ensayo de ELISASe utilizó el estuche comercial de ELISA para la búsqueda de anticuerpos IgG contra la toxina pertussis de Virion-Serion de acuerdo con el estudio de Rifflemann et al.27. El ensayo se realizó según las recomendaciones del fabricante a partir de 10μl de suero. Las lecturas se realizaron en el equipo Multiskan EX Thermoscientific (Alemania). Se consideraron muestras positivas con resultado ≥ 94 UE/ml13. Además, se tuvo en cuenta, en las condiciones de recolección de la muestra, que se hubiese tomado entre la tercera semana y hasta los 3 meses desde el inicio de la presentación de los síntomas, y que la última dosis de la vacuna hubiese sido aplicada con más de 3 años de anterioridad.
Ensayo de IFDEsta técnica fue realizada por el LSP de Antioquia de acuerdo con las recomendaciones del estuche comercial (Difco™ FA Bordetella pertussis, Beckton Dicikinson, Alemania), en la cual realizaron extendidos de los aspirados nasofaríngeos sobre láminas portaobjetos; luego usaron el conjugado comercial de anticuerpos policlonales marcados con isotiocianato de fluoresceína o FITC dirigidos contra los lipoligosacáridos y lipopolisacáridos de la pared de B. pertussis; por último, examinaron los extendidos en un microscopio de fluorescencia en el objetivo de inmersión (100X).
Análisis de datosLos datos obtenidos se analizaron con Epi-info 7.1 y Epidat 4.1. La prueba de chi-cuadrado se utilizó para comparar las proporciones de síntomas entre los casos positivos, negativos y por especie. La prueba t, para comparar las medias de duración de síntomas. El índice kappa se utilizó para analizar la concordancia de los resultados obtenidos de la IFD con PCR y ELISA.
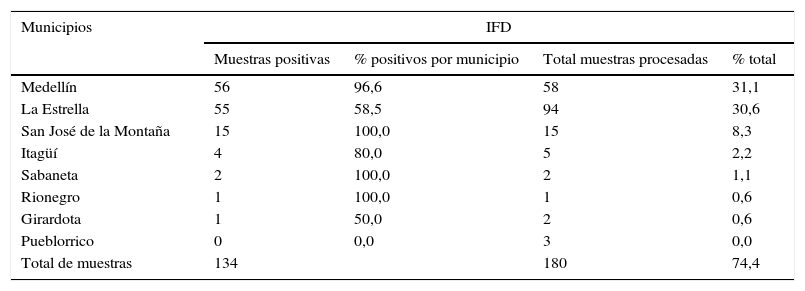
ResultadosDe las 180 muestras procesadas por el LSP de Antioquia, 134 (74%) fueron positivas por la técnica de IFD, de las cuales el 84% eran procedentes de los municipios de Medellín y La Estrella, y de estas muestras los resultados obtenidos por IFD para B. pertussis fueron n=56 (96,6%) y 55 (58,5%) respectivamente (ver tabla 2). De los 180 aspirados nasofaríngeos procesados por IFD, 109 (61%) muestras se pudieron analizar por PCR, de las cuales 94 eran procedentes del municipio de La Estrella (ver tabla 2); de estas muestras 55 (58,6%) fueron positivas para B. pertussis analizadas por la técnica de IFD, sin embargo, los resultados obtenidos por PCR en tiempo real arrojaron que, de las 94 muestras, 24 (25,5%) eran positivas para B. parapertussis, 18 (19,1%) eran positivas para coinfección B. pertussis y B. parapertussis, 11 (11,7%) eran positivas para Bordetella spp. y 2 (2,1%) eran positivas para B. pertussis (ver tabla 2). De acuerdo con los análisis realizados por IFD y por la PCR en tiempo real, de las muestras procedentes del municipio de La Estrella, el 55% de los resultados fueron positivos tanto por IFD como para PCR. Sin embargo, esta coincidencia no se observó reflejada en la concordancia entre las muestras analizadas por las 2 técnicas: PCR positivos e IFD negativos 23 (24%), PCR negativos e IFD positivos 23 (24%), y concordaron entre las 2 técnicas: 32 (34%) positivas y 16 (17%) negativas.
Resultados por técnica diagnóstica y municipios de Antioquia, 2013
| Municipios | IFD | |||
|---|---|---|---|---|
| Muestras positivas | % positivos por municipio | Total muestras procesadas | % total | |
| Medellín | 56 | 96,6 | 58 | 31,1 |
| La Estrella | 55 | 58,5 | 94 | 30,6 |
| San José de la Montaña | 15 | 100,0 | 15 | 8,3 |
| Itagüí | 4 | 80,0 | 5 | 2,2 |
| Sabaneta | 2 | 100,0 | 2 | 1,1 |
| Rionegro | 1 | 100,0 | 1 | 0,6 |
| Girardota | 1 | 50,0 | 2 | 0,6 |
| Pueblorrico | 0 | 0,0 | 3 | 0,0 |
| Total de muestras | 134 | 180 | 74,4 | |
| Municipios | ELISA | |||
|---|---|---|---|---|
| Muestras positivas | % positivos por municipio | Total muestras procesadas | % total | |
| Medellín | 20 | 38,5 | 52 | 24,7 |
| La Estrella | 1 | 50,0 | 2 | 1,2 |
| San José de la Montaña | 4 | 30,8 | 13 | 4,9 |
| Itagüí | 2 | 33,3 | 6 | 2,5 |
| Sabaneta | 0 | 0,0 | 2 | 0,0 |
| Rionegro | 1 | 100,0 | 1 | 1,2 |
| Girardota | 2 | 100,0 | 2 | 2,5 |
| Pueblorrico | 1 | 33,3 | 3 | 1,2 |
| Total de muestras | 31 | 81 | 38,3 | |
| Municipios | PCR en tiempo real | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| B. parapertussis | % positivos B. parapertussis por municipio | B. pertussis | % positivos B. pertussis por municipio | Bordetella spp. | % positivos Bordetella spp. por municipio | Coinfección B. pertussis/B. parapertussis | % positivos coinfección por municipio | Total muestras positivas PCR | % positivos por municipio | Total muestras procesadas | % total | |
| Medellín | 0 | 0,0 | 0 | 0,0 | 6 | 60,0 | 0 | 0,0 | 6 | 60,0 | 10 | 5.5 |
| La Estrella | 24 | 25,5 | 2 | 2,1 | 11 | 11,7 | 18 | 19,1 | 55 | 58,5 | 94 | 50.5 |
| San José de la Montaña | 1 | 20,0 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 1 | 20,0 | 5 | 0.9 |
| Itagüí | - | - | - | - | - | - | - | - | - | - | - | - |
| Sabaneta | - | - | - | - | - | - | - | - | - | - | - | - |
| Rionegro | - | - | - | - | - | - | - | - | - | - | - | - |
| Girardota | - | - | - | - | - | - | - | - | - | - | - | - |
| Pueblorrico | - | - | - | - | - | - | - | - | - | - | - | - |
| Total de muestras | 25 | 22,9 | 2 | 1,8 | 17 | 15,6 | 18 | 16,5 | 62 | 109 | 56.9 | |
Fuente: Grupo de Microbiología-INS.
-: no se realizó PCR.
Para las muestras procedentes del municipio de San José de la Montaña todas las muestras, 15 (100%), fueron positivas para B. pertussis de acuerdo con los resultados de IFD. Sin embargo, de estas 5 muestras que se enviaron para confirmar por PCR en tiempo real, ninguna fue positiva para esta especie excepto una (20%) que fue positiva para B. parapertussis. Para las muestras procedentes del municipio de Medellín, de las 58 muestras procesadas para IFD, 56 (96,6%) fueron positivas para B. pertussis; de estas, 10 muestras fueron enviadas para confirmación por PCR en tiempo real, donde se obtuvo que 6 (60%) muestras fueron positivas para Bordetella spp.
De las 81 muestras recolectadas para ELISA, el 65% pertenecían a los municipios de Medellín y San José de la Montaña, donde 20 (38,5%) y 4 (30,8%) fueron positivas, respectivamente, confirmando la presencia de niveles de anticuerpos asociados a infección por B. pertussis (ver tabla 2). Comparando los resultados de IFD y ELISA para las muestras procedentes del municipio de Medellín, de los 58 pacientes diagnosticados por IFD en Medellín, a 48 (83%) se les pudieron recolectar muestras de suero, donde 18 (37,5%) muestras fueron positivas para ELISA y 56 (96,6%) para IFD. De estas 48 muestras de suero con resultados de IFD, concordaron 18 (37,5%) muestras positivas y 2 (4,2%) negativas y no concordaron 28 (58,3%) muestras que fueron positivas para IFD y negativas para ELISA, que se interpreta como falsos positivos.
De 15 pacientes con muestras para IFD procedentes del municipio de San José de la Montaña solamente se obtuvieron 12 (80%) muestras para ELISA con resultados de IFD, donde 4 (33%) fueron positivas para ELISA de 12 (100%) muestras positivas para IFD. Por lo tanto, 4 (33%) muestras fueron concordantes para las 2 técnicas y 8 (66,6%) muestras fueron positivas para IFD y negativas para ELISA, que se interpretan como falsos positivos.
De acuerdo con los resultados encontrados por las diferentes técnicas, se realizó un análisis de concordancia entre lo emitido por IFD y PCR e IFD con ELISA. Para el análisis de concordancia de IFD y PCR se parte de que del total de 109 muestras procesadas para confirmación por PCR en tiempo real el 50,5% (55) de los resultados concordaron con los emitidos por IFD y el 49,5% (54) no fueron concordantes con la técnica de IFD; de los no concordantes el 28% (31) fueron falsos negativos y el 21% (23) falsos positivos. Tomando como técnica de referencia la PCR, el análisis de concordancia entre las 2 pruebas arrojó un índice kappa K = 0,0944, que se interpreta como fuerza de concordancia pobre (ver tabla 3). Con respecto a la concordancia de IFD y ELISA, de 75 pacientes que tenían tanto muestras de suero como aspirado nasofaríngeo, 28 (37,3%) resultados concordaron por las 2 técnicas y 43 (62,7%) no concordaron y, de estos resultados, 43 (57,3%) fueron falsos negativos y el 5,3% (4) fueron falsos positivos. Tomando como técnica de referencia la ELISA, el análisis de concordancia entre las 2 pruebas arrojó un índice Kappa K= −0,4533 que se interpreta como grado de no concordancia (ver tabla 3).
Concordancia de la IFD con PCR en tiempo real e IFD con ELISA en muestras del departamento de Antioquia, 2013
| PCR tiempo real multiplex | Serología | |||
|---|---|---|---|---|
| Positivo | Negativo | Positivo | Negativo | |
| IFD | ||||
| Positivo | 39 | 23 | 24 | 4 |
| Negativo | 31 | 16 | 43 | 4 |
| total | 109 | 75 | ||
| Índice kappa | 0,0944 | −0,4563 | ||
| Intervalo de confianza | (−0,2161-0,1537) | (−0,1647-0,0746) | ||
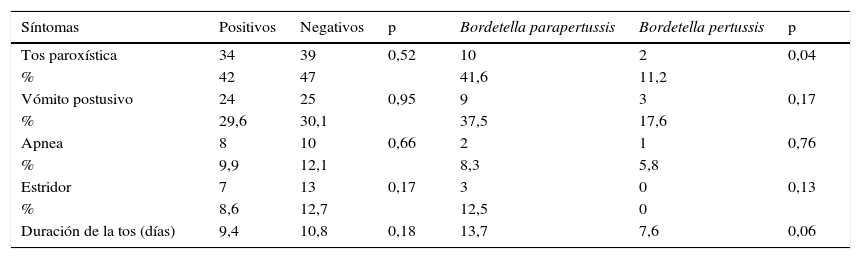
El 88% (164) de los casos probables se encontraron registrados en Sivigila; por tanto, el 12% (22) de los casos no tenían la información clínica ni epidemiológica ingresada al sistema nacional de vigilancia. Del total de casos probables, 81 (43,5%) fueron casos confirmados por ELISA o PCR, de los cuales estaban registrados en Sivigila 73 (90,1%) casos. La media de duración de tos fue de 9,4 días para los casos confirmados por PCR o ELISA, y la de casos negativos fue de 10,8 días, sin diferencias estadísticamente significativas (tabla 4). Con referencia a los otros síntomas registrados para los casos positivos, el 41,9% presentaron tos paroxística, 26,6% vómito postusivo y 10% apnea, sin diferencias significativas al compararlos con los casos negativos (ver tabla 4).
Análisis de síntomas según los resultados de PCR, ELISA y especie
| Síntomas | Positivos | Negativos | p | Bordetella parapertussis | Bordetella pertussis | p |
|---|---|---|---|---|---|---|
| Tos paroxística | 34 | 39 | 0,52 | 10 | 2 | 0,04 |
| % | 42 | 47 | 41,6 | 11,2 | ||
| Vómito postusivo | 24 | 25 | 0,95 | 9 | 3 | 0,17 |
| % | 29,6 | 30,1 | 37,5 | 17,6 | ||
| Apnea | 8 | 10 | 0,66 | 2 | 1 | 0,76 |
| % | 9,9 | 12,1 | 8,3 | 5,8 | ||
| Estridor | 7 | 13 | 0,17 | 3 | 0 | 0,13 |
| % | 8,6 | 12,7 | 12,5 | 0 | ||
| Duración de la tos (días) | 9,4 | 10,8 | 0,18 | 13,7 | 7,6 | 0,06 |
Con un total de 41 pacientes positivos para B. parapertussis y B. pertussis se encontró que la media de duración de tos fue mayor para los casos de B. parapertussis con 13,7 días comparada con 7,6 días de los casos con B. pertussis, sin diferencias estadísticamente significativas (tabla 4), aunque el 49% de los pacientes tenían tos de más de 2 semanas para los casos de B. pertussis comparada con el 41% de los casos de B. parapertussis. No obstante, hubo diferencia significativa en la proporción de tos paroxística de los casos de B. parapertussis comparada con los casos de B. pertussis (ver tabla 4).
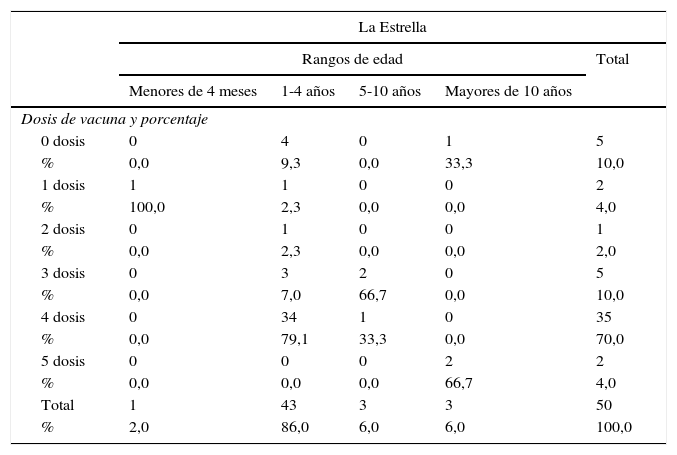
La edad media de los casos positivos en el municipio de La Estrella fue de 6,6 años y la mediana de 3 años (rango intercuartil: 2-4 años); de las 94 muestras procedentes de este municipio 55 (58,5%) fueron positivas por PCR o ELISA, de las cuales 50 (91%) de estos casos tenían registrado el antecedente de vacunación en Sivigila. En la tabla 5 se muestra por rangos de edad el antecedente de vacunación de los casos positivos, donde se observa que el 86% (n=43) de los casos se encuentran en el rango de edad de 1-4 años donde el 79% (n=34) tenían el esquema completo para 3 dosis y un refuerzo de acuerdo con el esquema de vacunación. Por otro lado, el 11% (n=5) tenían esquemas incompletos y el 9% (n=4) no tenían ninguna dosis aplicada (ver tabla 5). Analizando los resultados de especie y el estado de vacunación se observa en general para este municipio que el 70% (n=35) tenían un esquema completo de los cuales el 10% (n=5) fueron positivos para B. pertussis y el 24% (12) presentaban coinfección de B. pertussis-B. parapertussis (ver tabla 6).
Antecedente de vacunación por rangos de edad de los casos positivos del municipio La Estrella, Antioquia, 2013
| La Estrella | |||||
|---|---|---|---|---|---|
| Rangos de edad | Total | ||||
| Menores de 4 meses | 1-4 años | 5-10 años | Mayores de 10 años | ||
| Dosis de vacuna y porcentaje | |||||
| 0 dosis | 0 | 4 | 0 | 1 | 5 |
| % | 0,0 | 9,3 | 0,0 | 33,3 | 10,0 |
| 1 dosis | 1 | 1 | 0 | 0 | 2 |
| % | 100,0 | 2,3 | 0,0 | 0,0 | 4,0 |
| 2 dosis | 0 | 1 | 0 | 0 | 1 |
| % | 0,0 | 2,3 | 0,0 | 0,0 | 2,0 |
| 3 dosis | 0 | 3 | 2 | 0 | 5 |
| % | 0,0 | 7,0 | 66,7 | 0,0 | 10,0 |
| 4 dosis | 0 | 34 | 1 | 0 | 35 |
| % | 0,0 | 79,1 | 33,3 | 0,0 | 70,0 |
| 5 dosis | 0 | 0 | 0 | 2 | 2 |
| % | 0,0 | 0,0 | 0,0 | 66,7 | 4,0 |
| Total | 1 | 43 | 3 | 3 | 50 |
| % | 2,0 | 86,0 | 6,0 | 6,0 | 100,0 |
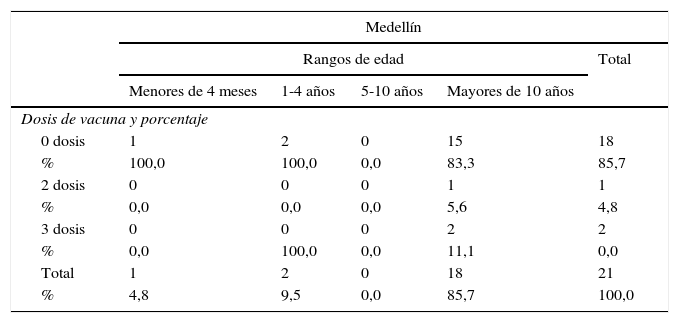
La edad media de los casos positivos en el municipio de Medellín fue de 28,7 años y la mediana de 25 años (rango intercuartil: 12-42 años). De las 58 muestras procedentes del municipio de Medellín, el 38% (n=22) fueron positivas por PCR o ELISA, de las cuales el 95% (n=21) tenían antecedente de vacunación registrado en Sivigila. En la tabla 7 se observa que el 86% (n=18) de los casos positivos en Medellín se agruparon en el rango de edad de mayores de 10 años y el 83% (n=15) no tenían ninguna dosis de vacuna aplicada, 6% (n=1) 2 dosis y el 11% (n=2) 3 dosis y, de acuerdo con el esquema de vacunación, ninguno de los casos cumplió con el esquema. En cuanto a los resultados por especie, todos los casos en Medellín fueron positivos para B. pertussis.
Antecedente de vacunación por rangos de edad de los casos positivos de los municipios de Medellín, Antioquia, 2013
| Medellín | |||||
|---|---|---|---|---|---|
| Rangos de edad | Total | ||||
| Menores de 4 meses | 1-4 años | 5-10 años | Mayores de 10 años | ||
| Dosis de vacuna y porcentaje | |||||
| 0 dosis | 1 | 2 | 0 | 15 | 18 |
| % | 100,0 | 100,0 | 0,0 | 83,3 | 85,7 |
| 2 dosis | 0 | 0 | 0 | 1 | 1 |
| % | 0,0 | 0,0 | 0,0 | 5,6 | 4,8 |
| 3 dosis | 0 | 0 | 0 | 2 | 2 |
| % | 0,0 | 100,0 | 0,0 | 11,1 | 0,0 |
| Total | 1 | 2 | 0 | 18 | 21 |
| % | 4,8 | 9,5 | 0,0 | 85,7 | 100,0 |
Los resultados del diagnóstico realizado a los casos probables de tos ferina con la técnica de IFD no fueron concordantes comparados con la técnica de PCR. De acuerdo con lo encontrado en la literatura, la técnica tiene una baja sensibilidad para detectar casos: 11,4%28, 18%29 y 52,2%16. Al comparar los resultados de IFD con ELISA el 89% (n=67) fueron muestras positivas para ELISA y el 37% (n=28) para IFD. Solo el 32% (n=24) de las muestras eran concordantes como positivas de las 75 muestras analizadas por las 2 técnicas. Actualmente la ELISA es una de las técnicas con mayor sensibilidad recomendada por el CDC y FDA para confirmación de brotes10.
En los protocolos usados para diagnóstico9,10 de tos ferina por el laboratorio, se realiza de forma rutinaria la especiación de las muestras debido a que diferentes agentes pueden causar manifestaciones clínicas similares a la tos ferina30,31. De acuerdo con los hallazgos de este estudio, al comparar los resultados de especies entre PCR e IFD, solo el 24% (n=26) de las muestras fueron positivas para el blanco IS481 del 57% (n=62) de muestras positivas por IFD. Estos resultados indican que el 33% (n=36) de las muestras analizadas por IFD no era B. pertussis. El conjugado que se usó para el diagnóstico en el LSP de Antioquia no detecta B. parapertussis y los resultados de la confirmación mostraron que el 22% (n=24) de las muestras positivas eran B. parapertussis, que se puede interpretar como una posible reacción cruzada. En general, la especificidad de la IFD es baja. De acuerdo con un brote en Canadá en el periodo 1989-1991 donde el LSP del norte de Alberta (Canadá) encontró que la especificidad de IFD comparada con la PCR era del 58,3%32, donde el 87% de las muestras eran falsos positivos y el 35% cumplían con los criterios de inclusión de caso probable; también evaluaron la reactividad cruzada con patógenos aeróbicos, anaerobios del microbioma de la cavidad oral y de la nasofaringe, en la cual encontraron que 3 microorganismos tenían reactividad cruzada con la prueba de IFD comercial32, por tanto, los resultados de IFD con anticuerpos poli- o monoclonales son dependientes del número de microorganismos presentes en la muestra y por tener la característica de ser un ensayo observador dependiente, subjetiva y codependiente de la experiencia del analista puede causar imprecisiones a la hora de interpretar la técnica. Según los análisis realizados con el índice kappa, se encontró un grado muy bajo de concordancia entre la técnica de IFD comparada con PCR y ELISA.Por tal razón, en el 2006 los Centros para el Control y Prevención de las Enfermedades (CDC), con el apoyo de la escuela de medicina de Harvard, publicaron en el reporte semanal de morbimortalidad (MMWR) que los métodos diagnósticos adecuados para confirmar casos de tos ferina son el cultivo, la PCR y la serología.
En el municipio de La Estrella, los resultados de PCR mostraron que, del total de casos positivos, el 42% (n=23) eran B. parapertussis y el 33% (n=18) presentaron infección mixta de B. parapertussis y B. pertussis. Por tanto, el 75% de los pacientes estaban infectados con B. parapertussis, que era el principal agente causal de la sintomatología en los pacientes entre 1 y 4 años clasificados como casos probables de tos ferina en ese municipio. Esta frecuencia es mayor que la observada en la provincia pakistaní de Khyber Pukhtoonkhawa, donde se ha reportado una frecuencia del 35%33, en Alemania con el 36% en la vigilancia de 1993-199534 o en Finlandia con el 39,2% de 1994-199735. Una duración de tos superior a 2 semanas se presentó en el 49 y el 41% de los casos confirmados para B. pertussis y B. parapertussis, respectivamente. Este resultado contrasta con lo encontrado en Alemania en el periodo 1992-1994 en que la proporción de tos de duración mayor a 2 semanas para B. pertussis y B. parapertussis fue del 26 y del 18%, captando el 57 y el 37% de los casos en la cuarta semana desde el inicio de los síntomas; este hallazgo puede indicar de manera indirecta una oportuna intervención de la Secretaría de Salud de Antioquia y su red hospitalaria en la captación de casos sospechosos de tos ferina36,37. El 70% de los casos en La Estrella tenían un esquema completo de vacunación. Sin embargo, la vacunación está dirigida a B. pertussis y estudios en modelos murinos han demostrado que la vacuna celular tiene una eficacia menor contra B. parapertussis que contra B. pertussis38. No obstante, el 30% de los casos no tenían el esquema completo de vacunación, lo que aumentó la probabilidad de ser una población susceptible y transmisora de B. pertussis.
Frecuentemente los casos positivos para B. pertussis presentan con mayor frecuencia tos paroxística comparados con B. parapertussis8. No obstante, en el municipio de La Estrella se encontraron más casos de paroxismos por B. parapertussis que con B. pertussis. Este hallazgo ha sido encontrado en 1/3 de los niños que han presentado manifestaciones típicas de tos ferina causadas por B. pertussis36. Aunque en general no se encontraron diferencias en la presentación de síntomas con excepción de la tos paroxística, tanto entre los confirmados por B. parapertussis como por B. pertussis, algunos estudios han reportado que existen diferencias en la media de recuento de leucocitos, causada, probablemente, por la producción de la toxina pertussis en B. pertussis y la no transcripción de este factor de virulencia en B. parapertussis por la ausencia de la zona promotora del gen36,39. Actualmente el recuento de leucocitos no se reporta en la ficha epidemiológica en Colombia, dato que podría aportar información en la clasificación de los casos. La discriminación por síntomas para asociar un agente etiológico causante del síndrome coqueluchoide sigue siendo un reto para el diagnóstico clínico, debido a la amplia lista de microorganismos que causan este síndrome: virus sincitial respiratorio, Chlamydophila pneumoniae, Mycoplasma pneumoniae y B. parapertussis, entre otros30,31. Por tal razón es necesario que los laboratorios clínicos y, especialmente, los laboratorios de referencia regionales tengan técnicas lo suficientemente específicas para conocer los agentes etiológicos que circulan en la población y para que sean un aporte a la toma de decisiones clínicas y de control, entre otras.
En el municipio de Medellín los casos no fueron confirmados por PCR. No obstante, el ELISA fue un ensayo fundamental para confirmar los casos por B. pertussis en adolescentes y adultos, por tal razón actualmente se ha convertido en la técnica para el diagnóstico en estos grupos de edad, debido a la mayor sensibilidad del ensayo en las etapas tardías de la enfermedad14. De los casos positivos en la población adolescente y adulta en Medellín, ninguno tenía el esquema completo de vacunación. No obstante, se ha reportado que la duración máxima de la inmunidad por vacuna celular en promedio se puede mantener 6 años; por tanto, la protección en Colombia, cumpliendo con el calendario de vacunación cuando el último refuerzo se aplica a los 5 años se puede deducir que la vacuna puede inducir una respuesta protectora hasta los 11 años de edad de acuerdo con los estudios de efectividad en la vacuna37. Actualmente se conoce que la principal fuente de transmisión de la tos ferina en neonatos e infantes40 es la población adolescente y adulta, sin embargo esta población tambien es susceptible a presentar la enfermedad como se reporta en varios países con alta cobertura. En Estados Unidos se encontró en el periodo 2006-2010, en pacientes entre 50 y 65 años, la incidencia reportada estuvo entre 2,1 y 4,1 casos/100.000 habitantes41. En Colombia también se han reportado casos en estas poblaciones: en el periodo 2012-2013 se confirmaron 596 y 458 casos, respectivamente, en mayores de 15 años42,43 y, de acuerdo con los datos encontrados en este estudio, 23 (12,4%) pacientes confirmados eran mayores de 18 años. De acuerdo con los hallazgos históricos, tener la posibilidad de considerar más medidas de control como la aplicación de un refuerzo de vacuna en adolescentes y adultos que disminuiría la incidencia en esta población, y también minimizaría la probabilidad de contagio a los menores de un año, que son los más afectados40,44.
En los últimos años se han reportado brotes de tos ferina a nivel mundial. En el 2012 el Secretario de Salud del Estado de Washington declaró una epidemia de tos ferina, puesto que el número de casos notificados en Washington en 2012 había llegado a 2.520 (37,5 casos/100.000 habitantes) un aumento de 1.300% comparado con el mismo periodo en 2011 y el mayor número de casos notificados que en cualquier otro año desde 1942; la frecuencia de B. pertussis y B. parapertussis fue de 90,7 y 5,7% respectivamente45. Se han presentado brotes con diferentes especies de Bordetella de los que se han descrito recientemente fue en Ohio donde la coinfección entre B. pertussis con 48 (29%) casos confirmados y B. holmesii con 112 (68%) muestras de 164 muestras de 298 muestras en total fueron captadas por PCR múltiple7. En la ciudad de San Petesburgo en Rusia, en el periodo 1998-2000, la frecuencia de B. parapertussis osciló en un 13%, incluyendo las infecciones mixtas con B. pertussis46. En Finlandia, un estudio en el periodo 1994-1997 señaló que la frecuencia de B. parapertussis fue del 32 y del 7,2% en infecciones mixtas35; las especies fueron diferenciadas por PCR y cultivo.
El 12% de los pacientes no estaban registrados en Sivigila, por lo tanto, es necesario hacer un llamado de atención a los grupos de vigilancia epidemiológica para disminuir la subnotificación. La especiación del género Bordetella en casos probables de tos ferina es fundamental para confirmar el agente causal9,26,46. No se realizaron cultivos durante el periodo de estudio, debido a que el ensayo no estaba implementado durante la época del brote en el LSP. Hay que considerar que, aunque se mantuvieron las muestras en congelamiento (−20°C), realizar cultivos posteriormente sin las condiciones mínimas de temperatura (4°C a 35°C) o sin mantener los aspirados después de obtenidos en medios de transporte semisólidos Regan Lowe y sin cultivarlos en menos de una semana en placas de medio Regan Lowe, hace que la probabilidad de recuperar el microorganismo hubiera sido mínima24,47,48. Fortalecer el cultivo no es solo importante para el diagnóstico, sino también para la vigilancia por el laboratorio, debido a que los aislamientos recuperados pueden analizarse por medio de tecnologías de tipificación molecular, por ejemplo: electroforesis de campos pulsados (Pulsed-field Gel Electrophoresis)49, tipificación multilocus de secuencias (Multilocus sequence typing)50, análisis de las repeticiones en tándem de número variable en múltiples loci (Multiple-Locus Variable number tandem repeat Analysis)51 y la secuenciación de genoma completo52, entre otras. Estas herramientas ofrecen la oportunidad de entender los cambios de la población de B. pertussis en el tiempo49, la caracterización específica de brotes53, la búsqueda de relaciones entre los aislamientos circulantes y las cepas o antígenos usados en vacunas54, y el efecto de la vacunación en la evolución del microrganismo52, entre otros.
En Colombia para el 2012 de todos los casos reportados a nivel nacional el 61,2% (n=2.419) de los casos confirmados no tenían ninguna dosis aplicada de vacuna, de los cuales 932 (38,5%) casos ocurrieron en menores de 2 meses, lo que explica el alto número de casos. Sin embargo, también se observaron casos en población vacunada: por ejemplo, de 580 casos, el 58,2% tenían aplicada la primera dosis en el rango de edad 2-3 meses, el 43,3% de 223 casos confirmados tenían aplicada la segunda dosis en el rango de edad de 4-5 meses y el 45,5% de 357 casos tenían la tercera dosis en el rango de edad de 6-11 meses. Para 2013 aumentó esta cifra de casos en población vacunada donde el 38% de 472 casos en el rango de edad de 4-5 meses tenían la segunda dosis y el 45,5% de 357 casos en el rango de edad de 6-11 meses tenían la tercera dosis23,42,55. De acuerdo con este estudio, también se halló que de un 70% (n=35) de los casos confirmados con esquema completo, el 10% (n=5) fueron infectados por B. pertussis y el 24% (n=12) de los casos con infección mixta dentro del rango de 1-4 años. Por tanto, obtener aislamientos a partir de la vigilancia por laboratorio sirve para conocer el tipo de cepas circulantes, debido a la evidencia de cambios en las características antigénicas y genotípicas de las cepas circulantes de B. pertussis. Por ejemplo, se ha reportado que los alelos que expresan los diferentes antígenos de las cepas circulantes en gran parte difieren de los expresados por las cepas utilizadas en la producción de vacunas56,57.
Desde el 2007, la Organización Mundial de la Salud (OMS) en cooperación con CDC han recomendado que la técnica adecuada para realizar el diagnóstico de tos ferina (definida como enfermedad causada por B. pertussis) sea la PCR en tiempo real debido a la alta sensibilidad y especificidad. Por otro lado, esta técnica tiene la característica de obtener resultados oportunos que mejoran y apoyan las acciones en salud pública. Otra ventaja es que desde un mismo ensayo se puede realizar la especiación de las muestras que aumenta la búsqueda de otras especies de Bordetella9,10,15. En la actualidad, Colombia, dentro de los lineamientos nacionales, recomienda el uso de esta técnica para el diagnóstico24. Sin embargo, preocupa que 33 de los 35 LSP no tengan implementada la técnica molecular y hasta el momento se siga centralizando el diagnóstico en el Laboratorio Nacional de Referencia (Grupo de Microbiología, INS)55, lo que afecta a la oportunidad de los resultados en un evento de notificación obligatoria y de impacto en salud pública.
Se aclara que el LSP de Antioquia en el 2013 realizó el diagnóstico con IFD, técnica con la que se venía trabajando desde 1995 y que a partir de varias capacitaciones y actualizaciones con el Grupo de Microbiología del INS, el LSP ha pasado por un proceso de transición con las 2 técnicas (IFD-PCR) desde finales de 2013 hasta 2015 y actualmente realiza el ensayo molecular y el cultivo como pruebas diagnósticas.
Entre las limitaciones de este análisis están que no se realizó el diagnóstico por cultivo para el aislamiento de los agentes involucrados en el brote y no se obtuvo muestra de suero para los pacientes con resultado de PCR con el fin de haber obtenido la concordancia entre la PCR y la ELISA.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
A la doctora Diana Posada del Laboratorio de Salud Pública de Antioquia y a la doctora Marcela Arrubla del Grupo de Vigilancia de la Secretaría de Salud de Antioquia.