INTRODUCCION
La prevalencia del síndrome del intestino irritable (SII) es muy elevada, lo que comporta una gran repercusión sanitaria, social y económica. El número de consultas médicas, de pruebas diagnósticas (en este caso no diagnósticas) y de prescripciones terapéuticas es muy grande, con el consiguiente gasto de recursos. Supone, además, una de las primeras causas de absentismo laboral. Por otra parte, si bien el SII no pone en riesgo la vida del paciente, sí que condiciona de forma considerable su calidad.
Se han publicado diversos estudios epidemiológicos sobre la prevalencia del SII, y ésta oscila entre un 5 y un 20%, según de la población estudiada y los criterios diagnósticos empleados1-3. En cualquier caso, el SII está presente en todos los países y es una causa importante de frecuentación médica4. Desde hace mucho tiempo se ha dicho que sólo la tercera parte de los sujetos con SII buscaban atención médica. Estos datos procedían de investigaciones realizadas en Estados Unidos5, pero los datos obtenidos de la población española demuestran que en nuestro medio más de las dos terceras partes de personas con SII acuden al médico6. Todavía no se han dilucidado los motivos por los que unas personas buscan asistencia sanitaria y otras no. Algunos estudios parecen indicar que la razón fundamental es la intensidad de las molestias, mientras que en otros son los factores psicosociales los determinantes. Otro de los factores que, sin duda, influyen en la decisión de consultar al médico es la facilidad de acceso y gratuidad del sistema sanitario en el que se encuentra el paciente. Así, en España el 58% de los sujetos con SII con estreñimiento y el 67% de SII con diarrea buscan atención sanitaria7.
¿HASTA QUÉ PUNTO ESTA AFECTADA LA CALIDAD DE VIDA EN LOS PACIENTES CON SINDROME DEL INTESTINO IRRITABLE?
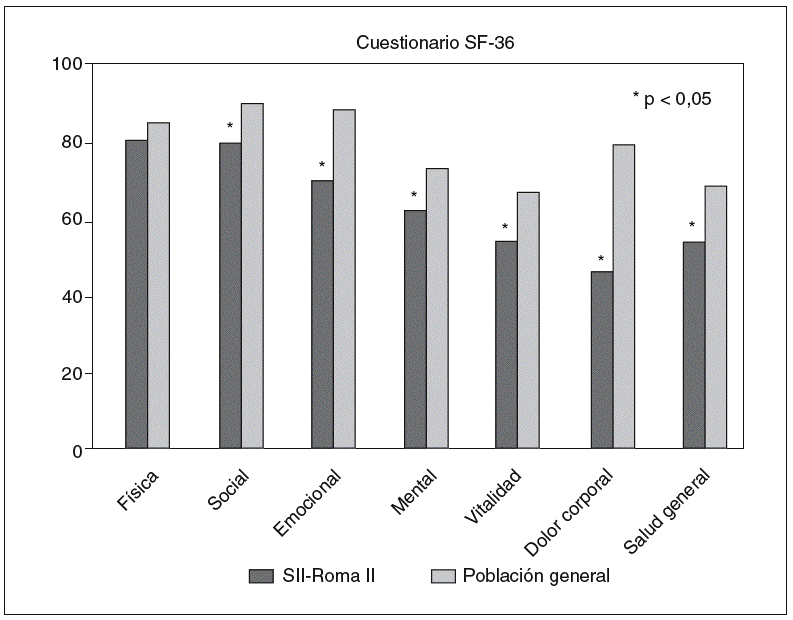
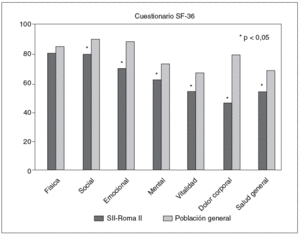
Diversos estudios han demostrado que los pacientes con SII tienen una peor calidad de vida que la población general (fig. 1). Mediante la utilización del SF-36, se ha comprobado que la calidad de vida relacionada con la salud (CVrS) está afectada tanto en los pacientes con SII que acuden a un hospital terciario como en los que pertenecen a asociaciones de pacientes8,9; los pacientes que son visitados en centros de atención primaria también presentan una peor calidad de vida que la población general10. Otro aspecto interesante es que, a pesar de lo que pudiera parecer, la CVrS se afecta de forma semejante en las personas mayores y en los jóvenes con SII11.
Fig. 1. Comparación de la calidad de vida en pacientes con síndrome del intestino irritable (de acuerdo con los criterios diagnósticos de Roma II) con la población general, según el cuestionario SF-36.
Se ha observado que hay una relación entre la intensidad de los síntomas del SII y el grado de deterioro de la CVrS12. Las personas que consultan al médico tienen una peor calidad de vida que los que no consultan13, y los que acuden a un centro hospitalario peor que los que acuden a un centro de atención primaria14. En relación con este punto, se concluyó en un excelente trabajo15, realizado en 2001, que tanto la intensidad de los síntomas digestivos como el estado psicológico parecen influir en la CVrS. Además, la calidad de vida percibida se relaciona con la representación propia de la enfermedad y con la capacidad de tolerancia y adaptación; así, un menor control se acompaña de una peor CVrS, menor satisfacción con el estado de salud y mayores índices de depresión16.
Es interesante apuntar que la CVrS está disminuida de forma semejante en el SII con estreñimiento que en el SII con diarrea, o cuando estreñimiento y diarrea se alternan, aunque en el subtipo con hábito deposicional alternante la frecuencia de dolor es mayor, así como el número de visitas médicas7. Por otra parte, es importante tener en cuenta que la CVrS puede diferir según los criterios utilizados para definir el SII. De tal forma, la calidad de vida es peor en los sujetos que cumplen los criterios de Roma II que sólo los de Roma I2. A su vez, la alteración de la CVrS puede ser diferente en distintos países; utilizando los mismos criterios de valoración clínica y el SF-36 como cuestionario genérico de calidad de vida y el IBSQOL como cuestionario específico, se observó que el efecto del SII sobre la CVrS era mayor en el Reino Unido que en Estados Unidos9.
COMPARACION DE LA CALIDAD DE VIDA DE LOS PACIENTES CON SINDROME DEL INTESTINO IRRITABLE CON LOS QUE SUFREN OTRAS ENFERMEDADES
Mediante el cuestionario SF-36, Gralnek et al8 observaron que los pacientes con SII visitados en un centro terciario tenían una peor calidad de vida que los pacientes con una enfermedad por reflujo gastroesofágico (ERGE), diabetes o insuficiencia renal. Otros estudios también han demostrado la alteración en la CVrS en pacientes con SII y la han comparado con otras enfermedades: nuevamente se demostró una peor calidad de vida que en los que tienen ERGE, asma o migraña, pero mejor que los que presentan trastornos de pánico o artritis reumatoide17.
Una enfermedad con la que resulta comparable el SII es la enfermedad inflamatoria intestinal; cuando se establece esta comparación, el resultado es que el índice de bienestar general es peor en el SII que en los pacientes con enfermedad inflamatoria intestinal en remisión18.
TRATAMIENTO «CONVENCIONAL» DEL SINDROME DEL INTESTINO IRRITABLE
Medidas generales
El primer paso, y fundamental, es explicar al paciente de forma clara y segura el síndrome que padece, así como tranquilizarle. En muchos pacientes la presencia de síntomas suscita una importante preocupación por el miedo a padecer un cáncer. Por consiguiente, para establecer una buena relación médico-paciente es básico que el diagnóstico se establezca con claridad. Los exámenes repetidos o inapropiados transmiten la inseguridad del médico y generan miedo e incertidumbre en el paciente.
Con frecuencia, se recomienda hacer modificaciones de la dieta como primer paso en el tratamiento de los pacientes con SII. Parece lógica la evitación de los nutrientes o estilos de vida que probablemente induzcan los síntomas (es decir, comidas copiosas, grasas, hidratos de carbono no absorbibles, café, té y lactosa); no obstante, ninguna prueba científica respalda esta estrategia, y las limitaciones excesivamente rigurosas de los hábitos dietéticos normales pueden incluso deteriorar más la calidad de vida. Los ensayos clínicos llevados a cabo sobre la valoración de las modificaciones en la dieta han prestado atención al alivio del dolor y a los cambios de las características de las heces. La mayoría de los ensayos controlados con placebo se han llevado a cabo con fibra. Una dieta rica en fibra (20-30 g/día) mejora el estreñimiento, acelera el tránsito intestinal y puede reducir la presión intracolónica. Sin embargo, en pacientes con SII no se identifica un menor consumo de fibra que en los individuos control asintomáticos19. Además, los ensayos clínicos no han demostrado un beneficio significativo de la utilización de fibra comparada con placebo20. Por otra parte, el tratamiento con fibra puede agravar los síntomas del SII porque reduce el umbral del dolor secundario a la distensión y favorece la distensión del colon a través de la formación de gas a partir de la fermentación bacteriana21. Por consiguiente, no se dispone de pruebas científicas que respalden que los cambios de los hábitos dietéticos o el estilo de vida mejoren la sintomatología del síndrome. La dieta con suplementos de fibra puede mejorar el estreñimiento en el SII con predominio de este síntoma, pero la aparición de síntomas relacionados con la formación de gas, o su agravación, limita su utilidad clínica.
Fármacos dirigidos a controlar la diarrea
La loperamida es el fármaco más utilizado para el SII con predominio de diarrea. La mayoría de los ensayos efectuados con este fármaco en el SII con predominio de diarrea ha demostrado un efecto beneficioso comparado con placebo. En un ensayo clínico doble ciego, controlado con placebo, de 13 semanas de duración, la loperamida mejoró significativamente la frecuencia de las deposiciones, la consistencia de las heces y la urgencia defecatoria22. Otro ensayo clínico a doble ciego, cuyos resultados se han publicado más recientemente, confirmó los de este estudio, pero también reveló un aumento del dolor nocturno en pacientes tratados con loperamida23. No obstante, la relevancia clínica de ambos ensayos está limitada por la elevada proporción de abandonos (el 19 y el 30%, respectivamente). Por lo tanto, las pruebas científicas de la eficacia de este fármaco para el tratamiento del SII son limitadas y se requieren ensayos adicionales.
Fármacos dirigidos a controlar el estreñimiento
Cuando en el SII predomina el estreñimiento, se suelen emplear agentes formadores de masa o laxantes suaves. Los agentes que aumentan el bolo intestinal se utilizan a veces como suplemento de la dieta rica en fibra, especialmente en los pacientes que no toleran el salvado de trigo. Los laxantes deben utilizarse como último recurso terapéutico del estreñimiento, en cuyo caso son preferibles los laxantes suaves (osmóticos o salinos) a los estimulantes, debido a los mayores efectos secundarios de estos últimos.
Fármacos espasmolíticos
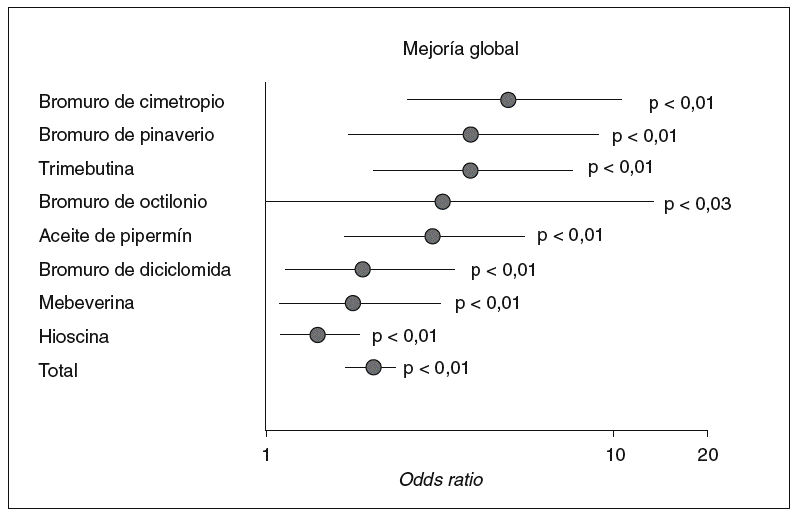
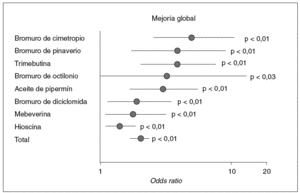
En el tratamiento del SII se utilizan con frecuencia los antiespasmódicos. Se han evaluado diversos agentes, pero la mayor parte de ensayos ha suscitado críticas debido a las limitaciones metodológicas (inclusión de un número reducido de pacientes, número elevado de abandonos, breve duración de los ensayos, etc.). De hecho, entre 36 ensayos clínicos aleatorizados, doble ciego, controlados con placebo, sobre fármacos antiespasmódicos, cuya duración fue superior a 2 semanas, sólo 15 evaluaron el dolor o la mejora sintomática general como variable principal; además, la proporción de abandonos fue del 59%. Sin embargo, entre los ensayos mencionados previamente, 26 fueron comparables desde un punto de vista metodológico y se incluyeron en el metaanálisis de Poynard et al24. Como consecuencia de este análisis, los antiespasmódicos fueron superiores a placebo desde un punto de vista de la mejora global (el 62 frente al 35%; p < 0,01) y el alivio del dolor abdominal (el 64 frente al 45%; p < 0,01). Estos resultados positivos se obtuvieron con 5 agentes diferentes: bromuro de cimetropio, bromuro de pinaverio, bromuro de octilonio, trimebutina y mebeverina24 (fig. 2). En otro metaanálisis, llevado a cabo años más tarde también por Poynard et al25, se puso de relieve que los relajantes del músculo liso y los anticolinérgicos fueron mejores que el placebo para algunos síntomas del SII. En una revisión sistemática que incluyó 13 estudios, 7 considerados de alta calidad, los autores llegaron a la conclusión de que los antiespasmódicos eran eficaces para el alivio del dolor abdominal en pacientes con SII26.
Fig. 2. Metaanálisis de los resultados terapéuticos obtenidos con diversos espasmolíticos en el síndrome del intestino irritable. (Tomado de Poynard et al25.)
En conclusión, y teniendo en cuenta algunas limitaciones metodológicas de los ensayos clínicos publicados, las pruebas científicas disponibles sugieren que estos agentes son útiles en el tratamiento del dolor del SII.
Fármacos dirigidos a controlar el dolor abdominal: antidepresivos tricíclicos y analgésicos viscerales
Los antidepresivos tricíclicos producen un efecto analgésico que se obtiene en dosis más bajas que las necesarias para el tratamiento de la depresión. Los mejores resultados se obtienen en el alivio del dolor del SII con predominio de diarrea. En un ensayo llevado a cabo con desipramina27 se demostró una disminución significativa de la frecuencia de las deposiciones, el dolor abdominal y la depresión, comparado con placebo y atropina. En otro estudio28, en el que los investigadores utilizaron trimipramina, se obtuvieron resultados similares.
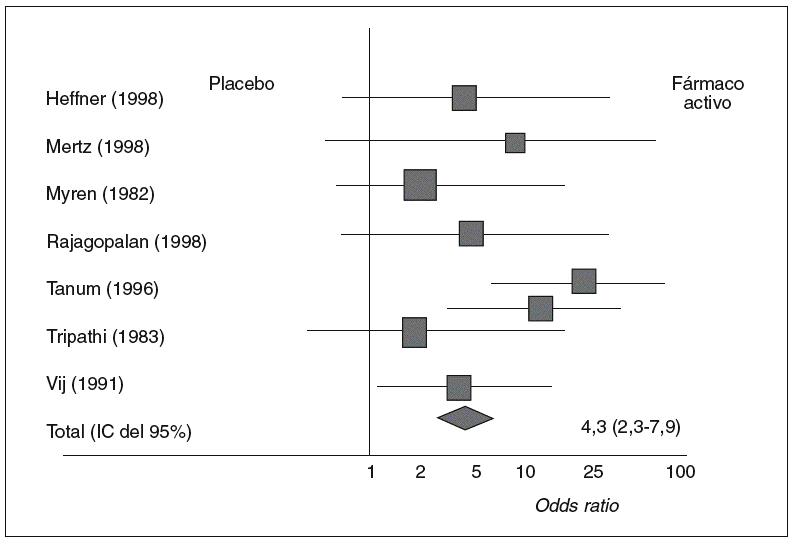
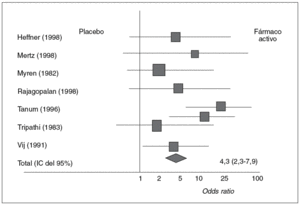
En un metanálisis29 de 11 ensayos aleatorizados, controlados, en los que se usaron antidepresivos para enfermedades gastrointestinales funcionales, incluidos 8 que evaluaron el SII, los investigadores pusieron de relieve una mejoría en uno de cada 3 pacientes (fig. 3). No obstante, es preciso tener en cuenta que estos agentes se asocian a efectos adversos (retención urinaria, xerostomía, etc.), lo que puede limitar su utilización en muchos pacientes. La desipramina y la nortriptilina provocan un menor número de efectos adversos que la imipramina y la amitriptilina.
Fig. 3. Metaanálisis de los resultados terapéuticos obtenidos con fármacos antidepresivos en el síndrome del intestino irritable. IC: intervalo de confianza. (Tomado de Jackson et al29.)
La investigación terapéutica también ha prestado atención a las nuevas moléculas capaces de modular la percepción visceral del trato gastrointestinal. La fedotozina, un agonista de los receptores kappa periféricos, ha sido evaluada en el tratamiento de pacientes con SII. En un ensayo llevado a cabo con este agente (3,5, 15 y 30 mg), los investigadores describieron que el grupo tratado con la dosis de 30 mg presentó una mejoría significativamente superior al placebo en el control del dolor abdominal, la distensión abdominal y la gravedad global de la enfermedad30. No obstante, debido a su beneficio clínico general escaso y a los supuestos efectos adversos, la fedotocina nunca se ha comercializado para su uso clínico.
Otros agentes, como la octreótida (un análogo de la somatostatina) y la leuprólida (un análogo de la hormona activadora del crecimiento), también podrían mejorar el dolor abdominal en algunos pacientes con SII. Un agonista *2-adrenérgico, la clonidina, disminuye la sensación de dolor durante la distensión del colon y aumenta la distensibilidad rectal en controles sanos y en pacientes con SII. No obstante, diversos problemas (vía de administración y efectos adversos) impiden su aplicación clínica. A su vez, la lidamidina (otro agonista *2) ha demostrado ser de escasa eficacia en el tratamiento del SII31,32.
Las taquiquininas (sustancia P, neuroquinina A y neuriquinina B) son mediadores fundamentales tanto para el control de la motilidad digestiva como para la transmisión de la información nociceptiva, en condiciones fisiológicas y en procesos de inflamación. En la actualidad, se están desarrollando estudios con antagonistas de los receptores NK2 (activados predominantemente por la neuroquinina A) y cuyo efecto es fundamentalmente analgésico33.
EN BUSQUEDA DE UN TRATAMIENTO PLURISINTOMATICO DEL SINDROME DEL INTESTINO IRRITABLE
Durante la última década, la búsqueda de tratamientos basados en los mecanismos fisiopatológicos del SII, y no sólo en los síntomas individuales, ha suscitado un gran interés34. En este contexto, el papel de la serotonina (5-HT) en el sistema nervioso entérico se ha convertido en una de las más importantes áreas de investigación. Es esencial destacar que alrededor del 95% de la serotonina se localiza en el tracto gastrointestinal, mientras que sólo un 5% está presente en el sistema nervioso central. En el sistema nervioso entérico se han identificado 2 vías diferentes de este neurotransmisor, con respuestas diferentes después de su estimulación. La vía intrínseca (mediada principalmente a través de receptores 5-HT4) participa en los reflejos peristálticos y en la secreción de iones y agua. La vía extrínseca (mediada principalmente por los receptores 5-HT3) se asocia con las sensaciones viscerales. Por consiguiente, este neurotransmisor desempeña un papel clave en, como mínimo, 2 de los mecanismos más importantes implicados en las manifestaciones del SII: motilidad intestinal anómala e hipersensibilidad visceral.
Antagonistas de los receptores 5-HT3 de la serotonina
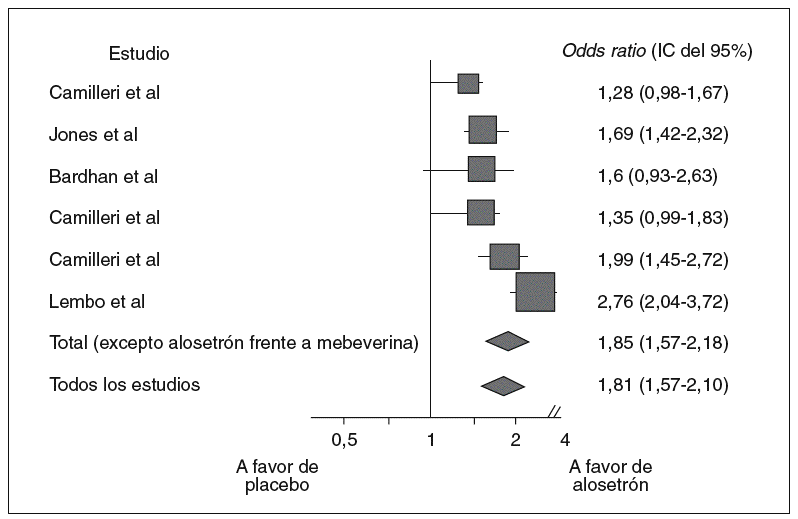
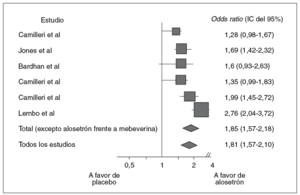
El antagonista 5-HT3 selectivo más evaluado en el SII ha sido alosetrón, que ha demostrado su capacidad para reducir el tránsito colónico y aumentar la absorción yeyunal de agua y sodio. En un ensayo35 llevado a cabo en 647 mujeres con SII sin estreñimiento, en el que los investigadores estudiaron el dolor abdominal, se demostró una mejoría en el 41% de las pacientes tratadas con alosetrón comparado con el 29% del grupo placebo. En un estudio similar36, llevado a cabo con 462 pacientes, se obtuvieron resultados equivalentes con diferencias significativas para alosetrón comparado con placebo en la reducción de la puntuación de diarrea y el aumento del número de días sin dolor. En la figura 4 se presentan los resultados de un metaanálisis de ensayos clínicos sobre alosetrón37. También se ha demostrado que alosetrón mejora significativamente la calidad de vida relacionada con la salud en mujeres afectas de SII con predominio de diarrea38. En una comparación efectuada de alosetrón con 2 agentes antiespasmódicos (mebeverina y trimebutina), los investigadores también demostraron diferencias significativas en favor de alosetrón en el control de la sintomatología relacionada con el síndrome39. Estos hallazgos propiciaron que este agente fuera el primero aprobado por la Food and Drug Administration para el tratamiento del SII con predominio de diarrea. No obstante, tras su comercialización, se observaron efectos adversos sustanciales, incluido el estreñimiento grave y la colitis isquémica40. Por estas razones, se retiró del mercado en marzo de 2001 aunque se reintrodujo nuevamente en Estados Unidos en noviembre de 2002. No obstante, para su utilización se han impuesto una serie de restricciones: sólo indicado en mujeres portadoras de SII con predominio de diarrea grave en las que han fracasado los tratamientos convencionales, formación y certificación obligatorias de los médicos responsables de su seguimiento, consentimiento informado por escrito de las pacientes y seguimiento cuidadoso del estreñimiento grave o la colitis isquémica.
Fig. 4. Metaanálisis de la eficacia de alosetrón en el tratamiento del síndrome del intestino irritable; se muestran los datos totales excluyendo e incluyendo el estudio de Jones et al, que utilizó mebeverina como tratamiento control. IC: intervalo de confianza. (Tomado de Cremonini et al37.)
Cilansetrón es otro antagonista muy específico y selectivo del receptor 5-HT3, significativamente superior a placebo en el alivio de los síntomas y la mejoría de la calidad de vida en varones y mujeres con SII y predominio de diarrea41-43. La aparición de algunos casos de colitis isquémica, todos ellos transitorios y sin complicaciones graves, ha hecho que se paralice su comercialización, y está pendiente de una nueva evaluación de la Agencia Europea de Evaluación de los Productos Médicos.
Agonistas de los receptores 5-HT4 de la serotonina
Tegaserod es un agonista parcial de los receptores 5-HT4 con un efecto procinético sobre el vaciado gástrico, que puede aumentar el tránsito colónico e intestinal. Estimula la secreción intestinal de agua y Cl, y disminuye la respuesta nociceptiva a la distensión rectal44. La eficacia de este agente se ha evaluado en diversos ensayos multicéntricos, aleatorizados, doble ciego45-48. Se ha documentado que alivia el dolor y la distensión abdominal, y aumenta la frecuencia de la deposición en mujeres con SII y predominio de estreñimiento. Tegaserod es bien tolerado, y sus efectos adversos referidos con más frecuencia son la diarrea y las cefaleas; la diarrea suele ser de carácter leve y transitorio.
Tegaserod está actualmente comercializado en más de 58 países, pero la Agencia Europea de Evaluación de los Productos Médicos aún no ha aprobado su comercialización en los países de la Unión Europea. Aun así, en Europa está disponible en Suiza.
¿SON NECESARIOS NUEVOS TRATAMIENTOS PARA EL SINDROME DEL INTESTINO IRRITABLE? ¿QUÉ BENEFICIOS SE BUSCA? ¿POR QUÉ NO SE DISPONE DE ELLOS?
Sin duda, se precisan nuevos tratamientos para los pacientes con SII y los motivos de esta necesidad son múltiples: los resultados conseguidos con los fármacos actuales distan de ser óptimos, los fármacos se han dirigido a aliviar síntomas individuales cuando el SII es un síndrome plurisintomático, hay manifestaciones clínicas muy frecuentes y molestas (p. ej., distensión abdominal) que quedan fuera del espectro de acción de los fármacos convencionales, un 20-30% de los pacientes padece un SII de intensidad media-grave que requiere tratamientos más potentes y específicos, y se necesitan «terapias de rescate» para los sujetos que no responden a los tratamientos convencionales.
Disponer de nuevos fármacos eficaces en el tratamiento del SII se acompañaría de importantes beneficios, como una mejor respuesta clínico-terapéutica, ganancia en la calidad de vida, mayor productividad, menor utilización de recursos, menor coste sanitario (directo e indirecto), etc.
Entonces, ¿por qué no se comercializan nuevos fármacos para el SII? La respuesta no es sencilla y abarca aspectos puramente científicos, como la falta de conocimiento de los mecanismos fisiopatológicos profundos del síndrome, y otros de tipo comercial (intereses económicos, precio de los fármacos, normativas de las agencias evaluadoras). El caso es que aun aceptando que el SII es un trastorno (¡una enfermedad!) muy frecuente, que altera de manera considerable la calidad de vida y que en ocasiones es grave, se sigue sin suscitar el interés suficiente como para desarrollar, aprobar y comercializar fármacos que podían ser útiles en estos pacientes.
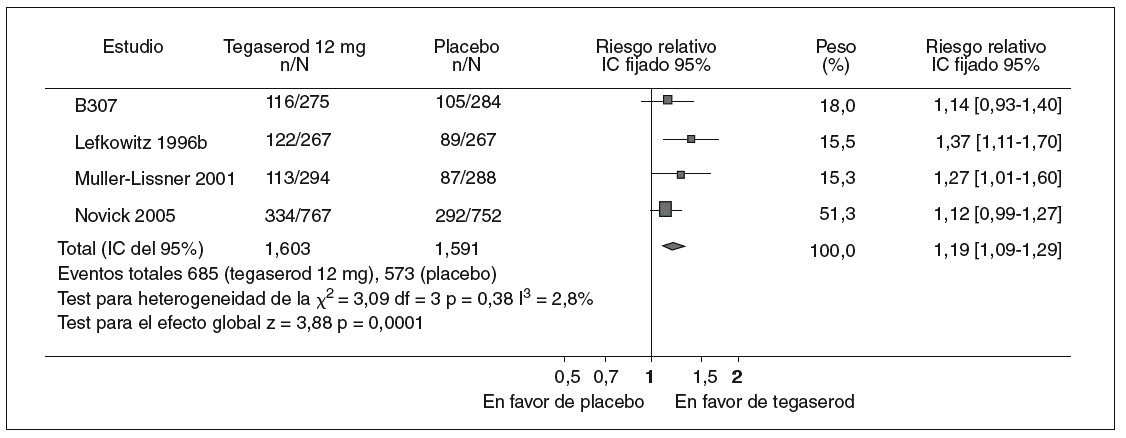
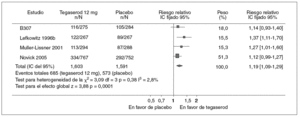
Al tratarse de una «enfermedad benigna» en la que no corre riesgo la vida de los pacientes, aunque son sometidos a cirugías abdominales innecesarias49 y el riesgo de suicidio está aumentado50, las agencias sanitarias evaluadoras exigen resultados de eficacia y seguridad difíciles de alcanzar en estos momentos. Sin embargo, tal como ocurrió con el caso de alosetrón en Estados Unidos, los pacientes reclaman nuevos tratamientos que les ayuden a mejorar su día a día. Es cierto que con los nuevos fármacos, como el tegaserod, la diferencia porcentual de pacientes que mejoran con respecto al placebo es del 15-20%, pero el número total de los que se benefician es de aproximadamente un 60%. Además, estas cifras, aunque no óptimas, ofrecen una esperanza a un determinado número de pacientes que ahora no la tienen (fig. 5).
Fig. 5. Metaanálisis de la eficacia de tegaserod 12 mg/día frente a placebo en la mejoría global de los síntomas en pacientes con síndrome del intestino irritable (Tomado de Evans et al. Cochrane Database Syst Rev. 2004;1:CD003960). IC: intervalo de confianza.
Con respecto a los efectos adversos, tema relacionado fundamentalmente con los antagonistas 5-HT3 y no con los agonistas 5-HT4, el problema podría pasar por una indicación restringida de los medicamentos, en casos seleccionados, con unas determinadas características cíclicas y criterios de gravedad. El estricto seguimiento de la posible aparición de estos efectos adversos, muy especialmente la colitis isquémicas, debería ser obligado.
En resumen, los pacientes con SII se cuentan por decenas de miles, muchos tienen afectada su calidad de vida a causa de la enfermedad (sí, la enfermedad), y aproximadamente un 15-20% padece un síndrome grave de difícil control terapéutico. Conocemos con mayor precisión los mecanismos fisiopatológicos y su relación con los síntomas, pero... los tratamientos que podemos ofrecer a nuestros pacientes siguen siendo los mismos ¡que hace 20 años!