El ser humano, único hospedador definitivo, contrae la teniasis por consumo de carne, cruda o poco cocinada, de cerdo o de vaca infectada con el cisticerco, que necesita entre 2 y 3 meses hasta convertirse en tenia adulta en el intestino1. En España, esta infección es autóctona, aunque de manera aislada y poco frecuente, por lo que no se considera un problema de salud pública, ya que se han detectado citas esporádicas a partir de casos importados procedentes de países de baja renta2,3.
En abril de 2015, a una niña de 8 años, natural de Valencia (España), se le observan unas estructuras blanquecinas en la ropa interior. Se le administra mebendazol a la dosis de 20mg/ml durante 4 días, repitiéndolo a las 2 semanas, por prescripción médica contra lombrices. En julio y en octubre de 2015, se repite dicho tratamiento sin desaparición de dichas estructuras. Se le receta metronidazol a la dosis de 125mg/5ml, 3 veces al día durante una semana. Como las estructuras persisten, se consulta a otro pediatra quien recomienda la administración de pirantel, a la dosis de 11mg/kg en dosis única durante 4 días y un análisis coprológico. El análisis de la niña se lleva cabo en noviembre de 2015, dando como resultado la parasitación por «tenia canina», Dipylidium caninum. El pediatra recomienda el tratamiento con niclosamida, o bien con praziquantel. La farmacéutica, por lo inusual del medicamento solicitado y al tratarse de un medicamento extranjero, la remite al Departamento de Parasitología de la Facultat de Farmàcia de la Universitat de València, donde se analizan 3 muestras fecales seriadas en el tiempo y 3 cintas de Graham en días consecutivos.
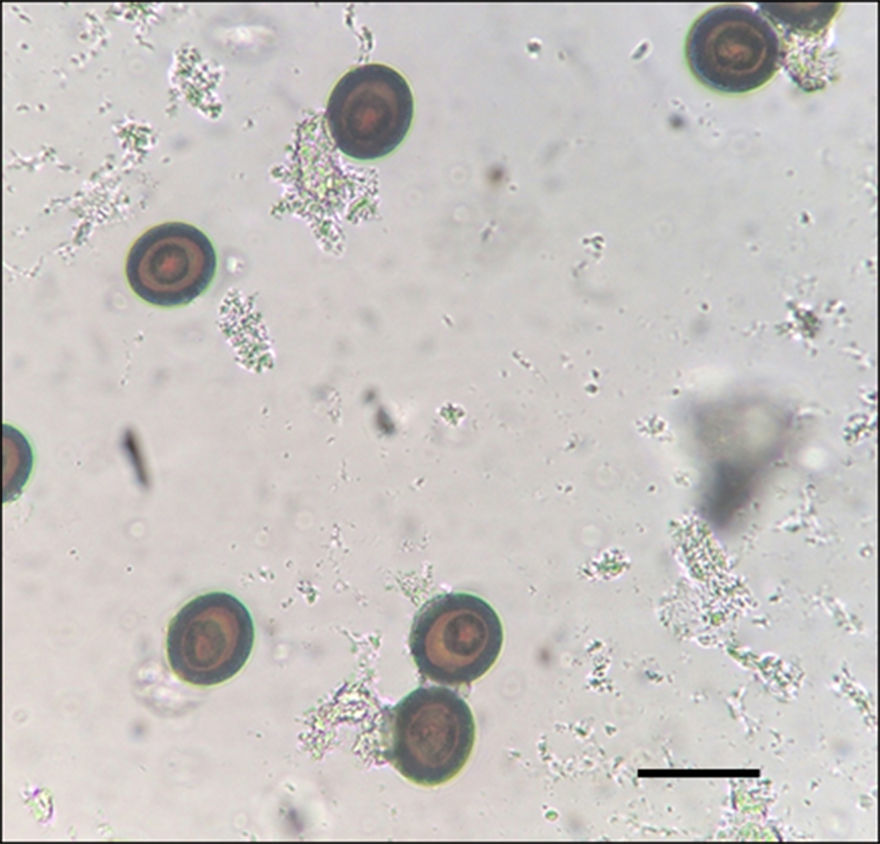
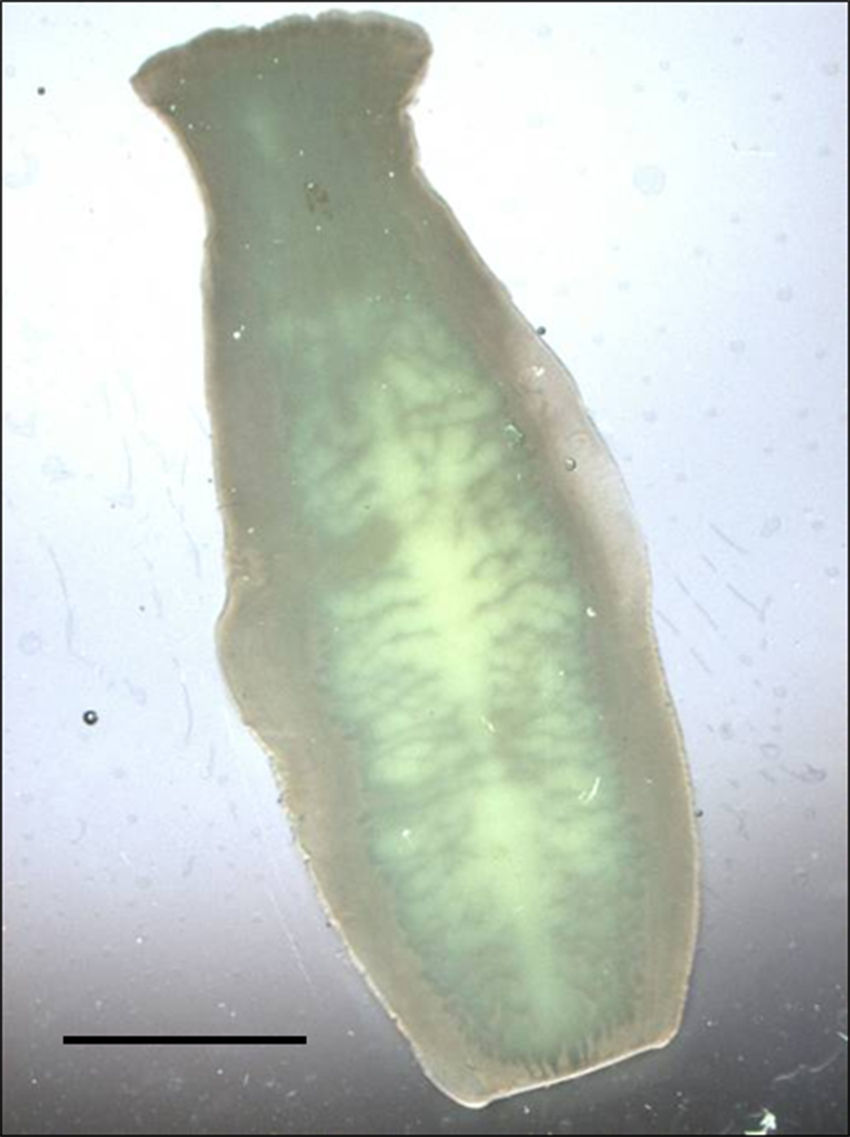
La observación macroscópica de varias estructuras blanquecinas aisladas, de aspecto alargado (11,4-13,7×4,0-4,4mm), fue sugestiva de proglótides de Taenia. En el examen de la materia fecal se evidenció la presencia de numerosos huevos esféricos, de 35,0-37,5μm de diámetro, con cubierta gruesa, de color pardo amarillento, que estaba estriada en forma radial y que contenía un embrión con 6 ganchos (hexacanto), llamado oncosfera. El test de Graham resultó negativo para huevos de oxiuro (Enterobius vermicularis), aunque se evidenció la presencia de numerosos huevos de Taenia (fig. 1). El análisis microscópico de un proglótide, montado con lactofenol de Amann entre 2 portaobjetos, constató la presencia de numerosas (más de 15) ramas laterales primarias a cada lado del eje uterino central (fig. 2), con la posición lateral del poro genital, lo que determinó el diagnóstico de Taenia saginata/Taenia asiatica. Los padres, y la gemela de la niña parasitada, no presentaron parasitación alguna. La administración oral de 50mg/kg de sulfato de paromomicina, dividida en 3 dosis/día, fue prescrita después de la identificación del cestodo en diciembre de 2015. Los controles parasitológicos fecales realizados en enero y febrero postratamiento resultaron negativos.
Los huevos en las heces sirven para adscribir al género Taenia. La adscripción específica pasa por el análisis de los proglótides grávidos, con tinciones permanentes o con lactofenol, para revelar el número de ramas laterales uterinas, o bien conocer si las proglótides han emergido espontáneamente del orifico anal o han sido eliminadas con las heces. Sin lugar a dudas, el caso que se aborda es T. saginata/T. asiatica, ya que ambas especies presentan las mismas características morfológicas4, requiriéndose el empleo de métodos moleculares para su diferenciación5-7.
La niña pudo haberse infectado durante su estancia en Francia, ya que los padres relatan un viaje en febrero de 2015, a visitar a sus abuelos, los cuales tienen la costumbre de comer steak tartar (carne cruda de ternera mezclada con yema de huevo crudo y especias). Este dato puede ser relevante a la hora de establecer la cadena epidemiológica del caso dado que el abuelo francés de la niña ya había sido tratado de teniasis 2 años antes. Además, la posible infección de la niña en Francia no sorprende debido a que se trata de un país en donde se estima una prevalencia anual media de teniasis humana del 0,11%8.
La ausencia de sintomatología por parte de la niña es un hecho constatado por los pacientes, ya que la patogenia de la teniasis es muy leve, con síntomas relacionados con dolor abdominal, distensión, diarrea, náuseas y anorexia9. La aparición de los proglótides en la ropa interior de la paciente se explicaría puesto que los de T. saginata/T. asiatica poseen movimiento propio, lo que les permite salir activamente sin necesidad de defecación. Cuando los proglótides se agrietan en su salida al exterior, los huevos pueden quedar adheridos a la zona perianal, lo que explicaría la detección de los mismos en la cinta de Graham.
El praziquantel (5-10mg/kg a dosis única) y la niclosamida (50mg/kg a dosis única, hasta un máximo de 2g) son los fármacos de elección10. El hecho de que ambos antiparasitarios son considerados como medicamentos extranjeros motivó utilizar el sulfato de paromomicina, ya que es un fármaco disponible en las farmacias11.
Cabe recordar que el simple hecho de aumentar el tiempo de cocción de la carne, o simplemente congelándola a –20¿C durante al menos 12h, sería suficiente para evitar la infección.
FinanciaciónProyecto N.o RD12/0018/0013, Red de Investigación Cooperativa en Enfermedades Tropicales-RICET, IV Programa Nacional de I+D+I 2008-2011, ISCIII-Subdirección General de Redes y Centros de Investigación Cooperativa y FEDER, Ministerio de Salud y Consumo, Madrid, España.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.