INTRODUCCIÓN
La insuficiencia hepática, ya sea aguda sin enfermedad hepática preexistente (fallo hepático fulminante [FHF]) o una descompensación aguda asociada a una hepatopatía crónica (insuficiencia hepática crónica agudizada [IHCA]) se asocia a una elevada mortalidad1. En pacientes con FHF, el trastorno en las funciones de síntesis y de detoxificación conlleva importantes complicaciones, que incluyen fallo renal, encefalopatía hepática, edema cerebral, hipotensión grave y aumento de la susceptibilidad a infecciones, y que finalmente derivan en fallo multiorgánico y la muerte2. El único tratamiento que ha demostrado una eficacia real en estos pacientes, y mejora las tasas de supervivencia, es el trasplante hepático (TH), si bien aproximadamente un tercio de estos pacientes fallece a la espera de un injerto3. Sin embargo, la insuficiencia hepática tanto aguda como crónica agudizada es potencialmente reversible, por lo que en los últimos años existe una importante actividad investigadora de cara al desarrollo de sistemas eficaces de soporte hepático artificial que permitan mejorar el pronóstico de estos pacientes (tabla I).
El desarrollo de estos sistemas se ha realizado en dos direcciones, los sistemas bioartificiales también llamados «hígado bioartificial», que pretenden sustituir todas las funciones del hígado sano y se basan en biorreactores que contienen hepatocitos vivos y funcionalmente activos, tanto humanos como porcinos, y por otro lado los sistemas extracorpóreos de detoxificación hepática que únicamente realizan funciones de detoxificación a través de distintas membranas y sorbentes4-6. Entre estos últimos se encuentra un nuevo sistema denominado MARS (Molecular Adsorbent Recirculating System) que es capaz de eliminar moléculas hidrosolubles y ligadas a la albúmina gracias a la biocompatibilidad y la selectividad de una nueva membrana de diálisis.
Características técnicas del sistema MARS
Este procedimiento se desarrolló la década pasada en Rostock (Alemania) y combina un equipo estándar de hemodiálisis o de hemofiltración, al que se adapta un circuito intermedio con albúmina humana a concentraciones del 10-20% y una membrana de polisulfona de alta selectividad, lo que permite la detoxificación selectiva tanto de productos tóxicos ligados a la albúmina como de sustancias hidrosolubles (tabla II)7-11.
El sistema utiliza una membrana que es capaz de simular las características biológicas de la membrana del hepatocito al transferir toxinas ligadas a proteínas y metabolitos tóxicos hidrofílicos desde el compartimiento sanguíneo del paciente al compartimiento de albúmina. Se trata de una membrana de diálisis de polisulfona perforada, cuya superficie de adsorción es de 2,2 m2 8,9 con unos poros que no permiten el paso de sustancias con un peso molecular mayor de 50 kD. Todas las sustancias hidrosolubles de bajo peso molecular, como el lactato, la creatinina y el amonio, pasan a través de los poros de la membrana, mientras que otras proteínas de mayor peso molecular, como las hormonas, los factores de coagulación y la antitrombina III, no lo hacen; esta selectividad permite mantener el equilibrio proteico del paciente, lo que no ocurre con otras técnicas de depuración extracorpórea.
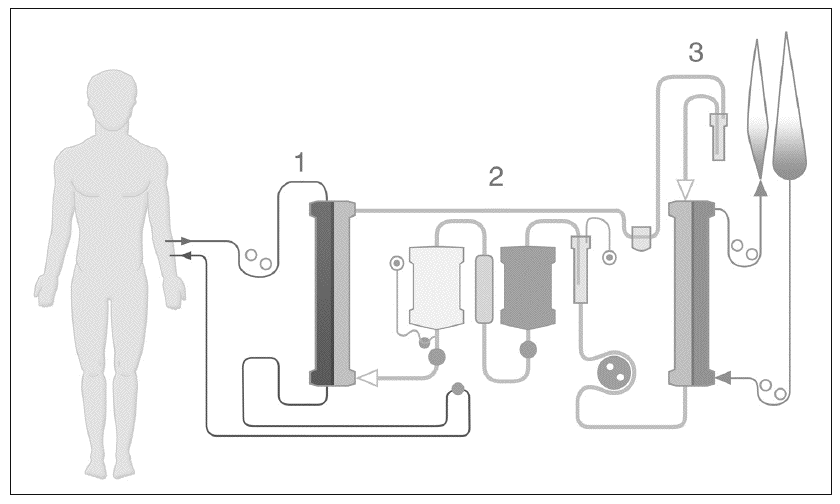
El sistema consta de 3 compartimientos o circuitos diferentes: circuito sanguíneo, circuito de albúmina y circuito de diálisis de bajo flujo (fig. 1). El circuito sanguíneo se conecta al paciente a través de un acceso venovenoso (catéter de doble luz) de forma que la sangre pasa a través de la membrana de diálisis de alto flujo (MARS® Flux, Teraklin AG, Rostock, Alemania) y a través de ésta se pone en contacto con la albúmina y se produce el intercambio de toxinas. El circuito de albúmina contiene 600 ml de albúmina al 20%. La albúmina del circuito cerrado pasa a través de una membrana de diálisis convencional de bajo flujo (diaFLUX®) donde se dializa y, posteriormente, por una columna de carbón activado y una segunda columna de resinas de intercambio aniónico donde se regenera. El paso progresivo de la albúmina por estas columnas permite eliminar las toxinas que se encuentran ligadas a sus receptores, con lo que se consigue que su recirculación sea efectiva. En el circuito de diálisis se eliminan las moléculas de menos de 30 kD y este circuito además añade las ventajas de la hemodiálisis al sistema MARS, al permitir realizar un correcto balance hidroelectrolítico y ultrafiltración si fuera necesario10.
Fig. 1. Esquema de los circuitos del sistema MARS: (1) sanguíneo, (2) albúmina, (3) diálisis.
Potenciales ventajas del sistema MARS y consideraciones clínicas
Comparado con los sistemas bioartificiales, el MARS es más sencillo de usar y relativamente menos caro. Las ventajas teóricas del sistema MARS son que permite la eliminación de toxinas ligadas a proteínas y toxinas hidrosolubles, simula el proceso de detoxificación de los hepatocitos, permite realizar un balance hidroelectrolítico y ácido-base, y controlar los valores de glucosa y lactato, tiene escasos efectos secundarios (menores que la diálisis y la hemofiltración), es coste-efectivo debido a que permite la recirculación de la albúmina, presenta alta biocompatibilidad, alta selectividad sin los riesgos asociados al componente biológico y es compatible con equipos estándar de diálisis.
La duración del tratamiento varía en función de la indicación y de la situación clínica del paciente, habitualmente se realizan tratamientos de 8 a 10 h/día en los pacientes hemodinámicamente estables (tratamientos intermitentes) y 24 h/día en pacientes inestables (normalmente dentro de unidades de cuidados intensivos). Para evitar la coagulación del circuito se utiliza heparina sódica en infusión continua (500-1.000 U/h) o epoprostenol ajustados según los parámetros de coagulación y plaquetas del paciente. Las indicaciones y contraindicaciones más habituales de este tratamiento se exponen en la tabla III.
El sistema MARS se tolera bien y no conlleva efectos adversos importantes, únicamente se ha descrito un descenso leve pero significativo del recuento de plaquetas durante el procedimiento que no parece asociarse a una mayor tasa de complicaciones hemorrágicas. Un factor a tener en cuenta es la aparición de complicaciones infecciosas, por lo que en pacientes con importante deterioro de la función hepática podría ser beneficiosa la profilaxis antibiótica.
Resultados clínicos de la terapia MARS
Hasta la fecha existen numerosas publicaciones del tratamiento MARS en una amplia variedad de afecciones, si bien la mayoría se trata de series prospectivas de casos por lo que sus resultados se deben interpretar con cautela, y son necesarios estudios controlados que evalúen su efecto en distintas indicaciones. En la actualidad se encuentran en marcha 2 ensayos clínicos multicéntricos, aleatorizados y controlados, uno en Europa que trata de evaluar el efecto sobre la supervivencia en pacientes con IHCA, y otro en Estados Unidos que está evaluando el efecto a corto plazo sobre la encefalopatía hepática. Además existe un registro internacional (MARS Registry) realizado por la Universidad de Rostock que contiene datos de más de 500 pacientes (aproximadamente sólo un 20% de los pacientes tratados)12.
Insuficiencia hepática crónica agudizada
La primera publicación de tratamiento MARS que incluye una serie amplia de pacientes con IHCA se realizó en el año 200013. En ésta se incluyó a 26 pacientes con hepatopatía avanzada, fundamentalmente alcohólica, que no habían respondido al tratamiento convencional. Presentaban una bilirrubina sérica superior a 15 mg/dl, 23 tenían encefalopatía hepática, 11 ascitis refractaria, 14 síndrome hepatorrenal y 23 infecciones de distintos tipos; se realizaron sesiones de MARS diarias o cada 48 h, en función de la situación clínica del paciente (media, 5,5 sesiones por paciente). Tras el tratamiento se objetivó una reducción significativa en los valores séricos de ácidos biliares y de bilirrubina además de mejoría de la encefalopatía hepática y del grado de Child-Pugh.
Posteriormente se han comunicado resultados similares de otros grupos que han tratado pacientes con IHCA14-29; se demostró una mejoría significativa de distintos parámetros bioquímicos, tanto de bilirrubina como de ácidos biliares y creatinina, así como descenso de la presión intracraneal, de la saturación del bulbo de la yugular, incremento de la presión arterial media y de las resistencias sistémicas, descenso en los valores séricos de renina plasmática y mejoría clínica, fundamentalmente neurológica.
En 2002 se publicó un estudio clínico prospectivo controlado30-32 en el que se incluyó a 24 pacientes con cirrosis de diversas etiologías que presentaron descompensación aguda por hemorragia digestiva, hepatitis aguda alcohólica o infecciones concomitantes. El objetivo primario del estudio era evaluar si el tratamiento con MARS mejoraba la cifra de bilirrubina y la encefalopatía hepática; la evaluación de la supervivencia a los 30 días fue un objetivo secundario. Los valores séricos de ácidos biliares y de bilirrubina descendieron una media del 43 y el 29%, respectivamente, en el grupo MARS después de una semana de tratamiento, pero no lo hicieron en el grupo control. También se produjo una mejoría de la insuficiencia renal y de la encefalopatía hepática y un aumento de la presión arterial media con el MARS. El tratamiento con MARS se asoció a una mejoría de la supervivencia a los 30 días (el 8,3% de mortalidad con MARS frente al 50% en los controles; p = 0,02). Hay que destacar que en este estudio se incluyó un grupo muy heterogéneo de pacientes de muy diversas etiologías (p. ej., un paciente con leptospirosis), que la muestra es pequeña (una muerte más en el grupo MARS no haría significativa esta diferencia; p = 0,09) y que evaluar la mortalidad no era el objetivo primario del estudio, por lo que los resultados deben avalarse con otros estudios más amplios.
Este año se ha publicado otro estudio aleatorizado y controlado, que incluye a 18 pacientes con IHCA de origen alcohólico, en el que se ha evaluado los efectos fisiopatológicos del tratamiento MARS en estos pacientes33. Tras tratar a 9 pacientes con MARS frente a 9 con tratamiento convencional, se objetivó una mejoría significativa de la encefalopatía hepática con MARS (p < 0,01), pero no en la función renal o en la presión arterial media. No se demostraron cambios en los valores de citocinas plasmáticas, de amonio ni de malondialdehído (como marcador de estrés oxidativo). Sin embargo, se demostró un descenso en los metabolitos del óxido nítrico (nitratos y nitritos) con MARS. La mortalidad intrahospitalaria fue la misma en los 2 grupos.
Otro ensayo clínico prospectivo, aleatorizado y controlado, analiza el efecto del MARS frente a la hemodiálisis convencional23 en pacientes con SHR tipo I. Los 13 pacientes presentaban oligoanuria o anuria y un sodio urinario por debajo de 20 mmol/l, a pesar de tener un adecuado volumen intravascular. La tasa de mortalidad a los 7 días fue del 100% en el grupo de hemodiálisis convencional y del 62,5% en el grupo MARS (el 75% a los 30 días) (p < 0,01). Hay que destacar que en los criterios de inclusión, la definición de síndrome hepatorrenal (SHR) incluía oliguria y concentraciones bajas de sodio urinario, pero no seguía la definición propuesta por el Club Internacional de la Ascitis34, por lo que probablemente se excluyó a algunos pacientes que cumplían criterios de SHR tipo I. Así, los pacientes de este estudio constituyen un subgrupo de especial gravedad y por tanto son los más difíciles de tratar, lo que puede explicar el hecho de que la mortalidad en el grupo control sea muy superior a la observada en otros trabajos. Además, el número de pacientes es muy pequeño y no se ha utilizado el tratamiento específico recomendado para esta afección (terlipresina, albúmina, TIPS). Otros estudios posteriores, aunque no controlados, en pacientes con SHR19-21 también han demostrado que tras el tratamiento MARS se produce un incremento de la presión arterial media, mejoría de la ascitis, de la encefalopatía hepática, del grado de Child-Pugh y de la oliguria presentes al inicio del estudio.
Fallo hepático agudo
El FHF es la forma más grave de fallo hepático agudo, y se asocia a una elevada mortalidad. La recuperación espontánea del hígado en estos casos puede darse hasta en un 30-40%, lo que dependerá de la etiología de base. Sin embargo, clínicamente es difícil determinar la función residual hepática en estos pacientes y la probabilidad de regeneración espontánea. Debido a esta variabilidad, el efecto del MARS en el curso del FHF puede ser impredecible. La recuperación del hígado puede deberse a la historia natural de la enfermedad en ese paciente en particular y no al efecto del MARS. Por lo tanto, son necesarios amplios estudios prospectivos, aleatorizados y controlados para responder a esta pregunta fundamental. Parece que el MARS podría ser una herramienta útil en estos pacientes cuando se analizan parámetros clínicos, hemodinámicos y analíticos, al posibilitar la estabilización del paciente hasta el TH. En el fallo hepático agudo se recomienda realizar tratamientos continuos, una vez estabilizada la situación clínico-hemodinámica del paciente, tratamientos intermitentes.
En un estudio piloto no controlado, de fase I, se evaluó el tratamiento MARS en 9 pacientes que presentaban fallo hepático agudo candidatos a trasplante hepático urgente (5 pertenecían al estadio UNOS I y 4 al UNOS IIA)35. La duración media de las sesiones MARS fue de 73,2 ± 12,2 h. El procedimiento se toleró bien en todos los pacientes y se objetivó un descenso significativo de los valores de amonio y creatinina, mejoría del grado de encefalopatía hepática e incremento del índice de Fisher (cociente entre aminoácidos ramificados y aromáticos). Además se produjo un incremento significativo del factor VII de la coagulación como marcador de síntesis hepática. De los pacientes UNOS I, uno recuperó la función hepática inicial y 3 fueron trasplantados. En otro centro en el que se realizó MARS en pacientes con fallo hepático fulminante36, 4 pudieron ser trasplantados gracias a este soporte, y se confirmó el descenso significativo de los valores de amonio sérico y bilirrubina y la mejoría neurológica.
En otro estudio prospectivo controlado, en pacientes con fallo hepático hiperagudo, se objetivó una tendencia a la normalización de la hemodinámica sistémica y un descenso en el consumo de oxígeno en pacientes tratados con una sesión de MARS37.
Se han comunicado también varios casos de «enfermedad de Wilson» de presentación fulminante38-41 tratados inicialmente con MARS y posteriormente trasplantados con éxito (intervalo de tratamiento de 4 a 28 días). Se objetivó un descenso significativo de los valores de cobre sérico, bilirrubina y amonio, así como mejoría de la función renal y de la situación neurológica. Los descensos más significativos de los valores de cobre sérico se produjeron en las primeras 4 h de tratamiento.
También se han tratado con MARS, asociado al tratamiento convencional, varios pacientes con FHF debido a intoxicación aguda por paracetamol38,42-44, envenenamiento por setas, fundamentalmente Amanita phalloides38,45-47, intoxicación por fenitoína48 y casos anecdóticos de pacientes con síndrome de Budd-Chiari de presentación aguda38 y amiloidosis (fiebre mediterránea familiar)24.
Pacientes con trasplante hepático
No existen muchos datos en la bibliografía médica de pacientes con TH tratados con MARS. Teóricamente podría ser útil al favorecer la recuperación completa del injerto, con lo que se podría evitar el retrasplante, o bien al mejorar parámetros clínicos, bioquímicos y hemodinámicos del paciente previamente a éste. Se han descrito tratamientos en pacientes con disfunción del injerto14,36,38, con incremento de la presión intracraneal24,35,49, o bien en trasplantes que presentan colestasis intrahepática progresiva14,18,35,36. Otro problema que se plantea en estos pacientes es la monitorización estrecha de los valores de fármacos inmunodepresores ya que podrían verse reducidos con la diálisis de albúmina.
Existe alguna experiencia de tratamiento MARS en pacientes con disfunción primaria del injerto después de la utilización de un segmento resultado de la partición hepática (trasplante Split). En un centro en el que se realizó tratamiento MARS en 4 pacientes con disfunción primaria del injerto y colestasis, 3 se recuperaron y 1 fue retrasplantado con éxito50. En otro centro, se trató a un niño que presentó disfunción tras un trasplante segmentario51, y permitió la estabilización hasta el retrasplante 2 semanas después. De otros 6 pacientes con disfunción primaria del injerto y bilirrubina superior a 15 mg/dl tratados, 5 se recuperaron sin necesidad de retrasplante, y se objetivó mejoría neurológica y del INR con descenso del amonio y de la bilirrubina36.
Prurito intratable en síndromes colestásicos crónicos
El prurito es un síntoma frecuente y muy invalidante en pacientes con colestasis, fundamentalmente en síndromes colestásicos crónicos (cirrosis biliar primaria, colangitis esclerosante primaria, colestasis intrahepática benigna recurrente o atresia biliar). Tiene un impacto negativo en la calidad de vida de estos pacientes y puede llevar incluso al suicidio, de forma que en ocasiones es indicación de TH independientemente de otros datos de insuficiencia hepática. El prurito leve suele responder al tratamiento con resincolestiramina. Otros tratamientos propuestos incluyen fármacos inductores del sistema microsomal hepático, como el fenobarbital y la rifampicina, agentes antihistamínicos, dosis subhipnóticas de propofol, ondansetron y antagonistas opiáceos como la naloxona y la naltrexona. En ocasiones se recurre a la terapia fotodinámica y hay casos descritos de prurito intratable tratado con hemoperfusión con carbón activado, plasmaféresis e incluso bypass ileales. Desde la aparición del MARS se ha postulado su potencial capacidad para eliminar algunas sustancias, todavía no bien identificadas, que se acumulan en la colestasis a consecuencia de una excreción biliar defectuosa, lo que puede mejorar el prurito en estos pacientes.
Todavía existe poca experiencia de tratamiento en este grupo de pacientes, aunque ya se han publicado algunas series con buenos resultados, incluso en pacientes trasplantados52-56. La tolerancia al tratamiento es buena, si bien el efecto parece ser transitorio y varía de unos pacientes a otros.
Otras indicaciones
También se ha utilizado el sistema MARS en el tratamiento de pacientes con colestasis tras fallo cardíaco o cirugía cardíaca57 y en pacientes en lista de espera para trasplante cardíaco que presentan fallo ventricular derecho, debido a su capacidad de elevar la presión arterial media y las resistencias vasculares sistémicas58. Recientemente, se ha publicado un estudio prospectivo, aleatorizado y controlado que compara el tratamiento MARS (n = 14) frente al tratamiento médico estándar (n = 13), en pacientes que presentan fallo hepático por bajo gasto tras shock cardiogénico en la cirugía cardíaca59. La supervivencia en el grupo MARS fue del 50% frente al 32% en el grupo control, diferencia que no llegó a ser estadísticamente significativa. A pesar de tratarse de un grupo pequeño de pacientes, estos resultados podrían ser alentadores y deberían realizarse estudios con mayor número de pacientes.
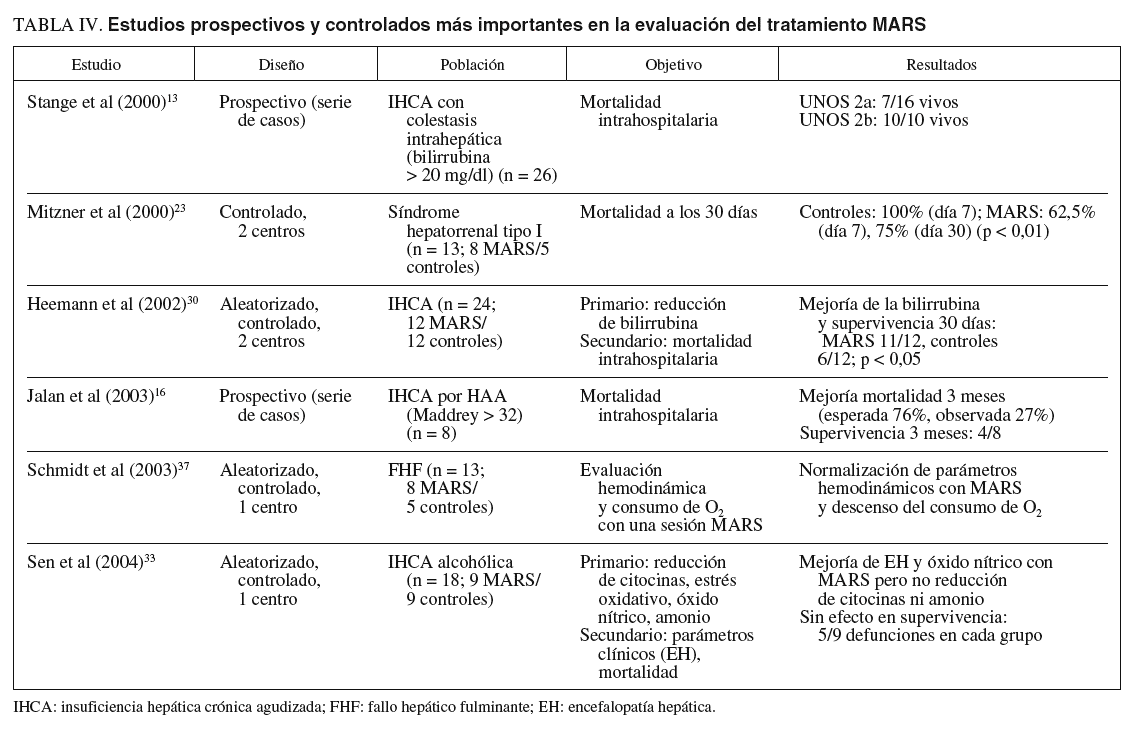
Un reciente metaanálisis ha evaluado el efecto del MARS en la supervivencia de pacientes con FHF e IHCA60. Tras un análisis detallado de la bibliografía existente hasta la fecha, únicamente se incluyeron 4 estudios aleatorizados y controlados, con un total de 67 pacientes y 2 estudios no aleatorizados (61 pacientes) para un posterior subanálisis. El MARS no parece reducir la mortalidad al compararse con el tratamiento estándar (riesgo relativo [RR] = 0,56; intervalo de confianza [IC] del 95%, 0,28-1,14; p = 0,11). La inclusión de los 2 estudios no aleatorizados sí parecía mejorar la supervivencia (RR=0,36; IC del 95%, 0,17-0,76; p = 0,007). Sin embargo, dado el escaso número de pacientes incluidos, es posible que la validez de las conclusiones sea limitada, por lo que son necesarios más ensayos adecuadamente diseñados para definir finalmente el papel del MARS en el tratamiento de pacientes con insuficiencia hepática. En la tabla IV se resumen los estudios más significativos del tratamiento con MARS.
Efectos clínicos de la terapia MARS
Aunque hasta la fecha no dispongamos de estudios que evalúen correctamente el efecto del MARS sobre la supervivencia de los pacientes con insuficiencia hepática, sí disponemos de datos que avalan su efecto favorable sobre distintos parámetros clínicos, entre los que se incluyen:
Situación hemodinámica sistémica y esplácnica
Los pacientes tratados con MARS presentan un incremento significativo de la presión arterial media y de las resistencias vasculares sistémicas junto con un descenso del gasto cardíaco y del gradiente de presión venosa hepática23,25,61.
Función cerebral
Se ha demostrado la mejoría del grado de encefalopatía hepática, tanto en el FHF como en la IHCA, el aumento del índice de Glasgow, el descenso de la presión intracraneal y del contenido de agua cerebral y el incremento del flujo sanguíneo cerebral14,17,19. Es importante destacar que en el último congreso de la AASLD se presentaron los resultados preliminares del ensayo multicéntrico que se está llevando a cabo en Estados Unidos sobre la influencia del MARS en la evolución de la encefalopatía hepática, y se demostró que éste mejora significativamente y de una forma más rápida la encefalopatía hepática grados 3 y 4 en comparación con el tratamiento médico estándar62.
Función hepática
En algunos estudios se ha documentado una mejoría de los parámetros de síntesis hepática (factor VII, actividad de protrombina, antitrombina III, colinesterasa y albúmina). Además el tratamiento MARS parece mejorar la ascitis y el índice de Child-Pugh23,35,36.
Función renal
El MARS produce un descenso significativo de los valores de urea y de creatinina, incrementa la diuresis y parece mejorar el SHR16,23.
Conclusiones
El escaso número de estudios controlados y con un pequeño número de pacientes disponibles hasta la fecha no permite evaluar correctamente los beneficios del tratamiento con diálisis de albúmina (MARS). Sin embargo, este tratamiento tiene evidentes efectos clínicos, biológicos y hemodinámicos, tanto en pacientes con insuficiencia hepática aguda como crónica. Estos resultados son estimulantes y abren la posibilidad de disponer de un procedimiento que permita la recuperación transitoria o definitiva de algunas de las funciones de detoxificación del hígado lesionado. Además, este procedimiento podría contribuir a un mejor conocimiento de las bases fisiopatológicas de la IHCA. Sin embargo, son necesarios más estudios controlados y metodológicamente correctos que permitan establecer claramente las indicaciones de este procedimiento y su efecto sobre la supervivencia.