INTRODUCCIÓN
El síndrome de Crigler-Najjar es una forma de ictericia familiar, de transmisión autosómica recesiva, producida por un déficit congénito de la bilirrubina-uridinadifosfato glucuronosiltransferasa (B-UGT). Esta rara enfermedad, descrita por Crigler y Najjar1 en 1952, se produce por un trastorno de la conjugación de la bilirrubina debido a mutaciones en el gen UGT1A1, situado en el cromosoma 2 y que codifica la B-UGT. Afecta a uno de cada millón de recién nacidos. Existen 2 tipos con diferente pronóstico: el síndrome de Crigler-Najjar tipo I, debido a una mutación homocigota del gen UGT1A1, en el que se produce una ausencia total de B-UGT y que tiene muy mal pronóstico, y el tipo II, debido a una mutación distinta de ambos alelos del gen UGT1A1 (heterocigotos compuestos), en el que existe un déficit casi absoluto de B-UGT y que goza de mejor pronóstico.
El síndrome de Gilbert, descrito en 19012, es la más común de las hiperbilirrubinemias no conjugadas familiares no hemolíticas y se debe a una mutación del promotor del gen UGT1A1. Tiene una escasa repercusión clínica, un buen pronóstico y comparte con el síndrome de Crigler-Najjar un déficit del sistema glucuroniltransferasa, responsable de la conjugación de la bilirrubina.
HISTORIA NATURAL Y FISIOPATOLOGÍA
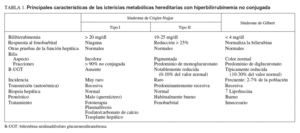
Crigler y Najjar describieron los 7 primeros pacientes con formas graves de ictericia congénita no hemolítica, con concentraciones de bilirrubina de 25-35 mg/dl. Seis de ellos fallecieron en la infancia por encefalopatía bilirrubínica o querníctero1. En 1962, Arias3 descubre la existencia de 2 formas de síndrome de Crigler-Najjar, pero no es hasta 1969 cuando el equipo de este mismo autor4 estudia la excreción de bilirrubina conjugada en la bilis y la respuesta al fenobarbital en 16 pacientes con síndrome de Crigler-Najjar y observan 2 tipos de comportamientos. El denominado tipo I, en pacientes que no responden al fenobarbital y que carecen de evidencia de trazas de bilirrubina conjugada en la bilis, es una forma habitualmente letal en la infancia, y el tipo II, o síndrome de Arias, se da en los pacientes con respuesta al fenobarbital y en los que sí se observan trazas de glucuronato en la bilis aunque, contrariamente a lo que sucede en los individuos normales, con predominio de monoglucuronato en lugar de diglucuronato. Estos autores constatan que, si bien la mayoría de los pacientes con síndrome de Crigler-Najjar tipo II llegan a la edad adulta, algunos también fallecen por querníctero. En el tipo II la hiperbilirrubinemia es menos grave, oscilando entre 10 y 25 mg/dl, y la presencia de glucuronatos en la bilis indica que estos pacientes tienen una cierta actividad de glucuronoconjugación de la bilirrubina que puede incrementarse con el uso de algunos inductores enzimáticos (tabla I).
MANIFESTACIONES CLÍNICAS Y BIOQUÍMICAS
Síndrome de Crigler-Najjar tipo I
Se caracteriza por una gran elevación de la bilirrubina no conjugada del suero, hasta concentraciones superiores a 20 mg/dl, que aparece en el período neonatal y que persiste de por vida. Otras pruebas bioquímicas hepáticas como las transaminasas y las fosfatasas alcalinas son normales y no existe evidencia de hemólisis. No se acompaña de coluria. La biopsia hepática muestra una histología esencialmente normal. No se detecta actividad enzimática B-UGT en el tejido hepático. La falta de respuesta a inductores enzimáticos como el fenobarbital o la difenilhidantoína hace que la bilirrubina se acumule en el plasma. Sin tratamiento se origina querníctero y el fallecimiento en el primer año de vida.
Síndrome de Crigler-Najjar tipo II
También se manifiesta por una ictericia secundaria a hiperbilirrubinemia no conjugada, de inicio neonatal, sin otras alteraciones bioquímicas. La ictericia es de menor intensidad que en el tipo I, con cifras de bilirrubina que oscilan entre 10 y 25 mg/dl. Suele ser poco sintomática y la mayoría de pacientes alcanza la edad adulta5, pero la ictericia persistente puede ocasionarles problemas en sus relaciones sociales.
Es infrecuente que se produzca querníctero, aunque se han descrito episodios de encefalopatía reversibles o reagudizaciones hiperbilirrubinémicas coincidiendo con enfermedades intercurrentes. En ocasiones, pacientes con síndrome de Crigler-Najjar tipo II leves son clínicamente difíciles de distinguir de casos de síndrome de Gilbert6.
DIAGNÓSTICO
El diagnóstico de síndrome de Crigler-Najjar debe sospecharse en todo paciente que presente cifras elevadas de bilirrubina, superiores a 4 mg/dl, con predominio de la fracción no conjugada, una vez que se haya descartado la existencia de hemólisis mediante la determinación de reticulocitos, lactatodeshidrogenasa y haptoglobina, de una hepatopatía crónica a partir de la exploración clínica y ecográfica, y también cuando el resto de pruebas hepáticas, incluidas transaminasas y enzimas de colestasis, sean normales. Los pacientes con síndrome de Gilbert mantienen cifras de bilirrubina no conjugada que no suelen superar los 4 mg/dl. Cuando un paciente presenta de forma aislada cifras elevadas de bilirrubina no conjugada en la edad adulta, en ausencia de hemólisis, hemos de sospechar que se trata de un síndrome de Crigler-Najjar tipo II, ya que los que presentan el tipo I suelen fallecer en la infancia si no reciben un trasplante.
El diagnóstico de seguridad del síndrome de Crigler-Najjar debería establecerse mediante la detección de las mutaciones del gen UGT1A1, que codifica la B-UGT, por aislamiento de ADN7-9 de leucocitos del paciente, pero esta prueba está sólo al alcance de centros especializados. En la práctica se utilizan criterios clínicos.
TRATAMIENTO
Síndrome de Crigler-Najjar tipo I
El tratamiento está orientado a conseguir concentraciones de bilirrubina indirecta o no conjugada por debajo de 20 mg/dl y a evitar la muerte por querníctero o las secuelas permanentes de éste.
La fototerapia, preferentemente con luz azul, que tiene una longitud de onda entre 420 y 460 nm, durante 12 h diarias es efectiva porque rompe los enlaces internos de hidrógeno de la bilirrubina no conjugada convirtiéndola en un fotoisómero hidrosoluble que se excreta en la bilis. No obstante, una vez dentro del intestino se vuelven a recomponer los enlaces y la bilirrubina convertida de nuevo en bilirrubina no conjugada puede ser reabsorbida por el intestino mediante difusión pasiva. Para prevenir esta reabsorción de bilirrubina se ha propuesto la utilización de quelantes que se unen a ella, como el fosfato de calcio, con el objetivo de incrementar la eficacia de la fototerapia. En un estudio controlado, doble ciego y cruzado Van der Veere et al10 evaluaron la utilidad de la administración oral de fosfato y carbonato cálcicos en 11 pacientes, 5 con síndrome de Crigler-Najjar tipo I, que además recibían fototerapia, y 6 con síndrome tipo II tratados con fenobarbital. El estudio demostró un descenso modesto aunque significativo (del 18%) de las cifras de bilirrubina sérica en los pacientes con síndrome de Crigler-Najjar tipo I, pero no en los del tipo II, y los autores concluyen que la administración oral de fosfato cálcico puede ser un tratamiento adyuvante a la fototerapia.
Se han utilizado otros quelantes de la bilirrubina como la colestiramina, que también reduce su circulación enterohepática, pero debido a su mal sabor, junto con problemas de malabsorción, no se ha generalizado su uso. En el período neonatal también se ha combinado la fototerapia y la exanguinotransfusión. Pasado el primer año de vida, y durante los episodios de gran elevación de la bilirrubina, se han utilizado conjuntamente fototerapia y plasmaféresis, o únicamente ésta11, para conseguir descensos rápidos de las cifras de bilirrubina.
La fototerapia no es un tratamiento exento de problemas. Son necesarias 12 h diarias (por lo que se ha propuesto su administración nocturna), el tratamiento pierde su eficacia con el tiempo al disminuir el cociente superficie corporal/peso, es incómoda de soportar y con la edad también disminuye su cumplimiento12. La intensidad del tratamiento favorece la aparición de efectos secundarios. La piel es frágil, se lesiona fácilmente y está muy pigmentada. La fototerapia prolongada puede producir asimismo daño en el ADN de las células expuestas y este efecto se incrementa por la bilirrubina13. En el tipo I el tratamiento definitivo en la actualidad es el trasplante hepático, que debe realizarse antes de que exista lesión neurológica12,14, particularmente en aquellas circunstancias en que no puede garantizarse un tratamiento bien hecho de fototerapia12. Se ha descrito de forma aislada el trasplante de hepatocitos, pero el efecto de esta técnica puede ser limitado15. La genoterapia puede ser una opción lógica y realista ante una enfermedad metabólica con alteración genética identificada en pacientes que tienen un hígado morfológicamente normal. Esta posibilidad terapéutica en estos momentos todavía se encuentra en fase experimental16,17.
Síndrome de Crigler-Najjar tipo II
Se utiliza la fototerapia en los primeros meses de vida, de 6 a 12 h diarias, especialmente cuando la bilirrubinemia es elevada (cercana a 15 mg/dl). También puede emplearse, con las limitaciones e inconvenientes citados, en la edad adulta. Sin embargo, en el tipo II el tratamiento de elección es la administración de fenobarbital a dosis de 1-2 mg/kg/día, lo que equivale a dosis entre 50 y 150 mg/día en niños y adultos, respectivamente. En lactantes puede utilizarse la dosis inicial de 4-6 mg/kg/día. Con este tratamiento, que debe ajustarse según la respuesta, se pueden reducir los valores de bilirrubina en un 25-30%. Se indica incluso, por motivos cosméticos, en pacientes con concentraciones poco elevadas de bilirrubina. En el tipo II es infrecuente que se produzca querníctero, aunque se han descrito episodios de encefalopatía reversibles coincidiendo a menudo con otras enfermedades intercurrentes, ayuno u otros factores que temporalmente eleven la concentración de bilirrubina y reduzcan la albúmina sérica. El fenobarbital es un inductor enzimático, incrementa la actividad de la B-UGT favoreciendo la conjugación de la bilirrubina y mejora también el flujo biliar18. Este fármaco es totalmente ineficaz en el síndrome de Crigler-Najjar tipo I. En el tipo II debe intentar administrarse a la mínima dosis que sea capaz de mejorar los síntomas del paciente. Una única dosis suele ser suficiente en la mayoría de los casos para realizar el tratamiento de mantenimiento y su administración nocturna reduce los efectos secundarios de sedación y somnolencia propios del fármaco. Aunque con el fenobarbital no es posible conseguir cifras normales de bilirrubina, debe intentar conseguirse cifras de bilirrubinemia en torno a los 5 mg/dl. Las dosis de fenobarbital anteriormente referidas, que se utilizan crónicamente en esta enfermedad, suelen tolerarse bien y no afectan a la vida cotidiana o al trabajo, una vez pasados los primeros días y cuando se han ajustado. No es necesario monitorizar las concentraciones de fenobarbital, como sucede en la epilepsia, ya que el ajuste de la dosis depende del efecto clínico y bioquímico de reducción de la bilirrubinemia con la mínima dosis posible.
La asociación de fenobarbital y fototerapia se ha comunicado como un tratamiento seguro para proteger al feto en los 2 embarazos de una paciente afectada de síndrome de Crigler-Najjar tipo II19. Quizá la fototerapia pueda ser también una técnica a tener en cuenta en situaciones de mala respuesta o intolerancia al fenobarbital, o en reagudizaciones de la enfermedad, administrada sola o asociada a quelantes de la bilirrubina no conjugada, como se demostró en pacientes con síndrome de Crigler-Najjar tipo I10.