La pustulosis exantemática aguda generalizada (PEAG) engloba un subgrupo de erupciones, caracterizadas por la aparición de numerosas pústulas estériles sobre un fondo eritematosoedematoso. Generalmente, son inducidas por fármacos y sus características indican un trasfondo inmunológico. El tratamiento consiste en la supresión del fármaco responsable. En general, el pronóstico es bueno, y la lesión cutánea se resuelve en unos pocos días, con su peculiar descamación.
Presentamos 3 casos de PEAG inducidos por omeprazol, un fármaco con un excelente perfil de seguridad, entre cuyos efectos secundarios se han descrito varios tipos de lesiones cutáneas, sin que hayamos encontrado en la revisión bibliográfica ninguna referencia a casos de PEAG por este fármaco. La PEAG relacionada con otros inhibidores de la bomba de protones es excepcional.
Acute generalized exanthematous pustulosis (AGEP) comprises a group of eruptions characterized by several small sterile pustules over an erythematousedematous skin. These eruptions are usually drug induced and show some characteristics that suggest an immunologic background. Treatment is based on withdrawal of the drug causing the eruption. Prognosis is generally good and the skin lesions usually resolve in a few days with characteristic postpustular pinpoint desquamation.
We report three cases of AGEP induced by omeprazole, a drug with a good safety profile. Some adverse cutaneous reactions have been described as secondary effects. However, to our knowledge, no cases of omeprazole-induced AGEP have previously been reported. AGEP related to other proton pump inhibitors is exceptional.
En 1980, Beylot et al acuñaron el término pustulosis exantemática aguda generalizada (PEAG) para designar un subgrupo de erupciones pustulosas que se desarrollan sobre la piel edematosa y eritematosa, iniciándose mayoritariamente en la cara o las zonas de los pliegues. Se caracterizan por la aparición de numerosas pústulas puntiformes, estériles, no foliculares, que cursan con prurito y quemazón y, ocasionalmente, confluyen simulando un signo de Nikolsky positivo. La afectación mucosa ocurre aproximadamente en el 20% de los casos, y con frecuencia se limita a una localización (generalmente oral). Los síntomas cutáneos se acompañan casi siempre de fiebre (38 oC) y leucocitosis neutrofílica, en ocasiones con una ligera eosinofilia. La histopatología típica muestra pústulas subcórneas y/o espongiformes intraepidérmicas, y a menudo un notable edema de la dermis papilar con infiltrados perivasculares de neutrófilos y algún eosinófilo. Las pústulas se resuelven espontáneamente en 4-10 días, con una característica descamación en collarete. La gran mayoría de los casos de PEAG son inducidos por fármacos, especialmente antibióticos, y son excepcionales los casos atribuidos a la administración de inhibidores de la bomba de protones (IBP). Presentamos 3 casos de PEAG desarrollados en el contexto de tratamientos con omeprazol.
OBSERVACIÓN CLÍNICACaso 1Mujer de 89 años de edad, sin alergias conocidas, con hipertensión, diabetes mellitus, hipertiroidismo, colecistolitiasis y antecedentes de adenocarcinoma de colon y trombosis venosa profunda, complicada con tromboembolia pulmonar 7 años antes. No presentaba hábitos tóxicos. En tratamiento con trandolapril, insulina, carbimazol, acenocumarol, bromazepam, pantoprazol y paracetamol.
Ingresó desde el servicio de urgencias por un cuadro de malestar general y episodio sincopal, refiriendo dolor en la fosa ilíaca izquierda y tendencia al estreñimiento en las últimas semanas. En la exploración física mostraba una presión arterial (PA) de 130/70 mmHg, una frecuencia cardíaca (FC) de 75 lat/min, una temperatura de 37 oC, un aceptable estado general, un buen estado de hidratación y palidez cutaneomucosa, y a la palpación, un ligero dolor en el hemiabdomen izquierdo, sin signos de irritación peritoneal. El resto de la exploración fue normal. En la analítica destacaba una anemia (hematocrito del 22%) ligeramente microcítica e hipocrómica, una leucocitosis (17.300/μl) con desviación izquierda, y una hiperamilasemia (735 U/l); el resto de la bioquímica, los iones, el proteinograma y el antígeno carcinoembrionario eran normales. El electrocardiograma y las radiografías de tórax y abdomen no mostraron alteraciones destacables.
Se mantuvo su tratamiento habitual, sustituyendo la anticoagulación oral por enoxaparina subcutánea y el pantoprazol por omeprazol (inicialmente intravenoso y posteriormente por vía oral), por ser éste el IBP disponible en nuestro centro. La paciente presentó desde el segundo día de ingreso picos febriles de 38-39 oC, y los urocultivos y hemocultivos fueron negativos. Con la sospecha de una enfermedad infecciosa-inflamatoria se instauró tratamiento antibiótico empírico (piperazilina/tazobactam y metronidazol, durante 5 días, sustituido posteriormente por amoxicilina-clavulánico). Se realizó una ecografía y una tomografía computarizada (TC) abdominopelviana, que mostraron la colelitiasis ya conocida, y un estudio endoscópico que puso de manifiesto una antritis erosiva y úlceras en sigma indicativas de colitis isquémica.
Al sexto día se observó una reacción eritematosa, con papulopústulas satélites inguinales. Dos días más tarde las lesiones se habían generalizado, muy palpables en el tronco y los brazos, por lo que se suspendió el tratamiento antibiótico con la sospecha de una toxicodermia. Ante la falta de respuesta a las 48 h, se solicitó la valoración de la paciente en el servicio de dermatología, donde se indicó biopsia de la lesión, la suspensión del omeprazol y la instauración de corticoterapia, con lo que desapareció la fiebre y la reacción cutánea. Se interpretó el cuadro como PEAG por fármacos (omeprazol como primera posibilidad frente a amoxicilina- clavulánico), con una biopsia compatible (pústula intracórnea con mínimo infiltrado de células redondas en la dermis papilar).
Caso 2Varón de 47 años, alérgico a las sulfamidas y a los ácaros, con diabetes mellitus tipo 2 controlada con dieta, e intervenido de sinusitis y timpanoplastia. Ex fumador y bebedor de 20 g de etanol/día.
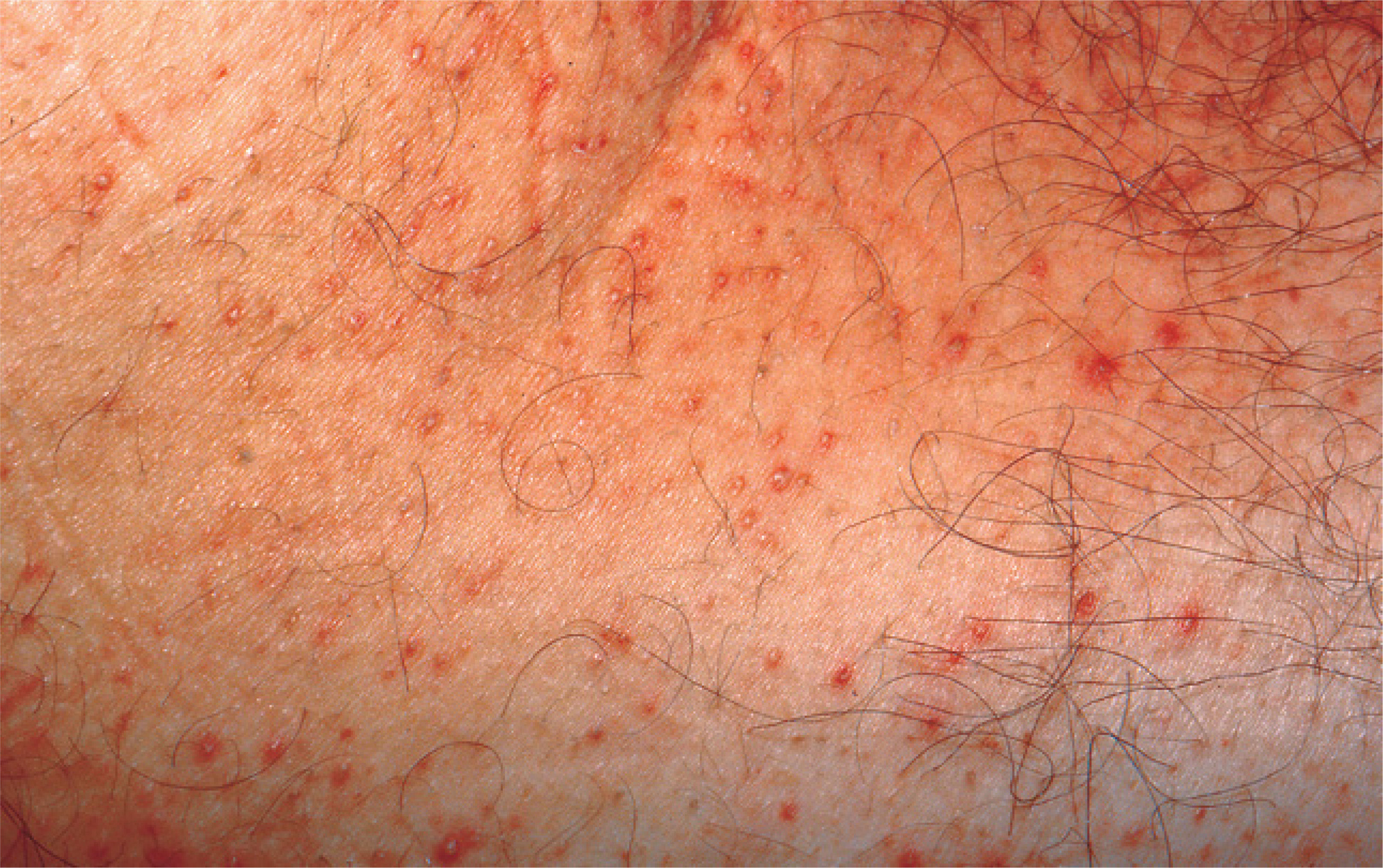
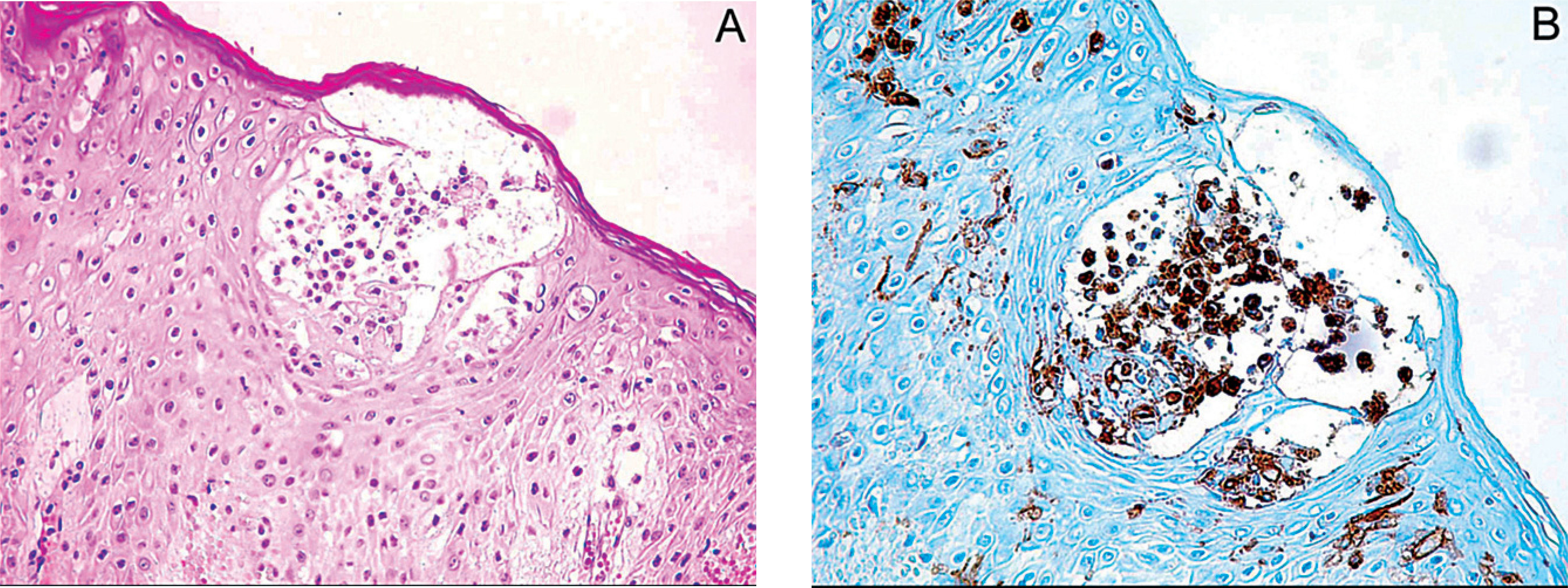
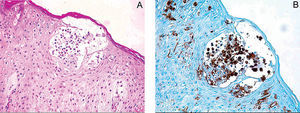
Acudió al servicio de urgencias por presentar deposiciones melénicas. En la exploración física presentaba una PA de 130/80 mmHg, una FC de 101 lat/min, una temperatura de 36,5 oC y un buen estado general y de hidratación; las radiografías de tórax y el electrocardiograma eran normales. Una gastroscopia puso de manifiesto un ulcus bulbar Forrest Ib, que se esclerosó con adrenalina y polidocanol. Las biopsias del antro demostraron una infección por Helicobacter pylori. Tras la endoscopia ingresó en el servicio de observación de urgencias, donde se instauró tratamiento con omeprazol y metoclopramida, presentando 20 h después prurito en la cara interna de los muslos y el abdomen inferior, por lo que se suspendió la metoclopramida y se pautó dexclorfeniramina. A su llegada a la planta del servicio de aparato digestivo, tras 48 h en observación, persistía el prurito y había desarrollado una reacción eritematosa, indurada, con pústulas aisladas en la cara interna de los muslos, los glúteos y el hemiabdomen inferior (fig. 1), por lo que se decidió no iniciar tratamiento erradicador para H. pylori y se suspendió el tratamiento con omeprazol, que se sustituyó por ranitidina, y se solicitó una valoración del paciente en el servicio de dermatología. La biopsia cutánea mostró pústulas intracórneas con edema dérmico y epidérmico, y acumulaciones de células de Langerhans en las pústulas intraepidérmicas (fig. 2). Tras la retirada del omeprazol, el paciente presentó una mejoría progresiva de las lesiones cutáneas, y tras el alta del hospital se encuentra asintomático.
Varón de 70 años de edad, sin alergias conocidas, hipertenso, con hiperlipemia e hiperuricemia, intervenido quirúrgicamente de herniorrafia inguinal bilateral. Sin hábitos tóxicos. En tratamiento con indapamida, atorvastatina y alopurinol.
Ingresó en nuestro servicio, procedente del servicio de urgencias con diagnóstico de pancreatitis aguda. Mostraba una PA de 120/70 mmHg, una FC de 63 lat/min, una temperatura de 35,8 oC y una saturación de oxígeno del 94%. La exploración física era normal. En la analítica presentaba un aumento de amilasa (391 U/l), lipasa (185 U/l) y ALT (47 U/l) en sangre, e hiperamilasuria (1.980 U/l). El electrocardiograma y las radiografías simples de tórax y abdomen eran normales. Una gastroscopia y una ecografía abdominal no mostraron alteraciones; la tomografía computarizada abdominal puso de manifiesto una afectación de la grasa peripancreática (Balthazar B), y la colangiorresonancia mostró microcoledocolitiasis. Se instauró analgesia con metamizol y tramadol y dieta absoluta, con lo que el paciente experimentó una buena evolución clínica, por lo que progresivamente se reinició la nutrición oral y se suspendió el tratamiento analgésico. Junto con la dieta oral, se inició tratamiento gastroprotector con omeprazol, y a las 24 h el paciente presentó una reacción pruriginosa, eritematoso-pustulosa, en la cara interna de los muslos, la región inguinal y los glúteos, con áreas descamativas. Con la sospecha de toxicodermia por omeprazol, se solicitó la valoración del paciente en el servicio de dermatología. Se biopsió la lesión (pústula subcórnea con ligera acantosis e infiltrado dérmico moderado linfocítico compatible con PEAG) y se suspendió dicha medicación, con lo que el paciente presentó una buena evolución posterior con la práctica desaparición de las lesiones dérmicas a las 48 h de la retirada del fármaco.
DISCUSIÓNPresentamos 3 casos de PEAG tras la administración de omeprazol, un IBP con un excelente perfil de seguridad durante tratamientos cortos. Así, la frecuencia de efectos adversos con omeprazol es de 1/12.200 tratamientos de 4 semanas1, y las reacciones cutáneas comunicadas (exantema, urticaria, angioedema, necrólisis epidérmica aguda, dermatitis de contacto, vasculitis leucocitoclástica y anafilaxia) son poco frecuentes.
Más del 90% de los casos de PEAG son inducidos por fármacos. Un gran número de ellos son potencialmente responsables, y los antibióticos (especialmente los betalactámicos y los macrólidos) son los más frecuentemente implicados. Sin embargo, en la revisión bibliográfica no hemos encontrado ninguna mención a los casos de PEAG atribuidos a omeprazol, únicamente un caso publicado inducido por lansoprazol2 y otro por ranitidina3. Raramente el origen de la PEAG se presenta en el curso de una infección por enterovirus (ECHO, Coxsackie), citomegalovirus o en relación con un tóxico (mercurio) o un alérgeno alimentario4.
Entre la administración del fármaco y la aparición de las lesiones cutáneas, puede haber un período de latencia de 1-3 semanas (sensibilización primaria), o bien aparecer rápidamente en horas-días (fenómeno de recuerdo). Con frecuencia los tests cutáneos a fármacos (pach-test) muestran una fuerte positividad, a veces incluso reacciones pustulosas. Estas características sugieren un mecanismo de recuerdo inmunológico.
El diagnóstico diferencial, una vez descartadas las causas infecciosas, debe establecerse con la psoriasis pustulosa (tipo Von Zumbusch), la pustulosis subcórnea de Sneddon- Wilkinson, la pustulosis aguda postestreptocócica5, el síndrome de hipersensibilidad a drogas o la necrólisis epidérmica tóxica.
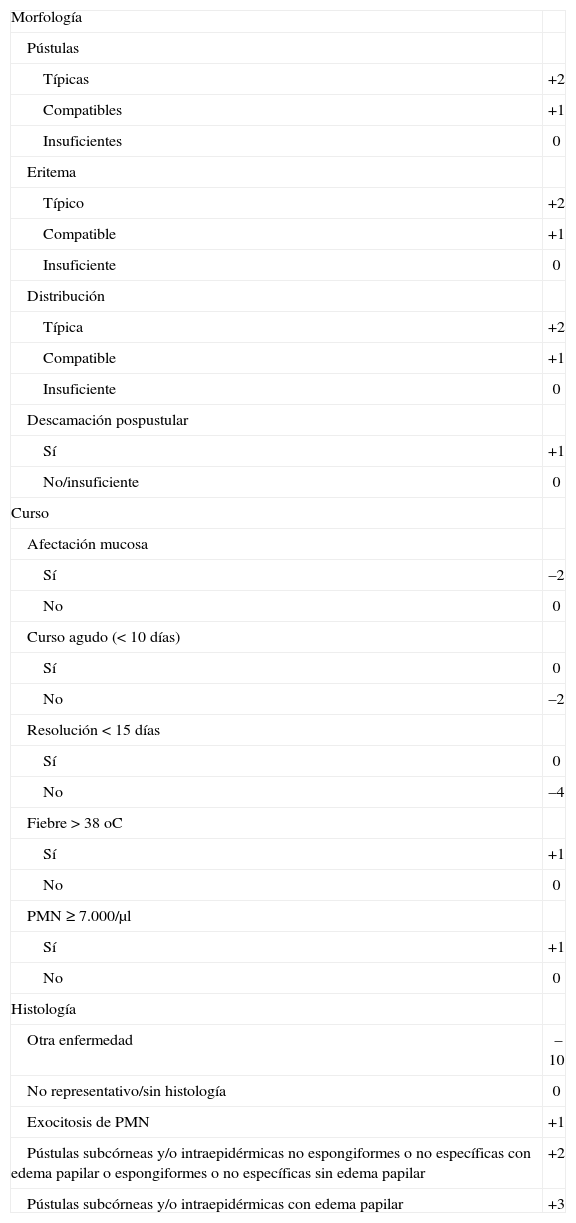
En 2001, Sidoroff et al6, dentro del proyecto EuroSCAR, realizaron una revisión de los criterios diagnósticos de PEAG establecidos en 1991 por Roujeau et al7, creando un sistema de puntuación más sofisticado (tabla I). En este estudio se estima que la incidencia, si bien realmente se desconoce debido a la gran variabilidad en la denominación de los casos de PEAG comunicados, es de 1-5 casos por millón al año6. No hay diferencias en función del sexo ni la edad. La presencia de algunos antígenos de histocompatibilidad (B51, DR11 y DQ3) en pacientes con PEAG es más frecuente que en la población general8. En general, el pronóstico es bueno, aunque la fiebre alta y las sobreinfecciones pueden ensombrecer la evolución en pacientes ancianos o con un deterioro subyacente, con una mortalidad del 1-2%4. El tratamiento consiste en la suspensión del fármaco sospechoso, y generalmente no se requieren otras medidas terapéuticas, como la corticoterapia.
Sistema de puntuación del grupo EuroSCAR para la validación de la PEAG
| Morfología | |
| Pústulas | |
| Típicas | +2 |
| Compatibles | +1 |
| Insuficientes | 0 |
| Eritema | |
| Típico | +2 |
| Compatible | +1 |
| Insuficiente | 0 |
| Distribución | |
| Típica | +2 |
| Compatible | +1 |
| Insuficiente | 0 |
| Descamación pospustular | |
| Sí | +1 |
| No/insuficiente | 0 |
| Curso | |
| Afectación mucosa | |
| Sí | –2 |
| No | 0 |
| Curso agudo (< 10 días) | |
| Sí | 0 |
| No | –2 |
| Resolución < 15 días | |
| Sí | 0 |
| No | –4 |
| Fiebre > 38 oC | |
| Sí | +1 |
| No | 0 |
| PMN ≥ 7.000/μl | |
| Sí | +1 |
| No | 0 |
| Histología | |
| Otra enfermedad | –10 |
| No representativo/sin histología | 0 |
| Exocitosis de PMN | +1 |
| Pústulas subcórneas y/o intraepidérmicas no espongiformes o no específicas con edema papilar o espongiformes o no específicas sin edema papilar | +2 |
| Pústulas subcórneas y/o intraepidérmicas con edema papilar | +3 |
PEAG: pustulosis exantemática aguda generalizada; PMN: polimorfonucleares. ≤ 0: sin PEAG; 1-4: posible; 5-7: probable; 8-12: definitiva.
En estos 3 casos, pese a estar polimedicados, la secuencia temporal de aparición y resolución de las lesiones guardó una clara correlación con la administración y la retirada del omeprazol. Es interesante señalar que en el caso 1 no pudimos excluir con seguridad la implicación de la amoxicilina- clavulánico en la patogenia, por ser éste un fármaco más frecuentemente implicado en este tipo de lesiones. Sin embargo, la falta de respuesta tras su supresión y el hecho de que la lesión se resolviese tras interrumpir el tratamiento con omeprazol apoyaron la implicación de este último en la etiología. Por este motivo, concluimos que es importante conocer la posibilidad de que las reacciones cutáneas indicativas de PEAG aparecidas en el contexto del tratamiento de un paciente, incluso polimedicado, puedan deberse a fármacos con un favorable perfil de seguridad, como el omeprazol, con rápida mejoría de las lesiones tras la retirada del fármaco.
CONFLICTOS DE INTERESESLos autores declaran no tener ningún conflicto de intereses.