Los pacientes celiacos tienen un incremento del riesgo de presentar linfomas gastrointestinales aunque la incidencia general es muy baja. Presentamos el caso de un varón de 36 an¿os con antecedentes de síndrome de Down, diabetes mellitus tipo 1 y enfermedad celiaca (EC) diagnosticada en la infancia con buena adherencia a la dieta sin gluten, sin datos de malabsorción y anticuerpos celiacos negativos. En la biopsia de control a los 19 años de edad persistía atrofia vellositaria Marsh 3a con linfograma por citometría de flujo compatible con EC activa, pero sin población linfocitaria aberrante.
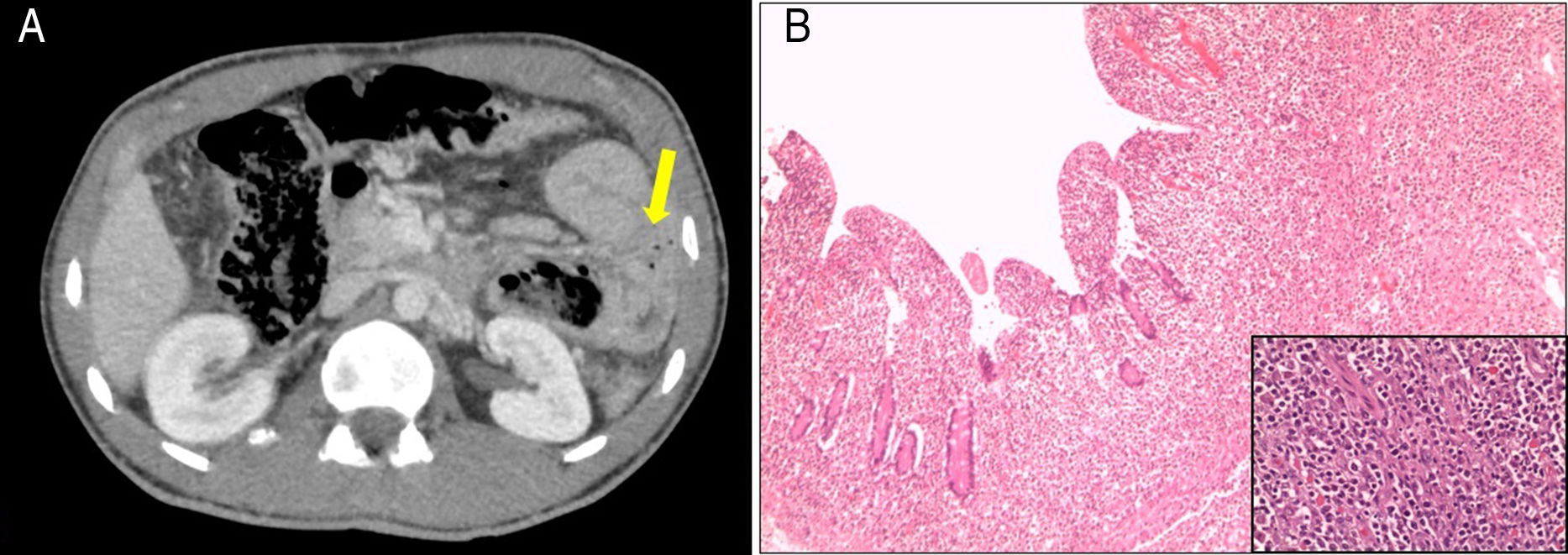
Acudió al hospital por dolor abdominal difuso de inicio progresivo asociado a náuseas y vómitos. En la exploración abdominal presentaba signos de irritación peritoneal. Analíticamente destacaba glucosa 317mg/dl, pH venoso 7.32, sin anemización ni leucocitosis. Una TAC abdomino-pélvica con contraste objetivó neumoperitoneo, líquido libre intraperitoneal y un asa de yeyuno dilatada de pared engrosada circunferencialmente y de aspecto tumoral, con burbujas de gas extraluminal adyacentes (fig. 1 A). Se visualizaron múltiples adenopatías de aspecto y tamaño patológico en la raíz mesentérica y un engrosamiento de un segmento largo de sigma. Dada la sospecha de perforación, se realizó una laparatomía con resección del yeyuno proximal y anastomosis primaria y una sigmoidectomía con colostomía terminal. El análisis histológico fue compatible con linfoma intestinal B difuso de células grandes de fenotipo activado, que afectaba a la mucosa produciendo ulceración de la misma, de la pared muscular y de la grasa subyacente, sin afectación ganglionar (fig. 1B). En la biopsia de médula ósea se descartó infiltración neoplásica y el virus de Epstein Barr fue negativo. Como tratamiento del linfoma se administraron 6 ciclos de CHOP-R (ciclofosfamida, doxorubicina, vincristina, prednisona y rituximab). Posteriormente se realizó reconstrucción del tránsito intestinal con anastomosis colosigmoidea. El PET-TAC y TAC abdominal de control a los 18 meses no detectaron datos de recidiva tumoral. En la actualidad, el paciente se encuentra bien, con buena adherencia a la dieta sin gluten y seguimientos periódicos de su EC.
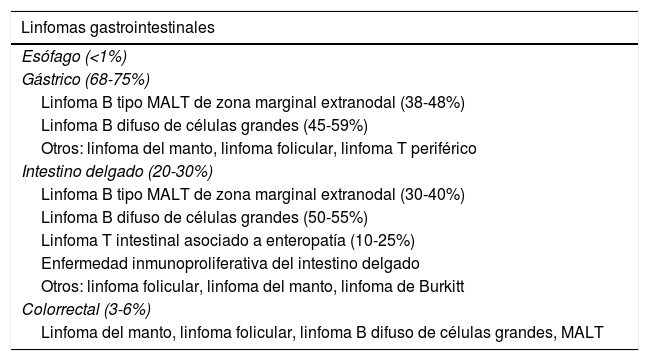
Los tumores primarios de intestino delgado suponen menos del 2% del total de neoplasias gastrointestinales, y de ellos los linfomas constituyen un 15-20% (tabla 1). Además, el tracto gastrointestinal es el lugar más frecuente de afectación extraganglionar de los linfomas1,2.
Frecuencia de los linfomas gastrointestinales según la región del tracto gastrointestinal afectada
| Linfomas gastrointestinales |
|---|
| Esófago (<1%) |
| Gástrico (68-75%) |
| Linfoma B tipo MALT de zona marginal extranodal (38-48%) |
| Linfoma B difuso de células grandes (45-59%) |
| Otros: linfoma del manto, linfoma folicular, linfoma T periférico |
| Intestino delgado (20-30%) |
| Linfoma B tipo MALT de zona marginal extranodal (30-40%) |
| Linfoma B difuso de células grandes (50-55%) |
| Linfoma T intestinal asociado a enteropatía (10-25%) |
| Enfermedad inmunoproliferativa del intestino delgado |
| Otros: linfoma folicular, linfoma del manto, linfoma de Burkitt |
| Colorrectal (3-6%) |
| Linfoma del manto, linfoma folicular, linfoma B difuso de células grandes, MALT |
En los linfomas gastrointestinales primarios el órgano más afectado es el estómago, seguido por el intestino delgado (60-65% afectan al íleon y el resto al yeyuno y duodeno)1. Casi el 90% corresponden a linfomas de células B, siendo los subtipos más frecuentes el linfoma B difuso de células grandes y el linfoma B tipo MALT de zona marginal extranodal1,2. Pueden presentarse con dolor abdominal, vómitos, pérdida ponderal y raramente como obstrucción, intususcepción, perforación (5-15%), hemorragia digestiva o diarrea1,2. La mayoría de los linfomas son tratados con una combinación de cirugía y quimioterapia3. El estadio tumoral y la presencia de síntomas B se asocian a un peor pronóstico3.
Los pacientes celiacos tienen un incremento del riesgo del 40% de presentar cualquier neoplasia en comparación con la población general4, con un riesgo 5 veces mayor de presentar un linfoma5. La neoplasia más frecuentemente asociada a EC son los linfomas no Hodgkin, con una incidencia de 1,3 por 1.000 personas-año4. De ellos, los más habituales son el linfoma difuso de células B grandes y el linfoma T asociado a enteropatía2,5. Aunque no se han encontrado diferencias en la supervivencia de los pacientes con EC y un proceso linfoproliferativo con respecto a la población general2, los linfomas de células B tienen mejor pronóstico que los de células T5. Entre las neoplasias digestivas asociadas a EC destacan el adenocarcinoma de intestino delgado, el cáncer de esófago y el colorrectal4.
El linfoma T asociado a enteropatía es el linfoma que tiene la asociación más estrecha con la EC. Es un linfoma T no Hodgkin de alto grado que supone menos de un 5% de los linfomas gastrointestinales y suele localizarse de forma primaria en el intestino delgado6.
El riesgo global de malignidad en pacientes celiacos disminuye con el tiempo después del diagnóstico y no aumenta significativamente después de 15 años de evolución, en probable relación con el diagnóstico precoz y el inicio temprano de la dieta sin gluten4,7. El seguimiento de una dieta sin gluten favorece la curación mucosa, pero en casi un 20% se encuentra atrofia vellositaria en la biopsia de control7,9. En los casos en los que persiste la atrofia vellositaria existe el doble de riesgo de presentar un proceso linfoproliferativo que en aquellos que tienen curación mucosa7.
Por otro lado, en el síndrome de Down hay un incremento del riesgo de mortalidad respecto a la población general debido principalmente a malformaciones cardíacas, demencia de inicio precoz y leucemia infantil. Además, presentan un riesgo 6 veces superior de padecer EC, aunque la asociación entre ambas enfermedades no comporta un incremento de mortalidad respecto al resto de la población con síndrome de Down10.
En conclusión, el correcto seguimiento de una dieta sin gluten disminuye el riesgo de desarrollar un linfoma y cualquier otro tumor asociado a la enfermedad celiaca5,7.