INTRODUCCIÓN
La obstrucción es un fenómeno patológico común a todos los órganos tubulares del organismo. Las consecuencias fisiopatológicas varían, lógicamente, según el lugar anatómico en que se produzca el fenómeno obstructivo.
Desde hace años, el desarrollo de la tecnología ha permitido utilizar distintos materiales para fabricar prótesis metálicas autoexpandibles (PMA) o stents. Las PMA son unos tubos cilíndricos, en forma de malla, de distintas longitudes y anchuras, que tienen la característica de poder insertarse plegadas. Esta propiedad permite atravesar estenosis muy importantes, sin que sea preciso dilatarlas previamente en la mayoría de las ocasiones. Una vez dentro de la zona obstruida, mediante un mecanismo de liberación, las PMA se abren, consiguiendo un diámetro suficiente para recanalizar la zona estenosada.
Las PMA con modificaciones según el lugar anatómico se utilizan para recanalizar la obstrucción de estructuras tubulares, como las coronarias, la tráquea, o gran parte del tubo digestivo y de la vía biliar1.
En 1991 se describió, por primera vez, la utilización de una PMA para paliar la obstrucción colónica aguda2. Desde entonces, se han producido mejoras tecnológicas en los stents. Han aparecido modelos específicamente diseñados para recanalizar las obstrucciones tumorales rectocolónicas y, además, ha aumentado su utilización por parte de los endoscopistas3-5. Las PMA en el colon permiten resolver la obstrucción inicialmente. Después, tras la evaluación clínica, el paciente puede ser intervenido de su neoplasia de forma electiva, o bien, si no es apto para la cirugía, la prótesis puede servir como tratamiento paliativo definitivo6.
Presentamos la experiencia en nuestro centro del tratamiento de la obstrucción colónica tumoral mediante PMA.
PACIENTES Y MÉTODOS
Se han revisado, de forma retrospectiva, los pacientes cuya obstrucción colónica intentó resolverse mediante la inserción de PMA durante un período de 42 meses (desde mayo 2002 hasta octubre de 2005). Algunos de estos pacientes se han comunicado previamente7,8.
Tras el diagnóstico clínico y radiológico de obstrucción colónica se realizó una colonoscopia en la que intentó insuflarse el menor aire posible. Una vez se diagnosticó la obstrucción de origen tumoral, se tomaron habitualmente biopsias y, de acuerdo con el equipo de cirugía, se valoró su resolución por medio de PMA. El paso más determinante para insertar una PMA es lograr atravesar la estenosis tumoral con una guía y situarla más allá de la neoplasia, en tejido sano. Sobre esta guía irá la prótesis plegada, que se abrirá después dentro del tumor, recanalizando así la obstrucción. Para tener la seguridad de que la guía estaba correctamente situada, se emplearon tres técnicas.
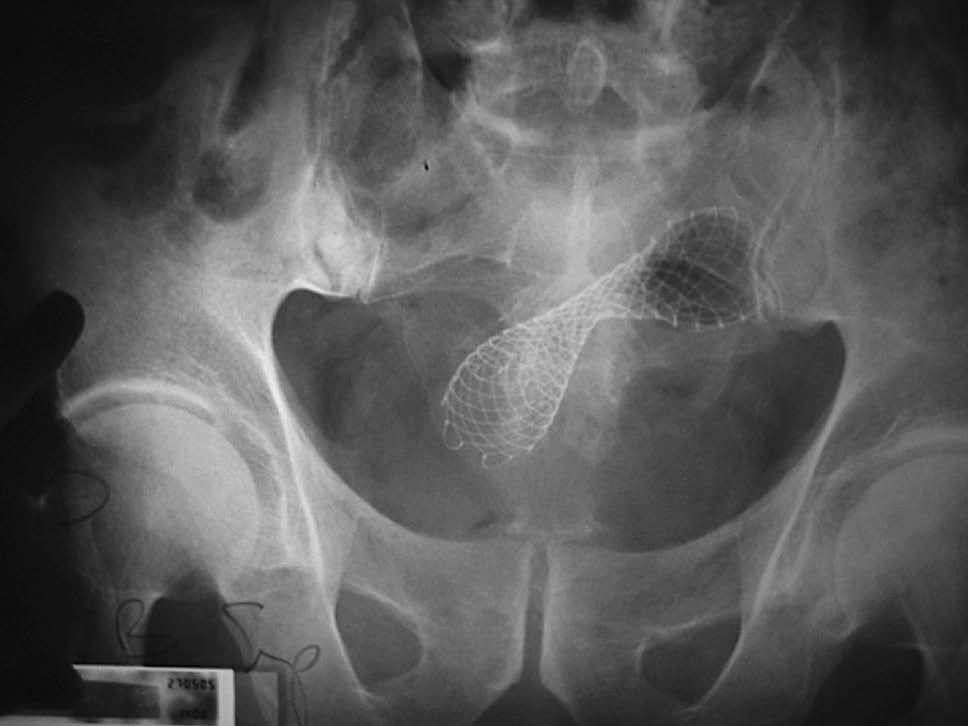
Fluroscopia. Cuando la PMA se colocó en la sala de radiología, se situó el colonoscopio con canal terapéutico en la parte más distal del tumor. Se pasó una guía de 0,035 pulgadas de diámetro (0,875 mm), con punta hidrofílica atraumática, a través de canal de trabajo del colonoscopio, con la intención de atravesar todo el segmento estenosado. La confirmación de que la guía había pasado la estenosis se obtuvo por fluorosocopia. Además, sobre la guía se introdujo un catéter biliar de los utilizados en la colangiopancreatografía retrógrada endoscópica (CPRE), y por medio de la inyección de contraste se delineó la obstrucción. Se retiró después el catéter y, siempre sobre la guía, se insertó la prótesis. Una vez que la PMA se colocó dentro de la estenosis, comenzó a abrirse gradualmente, hasta dejarla situada correctamente, con los extremos proximal y distal en zona colónica sana (fig. 1). Las prótesis insertadas a través del canal de trabajo del colonoscopio terapéutico (ATCTCT) fueron Wallstent, Wallflex y Niti-S. Las prótesis Ultraflex no pueden colocarse ATCTCT por ser, todavía plegadas, de calibre mayor que el del canal. Por lo que, una vez pasada la guía, se retiró el endoscopio (dejando la guía dentro de la estenosis). Sobre la guía se pasó la prótesis y su liberación se monitorizó con el endoscopio en paralelo y con fluoroscopia.
Fig. 1. Prótesis metálica autoexpandible de nitinol tipo Wallflex, situada en el sigma inmediatamente tras su liberación. Se observa que la zona media de la prótesis está situada justo en el centro de la obstrucción, adoptando una configuración como de «reloj de arena». De esta forma, ambos extremos están abiertos (en la zona colónica no obstruida). Asimismo, se trata de impedir la migración de la prótesis.
Endoscopio de calibre muy fino, capaz de atravesar la estenosis. La dificultad que tienen muchos gastroenterólogos de disponer de una sala de radiología para realizar técnicas de intervencionismo endoscópico, ha llevado a desarrollar técnicas que puedan suplir la seguridad que da la fluoroscopia. Hay varios modelos de endoscopios de calibre muy pequeño que pueden atravesar muchas estenosis colónicas (al menos en el recto y el sigma más distal). Según la técnica descrita por nosotros previamente9, una vez atravesado el tumor con un endoscopio de 6 mm de diámetro (Pentax EG-1870 K), se deja colocada una guía a través del canal de trabajo del endoscopio de calibre muy fino (ECMF). A continuación, se retira el ECMF, dejando la guía más allá de la estenosis. Esta guía puede insertarse después de manera retrógrada en el colonoscopio terapéutico y colocar con seguridad sobre ella una PMA a través de su canal de trabajo, o bien deslizar la guía una prótesis que no pueda introducirse ATCTCT y monitorizar su liberación con un endoscopio en paralelo.
Sensación táctil de que la guía ha pasado la estenosis. Cuando no se dispone de flluoroscopia ni de ECMF, la sensación táctil del endoscopista de que la guía ha pasado libremente, y la ausencia de imágenes en la pantalla del videoendoscopio de que la guía se vuelva, pueden utilizarse para colocar una PMA. La sensación táctil es similar, por ejemplo, a la facilidad con que la guía metálica debe pasar tras canalizar correctamente una vena subclavia y, en general, es una habilidad que suelen tener los médicos y el personal que realiza intervencionismo endoscópico. No obstante, no hay la seguridad absoluta de que la guía pueda estar correctamente colocada. Éste es un riesgo que puede asumirse ponderando las circunstancias concretas de cada caso.
Las prótesis utilizadas no tenían cubierta sobre la malla. Esto facilita que el tumor penetre en las celdas metálicas y se disminuya la posibilidad de migración. No obstante, el tumor puede crecer, con el tiempo, por dentro y obstruir la prótesis.
Tras la inserción de las PMA, el paciente permaneció ingresado para completar el estudio. En los días sucesivos se comprobó su mejoría clínica y se estuvo atento ante las posibles complicaciones. Se consideró éxito clínico la resolución del síndrome de obstrucción colónica tras la inserción de la prótesis, sin complicaciones importantes que precisaran, por ejemplo, cirugía.
RESULTADOS
Durante los 42 meses que comprende el estudio se han intentado colocar 43 PMA colónicas en 40 pacientes (lo que significa aproximadamente un procedimiento por mes). Los pacientes eran 26 varones (65%) y 14 mujeres (35%), con una media de edad de 72 años (rango, 41-94). La obstrucción tumoral se debía a adenocarcinomas colónicos primarios en todos los pacientes, excepto una mujer con cáncer de ovario. Hubo confirmación anatomopatológica en todos los casos.
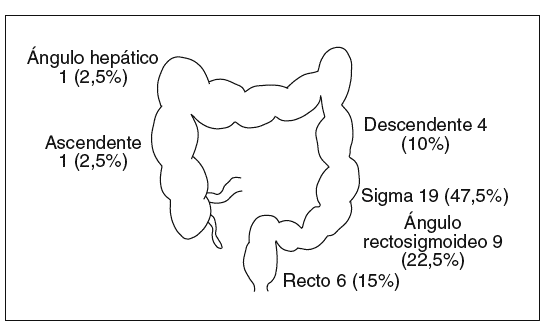
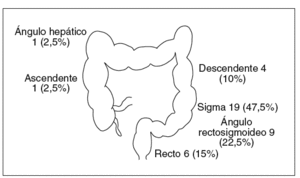
En un 95% de las ocasiones el lugar de la obstrucción estaba en el colon izquierdo (recto-sigma-descendente) (fig. 2).
Fig. 2. Lugar de la estenosis tumoral en los 40 pacientes.
La causa de obstrucción colónica se diagnosticó siempre por endoscopia y en ningún paciente fue preciso realizar un enema opaco.
En 23 (53,5%) procedimientos se utilizó sólo endoscopia. El método del ECMF se empleó en 18 ocasiones y el método de la sensación táctil en 5. Las otras 20 (46,5%) intervenciones se realizaron en una sala de radiología y se utilizó endoscopia y fluoroscopia. Uno de estos procedimientos se había comenzado con el ECMF, pero debió utilizarse finalmente fluoroscopia. Pudieron insertarse con éxito 41 (95%) PMA. Uno de los procedimientos fallados se realizó por la sensación táctil y el otro con fluoroscopia. El primer paciente fue intervenido de urgencia y el segundo (una mujer de 94 años) sólo recibió tratamiento paliativo. En general, no se utilizó sedación en ningún procedimiento. Ocasionalmente se administró dolantina y buscapina.
En la inserción de prótesis actuaron como endoscopistas principales 5 médicos en total. En el primer procedimiento de uno de ellos, una prótesis se liberó, por error, más allá de la estenosis. Se colocó otra correctamente y el paciente no presentó ninguna complicación hasta la cirugía electiva.
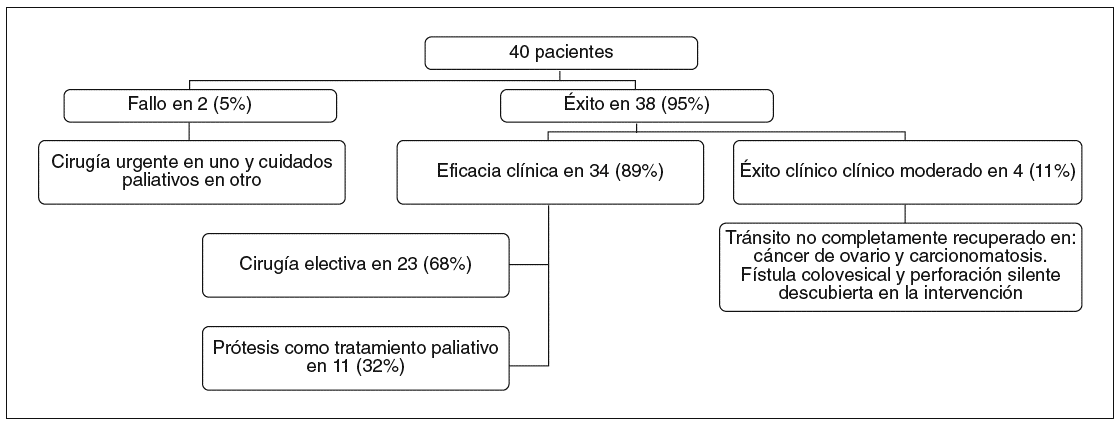
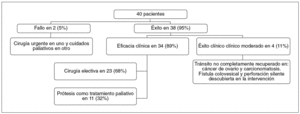
La evolución de los 38 pacientes en quienes pudo insertarse correctamente una PMA se indica en la figura 3. En 4 de estos pacientes no se obtuvo un éxito clínico total. En 2 mujeres (una con cáncer de ovario y otra con carcinomatosis peritoneal por el tumor colónico) no se recuperó totalmente el tránsito intestinal y continuaron hasta su fallecimiento con crisis oclusivas parciales. Sin embargo, no precisaron más intervenciones endoscópicas o quirúrgicas.
Fig. 3. Evolución de los pacientes en el primer intento de desobstruir mediante prótesis una estenosis tumoral del colon. Hubo en total 43 intentos sobre 40 pacientes. En 3 pacientes se insertaron prótesis en 2 ocasiones: 2 por prótesis migradas y 1 por obstrucción de la prótesis previa.
En un paciente con la PMA bien insertada en el recto, se observó en la cirugía colónica electiva que la prótesis había migrado cranealmente, perforando el sigma. No pudo realizarse una anastomosis primaria y el paciente precisó una colostomía. Al revisarse las radiografías, se observó que la PMA (colocada por el método del ECMF) tenía su extremo inferior dentro del tumor: no formaba claramente un «reloj de arena» (fig. 1) por lo que pudo deslizarse hacia arriba. Esta prótesis era la segunda que insertaba uno de los facultativos.
Por último, en una paciente con una neoplasia en el sigma, que ya inicialmente contactaba con la vejiga urinaria, apareció una fístula colovesical tras la inserción de dos PMA superpuestas. Debieron insertarse dos por la longitud de la estenosis. La fístula se selló, inicialmente, con una prótesis esofágica recubierta, colocada por dentro de las anteriores. Sin embargo, al mes reapareció y debió intervenirse a la paciente, que falleció tras la cirugía.
De los 34 pacientes con éxito clínico total tras la PMA, se operó de forma electiva a 23 (68%) y en 11 (32%) la prótesis se consideró como tratamiento paliativo definitivo.
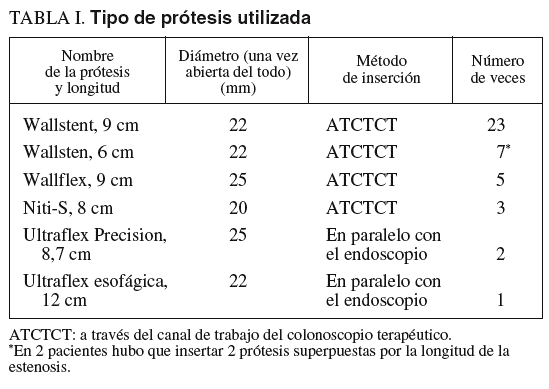
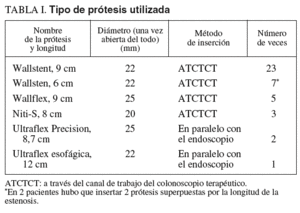
Los distintos tipos de prótesis utilizados se indican en la tabla I.
Además de la fístula colovesical y de la perforación reseñadas, hubo otras 7 complicaciones (9 en total [21%]). En 3 pacientes las prótesis migraron distalmente, por lo que tuvieron que extraerse del recto por endoscopia (en 2 casos las PMA se habían colocado con control radiológico y en otro por medio de la técnica del ECMF). Sólo uno de ellos necesitó una nueva prótesis. En los otros dos, la dilatación ocasionada por la prótesis fue duradera y no precisaron otra. Dos pacientes con prótesis rectales presentaron tenesmo moderado. Ambos fueron intervenidos quirúrgicamente de forma electiva. La prótesis se obstruyó en un paciente en el grupo paliativo. Se recanalizó mediante la inserción de otra PMA. Por último, un paciente desarrolló una bacteriemia tras la colocación de la prótesis, que se resolvió con antibioterapia. No hubo mortalidad relacionada con la inserción de las prótesis o sus complicaciones.
Las complicaciones se observaron desde el día siguiente a la inserción (bacteriemia, tenesmo), hasta varios meses después (obstrucción de la prótesis y migración al recto en el grupo paliativo).
DISCUSIÓN
La obstrucción aguda del colon forma parte del síndrome de abdomen agudo y debe resolverse con urgencia. Tradicionalmente, la única opción de tratamiento era la cirugía.
La morbimortalidad de los pacientes intervenidos por obstrucción colónica aguda es elevada10. Uno de los factores que más influye en las complicaciones de la cirugía es la deficiente preparación del colon. Los pacientes suelen tener una gran retención de heces que conlleva, con frecuencia, la contaminación del campo quirúrgico. Además, con la distensión progresiva del intestino grueso, se producen bacteriemias. El sigma es el lugar anatómico donde con más frecuencia se localiza la obstrucción. Las causas más frecuentes son los tumores y procesos benignos, como la diverticulitis.
El procedimiento quirúrgico habitual suele ser una colostomía de descarga, en primer lugar, y meses después, si es posible, la reconstrucción del tránsito colónico normal.
Sin embargo, el enfoque terapéutico de la obstrucción colónica aguda ha cambiado progresivamente desde que, en 1991, se describió, por primera vez, la utilización de una PMA para paliar la obstrucción2. En un estudio de Martínez Santos et al11 se compararon el tratamiento quirúrgico tradicional de la obstrucción colónica tumoral con el de la inserción de PMA. En los pacientes en que la obstrucción se resolvió inicialmente con PMA y se realizó cirugía programada posterior, se demostró una menor incidencia de complicaciones graves y una disminución de la estancia hospitalaria. Además, en el 39% (17 de 43) de los pacientes en quienes se insertó una PMA, el estudio de extensión recomendó no operar. La prótesis se consideró como tratamiento paliativo definitivo y se evitaron, por tanto, las intervenciones quirúrgicas.
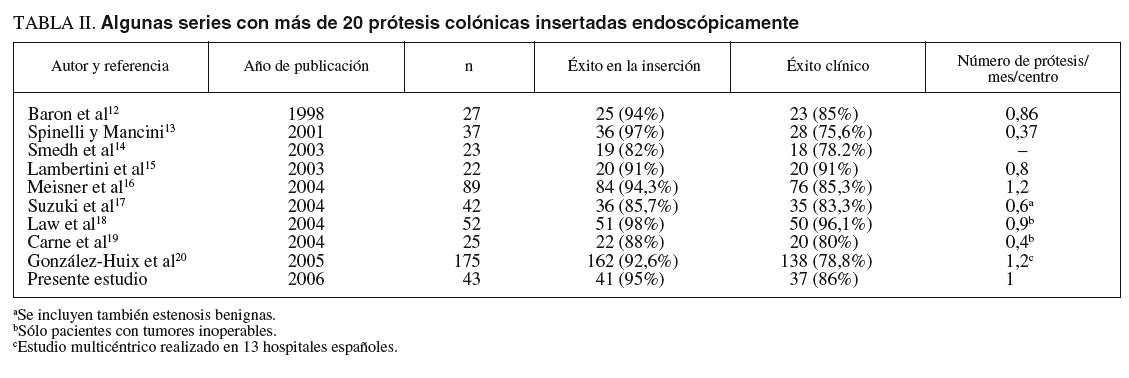
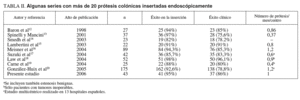
En la tabla II se señalan algunos trabajos con más de 20 prótesis cada uno, que reflejan la experiencia creciente de la inserción endoscópica de PMA12-20. Como se puede apreciar, la tasa media de PMA insertadas por mes varía entre 0,37 (una prótesis cada 3 meses) y 1,2 (algo más de una prótesis al mes). La media mensual de inserción en las series publicadas es de 0,7721. La experiencia actual en nuestro centro, con una tasa de aproximadamente un intento de inserción mensual es muy aceptable. Además, es preciso tener en cuenta que nuestro hospital se encuadra en el nivel II del Sistema Nacional de Salud y la mayoría de los trabajos publicados están realizados en grandes centros. Quizás la confianza de los cirujanos con los que trabajamos en la descompresión colónica por medio de PMA ha propiciado la proliferación de esta técnica en nuestro centro. No obstante, al ser un trabajo retrospectivo sobre la eficacia de las prótesis insertadas, no es posible saber con exactitud a cuántos pacientes fue preciso intervenir quirúrgicamente de urgencia por no disponer de la técnica endoscópica. En nuestro centro hay un endoscopista de guardia las 24 h del día. Sin embargo, la inserción de una PMA suele ser una técnica más compleja que las habituales endoscopias realizadas en pacientes sangrantes. Hay otros datos muy interesantes tiempo entre el diagnóstico de la obstrucción y colocación de la PMA, entre la colocación de la PMA y cirugía electiva, etc. que tampoco pueden aportarse con exactitud en este trabajo, debido, además de a su carácter retrospectivo, a la disparidad de criterios de todos los médicos que intervinieron en la atención de cada uno de los pacientes (diversos servicios: urgencias, medicina interna, oncología, cirugía, etc.).
La inserción endoscópica de PMA, dentro de la dificultad que toda técnica de intervencionismo comporta, nos parece un procedimiento más sencillo que, por ejemplo, la CPRE22 y con una curva de aprendizaje más corta. De todos modos, consideramos que para obtener unas tasas de éxito aceptables (superiores en general al 90%) (tabla II) es preciso tener una dedicación especial. Algunas complicaciones surgidas en nuestra serie se produjeron en la inserción de las primeras prótesis. Creemos que en un hospital como el nuestro sólo deberían dedicarse a la técnica dos o tres facultativos. Del mismo modo, y de una manera algo arbitraria, consideramos que 10 puede ser el número de prótesis de la curva inicial de aprendizaje.
En nuestra opinión, la inserción endoscópica de las prótesis debería hacerse siempre con control fluoroscópico. No obstante, los gastroenterólogos tienen frecuentemente dificultades para utilizar equipos radiológicos adecuados. Hasta que este problema pueda solucionarse, quizás el ECMF puede ser un método alternativo9 en obstrucciones de recto y sigma.
La técnica empleada por nosotros en unos pocos pacientes, basada en la sensación táctil, es peligrosa y probablemente no debería utilizarse. Sin embargo, no hemos constatado ninguna complicación en los pacientes en que ésta se empleó. Por tanto, queda a juicio de los médicos que atienden al paciente de acuerdo con él y sus familiares la posibilidad de intentar esta técnica en casos extremos.
Las complicaciones graves son pocas, aunque si se produce una perforación colónica durante la inserción, se necesita una intervención urgente y, lógicamente, en muy malas condiciones. La migración o la obstrucción pueden solucionarse fácilmente de forma endoscópica. En 2 de nuestros pacientes, la dilatación del tumor realizada por la prótesis impidió la reaparición de un síndrome obstructivo, a pesar de haber migrado, y no fue preciso insertar una nueva. Quizás debería considerarse emplear siempre una cobertura antibiótica, para evitar bacteriemias, como la que ocurrió en uno de nuestros pacientes. Sin embargo, no hay consenso generalizado sobre la antibioterapia profiláctica al insertar prótesis.
Una de nuestras pacientes desarrollo una fístula colovesical. Ya antes de la inserción de la prótesis el tumor contactaba con la vejiga urinaria. No puede descartarse que un cierto decúbito de la PMA influyera en la formación de la fístula. Como el tratamiento de las fístulas colónicas es otra indicación de las PMA (que en este caso deben ser recubiertas), se trató de este modo a la paciente, que inicialmente mejoró. Sin embargo, evolucionó como otras de origen tumoral, que frecuentemente recidivan si la supervivencia del paciente es larga y el tumor crece23.
En resumen, en nuestra experiencia, las PMA colónicas permiten recanalizar la obstrucción aguda, restableciendo el tránsito intestinal por medio de una técnica mínimamente invasiva y con pocas complicaciones graves. Después, si el paciente es operable, la intervención puede realizarse de forma electiva, con lo que se evita muchas veces la colostomía de descarga inicial. Actualmente, la descompresión inicial de la obstrucción por medio de una PMA y la cirugía laparoscópica posterior del tumor es una opción prometedora24. Si, por el contrario, el paciente es inoperable, la prótesis sirve para paliar de forma definitiva la obstrucción.
Los radiólogos tienen también experiencia en colocar PMA colónicas11,25. Aunque no se ha realizado ningún estudio comparativo entre la eficacia de la inserción endoscópica o radiológica, según los estudios publicados ésta parece ser la misma. De todos modos, quizás sea más fácil insertar endoscópicamente prótesis en segmentos del colon proximales al descendente6.
Por la buena experiencia obtenida en éste y otros trabajos anteriores, la inserción de PMA podría considerarse, en general, como el tratamiento inicial de la obstrucción colónica, especialmente en el colon izquierdo (recto-sigma-descendente), lugar donde asientan con mayor frecuencia los tumores del intestino grueso26. Por tanto, habría que reorganizar los recursos sanitarios, para que los pacientes puedan beneficiarse, en el momento que lo necesiten, de la inserción de PMA por equipos con experiencia.