El estreñimiento es un trastorno muy frecuente que afecta negativamente el bienestar y la calidad de vida de las personas. Para el correcto manejo y tratamiento eficiente y seguro de los pacientes, las guías de práctica clínica basadas en la evidencia son un elemento esencial.
El objetivo de esta guía es proporcionar a los profesionales sanitarios encargados de la asistencia a pacientes con estreñimiento crónico una herramienta que les permita tomar las mejores decisiones sobre la prevención, el diagnóstico y el tratamiento del estreñimiento.
La metodología utilizada en la elaboración de esta guía de práctica clínica se describe en la Parte 1. En este artículo expondremos las recomendaciones en el manejo, tanto diagnóstico como terapéutico del estreñimiento.
Constipation is a very common disorder that adversely affects well-being and quality of life. Evidence-based clinical practice guidelines are an essential element for proper patient management and safe, effective treatment.
The aim of these guidelines is to provide health care professionals who care for patients with chronic constipation with a tool that allows them to make the best decisions about the prevention, diagnosis and treatment of constipation.
The methodology used to draw up these guidelines is described in the Part 1. In this article we will discuss the recommendations for the diagnostic and therapeutic management of constipation.
Dieta rica en fibra
- -
Se recomienda consumir alimentos con alto contenido en fibra soluble (frutas, verduras, hortalizas, legumbres, frutos secos, pan de centeno (evidencia moderada, recomendación fuerte a favor).
- -
Se aconseja que la ingesta de alimentos ricos en fibra se realice de forma gradual para que el tracto gastrointestinal se pueda adaptar.
Aporte hídrico
Ejercicio físico
Medidas farmacológicasLaxantes formadores de masa
Laxantes osmóticos
- -
Se recomienda el polietilenglicol como una opción de tratamiento en personas con estreñimiento crónico (evidencia moderada, recomendación fuerte a favor).
- -
Se recomienda la lactulosa como una opción de tratamiento en personas con estreñimiento crónico (evidencia baja, recomendación fuerte a favor).
- -
Se sugiere utilizar con preferencia el polietilenglicol frente a la lactulosa (evidencia moderada, recomendación débil a favor).
Laxantes emolientes y lubricantes
- -
Se recomienda utilizar los laxantes estimulantes como opción de tratamiento de rescate (evidencia moderada, recomendación fuerte a favor).
- -
Se sugiere utilizar los laxantes estimulantes como una opción de tratamiento en personas con estreñimiento crónico que no han respondido a laxantes formadores de masa y/u osmóticos (evidencia moderada, recomendación débil a favor).
Laxantes procinéticos
Laxantes secretores
Otros tratamientosBiofeedback (rehabilitación del suelo pélvico)
Neuromodulación sacra
Cirugía (colectomía)
- -
La colectomía solo debe plantearse como opción de tratamiento en personas con estreñimiento crónico refractario grave que no responde a otros tratamientos y en los que se ha descartado una afectación extensa de la motilidad intestinal mediante pruebas especiales que incluyen la manometría gastrointestinal (evidencia baja, recomendación débil a favor).
El estreñimiento es un trastorno muy frecuente que afecta negativamente el bienestar y la calidad de vida de las personas. Para el correcto manejo y el tratamiento eficiente y seguro de los pacientes, las guías de práctica clínica basadas en la evidencia son un elemento esencial.
El objetivo de esta guía es proporcionar a los profesionales sanitarios encargados de la asistencia a pacientes con estreñimiento crónico una herramienta que les permita tomar las mejores decisiones sobre la prevención, el diagnóstico y el tratamiento del estreñimiento.
La metodología utilizada en la elaboración de esta guía de práctica clínica se describe en la Parte 1. En este artículo expondremos las recomendaciones en el manejo, tanto diagnóstico como terapéutico, del estreñimiento (figs. 1 y 2, tabla 1).
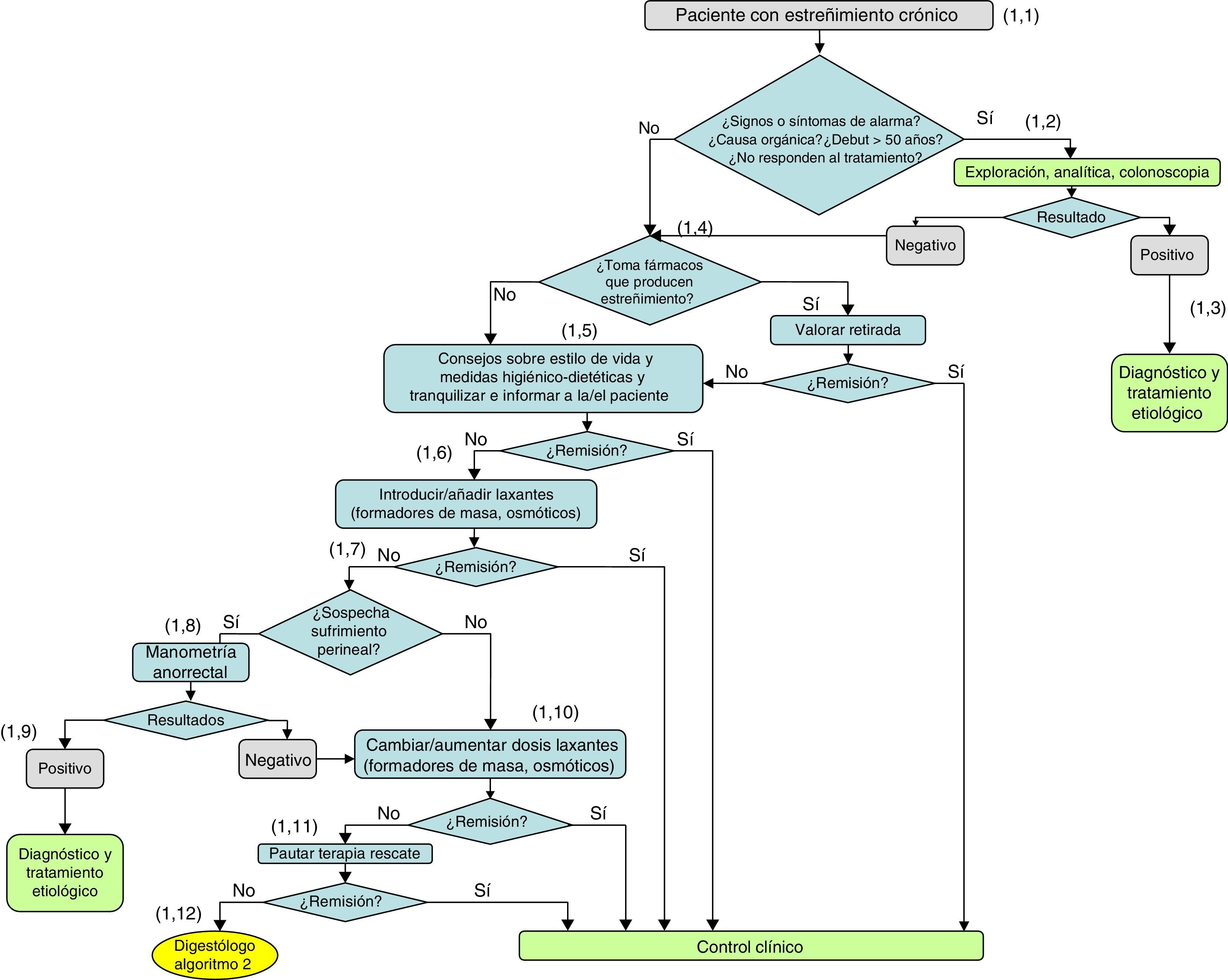
Diagnóstico y tratamiento inicial del estreñimiento crónico.
(1.1) En la mayoría de los casos no existe una causa orgánica subyacente, siendo calificado, tras una historia clínica y exploración física completa negativas, como estreñimiento crónico idiopático. Los pacientes que cumplen los criterios de Roma III para estreñimiento funcional generalmente no requieren de pruebas diagnósticas.
(1.2) Cuando en la historia clínica hay signos de alarma, se sospecha una posible causa orgánica o el estreñimiento comienza en una persona de más de 50años de edad se deben realizar estudios diagnósticos: analítica y colonoscopia. Estos estudios diagnósticos también están indicados en los pacientes con estreñimiento que no responden al tratamiento.
(1.3) El estreñimiento crónico secundario puede estar asociado a una amplia relación de enfermedades. Según los resultados se procederá al diagnóstico y tratamiento etiológico del estreñimiento. Las posibles causas orgánicas son diversas y se pueden consultar en la tabla 4 de la guía completa.
(1.4) Si el resultado es negativo y no se ha llegado a ningún diagnóstico etiológico, se tiene que valorar si el paciente toma fármacos que producen estreñimiento y si estos se pueden retirar. La lista de fármacos que pueden causar estreñimiento es amplia y se puede consultar en la tabla 5 de la guía completa.
(1.5) Si se han descartado posibles causas orgánicas y fármacos que producen estreñimiento y que no se pueden retirar (o reducir dosis), las primeras recomendaciones son las medidas no farmacológicas. Valorar los consejos sobre estilo de vida y medidas higiénico-dietéticas, la dieta rica en fibra, el ejercicio físico y una buena hidratación.
(1.6) El tratamiento médico con laxantes por lo general comienza después del fracaso de modificaciones en la dieta y el estilo de vida. Actualmente se dispone de una gran variedad de opciones terapéuticas. El tratamiento de primera línea es introducir laxantes formadores de masa y/o laxantes osmóticos. Si el paciente ya estuviera tomando alguno de estos laxantes, debe valorarse cambiar o añadir laxantes de estos grupos mencionados.
(1.7) Si no hay respuesta a los laxantes formadores de masa y/o a los laxantes osmóticos, se debe hacer énfasis en si el estreñimiento está provocando sufrimiento perianal que favorezca la aparición o cronificación de patología anorrectal. La aparición de inflamación o sangrado hemorroidal durante el esfuerzo defecatorio, la recidiva de fisura anal durante el esfuerzo defecatorio o la emisión involuntaria de orina pueden ser signos de alerta de sufrimiento perineal.
(1.8) Si se sospecha sufrimiento perineal, se debe contemplar la posibilidad de realizar una manometría anorrectal para valorar la presencia de un trastorno de la defecación.
(1.9) Si el resultado de la manometría es positivo, se procederá al diagnóstico y al tratamiento etiológico.
(1.10) Si la propia clínica no era sugestiva de sufrimiento perineal o cuando se hubiera realizado una manometría anorrectal con resultado negativo, hay que revisar los tratamientos con laxantes formadores de masa y/o laxantes osmóticos y proceder a cambiarlos o a incrementar su dosis.
(1.11) Si no hay respuesta a esta modificación de laxantes formadores de masa y/o laxantes osmóticos, debe valorarse la posibilidad de añadir terapia de rescate con laxantes estimulantes, enemas de limpieza o supositorios (tratamiento de segunda línea).
(1.12) Si no responden a esta modificación, o se produce necesidad de incrementos progresivos de la dosis de laxantes, heces líquidas continuas para poder evacuar, dolor abdominal, o empeoramiento de patología del suelo pélvico, el paciente será remitido al digestólogo.
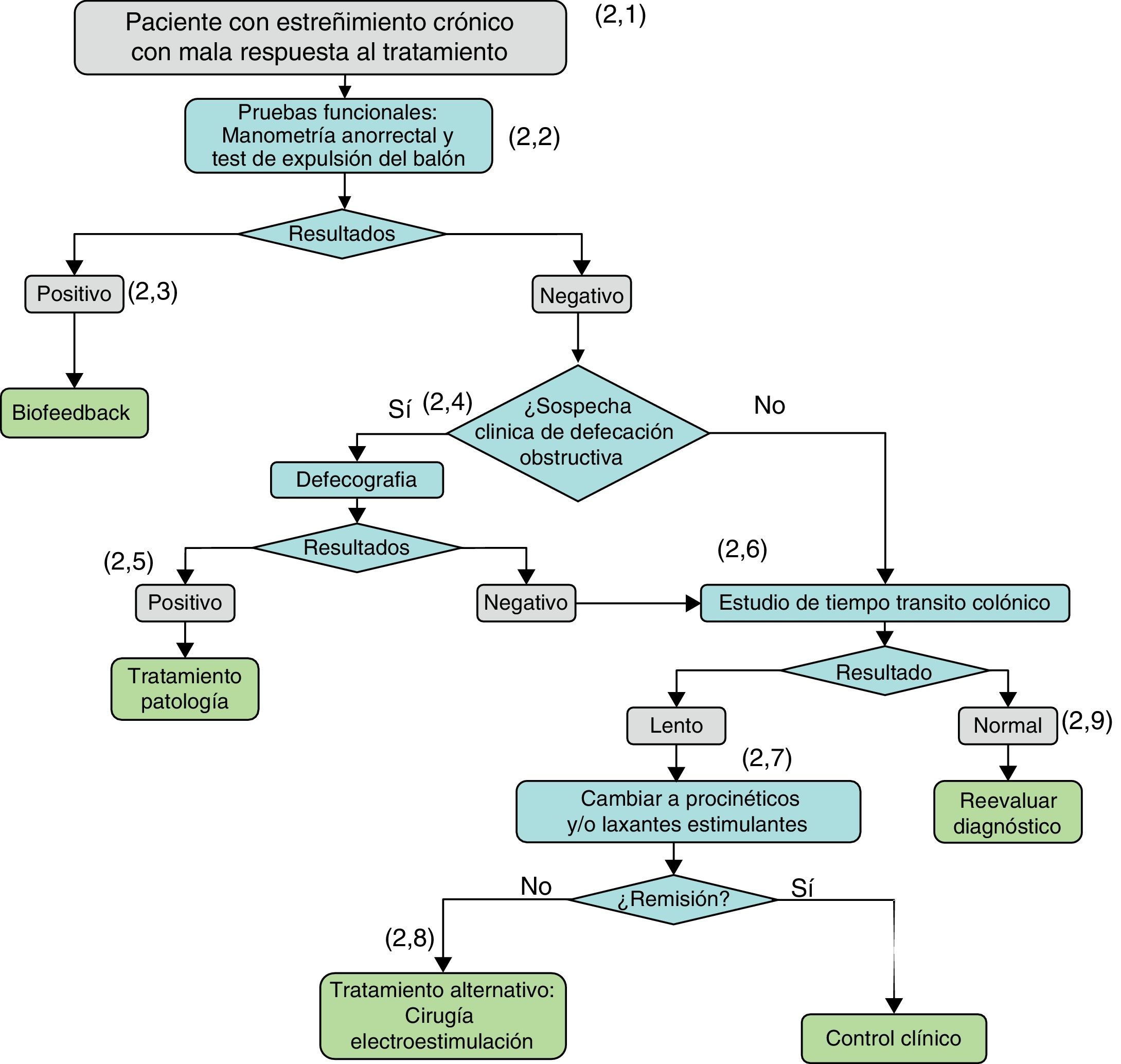
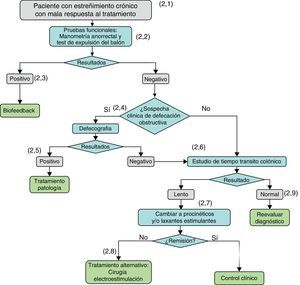
Diagnóstico y tratamiento del paciente que no responde a los laxantes formadores de masa ni a laxantes osmóticos.
(2.1) Cuando se ha descartado patología orgánica y/o toma de fármacos que producen estreñimiento y no hay respuesta a la medidas no farmacológicas (estilo de vida y medidas higienicodietéticas) ni a los tratamientos con laxantes formadores de masa y/o laxantes osmóticos, o las terapias de rescate no dan resultados satisfactorios, se debe sospechar que el estreñimiento está causado por una alteración de la función defecatoria y se debe derivar al digestólogo para estudio.
(2.2) Cuando se sospecha una alteración de la función defecatoria se debe realizar estudio funcional con manometría anorrectal (a aquellos pacientes que no se les hubiera realizado anteriormente) y un test de expulsión del balón.
(2.3) Si la manometría y/o el test de expulsión del balón demuestran una alteración de la defecación, se realizará tratamiento de la misma mediante biofeedback anorrectal.
(2.4) Si los resultados de la manometría y/o del test de expulsión del balón son negativos, o si el paciente persiste con estreñimiento una vez corregida una defecación disinérgica, se replanteará si persiste la sospecha clínica de defecación obstructiva (rectocele, enterocele), y en caso positivo se realizará una videodefecografía.
(2.5) Si la defecografía identifica la causa, se procederá al tratamiento etiológico.
(2.6) Si persiste el estreñimiento refractario al tratamiento, y/o si las pruebas realizadas hasta ahora persisten negativas, se determinará el tiempo de tránsito colónico (TTC). Un TTC lento puede ser consecuencia de alguna patología (metabólica, endocrina, enfermedad sistémica) o asociado a alteraciones neuropáticas o miopáticas de la pared colónica.
(2.7) Si el TTC es lento, se debe optimizar el tratamiento con laxantes, añadiendo procinéticos y/o laxantes estimulantes o secretores. Como medicación de rescate se pueden usar enemas de limpieza o supositorios.
(2.8) Si no hay respuesta a los laxantes procinéticos y a los laxantes estimulantes y secretores, se plantearán otros tratamientos: electroestimulación, cirugía.
(2.9) Si el TTC es negativo, se reevaluará al paciente y se valorará la posibilidad de diagnósticos alternativos.
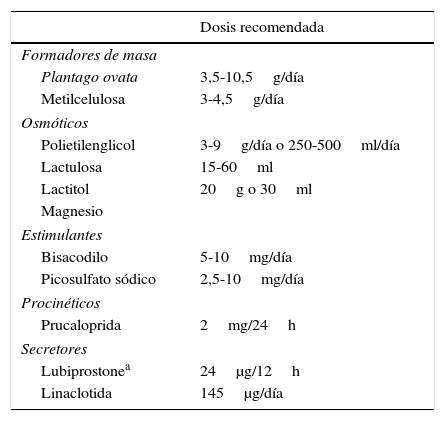
Clasificación de los diferentes tipos de laxantes
| Dosis recomendada | |
|---|---|
| Formadores de masa | |
| Plantago ovata | 3,5-10,5g/día |
| Metilcelulosa | 3-4,5g/día |
| Osmóticos | |
| Polietilenglicol | 3-9g/día o 250-500ml/día |
| Lactulosa | 15-60ml |
| Lactitol | 20g o 30ml |
| Magnesio | |
| Estimulantes | |
| Bisacodilo | 5-10mg/día |
| Picosulfato sódico | 2,5-10mg/día |
| Procinéticos | |
| Prucaloprida | 2mg/24h |
| Secretores | |
| Lubiprostonea | 24μg/12h |
| Linaclotida | 145μg/día |
En una gran mayoría de pacientes el diagnóstico de estreñimiento crónico idiopático se basa en la descripción de los síntomas y/o signos recogidos en la anamnesis y de los hallazgos de la exploración física. Se deben tener en cuenta 3 aspectos: 1)cumplimiento de los criterios diagnósticos de estreñimiento crónico; 2)determinación de las causas del estreñimiento, y 3)detección de signos de alarma (ver Parte 1). La exploración física incluye un examen abdominal, una inspección visual de la región perianal y rectal, y un tacto rectal que permite valorar el tono del esfínter anal, tanto en reposo como durante una maniobra defecatoria, si hay ocupación de la ampolla rectal y valorar la presencia de masas, prolapso, hemorroides, fisuras, rectocele, etc.
Pruebas complementariasAnalíticaUna revisión sistemática concluye que no hay evidencia de que una analítica general sea eficaz como prueba de rutina en los pacientes con estreñimiento1 y que el coste-utilidad de estos test probablemente sea muy bajo2. La analítica estará indicada en aquellos pacientes que presenten signos de alarma y en aquellos en que la historia clínica nos haga sospechar un posible trastorno causal del estreñimiento3. Algunas guías4,5 recomiendan como parte del estudio diagnóstico un hemograma con determinación de sideremia, ionograma, calcio y fósforo en suero, glucosa y hormonas tiroideas, además de aquellos test específicos que se juzguen necesarios en función de la sospecha clínica de la enfermedad causante del estreñimiento.
Pruebas de imagenColonoscopia. Diversos estudios han demostrado que el rendimiento diagnóstico de la colonoscopia en pacientes que presentan como única manifestación estreñimiento es similar al de la población asintomática6-9.
Las diferentes guías de práctica clínica indican la realización de una colonoscopia en todos los pacientes que presenten estreñimiento y signos y/o síntomas de alarma4,5,10 (ver Parte 1). Algunas de estas guías también indican la colonoscopia en aquellos pacientes con estreñimiento que no responden al tratamiento y en los pacientes mayores de 50 años o de menor edad y con antecedentes familiares de cáncer colorrectal que tras el inicio del estreñimiento no habían sido evaluados mediante colonoscopia4.
Enema opaco. No hay evidencia de que el enema opaco (2 estudios y 122 pacientes) sea eficaz como prueba de rutina en todos los pacientes con estreñimiento1. El enema opaco permite identificar la presencia de megacolon y megarrecto, y en niños con enfermedad de Hirschsprung permite conocer la extensión del segmento agangliónico. Sin embargo, dado que el enema opaco no permite la visualización directa y la toma de biopsias, su uso debería reservarse para aquellos casos en que la colonoscopia no se pueda realizar o genere dudas diagnósticas.
Pruebas funcionalesManometría anorrectal. La manometría consiste en la medición de las presiones en el canal anal y en el recto en reposo, y durante las maniobras defecatorias. Así mismo, permite evaluar la inervación anorrectal11, tanto intrínseca como extrínseca, el volumen y la sensibilidad del recto.
Se considera indicada en los pacientes que no responden al tratamiento con cambios de estilo de vida, agentes formadores de bolo, laxantes osmóticos y procinéticos. La manometría anorrectal es útil en pacientes con estreñimiento funcional que además tengan incontinencia fecal, fisura anal, enfermedad hemorroidal, rectocele…, dado que sería útil para diagnosticar disinergia12.
La manometría permite identificar diferentes tipos de disinergia del suelo pélvico (ver Parte 1)13, la presencia de alteraciones sensoriales rectales y patologías neurológicas, como la enfermedad de Hirschsprung, o la afectación de la inervación secundaria a enfermedades neurológicas. Así mismo, la manometría nos permite identificar a los pacientes que podrían beneficiarse del tratamiento del estreñimiento mediante biofeedback anorrectal14.
Test de expulsión del balón. El test de expulsión del balón es sencillo de realizar y ampliamente disponible. Consiste en la introducción de un balón en el recto que se infla con aire o líquido, y se le pide al paciente que lo evacúe. Idealmente el balón debe inflarse con un volumen que produzca sensación de deseo de defecar, y el paciente lo expulsará en un baño en condiciones de intimidad. La metodología para este test no está estandarizada15. El enfoque preferido es cuantificar el tiempo necesario para expulsar un globo rectal en la posición sentada; dependiendo de la técnica, los valores normales recomendados varían4.
El test de expulsión está indicado en los pacientes que no responden al tratamiento con cambios de estilo de vida, agentes formadores de bolo, laxantes osmóticos y procinéticos, en los que sospechemos que el estreñimiento está causado por una alteración de la defecación11.
Un estudio no controlado (106 pacientes con estreñimiento y 24 pacientes con trastornos defecatorios) ha evaluado la utilidad del test de expulsión del balón en el estreñimiento crónico para identificar disinergia defecatoria, mostrando una sensibilidad y especificidad del 87,5 y del 89% y unos valores predictivos positivos y negativos del 64 y del 97%, respectivamente16. Los autores concluyen que el test de expulsión permite identificar de forma muy sencilla a los pacientes que tienen un trastorno de la defecación y que se podrían beneficiar de un estudio completo de la función anorrectal con manometría para valorar la posibilidad de tratamiento con biofeedback16.
Determinación del tiempo de tránsito colónico. El tiempo de tránsito colónico se define como el tiempo que emplean las heces para pasar a través del colon. Su determinación se realiza mediante la ingesta de pequeños marcadores radioopacos de una sustancia plástica ligera (generalmente polietileno) y la posterior realización de radiologías simples de abdomen seriadas para cuantificar el tiempo de tránsito colónico. Existen diferentes protocolos; el más utilizado en España consiste en la toma de radiografías a los 4 y 7 días, en ocasiones incluso el décimo día17.
El tiempo de tránsito colónico está indicado en los pacientes que no responden al tratamiento con cambios de estilo de vida, agentes formadores de bolo, laxantes osmóticos y procinéticos11.
Esta prueba permite identificar a los pacientes que tienen estreñimiento por un tránsito colónico lento. Antes de considerar que el paciente tiene estreñimiento por un tránsito colónico lento (inercia colónica) se han de descartar —y en caso de que se confirme el diagnóstico tratar— los trastornos de la defecación (disinergia), los cuales también pueden causar un enlentecimiento del tránsito colónico18.
Otros test utilizados para evaluar los tiempos de tránsito colónico son la cápsula inalámbrica (smart pill) y los estudios gammagráficos. Resultados de una revisión sistemática (9 estudios) muestran que la cápsula en términos de sensibilidad, especificidad y curvas ROC presenta resultados similares con el tiempo de tránsito colónico medido con marcadores radiopacos y con los estudios gammagráficos. La cápsula es bien tolerada, tiene buen cumplimiento y evita los riesgos de la exposición a la radiación. Sin embargo, es más cara y en la mayoría de pacientes no está claro que proporcione un valor añadido15.
Defecografía. Existen 2 técnicas para identificar las alteraciones anatómicas: a)la fluoroscopia (radioscopia), que es una técnica muy accesible, rápida y que permite que el paciente esté cómodamente sentado, pero que irradia, y b)la resonancia magnética (RM), que tiene la ventaja de observar todos los órganos del suelo de la pelvis durante la defecación sin irradiar, pero que es de elevado coste y menos accesible que la fluoroscopia.
La principal indicación de estas técnicas es en pacientes con un trastorno de la defecación en los que se sospecha rectocele, enterocele o intususcepción como causa del mismo. También pueden usarse para diagnosticar disinergia del suelo pélvico, aunque se consideran test coadyuvantes, que no debe usarse como únicos en el diagnóstico del estreñimiento18. Permiten valorar la correcta rectificación del ángulo del recto y la relajación esfinteriana durante las maniobras defecatorias19.
TratamientoEl tratamiento no solo persigue aumentar el número de deposiciones, sino también que la evacuación sea completa, se realice sin esfuerzo, sin problemas de obstrucción recto-anal y que desaparezca la presencia de dolor y la distensión abdominal asociada. El objetivo fundamental es mejorar la consistencia y el volumen de las heces. La elección del tratamiento y el orden de su introducción dependerán de la etiología del estreñimiento crónico.
Medidas no farmacológicasLa mayoría de los pacientes que consultan por estreñimiento crónico presentan factores de riesgo relacionados con el estilo de vida (dieta baja en fibra, escasa hidratación y/o sedentarismo) (ver Parte 1), potencialmente modificables.
Educación sanitariaFomentar estilos de vida y reducir la dependencia de los laxantes. Adoptar un horario regular para la defecación, aprovechando los momentos de mayor motilidad del colon15. Disponer de tener un tiempo suficiente para defecar y adquirir una posición adecuada (cuclillas), entrenando los músculos pélvicos y esfínteres anales para conseguir realizar la maniobra expulsiva sin esfuerzos excesivos15.
Dieta rica en fibra. Diversos estudios han demostrado que la fibra mejora el estreñimiento funcional20-22. En un ensayo clínico aleatorizado (ECA) cruzado (40 pacientes) se muestra que 50g de ciruelas secas tomadas 2 veces al día durante 6 semanas aumentan el número de defecaciones semanales y la puntuación en la escala de Bristol y mejora la puntuación de síntomas asociados al estreñimiento y el esfuerzo defecatorio23. Los resultados de este estudio muestran que la ingesta de ciruelas secas es segura, agradable al paladar y que, comparado con el psyllium, es más eficaz en el tratamiento del estreñimiento de leve a moderada (ver apartado «Laxantes formadores de masa»).
En algunos pacientes, especialmente en aquellos con estreñimiento por tránsito lento, la dieta rica en fibra produce hinchazón abdominal y flatulencia24. Estos efectos pueden ser modulados empezando con pequeñas cantidades y aumentando lentamente la ingesta de fibra de acuerdo con la tolerancia y la eficacia25,26.
Muchos de los estudios disponibles presentan sesgos metodológicos con relación al diseño, el tamaño, los sujetos, la gravedad del estreñimiento, las intervenciones y las variables de eficacia evaluadas. Se necesitan nuevos estudios bien diseñados que evalúen el efecto de la dieta rica en fibra en el tratamiento del estreñimiento, teniendo en cuenta los eventos adversos.
- -
Se recomienda consumir alimentos con alto contenido en fibra soluble (frutas, verduras, hortalizas, legumbres, frutos secos, pan de centeno) (evidencia moderada, recomendación fuerte a favor).
- -
Se aconseja que la ingesta de alimentos ricos en fibra se realice de forma gradual para que el tracto gastrointestinal se pueda adaptar.
Aporte hídrico. Un ensayo clínico (117 pacientes) compara la ingesta diaria de fibra (25g) y agua (1,5-2l) con la ingesta de solo fibra27. En el grupo de fibra y agua se observa un mayor número de deposiciones semanales y una mayor disminución en el número de dosis de laxantes usados por semana.
No se dispone de estudios que evalúen los efectos indeseables de la ingesta de líquidos en pacientes con estreñimiento. El incremento de líquido es más importante en los pacientes deshidratados o que beben pocos líquidos que en pacientes correctamente hidratados.
Ejercicio físico. Diversos estudios muestran que el ejercicio físico (caminar, correr, ejercicios de resistencia) disminuye el tiempo de tránsito intestinal28-31, mientras que la inactividad física aumenta el tiempo de tránsito intestinal32. Otros estudios no muestran efectos del ejercicio físico sobre el tiempo de tránsito intestinal33,34.
Un ECA en personas de edad media con estilo de vida sedentario y con estreñimiento crónico (43 personas)30 no muestra cambios en el número de deposiciones semanales pero sí una disminución, estadísticamente significativa, del porcentaje de deposiciones duras, incompletas o que requirieran esfuerzo.
Los estudios disponibles son escasos y presentan sesgos metodológicos. Se requiere de ECA bien diseñados que evalúen los beneficios y riesgos de la actividad física. No obstante, la actividad física repercute positivamente en la salud.
Tratamiento farmacológicoEl tratamiento médico con laxantes por lo general comienza después del fracaso de modificaciones en la dieta y en el estilo de vida35. Actualmente se dispone de una gran variedad de opciones terapéuticas (anexo 3). La mayoría de los laxantes producen efectos secundarios, sobre todo dolor abdominal tipo retortijón, diarrea acuosa y distensión abdominal. Con frecuencia los diferentes laxantes producen acomodación y taquifilaxia y es necesario incrementar la dosis de forma progresiva y/o establecer periodos de rotación. En la elección del tratamiento inicial se debe considerar la eficacia, la seguridad, la conveniencia, el coste y la respuesta clínica15.
Según datos de una encuesta de ámbito europeo realizada en el año 2009, el uso de laxantes entre los pacientes con estreñimiento crónico es muy elevado, del 68%5. El tipo de laxante utilizado varía ampliamente entre los países participantes. Independientemente del tratamiento utilizado, el grado de satisfacción con los laxantes entre la población europea es bajo, situándose en promedio en un 28%. Según datos de la encuesta, en España la satisfacción se sitúa en el 19%, el porcentaje más bajo de todos los países participantes en la encuesta.
Laxantes formadores de masaLa fibra se puede tomar como suplemento. Se trata de polisacáridos no absorbibles que adecuadamente hidratados aumentan el volumen fecal favoreciendo la peristalsis. Estos laxantes mejoran el tránsito intestinal y la expulsión de las heces, de manera similar a lo observado con la fibra alimentaria. En esta categoría disponemos del psyllium (o ispágula, que se deriva de las cáscaras de Plantago ovata) y de diversos agentes semisintéticos como la metilcelulosa, el policarbofil cálcico y el dextrano (ver anexo 3).
Una revisión sistemática identificó 9 ECA realizados con psyllium (3 de ellos aleatorizados y comparados frente a placebo) y concluye que existe moderada evidencia para su uso36. Una revisión sistemática que evalúa el efecto de la fibra soluble en pacientes con estreñimiento (3 ECA con psyllium y un ECA con inulin y maltodextrim37) muestra que, en comparación con el placebo, la fibra soluble mejora los síntomas globales, el esfuerzo defecatorio, el dolor en la defecación y la consistencia de las heces, con un aumento en el número promedio de deposiciones por semana y una reducción en el número de días entre deposiciones. Los diferentes ECA no reportan efectos adversos. No obstante, la ficha técnica del psyllium señala calambres abdominales, estreñimiento, diarrea, obstrucción del esófago u obstrucción intestinal.
No se dispone de ECA con metilcelulosa frente a placebo en pacientes con estreñimiento crónico. Solo existe un ECA que compara el uso de metilcelulosa versus psyllium38. En este estudio se comparó el efecto de unidosis diarias de 1, 2 y 4g de metilcelulosa con 3,4g de psyllium en 59 pacientes con estreñimiento crónico. Se objetivó un aumento significativo respecto a las cifras pretratamiento en la frecuencia fecal y en el contenido sólido y líquido de las heces diarias para todas las dosis de metilcelulosa y psyllium ensayadas. No se dispone de ECA con policarbofil cálcico frente a placebo en pacientes con estreñimiento crónico. En una revisión sistemática36 se identifica un ECA que compara policarbofil cálcico versus psyllium y concluye que la evidencia para el uso de la policarbofil cálcico es insuficiente.
La revisión sistemática disponible más reciente39 no identifica nuevos ECA en relación a los suplementos de fibra y el estreñimiento crónico idiopático. Esta revisión también concluye que la calidad de la evidencia disponible sobre la eficacia del tratamiento del estreñimiento crónico idiopático con laxantes formadores de masa es moderada para los agentes naturales y baja para los semisintéticos, y la respuesta a estos laxantes no parece que sea superior a las medidas higienicodietéticas. Además, los laxantes formadores de masa pueden ocasionar molestias abdominales y otros efectos adversos, como sobrecarga de líquidos. El uso adecuado consiste en aumentar la dosis gradualmente.
Laxantes osmóticosLos laxantes osmóticos contienen iones o moléculas no absorbibles, por lo que crean un gradiente osmótico que favorece la secreción luminal de fluidos en el intestino. La hidratación de las heces y el aumento de su volumen permiten mejorar la peristalsis. Dentro de este grupo de laxantes se incluyen el polietilenglicol (macrogol), la lactulosa, el sorbitol, el glicerol y las sales de magnesio.
Dos revisiones sistemáticas comparan los laxantes osmóticos frente al placebo. La primera revisión (6 ECA) incluye 5 ECA que evalúan el polietilenglicol y un ECA que evalúa la lactulosa40. Globalmente, 149 de 396 pacientes (37,6%) asignados al grupo de laxantes osmóticos no respondieron a la terapia comparado con 193 de los 280 pacientes (68,9%) asignados al grupo placebo (RR=0,50; IC95%: 0,39-0,63) con un number need to treat (NNT) de 3 (IC95%: 2-4)40. No se encontró heterogeneidad significativa entre los estudios (I2=36%; p=0,18). Tres de los ECA informaron acerca de los síntomas, 2 de ellos sobre el esfuerzo defecatoria (118 pacientes) y 3 acerca de la dureza de las heces (269 pacientes)40. Los resultados indican una reducción significativa del riesgo de estos síntomas (RR=0,37; IC95%: 0,19-0,71, y RR=0,26; IC95%: 0,16-0,44, respectivamente)40. Estos ECA también han mostrado un efecto beneficioso en el número de deposiciones por semana en el grupo de los laxantes osmóticos, comparado con el grupo placebo (diferencia de medias=2,51 (IC95%: 1,30-3,71)40.
La segunda revisión disponible más reciente39 también identifica los 5 ECA para polietilenglicol, todos ellos con bajo riesgo de sesgo, y añade un segundo ECA para la lactulosa, situando a los 2 ECA con elevado riesgo de sesgo.
Solo 2 de los ECA evaluaron los efectos adversos (dolor abdominal, cefalea), y no se hallaron diferencias estadísticamente significativas entre el grupo de tratamiento y el grupo placebo39,40. El uso excesivo de laxantes osmóticos puede producir una sobrecarga de electrólitos y de volumen en pacientes con disfunción renal y cardíaca41.
Una revisión sistemática Cochrane (10 ECA y 868 pacientes) indica que el polietilenglicol es mejor que la lactulosa en cuanto a frecuencia de deposiciones por semana, consistencia de las heces, alivio del dolor abdominal y necesidad de productos adicionales contra el estreñimiento42. La revisión sistemática concluye que el polietilenglicol se debe utilizar en preferencia a la lactulosa en el tratamiento del estreñimiento crónico42.
Otros laxantes osmóticos no se han estudiado adecuadamente. Habitualmente se hace un uso excesivo de laxantes salinos (sales de magnesia). Las sales de magnesia son útiles cuando se necesita una deposición rápida. Los enemas de fosfato son útiles para la limpieza intestinal. Se deben evitar los laxantes que contienen magnesio en los pacientes con insuficiencia renal y hepática.
- -
Se recomienda el polietilenglicol como una opción de tratamiento en personas con estreñimiento crónico (evidencia moderada, recomendación fuerte a favor).
- -
Se recomienda la lactulosa como una opción de tratamiento en personas con estreñimiento crónico (evidencia baja, recomendación fuerte a favor).
- -
Se sugiere utilizar con preferencia el polietilenglicol frente a la lactulosa (evidencia moderada, recomendación débil a favor).
En España está comercializado el aceite de parafina y el docusato sódico. En general son sustancias poco agresivas y bien toleradas que favorecen la defecación al mejorar la consistencia de las heces mediante la emulsión del agua intestinal con la grasa del aceite. Estos laxantes se pueden utilizar de forma puntual y deben usarse con precaución en los pacientes con riesgo de aspiración, ya que se podría producir una neumonía lipoide. El aceite de parafina se utiliza poco en la población adulta, siendo su uso mayoritario en los niños43.
Laxantes estimulantesEstos laxantes incluyen sennósidos, bisacodilo, cáscara sagrada y aceite de ricino39. También se consideran estimulantes la glicerina y el docusato sódico. El bisacodilo y su derivado, el picosulfato sódico, son laxantes estimulantes derivados del difenilmetano. Estos laxantes son glucósidos inactivos que no se absorben en el intestino delgado y son hidrolizados en el colon por glucosidasas, dando lugar a moléculas activas que aumentan las ondas propulsivas y la secreción intestinal.
Una revisión sistemática (2 ECA) compara los laxantes estimulantes frente al placebo40. La revisión incluye un ECA que evalúa el bisacodilo44 y un ECA que evalúa el picosulfato durante 4 semanas45. Globalmente en estos 2 ECA, 202 de 480 (42,1%) pacientes asignados a tratamiento activo no respondieron al tratamiento comparado con 199 de 255 (78%) pacientes asignados a placebo (RR=0,54; IC95%: 0,42-0,69). El NNT fue de 3 (IC95%: 2-3,5)40. Estos ECA también han mostrado un efecto beneficioso en el número de deposiciones por semana en el grupo de los laxantes osmóticos, comparado con el grupo placebo (diferencia de medias=2,50 (IC95%: 0,93-4,07)40.
Solo en el estudio con bisacodilo se incluyeron todos los efectos adversos, y el RR de experimentar algún riesgo fue 1,94 (IC95%: 1,52-2,47). En los ECA que evalúan los laxantes estimulantes la diarrea ocurre con más frecuencia que en los que han evaluado los laxantes osmóticos (RR=13,75; IC95%: 2,82-67,14). Durante la preparación de la colonoscopia se han descrito efectos secundarios tales como dolor y distensión abdominal, sed, vómitos o vértigo46. Además se han descrito casos de severa rabdomiólisis e hiponatremia46. No obstante, estos problemas no se han asociado al uso del laxante en dosis terapéuticas.
La revisión sistemática disponible más reciente39 no identifica nuevos ECA con relación a los laxantes estimulantes. Los autores de esta revisión señalan que los otros laxantes estimulantes, aunque comúnmente utilizados por los enfermos, no se han estudiado de forma adecuada y no se pueden recomendar en este momento39.
- -
Se recomienda utilizar los laxantes estimulantes como opción de tratamiento de rescate (evidencia moderada, recomendación fuerte a favor).
- -
Se sugiere utilizar los laxantes estimulantes como una opción de tratamiento en personas con estreñimiento crónico que no han respondido a laxantes formadores de masa y/o osmóticos (evidencia moderada, recomendación débil a favor).
La prucaloprida es un agente procinético con actividad selectiva por el receptor de serotonina 5-HT4, con efecto estimulante del tránsito intestinal.
Una revisión sistemática (7 ECA, 2.639 pacientes) compara la prucaloprida frente al placebo40 en pacientes resistentes a otros laxantes o insatisfechos con el tratamiento. Solo 3 ECA tienen bajo riesgo de sesgos40. Globalmente, 1.288 de 1.796 pacientes (71,7%) asignados al grupo prucaloprida no respondieron a la terapia, comparados con 731 de los 843 pacientes (86,7%) asignados al grupo placebo (RR=0,82; IC95%: 0,76-0,88) y un NNT de 6 (IC95%: 5-9). La heterogeneidad entre los estudios fue significativa (I2=60%, p=0,02). El gráfico en embudo (funnel plot) mostró asimetría estadísticamente significativa (prueba Egger, p=0,04; prueba de Begg, p=0,07), sugiriendo riesgo de publicación40.
En los análisis de sensibilidad, la heterogeneidad dejaba de ser significativa cuando se analizaron solo los estudios con bajo riesgo de sesgo, los estudios que definían la respuesta al tratamiento como al menos 3 o más deposiciones completas y espontáneas a la semana, o aquellos ECA que utilizaron los criterios de ROMAII modificados40. Los análisis de acuerdo con la dosis de prucaloprida mostraron eficacia similar para la dosis de 2 y 4mg diarios.
En 6 ECA se incluyeron todos los efectos adversos, y el RR de experimentar algún riesgo fue de 1,14 (IC95%: 1,05-1,24), con un NNP=10 (IC95%: 6-29)40. Los efectos adversos de cefalea, náuseas y diarrea fueron estadísticamente significativos para el grupo de tratamiento con prucaloprida. No se han encontrado efectos adversos graves, aunque no se dispone de suficiente información sobre su eficacia y su seguridad a largo plazo40. Aunque en el momento actual los estudios específicos con prucaloprida en los ECA y en los estudios de seguimiento no han evidenciado alteraciones cardiovasculares, es importante en la práctica clínica tenerlos en consideración debido a su mecanismo de acción.
La revisión sistemática disponible más reciente39 identifica un nuevo ECA en relación con la prucaloprida e identifica un ECA que evalúa el velusetrag. En la misma línea esta revisión concluye que los agonistas 5-HT4, prucaloprida y velusetrag, son efectivos en el estreñimiento crónico idiopático, con muchos más estudios que apoyan la prucaloprida.
La European Medicine Agency (EMA) y el National Institute for Health and Care Excellence (NICE)47 plantean que la prucaloprida podría constituir una opción de tratamiento únicamente en mujeres (>18años) con estreñimiento crónico que han sido tratadas previamente con medidas higienicodietéticas y con al menos 2 tipos diferentes de laxantes orales (a la dosis máxima posible, durante al menos 6meses) sin conseguir un alivio adecuado, previamente a considerar la utilización de tratamientos más invasivos. NICE recomienda reevaluar a las pacientes a las 4 semanas de tratamiento con prucaloprida y suspenderlo en caso de ineficacia.
Laxantes secretoresLubiprostona. La lubiprostona es un compuesto que pertenece a la familia de las prostonas, que activa los canales de cloro tipo 2 (CIC-2) sin afectar a la proteína reguladora de la conductancia transmembrana de la fibrosis quística (CFTR, por sus siglas en inglés), aumentando así la secreción de cloro intestinal, sin alterar el equilibrio electrolítico sérico.
Una revisión sistemática (3 ECA, 610 pacientes) compara la lubiprostona frente al placebo40. Dos de los 3 ECA tienen riesgo de sesgos40. Globalmente, 151 de 335 pacientes (45,1%) asignados al grupo lubiprostona no respondieron a la terapia comparado con 184 de los 275 pacientes (66,9%) asignados al grupo placebo (RR=0,67; IC95%: 0,56-0,80) con un NNT de 4 (IC95%: 3-7)40. Al considerar la dosis de 24μg 2veces al día, el resultado de los 3 ECA se mantuvo similar (RR=0,64; IC95%: 0,55-0,76). Se dispone de pocos estudios para mostrar el gráfico en embudo (funnel plot).
Los 3 ECA evaluaron los efectos adversos, y la revisión sistemática muestra que la lubiprostona presenta efectos adversos significativamente superiores al placebo (RR=1,79; IC95%: 1,21-2,65) con un NNR de 4 (IC95%: 3-6)40. Tanto la diarrea (RR=4,46; IC95%: 1,28-15,48) como las náuseas (RR=7,27; IC95%: 3,76-14,06) fueron significativamente más frecuentes en el grupo que recibió lubiprostona40.
La revisión sistemática disponible más reciente39 actualiza los datos de esta revisión previa40. Identifica 2 nuevos ECA e incluye uno de ellos en su metaanálisis. De los 5 ECA, 2 presentan bajo riesgo de sesgo.
Un estudio prospectivo, multicéntrico, a largo plazo, no cegado que incluyó 248 pacientes con estreñimiento crónico compara la lubiprostona (48μg/día) versus placebo, durante 48 semanas. Los resultados muestran que la lubiprostona fue más eficaz que el placebo para reducir la gravedad del estreñimiento, distensión abdominal y malestar. Para minimizar el impacto de los efectos secundarios de ocurrencia de retiradas de tratamiento, el estudio permitió disminuir la dosis de lubiprostona48.
Linaclotida. La linaclotida es un péptido agonista del receptor de guanilato-ciclasa C (GC-C) presente en la superficie luminal del enterocito. La activación de la GC-C conlleva la activación del CFTR que da lugar a un aumento de la secreción de cloro y bicarbonato a la luz intestinal, lo que aumenta el volumen de secreción y acelera el tránsito intestinal.
La linaclotida ha sido recientemente aprobada por la Food and Drug Administration (FDA) estadounidense para el tratamiento del estreñimiento idiopático crónico, a dosis de 145μg/día15. En Europa la linaclotida no tiene indicación en el tratamiento del estreñimiento; solo se ha aprobado para SII-E.
Una revisión sistemática (3 ECA, 1.582 pacientes) compara la linaclotida frente al placebo40. Los 3 ECA tienen bajo riesgo de sesgos40. La variable dicotómica de respuesta en estos estudios exigía la presencia de ≥3DEC a la semana y un aumento de al menos un DEC por semana en comparación con el período pretratamiento. Globalmente, 860/1.089 (79%) de los pacientes asignados a linaclotida no respondieron al tratamiento, comparado con 468/493 (94,9%) de los pacientes asignados a placebo (RR=0,84; IC95%: 0,80-0,87), con un NNT de 6 (IC95%: 5-8)40. Se dispone de pocos estudios para mostrar el gráfico en embudo (funnel plot)40. El subanálisis de acuerdo con las dosis de 133 y 266μg/día demuestra una eficacia similar. Las variables cuantitativas, el dolor o las molestias, la distensión abdominal, la consistencia fecal valorada según la escala de Bristol y el esfuerzo defecatorio mejoraron de forma significativa respecto a placebo en los 3 ECA. La puntuación media en cuanto a satisfacción global con el tratamiento y la proporción de pacientes bastante o muy satisfechos con el tratamiento fueron significativamente superiores con linaclotida.
El número de efectos adversos fue similar para los grupos de tratamiento activo (33,6%) y placebo (31,9%). La aparición de diarrea fue más frecuente con la linaclotida (RR=3,08; IC95%: 1,27-7,48)40.
La revisión sistemática disponible más reciente39 no identifica nuevos ECA con relación a la linaclotida.
Otros tratamientosEnemas de limpiezaCuando los pacientes no responden a los laxantes orales y llevan varios días sin defecar se pueden valorar tratamientos con enemas de limpieza (1.500ml de agua en 25min), enemas comerciales (140-250ml de enemas salinos o minerales) y/o supositorios de glicerina o de bisacodilo.
Biofeedback (rehabilitación del suelo pélvico)El biofeedback es una técnica de tratamiento de aprendizaje o rehabilitación para adquirir el control del sistema de respuesta fisiológico por medio del entrenamiento. Se utiliza para corregir las contracciones inadecuadas de los músculos del suelo pélvico y del esfínter anal externo durante la defecación, en pacientes con estreñimiento crónico causado por disinergia o mala coordinación durante la defecación (ver Parte 1). Dos revisiones sistemáticas han incluido 8 ensayos clínicos no controlados o pobremente controlados en pacientes con disinergia49,50. En 4 de los estudios incluidos se compara el biofeedback con electromiograma (EMG) con otras técnicas de biofeedback (globo de presión, feedback verbal), y los 4 estudios más recientes comparan el biofeedback con laxantes u otros tratamientos (diazepam, botox, placebo). Estos estudios fueron realizados en hospitales altamente especializados. Los resultados del metaanálisis muestran que el biofeedback es más eficaz que el tratamiento con laxantes u otros tratamientos (OR=3,657; IC95%: 2,127-6,290; p<0,001) y que la eficacia del biofeedback con EMG es igual de eficaz que otras técnicas de biofeedback (OR=1,436; IC95%: 0,692-3,089; p=0,319)50. Ambas revisiones concuerdan en la mala calidad de los estudios49,50.
La revisión sistemática disponible más reciente39 identifica un nuevo ECA. Para los autores de la revisión los ECA o son poco claros o presentan un alto riesgo de sesgo debido a la incapacidad para cegar a los participantes por la naturaleza de las intervenciones, o la falta de información de los métodos utilizados para generar el programa de aleatorización u ocultar la asignación. En ninguno de los ECA se describieron efectos adversos.
Un estudio reciente muestra que las tasas de respuesta que se consiguen fuera de un ECA son solo discretamente inferiores51. Estos resultados se explican porque estas técnicas siempre deben ser realizadas por un profesional experto y experimentado.
Neuromodulación sacraEsta técnica se basa en el principio fisiológico de que la presencia de la actividad bioeléctrica en una vía neural puede modular una actividad preexistente en otra vía a través de interacciones sinápticas. Se lleva a cabo mediante la colocación percutánea de uno o más electrodos en las raíces sacras (generalmente S2-S3) a través de los agujeros sacros y la implantación de un dispositivo de estimulación debajo de la piel en las nalgas52.
La neuromodulación puede ser eficaz en pacientes con indicaciones muy individualizadas, pero aunque se han realizado diversos estudios53-59, la evidencia disponible es limitada. Se requieren estudios prospectivos para evaluar su función exacta y la seguridad en el manejo de pacientes con estreñimiento60 que además permitan conocer los eventos adversos asociados con esta técnica61.
Una revisión sistemática reciente muestra que la eficacia de la neuroestimulación va más allá de un efecto local sobre el área rectoanal, y que actúa tanto a través del sistema nervioso central como del autónomo, incrementando la aparición de ondas de gran amplitud en el colon y la sensibilidad visceral62. Los autores de esta revisión concluyen que, a pesar de los estudios disponibles, se desconoce qué pacientes se podrían beneficiar de la estimulación del nervio sacro62.
CirugíaEs un tratamiento de última opción que debe reservarse para casos muy excepcionales de pacientes con estreñimiento crónico con tiempo de tránsito colónico lento sin disinergia de la defecación, que son refractarios a todos los tratamientos y que presentan, a causa de este problema de salud, una afectación importante de la calidad de vida.
La técnica que se utiliza es la colectomía subtotal, que ha mostrado buenos resultados a corto y a largo plazo sobre el estreñimiento, el dolor abdominal y la calidad de vida en diferentes series a lo largo de los años60,63,64. La colectomía subtotal no está exenta de complicaciones. Aparte de las complicaciones relacionadas con la propia cirugía (infecciones, adherencias…), algunos pacientes pueden desarrollar diarrea, y no son infrecuentes los escapes nocturnos64.
Es importante tener en cuenta que estos pacientes pueden padecer una neuropatía generalizada, no limitada al colon, por lo que antes de indicar la cirugía es necesario hacer un estudio sobre la posible alteración de la motilidad a otros niveles del tracto digestivo, como el intestino delgado, para evitar cuadros de oclusión intestinal severa tras la cirugía.
Se han publicado otras técnicas quirúrgicas, como la ileostomía con enemas anterógrados, que tendría la ventaja de ser menos agresiva y reversible, pero no existen estudios controlados que avalen su eficacia60.
- -
La colectomía solo debe de plantearse como opción de tratamiento en personas con estreñimiento crónico refractario grave que no responde a otros tratamientos, y en las que se ha descartado una afectación extensa de la motilidad intestinal mediante pruebas especiales que incluyen la manometría gastrointestinal (evidencia baja, recomendación débil a favor).
Esta guía de práctica clínica ha contado con la financiación externa de Laboratorios Shire. Los patrocinadores no han influido en ninguna etapa de su elaboración.
Conflicto de interesesEl Dr. Serra es consultor de Norgine, y realiza conferencias y “advisory boards” para Allergan, Almirall y Reckit Benkiser.
Han actuado como revisores externos:
Carmen Vela Vallespín. Médico de familia. CAP del Riu Nord i Sud. Institut Català de la Salut. Santa Coloma, Barcelona.
Iván Villar Balboa. Médico de familia. CAP Florida Sud. Institut Català de la Salut, l’Hospitalet de Llobregat, Barcelona.
Mercè Barenys de Lacha. Gastroenteróloga, Hospital de Viladecans. Profesora de Gastroenterología. Universidad de Barcelona. IDIBELL Comité Científico.
Francisco Javier Amador Romero. Médico de familia. Centro de Salud Los Ángeles. Madrid.
Miguel Mínguez Pérez. Gastroenterólogo. Hospital Clínico Universitario de Valencia.
Esta guía de práctica clínica cuenta con el respaldo de la Asociación Española de Gastroenterología (AEG) y de la Sociedad Española de Medicina Familiar y Comunitaria (semFYC).