INTRODUCCIÓN
La enfermedad inflamatoria intestinal (EII), concepto que engloba básicamente la colitis ulcerosa (CU) y la enfermedad de Crohn (EC), es un trastorno crónico recurrente, cuya fisiopatología no se conoce del todo y en cuya patogenia participan factores genéticos y ambientales. Son diversas las opciones disponibles para su tratamiento, entre ellas principalmente 3 grandes grupos terapéuticos: los salicilatos, los corticoides y los inmunodepresores. En casos graves en que el tratamiento médico se muestre insuficiente y ante la aparición de determinadas complicaciones, asociadas más frecuentemente con la EC, es necesario recurrir al tratamiento quirúrgico. Recientemente ha aparecido una nueva modalidad terapéutica, la granulocitoaféresis (GCAP). Se ha señalado que la acción inmunomoduladora de este procedimiento permitiría controlar algunos casos de EII en que el tratamiento convencional resulta ineficaz.
Gracias a la colaboración de especialistas expertos en la materia, se ha elaborado este documento de consenso, con la finalidad de recopilar toda la información disponible en el momento actual sobre la GCAP, para emitir recomendaciones para su uso de acuerdo con el conocimiento disponible hasta la fecha. Este documento no pretende ser normativo, sino un instrumento de ayuda para el médico que atiende a pacientes con esta enfermedad y facilitar de este modo su manejo.
¿QUÉ SE CONOCE SOBRE LA GRANULOCITOAFÉRESIS?
A pesar de que no se conocen por completo los factores causantes de la primera manifestación de EII o de su recidiva, hay datos claros a favor de la asociación de los brotes agudos con un aumento en sangre periférica del número de granulocitos y monocitos/macrófagos, los cuales se ha observado que se encuentran en estado activado y tienen aumentada su vida media1-5. Del mismo modo se ha objetivado en pacientes con EII activa la presencia de concentraciones aumentadas de citocinas proinflamatorias en sangre periférica6-8. Por otro lado, la acción celular central de la inflamación intestinal es la infiltración del intestino por células inflamatorias, entre ella linfocitos y granulocitos, y macrófagos, que a partir de la secreción de mediadores inflamatorios como proteasas y radicales libres de oxígeno darán lugar a la aparición de daño tisular9.
Por otro lado, la concentración de neutrófilos en la mucosa intestinal también se ha relacionado de forma directa con la gravedad de la EII y definido como posible factor predictivo de recidiva, tanto en la CU como en la EC9. Tsukada et al10 determinaron que el perfil de citocinas de la mucosa intestinal, específicamente del ARN mensajero de la interleucina 8, se relacionaba con la actividad inflamatoria de la CU y era predictivo de respuesta positiva a la GCAP. Paralelamente, estudios recientes han observado que los valores fecales de neutrófilos y de calprotectina, proteína derivada de los neutrófilos, son marcadores de inflamación intestinal y predictores de recidiva en la CU9,11. Del mismo modo, la utilización de la gammagrafía con leucocitos marcados como técnica exploratoria de la extensión y actividad de la EII demuestra la importante implicación del reclutamiento de leucocitos circulantes hacia el intestino inflamado en la fisiopatología de esta enfermedad12.
En el momento actual se entiende la EII como una enfermedad en la que los neutrófilos/monocitos desempeñan un papel muy relevante. Gracias a su mecanismo inmunomodulador sobre la respuesta celular, la GCAP se presenta como alternativa terapéutica complementaria al tratamiento estándar de la EII.
¿CÓMO ACTUA LA GRANULOCITOAFÉRESIS?
El Adacolumn® es una columna de 335 ml de policarbonato/polipropileno (206 mm de largo ¥ 60 mm de diámetro) que contiene 200 g de gránulos de diacetato de celulosa (2 mm de diámetro) embebido de suero salino. La sangre del paciente se drena desde una vena del brazo y se filtra a través de la columna de abajo hacia arriba, para volver a una vena del brazo contralateral. La velocidad de perfusión es de 30 ml/min y la duración de las sesiones de 60 min. La pauta más utilizada de perfusiones es de una sesión a la semana durante 5 semanas consecutivas13. Durante el procedimiento se administra heparina para evitar problemas de coagulación en el sistema extracorpóreo.
Se cree que el mecanismo principal de adsorción de la GCAP está relacionado con la activación de la cascada del complemento, con la inducción de la adhesión de los granulocitos a la columna gracias a la interacción mediada por CD11b/CD18. Por otro lado, esta interacción interviene también en la activación de mecanismos reguladores de la respuesta inmunitaria innata14,15. En los pacientes que responden a la GCAP, se observa una clara disminución de todos los reactantes de fase aguda, velocidad de sedimentación globular y proteína C reactiva, entre otros16-19.
De todos modos, tras una sesión de GCAP no se observa una depleción masiva de leucocitos en sangre periférica, lo que indica que probablemente la GCAP actúa además induciendo la activación de diversos mecanismos antiinflamatorios, entre los que se incluyen la disminución en sangre periférica de la capacidad de los leucocitos de producir citocinas proinflamatorias como el factor de necrosis tumoral alfa y las interleucinas 1b, 6 y 820-23, el aumento del número de neutrófilos inmaduros (C10 negativos) con menor actividad proinflamatoria21, la disminución de la expresión de moléculas de adhesión en los leucocitos, que altera su capacidad para migrar a focos de inflamación de la mucosa intestinal21-24, y el aumento de la secreción por parte de los leucocitos de sustancias con actividad antiinflamatoria como la fracción soluble de los receptores I y II del factor de necrosis tumoral alfa25.
EXPERIENCIA EN EL USO DE LA GRANULOCITOAFÉRESIS
La granulocitoaféresis se ha aplicado en diversas enfermedades. Inicialmente se desarrolló para el tratamiento de pacientes con cáncer, con el objetivo de conseguir aumentar los linfocitos, que se creía deplecionados debido a su fagocitosis por los neutrófilos y monocitos14,26. En el momento actual, además de la EII, la enfermedad con que se tiene mayor experiencia en la aplicación de la GCAP es la artritis reumatoide27.
Las indicaciones aprobadas para el uso de la GCPA en España comprenden las siguientes entidades: CU, EC, artritis reumatoide, enfermedad de Behçet ocular y lupus eritematoso.
Colitis ulcerosa
Se describen a continuación los principales estudios publicados en que se ha evaluado la administración de GCAP en pacientes afectados de CU. La mayoría son estudios observacionales en los que ha participado un número limitado de pacientes y sin grupo control. A pesar de las limitaciones descritas, estos estudios proporcionan los primeros datos sobre la efectividad y seguridad de este procedimiento y suponen un estímulo para la realización de estudios de mayor envergadura.
Inicialmente, la GCAP se ha evaluado en pacientes con CU en quienes el tratamiento estándar a partir de la introducción de corticoides no ha sido efectivo. Son diversas las definiciones de corticorrefractariedad y corticodependencia utilizadas en los distintos trabajos. Entre los estudios evaluados, se definen los pacientes corticorrefractarios como aquellos que no presentan mejora tras la administración de tratamiento con corticoides orales o intravenosos a dosis altas en un período de 7 a 18 días28,29. Por otro lado, se considera corticodependientes a quienes no es posible disminuir la dosis de corticoides por debajo de los 10 mg/día debido al rebrote de la enfermedad29. En este grupo algunos autores incluyen también a los pacientes con 2 o más rebrotes de la enfermedad que requieren corticoides sistémicos en un período de 6 meses19. Por último, Hanai et al28 califican de corticodependientes a los pacientes que, respondiendo al tratamiento con esteroides orales durante 2 semanas o por vía intravenosa durante 7 días, presentan una recidiva al disminuir la dosis de esteroides por debajo de 15 mg/día.
Los primeros datos acerca de la eficacia de la GCAP provienen de un estudio llevado a cabo en Japón. Shimoyama et al30,31 realizaron un estudio prospectivo y aleatorizado en el que compararon a un grupo de pacientes con CU activa a los que se administró GCAP junto al tratamiento médico convencional manteniendo dosis similares de prednisolona (n = 53) con otro grupo que se mantuvo sólo con tratamiento médico incrementando las dosis de prednisolona (n = 52). El tratamiento convencional incluía prednisolona, sulfasalazina y ácido 5-aminosalicílico (5-ASA). Se aplicó una pauta estándar de 5 sesiones de GCAP. Al final del tratamiento la proporción de pacientes que alcanzaron la remisión o una mejora clínica endoscópica significativa fue del 58,5 frente al 44,2% de los casos, respectivamente (p = 0,045) (tabla I).
Pacientes con colitis ulcerosa corticorrefractarios
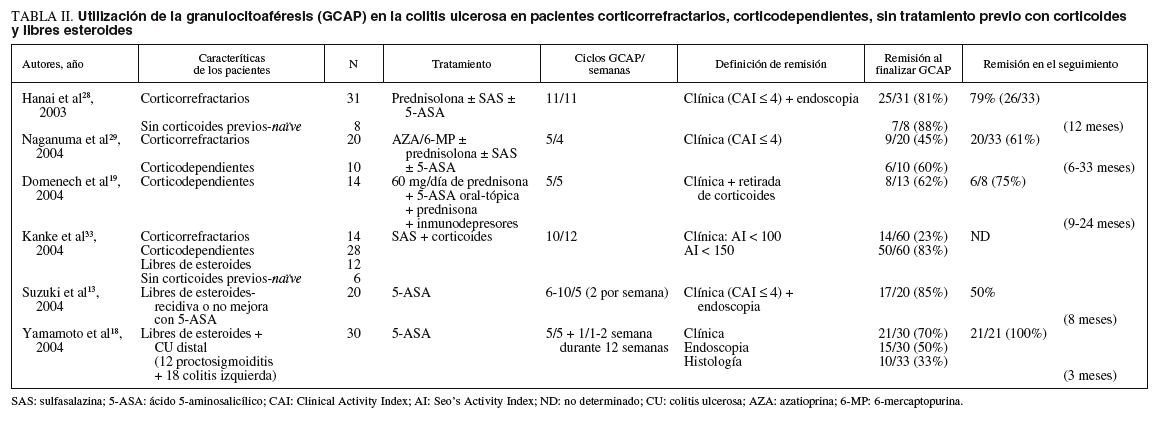
Diversos estudios han valorado la efectividad de la GCAP en pacientes corticorrefractarios. Hanai et al28 evaluaron a 31 pacientes en esta situación. Se realizó un número de sesiones de GCAP de acuerdo con la gravedad de los pacientes incluidos, con un máximo de 11 sesiones en 11 semanas. Se definió la remisión según criterios clínicos Clinical Activity Index (CAI) ¾ 4 y endoscópicos en función de la apariencia de la sigmoidoscopia Disease Activity Index (DAI). A las 12 semanas se observó remisión en un 81% de los pacientes y ésta se mantuvo en un 79% de los casos a los 12 meses. En otro estudio, Naganuma et al29 evaluaron a un grupo de 20 pacientes, en un 45% de los cuales se alcanzó la remisión tras 5 sesiones de GCAP en 4 semanas. La respuesta fue superior entre los pacientes con CU con actividad clínica moderada en comparación con la CU grave (el 70 frente al 20%, respectivamente) (tabla II).
Pacientes con colitis ulcerosa corticodependiente
Naganuma et al29 incluyeron en el mismo estudio citado anteriormente a un pequeño grupo de pacientes corticodependientes. En éstos la remisión clínica tras un ciclo de 5 sesiones de GCAP fue del 60%. En el 90% de los pacientes de este grupo se pudo disminuir la dosis de esteroides. En otro estudio publicado recientemente en el que participaron distintos centros de España, Domènech et al19 valoraron a 14 pacientes con CU corticodependiente sometidos a tratamiento de choque con 60 mg/día de prednisona y que a la semana de éste iniciaron una pauta estándar de GCAP. De acuerdo con la mejora del paciente, la dosis de esteroides se reducía a un ritmo de 10 mg por semana hasta su completa retirada en 6 semanas. En la semana 6, un 62% de los pacientes estaban en remisión, definida como un índice de actividad de Truelove modificado de 13 puntos o menos y eliminación completa de los esteroides. Un 75% de los pacientes que habían respondido a las 6 semanas mantuvieron la respuesta tras un seguimiento medio de 12,6 meses19. Estos datos confirman el efecto de la GCAP para conseguir disminuir más rápidamente la dosis de esteroides hasta su eliminación, con lo que se reducen los efectos adversos asociados a su uso prolongado (tabla II).
Hanai et al32 evaluaron a pacientes con CU incluidos consecutivamente que, tras la disminución de la dosis de corticoides, presentaron una recidiva. Compararon un grupo en el que se administró GCAP junto al tratamiento convencional, que se adaptó disminuyendo la dosis de esteroides en cada caso según necesidad (grupo I, n = 46), con otro grupo en el que se aumentó la dosis de esteroides al tiempo que se mantenía el tratamiento convencional (grupo II, n = 23). Se administraron en el grupo I un promedio de 2 sesiones de GCAP por semana durante 5 semanas. A las 12 semanas se determinó remisión clínica (CAI ¾ 4) en un 83 frente al 65% de los casos de los grupos I y II, respectivamente (p > 0,05), y la respuesta se mantuvo a los 6 meses en un 85 frente a un 70% (p > 0,05). La diferencia más importante entre ambos grupos fue la dosis media requerida de prednisolona, 10,4 ± 5,1 mg/día en el grupo I frente a 29,9 ± 12,2 mg/día en el grupo II (p < 0,05)32 (tabla I).
En otro trabajo, Kanke et al33 evaluaron a un grupo mixto de pacientes corticorrefractarios, corticodependientes y otros que no habían recibido esteroides previamente (naive en la bibliografía anglosajona), y realizaron a todos ellos un máximo de 10 sesiones en 12 semanas consecutivas. Se consiguió una mejora clínica de acuerdo con la reducción del índice de Seo (CAI < 150) en un 83% de los casos y la remisión fue total en un 23% (CAI < 100). La mejora se mantuvo durante un tiempo medio de 199 días (rango, 21-614) y se consiguió retirar totalmente los corticoides en un 68% de los pacientes con dependencia de ellos. La dosis media de prednisolona se redujo de 15,3 hasta 3,6 mg/día tras 10 sesiones de GCAP. Por otro lado, se observó una relación negativa entre la efectividad de la GCAP y la dosis de esteroides acumulada (0,38; p < 0,01) (tabla II).
Pacientes con colitis ulcerosa libres de esteroides
Se ha evaluado a este grupo de pacientes en un estudio realizado muy recientemente, aunque antes Hanai et al28 habían incluido ya a un pequeño grupo (n = 8) de pacientes con menor gravedad no tratados con esteroides durante el presente brote y a los que se administró GCAP al no presentar mejoría después de seguir tratamiento con mesalazina o sulfasalazina (tabla II). En este último estudio se administró un máximo de 11 sesiones de GCAP en 11 semanas y se observó remisión clínica (CAI ¾ 4) en el 88% de los casos en la semana 1228 (tabla II). Por otro lado, Suzuki et al15 llevaron a cabo un estudio con el objetivo principal de evaluar la eficacia de la GCAP como primera línea de tratamiento. Incluyeron a un total de 20 pacientes con CU de actividad moderada (n = 14) o grave (n = 6). Todos habían recibido tratamiento con 5-ASA (1,5-2,5 g/día) durante no menos de 8 semanas, sin obtener ninguna respuesta, antes de iniciar las sesiones de GCAP. Ningún paciente siguió tratamiento con corticoides. Se realizaron entre 6 y 10 sesiones de GCAP (2 sesiones/semana) durante 5 semanas consecutivas. Una semana después de la última sesión de GCAP, el 85% de los pacientes estaban en remisión clínica (CAI ¾ 4) y endoscópica. Después de 8 meses, el 50% de los pacientes se mantenían en remisión15 (tabla II).
Yamamoto et al18 evaluaron también a un grupo de pacientes libres de esteroides con colitis distal. La colitis distal, que se define como la lesión que afecta al colon por debajo del ángulo esplénico, representa un 60-85% del total de los casos de CU. En este estudio se incluyó a 12 pacientes afectados de proctosigmoiditis y a 18 con colitis izquierda. De forma concomitante, algunos pacientes mantuvieron tratamiento con sulfasalazina o mesalamina oral durante todo el estudio. En ningún caso se administró tratamiento con corticoides o inmunodepresores. Tampoco se permitió el uso de tratamiento tópico. Los pacientes siguieron GCAP en pauta estándar. En la semana 6 la remisión clínica, endoscópica e histológica se observó en un 70, un 50 y un 33% de los pacientes, respectivamente. Después de la quinta sesión de aféresis, se observaron cambios significativos en cuanto a la disminución del número de deposiciones y de la emisión de sangre y moco en las heces, aumento de la consistencia de éstas, desaparición del dolor abdominal y del tenesmo rectal. Presentaron mejoría clínica, endoscópica e histológica un 87, un 67 y un 43% de los pacientes, respectivamente. De acuerdo con la valoración subjetiva de los médicos, se definió «mucha mejoría», «mejoría», «mínima mejoría», «sin cambios» y «un poco peor» en un 23, un 50, un 13, un 10 y un 3% de los pacientes, respectivamente18. A 2 pacientes que no respondieron a las primeras 5 sesiones se les aplicaron 5 sesiones adicionales, tras las cuales la respuesta fue satisfactoria (tabla II).
Enfermedad de Crohn
El número de trabajos que han evaluado la eficacia y tolerabilidad de la GCAP en pacientes con EC es inferior, y todos ellos incluyen a grupos de pacientes muy reducidos.
Matsui et al5 evaluaron la respuesta a la GCAP en 7 pacientes con EC que no habían presentado respuesta al tratamiento convencional. Después de 5-6 sesiones semanales consecutivas, se objetivó remisión en 5 de estos pacientes. Cabe destacar que los pacientes que respondieron presentaban menor tiempo de evolución y lesiones limitadas al colon, mientras que los que no respondieron tenían mayor tiempo de evolución y presentaban afectación del íleon terminal. Cuenca et al34 informaron de 3 casos de pacientes con EC resistente al tratamiento convencional con esteroides e inmunodepresores que presentaron remisión tras la administración de una pauta estándar de GCAP, por lo que fue posible la disminución de la dosis de esteroides. Los 3 casos continuaban en remisión al año de seguimiento con sesiones de GCAP de mantenimiento (tabla III).
Domènech et al19 evaluaron a un grupo de 10 pacientes con EC corticodependiente, que, después de recibir
60 mg/día de corticoides durante una semana, al cabo de la cual la dosis se disminuyó de forma paulatina, iniciaron la pauta estándar de GCAP durante 5 semanas. Al final del tratamiento y tras la retirada completa de los corticoides, se evidenció remisión clínica en 7 casos (70%). Después de un seguimiento de 12 meses, un solo paciente continuaba en remisión (tabla III).
SEGURIDAD DE LA GRANULOCITOAFÉRESIS
Todos los estudios descritos en el apartado anterior han evaluado la tolerancia de la GCAP. En todos ellos fue escasa la aparición de efectos adversos (un 5-6% de los casos), que eran básicamente de carácter leve y no obligaron a interrumpir el procedimiento de aféresis. Entre los efectos adversos comunicados con más frecuencia figuran los siguientes: mareo, náuseas, fiebre, rubor y dolor abdominal. En un solo caso se observó una leve alteración de la función hepática18 y en 2 ocasiones se registraron complicaciones infecciosas, neumonía en un caso y septicemia del catéter en otro, que obligaron al ingreso hospitalario y a la administración de tratamiento antibiótico19.
Otros efectos adversos potenciales incluyen los propiamente asociados con el procedimiento de circulación extracorpórea. Entre éstos cabe mencionar la pérdida de sangre en el equipo para la aféresis, que puede estar determinada por el uso inapropiado de los anticoagulantes, así como las alteraciones en el recuento de células sanguíneas o de los fluidos corporales, que podrían dar lugar a la aparición de hipotensión o hipertensión. Asimismo pueden aparecer arritmias13.
A menudo, debido a la existencia de un acceso venoso difícil, la aplicabilidad del procedimiento se ve limitada tanto en niños como en adultos. La obesidad y la fragilidad vascular, asociadas frecuentemente al uso prolongado de corticoides, son las situaciones que con mayor frecuencia limitan el empleo de este procedimiento. Deberá valorarse de forma individualizada la utilización de vías venosas centrales para acceder al torrente sanguíneo.
SITUACIONES ESPECIALES
Embarazo
No se ha publicado ningún estudio que refiera la aplicación de la GCAP en pacientes con EII durante el embarazo, por lo que no puede recomendarse la utilización de este procedimiento en mujeres gestantes.
Pediatría
El manejo de la EII en pediatría no es fácil. A menudo la respuesta al tratamiento inicial con 5-ASA no es suficiente y se hace necesaria la introducción de corticoides en la pauta de tratamiento35. En estos casos no son pocos los pacientes que manifiestan corticorrefractariedad o corticodependencia. El uso prolongado de esteroides en la población infantil puede dar lugar a la aparición de efectos adversos graves. Son frecuentes el aumento de peso, la aparición de acné y de cambios en el estado de ánimo. De todos modos, son los trastornos relacionados con el retraso en el crecimiento los más preocupantes en relación con el uso de esteroides en población pediátrica36,37.
Son escasos los datos publicados sobre la efectividad y seguridad de la GCAP en población pediátrica. En forma de resumen, Martín de Carpi et al38 publicaron datos de una muestra de 6 niños (4 con CU y 2 con EC) refractarios o resistentes a los esteroides que habían seguido tratamiento estándar con GCAP. La tolerancia fue excelente en todos los casos, sin que se observara ningún efecto adverso o complicación. Al final de las 5 sesiones, 5 de los 6 niños tratados mostraron remisión (83%). Se evidenció en estos casos mejora de los síntomas clínicos y de los valores de laboratorio, así como de la exploración endoscópica e histológica. En 4 casos pudo reducirse la dosis de corticoides.
Tomomasa et al39 llevaron a cabo una valoración retrospectiva de 11 pacientes corticorrefractarios a los que se aplicó una sesión semanal de GCAP durante 5-10 semanas consecutivas. En 8 de los 11 casos (73%) al final del tratamiento se objetivó remisión clínica, además de mejora de los parámetros biológicos. Se observaron también mejoras endoscópicas y la dosis media de esteroides se redujo de 25,8 ± 4,9 hasta 13,8 ± 3,2 mg/día. Un 50% de los pacientes que respondieron a la GCAP mantenían la remisión tras un tiempo medio de 22,8 ± 18,1 días. La tolerancia al procedimiento fue muy buena; sólo se observó dolor de cabeza moderado en un caso39.
CONCLUSIONES y RECOMENDACIONES
En resumen, los datos disponibles hasta el momento indican un efecto beneficioso real de la GCAP en la EII activa. Los resultados son uniformes aunque las condiciones clínicas sean diferentes. Estos datos, junto con la excelente tolerancia al procedimiento, refuerzan su utilización en las situaciones que se describen en este documento.
Por otro lado, los estudios sobre la efectividad del procedimiento que se han revisado en este documento presentan múltiples limitaciones. En primer lugar, se han encontrado deficiencias importantes en las definiciones utilizadas para describir las situaciones de corticodependencia y corticorrefractariedad y de los pacientes libres de tratamiento con esteroides. En segundo lugar, la mayoría son estudios observacionales, sin grupo control y con un tamaño de la muestra reducido, lo que los limita a nivel C de evidencia.
Es necesaria la realización de estudios prospectivos con grupo control que permitan establecer mejor el lugar de la GCAP en el manejo de la EII. Del mismo modo, debe evaluarse la utilización de nuevas pautas de administración tanto en la inducción de respuesta en la fase aguda de la enfermedad como en su mantenimiento.
Las definiciones consensuadas para el tratamiento con esteroides40 se resumen en la tabla IV.
1. Corticodependencia. Comprende aquellas situaciones en que no es posible la retirada completa de los esteroides o cuando se producen 2 o más recidivas de la enfermedad en un período de 6 meses.
2. Corticorrefractariedad. Dentro de este grupo se incluyen 2 situaciones: a) los casos de CU con actividad intensa en que no existe respuesta al tratamiento con dosis altas (1 mg/kg/día) de esteroides por vía intravenosa durante una semana, y b) pacientes en brote de actividad no grave y con respuesta parcial a los corticoides orales, sin conseguir la remisión completa (situación denominada como enfermedad crónicamente activa).
3. Pacientes libres de esteroides. Los que nunca han utilizado esteroides para controlar su enfermedad (córtico-naïve) y aquellos a los que no se ha prescrito corticoides para el tratamiento de un brote actual de su enfermedad.
A pesar de las múltiples limitaciones de los estudios realizados hasta el momento, los datos preliminares que aportan permiten hacer las siguientes recomendaciones, que se resumen en la tabla V.
Colitis ulcerosa
Inducción de la remisión
Pacientes corticodependientes. Se recomienda el uso de GCAP en 2 situaciones:
1. Pacientes con toxicidad previa por corticoides o en los que éstos estén contraindicados debido a sus efectos secundarios. En estos casos se aconseja la introducción de azatioprina y puede indicarse la GCAP como tratamiento puente durante el tiempo en que aquélla no es aún efectiva. Son de especial interés en este grupo los pacientes pediátricos en quienes sean importantes los efectos secundarios de los corticoides relacionados con los trastornos del crecimiento.
2. Pacientes corticodependientes en los que la azatioprina se muestre ineficaz para el mantenimiento de la remisión o que presenten intolerancia a ella. La GCAP puede ser una alternativa previa al tratamiento quirúrgico. Son de especial interés los pacientes que cumplan estos requisitos y presenten una colitis izquierda.
Pacientes corticorrefractarios. No existen datos que permitan recomendar la utilización de GCAP en pacientes corticorrefractarios con enfermedad grave. En pacientes con actividad moderada de la CU y respuesta parcial a los corticoides, definidos anteriormente como crónicamente activos, podría considerarse, de forma individual, la indicación de GCAP.
Pacientes libres de esteroides. Se recomienda la GCAP en los pacientes en quienes el tratamiento con corticoides esté contraindicado por cualquier motivo o que presenten efectos secundarios graves. Serán de especial interés en este grupo los pacientes en edad pediátrica.
Mantenimiento de la remisión
En los pacientes con fracaso del tratamiento inmunodepresor (azatioprina), para el mantenimiento de la remisión puede utilizarse la GCAP, realizando una aféresis al mes, como paso previo a la cirugía.
Enfermedad de Crohn
Las pautas evaluadas hasta el momento indican la efectividad de la GCAP para inducir la remisión, pero no para mantenerla. Puede considerarse de forma individualizada el uso de GCAP para la inducción de la remisión en la EC en que haya fracasado el tratamiento convencional o en pacientes que presenten contraindicaciones formales para éste.
Dada la ausencia de datos, no puede recomendarse el uso de la GCAP en pacientes embarazadas.
Es necesario realizar estudios prospectivos con grupo control que permitan establecer mejor el lugar de la GCAP en el tratamiento de la EII. De la misma manera, debe evaluarse la utilización de nuevas pautas de administración tanto en la inducción de respuesta en la fase aguda de la enfermedad, como en su tratamiento. De todos modos, también se recomienda recoger la experiencia personal con GCAP, para poder disponer de datos observacionales, siempre útiles para corroborar los datos procedentes de estudios controlados.