DEFINICIÓN
La incontinencia anal (IA) es la pérdida del control voluntario del paso del contenido fecal o gaseoso a través del ano. Debe considerarse patológica a partir de los 4 años de edad en un sujeto con un desarrollo mental normal. Debemos distinguir 2 tipos: la orgánica, producida como consecuencia de alteraciones estructurales anatómicas o neurológicas, y la funcional. Por consenso, siguiendo los criterios de Roma II1, la IA funcional se define como la «existencia de escape involuntario de material fecal, como mínimo una vez al mes, en un individuo con edad mental mayor de 4 años asociada a impactación fecal y/o diarrea, y siempre en ausencia de disfunción anal secundaria a lesiones estructurales». Existen 3 tipos de incontinencia: incontinencia por urgencia, incontinencia pasiva y ensuciamiento fecal. Además, según las características del contenido se subdivide en incontinencia a gases, heces líquidas o heces sólidas.
EPIDEMIOLOGÍA
Se estima que, en la población general, entre un 2,2 y un 15,3% de los individuos presentan episodios de IA2-6, cuya prevalencia es más elevada en mayores de 65 años (7%), en pacientes institucionalizados (45-47%) y en determinadas patologías como espina bífida (80%), esclerosis múltiple (51%), diabetes mellitus (20%) y síndrome del intestino irritable (20%)7. Aproximadamente un tercio de los pacientes con IA no consultan a su médico por este síntoma8, y el 52% de las mujeres que presentan diarrea tienen IA, pero menos de la mitad la relatan a su médico9. En algunos países, la ocultación de este síntoma al médico llega a ser de hasta un 64,7% en mujeres5; por ello se desconoce la prevalencia real.
MECANISMOS PATOGENOS
La continencia anal depende fundamentalmente de la integridad funcional y anatómica de todas las estructuras que preservan la retención y de la capacidad que adquiere el ser humano para evacuar en el momento socialmente adecuado. En condiciones normales, las heces llegan al recto una o 2 veces al día mientras que los gases lo hacen con mayor frecuencia. El recto posee características viscoelásticas que permiten la acomodación del contenido y presorreceptores que advierten al sistema nervioso central de la llegada de heces/gases. El canal anal está permanentemente cerrado por la acción contráctil permanente del esfínter anal interno (músculo liso), del esfínter anal externo y del músculo puborrectal (músculos estriados). Esta acción muscular mantiene una barrera presiva (60-80 mmHg) que aumenta entre 2 y 3 veces su valor cuando voluntariamente se contrae la musculatura estriada. La llegada de material al recto desencadena, por incremento presivo, un acto reflejo a través del plexo mientérico que produce la relajación del esfínter anal interno y permite que una cantidad mínima del contenido rectal se ponga en contacto con la mucosa del canal anal proximal y estimule receptores sensibles a cambios térmicos, pH, etc., de tal manera que el individuo percibe, por aprendizaje, sus características fisicoquímicas. Si las circunstancias no son apropiadas para la expulsión se contraen voluntariamente los esfínteres estriados, la muestra pasa al recto, éste se adapta (disminuye la presión) y, sin necesidad de mantener voluntariamente contraída la musculatura esfinteriana estriada, tenemos memorizada la existencia y las características del contenido (gas, líquido o sólido) y elegimos el momento y la forma adecuados para la expulsión. Esquemáticamente, para que la continencia se mantenga es necesario: a) que el volumen, la consistencia y la frecuencia de llegada del contenido sean normales; b) que se preserve la capacidad viscoelástica del recto; c) que los mecanismos sensitivos rectales y anales estén intactos; d) que la función de los esfínteres anales interno y externo y del músculo puborrectal sea suficiente, y e) que la capacidad cognitiva y conductual del individuo sea la correcta para mantener la continencia.
CAUSAS DE INCONTINENCIA ANAL
Las causas de IA son, en general, multifactoriales y difieren en función del sexo, la edad y las enfermedades sistémicas o psiquiátricas asociadas (tabla I). En la población infantil predomina la impactación fecal y es más frecuente en el sexo masculino. Uno de los factores más frecuentes de incontinencia son las lesiones neurológicas y estructurales esfinterianas producidas durante el parto. La existencia de lesión muscular esfinteriana visible (desgarro grado III) se asocia a primiparidad, peso del feto mayor de 4 kg, posición occipitoposterior y utilización de fórceps. La rotura del esfínter anal externo tras desgarros grado III causa IA o urgencia fecal en el 47% de los pacientes10 y se mantiene a los 5 años del parto en el 40%11. Hasta el 13% de las primíparas y el 23% de las multíparas experimentan algún síntoma defecatorio tras el parto, fundamentalmente urgencia defecatoria e incontinencia fecal12; el 80-83% de las mujeres primíparas cuyo parto se realiza asistido con fórceps presenta lesiones de los esfínteres anales por ecografía12,13. La existencia de síndrome del intestino irritable contribuye a incrementar la presencia de incontinencia a gases tras el parto (el 35 frente al 13%)14. Sin embargo, la relación temporal entre existencia de lesiones esfinterianas mínimas y la presencia de IA no está claramente establecida; en la mayoría de las mujeres con antecedentes de partos que presentan IA y lesiones esfinterianas detectadas por ecografía, la incontinencia aparece en edades tardías (2 o 3 décadas tras el parto)3, por lo que debe de haber factores asociados que precipitan la clínica (edad, cirugía anal, menopausia, cambios de hábito defecatorio).
La esfinterotomía lateral interna produce IA en el 45% de los sujetos (el 53,4% de las mujeres y el 33,3% de los varones)15; sin embargo, en la mayoría de los casos es leve y transitoria, de manera que a los 5 años de la cirugía únicamente el 6% presenta incontinencia a gases, el 8% ensuciamiento y el 1% incontinencia a heces sólidas. La esfinterotomía abierta produce más episodios de ensuciamiento y de IA que la cerrada (el 26,7 frente al 16,1% y el 11,8 frente al 3,1%, respectivamente)16.
La fistulotomía por lesión de uno o más esfínteres (interno, externo, músculo puborrectal) y la hemorroidectomía (esfínter interno) son, asimismo, causa de incontinencia en ambos sexos17,18.
La alteración de la distensibilidad rectal por inflamación (actínica o inflamatoria) produce incontinencia por urgencia. En los pacientes con enfermedad de Crohn perineal se asocian lesiones esfinterianas y en todos los casos puede coexistir diarrea como factor precipitante.
Los pacientes sometidos a resección rectal o colónica, fundamentalmente cuando se realiza pancolectomía con anastomosis ileoanal con reservorio (colitis ulcerosa, poliposis familiar etc.), presentan con frecuencia incontinencia a heces, predominantemente nocturna, por ausencia de capacidad de almacenamiento, presencia de heces líquidas y, en ocasiones, lesión del esfínter interno inherentes al tipo de cirugía.
En la esclerosis múltiple hasta en un 51% de los pacientes se observa incontinencia19; las causas son multifactoriales y están relacionadas con la existencia de debilidad del esfínter anal externo y el grado de incapacitación (fatiga, debilidad muscular generalizada, espasticidad e imposibilidad de movilización).
DIAGNÓSTICO
El diagnóstico de incontinencia se debe establecer mediante un interrogatorio minucioso en todos los pacientes que acuden a la consulta con enfermedades o manifestaciones clínicas que hagan pensar en la existencia de IA, dado que frecuentemente se tiende a ocultar o a infravalorar el problema por pudor o vergüenza5. Cualquier paciente que acuda a consulta con diarrea crónica, urgencia defecatoria, estreñimiento grave, enfermedad neurológica sistémica, diabetes de larga evolución, antecedentes de cirugía anorrectal o partos vaginales múltiples o complicados debe ser interrogado de forma estructurada y utilizando una terminología individualizada culturalmente acerca de la existencia de manchado o ensuciamiento de ropa interior, escape de gases o heces o utilización de pañal protector. A menudo es la familia quien mejor nos explicará el problema y su gravedad. Existen diferentes encuestas protocolizadas que evalúan la gravedad de la incontinencia dando un valor numérico empírico a cada respuesta20-24. Básicamente se pregunta si la incontinencia se produce a gases, heces líquidas o heces sólidas, la frecuencia de los episodios, si se acompañan de sensación (urgencia defecatoria o sensación sin que el paciente tenga tiempo para llegar al aseo), la necesidad de llevar compresas o pañales de protección, la utilización de astringentes y la frecuencia en que los episodios de incontinencia condicionan las actividades cotidianas.
La exploración física aporta información inmediata sobre posibles causas de la incontinencia. La inspección del ano en reposo y durante maniobras de defecación permite evaluar la existencia de lesiones dérmicas, ensuciamiento, cicatrices, adelgazamiento del tabique rectovaginal, ano complaciente, prolapso o deformidades anatómicas, etc. Con el tacto anorrectal se puede detectar la existencia de fecalomas y evaluar la presión que sobre el dedo ejercen las paredes del canal anal en reposo (indica la capacidad del esfínter anal interno) y tras la maniobra voluntaria de retención (capacidad del esfínter anal externo y músculo puborrectal).
ESTUDIOS FUNCIONALES Y ANATÓMICOS
Endoscopia
La colonoscopia es imprescindible en los pacientes en los que existan cambios del hábito defecatorio o signos clínicos de alarma que hagan pensar en la presencia de una patología orgánica (enfermedad inflamatoria, neoplasias, etc.).
Manometría anorrectal
Es el estudio de elección para conocer objetivamente la capacidad funcional de la barrera presiva del canal anal en reposo (esfínter anal interno) y tras contracción voluntaria (esfínter anal externo y músculo puborrectal), la capacidad, distensibilidad y sensibilidad rectales y, además, el comportamiento reflejo rectoanal a la distensión del recto y durante la tos.
Ecografía anal y resonancia magnética
Permiten evaluar anatómicamente los esfínteres anales interno y externo y el músculo puborrectal. Objetivan lesiones estructurales (adelgazamiento, secciones, pérdida de tejido muscular, etc.) que pueden explicar las alteraciones funcionales detectadas por manometría. La resonancia magnética define anatómicamente con mayor precisión que la ecografía el suelo pélvico en su totalidad; es superior a ésta en la evaluación del esfínter anal externo, pero no en la del esfínter anal interno.
Latencia motora terminal del nervio pudendo
Mide la conducción distal del nervio pudendo y, por tanto, es un método para valorar la existencia de neuropatía distal.
TRATAMIENTO
El objetivo final del tratamiento del paciente con incontinencia es mejorar la calidad de vida y conseguir el control de la defecación.
Tratamiento médico
Debe instaurarse, siempre que se conozca, sobre la enfermedad de base; esto es especialmente importante en los pacientes con diabetes mal controlada, enfermedad inflamatoria intestinal o diarrea secundaria de cualquier causa.
Medidas generales
Deben aplicarse en todos los pacientes con IA porque pueden mejorar la calidad de vida de manera importante. La mayoría de los pacientes tiene un gran pudor a la hora de manifestar su síntoma y gran vergüenza ante los demás por temor a que adviertan olores o suciedad. El médico debe ganarse la confianza del paciente dándole consejos terapéuticos que aumenten su seguridad de que puede controlar la defecación, conseguir defecar en el tiempo y momento socialmente adecuados, prevenir los episodios de escape o disimularlos de manera tal que no los perciban otras personas. Para ello es de gran ayuda, conociendo el contexto cultural y laboral de cada paciente, explicar meticulosamente la utilidad del uso de pañales de continencia, tapones rectales y tapones anales, de los programas de estimulación de la defecación domiciliaria (consiguen mantener el recto vacío el máximo de tiempo posible), del empleo de astringentes (loperamida, codeína) a dosis altas como prevención, de medidas de limpieza sencillas y accesibles (toallitas húmedas), de llevar consigo ropa interior de repuesto, de frecuentar locales en los que el aseo sea accesible y cómodo, y de evitar todo tipo de alimentos que puedan incrementar el gas intestinal o desencadenar la defecación. Cuando el paciente utiliza astringentes a dosis elevadas, puede presentar secundariamente estreñimiento, que debe tratar con laxantes rápidos (enemas, supositorios), de manera que pueda controlar el momento de la defecación. Estas medidas son muy importantes en pacientes no institucionalizados que llevan una vida social normal.
En los pacientes con impactación fecal (niños y pacientes encamados), el tratamiento fundamental, tras la desimpactación, consiste en estimular la defecación diariamente con laxantes (orales, enemas, supositorios), así como establecer un horario regular de defecación. Con estas medidas se consigue controlar la evacuación en más del 60% de los casos25.
Biofeedback
El biofeedback es un tratamiento que se basa en el control de la continencia a través del aprendizaje del cierre del canal anal mediante la contracción de la musculatura estriada ante la mínima percepción de ocupación rectal. Este tratamiento, que carece de efectos secundarios, consigue evitar la incontinencia en el 48,6% de los pacientes y mejorarla en el 71,7%26. Está indicado en pacientes con incontinencia que presentan una capacidad intelectual normal, no sufren de enfermedades neurológicas graves ni de alteraciones conductuales negativas. Recientemente, Norton et al27 han publicado el primer estudio aleatorizado y controlado que compara, en 171 pacientes con IA, 4 tipos de actitudes terapéuticas médicas. En dicho trabajo el biofeedback no aumentó el porcentaje de mejoría respecto a los pacientes que sólo fueron tratados con medidas conservadoras y conductuales (el 53 frente al 54%). No hubo diferencias significativas entre los grupos al analizar los episodios de incontinencia, la calidad de vida y la escala de ansiedad-depresión. Este estudio, único de momento, es suficiente para subrayar la necesidad de disponer de equipos especialmente entrenados en el tratamiento de la IA, dado que consiguen beneficios terapéu-ticos con medidas conservadoras, sin necesidad de biofeedback, con la misma eficacia.
Tratamiento quirúrgico
La cirugía es el mejor tratamiento cuando existe rotura del esfínter anal externo tras traumatismos, fundamentalmente desgarros obstétricos28; la esfinteroplastia (solapamiento de extremos) es la mejor opción. Si existe una lesión neurológica grave, los resultados son peores y hay que recurrir a técnicas quirúrgicas más complejas. La elección de transposición de músculos (gracilis, glúteos) como neoesfínteres, con o sin estimulación eléctrica, depende de la experiencia de los equipos quirúrgicos y del grado de lesión. La implantación de esfínteres artificiales está aún en fase de consolidación debido al porcentaje elevado de fracasos. En pacientes en los que no es posible ningún otro tipo de tratamiento y su calidad de vida es mala, en ocasiones es necesario realizar una colostomía o una ileostomía de descarga.
PRONÓSTICO
Se desconoce la historia natural de la enfermedad y la mayoría de los estudios valoran la eficacia terapéutica con seguimientos cortos y catalogan como pacientes que responden al tratamiento a aquellos que mejoran de los síntomas, dado que la curación completa se alcanza en porcentajes muy pequeños. Por ello, se considera que la mayoría de los pacientes continuará con IA el resto de su vida en diferente grado de gravedad. En este sentido, los escasos estudios con seguimiento a largo plazo han observado que el 25% de los pacientes que han completado tratamiento con bio-feedback o con ejercicios de suelo pélvico no han conseguido mejoría alguna a los 26-56 meses29; únicamente el 6% de pacientes intervenidos mediante esfinteroplastia se considera totalmente continente a los 48-141 meses tras la cirugía, presentando incontinencia a heces sólidas o líquidas el 54%30, y sólo el 55-56% de pacientes considera que ha mejorado tras una graciloplastia dinámica a los 2 años de seguimiento31. Datos inquietantes procedentes de Japón32 relacionan la existencia de incontinencia (urinaria y fecal) con un aumento de la mortalidad en pacientes mayores de 65 años, observando que la presencia de incontinencia grave es un factor de riesgo independiente de muerte.
CALIDAD DE VIDA EN PACIENTES CON INCONTINENCIA ANAL
Todos los grupos de trabajo, históricamente, observaban que la IA tenía un gran impacto sobre la calidad de vida de los pacientes y asociaban empíricamente que, a mayor gravedad de la incontinencia, más repercusión tenía ésta sobre diferentes hechos sociales y personales, pero sólo en los últimos años se ha empezado a medir de forma objetiva mediante cuestionarios genéricos o específicos la repercusión que la incontinencia (en diferentes tipos y grados de gravedad) tiene sobre la calidad de vida y los cambios que experimentan los pacientes tras el tratamiento. De forma indirecta, valorando la importancia que tienen los síntomas intestinales sobre la calidad de vida en un estudio poblacional con 10.116 sujetos mayores de 40 años, se observó que el 51,7% de los pacientes con IA grave (ensuciamiento varias veces al mes) refería gran impacto de los síntomas sobre su calidad de vida, frente al 2,9% de los individuos que no presentaban IA (odds ratio de 12,4)4. La forma de medir la calidad de vida en pacientes con IA ha sido diferente en función del cuestionario utilizado; la manera más sencilla ha sido preguntar directamente al individuo cuánto influía la IA en su calidad de vida (nada, algo, mucho) y/o con qué frecuencia (desde nunca hasta siempre). Este tipo de preguntas no es capaz de discriminar los aspectos concretos de la vida alterados por la enfermedad, por lo que en ensayos clínicos o estudios específicos sobre la repercusión de la IA se utilizan cuestionarios, validados o no, que miden el estado de salud y la calidad de vida en diferentes dominios (actividad, función social, función física, etc.). Lo ideal sería disponer de un sistema de medición sencillo que evaluara el impacto concreto que la IA tiene sobre el individuo, que fuera capaz de medir la diferencia entre padecer o no IA, discriminar según la gravedad y tipo de IA, y muy sensible a los cambios producidos tras el tratamiento. En los últimos años se han utilizado 4 tipos de cuestionarios: a) los que miden la gravedad de la IA mediante preguntas sobre la frecuencia o intensidad con que los episodios de IA interfieren en la calidad de vida; b) los que utilizan sistemas de medición de salud y calidad de vida en función de síntomas gastrointestinales; c) los que emplean sistemas de medición de salud y calidad de vida genéricos, y d) los cuestionarios específicos de interferencia de la IA en la calidad de vida.
Evaluación de la calidad de vida en pacientes con incontinencia anal mediante preguntas específicas en el contexto de cuestionarios de gravedad de esta enfermedad
En 1991, en una reunión mundial de consenso en Roma33, se propuso que había que evaluar al paciente con IA mediante un cuestionario uniforme, en el que se incluían preguntas sobre cuánto interfería la enfermedad en su vida social, laboral y en las relaciones sexuales, por separado, la existencia de escape de gases, de heces líquidas y de heces sólidas. Los pacientes tenían un rango de respuesta del 0 (nunca) a 10 (lo peor). Esta clasificación, que no llegó a utilizarse, fue el primer intento de evaluar la importancia de la repercusión que la IA tenía sobre la vida cotidiana. En 1993, Jorge y Wexner20 proponen un sistema de puntuación (de 0 a 20) para evaluar la gravedad de la IA que incluye una pregunta sobre la frecuencia en que los episodios de IA alteran el estilo de vida (tabla II); dada su sencillez, este cuestionario, conocido como escala de Wexner, ha sido ampliamente utilizado34-38. Una puntuación de 9 o más en esta escala se asocia con una baja puntuación del índice de calidad de vida gastrointestinal (menor de 105)34, o sea, el confinamiento domiciliario y poca actividad social. Estos hallazgos llevan a utilizar el punto de corte 9 como medida indicadora de la repercusión en la calidad de vida y, por tanto, como orientación del médico de cara a ofrecer medidas terapéuticas agresivas.
Para evaluar el tratamiento de la IA con esfínter artificial se diseñó una escala de gravedad específica, en la que se puntúa la interferencia que la IA tiene sobre la calidad de vida. Denominado comúnmente FIS (Fecal Incontinence Score)39,40, limita el tiempo de valoración de las respuestas a las 4 últimas semanas y tiene un rango de 0 a 120, en el que el peso de las respuestas sobre la interferencia en la calidad de vida es mínimo (0-5).
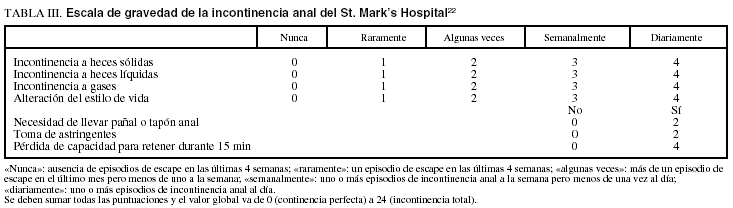
En 1999, Vaizey et al22 validan por primera vez una escala de gravedad de incontinencia, llamada Escala del Hospital San Marck (tabla III), en la que se puntúa la frecuencia con que la IA altera el estilo de vida. Esta escala presenta con respecto a otras gran estabilidad temporal (test-retest) y sensibilidad al cambio (pre y postratamiento), y la han utilizado diversos grupos de trabajo27,41.
Evaluación de la calidad de vida en pacientes con incontinencia anal mediante cuestionarios de calidad en función de los síntomas gastrointestinales
En pacientes con IA se ha utilizado el cuestionario de vida validado en 1995 por Eypasch et al42, que consta de 36 preguntas acerca de síntomas y alteraciones de la función física, emocional y social relacionadas con enfermedades gastrointestinales. Si un síntoma está presente, el paciente indica la importancia que tiene sobre su calidad de vida en una escala de 0 a 4 (0 es lo peor, 4 lo mejor). Este cuestionario se ha utilizado para evaluar en qué punto de gravedad (utilizando el cuestionario de Wexner) la IA influye sobre la calidad de vida34.
Evaluación de la calidad de vida en pacientes con incontinencia anal mediante cuestionarios genéricos validados en la población general
Los cuestionarios genéricos presentan la ventaja de que la calidad de vida está muy bien medida en la población general y que evalúan globalmente muy bien el impacto que tiene el «estar enfermo» sobre la salud en sus diferentes dimensiones. Sin embargo, tienen el inconveniente de que son incapaces de discriminar específicamente el impacto de la IA. Esto es muy importante porque en pacientes con IA las limitaciones más significativas pueden ser consecuencia de la/las enfermedad/es de base (esclerodermia, enfermedad inflamatoria intestinal, diabetes, demencia, etc.) y, por tanto, tras el tratamiento pueden ser incapaces de medir cambios, aunque exista mejoría de la IA. Por ello, la valoración de estos cuestionarios debe realizarse teniendo muy bien definidos los valores individuales pretratamiento y analizando dominios del cuestionario sobre los que, a juicio del paciente y del médico, más impacto tiene la IA, por ejemplo, la función social.
El SF-36, validado en España, se desarrolló para uso en el estudio de resultados médicos, cubre 8 dimensiones del estado de salud (función física y social, limitaciones del rol por problemas emocionales o físicos, salud mental, vitalidad, dolor y estado general de salud). En pacientes con IA, la mayoría de los autores utilizan el SF-36 solo o asociado a cuestionarios específicos. En pacientes con IA por esclerodermia tras tratamiento con electroestimulación sacra, se observa una mejoría de la función social41. La función social y física mejora en pacientes con IA tras inyección de silicona intraesfinteriana por disfunción del esfínter anal interno43 y tras tratamiento quirúrgico mediante graciloplastia dinámica31. El tratamiento médico conservador y conductual o con biofeedback mejora significativamente la vitalidad, la función social y la salud mental27.
El Perfil de Salud de Nottingham I (Nottingham Health Profile, NHP), que mide 6 dimensiones de salud (energía, dolor, movilidad física, reacciones emocionales, sueño y aislamiento social), está validado en español. Por su parte el Perfil de Salud de Nottingham II, que mide la capacidad de realizar tareas habituales (ocupación, tareas domésticas, relaciones personales, actividad sexual y vida social) se ha utilizado para evaluar los cambios en la calidad de vida de los pacientes con IA tras cirugía mediante graciloplastia dinámica44, y ha objetivado que en los pacientes que mejoran de la incontinencia se produce una mejora significativa de la movilidad física, disminuye el aislamiento social y experimentan una mejoría significativa en todas las capacidades para realizar las tareas habituales.
La causa más frecuente de IA permanente en los niños es la secundaria a cirugía por malformación anorrectal. Medir la calidad de vida en edades tempranas de la vida es muy difícil. Bai et al45 confeccionaron un cuestionario que, rellenado por los padres, puntuaba en niños (8-16 años) con IA la frecuencia de diferentes aspectos: absentismo escolar, infelicidad o ansiedad, restricción de alimentos y rechazo por sensación de no ser iguales a los demás. Observaron que los niños con IA tienen una calidad de vida significativamente disminuida respecto al grupo control y que ésta es peor cuanto más grave es la IA. Estos resultados, utilizando un cuestionario no validado y con defectos importantes en su estructura, ponen sin embargo de manifiesto la necesidad de elaborar un sistema de medición específico de la calidad de vida en los niños.
Evaluación de la calidad de vida en pacientes con incontinencia anal mediante cuestionarios específicos
Rockwood et al46 validaron en 2000 el primer cuestionario específico de calidad de vida para pacientes con IA, que consta de 29 preguntas que valoran 4 dominios de salud (estilo de vida, conducta, depresión/autopercepción y vergüenza). Este cuestionario, el Fecal Incontinence Quality of Life Scale (FIQLS), es el recomendado por la Sociedad Americana de Cirujanos de Colon y Recto, y ha sido validado en España por el Grupo Español para el Estudio de la Motilidad Digestiva (GEMD) (anexo I) en 111 pacientes con IA de etiología diversa. Significativamente, los pacientes con una puntuación en la escala de Wexner mayor de 9, pacientes que utilizan pañales y pacientes con incontinencia completa (gases, líquidos y sólidos), presentan una peor calidad de vida para todos los dominios. La alteración en la conducta y la sensación de vergüenza son los dominios más afectados en los pacientes con IA.
El FIQLS se ha empleado para evaluar la calidad de vida en diversos grupos de pacientes: tras esfinterotomía lateral interna47, tras tratamiento con calor controlado por radiofrecuencia35,36, sometidos a la inyección de sustancias incrementadoras de volumen (microesferas) en el esfínter anal interno48, tras implantación de esfínter artificial37,39, esfinteroplastia30 y neuroestimulación38. Tiene una correlación muy buena con el SF-36 y con los diferentes grados de gravedad de la incontinencia. Para la evaluación del esfínter artificial se utiliza este cuestionario con alguna modificación (39 preguntas)40, y se ha observado tras la activación del esfínter un descenso del uso de compresas de protección (el 54 frente al 88%) y de pañales (el 17 frente al 51%), disminución del porcentaje de pacientes que son incapaces de llegar al aseo (el 20 frente al 89%) y de los que limitan el tiempo de su actividad física (el 17 frente al 81%) o sienten que disfrutan menos de la vida debido a la IA (el 30 frente al 81%). Es importante resaltar estos datos dado que esta técnica se aplica a pacientes con IA grave que no responden a ninguna otra actitud terapéutica y que presentan una alteración de la calidad de vida extrema.
En el año 2001 Bugg et al49 validan un cuestionario de calidad de vida específico para mujeres con IA que consta de 32 preguntas y analiza 9 dimensiones (percepción general de salud, impacto que tiene la IA, rol, función física, función social, función personal, emoción, energía y severidad de las medidas para tratar la IA). Las dimensiones que más puntuación alcanzan son la severidad de la medidas para tratar la IA, el impacto que tiene la IA, los problemas emocionales y la función física. De momento este cuestionario no se ha utilizado para medir cambios tras tratamiento.
Pager et al29 utilizan por primera vez en pacientes con IA una forma diferente de medir la calidad de vida mediante el Direct Questioning of Objectives; es un método novedoso, validado, en el que el paciente indica aspectos importantes de su vida afectados por presentar IA que desea-ría mejoraran tras el tratamiento. Asigna un valor a cada aspecto a mejorar (objetivo) según la importancia que tiene para él en una escala del 0 al 10. Posteriormente se le pide que valore la proporción del objetivo que ha alcanzado en ese momento, en una escala del 0 al 10. El índice de calidad de vida es el producto de multiplicar el resul-tado de cada puntuación (importancia x porcentaje alcanzado) y dividirlo por 10, y posteriormente dividir este resultado por la puntuación dada a la importancia. Se trata de una valoración cuantitativa en una escala de 0 a 1 de la relación existente entre el grado de mejoría y la importancia del objetivo, de manera que 0 indica no haber conseguido nada --calidad de vida fatal para este objetivo-- y 1 haber conseguido todo. Por ejemplo, si para un paciente el objetivo salir de casa tiene una importancia de 8 y en el momento de la pregunta puntúa este objetivo con un 5, el índice de calidad de vida en este objetivo será de 0,5 (8 x 5/10 = 4; 4/8 = 0,5). Este sistema se ha aplicado, siempre por el mismo grupo de trabajo, para valorar los cambios en la calidad de vida tras tratamiento con biofeedback y ejercicios del suelo pélvico29, así como para evaluar la calidad de vida en pacientes con IA de origen neuropático, antes y después de biofeedback50. Los pacientes con IA neuropática predominantemente eligieron como objetivos (por orden de frecuencia) la socialización, las tareas domésticas, no tener temor por dónde está el aseo, no necesitar compresas o pañales, ir de compras, salir de casa, viajar, no sentir vergüenza, etc., y concedieron más importancia al aseo personal, los deberes familiares, el empleo, no tener vergüenza, la autoestima, ir de compras, no tener temor por dónde está el aseo, etc. La ventaja que tiene este sistema frente a encuestas con preguntas preestablecidas es que el paciente es el que decide qué aspectos de su vida son los que más afectados por la IA y la importancia que tienen, además de valorar, en cualquier momento, el nivel en el que logra mejorar estos aspectos. Es un sistema más individualizado que permite hacer hincapié en aspectos terapéuticos concretos.
Cuestionarios disponibles en español
Validados al español únicamente se encuentran el SF-36, el Perfil de Salud de Nottingham I y el FIQLS (este último está disponible en la página web del GEMD, www.blues.uab.es/gemd) (anexo I).
Cuestionarios que pueden usarse para evaluar la calidad de vida en pacientes con incontinencia anal
El más adecuado es el FIQLS, dado que está validado y lo utiliza la mayoría de los grupos en el mundo; sin embargo, es recomendable como mínimo usar el cuestionario de Wexner o el del St. Mark's Hospital, por su sencillez y rapidez. Aunque es necesaria más experiencia, el Direct Questioning of Objectives es un sistema a tener en cuenta, inicialmente complementario del FIQLS o de las escalas de Wexner o del St. Mark's Hospital, dada la importancia que tiene para conocer el impacto individual en la calidad de vida y, por tanto, individualizar el tratamiento y los resultados.