El cáncer de vejiga es relativamente frecuente. En México, en el año 2012 se reportaron 3,245 casos y 1,666 muertes. Los esquemas de quimioterapia basados en sales de platino son el estándar de primera línea en la enfermedad metastásica. En la actualidad no se ha establecido un estándar en segunda línea, y la información es variable y poco clara. Gemcitabina y paclitaxel se han estudiado en este contexto con tasas de respuesta modestas. Vinflunina, un alcaloide de la vinca semisintético de tercera generación, parece ser una opción razonable posteriormente a una primera línea de quimioterapia basada en platinos. Los pacientes con cáncer de vejiga con sobreexpresión de Her2 tienen un pronóstico pobre. No obstante, reportamos el caso de un hombre de 54 años de edad con cáncer de vejiga Her2 positivo tratado con vinflunina más trastuzumab debido a una recurrencia después de una primera línea de quimioterapia adyuvante con base en cisplatino, que logró una respuesta completa y un control prolongado de la enfermedad.
Bladder cancer is relatively common. In Mexico, in 2012, there were 3,245 new cases and 1,666 deaths in México. Platinum salt-based chemotherapy regimens are the standard first line treatment for metastatic disease. To date, no standard therapy has been established as second line, with the data being variable and unclear on this issue. Gemcitabine and Paclitaxel have been studied in this setting, with modest response rates. Vinflunine, a third-generation semi-synthetic vinca-alkaloid, appears to be a reasonable option for patients after first-line platinum-containing chemotherapy. Patients with advanced bladder cancer with over-expression of Her2, have a very poor prognosis. Nevertheless, the case is presented of a 54-year-old man with Her2 positive bladder cancer treated with Vinflunine plus Trastuzumab after recurrence with first-line adjuvant chemotherapy with cisplatin, who achieved a complete response and long-term disease control.
A nivel mundial, el cáncer de vejiga es una neoplasia relativamente frecuente, cada año se diagnostican 429,793 casos y se reportan 165,084 muertes; en México, en el año 2012 se documentaron 3,245 casos nuevos y 1,166 muertes1,2. Uno de los aspectos de mayor importancia para estimar la supervivencia de los pacientes es el momento del diagnóstico. De acuerdo con datos del programa Surveillance, Epidemiology, and End Results, el 86% de los tumores se diagnostica en etapas tempranas, el 7% localmente avanzado y el 4% como enfermedad metastásica (el 3% se reporta como no clasificable); la supervivencia a 5 años para las etapas localmente avanzada y metastásica es de 34 y 5.4%, respectivamente3.
En pacientes con enfermedad localmente avanzada o metastásica candidatos a quimioterapia, los esquemas basados en sales de platino son el tratamiento estándar, ya que han demostrado impacto en el control de la enfermedad y supervivencia4–8. En pacientes con falla a una primera línea, tradicionalmente las opciones de manejo sistémico en segunda línea con taxanos o gemcitabina ofrecen paliación y supervivencia global pobres, por lo que para muchos especialistas los cuidados paliativos han constituido una opción válida de tratamiento9–12. Más recientemente, vinflunina, un agente antimicrotúbulos, ha sido considerada un fármaco adecuado en pacientes con cáncer de vejiga previamente tratados al demostrar, en un estudio fase iii, su eficacia versus mejores cuidados de soporte13. El papel de Her2 y sus implicaciones terapéuticas en pacientes con cáncer de vejiga no están del todo claras en la actualidad, por lo que representa un área terapéutica potencial a futuro14–16.
En este reporte se describe el caso clínico de un paciente con cáncer de vejiga positivo para Her2 tratado con vinflunina más un agente anti-Her2, quien logró una respuesta completa prolongada.
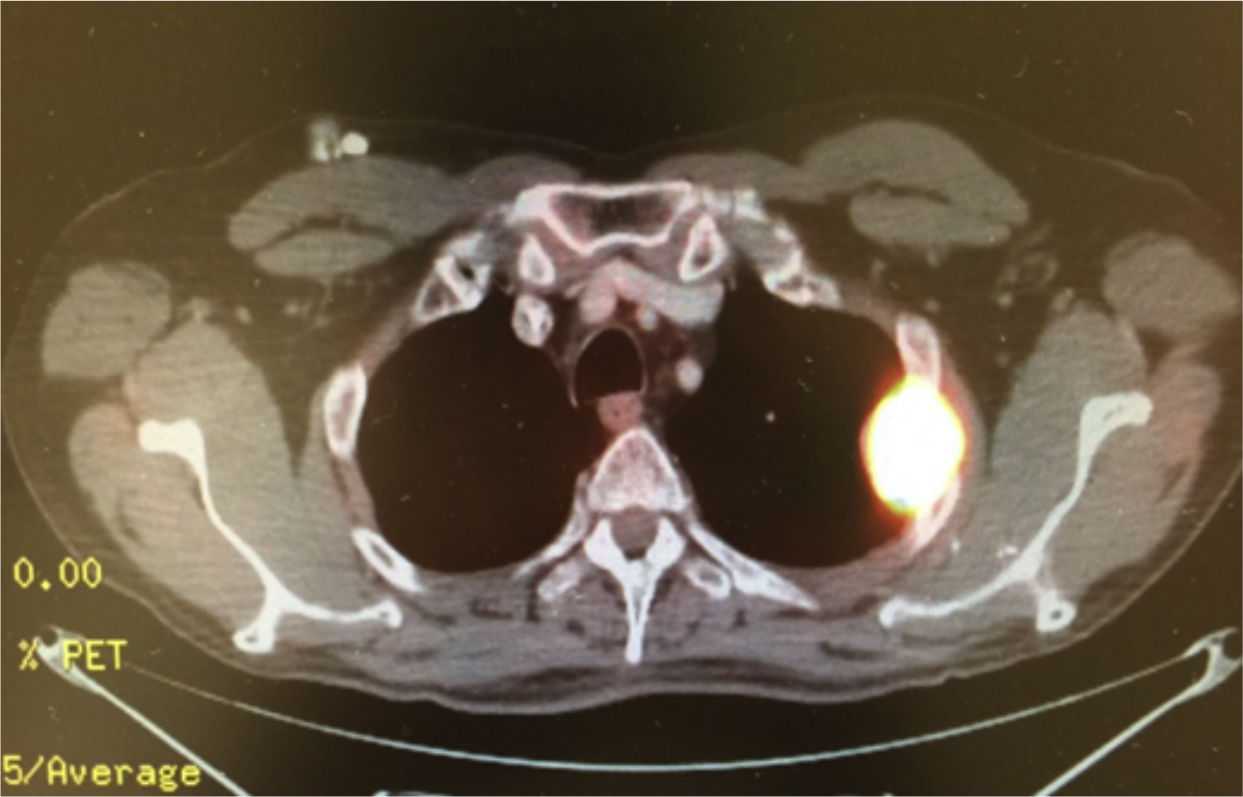
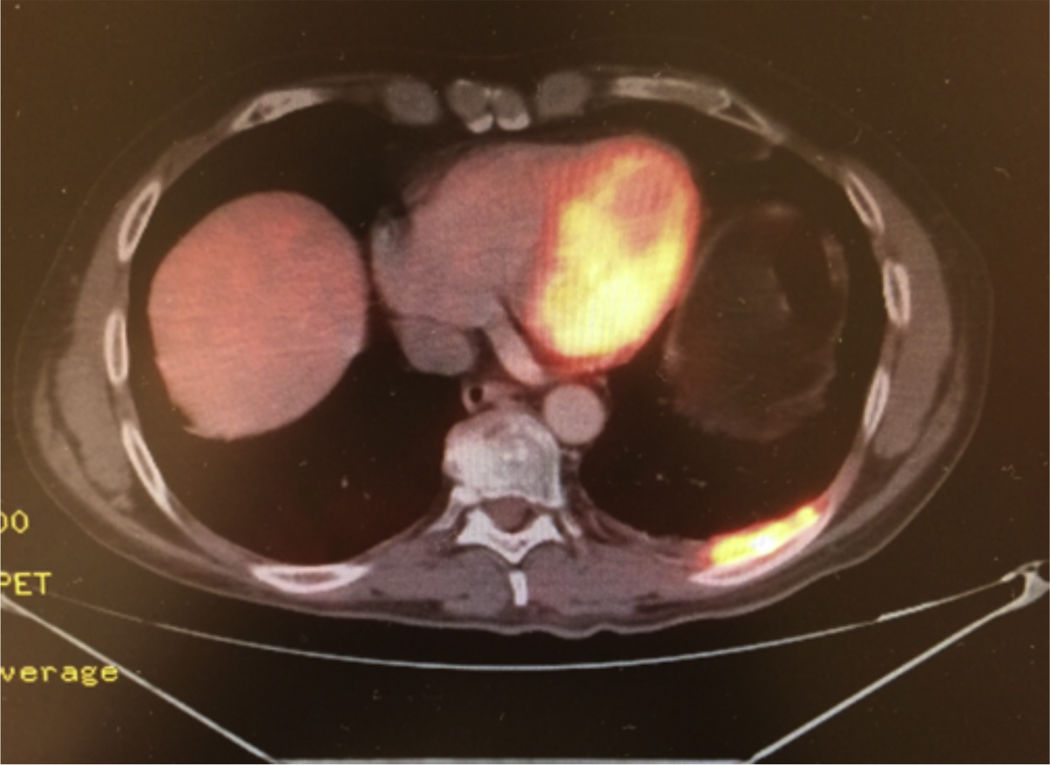
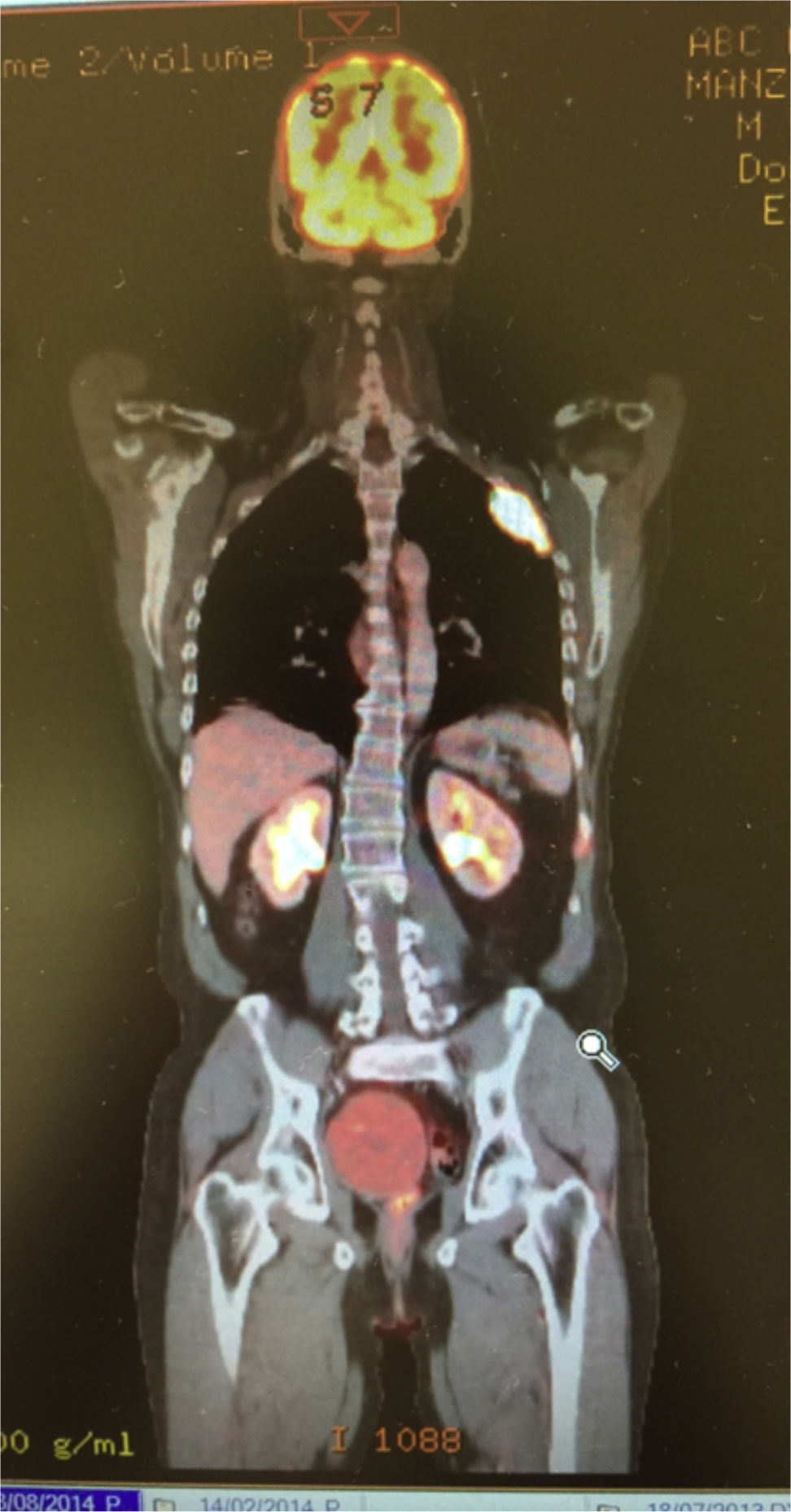
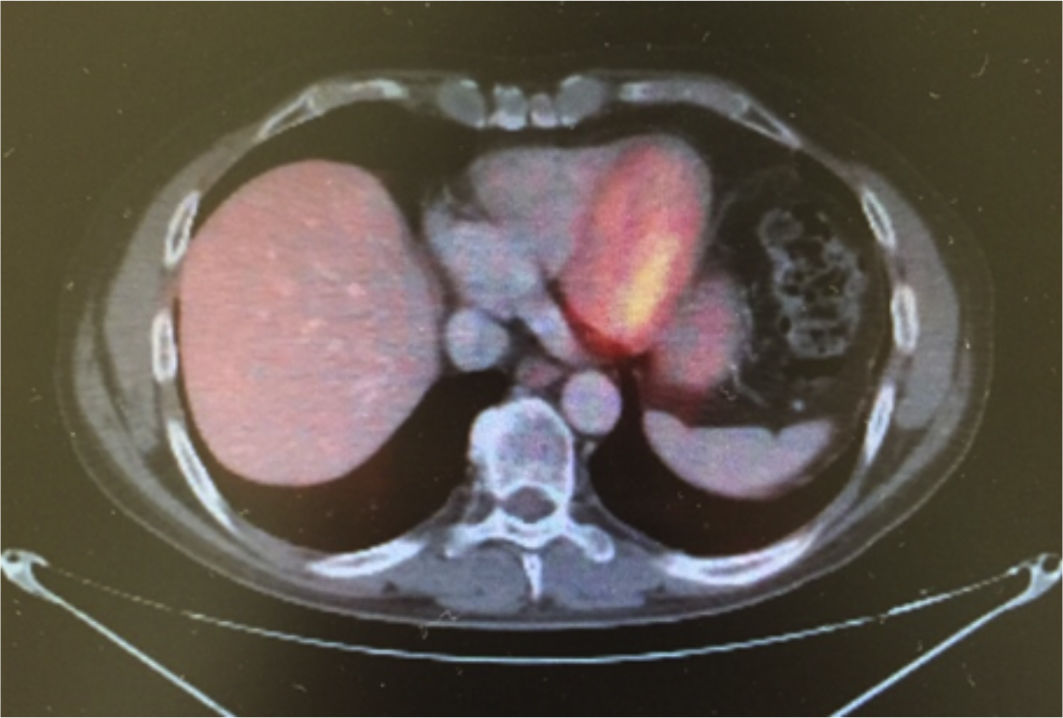
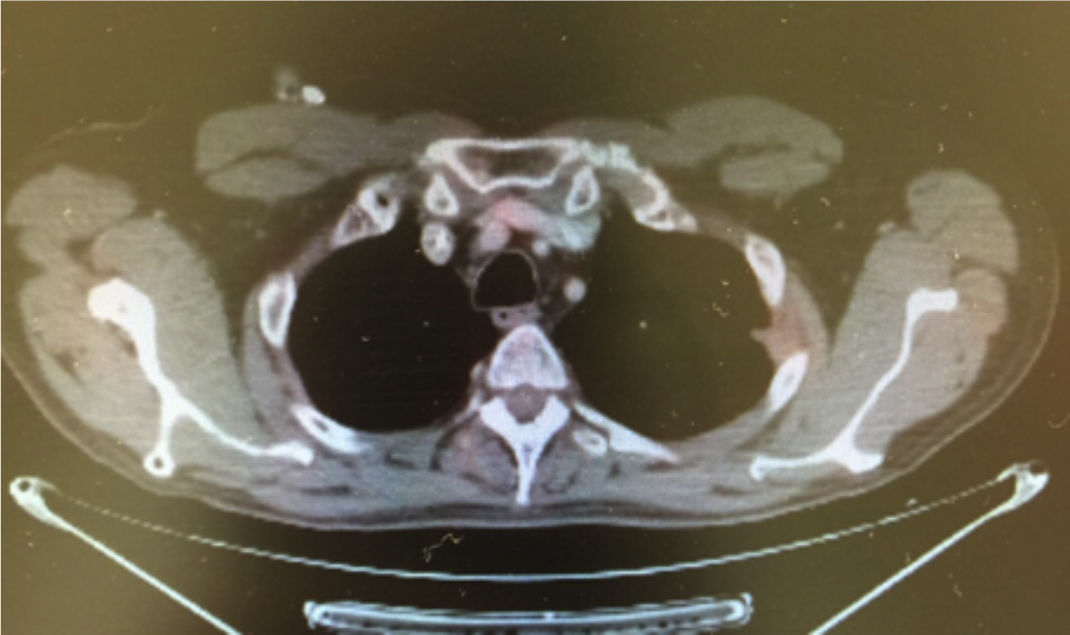
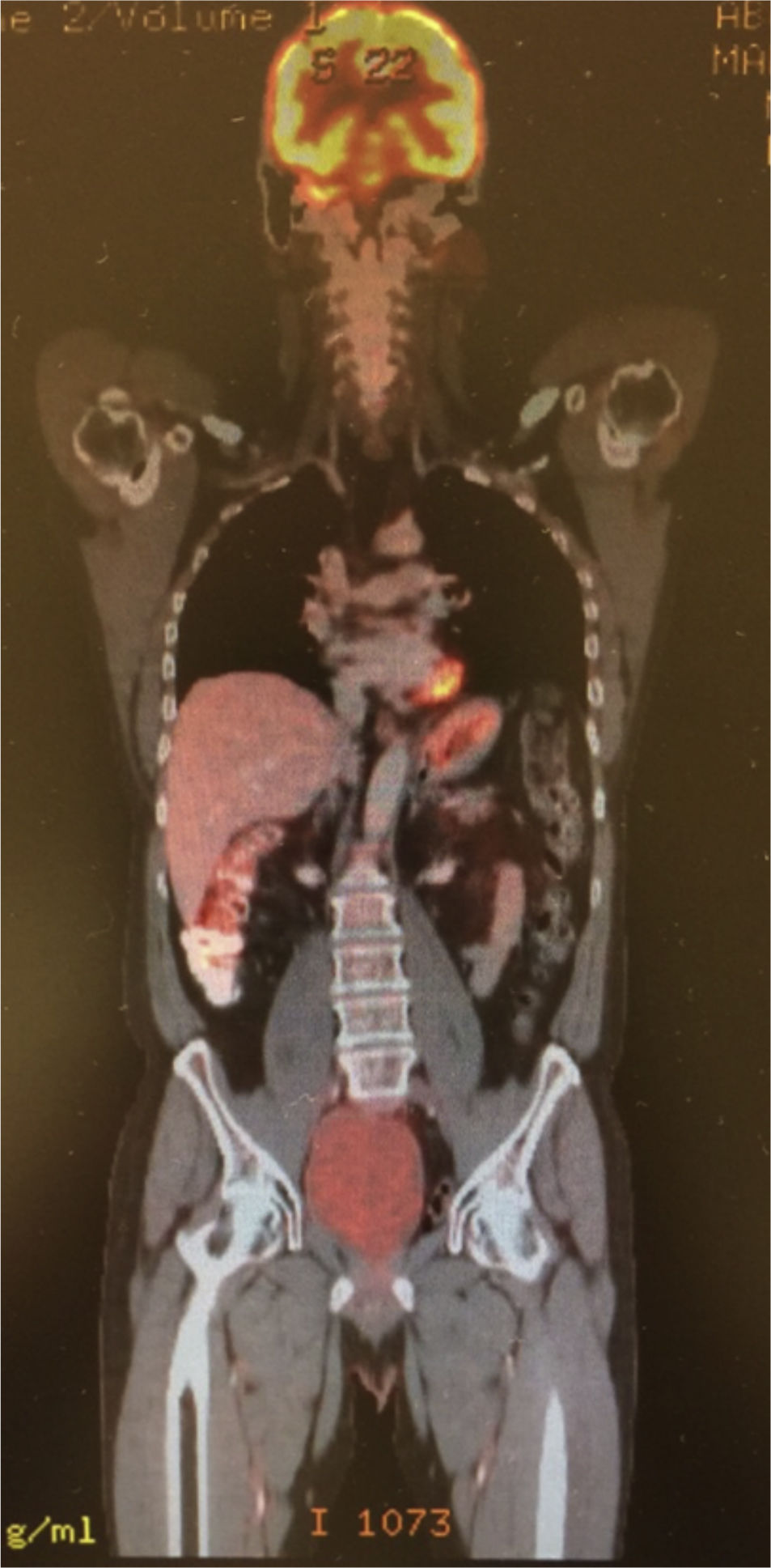
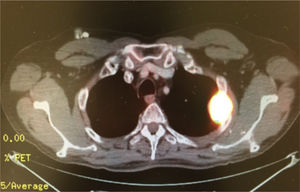
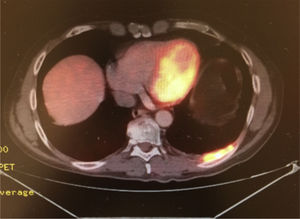
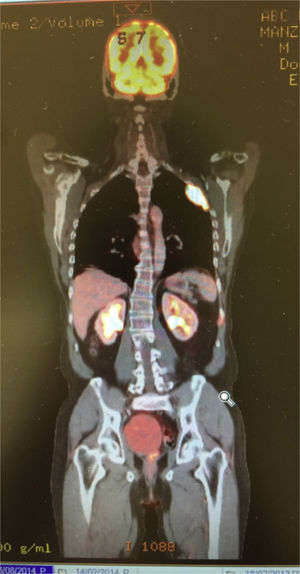
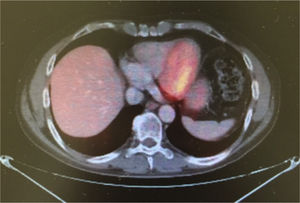
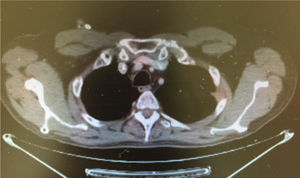
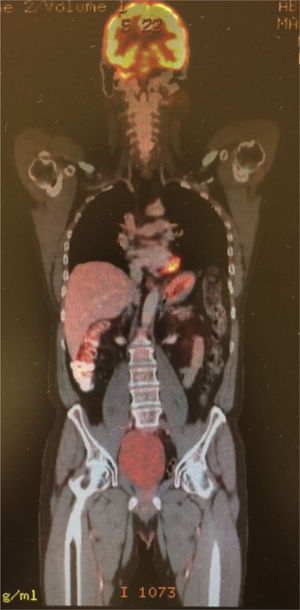
Caso clínicoSe trata de un hombre de 54 años de edad con antecedente de tabaquismo positivo durante 26 años. En febrero de 2013 presentó hematuria macroscópica, motivo por el cual se realizaron abordajes diagnósticos que condujeron al hallazgo de una tumoración maligna en la vejiga. Se sometió a una cistectomía radical con reporte de Anatomía Patológica: carcinoma poco diferenciado de vejiga con metástasis en 1/34 ganglios disecados. Se estadificó como una etapa iv (T3b, N1, M0) y recibió tratamiento con quimioterapia adyuvante con esquema de cisplatino más gemcitabina, finalizando en diciembre de 2013. Un estudio PET-CT de control en febrero de 2014 resultó negativo a malignidad, por lo que permaneció en vigilancia. En agosto de 2014 presentó dolor costal izquierdo asociado a tos, motivo por el cual se realizó una PET-CT (figs. 1–3) con hallazgo de lesiones metastásicas en la región costal, así como pleural izquierda con SUVmáx de 25. Una biopsia guiada por TAC reportó: carcinoma de alto grado con sobreexpresión de Her2 por inmunohistoquímica. En octubre de 2014 se decidió iniciar quimioterapia con vinflunina a dosis de 320mg/m2 al día, una cada 3 semanas más trastuzumab, dosis de carga 8mg/kg seguido posteriormente con 6mg/kg cada 3 semanas. Después de 4 ciclos de tratamiento mostró una excelente respuesta clínica, refiriendo solo náuseas y mucositis grado 2, así como astenia grado 1. La PET-CT (figs. 4–6) mostró control con respuesta completa a nivel costal y pleural; sin embargo, hubo hallazgo de metástasis en SNC, los cuales se confirmaron por IRM; clínicamente sin datos neurológicos, se decidió someterlo a radiocirugía, la cual se realizó sin complicaciones. Se decidió completar 8 ciclos de tratamiento con vinflunina y trastuzumab y, posteriormente, continuar el mantenimiento con trastuzumab.
DiscusiónEl tratamiento estándar para la enfermedad avanzada se ha basado en esquemas con sales de platino (cisplatino), como son el MVAC o cisplatino más gemcitabina; ambos esquemas muestran una eficacia similar, pero tiene mejor tolerancia el esquema con gemcitabina, lo que lo ha convertido en el esquema ideal en primera línea8. A pesar de que las tasas de respuesta en primera línea llegan a ser del 40-60%, alrededor de los 8 meses después la mayoría de pacientes progresarán17. Históricamente, una de las áreas de oportunidad en el manejo del cáncer de vejiga es la segunda línea, en donde la información para establecer un estándar de tratamiento ha sido limitada. Un metanálisis sobre segunda línea de quimioterapia en pacientes con cáncer de urotelio metastasico publicado por Raggli y colaboradores en 2016, documentó que no existe diferencias entre taxanos y vinflunina en beneficio de sobrevida libre de progresión ni sobrevida global. Tampoco los dobletes de quimioterapia fueron superiores a vinflunina en SG, lo cual reafirma el beneficio de esta droga en segunda línea18; la combinación de paclitaxel y gemcitabina reporta tasas de respuesta globales del 41.5%, un tiempo a la progresión de 3.1 meses y una supervivencia de 8 meses19.
Vinflunina es un derivado de los alcaloides de la vinca bifluorinado de tercera generación que se caracteriza por tener una mayor eficacia que sus predecesores, incluyendo una tasa menor en el desarrollo de resistencia a fármacos20. Uno de los primeros estudios realizados con vinflunina en cáncer de vejiga valoró, en un ensayo fase ii, a 51 pacientes previamente tratados con sales de platino; los resultados demostraron una tasa de respuesta del 18%, una tasa de control de la enfermedad del 67%, una mediana de duración de la respuesta de 9.1 meses y un tiempo a la progresión de 3 meses. Uno de los hallazgos de interés en este estudio fue el hecho de que la población que más se benefició fue aquella con una rápida progresión (<12 meses) a sales de platino21. El estudio fase iii de aprobación de vinflunina versus mejor terapia de soporte demostró una tasa de supervivencia de 6.9 meses frente a 4.6 meses, respectivamente, en donde el análisis multivariado para supervivencia ajustado a factores pronósticos preespecificados reportó una significación estadística (p=0.036) en favor de vinflunina, con una reducción en el riesgo de muerte del 23% (HR=0.77; IC 95% 0.61 a 0.98); la tasa de control de la enfermedad fue del 41% y el tiempo a la progresión de 3 meses a favor de vinflunina, con significación estadística13.
Al igual que en los estudios de vinflunina, en este paciente se pudo observar la eficacia y seguridad del fármaco; asimismo, es de particular interés enfatizar que tuvo una recaída de su enfermedad después del primer esquema de tratamiento basado en sales de platino de forma relativamente rápida (8 meses), pese a lo cual se logró una respuesta completa. Como comentamos previamente, es precisamente este grupo de pacientes, el que progresa rápidamente a sales de platino, el que más se beneficia de vinflunina21. Por otro lado, en el estudio fase iii el 81% de los pacientes que recibieron vinflunina progresaron de la misma manera, en un periodo relativamente corto, a sales de platino, lo cual no fue un factor que limitara la eficacia del tratamiento13.
Otro de los aspectos de interés es la expresión de Her2 en pacientes con cáncer de vejiga. La incidencia reportada de la proteína Her2/neu varía considerablemente, con rangos de 9-81% en sobreexpresión y 0-32% en la amplificación del gen22. El análisis de los datos confirmó la presencia de Her2 como un factor de mal pronóstico, presentándose principalmente en tumores grado 323. La positividad de Her2 puede variar de forma importante; por ejemplo, otros estudios han reportado una frecuencia del 39% en tumores avanzados de vejiga24.
La sobreexpresión de Her2 en el caso expuesto en este artículo se correlaciona claramente con lo descrito en la literatura al contar con un reporte de tumor de alto grado, tal y como informan Underwood et al., en donde 20 de 54 tumores grado 3 estudiados fueron positivos para Her2, frente a solo 4 casos positivos en 173 tumores grado 1-223.
Al hacer una revisión de la literatura, es escasa la información de relevancia en pacientes con cáncer de vejiga en tratamiento con agentes anti-Her2±quimioterapia u otros fármacos. Recientemente, en estudios en cultivos celulares, una publicación demostró la actividad de trastuzumab y TDM-1 (el más activo) con la inhibición de los mismos25. Un estudio fase ii con 54 pacientes con cáncer urotelial tratados con quimioterapia a base de paclitaxel, carboplatino, gemcitabina y trastuzumab demostró una tasa de respuestas confirmadas del 57%, un tiempo a la progresión de 9.3 meses y una supervivencia global de 14.1 meses16. Por último, existe un reporte de caso de una mujer con cáncer de vejiga positivo para Her2 tratada en primera línea con neratinib, un inhibidor de tirosina cinasa, quien logró una respuesta parcial y 11 meses de intervalo libre de progresión; ante la progresión se trató nuevamente con neratinib más capecitabina, logrando nuevamente respuesta26.
Existen varios análisis sobre factores predictores de respuesta a quimioterapia en segunda línea; el más usado es el propuesto por Bellmunt et al., un modelo de 3 valores que incluyen: estado funcional (ECOG 0-1 vs. >2), hemoglobina (≥10 vs. ≤10), metástasis hepáticas (no vs. si). La media de sobrevida según el número de factores presentes son:
- -
0 riesgos: 14.2 meses
- -
1 riesgo: 7.3 meses
- -
2 riesgos: 3.8 meses
- -
3 riesgos: 1.7 meses27,28.
Si bien existe poca información acerca del uso de fármacos anti-Her2 en pacientes con cáncer de vejiga avanzado que sobreexpresan Her2, no podemos dejar de lado la posibilidad de explorar este tipo de tratamiento, incluso con resultados positivos, como se muestra en el caso de este paciente, idealmente dentro de un ensayo clínico. Considerando la tendencia actual de caracterizar molecularmente los diferentes tipos de tumores con el objetivo de personalizar los tratamientos y minimizar la toxicidad o el sobretratamiento de pacientes sin beneficio clínico, parece razonable explorar el uso de terapia blanco sumada al agente estándar (EMEA 2009) en segunda línea para cáncer de vejiga, como es vinflunina29. Los resultados, aunque aún contradictorios, nos permiten mantener la hipótesis del potencial beneficio de este tipo de tratamiento en pacientes con características moleculares específicas, así como desarrollar futuros estudios evaluando el uso de vinflunina más un agente anti-Her2 en pacientes con falla a un esquema de primera línea.
ConclusionesVinflunina es el agente de elección como terapia de segunda línea en pacientes con cáncer de vejiga avanzado. La presencia de Her2 confiere mal pronóstico y el uso de agentes anti-Her2 debe ser evaluado de forma amplia en el contexto de un ensayo clínico.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.