La seguridad de los pacientes críticos en situaciones de crisis: pandemia y proyectos Zero
Más datosEl proyecto Bacteriemia Zero (BZ) fue el primero de los Proyectos Zero que se implementó en las Unidades de Cuidados Intensivos (UCI), consiguiendo una disminución de las tasas de infección relacionadas con catéter por debajo de las recomendadas por los estándares de calidad de las sociedades científicas. A raíz de la pandemia causada por el SARS-CoV-2 en las UCI, se ha observado un incremento importante de estas tasas de infección. El incremento de las tasas de infección y la necesidad de incorporar en la práctica clínica la mejor evidencia disponible, justifica la necesidad de actualizar las recomendaciones del proyecto BZ. Se constituyó un grupo de trabajo formado por miembros de las diferentes sociedades científicas que consideró que el paquete de medidas obligatorias del proyecto no debía modificarse debido a su eficacia demostrada y decidió incorporar, después de su revisión, las siguientes medidas opcionales: uso de catéteres impregnados con antimicrobianos, uso de apósitos impregnados con clorhexidina, uso de tapones con solución antiséptica en los conectores e higiene corporal diaria con clorhexidina.
The Bacteraemia Zero (BZ) Project was the first of the Zero Projects to be implemented in Intensive Care Unit (ICU), achieving a decrease in catheter-related infection rates below those recommended by the quality standards of scientific societies. Following the SARS-CoV-2 pandemic in ICU, a significant increase in these infection rates has been observed. Increase in infection rates and the need to incorporate the best available evidence into clinical practice justifies the need to update the recommendations of the BZ project. A working group formed by members of the different scientific societies considered that the mandatory measures of the project should not be modified due to its proven efficacy. In addition, this group decided to incorporate the following optional measures: use of catheters impregnated with antimicrobials, use of dressings impregnated with chlorhexidine, use of caps with an antiseptic solution in connectors, and daily body hygiene with chlorhexidine.
Las Unidades de Cuidados Intensivos (UCI) adheridas al proyecto de seguridad del paciente crítico Bacteriemia Zero (BZ) que aplicaron el paquete de recomendaciones destinadas a prevenir estas infecciones e implementaron el plan de seguridad integral, consiguieron disminuir de forma significativa las tasas de infecciones relacionadas con estos dispositivos1. Los resultados obtenidos durante el periodo de implementación del programa se han consolidado posteriormente, tanto en el número de unidades adheridas al mismo, como en las tasas de infección2,3, que se han mantenido por debajo del estándar de calidad recomendado por la Sociedad Española de Medicina Intensiva Crítica y Unidades Coronarias (SEMICYUC)4.
Sin embargo, en la actualidad, y relacionado con el impacto de la pandemia causada por el SARS-CoV-2 en las UCI, se ha observado un incremento alarmante de las tasas de infección relacionada con dispositivos5. En el periodo de vigilancia del registro del Estudio Nacional de Vigilancia de Infecciones Nosocomiales (ENVIN) realizado en 20206, coincidiendo con la segunda ola de la pandemia, las densidades de incidencia (DI) de bacteriemia primaria (BP) y bacteriemia relacionada con catéter (BRC) fueron de 6,27 y 2,91 episodios por 1.000 días de catéter venoso central (CVC) respectivamente, situándonos en cifras superiores a las del periodo previo al inicio del proyecto2. Los cambios provocados por la pandemia en la organización asistencial y las adaptaciones que se han tenido que realizar para hacerle frente, han alterado las rutinas de trabajo de las unidades y ha sido necesario adaptar los programas de intervención de acuerdo con las barreras y dificultades identificadas7. El incremento de las tasas de infección y la necesidad de incorporar en la práctica clínica la mejor evidencia disponible justifica la necesidad de actualizar las recomendaciones del proyecto BZ, así como su módulo de formación y los documentos de apoyo con la intención de facilitar la formación de los profesionales sanitarios incorporados a la atención de pacientes críticos.
El objetivo de este artículo es presentar la actualización de las recomendaciones del proyecto Bacteriemia Zero con base en la mejor evidencia científica disponible. Se espera que la actualización de estas recomendaciones sirva para reducir la media estatal de la DI de la BP a < 3 episodios x 1.000 días de CVC y recuperar las tasas previas a la pandemia.
MetodologíaPara actualizar las recomendaciones del proyecto BZ y adaptarlas a la situación de pandemia se constituyó un grupo de trabajo formado por miembros de la SEMICYUC, Sociedad Española de Enfermería Intensiva y Unidades Coronarias (SEEIUC), Asociación Española de Enfermería de Prevención y Control de Infecciones (AEEPyCI) y Sociedad Española de Medicina Preventiva, Salud Pública e Higiene (SEMPSPH) todos ellos expertos en metodología y/o con experiencia en el diseño y dirección de proyectos de intervención «Tolerancia Zero» y miembros del Consejo Asesor de Proyectos de Seguridad en Pacientes Críticos (CAPSPC).
La primera fase consistió en la selección de las medidas con un potencial impacto en la prevención de las infecciones relacionadas con los dispositivos vasculares.
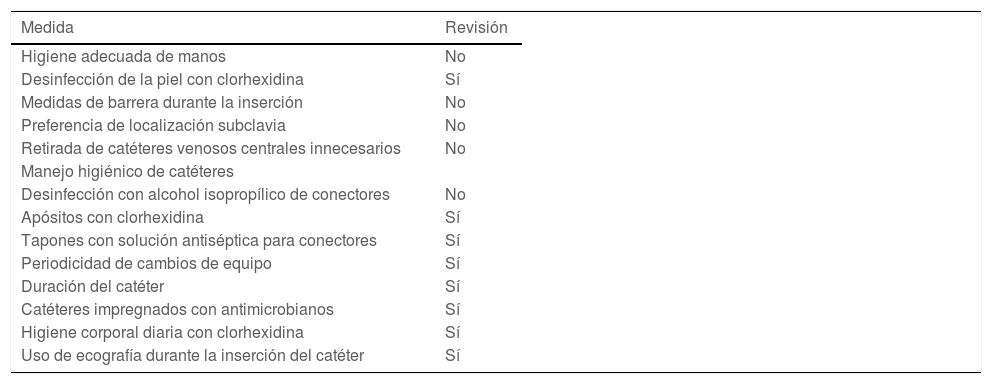
El grupo de trabajo consideró que el paquete de medidas del proyecto original (2009) no debería modificarse ya que había demostrado su eficacia en la prevención de las BP por la disminución de las tasas y la consolidación de estas en las unidades adheridas al proyecto. Algunas de las medidas originales se incluyeron en la revisión para valorar si su grado de evidencia/recomendación había variado (tabla 1).
Revisión de las medidas preventivas de Bacteriemia Zero 2021
| Medida | Revisión |
|---|---|
| Higiene adecuada de manos | No |
| Desinfección de la piel con clorhexidina | Sí |
| Medidas de barrera durante la inserción | No |
| Preferencia de localización subclavia | No |
| Retirada de catéteres venosos centrales innecesarios | No |
| Manejo higiénico de catéteres | |
| Desinfección con alcohol isopropílico de conectores | No |
| Apósitos con clorhexidina | Sí |
| Tapones con solución antiséptica para conectores | Sí |
| Periodicidad de cambios de equipo | Sí |
| Duración del catéter | Sí |
| Catéteres impregnados con antimicrobianos | Sí |
| Higiene corporal diaria con clorhexidina | Sí |
| Uso de ecografía durante la inserción del catéter | Sí |
Las nuevas medidas que se incorporaron en la revisión del proyecto BZ fueron:
- •
Uso de catéteres impregnados con antimicrobianos.
- •
Uso de apósitos impregnados con clorhexidina.
- •
Uso de tapones con solución antiséptica en los conectores.
- •
Higiene corporal diaria con clorhexidina.
- •
Uso de la ecografía durante la inserción del catéter.
Cada una de las medidas se analizó de forma independiente, por al menos dos miembros del grupo de trabajo, con base en datos extraídos de ensayos clínicos y/u otros artículos. Para ello, se llevó a cabo una revisión sistemática de la literatura en las principales bases de datos electrónicas y una revisión iterativa de las recomendaciones de sociedades científicas y/o grupos de expertos relacionados con cada medida.
Para la clasificación de la calidad de la evidencia y fuerza de las recomendaciones se siguió la propuesta del grupo Grading of Recommendations, Assessment, Development and Evaluation (GRADE)8, y que tiene en cuenta no solo el número y diseño de los estudios realizados sino también la calidad de la evidencia. Según esta clasificación se considera la calidad de la evidencia alta, moderada, baja y muy baja y el grado de recomendación fuerte y débil. Para determinar el grado de recomendación, cada medida fue puntuada por todos los miembros del grupo de trabajo en relación con su efectividad, tolerabilidad y aplicabilidad en las UCI españolas a corto plazo. Se seleccionaron aquellas medidas que alcanzaron la máxima puntuación. Se solicitó el apoyo de expertos externos en alguna de las medidas que se revisaron (tabla 2).
Clasificación de la evidencia y el grado de recomendación según el sistema GRADE
| Clasificación de la evidencia | |
|---|---|
| Alta | Es muy poco probable que nuevos estudios cambien la confianza que tenemos en el resultado estimado |
| Moderada | Es probable que nuevos estudios tengan un impacto importante en la confianza que tenemos en el resultado estimado y que puedan modificar el resultado |
| Baja | Es muy probable que nuevos estudios tengan un impacto importante en la confianza que tenemos en el resultado estimado y que puedan modificar el resultado |
| Muy baja | Cualquier resultado estimado es muy incierto |
| Grado de recomendación | |
| Fuerte | Se refiere a la decisión que tomaría la mayoría de las personas bien informadas |
| Débil | Se refiere a la decisión que tomaría la mayoría de las personas bien informadas, aunque una minoría considerable no lo haría |
De acuerdo con la revisión bibliográfica y la ponderación de eficacia, tolerancia y aplicabilidad, las recomendaciones se clasificaron en obligatorias, opcionales y medidas a no realizar.
De este modo, el grupo de trabajo propone mantener las recomendaciones incluidas en el paquete de medidas original de BZ (2009) que deberían aplicarse de forma obligatoria en todas las unidades adheridas al proyecto.
El paquete de medidas original de BZ (Intervención estandarizada para reducir la BRC en la inserción y manejo de catéteres [STOP-BRC]), se complementa con unas recomendaciones opcionales que pueden considerarse en determinadas situaciones especiales o cuando no se consiga disminuir las tasas de bacteriemia con la aplicación de las recomendaciones obligatorias.
Medidas obligatorias. Paquete de medidas originales BZ (STOP-BRC)- •
Higiene adecuada de manos
Realizar una higiene apropiada de las manos antes y después de palpar los lugares de inserción de los catéteres, así como antes y después de insertar, remplazar, acceder, reparar o proteger un catéter intravascular. El uso de guantes no exime de la higiene de manos. (Evidencia alta/recomendación fuerte) (No revisada).
- •
Uso de solución alcohólica de clorhexidina en la preparación de la piel
Un Ensayo Clínico Aleatorizado (ECA) de 20159 evaluó el uso de clorhexidina alcohólica (clorhexidina 2% + alcohol isopropílico 70%) vs. una solución yodada alcohólica (povidona yodada 5% + etanol 69%) para la preparación de la piel antes de la inserción de un CVC o un catéter de hemodiálisis. La clorhexidina alcohólica se asoció con una menor incidencia de infecciones relacionadas con el catéter.
La revisión sistemática de la literatura10 publicada por la Organización Mundial de la Salud (OMS) sobre la desinfección de la piel en procedimientos quirúrgicos con el objetivo de comparar el efecto de diferentes soluciones y distintos agentes antisépticos, concluyó que las soluciones alcohólicas son más eficaces que las acuosas en la disminución del riesgo de infección del sitio quirúrgico. Las recomendaciones no incluyen la concentración del antiséptico debido a la falta de datos concluyentes.
En las distintas guías publicadas por Sociedades científicas se recomienda el uso de soluciones alcohólicas de clorhexidina para la preparación de la piel previa a la inserción de los dispositivos vasculares11–15 con un elevado grado de evidencia.
Después de la revisión bibliográfica la nueva recomendación es:
Desinfectar la piel con una solución alcohólica de clorhexidina que contenga una concentración entre 0,5 y 2% y alcohol de 70° antes de la inserción del CVC. Si existe una contraindicación para el uso clorhexidina (ej. hipersensibilidad), se pueden utilizar como alternativas soluciones alcohólicas yodadas. El antiséptico utilizado debe dejarse secar completamente después de la aplicación en la piel y previamente a la inserción del catéter. (Evidencia alta/recomendación fuerte).
- •
Uso de medidas de barrera total durante la inserción de los catéteres venosos centrales (CVC)
Utilizar una técnica aséptica para insertar el CVC. La adopción de barreras de máxima esterilidad (gorro, mascarilla, bata estéril, guantes estériles y paño estéril grande que cubra al paciente) durante la inserción de CVC reduce sustancialmente la incidencia de BRC. (Evidencia alta/recomendación fuerte) (No revisada).
- •
Preferencia de la vena subclavia como lugar de inserción
Utilizar la vena subclavia como lugar de inserción, cuando no es posible un acceso periférico, pero deben tenerse en cuenta otros factores como posibilidad de complicaciones no infecciosas y la habilidad del médico a la hora de insertar el catéter. (Evidencia alta/recomendación fuerte) (No revisada).
- •
Retirada de todos los catéteres venosos centrales innecesarios
Evaluar, al menos una vez al día, la necesidad de los dispositivos vasculares que lleva el paciente. (Evidencia alta/recomendación fuerte) (No revisada).
- •
Manejo higiénico de los catéteres
- ∘
Reducir al mínimo imprescindible la manipulación de conexiones y limpiar los puntos de inyección del catéter con alcohol isopropílico de 70° antes de acceder a través de ellos al sistema venoso. (Evidencia alta/recomendación fuerte) (No revisada).
- ∘
Sustituir los equipos de infusión, alargaderas y conectores que se utilizan de forma continua, con una frecuencia no inferior a 96 horas, pero al menos cada siete días (salvo que se indique lo contrario en las instrucciones de uso del fabricante), y siempre que estén las conexiones visiblemente sucias o en caso de desconexión accidental. En el caso de nutrición parenteral el cambio de equipos se realizará cada 24 horas y de emulsión lipídica el cambio de equipos se realizará cada seis a 12 horas. (Evidencia baja/ recomendación fuerte).
Esta recomendación se basa en las guías clínicas americanas, inglesas, asiáticas y el Center for Disease Control and Prevention (CDC) para la población adulta. Las guías francesas y argentinas no incluyen ninguna recomendación al respecto11–26.
Un ECA multicéntrico de 201721 sugiere que la sustitución rutinaria de los equipos de administración intravenosa antes del séptimo día no es eficaz para la prevención de BRC.
En población infantil, una revisión sistemática de 201323 concluye que no hay suficiente evidencia para apoyar o refutar esta recomendación.
Medidas opcionalesSe recomienda considerar el uso de alguna/s de las medidas opcionales aplicables en:
- a)
adultos en las UCI con altas tasas de BRC a pesar del adecuado cumplimiento de las medidas obligatorias del proyecto BZ.
- b)
pacientes con mayor riesgo de BRC (inmunodeprimidos, alteraciones de la integridad cutánea), pacientes con accesos con mayor riesgo de BRC (accesos altos con traqueostomía o vena femoral) y pacientes con mayor riesgo de complicaciones si desarrollasen BRC (implantación reciente de válvulas cardiacas o prótesis aórticas).
Las medidas opcionales son:
- •
Uso de catéteres impregnados con antimicrobianos11,13–15,17,27–43. (Evidencia alta/ recomendación fuerte)
Se han revisado tres metaanálisis27–29 que objetivaron que los CVC impregnados en antimicrobianos presentaban menor riesgo de BRC que los CVC estándares, aunque no había diferencias en la mortalidad. En población infantil, un metaanálisis de 202130 muestra que no se encontró diferencias significativas en la incidencia de BRC entre los CVC impregnados y los CVC estándar.
Respecto a las recomendaciones de diferentes sociedades científicas, las estadounidenses13, las inglesas11 y las argentinas17 proponen la utilización de CVC impregnados en pacientes adultos si las tasas de BRC siguen altas. No son propuestos por las recomendaciones francesas publicadas en 202015.
Las limitaciones descritas para el uso de CVC impregnados son la posible aparición de infecciones por microorganismos resistentes al antimicrobiano (reportadas en estudios in vitro y en modelos animales)32–33 y de alergias al antimicrobiano (casos aislados)34–43. Estos factores limitantes se han reportado principalmente en los catéteres impregnados en clorhexidina/sulfadiazina argéntica.
- •
Higiene corporal diaria con clorhexidina 12,44–53. (Evidencia moderada/recomendación fuerte)
La higiene diaria con clorhexidina (HDC) se ha propuesto como una medida preventiva de las infecciones adquiridas en UCI, incluida la bacteriemia, mediante la disminución de la carga bacteriana cutánea44.
Se han revisado cuatro metaanálisis45,49. Todos ellos sugieren que la HDC reduce el riesgo de BRC. El metaanálisis de Frost et al.47 aporta que el número necesario de pacientes a tratar para evitar un caso de BRC se estima en 360 cuando la densidad de incidencia de bacteriemia es de cinco episodios por 1.000 días de dispositivo. Se necesitarían 1.780 higienes para evitar un episodio de BRC cuando la incidencia es de un episodio por 1.000 días de dispositivo. Los autores sugieren, por lo tanto, que se evalúe el riesgo de BRC antes de implementar la medida.
Con referencia a las guías publicadas, tanto las del CDC12, como las de la Society for Healthcare Epidemiology of America - Infectious Diseases Society of America (SHEA-IDSA)13 y las asiáticas14, incluyen la HDC como recomendación en la prevención de la BRC, con diferentes niveles de evidencia.
Unas guías recientes sobre estándares en la terapia de infusión sugieren considerar el HDC en unidades con altas tasas de BRC (incluidos los lactantes de > 2 meses) cuando otras estrategias no han sido efectivas16.
No se contempla la HDC en las recomendaciones de la Joint Comissión50, el Institut for Health improvement51, ni en las guías francesas52.
Las principales limitaciones para el uso de la HDC son la potencial aparición de resistencias a la clorhexidina y el incremento de bacteriemia por gramnegativos, así como la tolerancia y los efectos adversos en los tratamientos prolongados52.
- •
Uso de tapones con solución antiséptica en los conectores53–60. (Evidencia moderada/ recomendación fuerte)
Con base en las guías clínicas y estudios publicados, se recomienda la desinfección de los puertos con antiséptico antes de usar el conector, aplicar una toallita/gasa con antiséptico y desecharla después de su limpieza enérgica. La evidencia en torno a este tema es moderada debido a la heterogeneidad en el uso de diferentes antisépticos, en los tiempos necesarios de aplicación y en el tipo de conectores y cobertores, así como la calidad de los estudios.
Gorski et al.53 recomienda el uso de desinfección activa o pasiva siguiendo las instrucciones del fabricante. Sugiere realizar una desinfección pasiva aplicando un tapón o cubierta que contenga un agente desinfectante para crear una barrera física a la contaminación entre usos.
Flynn et al.55 en una revisión sistemática que incluía 12 estudios cuasiexperimentales encontraron que las toallitas de gluconato de clorhexidina alcohólica se asociaron con una cantidad significativamente menor de BRC que las toallitas con alcohol al 70%. Los capuchones impregnados de alcohol se asociaron con una cantidad significativamente menor de BRC que las toallitas con alcohol al 70%. Estos resultados, deben tratarse con cautela debido al diseño de los estudios.
- •
Uso de apósitos impregnados con clorhexidina 12,61–75. (Evidencia moderada/ recomendación fuerte)
Se han analizado cinco metaanálisis61–65 y cuatro ECA controlados66–69, se revisaron las recomendaciones de siete sociedades científicas12,70–73 y dos revisiones sistemáticas74,75.
Los metaanálisis concluyen, en mayor o menor medida, que los apósitos impregnados con clorhexidina son beneficiosos para prevenir la colonización y la BRC. El metaanálisis de Safdar et al.65 justifica su uso rutinario en pacientes con alto riesgo de BRC o colonización de CVC o catéteres arteriales en UCI.
En cuanto a los ensayos clínicos, todos ellos consideran que estos apósitos disminuyen el riesgo de infección y colonización del CVC. El estudio de Timsit et al.66 concluye que el uso de estos apósitos en CVC en UCI reduce el riesgo de infección incluso cuando las tasas de infección de fondo son bajas. Otro ensayo del mismo grupo67 que valoraba los apósitos impregnados en clorhexidina frente a los apósitos adhesivos, mostró disminuciones en la colonización del CVC y en las tasas de colonización de la piel al retirar el catéter, aunque refiere que la tasa de dermatitis de contacto fue del 1,1% con el apósito de clorhexidina y del 0,29% con el apósito sin ella. Un estudio68 en pacientes pediátricos con el mismo objetivo concluyó que los apósitos impregnados en clorhexidina redujeron las tasas de BRC, contaminación, colonización e infección local del catéter, pero no fue significativamente mejor que el uso de apósitos estándar.
Respecto a las recomendaciones de las sociedades científicas, las francesas15, las americanas12,13,70–72, las asiáticas14 y escocesas73 recomiendan la utilización de los apósitos impregnados en clorhexidina (en sus diferentes presentaciones) para disminuir las tasas de colonización y de infección del catéter. A excepción de la guía de la Infectious Diseases Society of America la recomendación se realiza en pacientes mayores de dos meses.
La guía de la Asia Pacific Society of Infection Control (APSIC)14 recomienda usar apósitos de esponja impregnados de clorhexidina para los CVC si la tasa de infección por BRC es alta y no disminuye a pesar del cumplimiento de las medidas básicas de prevención, incluida la educación y la formación. Esta misma recomendación la realiza la guía de la Association for Professionals in Infeccion Control and Epidemiology (APIC)72.
La revisión sistemática llevada a cabo por Puig-Asensio et al.75 informa de dermatitis de contacto asociada al uso de apósitos con clorhexidina (RR = 5,16; IC del 95%: 2,09-12,70), especialmente en neonatos y poblaciones pediátricas en las que se produjeron reacciones graves.
- •
La evidencia sobre la utilidad de la ecografía durante la inserción del catéter como medida preventiva de infección es muy limitada. No obstante, se recomienda realizar la inserción de los CVC guiada por ecografía para reducir el número de intentos de canulación y las complicaciones mecánicas. La inserción ecoguiada debe de efectuarse por personal capacitado en esta técnica.
Se ha considerado adecuado resaltar algunas medidas que se deben evitar mediante la inclusión del apartado «NO HACER»:
- •
No utilizar profilaxis antibiótica para la inserción de los CVC. (Evidencia moderada/ recomendación fuerte)(No revisada).
- •
No realizar cambios periódicos rutinarios de los CVC por punción. (Evidencia moderada/ recomendación fuerte).
Los estudios controlados que han evaluado la eficacia del cambio rutinario de CVC vs. el cambio motivado por indicación clínica se realizaron en la década de los 90 del siglo pasado76–78. En ninguno de estos tres estudios controlados, en que se incluyeron pacientes de UCI, se observa que la estrategia del cambio rutinario de los catéteres como medida de prevención de la BRC fue superior al cambio motivado por indicación clínica.
- •
No realizar cambios periódicos rutinarios de los CVC mediante guía. (Evidencia moderada/ recomendación fuerte)
Se revisó un metaanálisis79 que incluyó 12 ensayos clínicos controlados, en los que se comparaba la eficacia del recambio rutinario a través de guía vs. la inserción en un sitio nuevo. La recolocación a través de guía se asoció a una mayor tendencia de colonización de catéter independientemente de la sospecha de infección en el momento del recambio. El recambio con guía se asoció también a una tendencia de mayor frecuencia de infección en el sitio de inserción y de BRC.
- •
No utilizar antibióticos y antisépticos tópicos en pomada para proteger el punto de inserción (Evidencia moderada/ recomendación fuerte)(No revisada).
- •
No utilizar el mismo equipo de infusión con cada nueva bolsa de hemoderivados. (No revisada).
- •
No dejar sin tapón cualquier puerto que no esté en uso. (No revisada).
Con base en la revisión realizada y en la ponderación de eficacia, tolerancia y aplicabilidad, se han identificado seis recomendaciones que deben aplicarse de forma obligatoria en todas las unidades adheridas a proyecto BZ. Además, se han añadido al proyecto cuatro recomendaciones opcionales, solo para los pacientes adultos con más alto riesgo de BRC con una evidencia fuerte o moderada y con recomendación fuerte. Por último, se consideró oportuno incluir seis recomendaciones de lo que no debe realizarse, con grado de evidencia moderado y recomendación fuerte.
FinanciaciónFinanciado, en parte, por el Ministerio de Sanidad, Política Social e Igualdad de España a través de un contrato (Expediente n.° 2021/48603/001).
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.