El objetivo del estudio Perfil-es era conocer, en la práctica clínica, la proporción de TARV de inicio basado en ITINAN o IP/r e identificar los factores implicados en la decisión terapéutica.
MétodosEstudio observacional, retrospectivo en 65 hospitales.
ResultadosSe iniciaron 1.687 TARV: un 53% basado en ITINAN y un 42% en IP/r. Se analizaron 642 pacientes. El 72% presentaba un recuento de CD4<350 células/μl.
ConclusiónEn España el TARV de inicio sigue siendo tardío. Los ITINAN son la elección más frecuente aunque los IP/r desempeñan un importante papel.
The purpose of Perfil-es study was to identify the proportion of patients starting ARV treatment based on NNRTIs or PI/r, and to identify the variables involved in the therapeutic decision-making in standard clinical practice.
MethodsAn observational restrospective study performed in 65 Spanish hospitals.
ResultsWas a total of 1,687 starts: 53% with NNRTI-based regimen and 42% with PI/r, and of the 642 patients analyzed, 72% had a CD4 count<350 cells/μl.
ConclusionThe initiation of ARV treatment is still late in Spain. NNRTIs are the more frequent choice, although PI/r plays an important role.
Las guías de tratamiento antirretroviral (TARV)1–3 recomiendan como terapia de inicio la combinación de 2 análogos de nucleósidos/nucleótidos asociados a un tercer fármaco. La elección de este último, ya sea un inhibidor de la transcriptasa inversa no análogo de nucleósido (ITINAN), un inhibidor de la proteasa potenciado con ritonavir (IP/r) o un inhibidor de la integrasa, se fundamenta sobre los datos de eficacia y seguridad de los ensayos clínicos y sobre varios factores específicos del paciente.
En los últimos años, la aparición de nuevos IP/r, con reducción de dosis e intervalo de ritonavir, administrados una vez al día, y con eficacia y tolerabilidad mejoradas2,4–6, han conseguido que la decisión acerca del tercer fármaco del TARV de inicio sea más discutida. Hasta la fecha, no disponemos en España de estudios comparativos actualizados que aclaren cuál es el TARV de inicio más idóneo, o si depende de diferentes perfiles de pacientes.
El objetivo principal de este estudio fue conocer la proporción de inicios de TARV basados en ITINAN, en IP/r o en otra clase de antirretrovirales, y comparar el perfil clínico de los pacientes que comienzan con un ITINAN o un IP/r en la práctica clínica en España.
MétodosDiseño del estudio, investigadores y pacientesEstudio observacional, multicéntrico, realizado en 65 hospitales españoles y con la participación de 72 investigadores. El estudio se desarrolló en 2 fases. En la primera fase del estudio (fase i), de corte transversal, se recogieron todos los inicios de TARV que tuvieron lugar entre el 15 de enero 2010 y el 15 de julio 2010 en los hospitales participantes. Únicamente se registró si el TARV de inicio estaba basado en ITINAN, IP/r o en otra clase diferente, y si el paciente participaba en un ensayo clínico o no. En la segunda fase (fase ii) se solicitó consentimiento informado para incluir a los pacientes de manera retrospectiva, consecutiva y pareada 1:1, cuando acudían a consulta ordinaria para la recogida de datos de la historia clínica. Se excluyeron pacientes participantes en ensayos clínicos, con primoinfección por el VIH o que usaran una combinación diferente a ITINAN o IP/r. El estudio fue aprobado por el Comité Ético de Investigación Clínica de Galicia, y se desarrolló de acuerdo a la Declaración de Helsinki y a las Guías de Buena Práctica Clínica.
Análisis estadísticoSe realizó un análisis estadístico descriptivo de las variables clínicas al inicio del TARV. La relación entre las características clínicas de los pacientes que inician el TARV con un régimen basado en un ITINAN o un IP/r se evaluó mediante un análisis bivariante, utilizando el test de Student para las variables cuantitativas y el test de Chi-cuadrado para el resto de las variables independientes cualitativas. Las variables clínicas con significación estadística en el modelo bivariante fueron incluidas en un análisis de regresión logística multivariante y se calcularon los odds ratio (OR) para los factores que influían de forma independiente en la selección de IP/r respecto a ITINAN. El análisis estadístico fue realizado mediante el paquete estadístico SPSS versión 17.0 (SPSS Inc, Chicago, IL, EE. UU.).
ResultadosModalidades de tratamiento antirretroviral de inicioDurante los 6 meses de la fase i se registraron 1.687 inicios de TARV. El 53% de inicios de TARV se basaba en ITINAN, mientras que en un 42% estaba basado en IP/r. Un 3% usaban pautas con combinaciones diferentes, y un 2% participaban en ensayos clínicos con antirretrovirales.
Características basales al inicio del tratamiento antirretroviralEn la fase ii del estudio se incluyeron 642 pacientes (341 comenzaron con un régimen con ITINAN y 341 con IP/r). La media desde el diagnóstico de infección por VIH al inicio del TARV fue de 3,6±5,3 años. Al inicio del TARV, el 28% de los pacientes mostraban un recuento de CD4<200 células/μl, y el 72% presentaban un recuento de CD4<350 células/μl.
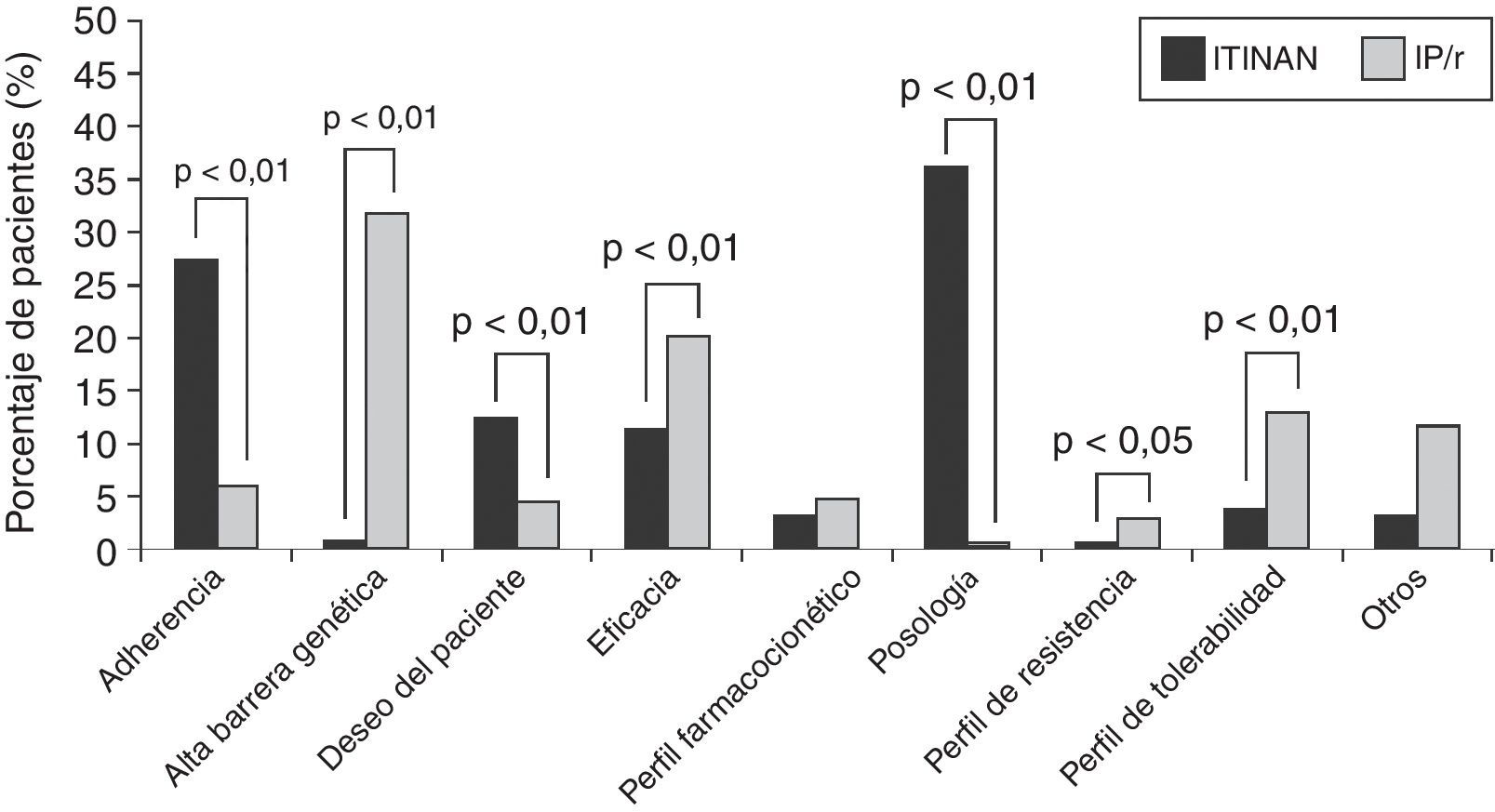
Motivos de elección/preferencia del tercer antirretroviralLa preferencia por los ITINAN estaba motivada por la mejor adherencia, posología y por el propio deseo del paciente. Los motivos para la elección de IP/r fueron la alta barrera genética, la eficacia, el perfil de resistencias, la no disponibilidad del test de resistencia y el perfil de tolerabilidad (fig. 1). El no disponer del resultado del test de resistencia previo al TARV de inicio condicionaba la elección de IP/r.
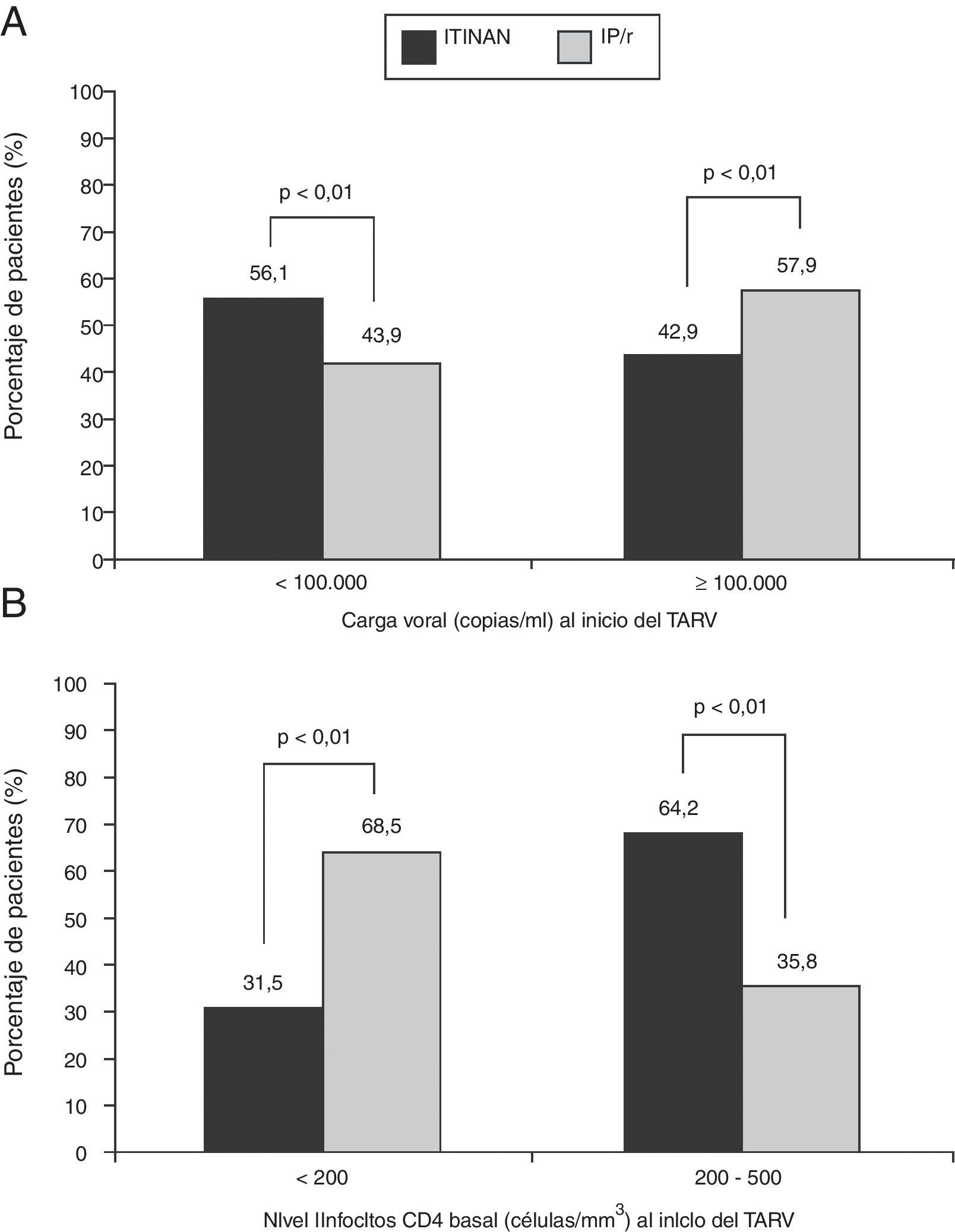
Relación entre las características clínicas de los pacientes y la selección del tratamiento antirretroviral de inicioEl análisis del perfil clínico de estos pacientes reveló que los IP/r se utilizaron con una frecuencia significativamente mayor que los ITINAN, en pacientes con alta carga viral (≥100.000 copias/ml), recuentos de CD4<200 células/μl (fig. 2) y en estadio C de la enfermedad (65 vs. 35%; p<0,01). El análisis de regresión logística identificó la carga viral≥100.000 copias/ml (OR: 1,49; IC 95%: 1,06-2,11) y el recuento de CD4<200 células/μl (OR: 0,41; IC95%: 0,28-0,60) como factores que influyen de forma independiente en la selección de IP/r respecto a ITINAN.
A) Carga viral (copias/ml) al inicio del primer régimen antirretroviral con un ITINAN o un IP/r; B) Recuento de CD4 al inicio del régimen ARV con un ITINAN o un IP/r. El análisis del perfil clínico de estos pacientes reveló que los IP/r se utilizaron con frecuencia significativamente mayor que los ITINAN en pacientes con alta carga viral (≥100.000copias/ml), con recuento de CD4<200células/μl.
El estudio Perfil-es constituye una amplia muestra de pacientes que inician su primer TARV en España. Los hallazgos descritos en el presente estudio plantean que, en la actualidad, la simplicidad y comodidad de efavirenz siguen favoreciendo su uso como primera pauta antirretroviral mientras que los IP/r son seleccionados por los clínicos por su potencia, particularmente debido a su elevada barrera genética, y buena tolerabilidad.
En cuanto al perfil clínico de los pacientes, el presente estudio apunta a que actualmente sigue existiendo una tendencia a pautar un régimen basado en un IP/r como TARV de inicio en aquellos pacientes que presentan características asociadas a un peor pronóstico de la enfermedad, en concordancia con los resultados de estudios de cohortes españolas realizados entre 2004 y 20087,8.
Actualmente existe un debate en la comunidad científica en torno a si es necesario iniciar el TARV con cifras de linfocitos CD4>350 células/μl, siendo este un marcador independiente de progresión de la infección por el VIH. En España aún existe un diagnóstico tardío del VIH9, que implica a su vez un inicio tardío del TARV. Así se refleja en los resultados del presente estudio, donde el 30% de los pacientes partía de una situación inmunológica basal con cifras de CD4<200 células/μl y la mayoría de los pacientes (72%) iniciaron el TARV con un recuento de CD4<350 células/μl.
Además de las limitaciones obvias por la naturaleza retrospectiva del estudio, el análisis se encuentra limitado por el hecho de que no se recogieron los datos clínicos de todos los inicios de TARV en 2010. Otra limitación reseñable podría ser la imposibilidad de estudiar a los pacientes que no acceden al sistema sanitario ni a las personas infectadas por el VIH pero no diagnosticadas, que afecta a la generalización de los datos. No obstante, esta limitación es común a cualquier estudio realizado en el marco hospitalario.
Si bien globalmente el TARV de inicio basado en un ITINAN sigue siendo la opción más frecuente, los últimos IP/r incorporados al arsenal terapéutico presentan un importante y creciente papel en este escenario, particularmente en aquellos pacientes con elevada carga viral y con recuento de CD4<350 células/μl. La presente recogida de inicios de TARV constituye una fuente de información clínica basada en una amplia muestra de pacientes que ofrece una visión global del panorama actual de inicios de TARV en el paciente infectado por VIH en España.
Conflicto de interesesEl presente estudio ha sido financiado plenamente por Janssen. Los autores declaran haber recibido compensación económica por haber realizado labores de asesoramiento para Janssen, compañía promotora del estudio. Francisco Ledesma, Marta Palazuelos y Henar Hevia pertenecen al Departamento Médico de Janssen.
Los autores quieren expresar su agradecimiento al resto de los investigadores del estudio Perfil-es. Aguirrebengoa Ibarguren, K.; Antela López, A.; Arazo Garcés, P.; Asensi, V.; Bassa, A.; Berenguer Berenguer, J.; Boix Martínez, V.; Calvo Sánchez, M.; Canet, R.; Cano Sánchez, A.; Cardenes Santana, M. A.; Carmena Carmena, J.; Cartón, J.A.; Casas García. E.; Castaño Carracedo, M. A.; Cervero Jiménez, M.; Clotet Sala, B.; Condés Moreno, E.; Cordero Sánchez, M.; Cortés, M.C.; Crusells Canales, M.J.; Cucurull, J.; Curran, A.; Dalmau, D.; de la Fuente García, B.; Deig, E.; Domingo Pedrol, P.; Estrada Pérez, V.; Fariñas Álvarez, M. C.; Fernández Rodríguez, R.; Fernández, P.; Ferrero Beneitez, O.L.; Flores Cid, J.; Galindo Puerto, M.J.; Garcia Deltoro, M.; Goenaga Sánchez, M.A.; Gómez Sirvent, J. L.; González García. J.; Gutierrez, F.; Knobel, H.; Labarga Echevarría, P.; Linares, M.; López Aldeguer, J.L.; López Cortés, L.; López Ruz, M. A.; Lorenzo González, J.F.; Mallolas, J.; Martín Jiménez, T.; Martín Ruiz, C.; Merino Muñoz, D.; Moreno Torrico, A.; Ocampo Hermida, A.; Oteo Revuelta, J.A.; Pardo Reche, P.; Pedreira Andrade, J.D.; Pedrol Clotet, E.; Pérez Elías. M.J.; Pérez Guzmán, E.; Pérez-Cecilia, E.; Podzamczer, D.; Portu Zapirain, J. J.; Pulido Ortega, F.; Ribera Pascuet, E.; Riera Jaume, M.; Rivero Román, A.; Rodríguez, R.; Rubio, R.; Santos González, J.; Sanz Sanz, J.; Tellez Pérez, F.; Tellez, M. J.; Tornero Estébanez, C.; Vera Méndez, F. J.; Vergas, J.; Vicina Fernández, P.