La política de antibióticos es el conjunto de estrategias y actividades llevadas a cabo para organizar el tratamiento antimicrobiano en el hospital, y conseguir resultados en salud para los pacientes. Los principios básicos que deben dirigirla son la medicina basada en la evidencia, la epidemiología local y la libertad de prescripción de los facultativos. En la actualidad, la política de antibióticos es más necesaria que nunca por razones clínicas, epidemiológicas y económicas. La Comisión de Infecciones es la responsable de la política de antibióticos en los hospitales. Sus funciones, como órgano asesor de la dirección médica, son el análisis de la epidemiología de las infecciones del centro, las medidas para su prevención y control, la mejora del uso apropiado de los antimicrobianos, la formación y la producción de conocimientos. Conseguir los objetivos clínicos, ecológicos y económicos de la política de antibióticos no es tarea fácil. Poner de acuerdo a cientos de profesionales en torno a las recomendaciones sobre indicaciones, posología y duración del tratamiento antibiótico basadas en las mejores evidencias científicas y en las guías locales, es complejo, pero se puede hacer. Para ello es clave que la Comisión de Infecciones desarrolle el PROA a través de un equipo multidisciplinar y con liderazgo profesional, y que cuente con el apoyo institucional que asegure que el buen uso de los antimicrobianos es un objetivo prioritario del centro, y por lo tanto de cada uno de los servicios implicados, y que el equipo de PROA dispone de los recursos necesarios.
The antibiotic policy is the set of strategies and activities undertaken to organize the antimicrobial treatment in the hospital, and achieve health outcomes for patients. The basic principles are to be direct evidence-based medicine, local epidemiology and freedom for prescribing physicians. An antibiotic policy is now more necessary than ever for clinical, epidemiological and economic reasons. The Infection Committee is responsible for the antibiotics policy in hospitals. Its functions as an advisory body to the medical directorate are the analysis of the epidemiology of the infections in the center, measures for its prevention and control, improving the appropriate use of antimicrobials, training, and knowledge production. To achieve clinical, environmental and economic policy objectives of antibiotics is not easy. The agreement of hundreds of professionals for recommendations on indications, dosage and duration of antibiotic treatment, based on the best scientific evidence and local guides is complex, but it can be done. The key to this is that the Infection Committee develops antimicrobial stewardship through a multidisciplinary team and professional leadership, and has the institutional support to ensure that the proper use of antimicrobials is a priority for the center, and therefore of each of the services involved, and that the team has the resources for antimicrobial stewardship.
La política de antibióticos es el conjunto de estrategias y actividades llevadas a cabo para organizar el tratamiento antimicrobiano en el hospital, mejorar el uso apropiado de los antibióticos y conseguir resultados en salud de los pacientes. Los principios básicos que deben dirigir la política de antibióticos son tres: la medicina basada en la evidencia, la epidemiología local y la libertad de prescripción de los facultativos. La Comisión de Infecciones y Antimicrobianos (CI) es la responsable de la política de antibióticos en los hospitales.
En la actualidad, la política de antibióticos es más necesaria que nunca por razones clínicas, epidemiológicas y económicas. Por razones clínicas porque el 50% de las prescripciones de antibióticos son inapropiadas y sus consecuencias son muy graves: reducción de las posibilidades de curación de las infecciones, aumento del riesgo de muerte y de secuelas en las infecciones graves, e incremento de los efectos adversos1.
La razón principal de este uso inapropiado tan elevado es el déficit de conocimientos de los médicos prescriptores sobre las enfermedades infecciosas en general y de los antibióticos en particular. Este déficit es proporcional al desequilibrio creciente entre la ingente cantidad de conocimientos generados sobre los antibióticos y las infecciones, y el tiempo que se dedica a la formación2. Los antimicrobianos son muy numerosos y complejos. Comprenden decenas de fármacos, pertenecientes a 10 familias de antibióticos y 4 de antifúngicos, con mecanismos de acción, espectros de actividad antimicrobiana, posología, farmacocinética, farmacodinamia, efectos adversos, interacciones y costes muy diferentes. Sin embargo, la dedicación a la formación continuada en antibióticos es secundaria en la mayoría de las especialidades clínicas que los usan a diario. Esta situación de conocimiento insuficiente de muchos médicos prescriptores produce inseguridad, y en ella el marketing comercial es muy influyente, y contribuye a la situación de sobreuso actual.
La política de antibióticos es más necesaria que nunca por razones ecológicas, y más aún en nuestro país, en el que las tasas de resistencia bacteriana están entre las más altas de Europa3. Entre las consecuencias negativas del uso inapropiado de antimicrobianos está la generación y diseminación de las resistencias bacterianas, y con ello el agotamiento global de los antimicrobianos activos, especialmente frente a bacilos gramnegativos. Por ello, al objetivo tradicional de mejorar el pronóstico de los pacientes con infecciones es imprescindible añadir el impacto ecológico de los antimicrobianos.
La política de antibióticos es también más necesaria que nunca por razones económicas, y más aún en nuestro país, en el que el consumo de antimicrobianos en los hospitales, estimado del porcentaje de pacientes en tratamiento antibiótico, es un 40% superior a la media europea3, y en el que la crisis económica y política está poniendo en riesgo el sistema sanitario universal y gratuito. Por ello, a los objetivos tradicionales de la política de antibióticos resulta imprescindible añadir objetivos de eficiencia en el uso de los antimicrobianos.
La Comisión de Infecciones: composición y funcionesLa política de antibióticos es responsabilidad de la CI, que es una comisión de calidad del hospital, dependiente de la dirección médica4. La CI está compuesta por el presidente/secretario y los vocales. Para darle el máximo carácter institucional el presidente debería ser el director médico. El secretario de la comisión debería ser uno de sus miembros, elegido por su experiencia y conocimientos en las enfermedades infecciosas y los antimicrobianos, y por su capacidad de liderazgo. Los vocales deben ser representativos de los servicios más implicados en la prevención, diagnóstico y tratamiento de las infecciones relacionadas con la asistencia sanitaria (IRAS). La composición debería incluir con carácter fijo a especialistas en medicina preventiva, enfermedades infecciosas, microbiología, farmacia hospitalaria, medicina intensiva y enfermería. Otras especialidades, como la pediatría y las especialidades quirúrgicas, deberán incluirse en función de las características de cada hospital. El trabajo de los miembros de la CI tiene que ser dinámico y proactivo, participando en las actividades de la comisión, en la elaboración de indicadores, informes y estudios. Las funciones tradicionales del secretario son elaborar el orden del día de cada reunión, dirigir y moderar las reuniones, vigilar el cumplimiento de las normas, comunicar a la dirección del centro las actividades e informes realizados, realizar las actas y la memoria anual; pero el secretario ideal debe además liderar la comisión, impulsando y proponiendo proyectos que respondan a los problemas reales del centro.
La CI debe reunirse mensualmente o bimensualmente según las necesidades del hospital. Sus funciones, como órgano asesor de la dirección médica del centro, son las siguientes:
- 1.
Análisis de la epidemiología de las infecciones del centro. La CI debe coordinar las actividades del equipo de control de las IRAS y diseñar las estrategias para su aplicación institucional; la monitorización y registro de las tasas globales de prevalencia e incidencia de IRAS y de procedimientos singulares, como las infecciones posquirúrgicas, o las bacteriemias relacionadas con el catéter, las actividades de formación, la retroalimentación de la información generada, y la propuesta de nuevos objetivos y medidas de mejora. Es necesario realizar análisis periódicos con los datos microbiológicos de las muestras más relevantes desde el punto de vista clínico y/o epidemiológico: microorganismos aislados en hemocultivos, aspirados bronquiales, orina, estudios de portadores y otras muestras, expresados en valor absoluto y porcentaje respecto al total de las muestras; así como el perfil de sensibilidades de los mismos. Los resultados deben mostrarse de forma global y desglosados por servicio, y presentarse al menos anualmente para todo el centro, y en las áreas con mayor incidencia es necesario hacerlo con mayor frecuencia, al menos trimestralmente.
- 2.
Medidas para la prevención y control de las infecciones. La CI debe elaborar las medidas necesarias para la vigilancia y control de las IRAS, como las recomendaciones de los diferentes tipos de aislamiento, las recomendaciones para prevenir la infección relacionada con el catéter, de la herida quirúrgica, las recomendaciones de la higiene de manos, y para la detección y control de los brotes en cada centro. La aplicación de estas medidas establecidas por la CI para todo el hospital las llevará a cabo el equipo de control de infección.
- 3.
La mejora del uso apropiado de los antimicrobianos. Es una de las principales funciones de la CI, y la debe enmarcar dentro de los programas de optimización de antimicrobianos (PROA)1,5 La CI debe diseñar el PROA, buscar el apoyo institucional y elegir al equipo multidisciplinar para llevarlo a cabo en el día a día. Las medidas del PROA incluyen la elaboración de las guías locales de antimicrobianos, las actividades de intervención, como las asesorías o las auditorías, los cursos, y los informes periódicos a los diferentes servicios y unidades así como a la propia CI. Las guías para el diagnóstico y tratamiento empírico, y de profilaxis quirúrgica, contienen las recomendaciones del tratamiento antimicrobiano basadas en la epidemiología local. Para que sean bien acogidas y aplicadas es preciso que sean muy participativas, incluyendo en la autoría y en la discusión previa a su publicación a profesionales de los servicios/unidades más implicadas en el tratamiento del síndrome clínico concreto. Cada antimicrobiano incluido en el centro debe aprobarse por la CI con unas indicaciones concretas que ayudarán al buen uso del mismo. El resto de las medidas y actividades de los PROA no es objetivo de esta revisión.
- 4.
La formación. Para alcanzar estos objetivos es determinante la formación de los profesionales del centro. Es responsabilidad de la CI diseñar la estrategia de formación. Las sesiones clínicas de cada unidad o servicio son el escenario ideal para presentar los programas frente a las IRAS y los PROA, así como para periódicamente presentar y discutir los resultados obtenidos.
- 5.
La producción de conocimientos. La CI debería impulsar la producción del conocimiento en torno a las actividades que realiza, aprovechando así el incentivo profesional que los resultados científicos suponen6.
Conseguir los objetivos clínicos, ecológicos y económicos de la política de antibióticos no es tarea fácil. Poner de acuerdo a cientos de profesionales en torno a las recomendaciones acordadas sobre indicaciones, posología y duración del tratamiento antibiótico, basadas en las mejores evidencias científicas y en las guías locales de antibioterapia es complejo, pero se puede hacer y es necesario7,8. Para ello es clave que la CI desarrolle el PROA a través de un equipo multidisciplinar que tenga el suficiente liderazgo profesional para llevar a cabo un programa transversal de esta envergadura, y cuente con el apoyo institucional que asegure que el uso de los antimicrobianos es un objetivo prioritario del centro, y por lo tanto de cada uno de los servicios implicados, y que el equipo de PROA cuente con los recursos necesarios. El equipo del PROA es el brazo operativo de las estrategias de la política antibiótica diseñadas por la CI. Es importante entender que ambos son complementarios porque, aunque sus funciones y tareas son diferentes, sus objetivos finales en cuanto al uso de los antimicrobianos son los mismos.
El 90% del consumo humano de antibióticos se realiza en la comunidad. Por ello la desconexión con atención primaria es una de las debilidades de las políticas de antibióticos al uso, que están centradas en el hospital. Para resolverla es necesario que los PROA de hospital conecten con atención primaria, y realicen una política de antibióticos coordinada que trascienda al centro, a semejanza de como hacen las bacterias multirresistentes que no entienden de tabiques.
Monitorización del consumo de antimicrobianosEl uso de antibióticos en los hospitales tiene unas características particulares, que le dan especial relevancia. Es más complejo, porque en el hospital se atienden las infecciones graves adquiridas en la comunidad, además de las adquiridas en el hospital, por lo que la etiología es más amplia y diversa, con microorganismos más difíciles de tratar. Y la densidad de consumo, expresada por persona y superficie es muy superior al comunitario. Alrededor del 46% de los pacientes ingresados en los hospitales de nuestro país reciben tratamiento antibiótico durante su estancia3, lo que supone una elevada densidad de consumo de antibióticos por metro cuadrado de superficie, que es máxima en las unidades de cuidados intensivos. Consecuencias directas de sendas características del uso de antimicrobianos en los hospitales son el aumento de patógenos multirresistentes, la dificultad para tratar las IRAS causadas por estas bacterias, su mayor morbimortalidad y el incremento del coste del tratamiento de estas infecciones, incluido el gasto farmacéutico directo5. La monitorización del consumo de antibióticos es uno de los indicadores clave para guiar la política de antibióticos de un hospital. Su objetivo es mejorar la eficacia terapéutica, la seguridad, incluido el desarrollo de resistencias y la eficiencia6. La monitorización del consumo de antibióticos permite medir el perfil de consumo, la tendencia en el tiempo, y comparar los resultados de los servicios y centros con ellos mismos y con otros semejantes. La monitorización permite establecer objetivos, evaluar el impacto de los PROA, detectar precozmente desviaciones del perfil esperado y diseñar, en función de los resultados, nuevos objetivos y medidas de mejora.
¿Cuál es el mejor indicador para medir el consumo antimicrobiano? Habitualmente, el cálculo de consumo de antibióticos se ha realizado utilizando datos agregados de consumo de los fármacos en el hospital, basados en un cociente de numerador y denominador. Para el denominador, a nivel hospitalario, clásicamente se han utilizado el número de estancias hospitalarias, número de ingresos o número de altas, expresándose por cada 100 o cada 1.0009. La medida más empleada es el consumo por cada 100 o 1.000 estancias hospitalarias (pacientes/día), ya que es la más útil para realizar un seguimiento más estrecho e independiente de determinados servicios o unidades10 con el fin de implementar medidas de mejora dirigidas a las mismas. Una limitación de este indicador es que no incluye el tratamiento antibiótico realizado en el servicio de urgencias ni el tratamiento antibiótico a pacientes ambulatorios que se dispensa en el hospital.
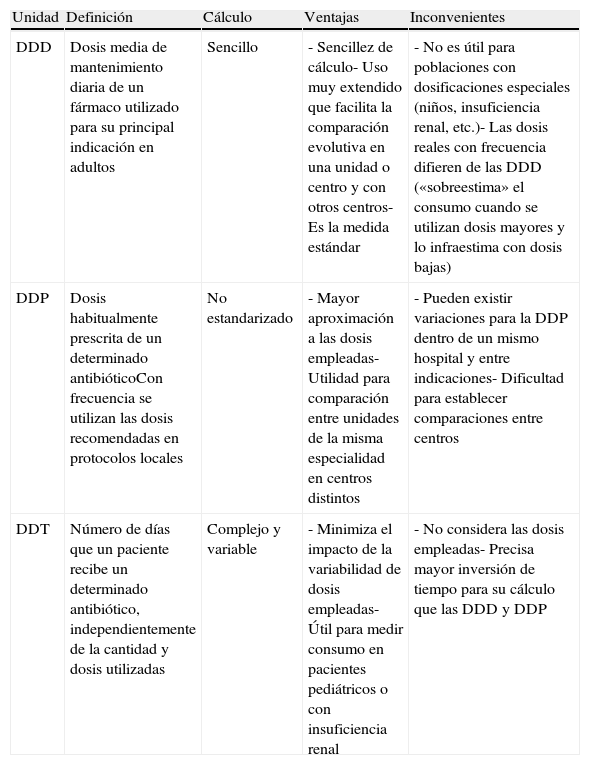
Para el numerador se utilizan 3 unidades de medida distintas, a) las dosis diarias definidas (DDD), de la World Health Organization (WHO) Collaborating Centre for Drug Statistics Methodology11; b) las dosis diarias prescritas12 y/o c) los días de terapia, una nueva unidad utilizada en EE. UU.13. Cada una de ellas presenta ventajas e inconvenientes, a la hora del cálculo y de la estandarización para realizar comparaciones intercentros, que se exponen en la tabla 1.
Unidades de medida para la monitorización del consumo de antibióticos en los hospitales
| Unidad | Definición | Cálculo | Ventajas | Inconvenientes |
| DDD | Dosis media de mantenimiento diaria de un fármaco utilizado para su principal indicación en adultos | Sencillo | - Sencillez de cálculo- Uso muy extendido que facilita la comparación evolutiva en una unidad o centro y con otros centros- Es la medida estándar | - No es útil para poblaciones con dosificaciones especiales (niños, insuficiencia renal, etc.)- Las dosis reales con frecuencia difieren de las DDD («sobreestima» el consumo cuando se utilizan dosis mayores y lo infraestima con dosis bajas) |
| DDP | Dosis habitualmente prescrita de un determinado antibióticoCon frecuencia se utilizan las dosis recomendadas en protocolos locales | No estandarizado | - Mayor aproximación a las dosis empleadas- Utilidad para comparación entre unidades de la misma especialidad en centros distintos | - Pueden existir variaciones para la DDP dentro de un mismo hospital y entre indicaciones- Dificultad para establecer comparaciones entre centros |
| DDT | Número de días que un paciente recibe un determinado antibiótico, independientemente de la cantidad y dosis utilizadas | Complejo y variable | - Minimiza el impacto de la variabilidad de dosis empleadas- Útil para medir consumo en pacientes pediátricos o con insuficiencia renal | - No considera las dosis empleadas- Precisa mayor inversión de tiempo para su cálculo que las DDD y DDP |
La DDD es, hasta la fecha, el único método estandarizado y validado, por lo que se considera de referencia para expresar y realizar comparaciones nacionales e internacionales de presión antibiótica. Ha sido definido por el WHO Collaborating Centre for Drug Statistics Methodology, que utiliza la metodología ATC/DDD, expresando los resultados en función de cada 100 o 1.000 estancias (paciente/día) hospitalarias. Algunos estudios han mostrado la existencia de notables discrepancias al comparar las DDD definidas por el WHO Collaborating Centre for Drug Statistics Methodology y las PDD, entre las que destacan una sobreestimación de consumo de algunos antibióticos como quinolonas14 y cefalosporinas15 con respecto al tratamiento real recibido en el hospital, lo que debe tenerse en cuenta a la hora de interpretar resultados de presión antimicrobiana, especialmente en el caso de fármacos con DDD altas, para los que este efecto tiene mayor relevancia.
Cálculo DDD/100 estancias (WHO Collaborating Centre for Drug Statistics Methodology). El sistema ATC identifica los componentes terapéuticos de cada fármaco para uso humano en relación con el órgano o sistema sobre el que actúan y sus propiedades: químicas, farmacológicas y terapéuticas. Es el sistema de clasificación internacional de fármacos en los estudios de consumo16. La metodología del sistema ATC/DDD constituye una herramienta para el estudio de utilización de fármacos con el fin de mejorar la calidad de prescripción de los mismos y establecer comparaciones de estadísticas de consumo a diferentes niveles. El cálculo del indicador se realiza mediante la siguiente fórmula: n.o DDD/100 estancias=consumo antibiótico/DDD×100/n.o estancias.
Consumo antibiótico es el consumo de antibióticos durante el periodo estudiado expresado en gramos. A la hora de la obtención de datos de consumo solo debe tenerse en cuenta el tratamiento administrado a los pacientes ingresados en el hospital, excluyendo el administrado en el hospital de día, urgencias, pacientes ambulatorios o tratamientos al alta. La DDD asignada por el WHO Collaborating Centre for Drug Statistics Methodology para el antibiótico es la dosis media de mantenimiento diaria de un fármaco utilizado para su principal indicación en adultos.
Número de estancias. Una estancia hospitalaria es una cama ocupada un día durante un tiempo determinado. n.o estancias=n.o camas×días×ocupación. Y la ocupación=n.o días cama ocupada/ n.o días en que la cama podría haber estado ocupada.
¿Cuándo hacerlo? Es necesario medir sistemáticamente el consumo de antibióticos y las tendencias en el tiempo. Existen diferentes proyectos europeos, que promueven esta iniciativa como la European Surveillance of Antimicrobial Consumption Network (ESAC-net)17. A la hora de planificar y llevar a cabo la medición y el seguimiento de los datos agregados de consumo antimicrobiano y ante la complejidad que supone, se plantean una serie de dudas respecto a la periodicidad de la misma, antibióticos clave sobre los que actuar y unidades hospitalarias concretas a las que dirigir estrategias de mejora a implementar, ya que de ello dependerá le efectividad y el impacto sanitario de la monitorización.
En primer lugar, la periodicidad, tal y como establecen las últimas recomendaciones7, dependerá del tamaño y el volumen de carga asistencial del centro; así, podrán realizarse de forma trimestral, semestral o anual. En este punto también influye la necesidad de evaluación de medidas de mejora iniciadas, en función del carácter de estas y del periodo de tiempo que requieran para mostrar su efecto. Por otro lado, los antibióticos a monitorizar serán todos los utilizados en el hospital, haciendo un análisis global y estratificado por familias e individual de cada antimicrobiano, con especial atención a aquellos con mayor impacto asistencial, ecológico y económico.
Este análisis debe realizarse para la totalidad del hospital de cara a la posibilidad de establecer comparaciones intercentros y desglosarlo por servicios y unidades.
¿Cómo hacerlo? Es necesario el desarrollo de estrategias de monitorización de consumo para poder establecer medidas que conduzcan a un control en las resistencias a los antimicrobianos, y que deben abordarse desde un punto de vista multidisciplinar e integral en el seno de los PROA de cada hospital5.
Igualmente es muy importante relacionar la evolución del consumo de antibióticos con indicadores de resultados en calidad de salud, como morbimortalidad de los pacientes con infecciones graves, calidad del uso de antimicrobianos y evolución de las resistencias microbianas, porque la monitorización del consumo es un objetivo intermedio que alcanza todo su valor cuando se relaciona con los objetivos finales en salud antes comentados.
Finamente, la monitorización del consumo de antimicrobianos tiene como objetivo la comparación primero de cada servicio/unidad y hospital consigo mismo, con el fin de ver los éxitos alcanzados o por el contrario la necesidad de mejora, y más adelante la comparación con otros servicios/unidades y hospitales de características semejantes, sabiendo que será necesario tener en cuenta la multitud de factores que influyen en el consumo de antimicrobianos y que hacen compleja esta comparación.
Por último, el estudio de la evolución del gasto económico derivado de este grupo de fármacos también aporta una información valiosa, que complementa la evolución del consumo en DDD y los objetivos primarios de la CI de los PROA.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Nota: sección acreditada por el Consell Català de Formació Continuada de les Professions Sanitàries. Consultar preguntas de cada artículo en: http://www.eslevier.es/eimc/formacion.