A pesar de que para la OMS la polio debería haber sido erradicada en el año 2000 –gracias a la vacunación y a los recursos institucionales, públicos y privados, destinados a tal fin– en 2013 la enfermedad siguió siendo endémica en tres países, Afganistán, Pakistán y Nigeria y se describieron casos en otros cinco. La circulación de poliovirus tipo 1 salvaje en Israel, Gaza y Cisjordania y los casos de Siria fueron una llamada de atención, como en su momento lo fueron los virus derivados de la vacuna oral que siguen siendo un problema. Los viajes «desde» y «a» zonas endémicas son un factor a tener en cuenta en la exportación de los virus y su difusión cuando llegan a zonas con carencias vacunales. Los conflictos bélicos, las persecuciones, la intolerancia, la incultura y la proliferación de grupos y movimientos «antivacunación» son en gran parte la causa de la ausencia y del abandono de la vacunación. En 2014 la situación se ha complicado, tanto que el Comité de Emergencias de la OMS se reunió en mayo para abordar el problema. Es necesario conocer la enfermedad y su agente causal, en el primer caso porque habrá que pensar en ella a la hora de hacer un diagnóstico diferencial de la parálisis flácida y seguir vacunando y en el segundo porque será imprescindible seguir buscando en muestras ambientales el virus de la polio, del que se desconocen muchos aspectos, pues es un modelo para el estudio de otros muchos virus.
Although the WHO original target date for the global eradication of poliomyelitis was the year 2000 –thanks to vaccination and institutional, public and private, resources for that purpose–, in 2013 the disease remained endemic in three countries, Afghanistan, Pakistan and Nigeria, and some cases were described in five others. The circulation of wild type 1 poliovirus in Israel, Gaza and the West Bank and the cases in Syria were a wakeup call, as at that time there were polioviruses derived from the oral vaccine that are still circulating among the human population and can cause the development of the disease. Travelling “from” and “to” endemic areas are factors to consider in poliovirus exportation and in its spread when it reaches areas with poor immunogenicity. Wars, terrorism, intolerance, lack of culture and proliferation of anti-vaccine groups and the rise of the anti-vaccination movement are important factors in the maintenance and expansion of the virus and in the “non-vaccination” against it. Based on the international situation to date, the Emergency Committee of WHO met in May 2014 to address the problem. It is still necessary to enhance the knowledge of the disease and its agent. In the first case to perform a differential diagnosis of flaccid paralysis and to continue vaccination programs, and in the second case to keep studying and looking for the poliovirus in environmental samples, which is a model for the study of many other viruses.
En sentido estricto la poliomielitis (del griego πολιóζ [polios]: gris, μι¿λóζ [myelos]: médula, e íτιζ [itis]: inflamación1) o polio es una enfermedad infecciosa caracterizada por la aparición de una parálisis flácida, aguda, asimétrica, en ocasiones mortal, de la que puede o no haber recuperación y que está producida por los virus de la polio cuando se replican y destruyen las motoneuronas de las astas anteriores medulares y/o bulbares. En la mayoría de las ocasiones la infección por poliovirus es asintomática, a veces producen cuadros leves y solo muy raramente parálisis2.
En el siglo pasado se convirtió en una plaga que azotó a multitud de países, tanto ricos como pobres, marcando profundamente la conciencia de sus habitantes3.
Cuando se producía afectación del bulbo y parálisis de los músculos respiratorios muchos pacientes sobrevivieron gracias a la utilización del pulmón de acero4. La mayoría pudieron abandonarlo al mejorar o recuperarse pero en otros casos su supervivencia inexorablemente dependió del uso de respiradores artificiales.
Durante mucho tiempo sus consecuencias han sido visibles por las discapacidades residuales que dejó al pasar el periodo agudo. Eran frecuentes las imágenes de incapacidad de movimiento autónomo, cojeras y dependencia de terceras personas al igual que las de los artilugios utilizados para mitigar sus consecuencias, bastones, muletas, órtesis, alzas, sillas de ruedas o automóviles adaptados.
Hasta un poco después de la primera mitad del siglo XX en cada clase había uno o más alumnos afectados y las familias esperaban con terror la afectación de uno de sus miembros, hechos que han sido magistralmente recogidos en Némesis, la novela de Philip Roth ambientada en 19445.
En la primera mitad del siglo pasado se ensayaron numerosos procedimientos para luchar contra la infección, la parálisis y las deformidades incluyendo la seroterapia, el uso de inmunoglobulinas, la rehabilitación o las inmovilizaciones pero todos pasaron al arsenal de la historia de la Medicina con el desarrollo de las vacunas.
La vacunación antipolio ha sido un espaldarazo más a la eficacia general de esta práctica a pesar de que su utilización se ha acompañado de incidencias y controversias. Su introducción en los distintos países ha estado seguida por una disminución del número de casos hasta llegar a la eliminación total, siendo los países donde circula el virus muy limitados6. Los países que retrasaron su instauración pagaron un precio muy alto en mortalidad y consecuencias a largo plazo.
En la actualidad gracias a una iniciativa internacional la polio está camino de la erradicación. Previsiblemente será la segunda enfermedad infecciosa en serlo, tras la viruela. En 2013 solo era endémica en Pakistan, Afganistan y Nigeria7. Sin embargo los conflictos bélicos y los movimientos migratorios relacionados con estos siguen siendo un problema en su control: se deja de vacunar y se mueven los portadores, recuérdese al respecto, por ejemplo, el reciente ejemplo de Siria. Otro acontecimiento ha llamado la atención para no bajar la guardia, la circulación de virus en el agua en Israel8. En 2014 la situación ha empeorado.
En el bastante probable escenario de la erradicación la polio no habrá dejado de ser un problema. Durante muchos años quedarán sus secuelas –parálisis, deformidades y síndrome postpolio– y además habrá que seguir vacunando y mantener la vigilancia para estar seguros de su desaparición.
La polio (código CIE-10: A80 de la Clasificación Internacional de Enfermedades) también se ha conocido como poliomielitis aguda anterior, parálisis infantil –porque afectaba particularmente a este segmento poblacional– y enfermedad de Heine-Medin. El día 24 de octubre de cada año se celebra el Día Mundial de la Lucha contra la Poliomielitis.
La enfermedad sigue suscitando interés en la clase médica, hecho objetivable en la elevada cantidad de literatura publicada en los últimos años en revistas indexadas en bases de datos científicas, sanitarias y libros9–12. Este fenómeno también se ha observado en España13–17.
HistoriaSin duda la enfermedad ha afectado desde tiempos remotos al hombre y tradicionalmente se cita como un primer registro gráfico a una estela egipcia de la XVIII dinastía (1580-1350 AC), que se encuentra en el Carlsberg Glyptotek de Copenhague, y que muestra a un sacerdote que usa una muleta a consecuencia de su pierna derecha atrófica y acortada con un pie equino (fig. 1)18.
La primera descripción de la polio se debe a Michael Underwood, un médico inglés que en 1789 la describió en su libro A Treatise on the Diseases of Children, que en su segundo volumen recoge el cuadro Debility of the Lower Extremities (fig. 2) que se corresponde con la enfermedad19.
En 1840 Jacob von Heine, un médico ortopedista alemán, la individualizó clínicamente separándola de otras parálisis y la denominó parálisis espinal infantil en razón a su posible origen medular20.
La última década del siglo XIX marca el comienzo de las epidemias, primero en los países escandinavos y EE. UU, situación que fue in crescendo en la primera mitad del siglo XX18.
En 1908 Karl Landsteiner y Erwin Popper identificaron el origen viral de la enfermedad al inocular intraperitonealmente un filtrado de médula espinal procedente de un niño fallecido por polio a dos monos, un babuino y un rhesus, el primero murió y el segundo desarrolló una parálisis de las extremidades posteriores21.
En esa época (1907-1911) el pediatra sueco Ivar Wickman hizo importantes aportaciones clínicas y epidemiológicas tras el estudio de la epidemia que asoló su país. Demostró su carácter estacional, la mayor incidencia de formas abortivas y no paralíticas, la trasmisión por contacto y que la enfermedad podía aparecer fuera del periodo infantil22.
Durante muchos años, a pesar de observaciones en contra, se consideró que el virus era estrictamente neurotrópico y que probablemente llegaba al sistema nervioso por vía nasal22.
En la historia de la polio, 1916 es una fecha clave, pues durante el verano de este año se produjo en Nueva York una de las mayores y peores epidemias de la enfermedad23.
Los australianos Frank M. Burnet y Jean Macnamara en 1931 demostraron que había al menos dos tipos de virus de la polio24, una aportación trascendental en el desarrollo de las vacunas pues la inmunidad frente a uno no protegía frente al otro.
Albert B Sabin y Robert Ward en 1941 demostraron fehacientemente la transmisión por vía entérica. En las conclusiones de su trabajo señalaron que: «…el virus se distribuye predominantemente en dos sistemas: (a) ciertas regiones del sistema nervioso y (b) el tracto alimentario…», además que «la no demostración del virus en la mucosa nasal, bulbo olfatorio y sustancia perforada anterior sugiere que ni el tracto respiratorio superior ni la vía olfatoria se afectaron en los casos» estudiados por ellos25.
En 1949 John F Ender, Thomas H. Weller y Frederick C Robbins lograron cultivar el virus en cultivos de células embrionarias humanas26 abriendo el camino al desarrollo de las vacunas. Este mismo año David Bodian, Isabel M. Morgan y Howard A Howe separaron serológicamente los tres tipos de poliovirus (PV1, PV2 y PV3)27.
El gran salto se produce en 1955 con la introducción en EE. UU. de la primera vacuna, la inactivada desarrollada por Jonas Salk28,29. En 1963 lo haría la atenuada trivalente de Sabin.
En el trascurso de 1981 Vincent R. Racaniello y David Baltimore dieron a conocer la clonación y secuenciación del PV130.
En 1988 la OMS resuelve abordar la erradicación de la poliomielitis y fijarla para el año 200031. Con la estrategia diseñada en 1999 se logró erradicar el PV232, desde el 10 de noviembre de 2012 no se ha detectado el PV333 y se ha conseguido reducir el número de países endémicos a los tres tipos7.
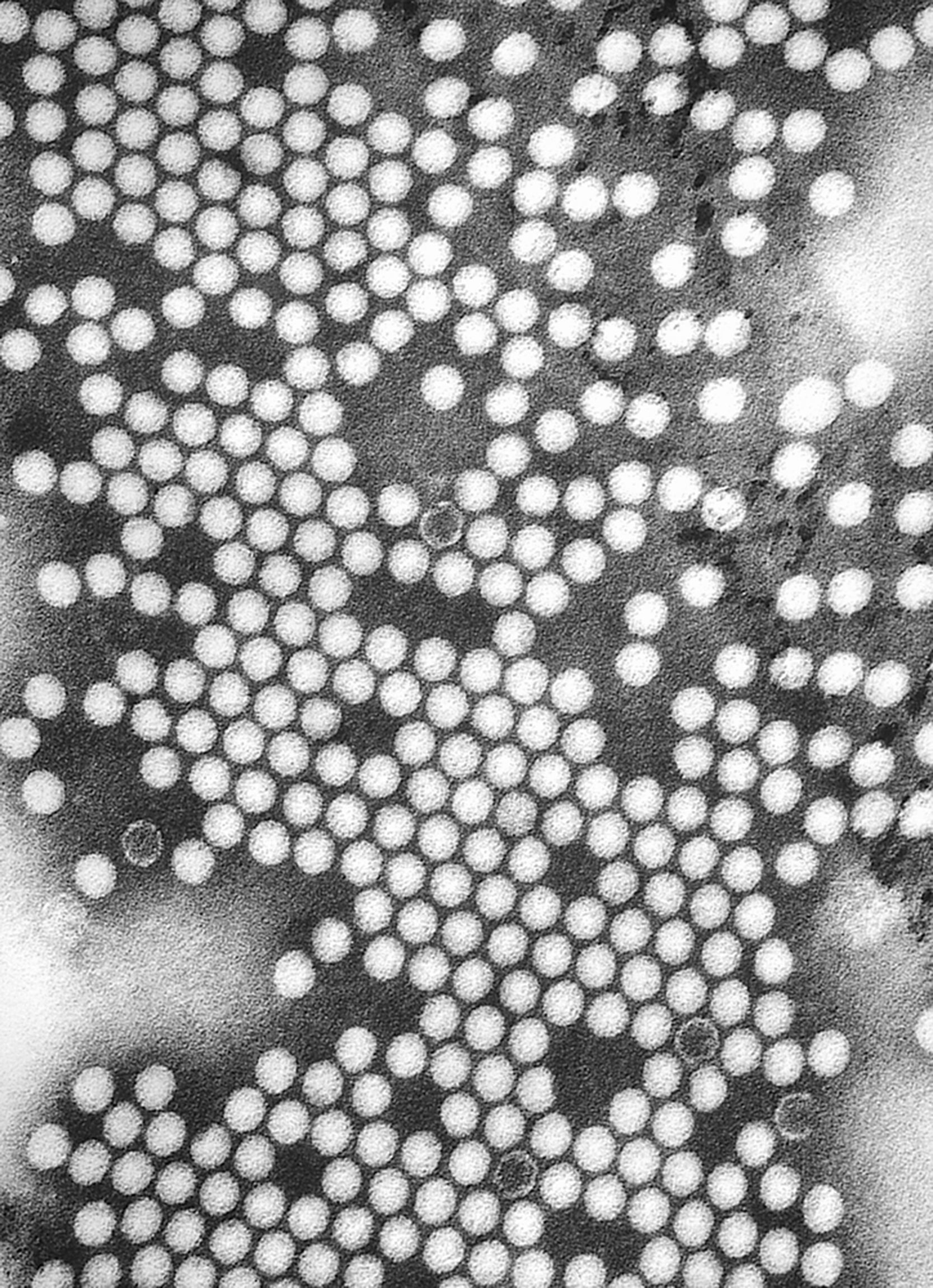
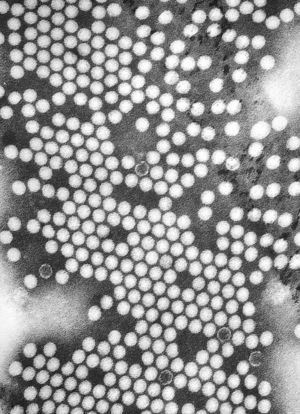
Etiología (aspectos virológicos) y clasificaciónLos virus de la polio son ribovirus, de simetría icosaédrica, desnudos, de forma icosaédrica o redondeada y de tamaño pequeño (30nm), (fig. 3)34,35.
Su genoma está constituido por una sola cadena lineal de ácido ribonucleico de polaridad positiva (ARNss [+]). Su extremo 5′ está covalentemente unido a una pequeña proteína, la VPg, que se supone actúa como iniciador (primer) en la síntesis del ARN36. Tiene alrededor de 7.500 bases34.
Los poliovirus, tanto los salvajes como los utilizados en la vacuna de Sabin, son genéticamente inestables y tienen una gran capacidad de evolución por mutación y recombinación37,38. Se ha estimado que la velocidad de evolución de los genomas de poliovirus es de aproximadamente 10−2 sustituciones nt/sitio/año39. Este hecho es muy relevante desde distintos puntos de vista: la atenuación para obtener vacunas40, la diversificación, la epidemiología, el diagnóstico, el aumento de virulencia y la patogenicidad.
El ARN y la proteína VPg están rodeados y protegidos por una cápsida de simetría icosaédrica formada por 60 proteínas (protómeros). Cada protómero está constituido por cuatro proteínas (VP: viral proteins), de VP1 a VP441, tres superficiales (VP1, VP2 y VP3) y una interna (VP4). Las VP1 (cinco) se disponen en los vértices del icosaedro y las VP2 y VP3 en las caras34. Entre la VP1 y las VP2-VP3 hay una hendidura (cañón), que interviene en la unión a los receptores celulares42 que se han identificado con la glucoproteína CD15543. A la VP4 se une un lípido, el ácido mirístico44. La cápsida interviene en la fijación y en la respuesta inmune específica frente a cada uno de los tres serotipos (PV1, PV2 y PV3)41.
Son virus desnudos, por lo tanto resistentes a muchos agentes externos, incluidos los solventes de los lípidos, lo que permite que pueda ser trasmitido por mecanismos indirectos (agua, fómites,…). Son sensibles al cloro y al glutaraldehido45.
Se replican en el citoplasma, pertenece al grupo IV de Baltimore y su trascripción sigue el patrón ARNss (+)→ARNss (-)→ARNm, su propio ARN al ser de polaridad positiva puede actuar como ARNm. El ARNss (-) es el molde para la replicación en ARNss (+)46. Producen diversas alteraciones citopáticas y son citolíticas47.
Los tres serotipos de virus de la polio se clasifican dentro de la familia Picornaviridae (picornavirus) en el género Enterovirus y en la especie Enterovirus C humanos, en la que también se encuentran otros virus relacionados35. El término picornavirus es un acrónimo formado por la palabra latina pico (pequeño), RNA y virus y define algunas características virológicas de los miembros de esta familia. El nombre Enterovirus deriva del griego
Con relación a la divergencia que puede existir en cada tipo con la correspondiente cepa de la vacuna Sabin se dividen en: 1) virus relacionados (VRPV), aquellos que tienen una divergencia menor al 1% en el caso de los PV1 y PV3 o del 0,6% en el de los PV2, 2) virus derivados (VDPV), aquellos que tienen una divergencia mayor al 1% en el caso de los PV1 y PV3 o del 0,6% en el de los PV2 y 3) virus salvajes (WPV1, WPV2 y WPV3), en los que no hay desviación. Los VDPV se han dividido en tres grupos, en los que hay trasmisión cruzada en la comunidad o circulantes (cVDPV), los aislados en inmunodeficiencias B primarias con infecciones y excreciones muy prolongadas (iVDPV) y los ambiguos que se aíslan de personas sin inmunodeficiencias o de aguas residuales sin fuente conocida (aVDPV)39,48.
Los virus relacionados son fruto de mutaciones y de recombinaciones entre tipos49. La mayoría de los cVDPV se deben a recombinaciones con otros enterovirus C no polio y solo se ha descrito un brote, en China, que no ha seguido este patrón38,50. En los iVDPV se han detectado mutaciones y recombinaciones intertípicas38.
EpidemiologíaEl único reservorio conocido de los poliovirus es humano, solo el hombre y algunos primates tienen receptores para ellos51. Está constituido tanto por los pacientes que sufren una enfermedad activa como por los individuos con infecciones asintomáticas. Se eliminan por heces y por vía respiratoria, en estas se encuentran no solo durante la enfermedad activa sino que se detectan tiempo después. En niños la eliminación fecal es de 3-4 semanas52.
El contagio se produce especialmente por un mecanismo fecal-oral a través del agua, de alimentos o manos, contaminados con heces infectadas. Puede existir un contagio persona a persona, oral-oral. La trasmisión respiratoria seguramente es importante en los ambientes de higiene elevada40.
La población susceptible es la que no tiene anticuerpos como se demostró al prevenirla administrando inmunoglobulina53. Es un virus muy contagioso pues prácticamente el 100% de los individuos que no tienen anticuerpos se infectan.
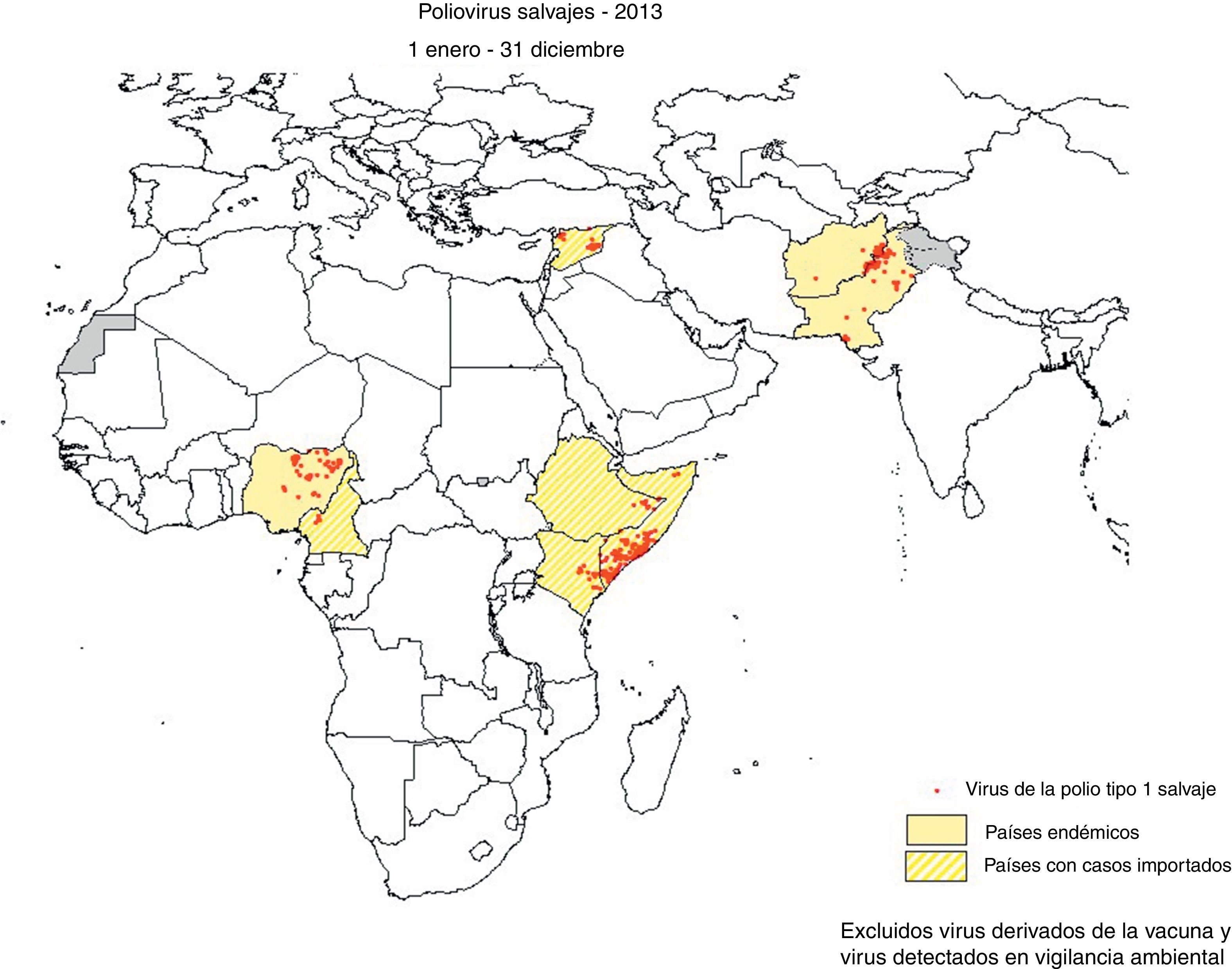
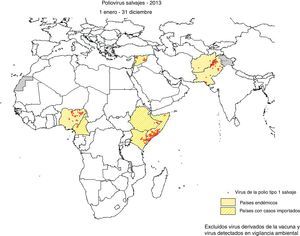
La enfermedad ha tenido una distribución mundial aunque actualmente está limitada a un número limitado de países, siendo endémica en Afganistán, Nigeria y Pakistán, desde los cuales hay riesgo de exportación, especialmente a los países del África occidental y del Cuerno de África. En 2013 se comunicaron un total de 416 casos, 160 casos en los tres países endémicos: Pakistán (93 casos), Afganistán14 y Nigeria53 y además en Camerún4, Somalia (194), Siria35, Etiopia9 y Kenia14. Desde febrero de 2013 se ha detectado la circulación de virus de la polio tipo 1 salvaje en Israel, Cisjordania y Gaza8.
Las infecciones en las zonas templadas del hemisferio norte son más frecuentes en verano y principio de otoño6.
A finales del siglo XIX la polio, que había sido endémica desde tiempos inmemoriales, se convirtió en epidémica en Europa, Norteamérica y Australia, una situación que se ha relacionado con la mejora de las condiciones higiénicas. Con anterioridad la infección era más precoz, cuando los niños tenían aún anticuerpos maternos, por lo que no se producía el cuadro y se incrementaba la inmunidad. La situación cambió al mejorar las condiciones higiénicas, la infección se producía más tarde y no había protección6,54. Solo la introducción de la vacuna fue capaz de frenar el constante crecimiento de la polio en la primera mitad del pasado siglo6.
La polio es una enfermedad básicamente infantil. En los países en vías de desarrollo afectó y afecta fundamentalmente a los lactantes mientras que en los países desarrollados la edad fue incrementándose. Así en los años 50 en EE. UU eran mucho más numerosos los casos en mayores de 10 años que entre los 5 y 10 y estos que los de menos de 56.
La importación es el principal riesgo para la introducción de los virus en zonas indemnes. Los conflictos bélicos y los movimientos de la población son una causa muy importante de la difusión de los virus de la polio como se constata por la situación actual.
Desde un punto de vista epidemiológico son muy importantes y un problema por su prolongada replicación y fácil transmisión los VDPV. Desde que en 2000 se detectó en la isla de La Española el primer brote de polio paralítica producido por cVDPV55 se han comunicado otros muchos en diversos países39,50. Así, de julio de 2012 a diciembre de 2013 siguieron los brotes existentes en Afganistán, Somalia (con extensión a Kenia) y Nigeria, este con incidencia muy baja, y aparecieron nuevos en Chad (con extensión a Camerún, Níger y Nigeria), China, Pakistán (con extensión a Afganistán) y Yemen. Todos fueron debidos a cVDPV2 salvo el de Yemen que fue ocasionado cVDPV348. Estos datos dejan clara la capacidad de las cepas de cVDPV de convertirse en endémicas y de exportarse. Tienen menos interés epidemiológico los casos relacionados con la vacunación en inmunocompetentes e inmunodeprimidos y sus contactos39.
PatogeniaLos poliovirus penetran por vía oral y se replican en el tracto digestivo a nivel orofaríngeo e intestinal y se extienden a los linfáticos regionales25 produciendo una primera viremia. Esta siembra les lleva al sistema retículo endotelial donde se replican de nuevo y producen una segunda viremia por la que llegan a distintos órganos, incluido el SNC. El virus penetra en él en el trascurso de esta viremia y quizás, también, por transporte axonal a partir de la sinapsis neuromuscular40.
Su capacidad de infectar por vía oral exclusivamente al hombre y a algunos primates se debe a que las células del epitelio asociado a los folículos, las células M y las placas de Peyer expresan su receptor específico, el CD155,51 al que se fija la cápsida, este receptor es el que explica su tropismo ulterior.
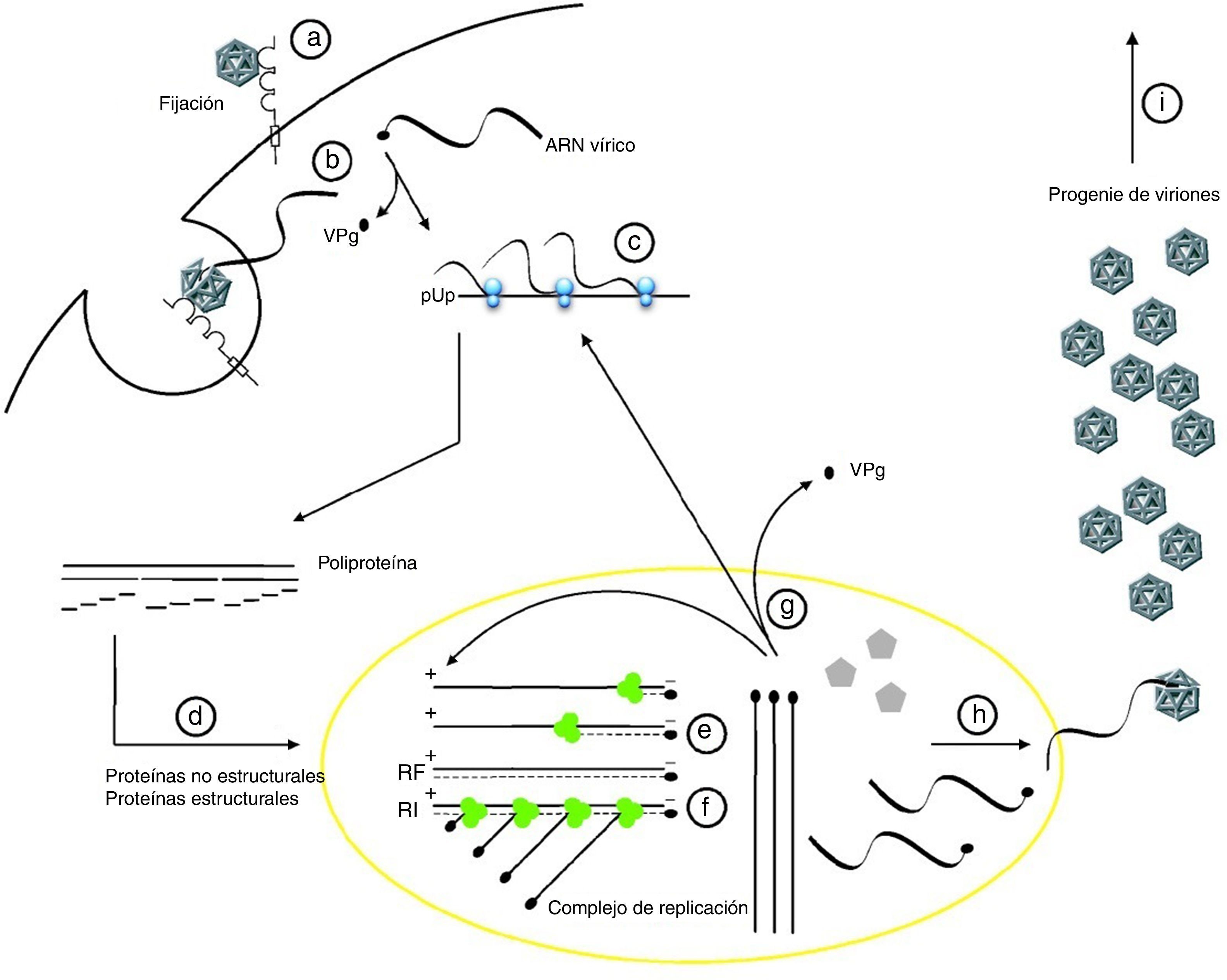
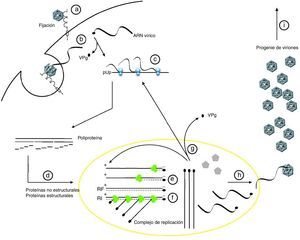
La replicación de los virus de la polio sigue los pasos siguientes (fig. 4): se fijan a su receptor el CD155 y penetra por endocitosis (a). Pierde la cápsida en el interior de la célula que parasitan (b). La proteína VPg es escindida por una fosfodiesterasa celular y se produce la traducción del ARN ss (+) del virus, que actúa como ARNm, por un mecanismo mediado por el Internal Ribosome Entry Site, no por el cap (contienen en su extremo 5’ terminal una guanina metilada o estructura cap, que es el sitio en donde inicialmente se une el ribosoma), produciéndose una poliproteína (c). A partir de la poliproteína y por un proceso de proteólisis se producen las proteínas estructurales y no estructurales del virus (d). La cadena ARN de polaridad positiva del virus sirve de plantilla para la síntesis de una complementaria de polaridad negativa produciéndose un ARN bicatenario (la forma de replicación o RF) (e). El ARN (-) se utiliza a la vez para la replicación de varias cadenas ARN ss (+), formándose el intermedio replicativo (RI) (f). Las ARN ss (+) se pueden utilizar para nuevos procesos de traducción (g) o unirse a los precursores de la cápsida, encapsidarse e inducir la maduración (precursor polipeptidico P1>VP0, VP1 y VP3, Vp0> VP2 y VR4) (h) y liberar la progenie de viriones por lisis celular (i)56.
Ciclo replicativo del virus de la polio (esquema de E.H. de Jesus, www.virologyj.comcontent4170)56.
Si la replicación se lleva a cabo en las motoneuronas de las astas anteriores de la médula espinal o del bulbo, estas son destruidas y aparece una parálisis flácida, cuya persistencia está en relación con el la intensidad y extensión del daño.
Los tres tipos de virus muestran no solo una distinta antigenicidad sino también una patogenicidad diferente, el que más parálisis producía era el tipo 1 y el que menos el 26. Las cepas cVDPV y muchas de iVDPV son capaces de producir polio paralítica39.
Cuadro clínicoLa infección suele ser asintomática o inaparente en más de un 90% de las ocasiones57. El periodo de incubación suele ser de 7 a 10 días con un intervalo de 4 a 35 días33. En las formas sintomáticas la polio puede ser abortiva, leve o menor (4-8%), (enfermedad febril con manifestaciones faríngeas y digestivas, que corresponden a la multiplicación inicial del virus y es difícilmente diagnosticable), no paralítica o meníngea (1-2%), (como la anterior con manifestaciones meníngeas) o paralítica (un 1% o menos), (tras las manifestaciones de una polio abortiva aparece una parálisis flácida y asimétrica y contracturas dolorosas de los músculos no afectados) a consecuencia de las lesiones que produce el virus en las motoneuronas57. Como se pueden afectar tanto las medulares como las bulbares se han descrito tres formas clínicas, la espinal, la bulbar y la bulbo-espinal. La más frecuente es la espinal que afecta a las extremidades, particularmente a las piernas. El grado y extensión de la lesión marca el que la parálisis sea reversible o no33, la recuperación generalmente ocurre en los seis meses siguientes al cuadro agudo. En caso contrario se producen las deformidades, atrofias y contracturas típicas en su fase de secuelas permanentes57 (fig. 5). Hay casos mortales, más en adolescentes y adultos (15-30%) que en niños (5-10%), que se deben particularmente a la parálisis respiratoria derivada de la afectación bulbar. No se afecta ni la sensibilidad ni la conciencia33.
Hay casos de polio paralítica producidos, además de por los virus salvajes, por los utilizados en la vacuna oral (VDPV) y por derivados de estos (VDPV)39,48. El periodo de incubación en pacientes inmunodeprimidos con infección con virus derivados de la vacuna puede ser muy largo, habiéndose comunicado un caso de 12 años58.
En pacientes que padecieron una polio en la infancia puede aparecer un cuadro al cabo de muchos años, quince o más, caracterizado por debilidad, atrofia y fatiga musculares de causa desconocida que se ha denominado síndrome pospolio. Se estima que puede afectar entre el 20-85% de esta población. Carece de tratamiento específico13.
DiagnósticoLa polio es una de las causas a considerar dentro del diagnóstico diferencial de las parálisis flácidas agudas que pueden tener otras etiologías infecciosas o de otro tipo.
La OMS ha editado sucesivas ediciones de un Manual de Laboratorio para la polio que recoge todo el proceso diagnóstico, desde la recogida y el transporte de las muestras hasta la caracterización de los virus. En él se recomienda el cultivo de heces y la caracterización serológica (neutralización) del tipo y para diferenciar si es salvaje o VDPV un ELISA, una hibridación o una PCR59. Este procedimiento está superado pues la mayoría de los laboratorios de la red sanitaria utilizan una PCR-TR y para la caracterización de los VDPV una PCR-TR de los genes que codifican la VP148. Dada la plasticidad genética de los poliovirus los estudios de epidemiología molecular son esenciales60. Se ha desarrollado PCR-TR que permite detectar los virus de la vacuna directamente en heces y aguas residuales61.
Los virus también se pueden buscar en secreciones respiratorias y LCR.
TratamientoLa polio no tiene tratamiento específico. En el periodo agudo deben ponerse en marcha las medidas de soporte necesarias que pueden llegar a incluir la respiración asistida. Debe hacerse fisioterapia para minimizar las secuelas y facilitar en lo posible la recuperación. Para las deformidades y parálisis se puede recurrir a la cirugía correctora, al uso de órtesis y otros aparatos ortopédicos33,62.
PrevenciónLa vacuna es muy eficaz y ha hecho que la polio sea una enfermedad erradicable al ser el hombre el único reservorio conocido. La prevención está fundamentada en la vacunación sistemática de la población lo que está permitiendo su erradicación mundial. Aparte hay que poner en marcha medidas generales, como la cloración del agua de bebida y de las piscinas, que es eficaz para prevenir la trasmisión del virus63. No está indicada la cuarentena.
Se han desarrollado dos tipos de vacunas, las inactivadas y las atenuadas. De las primeras se utiliza la conseguida por Salk y su equipo y de las segundas la de Sabin y su grupo.
El 12 de abril de 1955 se anunció que la vacuna obtenida por Salk era eficaz en la prevención de la polio paralítica29, los estudios preliminares habían sido publicados dos años antes28, la comunicación abría una nueva era. Esta vacuna se había conseguido cultivando los poliovirus en células de riñón de mono e inactivándolos con formalina64.
Por su parte Sabin y su equipo en 1953 comprobaron que el cultivo de poliovirus muy paralitogénicos en células de riñón de macaco permitía la selección de virus no paralitogénicos lo que le llevó al desarrollo de su vacuna oral que en su forma trivalente fue introducida en EE. UU. en la vacunación sistemática infantil en 1965. Las cepas de la vacuna se multiplican activamente en intestino, pasan a la familia y a la población e inmunizan a la población no vacunada65. En la mayoría de los países la vacuna oral sustituyó a la parenteral, en ello mucho tuvo que ver, en EE. UU. el «incidente Cutter»9, y es la vacuna que la OMS ha utilizado en la erradicación.
La vacunación antipolio no ha estado exenta de problemas y polémicas. El primero fue el «incidente Cutter» que aconteció en 1955 al poco de introducirse y que se debió a una inadecuada inactivación de la vacuna Salk por los laboratorios Cutter de California, a consecuencia de lo que hubo 40.000 casos de polio, 200 paralítica y 10 muertes9.
Aunque son infrecuentes, puede ocurrir que aparezcan casos de polio paralítica tras la vacunación oral (VAPP) tanto en receptores como en contactos, especialmente tras la primera dosis. En EE. UU. se ha estimado una frecuencia de un caso por cada 2,6 millones de dosis distribuidas66.
En 1960 se comunicó el descubrimiento del SV40 en células de riñón de monos y en depósitos de vacunas de Sabin y adenovirus. El SV40 resistía además la inactivación con formalina utilizada en la preparación de la vacuna Salk. Por estos datos se sabe que hasta 1963, millones de personas en EE. UU. y otros países recibieron el SV40 al vacunarse, que es oncogénico en animales. El papel de este virus en la génesis de tumores en las personas que lo recibieron está por determinar67.
En 1991 Pascal intentó correlacionar el origen del sida con las vacunaciones en masa que se hicieron en África con la vacuna atenuada de Koprowski que se obtenía de cultivos en células de riñón de mono68. Esta teoría ha sido refutada69.
El brote de polio paralítica producida por cVDPV en La Española (actual Santo Domingo y Haití)55 y los que le han seguido39,50 han generado polémica70 y obligado a poner en marcha estrategias para minimizar su extensión y acción. En este sentido la extensión de una cepa cVDPV1 en Minnesota en 2005 en una población no vacunada71 refuerza la idea de que la mejor forma de enfrentarse a estos hechos es conseguir una amplia y correcta cobertura vacunal, si es baja, los poliovirus de la polio oral pueden circular y evolucionar a tipos con neurotoxicidad39. Así mismo se estima que es necesario conseguir nuevas vacunas inactivadas72 u orales más estables genéticamente39,73.
En 2014 la OMS ha actualizado su posición con relación a la vacunación antipolio. Resalta la recomendación de añadir, en los países donde se usa la vacuna oral, al menos una dosis de vacuna inactivada con el fin de reducir el riesgo de que reaparezca el PV2 tras retirarse de la vacuna oral el Sabin tipo 2. Reconoce, independientemente del coste-efectividad, que el cambio de la vacuna oral por inactivada o el comienzo por esta y la continuación con la oral reduce o evita el riesgo de VAPP33.
En España la vacunación, no gratuita, comenzó en 1958 utilizando la vacuna tipo Salk pero no sería hasta 1963 cuando comenzaron las campañas de vacunación gratuita empleando la vacuna tipo Sabin, el precio que se pagó por el retraso fue muy alto74. El último caso autóctono por virus salvaje declarado en España se remonta a 1988, luego ha habido 4 casos relacionados con la vacuna, uno importado y otro derivado de la vacuna oral en 199715. En 2002 la OMS concedió a Europa el certificado de la erradicación de la polio75. Siguiendo las normas de esta institución en 2004 se sustituyó la vacuna oral (tipo Sabin) por la inactivada (tipo Salk)15 que está incluida en el calendario de vacunación recomendado por el Consejo Interterritorial del Sistema Nacional de Salud español, junto con otras vacunas, a los 2, 4, 6 y 18 meses76.
La poliomielitis es una enfermedad de declaración obligatoria. Existe un plan nacional para mantener España libre de polio77. La vigilancia epidemiológica incluye: la vigilancia de las parálisis flácidas agudas en menores de 15 años, el alcanzar y mantener altas coberturas vacunales (del 95% en la serie primaria, en menores de 2 años) y la vigilancia medioambiental de enterovirus15. En esta línea están los informes sobre la vigilancia de la parálisis flácida aguda78.
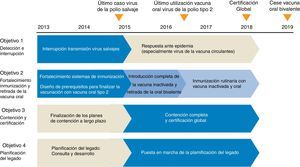
Erradicación de la polioEn 1988 la OMS aprobó una resolución en la que se decidía poner en marcha las medidas necesarias para que la poliomielitis estuviera erradicada en el año 200031. Tras el éxito de la eliminación de la viruela y dadas las características de la polio y sus agentes causales era una tarea que podía llevarse a cabo. Aunque las previsiones iniciales no se han cumplido, lo logrado ha sido ingente, inimaginable y el horizonte de erradicación se mantiene aunque se ha retrasado a 201879. Con la estrategia diseñada desde 1988 los casos de polio han disminuido en más del 99%, de los más de 350.000 casos distribuidos en más de 125 países endémicos se ha pasado a 416 casos en 2013 con solo 160 en las 3 zonas endémicas, Afganistán, Pakistán y Nigeria, siendo el resto debidos a la propagación a zonas ya libres de los virus, a Camerún, Siria, Etiopía, Somalia y Kenia7,8,80. En 1999 se logró erradicar el PV232 y desde el 10 de noviembre de 2012 no se ha detectado el PV333 (fig. 6).
En la Iniciativa Global de Erradicación de la Polio están participando los gobiernos de los distintos países, los Centers for Disease Control and Prevention, la fundación Rotary Internacional, la OMS, la UNICEF y la Fundación Bill y Melinda Gates79.
La estrategia se ha basado en la vacunación y en la vigilancia.
Con las campañas de vacunación con los tres tipos dirigidas a niños de menos de 5 años se pretendía, y se ha conseguido, proteger a los individuos y generar una inmunidad de grupo que dificultara la transmisión de los virus. Por sus características se eligió la vacuna oral trivalente. El PV2 se eliminó de ella cuando se consiguió erradicar y por la aparición de brotes producidos por cVDPV2. En este momento la OMS ha recomendado añadir una dosis de vacuna inactivada de PV233. Los conflictos bélicos y la falta de formación han dificultado las campañas de vacunación y ha disminuido la cobertura vacunal, por eso se ha ralentizado el proceso y aún sigue habiendo tres países endémicos desde los que los virus salvajes, por los movimientos migratorios, han vuelto a aparecer en países donde se habían erradicado, ocasionando casos de polio paralítica si la cobertura vacunal era insuficiente, como fue, por ejemplo, el caso de Siria en 201381 o simplemente circulando, como ha ocurrido en Israel, Gaza y Cisjordania8. En Israel el virus estaba presente en aguas residuales y hubo transmisión entre portadores sanos, básicamente niños vacunados con vacuna parenteral82. Las dificultades geográficas de acceso a la vacuna y los conflictos bélicos han demostrado ser un aliado de la polio pero también la falta de formación. En Nigeria, país endémico donde la cobertura vacunar es insuficiente, en 2003, en la zona norte, se extendió un rumor que decía que la vacuna contenía fármacos que producían esterilidad, causaba casos de polio y extendía el sida, como consecuencia muchos padres se han negado a vacunar a sus hijos83. Es fundamental vacunar, hacerlo adecuadamente y mantener la inmunización.
En lo que va de 2014 la situación ha empeorado y lo ha hecho en una época climatológica de baja transmisibilidad de la polio. Si se comparan los datos de enero al 20 de mayo de 2013 con los del mismo periodo de 2014 se ha pasado de 34 casos a 8284. Ante estos datos el 5 de mayo de 2014 la OMS consideró la situación como una urgencia de salud pública de importancia internacional. El riesgo está en la propagación internacional y por eso recomienda, entre otras medidas, tanto en países exportadores de virus salvajes (Pakistán, Camerún y Siria) como en los que circulan (Afganistán, Guinea Ecuatorial, Etiopía, Iraq, Israel, Somalia y Nigeria) que los ciudadanos y residentes de largo plazo (de más de 4 semanas) que vayan a realizar un viaje internacional reciban una dosis de vacuna oral o inactivada de 4 semanas a 12 meses antes de realizarlo. En caso de desplazamientos de urgencia y si no han recibido vacunas entre este tiempo una dosis en el momento de salida. En el primer grupo de países los gobiernos deben asegurarse de que así ocurra y en segundo fomentarlo85.
La vigilancia es el otro pilar de la erradicación. Es necesario conocer todos los casos de polio para saber cómo progresa el proceso y tomar las medidas oportunas si son necesarias, además es preciso saber si hay virus circulantes. Para ello la OMS dispone de una red de laboratorios que son capaces de identificar los virus de la polio salvajes y derivados de la vacuna oral muchos de ellos a nivel genético48,86. La vigilancia de la etiología de las parálisis flácidas es esencial en este empeño, hay que separar las infecciosas de las producidas por otras causas y de las primeras saber su agente y si es un poliovirus llegar a caracterizarlo genéticamente. España como beneficiaria del Certificado de Erradicación de la Poliomielitis en la Región de Europa de la OMS participa en esta labor77,78.
Los brotes de Siria y el Cuerno de África y la circulación de poliovirus salvajes en Israel han levantado la voz de alarma en Europa ante la posible introducción y difusión de virus salvaje y se han generado unas normas que, como en el caso de la erradicación, se basan en la vacunación y en la vigilancia87.
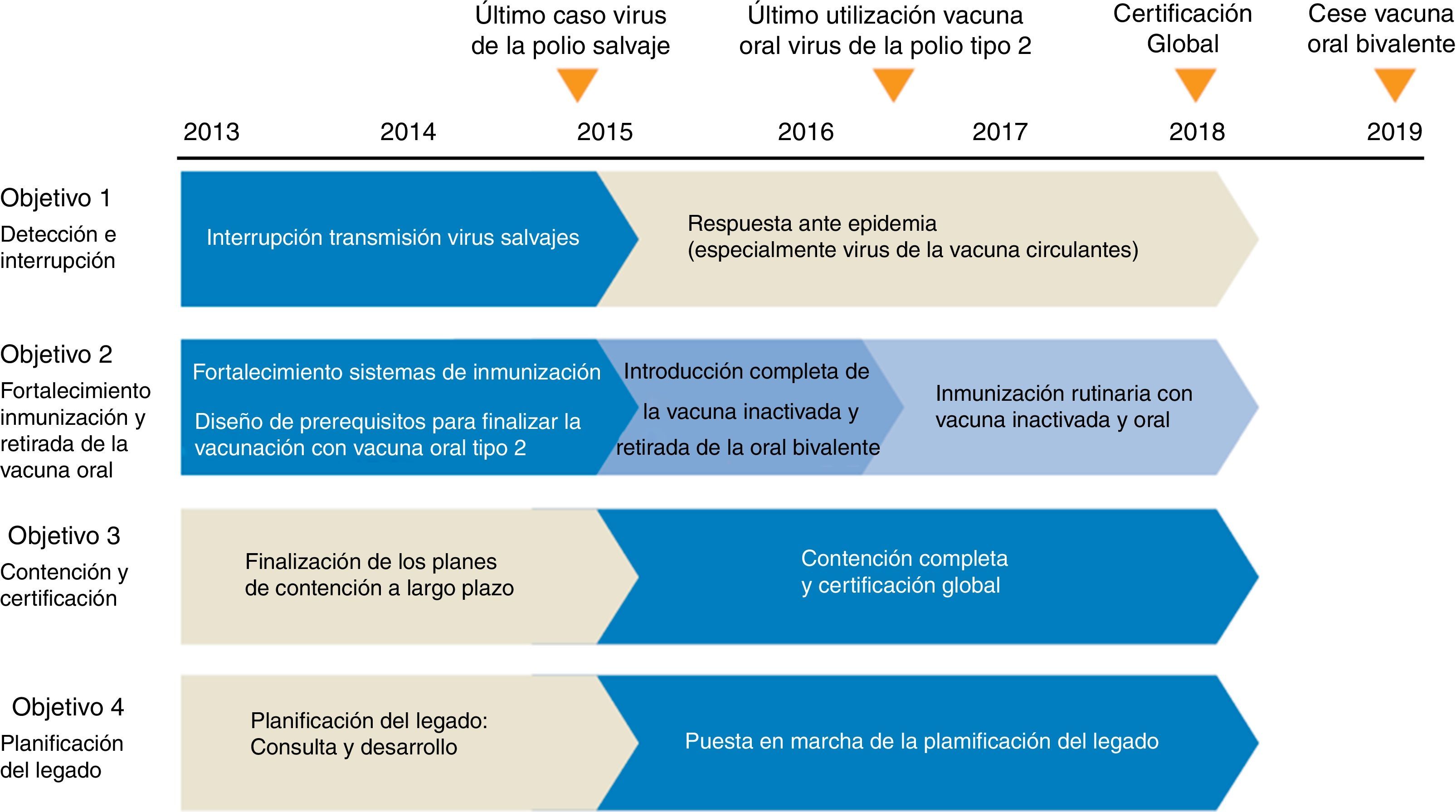
Esperemos que 2018 sea el último juego de la partida y no una página más de una historia interminable (fig. 7).