Establecer posibles asociaciones entre las nuevas especies incluidas en grupo Streptococcus bovis aisladas de hemocultivos, con los datos clínicos de los pacientes correspondientes.
MétodosCuarenta y cuatro hemocultivos debidos a S. bovis se identificaron mediante pruebas fenotípicas y se correlacionaron con los datos clínicos de los pacientes correspondientes.
ResultadosIdentificamos 15 Streptococcus gallolyticus subsp. gallolyticus, 24 Streptococcus gallolyticus subsp. pasteurianus, y 5 Streptococcus infantarius en los 44 episodios de bacteriemia.
ConclusionesLa asociación entre bacteriemia por S. bovis y endocarditis y/o cáncer de colon está fuertemente asociada a la especie causal.
Streptococcus gallolyticus subsp. gallolyticus se relaciona con endocarditis y/o enfermedad colónica, mientras Streptococcus gallolyticus subsp. pasteurianus está significativamente relacionado con patología hepato-biliar.
We sought to identify possible diseases associated with bloodstream infections caused by new species of S. bovis group isolated in blood cultures and by studying patient records
MethodsForty-four consecutive blood culture isolates initially designated S. bovis were further characterised using phenotypic methods Patient records were examined.
ResultsWe identified 15 Streptococcus gallolyticus subsp. gallolyticus, 24 Streptococcus gallolyticus subsp. pasteurianus, and 5 Streptococcus infantarius isolates in 44 BSI episodes.
ConclusionsThe association between S. bovis bacteraemia and endocarditis and/or colon carcinoma is highly dependent on the causative species.
Streptococcus gallolyticus subsp. gallolyticus is a surrogate for endocarditis and/or bowel disease, whereas Streptococcus gallolyticus subsp. pasteurianus is a surrogate for hepato-biliary disease.
La asociación entre neoplasias de colon y aislamiento de Streptococcus bovis en hemocultivos es conocida desde hace tiempo1. Además S. bovis constituye uno de los grupos de estreptococos frecuentemente relacionados con endocarditis bacteriana2 y la conjunción de ambos cuadros clínicos ha sido descrita abundantemente3–5. Más recientemente se ha descrito la posible asociación de bacteriemia por estos microorganismos con diferentes cuadros de patología hepato-biliar6.
En la actualidad se sabe que el término S. bovis incluye un grupo de cocos gram-positivos pertenecientes a un conjunto de especies relacionadas genéticamente que tradicionalmente se habían dividido en tres biotipos con arreglo a sus comportamientos bioquímicos7. En la actualidad, el biotipo S. bovis I, que comprendía cepas fermentadoras de manitol y capaces de hidrolizar almidón, se adscribe a la especie Streptococcus gallolyticus subsp. gallolyticus, mientras que los llamados S. bovis II/2 carentes de esta capacidad sacarolítica, pero con presencia de ß-glucuronidasa y ¿-galactosidasa, se clasifican como Streptococcus gallolyticus subsp. pasteurianus. Finalmente, los encuadrados como S. bovis II/1, que poseen este último enzima pero carecen de ß-glucuronidasa y conservan la capacidad hidrolítica para el almidón, se encuadran como Streptococcus infantarius subsp. coli8,9.
La posible asociación entre cada una de estas nuevas especies y subespecies con los distintos cuadros clínicos relacionados con el conjunto de estos microorganismos se ha intentado poner de manifiesto con resultados contradictorios10,11.
En un intento de aportar nuevos datos a la hora de establecer estas posibles asociaciones, hemos estudiados los aislamientos de hemocultivos de estos últimos años, previamente identificados como S. bovis, confrontándolos con los datos clínicos de los pacientes correspondientes, de acuerdo a la actual clasificación de estos microorganismos.
Material y métodosCuarenta y cuatro aislados inicialmente identificados como S. bovis, procedentes de hemocultivos obtenidos de otros tantos pacientes vistos en nuestros hospitales durante el periodo 2003-2009, y que habían sido conservados en leche descremada a −20°C hasta el momento de su estudio, fueron subcultivados en placas de agar Müller-Hinton suplementado con 5% de sangre de carnero (Oxoid, Bashington, Reino Unido) durante 18-24 horas a 35°C en una atmósfera con 5% de CO2.
Las cepas se identificaron, en esta ocasión, utilizando galerías comerciales API20 Strep (bio-Merieux, Marcy l¿Etoile, Francia) conforme a las instrucciones del fabricante y con arreglo a la versión 2.0 del citado sistema. Además se estudió la capacidad de crecimiento y desdoblamiento de la esculina en tubos de agar bilis-esculina (Oxoid, Bashington, Reino Unido) y la presencia en las cepas de antígeno grupo D de Lancefield mediante antisueros comerciales (Oxoid, Bashington, Reino Unido).
La sensibilidad de los microorganismos se llevó a cabo utilizando paneles de microdilución del sistema Wyder. Los resultados se interpretaron siguiendo las recomendaciones del CLSI12.
Los historiales clínicos de los 44 pacientes fueron revisados de acuerdo a un protocolo previamente establecido que incluía la edad y el sexo de los mismos, número de hemocultivos positivos por cada episodio, comorbilidades preexistentes y el diagnóstico clínico en el momento de la bacteriemia, junto con la evolución clínica de los pacientes, entre otros datos.
ResultadosEn las 44 bacteriemias estudiadas, causadas por el previamente denominado Streptococcus grupo bovis y correspondientes a otros tantos pacientes, identificamos 15 S. gallolyticus subs. gallolyticus (SGG), 24 S. gallolyticus subs. pasterurianus (SGP) y 5 S. infantarius (SI), 2 correspondientes a la subespecie coli y 3 pertenecientes a la subespecie infantarius.
Todas las cepas hidrolizaban esculina en presencia de 40% de bilis y acidificaban sacarosa, lactosa y rafinosa, pero solo 29 (65%) reaccionaban con el antisuero correspondiente al antígeno del grupo D de Lancefield. La identificación a nivel de especie y subespecie se llevó a cabo mediante el sistema API 20Strep v7.0 con porcentajes de identificación superiores en cualquier caso al 90%.
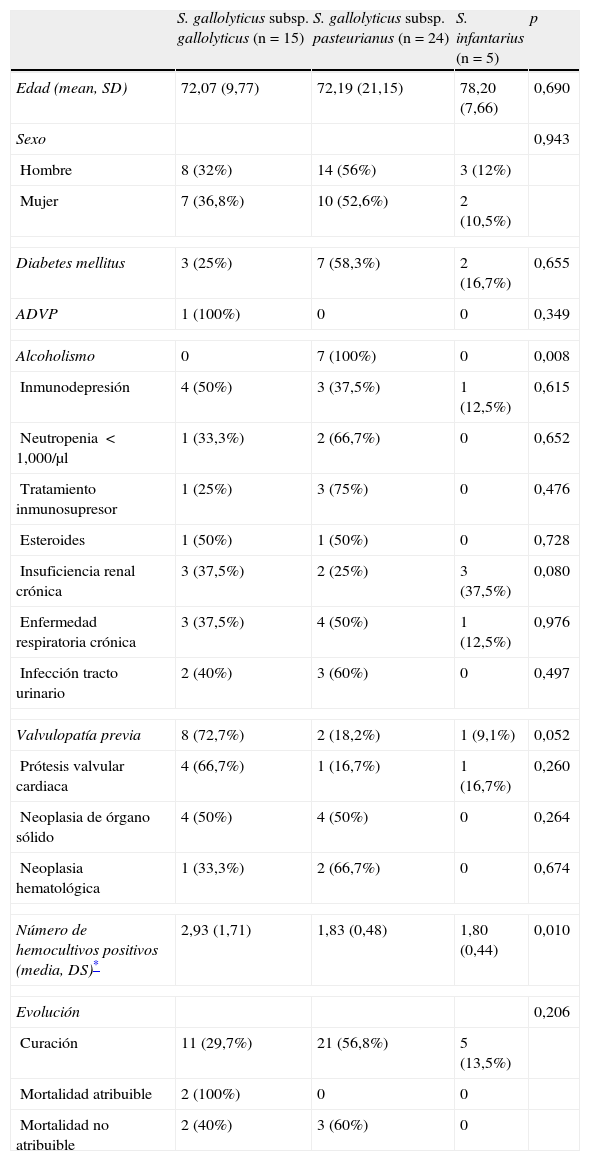
En la tabla 1 se expresan las características demográficas y comorbilidades preexistentes en los pacientes estudiados, relacionándolos con los microorganismos correspondientes aislados de sus hemocultivos. No existieron diferencias en la distribución de sexo, edad y patologías previas asociadas en relación al microorganismo aislado, excepto la existencia de valvulopatía previa en bacteriemia por SGG, 8 casos (72,7%) vs. 3 (28,3%) para el resto, o el antecedente de alcoholismo con 7 casos encontrados, todos ellos con bacteriemia por SGP. El número de hemocultivos positivos fue significativamente más alto en los casos de aislamiento de SGG (p≤ 0,010).
Características demográficas y comorbilidades de los 44 pacientes estudiados
| S. gallolyticus subsp. gallolyticus (n=15) | S. gallolyticus subsp. pasteurianus (n=24) | S. infantarius (n=5) | p | |
| Edad (mean, SD) | 72,07 (9,77) | 72,19 (21,15) | 78,20 (7,66) | 0,690 |
| Sexo | 0,943 | |||
| Hombre | 8 (32%) | 14 (56%) | 3 (12%) | |
| Mujer | 7 (36,8%) | 10 (52,6%) | 2 (10,5%) | |
| Diabetes mellitus | 3 (25%) | 7 (58,3%) | 2 (16,7%) | 0,655 |
| ADVP | 1 (100%) | 0 | 0 | 0,349 |
| Alcoholismo | 0 | 7 (100%) | 0 | 0,008 |
| Inmunodepresión | 4 (50%) | 3 (37,5%) | 1 (12,5%) | 0,615 |
| Neutropenia <1,000/μl | 1 (33,3%) | 2 (66,7%) | 0 | 0,652 |
| Tratamiento inmunosupresor | 1 (25%) | 3 (75%) | 0 | 0,476 |
| Esteroides | 1 (50%) | 1 (50%) | 0 | 0,728 |
| Insuficiencia renal crónica | 3 (37,5%) | 2 (25%) | 3 (37,5%) | 0,080 |
| Enfermedad respiratoria crónica | 3 (37,5%) | 4 (50%) | 1 (12,5%) | 0,976 |
| Infección tracto urinario | 2 (40%) | 3 (60%) | 0 | 0,497 |
| Valvulopatía previa | 8 (72,7%) | 2 (18,2%) | 1 (9,1%) | 0,052 |
| Prótesis valvular cardiaca | 4 (66,7%) | 1 (16,7%) | 1 (16,7%) | 0,260 |
| Neoplasia de órgano sólido | 4 (50%) | 4 (50%) | 0 | 0,264 |
| Neoplasia hematológica | 1 (33,3%) | 2 (66,7%) | 0 | 0,674 |
| Número de hemocultivos positivos (media, DS)* | 2,93 (1,71) | 1,83 (0,48) | 1,80 (0,44) | 0,010 |
| Evolución | 0,206 | |||
| Curación | 11 (29,7%) | 21 (56,8%) | 5 (13,5%) | |
| Mortalidad atribuible | 2 (100%) | 0 | 0 | |
| Mortalidad no atribuible | 2 (40%) | 3 (60%) | 0 | |
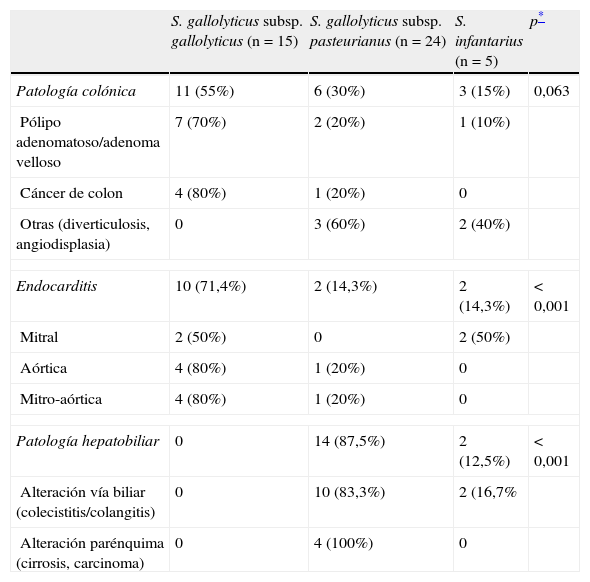
Las formas de presentación clínica asociadas a los microorganismos estudiados se representan en la tabla 2. Un tercio del total de los pacientes desarrollaron una endocarditis. Los aislamientos de SGG fueron significativamente más frecuentes para esta patología (71,4% % para SGG vs. 14,3% para SGP, p≤0,001), mientras que las bacteriemias ocasionadas por SGP presentan una fuerte asociación con cuadros de patología biliar (colecistitis, colangitis) o hepática (cirrosis, carcinoma hepático) (p≤0,001). En el 50% de todos pacientes, se practicó una colonoscopia con diagnósticos de poliposis adenomatosa/vellosa en 10 de ellos, cáncer de colon en 5 y otras patologías (diverticulitis, angiodisplasia) en otros 5 casos. En conjunto, la patología colónica fue más frecuente entre los pacientes con bacteriemia por SGG, 55 vs. 30% o 15%, que entre los pacientes con aislamiento en los hemocultivos de SGP o SI, respectivamente.
Formas de presentación clínica asociadas a bacteriemia por Streptococcus grupo bovis
| S. gallolyticus subsp. gallolyticus (n=15) | S. gallolyticus subsp. pasteurianus (n=24) | S. infantarius (n=5) | p* | |
| Patología colónica | 11 (55%) | 6 (30%) | 3 (15%) | 0,063 |
| Pólipo adenomatoso/adenoma velloso | 7 (70%) | 2 (20%) | 1 (10%) | |
| Cáncer de colon | 4 (80%) | 1 (20%) | 0 | |
| Otras (diverticulosis, angiodisplasia) | 0 | 3 (60%) | 2 (40%) | |
| Endocarditis | 10 (71,4%) | 2 (14,3%) | 2 (14,3%) | <0,001 |
| Mitral | 2 (50%) | 0 | 2 (50%) | |
| Aórtica | 4 (80%) | 1 (20%) | 0 | |
| Mitro-aórtica | 4 (80%) | 1 (20%) | 0 | |
| Patología hepatobiliar | 0 | 14 (87,5%) | 2 (12,5%) | <0,001 |
| Alteración vía biliar (colecistitis/colangitis) | 0 | 10 (83,3%) | 2 (16,7% | |
| Alteración parénquima (cirrosis, carcinoma) | 0 | 4 (100%) | 0 | |
Siete pacientes murieron durante su estancia en el hospital aunque solo en 2 casos esta mortalidad puede ser atribuible a la bacteriemia debida a estos microorganismos.
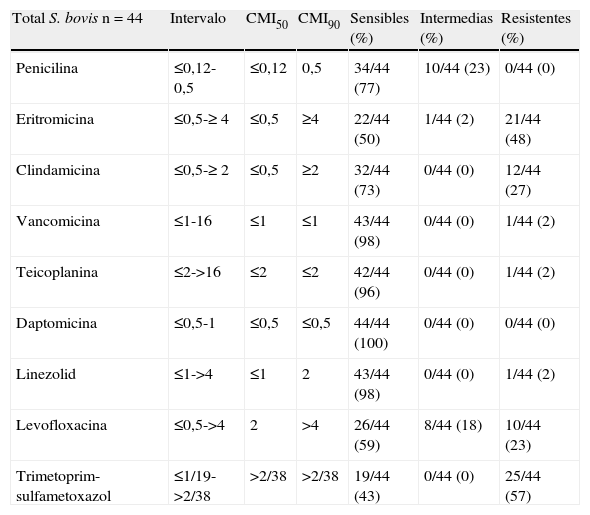
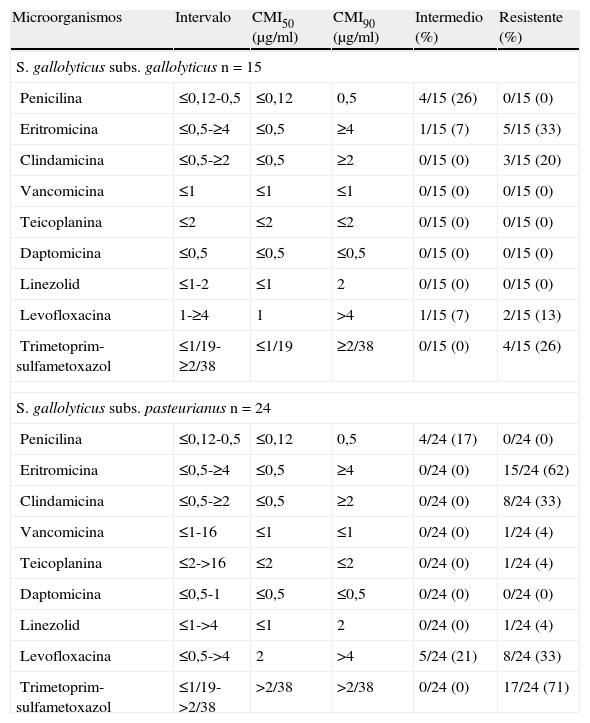
En las tablas 3 y 4 se señalan el intervalo, CMI50, CMI90 y porcentajes de sensibilidad encontrados para cada una de las especies/subespecies estudiadas. Los 44 aislamientos se mostraron uniformemente sensibles a daptomicina con CMI ≤ 1μg/ml del antibiótico en todos los casos. Por otro lado no se observaron cepas resistentes a penicilina aunque el 23% de las mismas se categorizan como de sensibilidad intermedia al presentar una CMI de 0,5μg/ml para el betalactámico. Solamente una cepa era resistente a los glicopéptidos probados, con altas CMI de los mismos, 16μg/ml para vancomicina y>16μg/ml para teicoplanina. También una única cepa se consideró resistente a linezolid con una CMI de>4μg/ml para este antimicrobiano. Los porcentajes de resistencia para eritromicina y clindamicina fueron elevados, el 48% para el macrólido y el 27% para la lincosamina. La categorización de sensible frente a levofloxacina solo se obtuvo en el 59% de los casos, considerándose el resto como resistentes o de sensibilidad intermedia. La resistencia al cotrimoxazol fue igualmente elevada, ascendiendo al 57% de los aislados. En general, los porcentajes de resistencia más altos ocurrieron entre las cepas de SGP, especialmente los referidos a eritromicina y cotrimoxazol (tabla 4). Además las únicas dos cepas resistentes a los glicopéptidos o a linezolid pertenecían también a esta subespecie.
Sensibilidad antimicrobiana de 44 aislamientos del grupo Streptococcus bovis
| Total S. bovis n=44 | Intervalo | CMI50 | CMI90 | Sensibles (%) | Intermedias (%) | Resistentes (%) |
| Penicilina | ≤0,12-0,5 | ≤0,12 | 0,5 | 34/44 (77) | 10/44 (23) | 0/44 (0) |
| Eritromicina | ≤0,5-≥ 4 | ≤0,5 | ≥4 | 22/44 (50) | 1/44 (2) | 21/44 (48) |
| Clindamicina | ≤0,5-≥ 2 | ≤0,5 | ≥2 | 32/44 (73) | 0/44 (0) | 12/44 (27) |
| Vancomicina | ≤1-16 | ≤1 | ≤1 | 43/44 (98) | 0/44 (0) | 1/44 (2) |
| Teicoplanina | ≤2->16 | ≤2 | ≤2 | 42/44 (96) | 0/44 (0) | 1/44 (2) |
| Daptomicina | ≤0,5-1 | ≤0,5 | ≤0,5 | 44/44 (100) | 0/44 (0) | 0/44 (0) |
| Linezolid | ≤1->4 | ≤1 | 2 | 43/44 (98) | 0/44 (0) | 1/44 (2) |
| Levofloxacina | ≤0,5->4 | 2 | >4 | 26/44 (59) | 8/44 (18) | 10/44 (23) |
| Trimetoprim-sulfametoxazol | ≤1/19->2/38 | >2/38 | >2/38 | 19/44 (43) | 0/44 (0) | 25/44 (57) |
Intervalo, CMI50, CMI90 y porcentajes de cepas no sensibles de S. gallolyticus subs. gallolyticus y S. gallolyticus subs. pasteurianus
| Microorganismos | Intervalo | CMI50 (μg/ml) | CMI90 (μg/ml) | Intermedio (%) | Resistente (%) |
| S. gallolyticus subs. gallolyticus n=15 | |||||
| Penicilina | ≤0,12-0,5 | ≤0,12 | 0,5 | 4/15 (26) | 0/15 (0) |
| Eritromicina | ≤0,5-≥4 | ≤0,5 | ≥4 | 1/15 (7) | 5/15 (33) |
| Clindamicina | ≤0,5-≥2 | ≤0,5 | ≥2 | 0/15 (0) | 3/15 (20) |
| Vancomicina | ≤1 | ≤1 | ≤1 | 0/15 (0) | 0/15 (0) |
| Teicoplanina | ≤2 | ≤2 | ≤2 | 0/15 (0) | 0/15 (0) |
| Daptomicina | ≤0,5 | ≤0,5 | ≤0,5 | 0/15 (0) | 0/15 (0) |
| Linezolid | ≤1-2 | ≤1 | 2 | 0/15 (0) | 0/15 (0) |
| Levofloxacina | 1-≥4 | 1 | >4 | 1/15 (7) | 2/15 (13) |
| Trimetoprim-sulfametoxazol | ≤1/19-≥2/38 | ≤1/19 | ≥2/38 | 0/15 (0) | 4/15 (26) |
| S. gallolyticus subs. pasteurianus n=24 | |||||
| Penicilina | ≤0,12-0,5 | ≤0,12 | 0,5 | 4/24 (17) | 0/24 (0) |
| Eritromicina | ≤0,5-≥4 | ≤0,5 | ≥4 | 0/24 (0) | 15/24 (62) |
| Clindamicina | ≤0,5-≥2 | ≤0,5 | ≥2 | 0/24 (0) | 8/24 (33) |
| Vancomicina | ≤1-16 | ≤1 | ≤1 | 0/24 (0) | 1/24 (4) |
| Teicoplanina | ≤2->16 | ≤2 | ≤2 | 0/24 (0) | 1/24 (4) |
| Daptomicina | ≤0,5-1 | ≤0,5 | ≤0,5 | 0/24 (0) | 0/24 (0) |
| Linezolid | ≤1->4 | ≤1 | 2 | 0/24 (0) | 1/24 (4) |
| Levofloxacina | ≤0,5->4 | 2 | >4 | 5/24 (21) | 8/24 (33) |
| Trimetoprim-sulfametoxazol | ≤1/19->2/38 | >2/38 | >2/38 | 0/24 (0) | 17/24 (71) |
La adaptación de nuevas nomenclaturas a microorganismos previamente conocidos suele ser, en ocasiones, fuente de conflictos entre clínicos y microbiólogos, ya que la mayoría de las veces tiene como objetivo preferente una modernización en la sistemática que suele seguir a un conocimiento estructural más profundo del microorganismo. Pero también, otras veces, la nueva nomenclatura sirve para clasificar nuevas especies, subespecies o genoespecies con peculiaridades en su implicación en diferentes cuadros infecciosos.
La separación dentro del grupo S. bovis de dos nuevas especies, S. gallolyticus y S. infantarius con otras dos subespecies para cada una de ellas, S. gallolyticus subs. gallolyticus, y S. gallolyticus subs. pasteurianus por una parte y S. infantarius subsp. infantarius y S. infantarius subsp. coli por otra puede ser un ejemplo de lo anterior.
En nuestro estudio se recogieron 44 bacteriemias por el grupo S. bovis correspondientes a otros tantos pacientes, sin encontrar diferencias significativas en cuanto al sexo de los mismos, siendo la edad media del grupo más alta en nuestra serie que en otros estudios similares, presentando los pacientes una edad media superior a los 72 años.
Las comorbilidades encontradas más frecuentemente y que afectaban, como mínimo, a más de una tercera parte de los pacientes incluían patología cardiovascular en el 56% de los casos, enfermedad colónica en el 45,5% y patología hepatobiliar en el 36%.
S. gallolyticus subs. pasterurianus, antiguo S. bovis II/2, fue la especie más frecuentemente encontrada con 24 aislamientos y una fuerte correlación con alteraciones de la vía biliar y/o del parénquima hepático, ya que el 90% de las bacteriemias debidas a este agente ocurrían en cuadros de patología hepatobiliar. De forma inversa, los aislamientos de S. gallolyticus subs. gallolyticus, antiguo S. bovis I, en ningún caso se asociaron con esta patología.
Por el contrario, la presencia de endocarditis, tanto sobre válvula nativa como protésica se presentó en un tercio de los pacientes y se relacionó de forma significativa con el aislamiento de SGG. La existencia de diferentes tipos de adhesinas fijadoras al colágeno presentes en este microorganismo, con gran capacidad de adherencia a distintas matrices extracelulares, ha sido puesta de manifiesto en la literatura13 y estaría en la base de esta asociación.
También la patología colónica se relacionó más frecuentemente con bacteriemia por SGG, con un 64% de estos pacientes con poliposis colónica y hasta un 36% con carcinoma de colon en nuestra serie. Una explicación completamente satisfactoria para esta asociación no parece encontrarse en la literatura, aunque se especula con la hipótesis de la estimulación en la producción de citoquinas pro-inflamatorias y la inducción de lesiones premalignas a través de la formación de criptas colónicas aberrantes por medio de distintos antígenos de membrana de estos microorganismos14. Estas citoquinas condicionarían a su vez un aumento de la permeabilidad vascular que facilitaría el acceso del microorganismo al torrente circulatorio, cerrando la secuencia que habría empezado con el incremento de SGG en la flora intestinal, continuaría con la citada producción de lesiones precancerosas y culminaría con el cuadro de bacteriemia en estadios posteriores.
El pequeño número de bacteriemias causadas por S. infantarius no permite avistar correlaciones con las patologías apuntadas u otras, aunque en la literatura, y en nuestros mismos datos a pesar de su escasez, se entrevé una posible similitud con los resultados observados para SGP15.
Los datos de sensibilidad muestran que el antiguo grupo S. bovis sigue sin presentar cepas resistentes a penicilina11,16, aunque en nuestra serie un 23% puede catalogarse como de sensibilidad intermedia, hecho reseñado para otras especies próximas como S. salivarius17, correspondiéndose estos organismos preferentemente con SGG. Curiosamente, encontramos una cepa de SGP resistente a glicopéptidos con una CMI de 16mg/l de vancomicina y >16mg/l de teicoplanina, hecho muy infrecuente pero ya reflejado en la literatura18 y otra de ellas resistente a linezolid con CMI>4mg/l. Los porcentajes de sensibilidad a eritromicina por un lado y a levofloxacina por el otro fueron más bajos en nuestra serie que en otros estudios similares, especialmente los referidos a la fluorquinolona11,19.
Nuestros resultados, a diferencia de los señalados por Beck et al.11 en los que las bacteriemias por el grupo S. bovis en conjunto y patologías asociadas no tienen una relevancia suficiente, sí están en consonancia con otras series clásicas como la de Ruoff et al.10 que asocian la bacteriemia por SGG y endocarditis en un 94% de los casos, mientras que la bacteriemia por SGP o SI solo se relacionaba en un 18% de los mismos.
De igual manera la bacteriemia por SGG se correlacionaba con neoplasia colónica subyacente en un 71% de los casos estudiados, siendo esta correlación tan solo del 17% para las bacteriemias por SGP o SI.
Del mismo modo, Corredoira et al. observan en su serie17 una fuerte asociación de bacteriemias por SGG con endocarditis (74%) y cáncer de colon (57%). Por otro lado estos autores señalan que la bacteriemia causada por SGP o SI tenía un origen hepatobiliar en el 50% de sus pacientes15.
Nuestras cifras de 71,4% para la asociación de bacteriemia por SGG y endocarditis o del 55% en pacientes con patología colónica están de acuerdo con ellas. Además, nuestros porcentajes de bacteriemia por SGP y patología hepatobiliar concomitante llega hasta el 87,5% y en ninguna ocasión se asoció esta última con el aislamiento en sangre de SGG.
Podemos concluir, por tanto, que a partir de los resultados obtenidos, se refuerza la hipótesis que incide en la asociación destacada entre la presencia de bacteriemias por el grupo S. bovis con cuadros de endocarditis, patología colónica o hepatobiliar.
Además estas asociaciones están igualmente relacionadas con las diferentes especies y/o subespecies del grupo, estableciéndose una correlación preferente entre las bacteriemias por SGG con cuadros de endocarditis y/o patología del colon, mientras que la bacteriemia por SGP se asocia fuertemente con la existencia de patología hepatobiliar.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.